ALEXANDER NEDOSHIVIN. PARVOLETA T. S. PETROVA. YURI KARPOV
Người dịch: ThS. BS. TRẦN ĐẠI CƯỜNG
Đại học Y Dược TP Hồ Chí Minh
(…)
Kết cục hiệu quả chính
Trong 7 nghiên cứu được phân tích, 5 nghiên cứu đã chứng minh giảm tần số tim sau 1 tháng điều trị kết hợp Ivabradine và chẹn bêta [15, 20, 21, 23, 25]. Phân tích thống kê về hiệu quả tần số tim trong 5 nghiên cứu cho thấy giảm tần số tim ở tất cả nghiên cứu (Hình 3a) với mức giảm chung là 12,6 lần/phút ở bệnh nhân điều trị kết hợp Ivabradine và chẹn bêta (p < 0,0001).

Hình 3. Giảm tần số tim ở thời điểm a 1 tháng (Tính không đồng nhất I2 = 99,3%) và b 4 tháng (Tính không đồng nhất I2 = 98,5%) sau khi kết hợp Ivabradine và chẹn bêta, ES: Effect size (Độ ảnh hưởng)
Trong 5 nghiên cứu có thể đánh giá [15, 20, 21, 23, 25], điều trị kết hợp Ivabradine và chẹn bêta có liên quan đến giảm số lượng cơn đau thắt ngực trung bình mỗi tuần vào thời điểm 1 tháng (Hình 4a).
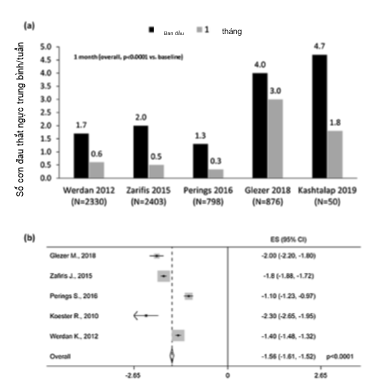
Hình 4. Tần suất cơn đau thắt ngực thời điểm a 1 tháng (chung, p < 0,0001 so với ban đầu) và b 4 tháng sau khi kết hợp Ivabradine và chẹn bêta, CI: khoảng tin cậy, ES: Độ ảnh hưởng
Tương tự, trong số 3 nghiên cứu có thể đánh giá, việc sử dụng nitrate tác dụng ngắn trong tháng đầu tiên cũng giảm đáng kể so với ban đầu (Hình 5a) [15, 20, 25]. Đánh giá hiệu quả cho thấy việc sử dụng nitrate tác dụng ngắn giảm chung 1,25 lần mỗi tuần (p < 0,0001).
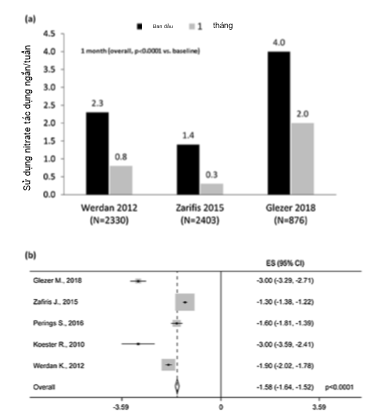
Hình 5. Sử dụng nitrate tác dụng ngắn thời điểm a 1 tháng (chung, p < 0,0001 so với ban đầu) và b 4 tháng (Tính không đồng nhất I2 = 97,9%) sau khi kết hợp Ivabradine và chẹn bêta, CI: khoảng tin cậy, ES: Độ ảnh hưởng
Kết cục hiệu quả phụ
Trong 6 nghiên cứu có thể đánh giá, tất cả cho thấy giảm tần số tim so với ban đầu kéo dài 4 tháng (Hình 3b) trong đó 4 nghiên cứu cho thấy giảm tần số tim sau 1 tháng điều trị và tiếp tục giảm sau 4 tháng [15, 20, 23, 25]. Tần số tim giảm trung bình chung sau 4 tháng là 18 lần/phút (p < 0,0001).
Tần suất các cơn đau thắt ngực hàng tuần giảm rõ rệt so với ban đầu lúc 4 tháng trong cả 5 nghiên cứu có thể đánh giá [15, 20, 22, 23, 25]. Bốn nghiên cứu cho thấy giảm số cơn đau thắt ngực hàng tuần sau 1 tháng và kéo dài đến 4 tháng [15, 20, 23, 25]. Phân tích cho thấy giảm 1,1 – 2,3 cơn đau thắt ngực mỗi tuần trong mỗi nghiên cứu và số giảm chung là 1,56 cơn/tuần sau 4 tháng điều trị (p < 0,0001) (Hình 4b).
Trong số 5 nghiên cứu có thể đánh giá, việc sử dụng nitrate tác dụng ngắn mỗi tuần cũng giảm so với ban đầu lúc 4 tháng ở tất cả nghiên cứu [15, 20, 22, 23, 25] với ba nghiên cứu cho thấy giảm sử dụng nitrate mỗi tuần từ 1 tháng kéo dài đến 4 tháng [15, 20, 25]. Thống kê cho thấy mức giảm chung đối với việc sử dụng nitrate tác dụng ngắn là 1,58 lần/tuần (p < 0,0001) (Hình 5b).
Sự kết hợp Ivabradine và chẹn bêta cũng liên quan đến cải thiện lâm sàng sau 4 tháng điều trị với bằng chứng là sự thay đổi phân độ CCS giữa các bệnh nhân. Có sự gia tăng tỉ lệ bệnh nhân CCS I được ghi nhận trong 6 nghiên cứu có thể đánh giá điều này [15, 20, 22 – 25] với tỉ lệ tăng bệnh nhân CCS I chung là 42% (Hình 6).
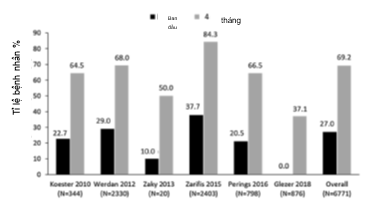
Hình 6. Tỉ lệ bệnh nhân đau thắt ngực phân độ CCS I sau 4 tháng điều trị kết hợp Ivabradine và chẹn bêta.
Cải thiện chất lượng sống của được quan sát thấy ở nhóm kết hợp Ivabradine và chẹn bêta trong 3 nghiên cứu có thể đánh giá nhưng phân tích thông kê chính thức các dữ liệu này không thể tiến hành [15, 20, 25]. Trong nghiên cứu của Zarifis và cộng sự [25], điểm chỉ số EQ-5D trung bình cải thiện khi kết thúc nghiên cứu với tăng 0,3 điểm so với ban đầu (từ 0,6±0,3 đến 0,9±0,2) trong khi đó điểm VAS cải thiện khoảng 16 điểm (từ 62,8±16,3 đến 78,9±17,0). Tương tự, trong nghiên cứu của Werdan và cộng sự [15], điểm chỉ số EQ-5D cũng cải thiện từ 0,661±0,267 ban đầu lên 0,749±0,222 lúc 1 tháng và 0,827±0,196 lúc 4 tháng. Điểm VAS cải thiện từ 57,4 ±18,3 ban đầu lên 65,6±16,0 lúc 1 tháng và 72,7±15,4 lúc 4 tháng. Cuối cùng, trong nghiên cứu của Glezer và cộng sự [20], điểm VAS trung vị cải thiện từ 65 (48 – 78) lúc ban đầu đến 32 (18 – 47) lúc kết thúc điều trị.
Tính an toàn
Trong số 5 nghiên cứu có thể đánh giá, tần suất tác dụng phụ nhìn chung dao động từ 0,6% đến 9,4% tuỳ theo nghiên cứu (Bảng 2). Tác dụng phụ phổ biến nhất là nhịp tim chậm, được ghi nhận từ 0,04 đến 1,3% trong các nghiên cứu và thống kê chung cho toàn bộ là 0,1%. Các tác dụng phụ khác rất hiếm và được báo cáo không quá 1,8% bệnh nhân trong các nghiên cứu.
Bảng 2. Tính an toàn
| n % | Koester và cs. 2010 [22]
(N = 344) |
Werden và cs. 2012 [15]
(N = 2330) |
Zarifis và cs. 2015 [25]
(N = 2403) |
Perings và cs. 2016 [23]
(N = 798) |
Glezer và cs. 2018 [20]
(N = 876) |
| Tác dụng phụ | 5 (1,5) | 14 (0,6) | 31 (1,3) | 18 (2,3) | Không báo cáo (9,4) |
| Tác dụng phụ nghiêm trọng | 0 | 0 | – | 0 | – |
| Nhịp chậm | 1 (0,3) | 1 (0,04) | 8 (0,3) | 3 (0,4) | 11 (1,3) |
| Đom đóm mắt | 0 | 3 (0,13) | 3 (0,1) | 2 (0,3) | 10 (1,1) |
| Đau đầu | 1 (0,3) | 3 (0,13) | – | – | 7 (0,8) |
| Rung nhĩ | – | – | 2 (0,1) | 1 (0,1) | – |
| Chóng mặt/ngất | 2 (0,6) | – | – | 2 (0,3) | 10 (1,1) |
| Hồi hộp | – | – | – | 2 (0,3) | – |
| Dạ dày ruột | – | – | – | – | 8 (0,9) |
| Ho | – | – | – | – | 5 (0,6) |
| Rối loạn tình dục | – | – | – | – | 2 (0,2) |
| Tụt huyết áp | – | – | – | – | 8 (0,9) |
| Yếu | – | – | – | – | 16 (1,8) |
| Mệt mỏi | – | – | – | – | 1 (0,1) |
| Co giật, đau cơ ở chân | – | – | – | – | 1 (0,1) |
| Rối loạn giấc ngủ | – | – | – | – | 1 (0,1) |
| Buồn nôn | 2 (0,6) | – | – | – | – |
BÀN LUẬN
Tổng quan có hệ thống này đã đánh giá hiệu quả và tính an toàn của Ivabradine ở bệnh nhân đau thắt ngực kiểm soát không đầy đủ bằng chẹn bêta. Tổng quan này dựa phần lớn trên dữ liệu từ các nghiên cứu quan sát, bao gồm các tình huống khác nhau trong thực hành lâm sàng đời thực. Việc thêm điều trị Ivabradine vào chẹn bêta giúp giảm kéo dài tần số tim, triệu chứng đau thắt ngực và việc sử dụng nitrate tác dụng ngắn trong vòng 1 tháng sau khi khởi trị và tiếp tục cải thiện đến 4 tháng với cải thiện phân độ CCS sau 4 tháng. Ngoài ra, kết hợp Ivabradine và chẹn bêta được dung nạp tốt. Những dữ liệu này gợi ý rằng Ivabradine có thể đóng một vai trò có giá trị trong việc cá thể hoá điều trị chống đau thắt ngực sớm, đặc biệt khi được sử dụng kết hợp với thuốc chẹn bêta ở bệnh nhân đau thắt ngực ổn định mạn tính. Tối ưu hoá sớm điều trị chống đau thắt ngực sẽ đảm bảo kiểm soát tần số tim và triệu chứng nhanh hơn và hiệu quả hơn kèm với khả năng dung nạp được cải thiện.
Kết quả của phân tích này cũng phù hợp với các kết quả của hai phân tích gộp trước đó [16, 26]. Một phân tích gộp dựa trên 5 thử nghiệm lâm sàng ngẫu nhiên có đối chứng với khoảng 2400 bệnh nhân đau thắt ngực ổn định có triệu chứng [26] và một phân tích gộp với dữ liệu từ 3 nghiên cứu quan sát với khoảng 8500 bệnh nhân đau thắt ngực có triệu chứng được điều trị với Ivabradine trong 3 – 4 tháng [16] đều cho thấy giảm tần suất cơn đau thắt ngực và mức độ sử dụng nitrate tác dụng ngắn với Ivabradine trên nhiều phân nhóm bệnh nhân đau thắt ngực gặp trong thực hành lâm sàng, điều này không phụ thuộc vào tuổi, bệnh đi kèm và việc sử dụng chẹn bêta.
Bất chấp những tiến bộ và phát triển của các biện pháp điều trị và kỹ thuật tái thông mạch máu trong những thập kỷ qua, việc kiểm soát triệu chứng đau thắt ngực vẫn còn nhiều thách thức. Đau thắt ngực vẫn còn phổ biến ở những bệnh nhân cấp cứu với suy giảm chất lượng sống và những hậu quả kinh tế đối với bệnh nhân. Chẳng hạn trong nghiên cứu sổ bộ BRIDGE, hơn 50% bệnh nhân có đau thắt ngực mỗi tháng với tỉ lệ cao đau thắt ngực tương đương khi gắng sức [27]. Một điểm đáng lưu ý là tiền căn tái thông mạch máu không liên quan đến việc cải thiện triệu chứng, 40% bệnh nhân cho biết suy giảm chất lượng sống (tỉ lệ cao hơn đáng kể ở những bệnh nhân mới được chẩn đoán gần đây) và 78% ghi nhận tác động tiêu cực đến công việc. Bệnh nhân trong nghiên cứu này cũng được điều trị với trung bình ít hơn 2 loại thuốc chống đau thắt ngực [27], điều này có thể giúp giải thích một phần việc kiểm soát không hiệu quả các triệu chứng đau thắt ngực trong nhóm này.
Trong nghiên cứu sổ bộ CLARIFY, hầu hết bệnh nhân đau thắt ngực có triệu chứng ban đầu đã được điều trị trung bình với hai loại thuốc chống đau thắt ngực, trong đó chủ yếu là nhóm thuốc hàng thứ nhất (ví dụ chẹn bêta và chẹn kênh canxi) và nitrate tác dụng dài [28]. Tuy nhiên 50% vẫn còn triệu chứng trong vòng 1 năm theo dõi dù đã được điều trị và áp dụng các biện pháp tái thông mạch máu (khi được đánh giá phù hợp bởi bác sĩ điều trị) [28]. Hơn thế nữa, trong nghiên cứu có đối chứng với giả dược ORBITA đánh giá tối ưu hoá điều trị chống đau thắt ngực 6 tuần và tái thông mạch vành, hơn 50% bệnh nhân vẫn còn triệu chứng mặc dù hơn 90% được điều trị kết hợp bộ ba với chẹn bêta, chẹn kênh canxi và nitrate tác dụng dài [29-31].
Khuyến cáo của Hội Tim châu Âu năm 2020 về Hội chứng mạch vành mạn xác nhận thiếu bằng chứng cho thấy hiệu quả vượt trội giữa các nhóm điều trị chống đau thắt ngực cũng như bằng chứng hạn chế về lợi ích của việc kết hợp các thuốc chống đau thắt ngực hàng thứ nhất, không có dữ liệu về việc sử dụng các thuốc này với nitrate tác dụng dài [10]. Hướng dẫn của Hội Tim châu Âu xác nhận rằng các điều trị chống đau thắt ngực cần được cá thể hoá cho mỗi bệnh nhân, tình trạng huyết động và sự hiện diện các bệnh đi kèm, khuyến cáo việc kết hợp sớm thuốc chống đau thắt ngực hàng thứ nhất và hàng thứ hai, như Ivabradine để nhanh chóng giảm triệu chứng đau thắt ngực trong 2 – 4 tuần nếu có thể [10]. Tối ưu hoá điều trị trong đau thắt ngực được định nghĩa bởi Hội Tim châu Âu là có thể đạt được hiệu quả điều trị với dung nạp tốt để đảm bảo khả năng tuân thủ điều trị lâu dài [10], trong trường hợp này là cho cuộc sống.
Các thuốc chống đau thắt ngực liên quan huyết động hàng thứ nhất có những hạn chế về việc đạt được liều cần thiết trong thực hành lâm sàng hàng ngày. Trong nghiên cứu sổ bộ CLARIFY, hơn 33000 bệnh nhân bệnh mạch vành, 44% bệnh nhân có triệu chứng duy trì tần số tim khi nghỉ là 70 lần/phút hoặc cao hơn dù đa số (75%) đã điều trị chẹn bêta [32, 33]. Đáng chú ý là liều lượng chẹn bêta trong CLARIFY chỉ là 35 – 76% mức liều tối đa được khuyến cáo [32]. Đạt được liều chẹn bêta mục tiêu vẫn là một thách thức, ngay cả trong một nghiên cứu lâm sàng như ORBITA, 46% bệnh nhân không đạt được liều đích chẹn bêta trong 6 tuần tối ưu hoá điều trị chống đau thắt ngực [31]. Những hạn chế của việc tăng liều chẹn bêta để đạt được tần số tim mục tiêu đã được nhấn mạnh trong nghiên cứu CONTROL-2 [20]. Trong khi tăng liều để giảm tần số tim (từ 83,2±10,9 lần/phút xuống 63±8 lần/phút và tần số tim mục tiêu (55 – 60 lần/phút) đạt được ở khoảng 50% bệnh nhân, các tác dụng phụ trở nên nhiều hơn, phổ biến hơn đáng kể so với những bệnh nhân được điều trị kết hợp Ivabradine và chẹn bêta (18,4% so với 9,4%, p < 0,001). Tỉ lệ hen, khó thở, tụt huyết áp và mệt mỏi cũng cao hơn đáng kể ở nhóm tăng liều chẹn bêta.
Một chiến lược điều trị sớm với kết hợp thuốc chống đau thắt ngực hàng thứ nhất và thứ hai (như Ivabradine) để đạt được kiểm soát tần số tim và triệu chứng đau thắt ngực nhanh hơn có vẻ là một tiếp cận thực tế hơn so với việc sử dụng thuốc hàng thứ nhất đơn trị, đặc biệt là trong thực hành lâm sàng thực tế. Trong tình huống này, bệnh nhân có thể có nhiều tình huống lâm sàng và bệnh lý đồng mắc khác nhau, điều này có thể hạn chế việc sử dụng và hiệu quả của chẹn bêta hoặc việc kết hợp chúng với nhóm chẹn kênh canxi hoặc nitrate tác dụng dài. Hơn thế nữa, trong khi Ivabradine có một cơ chế tác động chính khác biệt với chẹn bêta, chẹn bêta cũng có thể ảnh hưởng đến kênh If và điện thế động ở tế bào nút (bằng ức chế gián tiếp sự tạo thành cAMP) [34], từ đó cho tác động hiệp đồng, tăng hiệu quả trong điều trị. Ivabradine cũng có một dữ liệu lâm sàng tốt về tính an toàn, không ảnh hưởng đến huyết áp và không giống chẹn bêta, thuốc cho thấy tác dụng bảo tồn tình trạng giãn mạch vành khi gắng sức [35]. Ngoài ra, Ivabradine còn giúp tăng tưới máu cơ tim tốt hơn cho mỗi tần số tim giảm so với chẹn bêta và không có nguy cơ nhịp chậm vì tần số tim giảm tuỳ theo tần số tim bệnh nhân trước điều trị [37].
Có một số hạn chế trong nghiên cứu này. Đầu tiên, chỉ có hai thử nghiệm ngẫu nhiên được đưa vào phân tích. Ngoài ra, các thiết kế quan sát nhãn mở của các nghiên cứu đưa vào phân tích có thể gây ra sai lệch trong diễn giải kết quả. Nguy cơ của sai lệch này có thể giảm một phần do hiệu quả lâm sàng lớn của can thiệp đã được ghi nhận trong các nghiên cứu với cỡ mẫu tương đối lớn. Đánh giá của chúng tôi chủ yếu tập trung vào đời thực, các nghiên cứu nhãn mở tuy thiếu nhóm chứng giả dược – có thể cũng được coi là một hạn chế, tuy nhiên các nghiên cứu đời thực cũng đã chứng minh giá trị bên ngoài và cung cấp các thông tin bổ sung cho các thử nghiệm lâm sàng ngẫu nhiên có đối chứng – các nghiên cứu mà đối tượng bệnh nhân tham gia rất chọn lọc [38]. Dữ liệu từ đời thực ngày nay được xem là một trong những thông tin đủ mạnh để hỗ trợ việc ra quyết định và liên quan đến các xét duyệt [39]. Tần số tim trung bình ở bệnh nhân trong các nghiên cứu của phân tích này từ 80,6 đến 86,9 lần/phút, là đối tượng mà việc kết hợp chẹn bêta và Ivabradine được khuyến cáo theo Hướng dẫn của Hội Tim châu Âu [10]. Vì vậy, dữ liệu từ phân tích của chúng tôi có thể không được tổng quát hoá cho bệnh nhân mà tần số tim được kiểm soát tốt với chẹn bêta.
KẾT LUẬN
Tổng quan có hệ thống và phân tích tổng hợp này cho thấy kết hợp ivabradine và chẹn bêta có hiệu quả ngay từ tháng đầu tiên của điều trị cũng như dung nạp tốt trong thực hành lâm sàng đời thực ở bệnh nhân đau thắt ngực không kiểm soát đầy đủ với chẹn bêta, bao gồm những bệnh nhân có nhiều bệnh đồng mắc. Bên cạnh điều trị theo khuyến cáo, kết hợp Ivabradine và chẹn bêta có thể là một điều trị chống đau thắt ngực hiệu quả để tối ưu hoá kiểm soát triệu chứng ở bệnh nhân đau thắt ngực ổn định mạn tính.
CÔNG BỐ
Tài trợ: Servier, Pháp đã tài trợ cho Tổng quan này và chi trả cho phí truy cập.
Viết, biên tập và các hỗ trợ khác: Trích xuất dữ liệu và phân tích thống kê được thực hiện bởi Elena Lantsova, Irina Nikitina và Alexander Akimov từ ScienceFiles, hỗ trợ bởi Yuriy Burtsev từ Servier, Nga. Hỗ trợ biên tập trong quá trình chuẩn bị và chỉnh sửa bài báo này bởi Andrea Bothwell và Kate Palmer, đại diện Springer Healthcare. Hỗ trợ này được tài trợ bởi Servier, Pháp
Quyền tác giả: Tất cả các tác giả có tên đều đáp ứng các tiêu chí về quyền tác giả của bài báo này theo ICMJE, chịu trách nhiệm về tính toàn vẹn và chấp nhận công bố bài báo này.
Sự đóng góp: Tất cả các tác giả đều đã đóng góp vào thiết kế nghiên cứu và đánh giá kết quả. Phác thảo bản thảo được chuẩn bị bởi Parvoleta Petrova. Tất cả các tác giả đã nhận xét vào các phiên bản trước của bản thảo, đọc và phê duyệt tất cả các bản nháp.
Công khai thông tin: Alexander Nedoshivin là thành viên của EORP, tổng thư ký của Hội Tim mạch Nga và đã nhận được phí diễn giả từ Berlin Chemie AG, Menarini và Servier. Parvoleta Petrova là nhân viên của Servier. Yuri Karpov đã từng là chuyên gia cố vấn, điều phối viên nghiên cứu quốc gia và là diễn giả cho Servier cũng như từng là diễn giả cho AstraZeneca, Novartis, Stada, Zentiva, Novo Nordisk, Bayer, Berlin Chemie, Sanofi và Teva.
Y đức: Đây là bài báo dựa trên các nghiên cứu đã được thực hiện trước đây và không chứa bất kì nghiên cứu mới nào với sự tham gia của người hoặc động vật được thực hiện bởi bất kì tác giả nào.
Tính sẵn có của dữ liệu: Tất cả dữ liệu được tạo hoặc được phân tích trong nghiên cứu này được bao gồm trong các bài báo đã xuất bản và các phụ lục.
Truy cập mở: Bài báo này được cấp phép theo Creative Commons Attribution-Non-
Commercial 4.0 International License, cho phép sử dụng trong mọi hoạt động, chia sẻ phi thương mại, việc chuyển ngữ, phân phối, tái sử dụng trong bất kì phương tiện hoặc định dạng nào miễn là bạn cung cấp nguồn phù hợp đối với tác giả ban đầu, cung cấp liên kết đến Creative Commons licence và cho biết nếu có thay đổi. Hình ảnh và tài liệu bên thứ ba khác trong bài viết này được bao gồm trong giấy phép Creative Commons licence, trừ khi được chỉ định đến một nguồn khác. Nếu tài liệu không được bao gồm trong Creative Commons licence và mục đích sử dụng của bạn không được cho phép bởi quy định pháp luật, bạn cần phải xin phép trực tiếp từ chủ sở hữu bản quyền. Xem bản sao của giấy phép này tại http://creativecommons.org/licenses/by-nc/4.0/.
TÀI LIỆU THAM KHẢO
- Roth GA, Mensah GA, Johnson CO, et al. Global burden of cardiovascular diseases and risk factors, 1990–2019: update from the GBD 2019 study. J Am Coll Cardiol. 2020;76:2982–3021.
- GBD 2017 Disease and Injury Incidence and Prevalence Collaborators. Global, regional, and national incidence, prevalence, and years lived with disability for 354 diseases and injuries for 195 countries and territories, 1990–2017: a systematic analysis for the Global Burden of Disease Study 2017. Lancet. 2018;392:1789–858.
- Steg PG, Greenlaw N, Tendera M, et al. Prevalence of anginal symptoms and myocardial ischemia and their effect on clinical outcomes in outpatients with stable coronary artery disease: data from the international observational CLARIFY registry. JAMA Intern Med. 2014;174:1651–9.
- Heusch G. Heart rate in the pathophysiology of coronary blood flow and myocardial ischaemia: benefit from selective bradycardic agents. Br J Pharmacol. 2008;153:1589–601.
- Ferrari R, Fox K. Heart rate reduction in coronary artery disease and heart failure. Nat Rev Cardiol. 2016;13:493–501.
- Andrews TC, Fenton T, Toyosaki N, et al. Subsets of ambulatory myocardial ischemia based on heart rate activity. Circadian distribution and response to anti-ischemic medication. The Angina and Silent Ischemia Study Group (ASIS). Circulation. 1993;88: 92–100.
- Kop WJ, Verdino RJ, Gottdiener JS, O’Leary ST, Bairey Merz CN, Krantz DS. Changes in heart rate and heart rate variability before ambulatory ischemic events(1). J Am Coll Cardiol. 2001;38:742–9.
- Pratt CM, McMahon RP, Goldstein S, et al. Comparison of subgroups assigned to medical regimens used to suppress cardiac ischemia (the Asymptomatic Cardiac Ischemia Pilot [ACIP] study). Am J Cardiol. 1996;77:1302–9.
- Bertero E, Heusch G, Munzel T, Maack C. A pathophysiological compass to personalize antianginal drug treatment. Nat Rev Cardiol. 2021;18:838–52.
- Knuuti J, Wijns W, Saraste A, et al. 2019 ESC Guidelines for the diagnosis and management of chronic coronary syndromes. Eur Heart J. 2020;41: 407–77.
- DiFrancesco D. Cardiac pacemaker I(f) current and its inhibition by heart rate-reducing agents. Curr Med Res Opin. 2005;21:1115–22.
- DiFrancesco D, Camm JA. Heart rate lowering by specific and selective I(f) current inhibition with ivabradine: a new therapeutic perspective in cardiovascular disease. Drugs. 2004;64:1757–65.
- Tardif JC, Ford I, Tendera M, Bourassa MG, Fox K, INITIATIVE Investigators. Efficacy of ivabradine, a new selective I(f) inhibitor, compared with atenolol in patients with chronic stable angina. Eur Heart J. 2005;26:2529–36.
- Tardif JC, Ponikowski P, Kahan T, ASSOCIATE Study Investigators. Efficacy of the I(f) current inhibitor ivabradine in patients with chronic stable angina receiving beta-blocker therapy: a 4-month, randomized, placebo-controlled trial. Eur Heart J. 2009;30:540–8.
- Werdan K, Ebelt H, Nuding S, Hopfner F, Hack G, Muller-Werdan U. Ivabradine in combination with beta-blocker improves symptoms and quality of life in patients with stable angina pectoris: results from the ADDITIONS study. Clin Res Cardiol. 2012;101:365–73.
- Werdan K, Perings S, Koster R, et al. Effectiveness of ivabradine treatment in different subpopulations with stable angina in clinical practice: a pooled analysis of observational studies. Cardiology. 2016;135:141–50.
- Moher D, Shamseer L, Clarke M, et al. Preferred reporting items for systematic review and metaanalysis protocols (PRISMA-P) 2015 statement. Syst Rev. 2015;4:1.
- Higgins JPT, Thomas J, Chandler J, et al. Cochrane handbook for systematic reviews of interventions. Version 6.2. 2021. https://doi.org/10.1002/14651858.ED000142. Accessed 13 Apr 2022.
- Sterne JA, Hernan MA, Reeves BC, et al. ROBINS-I: a tool for assessing risk of bias in non-randomised studies of interventions. BMJ. 2016;355: i4919.
- Glezer M, Vasyuk Y, Karpov Y. Efficacy of ivabradine in combination with beta-blockers versus uptitration of beta-blockers in patients with stable angina (CONTROL-2 study). Adv Ther.2018;35:341–52.
- Kashtalap VV, Barbarash OL, Sedykh DY, Krivoshapova KE, Tsygankova DP, Tsygankova OV. Possibilities of combination of beta-blockers and ivabradine in patients with stable angina pectoris. Rational Pharmacother Cardiol. 2019;15:663–9.
- Koester R, Kaehler J, Ebelt H, Soeffker G, Werdan K, Meinertz T. Ivabradine in combination with betablocker therapy for the treatment of stable angina pectoris in every day clinical practice. Clin Res Cardiol. 2010;99:665–72.
- Perings S, Stockl G, Kelm M, RESPONSIfVE study investigators. Effectiveness and tolerability of ivabradine with or without concomitant beta-blocker therapy in patients with chronic stable angina in routine clinical practice. Adv Ther. 2016;33:1550–64.
- Zaky H, Elzein H, Alsheikh-Ali AA, Al-Mulla A. Short-term effects of ivabradine in patients with chronic stable ischemic heart disease. Heart Views. 2013;14:53–5.
- Zarifis J, Grammatikou V, Kallistratos M, Katsivas A, on behalf of the Investigators of the Prospective, Noninterventional Observational Study of the Antianginal Efficacy of Ivabradine During a Month Treatment of a Greek Population With Coronary Artery Disease. Treatment of stable angina pectoris with ivabradine in everyday practice: a pan-hellenic, prospective, noninterventional study. Clin Cardiol. 2015;38:725–32.
- Tendera M, Borer JS, Tardif JC. Efficacy of I(f) inhibition with ivabradine in different subpopulations with stable angina pectoris. Cardiology. 2009;114:116–25.
- Manolis AJ, Ambrosio G, Collins P, et al. Impact of stable angina on health status and quality of life perception of currently treated patients. The BRIDGE 2 survey. Eur J Intern Med. 2019;70:60–7.
- Mesnier J, Ducrocq G, Danchin N, et al. International observational analysis of evolution and outcomes of chronic stable angina: the multinational CLARIFY study. Circulation. 2021;144:512–23.
- Al-Lamee R, Howard JP, Shun-Shin MJ, et al. Fractional flow reserve and instantaneous wave-free ratio as predictors of the placebo-controlled response to percutaneous coronary intervention in stable single-vessel coronary artery disease. Circulation. 2018;138:1780–92.
- Al-Lamee R, Thompson D, Dehbi HM, et al. Percutaneous coronary intervention in stable angina (ORBITA): a double-blind, randomised controlled trial. Lancet. 2018;391:31–40.
- Foley M, Rajkumar CA, Shun-Shin M, et al. Achieving optimal medical therapy: insights from the ORBITA trial. J Am Heart Assoc. 2021;10: e017381.
- Tendera M, Fox K, Ferrari R, et al. Inadequate heart rate control despite widespread use of beta-blockers in outpatients with stable CAD: findings from the international prospective CLARIFY registry. Int J Cardiol. 2014;176:119–24.
- Steg PG, Ferrari R, Ford I, et al. Heart rate and use of beta-blockers in stable outpatients with coronary artery disease. PLoS ONE. 2012;7: e36284.
- DiFrancesco D, Borer JS. The funny current: cellular basis for the control of heart rate. Drugs. 2007;67(Suppl 2):15–24.
- Simon L, Ghaleh B, Puybasset L, Giudicelli JF, Berdeaux A. Coronary and hemodynamic effects of S16257, a new bradycardic agent, in resting and exercising conscious dogs. J Pharmacol Exp Ther. 1995;275:659–66.
- Tagliamonte E, Cirillo T, Rigo F, et al. Ivabradine and bisoprolol on doppler-derived coronary flow velocity reserve in patients with stable coronary artery disease: beyond the heart rate. Adv Ther. 2015;32:757–67.
- Borer JS, Le Heuzey JY. Characterization of the heart rate-lowering action of ivabradine, a selective I(f) current inhibitor. Am J Ther. 2008;15:461–73.
- Kennedy-Martin T, Curtis S, Faries D, Robinson S, Johnston J. A literature review on the representativeness of randomized controlled trial samples and implications for the external validity of trial results. Trials. 2015;16:495.
- Purpura CA, Garry EM, Honig N, Case A, Rassen JA. The role of real-world evidence in FDA-approved new drug and biologics license applications. Clin Pharmacol Ther. 2022;111:135–44.







