1.Tổng quan:
Những bệnh cảnh tim mạch khác nhau có thể có lợi từ việc sử dụng dụng cụ hỗ trợ huyết động qua da bao gồm: suy tim mất bù cấp, viêm cơ tim tiến triển nhanh, nhồi máu cơ tim có shock tim và can thiệp mạch vành qua da bệnh nhân nguy cơ cao.
Ths.Bs.Hồ Minh Tuấn
Khoa Tim Mạch Can Thiệp, BV Tim Tâm Đức
Dụng cụ hỗ trợ huyết động qua da lý tưởng là: an toàn, dễ sử dụng, nhiều tác dụng đủ để đáp ứng cần thiết trong các tình huống lâm sàng khác nhau, bên cạnh đó cần có hỗ trợ huyết động tối đa và bảo vệ chống thiếu máu cơ tim [1].
Nhồi máu cơ tim cấp chiếm 75% tất cả các shock tim và shock tim chiếm tỉ lệ 6-8% trong các bệnh nhân nhồi máu cơ tim[2][3][4]. Nguyên nhân gây ra Shock tim trong nhồi máu cơ tim là do: suy chức năng thất trái (chiếm 80%), biến chứng cơ học hở van hai lá cấp do đứt cơ trụ, dây chằng (chiếm 6,9%), thủng vách liên thất (3,9%), thủng thành tự do thất trái (chiếm 1,4%). Tái tưới máu mạch vành cấp cứu là điều trị quan trọng nhất trong shock tim do nhồi máu cơ tim[5].
Với mục đích này chúng tôi tổng kết dụng cụ hỗ trợ huyết động qua da trong can thiệp mạch vành nguy cơ cao.
2.Chỉ định lâm sàng dụng cụ hỗ trợ huyết động qua da
– Theo Hướng Dẫn Tái Tưới Máu Mạch Vành của Hiệp Hội Tim Mạch Châu Âu 2014: Bóng đối xung động mạch chủ (IABP) chỉ định (Class IIa) ở bệnh nhân huyết động không ổn định hoặc shock tim do biến chứng cơ học của Nhồi máu cơ tim[5].
– Theo Hướng Dẫn Nhồi Máu Cơ Tim ST Chênh Lên của Hiệp Hội Tim Mạch Hoa Kỳ 2013: Bóng đối xung động mạch chủ (IABP) chỉ định (Class IIa) ở bệnh nhân shock tim sau Nhồi máu cơ tim ST chênh lên[6].
– Theo Hướng Dẫn tái tưới máu mạch vành của Hiệp Hội Tim Mạch Hoa Kỳ 2011[7]:
+ Dụng cụ hổ trợ huyết động chỉ định (Class I) ở bệnh nhân shock tim sau Nhồi máu cơ tim ST chênh lên.
+ Dụng cụ hỗ trợ huyết động chỉ định (Class IIb) ở bệnh nhân can thiệp mạch vành qua da nguy cơ cao.
3. Mục đích và nguyên lý hoạt động của dụng cụ hỗ trợ huyết động qua da
3.1.Bóng đối xung động mạch chủ (IABP)[8]
Bóng đối xung động mạch chủ thường được đặt qua đường động mạch đùi và bóng nằm trong động mạch chủ giữa động mạch dưới đòn trái và động mạch thận.
Nguyên lý hoạt động:
– Khi bóng bơm kỳ tâm trương (Hình 1A): tạo dòng máu ngược dẫn đến:
o Tăng huyết áp tâm trương ở cung động mạch chủ
o Tăng tưới máu mạch vành kỳ tâm trương
o Tăng huyết áp trung bình
o Tăng tưới máu hệ thống
o Tăng cung cấp oxy
– Khi bóng xả kỳ tâm thu (Hình 1B): giảm hậu tải dẫn đến:
o Giảm thể tích và áp lực máu cung động mạch chủ
o Giảm hậu tải dẫn đến giảm nhu cầu oxy cơ tim
o Giảm thể tích nhát bóp
o Giảm thời gian tâm thu dẫn đến tăng thời gian tâm trương, tăng tưới máu mạch vành
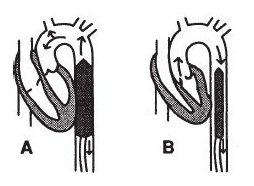
Hình 1. Bóng đối xung động mạch chủ đặt ở vị trí động mạch chủ xuống qua đường động mạch đùi. A: bơm bóng; B: xả bóng
3.2.Dụng cụ Impella[8]
Sử dụng bơm theo trục thu nhỏ đặt trong ống thông Pigtail, hút máu trực tiếp từ thất trái đưa vào động mạch chủ (Hình 2). Có hai dụng cụ Impella là : Impella 2.5: vận chuyển lưu lượng máu 2,5 lít/phút và Impella 5.0: vận chuyển lưu lượng máu 5 lít/phút.
Impella được đặt qua động mạch đùi, đưa đầu ống thông Pigtail vào thất trái, với kích cỡ Impella 2.5 là 13 French và Impella 5.0 là 21 French.
Lợi điểm tim mạch của Impella là hỗ trợ huyết động và bảo vệ chống thiếu máu cơ tim:
+ Hút máu từ thất trái: Trực tiếp giảm tải thất trái do đó giảm áp lực cuối tâm trương thất trái, giảm nhu cầu oxy cơ tim, giảm áp lực mạch máu phổi.
+ Bơm máu vào Động mạch chủ: Tăng huyết áp trung bình.
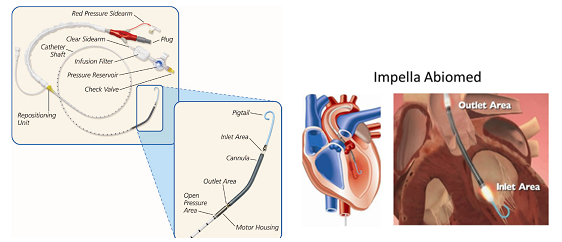
Hình 2. Implla gồm lỗ hút máu vào ở thất trái và bơm máu ra ở ĐMC (vòng tua tối đa 51000 vòng/phút), bơm liên tục 2,5 lít máu/phút
3.3.Dụng cụ TandemHeart System[8]
Là dụng cụ hỗ trợ huyết động cầu nối giữa nhĩ trái và động mạch đùi, bằng cách sử dụng bơm ly tâm hút máu từ nhĩ trái và bơm liên tục vào động mạch đùi với tốc độ 3,5-4 lít/phút.
Dụng cụ được đặt qua đường động mạch và tĩnh mạch đùi (Hình 3):
+ Tĩnh mạch đùi: ống thông cỡ 21 French qua tĩnh mạch đùi, qua vách liên nhĩ đặt vào nhĩ trái, hút máu từ nhĩ trái và nối với bộ quay ly tâm ngoài.
+ Động mạch đùi: ống thông cỡ 12, 15 hoặc 17 French tiếp cận động mạch đùi nối với bộ quay ly tâm ngoài bơm máu vào đông mạch đùi.
Dụng cụ có tác dụng hổ trợ huyết động và bảo vệ chống thiếu máu cơ tim:
+ Hút máu từ nhĩ trái: gián tiếp làm giảm áp lực thất trái, giảm áp lực mạch máu phổi và giảm nhu cầu oxy cơ tim.
+ Bơm máu vào động mạch đùi: làm tăng huyết áp trung bình và tăng tưới máu hệ thống.
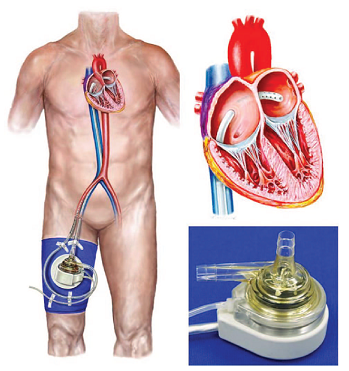
Hình 3. Tandemheart gồm ống thông 21 French vào nhĩ trái và ống thông 15 hoặc 17 French vào động mạch đùi. Mô tơ quay ly tâm ngoài có tốc độ tối đa 7500 vòng /phút, tốc độ hút và bơm máu liên tục 4 lít/phút.
3.4.Dụng cụ ECMO[9]
ECMO (Extracorporeal membrane oxygenation ) là dụng cụ bắc cầu qua tim phổi, trao đổi oxy ngoài cơ thể (Hình 4). ECMO được cài đặt theo 3 kiểu:
+ Tĩnh mạch- động mạch (V-A ECMO): cho phép trao đổi khí và hỗ trợ huyết động, máu được bơm từ tĩnh mạch qua động mạch.
+ Tĩnh mạch- tĩnh mạch (V-V ECMO): máu được rút từ tĩnh mạch, trao đổi khí và bơm trở lại tĩnh mạch, không có hỗ trợ huyết động.
+ Động mạch- tĩnh mạch (A-V ECMO): hổ trợ trao đổi oxy bằng cách sử dụng áp lực máu động mạch của chính bệnh nhân bơm máu từ động mạch vào tĩnh mạch
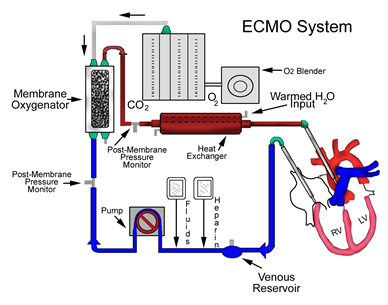
Hình 4. Hút máu từ nhĩ trái, vận chuyển của máu được hổ trợ bởi bơm bên ngoài, đẩy máu qua màng lọc cho phép trao đổi oxy và CO2, sau đó được làm ấm và quay lại tuần hoàn cơ thể.
4.Các nghiên cứu lâm sàng về dụng cụ hỗ trợ huyết động qua da
4.1.Bóng đối xung động mạch chủ ( IABP)
Nghiên cứu AMI CRISP[10]: nghiên cứu tiến cứu, ngẫu nhiên, đa trung tâm gồm 337 bệnh nhân NMCT ST chênh lên không có shock tim chia làm 2 nhóm: can thiệp mạch vành có bóng đối xung động mạch chủ và can thiệp mạch vành không có bóng đối xung động mạch chủ:
+ Đánh giá vùng hoại tử cơ tim vào ngày thứ 3-5 sau can thiệp bằng MRI: khác biệt không có ý nghĩa thống kê
+ Kết quả theo dõi lâm sàng ở thời điểm 30 ngày và 6 tháng về chảy máu, biến chứng mạch máu, tử vong: không khác biệt giữa 2 nhóm.
+ Tuy nhiên, có 8,5% bệnh nhân trong nhóm can thiệp mạch vành không có bóng đối xung động mạch chủ cần đặt bóng đối xung sau đó. Điều này cho thấy: bóng đối xung động mạch chủ cần sẵn sàng cho NMCT ST chênh lên nguy cơ cao hơn là sử dụng thường quy.
Nghiên cứu BSIC 1[11]: nghiên cứu tiến cứu, ngẫu nhiên, đa trung tâm gồm 301 bệnh nhân có EF<30% và bệnh mạch vành lan tỏa (Jeopardy score≥8/12) được can thiệp mạch vành chia làm 2 nhóm: có và không có đặt bóng đối xung động mạch chủ. Kết quả:
+ Biến cố tim mạch chính trong thời gian nằm viện gồm: tử vong, NMCT, tai biến mạch máu não và tái tưới máu mạch vành: nhóm có đặt bóng đối xung động mạch chủ :15,2% và nhóm không có đặt bóng đối xung động mạch chủ: 16%, khác biệt không có ý nghĩa thống kê ( P= 0,85; OR: 0,94; khoảng tin cậy 95%( 0,51-1,76)).
+ Tử vong do mọi nguyên nhân trong 6 tháng: nhóm có đặt bóng đối xung động mạch chủ: 4,6% và nhóm không có đặt bóng đối xung động mạch chủ: 7,4%, khác biệt không có ý nghĩa thống kê ( P= 0,32; OR: 0,61; khoảng tin cậy 95%( 0,24-1,62))
Nghiên cứu SHOCK-II[12]:nghiên cứu ngẫu nhiên, tiến cứu, đa trung tâm gồm 600 bệnh nhân shock tim do NMCT ST chênh lên hoặc không chênh lên, tất cả bệnh nhân được can thiệp mạch vành cấp cứu hoặc mổ bắc cầu mạch vành, chia làm 2 nhóm: nhóm có đặt bóng đối xung động mạch chủ và nhóm không có đặt bóng đối xung động mạch chủ. Kết quả:
+ Tử vong do mọi nguyên nhân trong 30 ngày: nhóm có đặt bóng đối xung động mạch chủ : 39,7% và nhóm không có đặt bóng đối xung động mạch chủ: 41,3%, khác biệt không có ý nghĩa thống kê ( P= 0,69; OR: 0,96; khoảng tin cậy 95%( 0,79-1,17)).
+ Các tỉ lệ: chảy máu nặng, thiếu máu chi, nhiễm trùng huyết, đột quỵ trong thời gian nằm viện khác biệt không có ý nghĩa thống kê giữa 2 nhóm.
4.2.Dụng cụ Impella:
Nghiên cứu PROTECT-I [13]:nghiên cứu tiến cứu, đa trung tâm gồm 20 bệnh nhân can thiệp mạch vành nguy cơ cao (EF<35%, can thiệp thân chung trái không bảo vệ hoặc chỉ còn 1 cầu nối mạch vành thông thường), có dụng cụ Impella 2.5 hỗ trợ. Kết quả 30 ngày cho thấy dụng cụ sử dụng an toàn:
+ Biến cố tim mạch chính trong 30 ngày là: 20%.
+ Không có tổn thương van Động mạch chủ, thủng tim hay thiếu máu chi. Không có bệnh nhân thay đổi xấu huyết động trong thời gian can thiệp.
+ Có 10% huyết tán nhẹ thoáng qua.
Nghiên cứu PROTECT-II[14]: nghiên cứu tiến cứu, đa trung tâm, ngẫu nhiên gồm 452 bệnh nhân bệnh 3 nhánh mạch vành hoặc thân chung trái có phân xuất tống máu <30%. Được can thiệp mạch vành qua da, chia làm 2 nhóm: nhóm đặt bóng đối xung động mạch chủ và nhóm đặt dụng cụ Impella 2.5 trong thời gian can thiệp. Theo dõi cộng dồn biến cố chính gồm: tử vong do mọi nguyên nhân, NMCT, đột quỵ, tái tưới máu mạch vành, suy thận cấp, tụt huyết áp nặng trong thủ thuật, hồi sức tim phổi, nhịp nhanh thất, hở chủ và thất bại trên hình ảnh can thiệp. Kết quả:
+ Trong 30 ngày: tỉ lệ biến cố cộng dồn: nhóm can thiệp + đặt bóng đối xung động mạch chủ: 40,1% và nhóm can thiệp + đặt Impella: 35,1% khác biệt không có ý nghĩa thống kê P=0,227.
+ Trong 90 ngày: tỉ lệ biến cố cộng dồn: nhóm can thiệp + đặt bóng đối xung động mạch chủ: 49,3% và nhóm can thiệp + đặt Impella: 40,6% khác biệt không có ý nghĩa thống kê P=0,066. Tuy nhiên, có xu hướng cải thiện hơn trong đặt dụng cụ Impella 2.5.
4.3. Tendamheart system
– Các nghiên cứu lâm sàng so sánh Tendamheart và bóng đối xung động mạch chủ trong can thiệp bệnh nhân shock tim do NMCT can thiệp mạch vành cho thấy không có sự khác biệt về tử vong. Tuy nhiên, tỉ lệ chảy máu nặng của Tendamheart là 40-90% [16][17][18]
– Nghiên cứu 37 bệnh nhân có nguy cơ cao can thiệp mạch vành qua da hoặc shock tim: 74% đặt dụng cụ Tendamheart trong lúc thủ thuật, 26% cần duy trì dụng cụ sau đó. Kết quả 71% sống và xuất viện sau đó theo dõi đến 30 ngày không có tử vong thêm. Tuy nhiên, tỉ lệ xuất huyết cần truyền máu là 82% [15].
4.4. ECMO
–Tĩnh mạch-động mạch ECMO (VA-ECMO) thường chỉ định trong các trường hợp shock tim dù đã điều trị tích cực đủ tiền tải, > 2 loại vận mạch, bóng đối xung động mạch chủ nhưng vẫn còn dấu hiệu cung lượng tim thấp [20]
– Nghiên cứu hồi cứu 33 bệnh nhân gồm: 15 ngưng tim và 18 shock tim nặng tiến triển. Tỉ lệ sống còn ở bệnh nhân shock tim do thiếu máu cơ tim là 6,25% và nguyên nhân khác là 35,3%, nguyên nhân tử vong là do shock không hồi phục suy đa cơ quan [19].
5.Kết luận:
Dụng cụ hỗ trợ huyết động tim được sử dụng ngày càng nhiều trong những năm qua đặt biệt là bóng đối xung động mạch chủ. Nhiều nghiên cứu thực hiện đánh giá lợi ích của dụng cụ hỗ trợ huyết động ở những bệnh nhân nguy cơ cao can thiệp mạch vành hoặc shock tim do nhồi máu cơ tim. Khuyến cáo của các hiệp hội tim mạch Hoa Kỳ và Châu Âu rõ ràng hơn trong những trường hợp shock tim do nhồi máu cơ tim. Tuy nhiên, cần có thêm các nghiên cứu sàng về dụng cụ hỗ trợ huyết động trong can thiệp mạch vành.
Tài liệu tham khảo
1. Daniel Burkhoff et al. The Science Behind Percutaneous Hemodynamic Support: A Review and Comparison of Support Strategies; Catheterization and Cardiovascular Interventions (2012).
2. Lindholm MG, Kober L, Boesgaard S, Torp-Pedersen C, Aldershvile J, Trandolapril Cardiac Evaluation study. Cardiogenic shock complicating acute myocardial infarction; prognostic impact of early and late shock development. Eur Heart J 2003;24(3):258–265
3. Katz JN, Stebbins AL, Alexander JH, Reynolds HR, Pieper KS, RuzylloW,Werdan K, Geppert A, Dzavik V, Van de Werf F, Hochman JS, Investigators T. Predictors of 30-day mortality in patients with refractory cardiogenic shock following acutemyocardial infarction despite a patent infarct artery. Am Heart J 2009;158(4):680–687.
4. Zeymer U, Vogt A, Zahn R,Weber MA, Tebbe U, Gottwik M, Bonzel T, Senges J, Neuhaus KL, Arbeitsgemeinschaft Leitende Kardiologische K. Predictors of in-hospital mortality in 1333 patients with acute myocardial infarction complicated by cardiogenic shock treated with primary percutaneous coronary intervention (PCI); Results of the primary PCI registry of the Arbeitsgemeinschaft Leitende Kardiologische Krankenhausarzte (ALKK). Eur Heart J 2004;25(4):322–328.
5. StephanWindecker et al. 2014 ESC/EACTS Guidelines onmyocardial Revascularization; European Heart Journal Advance Access published September 10, 2014
6. Patrick T. OGara et al. 2013 ACCF/AHA Guideline for the Management of ST-Elevation Myocardial Infarction; Journal of the American College of Cardiology Vol. 61, No. 4, 2013
7. Glenn N. Levin et al. 2011 ACCF/AHA/SCAI Guideline for Percutaneous Coronary Intervention; Journal of the American College of Cardiology Vol. 58, No. 24, 2011
8. Srihari S. Naidu; Novel Percutaneous Cardiac Assist Devices: The Science of and Indications for Hemodynamic Support; Circulation. 2011;123:533-543.
9. Guillermo Martinez, et al. Extracorporeal Membrane Oxygenation in Adults; Cont Edu Anaesth Crit Care and Pain.2012;12(2):57-61
10. Manesh R. Patel et al. Intra-aortic Balloon Counterpulsation and Infarct Size in Patients With Acute Anterior Myocardial Infarction Without Shock, JAMA September 28, 2011
11. Divaka Perera et al. Elective Intra-aortic Balloon Counterpulsation During High-Risk Percutaneous Coronary Intervention; JAMA, August 25, 2010—Vol 304, No. 8
12. Holger Thiele et al. Intraaortic Balloon Support for Myocardial Infarction with Cardiogenic Shock; n engl j med 367;14 nejm.org october 4, 2012
13. Simon R. Dixon et al. A Prospective Feasibility Trial Investigating the Use of the Impella 2.5 System in Patients Undergoing High-Risk Percutaneous Coronary Intervention (The PROTECT I Trial); J Am Coll Cardiol Intv 2009;2:91– 6
14. William W. ONeill et al. A Prospective, Randomized Clinical Trial of Hemodynamic Support With Impella 2.5 Versus Intra-Aortic Balloon Pump in Patients Undergoing High-Risk Percutaneous Coronary Intervention The PROTECT II Study; Circulation. 2012;126:1717-1727
15. Thomas JL et al. Use of a percutaneous left ventricular assist device for high-risk cardiac interventions and cardiogenic shock. J Invasive Cardiol. 2010
16. Thiele H et al.. Randomized comparison of intra-aortic balloon support with a percutaneous left ventricular assist device in patients with revascularized acute myocardial infarction complicated by cardiogenic shock. Eur Heart J. 2005;26:1276 –1283
17. Burkhoff D et al. A randomized multicenter clinical study to evaluate the safety and efficacy of the Tandem Heart percutaneous ventricular assist device versus conventional therapy with intra-aortic balloon pumping for treatment of cardiogenic shock. Am Heart J. 2006;152: 469.e1– e8
18. Sjauw KD et al. Percutaneous mechanical cardiac assist in myocardial infarction: where are we now, where are we going? Acute Card Care. 2007;9:222–230.
19. Satya Shreenivas et al. VA ECMO for Cardiac Arrest and Severe Refractory Cardiogenic Shock; Circulation. 2012; 126:A55
20. Chen YS, Yu HY, Huang SC, et al. Extracorporeal membrane oxygenation support can extend the duration of cardiopulmonary resuscitation.Crit Care Med2008;36:2529–35







