TS. PHẠM HỮU VĂN
6.2 Định nghĩa và đánh giá gánh nặng rung nhĩ
Thuật ngữ ‘gánh nặng’ đề cập đến các khía cạnh khác của AF khác nhau (ví dụ: dịch tễ học, kinh tế). [144] Về theo dõi liên tục dựa trên thiết bị, ‘gánh nặng AF’ hiện được định nghĩa là tổng thời gian dành cho AHRE / AF dưới lâm sàng trong một khoảng thời gian theo dõi cụ thể (ví dụ: 1 ngày). Cần ghi nhận cả thời gian AF và khoảng thời gian theo dõi khi báo cáo gánh nặng AF (hầu hết các nghiên cứu báo cáo thời gian tối đa dành cho AF trong khoảng thời gian 24 giờ), nhưng các biện pháp tối ưu vẫn chưa được xác định. [152] Thuật ngữ ‘gánh nặng AF’ (AF burden) khác với ‘gánh nặng của AF’ (Burden of AF), thuật ngữ sau đề cập đến hậu quả AF.
Gánh nặng AF lâm sàng được xác định thường quy bằng mẫu thời gian AF [146] (Bảng 4) và theo dõi điện tâm đồ ngắt quãng, [153] không tương ứng tốt với theo dõi điện tâm đồ dài hạn. Mối quan hệ của gánh nặng AF lâm sàng với các kết cục cụ thể không được đặc trưng rõ ràng, [154] nhưng có thể liên quan đến nguy cơ cao hơn về biến cố HF [155] và tử vong do mọi nguyên nhân, [156] trong khi mối liên quan với chất lượng cuộc sống (QoL) là phức tạp và thiếu dữ liệu về suy giảm nhận thức / sa sút trí tuệ. [86] Dữ liệu thử nghiệm ngẫu nhiên có đối chứng (RCT) gần đây liên tục cho thấy nguy cơ thuyên tắc huyết khối tồn lưu thấp hơn đáng kể ở những bệnh nhân kháng đông có AF kịch phát so với dai dẳng, [156159] trong khi dữ liệu quan sát dựa trên thử nghiệm trước đó [161,162] còn mâu thuẫn. Trong số những bệnh nhân không dùng kháng đông, nguy cơ đột quỵ thấp hơn với AF kịch phát so với AF không kịch phát, [156] và gánh nặng AF toàn phần lớn hơn (nhưng không phải là đợt AF dài nhất) có liên quan độc lập với tỷ lệ biến cố thuyên tắc huyết khối cao hơn.[163] Gánh nặng AF lâm sàng có thể ảnh hưởng đến đáp ứng với liệu pháp kiểm soát nhịp. [164,165] Sự hiện diện của AF > 6 giờ mỗi tuần (đặc biệt khi tiến triển đến > 24 giờ hàng tuần) có liên quan đến tăng tỷ lệ tử vong, đặc biệt là ở phụ nữ. [166]
Bằng chứng hiện có về mối liên quan của gánh nặng AF với các kết cục liên quan đến AF không đủ để hướng dẫn điều trị và không phải là yếu tố chính trong quyết định điều trị. Quản lý toàn diện các yếu tố nguy cơ tim mạch có thể thay đổi / bệnh đi kèm làm giảm gánh nặng AF (mục 10.3).
6.3 Tiến triển rung nhĩ
Chuyển từ AF kịch phát sang AF không kịch phát (hoặc từ AF dưới lâm sàng sang AF lâm sàng) [154,167169] thường được đặc trưng bằng tái tạo cấu trúc tâm nhĩ gia tăng hoặc làm xấu đi bệnh cơ tâm nhĩ. [170,171]
Đánh giá sự tiến triển của AF phụ thuộc vào khoảng thời gian theo dõi nhịp và nền bệnh cơ bản. [172,173] Tỷ lệ tiến triển AF kịch phát hàng năm được báo cáo nằm trong khoảng từ < 1% đến 15% (đến 27 đến 36% trong các nghiên cứu với 10 năm theo dõi). [169,174] Các yếu tố nguy cơ đối với tiến triển AF bao gồm tuổi, HF, tăng huyết áp, CKD, bệnh phổi mãn tính, đái tháo đường, đột quỵ trước đó và kích thước tâm nhĩ trái (LA), [167] trong khi giá trị dự đoán bổ sung của các chỉ dấu sinh học hiện chưa được xác định rõ. Tuổi già có liên quan đến AF vĩnh viễn, [82,117,154] và các yếu tố kích hoạt khác nhau cũng có thể đóng một vai trò nào đó, với các mô hình tiến triển khác nhau do sự tương tác của chúng với tái cấu trúc nền bệnh. [171] Tiến triển thành AF dai dẳng / vĩnh viễn có liên quan đến các biến cố tim mạch bất lợi, nhập viện và tử vong, [166] nhưng vẫn chưa rõ liệu sự tiến triển của AF có phải là yếu tố quyết định tiên lượng xấu hay đúng hơn là chỉ dấu của một bệnh cơ bản tiến triển / nền bệnh. [175,176] Tác động thực sự của các can thiệp điều trị khác nhau ở các giai đoạn bệnh khác nhau đối với sự tiến triển của AF và các kết cục liên quan cũng ít được xác định rõ hơn.
6.4 Bệnh cơ tâm nhĩ: định nghĩa, phân loại, ý nghĩa lâm sàng và đánh giá chẩn đoán
Tiến bộ quan trọng trong việc hiểu cơ chế AF và khả năng sinh huyết khối xem xét lại vai trò của bệnh cơ tim tâm nhĩ (tức là những thay đổi về cấu trúc, kiến trúc, co bóp hoặc điện sinh lý của tâm nhĩ với các biểu hiện lâm sàng có liên quan). [170]
Phân loại lâm sàng bệnh cơ tim tâm nhĩ phải dựa trên cấu trúc, hình thái, chức năng điện và cơ của tâm nhĩ, và chẩn đoán có thể dựa trên các thông số dễ tiếp cận (ví dụ: nguyên nhân, trạng thái huyết khối, [177] và thể tích / chức năng LA bất thường). [178] Các vấn đề lâm sàng chính trong AF (tức là phòng ngừa các biến chứng huyết khối tắc mạch và sự tiến triển của AF) bị ảnh hưởng bởi quá trình tái cấu trúc tâm nhĩ; và quan trọng là AF không chỉ là một yếu tố nguy cơ mà còn là một dấu hiệu của bệnh cơ tim tâm nhĩ, có thể giải thích về thiếu mối quan hệ thời gian giữa AF được phát hiện và đột quỵ. [179]
Thuật toán chẩn đoán bệnh cơ tâm nhĩ nên theo cách tiếp cận từng bước, xác định các yếu tố nguy cơ của bệnh cơ tâm nhĩ, [170] rối loạn chức năng cơ và điện học tâm nhĩ, [180] và tăng nguy cơ huyết khối. [181] Cần có thêm dữ liệu để xác định ý nghĩa tiên lượng và điều trị của các hình thái bệnh cơ tâm nhĩ khác nhau về hình thái chức năng.
- Tầm soát rung nhĩ
Nhiều yếu tố (như tần suất AF ngày càng tăng, phát hiện AF mà trước đó còn chưa từng biết ở khoảng 10% tổng số đột quỵ do thiếu máu cục bộ, [4,182] tỷ lệ AF không triệu chứng cao, [117] tiềm năng ngăn ngừa đột quỵ liên quan đến AF với điều trị thích hợp và ngày càng có nhiều công cụ phát hiện AF) đã thúc đẩy các sáng kiến quốc tế nhằm triển khai sàng lọc AF trong thực hành lâm sàng. [172]
AF lâm sàng không triệu chứng có liên quan độc lập với tăng nguy cơ đột quỵ và tử vong so với AF có triệu chứng. [82,117,127,183] Dữ liệu thu được từ các nghiên cứu về AF không triệu chứng được phát hiện ngẫu nhiên là con số gần đúng nhất có thể về nguy cơ đột quỵ và tử vong ở các đối tượng AF được phát hiện do tâm soát, do việc trì hoãn điều trị để làm rõ (discern) bệnh sử tự nhiên sẽ là phi đạo đức. Dữ liệu quan sát cho thấy AF phát hiện do tâm soát đáp ứng với điều trị tương tự như AF được phát hiện bởi chăm sóc định kỳ, [183] do đó ưa chuộng việc sàng lọc AF.
Mặc dù AF đáp ứng nhiều tiêu chí để sàng lọc bệnh [184] (Hình 2 bổ sung), dữ liệu RCT để xác nhận những lợi ích sức khỏe từ việc sàng lọc AF và thông báo cho việc lựa chọn các chương trình và chiến lược sàng lọc tối ưu để thực hiện vẫn còn khan hiếm. [185,186] Các tiến bộ trong công nghệ áo để mặc tầm soát có thể sẽ mang lại các tùy chọn rẻ tiền và thiết thực để phát hiện AF và đánh giá gánh nặng AF trong tương lai gần.
7.1 Các công cụ tầm soát
Các hệ thống được sử dụng để tâm soát AF được thể hiện trong Bảng 5 và Hình 6. [173,187]
Công nghệ sức khỏe di động (mobile heath technologies) đang phát triển nhanh chóng để phát hiện AF và các mục đích khác (hơn 100 000 áp dụng sức khỏe lưu động và hơn 400 máy theo dõi hoạt động có thể mặc được). [197] Cần thận trọng khi sử dụng chúng trên lâm sàng, vì nhiều loại này không được xác nhận về mặt lâm sàng. Một số nghiên cứu đã đánh giá khả năng phát hiện AF bằng cách sử dụng đồng hồ thông minh, [198,199] do đó mở ra triển vọng mới để phát hiện AF nhắm mục tiêu đến các nhóm dân số cụ thể có nguy cơ. Máy học và trí tuệ nhân tạo (artificial intelligence) có thể có khả năng xác định các cá nhân có các đợt AF trước đó từ bản ghi ECG nhịp xoang, [200] sẽ là một bước đột phá công nghệ lớn trong phát hiện AF. [200]
Nghiên cứu của Apple Heart [201] gồm 419 297 người dùng ứng dụng đồng hồ thông minh tự đăng ký (độ tuổi trung bình là 40 tuổi) ở Hoa Kỳ, trong đó 0,5% nhận được thông báo mạch không đều (0,15% trong số những người 65 tuổi năm). Theo sau (ghi nhận được khởi kích) theo dõi bằng miếng dán ECG 1 tuần phát hiện AF ở 34% người tham gia theo dõi. Nghiên cứu về Tim của Huawei [202] gồm 187 912 cá nhân (trung bình 35 tuổi, 86,7% nam), trong đó 0,23% nhận được thông báo ‘nghi ngờ AF’. Trong số những người được theo dõi hiệu quả, 87,0% được xác nhận là có AF, với giá trị dự báo dương tính của tín hiệu chụp cắt lớp quang tuyến là 91,6% [Khoảng tin cậy (CI) 95% [91,5 – 91,8]. Trong số những người có AF được xác định, 95,1% đã tham gia chương trình quản lý AF tích hợp bằng Ứng dụng AF di động (mAFA).
Khi AF được phát hiện bằng một công cụ sàng lọc, gồm thiết bị di động hoặc thiết bị có thể mặc được, một đường ghi ECG một đạo trình ≥ 30 s hoặc ECG 12 đạo trình cho thấy AF được phân tích do bác sĩ có chuyên môn về giải thích nhịp ECG là cần thiết để thiết lập chẩn đoán xác định AF (các thiết bị có khả năng ghi điện tâm đồ cho phép phân tích trực tiếp các dấu vết do thiết bị cung cấp). Khi phát hiện AF không dựa trên bản ghi điện tâm đồ (ví dụ: với các thiết bị sử dụng máy chụp cắt lớp quang tuyến) hoặc trong trường hợp không chắc chắn trong việc giải thích theo dõi điện tâm đồ do thiết bị cung cấp, phải có chẩn đoán điện tâm đồ xác nhận bằng cách sử dụng bản ghi điện tâm đồ bổ sung (ví dụ: điện tâm đồ 12 chuyển đạo , theo dõi Holter, v.v.)
Dữ liệu báo cáo ở Bảng 5 nên được giải thích một cách thận trọng, vì đánh giá độ nhạy và độ đặc hiệu trong nhiều nghiên cứu dựa trên các nhóm thuần tập quan sát nhỏ, với nguy cơ sai lệch đáng kể do lựa chọn tín hiệu. Hơn nữa, có một sự phát triển liên tục của các thuật toán và công nghệ có sẵn trong các thiết bị thương mại.
Hai báo cáo gần đây đã báo cáo tâm soát AF bằng cách sử dụng ECG sẽ không phát hiện nhiều trường hợp hơn so với sàng lọc bằng sờ mạch. [215]
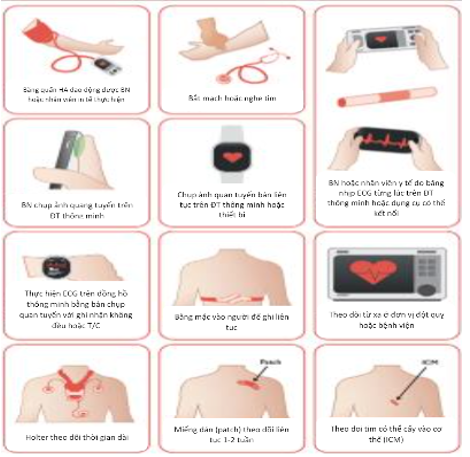
Hình 6. Hệ thống được sử dụng để sàng lọc AF.
Bắt mạch, máy theo dõi HA tự động, thiết bị ECG một đạo trình, thiết bị PPG, các cảm biến khác (sử dụng ghi rung động tim (seinsmocardiography), gia tốc kế và con quay hồi chuyển, v.v.) được sử dụng trong các ứng dụng cho điện thoại thông minh, dây đeo tay và đồng hồ. Có thể phát hiện AF không liên tục trên đồng hồ thông minh thông qua ghi PPG hoặc ECG. Đồng hồ thông minh và ‘thiết bị đeo được’ khác có thể đo tốc độ xung từ cổ tay một cách thụ động bằng cách sử dụng cảm biến quang học cho PPG và cảnh báo cho người tiêu dùng về sự bất thường của xung (dựa trên một thuật toán cụ thể để phát hiện AF phân tích sự bất thường và biến đổi của xung). [172,173,188-196] AF = rung nhĩ; BP = huyết áp; ECG = điện tâm đồ; PPG = photoplethysmography: chụp ảnh quang tuyến. BN: bệnh nhân. ĐT: điều trị. T/C: triệu chứng. ICM: theo dõi tim có thể cấy.
Bảng 5. Độ nhạy cảm và đặc hiệu của các dụng cụ tầm soát AF khác nhau so với ECG 12 chuyển đạo như là tiêu chuẩn vàng [173]
| Độ nhạy cảm | Độ đặc hiệu | |
| Bắt mạch [203] | 87 – 97% | 70 – 81% |
| Theo dõi huyết áp tự động [204, 207] | 93 – 100% | 86 – 92% |
| ECG một chuyển đạo
[208. 211] |
94 – 98% | 76 – 95% |
| Áp dụng smartphone [188,189,191,195,212,213] | 91.5 – 98.5% | 91.4 – 100% |
| Đồng hồ [196,198,213,214] | 97 – 99% | 83 – 94% |
| AF = rung nhĩ; BP = huyết áp; ECG = điện tâm đồ. | ||
 Hình 7. Các lợi ích tiềm tàng từ các nguy cơ tầm soát AF.
Hình 7. Các lợi ích tiềm tàng từ các nguy cơ tầm soát AF.
AF = rung nhĩ ; ECG = điện tâm đồ; OAC = chống đông đường uống; SE = thuyên tắc hệ thống. ĐT = điều trị. G/T= giải thích.
7.2 Các loại tầm soát và các chiến lược
Các loại và chiến lược sàng lọc AF thường được sử dụng [172,173,216] gồm sàng lọc cơ hội hoặc có hệ thống đối với những cá nhân trên một độ tuổi nhất định (thường ≥ 65 tuổi) hoặc với các đặc điểm khác gợi ý tăng nguy cơ đột quỵ, sử dụng ghi điện tâm đồ đơn điểm không liên tục hoặc lặp lại trong 30 giây qua 2 tuần. Tần suất giám sát thích hợp bằng điện thoại thông minh hoặc đồng hồ là không xác định. Dịch vụ chăm sóc ban đầu, nhà thuốc hoặc sàng lọc cộng đồng trong các biến cố đặc biệt là một cơ sở tốt để sàng lọc AF. [172,173] Nhìn chung, không có sự khác biệt đáng kể giữa sàng lọc hệ thống so với cơ hội hoặc thực hành chung so với sàng lọc cộng đồng trong một phân tích tổng hợp, nhưng tim được lặp lại liên quan đến hiệu quả tốt hơn đáng kể so với đánh giá đơn lẻ. [215] Quan trọng là, cần tổ chức giới thiệu có cấu trúc các trường hợp AF được phát hiện do tầm soat hoặc nghi ngờ để đánh giá lâm sàng thêm, để đưa ra cách xử trí thích hợp.
7.3 Lợi ích và nguy cơ tâm soát rung nhĩ
Ưu điểm và nhược điểm tiềm ẩn của việc phát hiện AF chưa được chẩn đoán trước đó thông qua sàng lọc được thể hiện trong Hình 7. [173]
Việc sàng lọc cũng có thể làm nổi bật các trường hợp AF đã biết được quản lý dưới mức tối ưu. [217] Ghi ECG từng lúc đã tăng khả năng phát hiện AF mới lên gấp bốn lần. [217] Trong nghiên cứu có kiểm soát REHEARSE-AF (REmote HEArt Rhythm Sampling using the AliveCor heart monitor to scrEen for Atrial Fibrillation: Lấy mẫu nhịp tim từ xa sử dụng theo dõi nhịp tim trực tiếp để tầm soát rung nhĩ) bằng cách sử dụng hệ thống điện tâm đồ một đạo trình dựa trên điện thoại thông minh / máy tính bảng hai lần mỗi tuần trong 12 tháng so với chăm sóc định kỳ dẫn đến kết quả tăng 3,9 lần phát hiện AF ở bệnh nhân ≥ 65 tuổi. [218] Tổ chức chương trình sàng lọc và thông tin bệnh nhân phù hợp với khả năng làm rõ ECG nhanh chóng có thể làm giảm lo lắng do nghi ngờ bất thường.
7.4 Hiệu quả và chi phí của tầm soát rung nhĩ
Chi phí y tế liên quan đến AF cao hơn biện minh cho các chiến lược xác định và điều trị AF không được chẩn đoán. [219] Tầm soát AF cơ hội có liên quan đến chi phí thấp hơn so với tầm soát hệ thống. [173] Lựa chọn công cụ và cài đặt sàng lọc phù hợp là rất quan trọng, [220] và hồ sơ hiệu quả chi phí thuận lợi đã được ước tính cho các chương trình sàng lọc dựa trên bắt mạch, thiết bị điện tâm đồ cầm tay và điện thoại thông minh có thuật toán chụp xung quang tuyến. [172] Cả sàng lọc cơ hội và hệ thống đều có hiệu quả chi phí cao hơn so với thực hành thông thường cho bệnh nhân trên 65 tuổi, với sàng lọc cơ hội có nhiều khả năng tiết kiệm chi phí hơn so với sàng lọc dân số có hệ thống. [1491]
7.5 Tầm soát ở các quẩn thể nguy cơ cao
7.5.1 Người lớn tuổi
Nguy cơ AF (thường không có triệu chứng) và đột quỵ tăng theo tuổi, [82,127,221] do đó biện minh cho việc sàng lọc AF ở người cao tuổi. Sàng lọc AF cơ hội có vẻ hiệu quả về chi phí ở những người cao tuổi (≥65 tuổi) [222] và trong số những người 75 – 76 tuổi trải qua tầm soát ECG từng lúc trong 2 tuần. [223]
Việc bắt mạch và / hoặc ECG ngắn hạn ở người cao tuổi (≥65 tuổi) mang lại tỷ lệ AF là 4,4%, với AF chưa được chẩn đoán trước đó là 1,4%, cho thấy con số cần thiết để sàng lọc là 70. [224] Ghi ECG cầm tay được lặp lại trong hơn 2 tuần ở một nhóm dân số 75 – 76 tuổi không được chọn lọc đã làm tăng khả năng phát hiện AF không triệu chứng lên đến 7,4% ở những đối tượng có ≥ 2 yếu tố nguy cơ đột quỵ. [225]
Khuyến cáo tầm soát để phát hiện AF
| Khuyến cáo | Classa | Levelb |
| Tầm soát cơ hội AF bằng cách bắt mạch hoặc băng nhịp ECG được khuyến cáo ở bệnh nhân ≥ 65 tuổi. [188,211,223,225] | I | B |
| Nên thường xuyên kiểm tra tư liệu lưu trữ máy tạo nhịp tim và máy khử rung tim được cấy để tìm AHRE.c [224,226] | I | B |
| Khi tầm soát AF, người ta khuyến cáo: [217,218]
• Các cá thể đang được tầm soát được thông báo về ý nghĩa và tầm quan trọng điều trị của việc phát hiện AF. • Một nền tảng chuyển tuyến có cấu trúc được tổ chức cho các trường hợp dương tính với tâm soát để đánh giá lâm sàng thêm do bác sĩ hướng dẫn để xác định chẩn đoán AF và cung cấp cách quản lý tối ưu cho những bệnh nhân có AF đã được xác nhận. • Chẩn đoán xác định AF trong các trường hợp dương tính khi tầm soát chỉ được thiết lập sau khi bác sĩ xem xét bản ghi ECG một đạo trình ≥ 30 s hoặc ECG 12 đạo trình và xác nhận cho thấy AF. |
I |
B |
| Tầm soát điện tâm đồ hệ thống nên được xem xét để phát hiện AF ở những người ≥ 75 tuổi, hoặc những người có nguy cơ đột quỵ cao. [212,224,227] | IIb | B |
AF = rung nhĩ; AHRE = cơn tần số nhĩ cao; ECG = điện tâm đồ.
a Class khuyến cáo. b Mức độ bằng chứng. c Xem phần 3.2 và 3.3 để biết các tiêu chí chẩn đoán AF và AHRE, và phần 16 về quản lý bệnh nhân AHRE.
- Đánh giá chẩn đoán rung nhĩ
Thường xảy ra ở những bệnh nhân có các yếu tố nguy cơ tim mạch / bệnh đi kèm, AF đôi khi có thể là dấu hiệu của các tình trạng chưa được chẩn đoán. Do đó, tất cả bệnh nhân AF sẽ được hưởng lợi từ đánh giá tim mạch toàn diện (Hình 8).
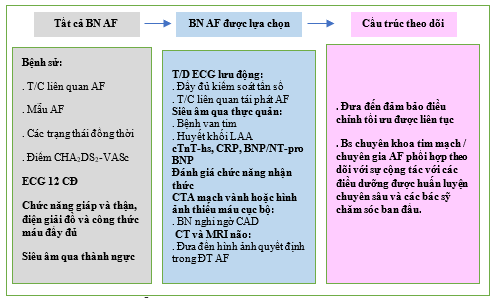
Hình 8. Công việc chẩn đoán và theo dõi ở bệnh nhân AF.
AF = rung nhĩ; BNP = B-type natriuretic peptide; CHA2DS2-VASc = Suy tim sung huyết, Tăng huyết áp, Tuổi ≥75, Đái tháo đường, Đột quỵ, Bệnh mạch máu, Từ 65 – 74 tuổi, Giới tính (nữ); CAD = bệnh động mạch vành; CRP = protein phản ứng C; CT = chụp cắt lớp vi tính; CTA = chụp mạch cắt lớp vi tính; cTnT-hs = troponin T của tim có độ nhạy cao; ECG = điện tâm đồ; LAA = tiểu nhĩ trái; LGE-CMR = cộng hưởng từ tim tăng cường tương phản gadolinium muộn; MRI = chụp cộng hưởng từ; NT-ProBNP = N-terminal (NT)-prohormone B-type natriuretic peptide.. T / D = theo dõi. T / C = triệu chứng. CĐ = chuyển đạo.
Gói tiêu chuẩn’ để đánh giá chẩn đoán bệnh nhân AF phải gồm bệnh sử đầy đủ và đánh giá các tình trạng đồng thời, kiểu AF, nguy cơ đột quỵ, các triệu chứng liên quan đến AF, thuyên tắc huyết khối và rối loạn chức năng LV. [143] ECG 12 chuyển đạo được khuyến cáo ở tất cả bệnh nhân AF, để thiết lập chẩn đoán AF, đánh giá nhịp thất trong thời gian AF, và kiểm tra sự hiện diện của các khiếm khuyết dẫn truyền, thiếu máu cục bộ, hoặc các dấu hiệu của bệnh tim cấu trúc. Các xét nghiệm cận lâm sàng (chức năng tuyến giáp và thận, điện giải huyết thanh, công thức máu đầy đủ) và siêu âm tim qua lồng ngực (kích thước và chức năng LV, kích thước LA, bệnh van tim, kích thước tim phải và chức năng tâm thu) để hướng dẫn điều trị. Dựa trên đặc điểm của bệnh nhân, thông tin bổ sung cụ thể có thể được thu thập. Hầu hết bệnh nhân AF cần được theo dõi thường xuyên (chăm sóc ban đầu) để đảm bảo tiếp tục quản lý tối ưu.
8.1 Triệu chứng và chất lượng cuộc sống
Vì các triệu chứng liên quan đến AF có thể phạm vi từ không đến mức độ tàn phế, và các quyết định điều trị kiểm soát nhịp (gồm triệt phá qua catheter) bị ảnh hưởng do mức độ nghiêm trọng của triệu chứng, tình trạng triệu chứng nên được đặc trưng bằng cách sử dụng thang điểm triệu chứng của Hiệp hội Nhịp tim Châu Âu (EHRA) [228] (Bảng 6), và mối liên hệ của các triệu chứng (đặc biệt nếu không đặc hiệu, chẳng hạn như khó thở, mệt mỏi, khó chịu ở ngực, v.v.) với AF cần được làm sáng tỏ vì các triệu chứng cũng có thể là kết quả của các yếu tố nguy cơ tim mạch đồng thời chưa được chẩn đoán hoặc quản lý chưa tối ưu hoặc các tình trạng bệnh lý. [229]
Ở một số bệnh nhân AF được chọn, nên theo dõi điện tâm đồ lâu dài để đánh giá mức độ thích hợp của việc kiểm soát tần số hoặc liên quan các triệu chứng với các đợt AF. Đôi khi mối liên hệ của các triệu chứng với AF chỉ có thể được thiết lập hồi cứu, sau khi can thiệp kiểm soát nhịp thành công. Ở một số bệnh nhân được chọn, một thử nghiệm nhịp xoang bằng cách sử dụng phương pháp chuyển nhịp và định lượng nhận thức của bệnh nhân về các triệu chứng bằng công cụ đánh giá đã được xác nhận (Bảng bổ sung 4) có thể thông báo quyết định về việc triệt phá AF qua catheter tiếp theo (phần 10.2).
Cải thiện triệu chứng và chức năng với các liệu pháp kiểm soát nhịp (chuyển nhịp tim, [232,234] thuốc chống loạn nhịp, và thủ thuật triệt phá AF qua catheter [235,242] phần lớn phụ thuộc vào duy trì nhịp xoang [243]; tuy nhiên, QoL có thể cải thiện bất chấp AF tái phát, trừ khi gánh nặng AF cao [244] (ví dụ > 2 giờ mỗi ngày [100] do quản lý tối ưu các yếu tố nguy cơ tim mạch hoặc bệnh đi kèm [245] hoặc hiệu quả điều trị. Hiệu quả của điều trị AF [246,247] được hỗ trợ bằng các báo cáo về QoL được cải thiện liên tục 10 năm sau khi triệt phát AF qua catheter kịch phát ở những bệnh nhân có tỷ lệ tiến triển AF thấp. [248]
(Vui lòng xem tiếp trong kỳ sau)







