BS. TRẦN DUY BÁCH*
BS. NGUYỄN THANH HIỀN
*Khoa TM tổng quát, BV Nhân dân 115
- MỞ ĐẦU.
Bệnh tim mạch là nguyên nhân hàng đầu gây tàn phế và tử vong ở những người mắc đái tháo đường và đái tháo đường là một trong những nguyên nhân hàng đầu gây xơ vữa sớm cả 2 giới.Đái tháo đường là một yếu tố nguy cơ độc lập của bệnh tim mạch và làm tăng nguy cơ mắc bệnh tim mạch ở cả giới nữ.
Rối loạn lipid máu thường gặp ở bệnh nhânđái tháo đường type 2, tỉ lệ 72%-85%, với kiểu hình lipid gây xơ vữa bao gồm tăng triglyceride, tăng ApoB, tăng non-HDL, LDL và giảm HDL. Hiểu được rối loạn lipid do đái tháo đường rất quan trọng bởi nó có thể xảy ra và gây biến cố tim mạch trước khi đái tháo đường được chẩn đoán.Những bằng chứng gần đây khuyến cáo nên bắt đầu thường quy liệu pháp hạ lipid máu cho các bệnh nhântrẻ mắc đái tháo đường ở cả 2 type. Bởi lẽ đái tháo đường làm giảm tuổi thọ ở nhóm bệnh nhân này, nên việc phòng ngừa rối loạn lipid máu càng sớm càng tốt.
Ở những bệnh nhân đề kháng insulin lúc trẻ và phát triển thành đái tháo đường type 2 do béo phì quá mức hoặc do kiểu gen thì nguy cơ tim mạch lại vô cùng cao.Ở bệnh nhânđái tháo đường nguy cơ tim mạch thường do kết hợp đồng thời nhiều yếu tố như béo phì, tăng huyết áp, rối loạn lipid máu. Các nghiên cứu hiện tại chỉ ra rằng tỉ lệ mới mắc bệnh tim mạch gia tăng là do điều trị chưa kiểm soát tốt huyết áp và lipid máu.Qua đó nhắc nhở chúng ta lợi ích của liệu pháp hạ lipid máu là vô cùng lớn.
Statins được xem như là thuốc đầu tay ở bệnh nhân đái tháo đường type 2, thậm chí khi vừa chẩn đoán, mà không cần quan tâm các yếu tố nguy cơ khác. Chỉ khác ở chỗ nếu bệnh nhân có nhiều yếu tố nguy co tim mạch thì khuyến cáo dùng statins liều cao. Gần đây đã có nhiều thuốc mới đã và đang được đưa vào sử dụng và nghiên cứu, các khuyến cáo mới về điều trị rối loạn mỡ máu cũng không ngừng được cập nhật. Bài viết này cập nhật các thuốc mới và các hướng dẫn điều trị rối loạn mỡ máu mới ở bệnh nhân đái tháo đường hiện nay.
- SINH LÝ BỆNH CỦA RỐI LOẠN LIPID MÁU DO ĐÁI THÁO ĐƯỜNG.
Dạng rối loạn lipid máu thường gặp nhất là tăng triglyceride có liên quan với tăng độ tập trung triglyceride giàu lipoproteins, mà thành phần chính của chất này là các phân tử lớn lipoproteins trọng lượng phân tử rất thấp ( VLDL1) và các phần nhỏ của VLDL1. Nồng độ HDL giảm (chủ yếu do giảm số lượng phân tử HDL2 thứ phát do tăng dị hóa HDL), và LDL bình thường hoặc tăng nhẹ với LDL dạng phân tử nhỏ đậm đặc (sdLDL) chiếm ưu thế là những nhân tố mạnh gây xơ vữa. Còn nhiều phân tử chưa thể đo được trong xét nghiệm LDL thường quy. Khi quá trình glycat hóa và oxi hóa của các phân tử tăng lên dẫn đến tăng nguy cơ tim mạch và mục tiêu chính của điều trị ở bệnh nhân đái tháo đường là kiểm soát các quá trình đó.
Insulin có vai trò quan trọng trong điều hòa chuyển hóa lipid. Nó hoạt động tại gan bằng cách ức chế sản xuất VLDL, tăng số lượng thụ thể LDL, giảm acid báo tự do và giảm sản xuất ApoB. Thêm vào đó, insulin ức chế hormon nhạy lipase trong tế bào mỡ, qua đó kích hoạt phân giải lipoprotein trong hệ tuần hoàn và làm tăng dị hóa chilomycron. Lipids có thể bất thường cả về số lượng, chất lượng và dược động học ( hình 1, Bảng 1)
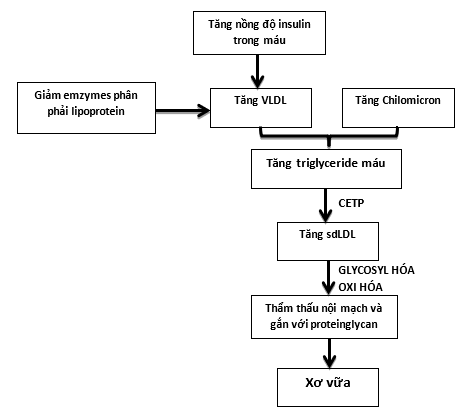 Hình 1. Sinh lý bệnh của rối loạn lipid do đái tháo đường (5)
Hình 1. Sinh lý bệnh của rối loạn lipid do đái tháo đường (5)
Bảng 1. Các thay đổi chính trong chuyển hóa của lipoproteins ở bệnh nhân đái tháo đường 2 (1)
| Lipoproteins | Thay đổi về số lượng | Thay đổi về chất lượng | Thay đổi về dược động học/ chuyển hóa |
| LDL | Không đổi hoặc tăng nhẹ | Tăng tỉ lệ phân tử nhỏ đậm đặc
Tăng oxi hóa Glycat hóa |
Giảm dị hóa |
| HDL | Giảm độ tập trung trong máu | Glycat hóa | Tăng dị hóa |
| VLDL | Tăng độ tập trung trong máu | Tăng tỉ lệ phân tử lớn (VLDL1)
Glycat hóa |
Tăng sản xuất
Giảm đi hóa |
Đôi khi nồng độ LDL trong giới hạn bình thường và các xét nghiệm lipid thường dùng trên lâm sàng không phải bao giờ cũng thấy được xu hướng xấu đi của rối loạn lipid do đái tháo đường, nên tốt hơn chúng ta nên nhìn ở khía cạnh non-HDL.Non-HDL-C hay Apo-B là những chất chỉ điểm tốt hơn triglycerides hay LDL-c, thêm vào đó chúng cũng là mục tiêu điều trị hàng thứ hai. Ở các bệnh nhân nguy cơ cao, mục tiêu Non-HDL-C < 2.6 mmol/L (<100 mg/dL) và ApoB <80 mg/dL, còn các bệnh nhân nguy cơ rất cao thì mục tiêu này là non-HDL-C <2.2 mmol/L (<85 mg/dL) và ApoB <65 mg/dL. Đối với các bệnh nhân nguy cơ rất cao với biến cố bệnh mạch máu do xơ vữa tái phát thì mục tiêu nên xem xét là non-HDL-C <1.8 mmol/L (<70 mg/dL) và ApoB <55 mg/dL.
- MỤC TIÊU ĐIỀU TRỊ
Cơ bản trong điều trị hạ lipid tập trung vào thuốc. Khuyến cáo và các chỉ dấu sinh học được thay đổi trong các guidelines nhưng điều quan trọng là phân tầng nguy cơ và xác định mục tiêu điều trị: LDL đích. Hiện tại mục tiêu trong hạ lipid máu ở bệnh nhânđái tháo đường chưa đạt được đồng thuận giữa các hiệp hội y học. Gần đây đái tháo đường được xem như là một tình trạng nguy cơ cao mà các yếu tố làm tăng thêm nguy cơ bao gồm: thời gian >10 năm đối với đái tháo đường 2, >20 năm với đái tháo đường 1, albumin niệu > 30mg/G creatinine, eGRF< 60ml/phút/1.73m2, bệnh lý võng mạc, bệnh lý thần kinh và chỉ số ABI <0.9. Tăng huyết áp, rối loạn lipid máu, béo bụng và gan nhiễm mỡ không do rượu (NAFLD) thường là những bệnh đồng mắc với đái tháo đường 2 và làm tăng nguy cơ tim mạch. Những trường hợp trên cần được chỉ định statin để điều trị rối loạn lipid máu do đái tháo đường.
Điều trị rối loạn lipid máu do đái tháo đường có thể chia làm 2 giai đoạn: không dùng thuốc và dùng thuốc.Điều trị không dùng thuốc bao gồm liệu pháp dinh dưỡng tập trung vào giảm mỡ bão hòa và mỡ đồng phân trans ăn vào, thay vào đó là tăng thêm chất xơ, giảm cân bao gồm phẫu thuật giảm béo (nếu cần) và hoạt động thể chất.
- CÁC NGHIÊN CỨU
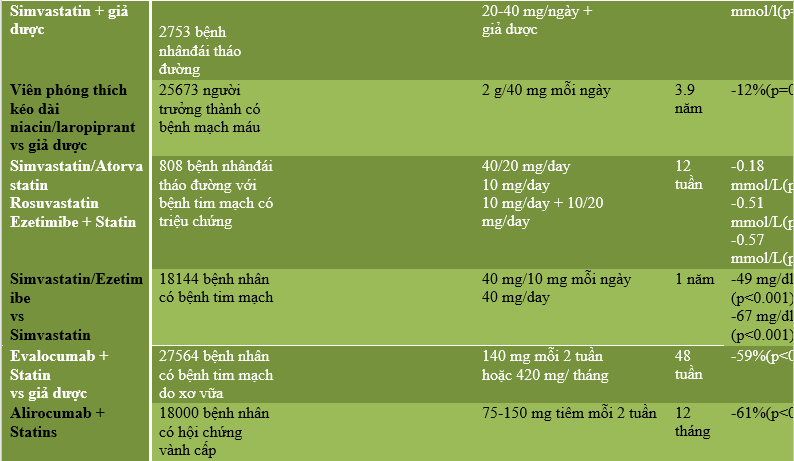
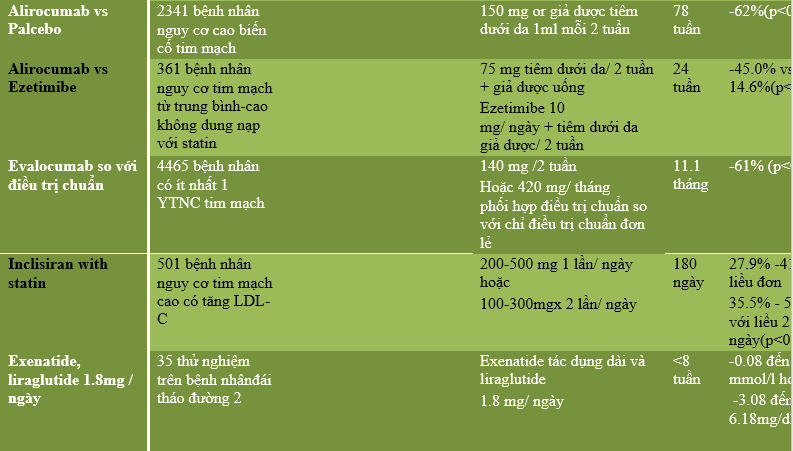
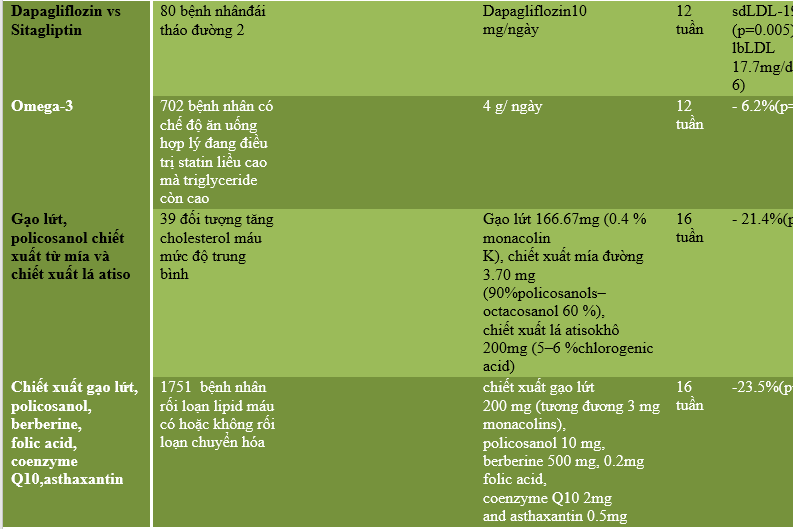
Tóm tắt các nghiên cứu chính về điều trị rối loạn lipid máu ở bệnh nhân đái tháo đường nêu ở bảng 2.
Bảng 2. Tóm tắt các nghiên cứu (2)

- ĐIỀU TRỊ
Điều trị bao gồm không dùng thuốc và thuốc.
Giảm cân được cho thấy cải thiện nhiều yếu tố nguy cơ, như HbA1c và huyết áp; tuy vậy nghiên cứu “Look AHEAD” lại không cho thấy sử cải thiện biến cố tim mạch sau 1 thời gian giảm cân và thay đổi lối sống tích cực, qua đó cho thấy sự cần thiết của liệu pháp dùng thuốc để làm giảm bệnh lý tim mạch do xơ vữa (ASCVD).
Các thuốc cổ điển dùng để điều trị rối loạn lipid máu do đái tháo đường bao gồm statins, ức chế hấp thu cholesterol, niacin, fibrates, chất bất hoạt acid mật (BAS) và omega-3 không acid béo. Một thuốc tương đối mới là chất ức chế PCSK9 (proprotein convertase subtilisin/kexin type 9) và các thuốc khác vẫn đang được nghiên cứu(như icosapen thyl (IPE), bempedoic acid (BA) và inclisiran) là những lựa chọn để kiểm soát yếu tố nguy cơ quan trọng này.
Rối loạn lipid do đái tháo đường nên được điều trị với statins. Tuy nhiên, đối với bệnh nhân không đạt được mục tiêu LDL-C đưa ra thì cần phối hợp thuốc.
- THUỐC
Hình 2.Các thuốc hạ lipid máu và cơ chế tác động của chúng (3).
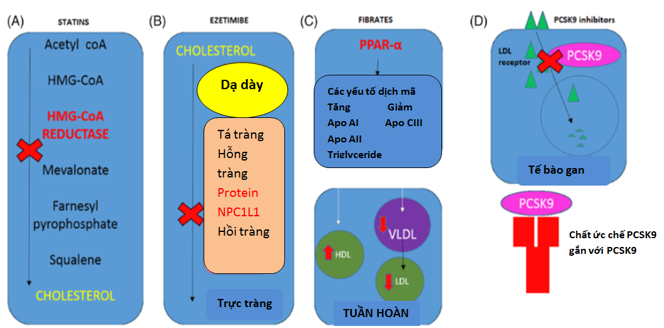
(A) statins ức chế tổng hợp cholesterol bằng cách ức chế hydroxymethylglutaryl CoA reduc-tase (HMG CoA reductase); (B) Ezetimibe ức chế hấp thu cholesterol trong hồi tràng thông qua protein Niemann–pick C1–like 1 (NPC1L1); (C) fibrates hoạt hóa thụ thể peroxisome proliferator-activated (PPAR-α) làm tăng HDL và giảm triglycerides (TG), VLDL và LDL; (D) chất ức chế proprotein convertase subtilisin-kexin type 9 (PCSK9) chống thoái giáng thụ thể LDL qua đó làm tăng độ thanh thải LDL.
- Statins
Statins ức chế cạnh tranh với 3-hydroxymethylglutaryl coenzyme A, làm giảm tín hiệu tổng hợp cholesterol ở gan. Statin được xem là thuốc đầu tay điều trị rối loạn lipid ở bệnh nhânđái tháo đường 2, ngay cả khi mới chẩn đoán. Bởi vậy, statins có liên quan tới giảm độ tập trung LDL cũng như giảm nguy cơ tim mạch ở cả dự phòng tiên phát và thứ phát cho bệnh nhân mắc đái tháo đường. Quan điểm này được ủng hộ bởi nhiều thử nghiệm ngẫu nhiên có đối chứng (RCT) và nên xem xét việc cho statin ở các cá thể mắc đái tháo đường 2 có nguy cơ tim mạch cao bất kể nồng độ LDL nền.Theo Guidelines, tất cả bệnh nhân đái tháo đường nên được điều trị với statin nếu có thể dung nạp được, với mục tiêu LDL dựa trên type đái tháo đường, nguy cơ tim mạch và biến chứng.
Statins làm giảm lắng đọng cholesterol, tăng biểu lộ thụ thể LDL tại gan và gia tăng nhập bào LDL trong hệ tuần hoàn.Statins cũng có tác động đa hướng, làm giảm hsCRP và các marker viêm khác giúp làm ổn định mảng xơ vữa, cải thiện chức năng nội mạc, giảm viêm mạch và mất cân bằng oxi hóa.
Statins được chia thành:
Liều cao: làm giảm ≥ 50% LDL ( atorvastatin 40-80mg, rosuvastatin 20-40mg)
Liều trung bình: giảm 30-50% LDL ( atorvastatin 10-20mg, rosuvastatin 5-10mg, simvastatin 20-40mg, pravastatin 40mg, lovastatin 40mg, fluvastatin 80mg, pitavastatin 2-4mg)
Liều thấp: giảm <30% LDL (simvastatin 10mg, pravastatin 10-20mg, lovastatin 20mg, fluvastatin 20-40mg, pitavastatin 1mg).
Nhiều thử nghiệm đã cho thấy giảm biến cố tim mạch khi sử dụng statin. Theo báo cáo của nghiên cứu Heart Protection tỉ lệ biến cố giảm 22% bao gồm cả đột quỵ. Một phân tích tổng hợp 14 thử nghiệm lâm sàng với hơn 18,000 bệnh nhân đái tháo đường 2, thời gian theo dõi trung bình là 4.3 năm, liệu pháp statins giúp giảm biến cố tim mạch đến 21% và với mỗi 39 mg/dL LDL giảm được thì tử vong do mạch máu giảm 13%. Điều này cho thấy lợi ích rõ rệt của việc sử dụng statins ở bệnh nhânđái tháo đường, độc lập với chỉ số LDL hay lipid.
Statins thường dễ dung nạp, tác dụng phụ thường gặp là đau cơ. Hoại tử cơ tự miễn và tiêu cơ vân rất hiếm gặp. Tuy nhiên, vẫn phải lưu ý ở bệnh nhân lớn tuổi, đặc biệt ở những người có bệnh thận mạn, cường giáp dưới lâm sàng hoặc cường giáp lâm sàng chưa được điều trị và những thuốc tương tác với statins. Statins cũng có thể gây đái tháo đường mới, nhưng tỷ lệ rất thấp, không là gì với lợi ích giảm biến cố tim mạch mà statins mang lại. Cần xác định rõ việc không dung nạp được statins để tránh việc dừng hoặc không dùng statin mà làm giảm lợi ích cho bệnh nhân.
- Ezetimibe-chất ức chế hấp thu cholesterol
Ezetimibe tác động lên ruột làm ức chế hấp thu bằng cách gắn với các chất vận chuyển sterol là Niemann-Pick C1-Like 1 (NPC1L1), làm giảm đáng kể nồng độ LDL. Ezetimibe làm tăng nhạy cảm insulin ở các bệnh nhân đề kháng insulin, đặc biệt hiệu quả trên bệnh nhânđái tháo đường, làm giảm LDL đến 24%. Ezetimibe có tác động hiệp đồng với statins giúp giảm LDL hiệu quả. Trong thử nghiệm IMPROVE-IT, ezetimibe phối hợp với simvastatin đặc biệt hiệu quả trên bệnh nhânđái tháo đường, làm giảm nguy cơ tương đối biến cố tim mạch đến 15% và giảm nguy cơ tuyệt đối đến 5.5%. Một phân tích tổng hợp (cỡ mẫu 109.244 bệnh nhân) cho thấy sự kết hợp ezetimibe và statin làm giảm đáng kể biến cố tim mạch ở bệnh nhân có nguy cơ cao.
Ezetimibe có chỉ định phối hợp với statins ở bệnh nhânđái tháo đường chưa đạt mục tiêu lipid mặc dù đã tối ưu liều statins hoặc ở những bệnh nhân không dung nạp được với liều cao của statin, đôi khi có thể đơn trị liệu ezetimibe ở bệnh nhân không dung nạp statin.
- Niacin
Niacin là thuốc có hiệu lực trung bình trong việc làm tăng HDL và giảm LDL và TRG, thuốc còn giúp hạ nồng độ lipoprotein(a) khoảng 25%. Tuy nhiên, chưa có nghiên cứu chứng minh lợi ích trong việc làm giảm biến cố tim mạch. Trong lâm sàng, việc sử dụng niacin còn hạn chế do tác dụng phụ của thuốc này: ở liều tiêu chuẩn khoảng 80% bệnh nhân có cảm giác đỏ bừng mặt, 20% còn lại thì than ngứa, dị cảm và buồn nôn.
Nghiên cứu AIM-HIGH cho thấy không có lợi ích trên lâm sàng của việc cải thiện rõ rệt nồng độ HDL và triglyceride. Do đó, phối hợp thuốc giữa statins và niacin ở bệnh nhânđái tháo đường nên tránh vì không có lợi ích trên lâm sàng.
- Fibrates
Fibrates làm giảm nồng độ triglyceride và tăng nồng độ HDL bằng cách hoạt hóa peroxisome proliferator-activated receptor α (PPAR-α) thông qua đó làm giảm LDL. Fenofibrates giúp giảm triglyceride từ 30-50% và tác dụng rõ ở bệnh nhânđái tháo đường nguy cơ tim mạch cao có nồng độ triglyceride trong máu cao. Trong một phân tích tổng hợp gồm 45,058 bệnh nhân, kết quả cho thấy fibrates giúp làm giảm nguy cơ tương đối các biến cố chính khoảng 10% và giảm nguy cơ biến cố mạch vành đến 13%.Fibrates được chuyển hóa tại thận, vì vậy nên tránh hoặc thận trọng khi sử dụng ở bệnh nhân bệnh thận mạn.
Pemafibrates là thuốc điều chỉnh PPAR-α có chọn lọc thế hệ mới và tác động mạnh hơn fibrates.Khác với fibrates, Pemafibrates được chuyển hóa tại gan và bài tiết qua mật nên có thể sử dụng ở bệnh nhân rối loạn chức năng thận.Các nhà nghiên cứu đang tiến hành thử nghiệm PROMINENT để đánh giá hiệu quả giảm biến cố tim mạch của pemafibrates.
- Chất cô lập acid mật (BAS)
BAS gắn với acid mật trong lòng ruột non, tác dụng làm bẻ gãy chu trình gan- ruột của acid mật, làm giảm nồng độ LDL lên đến 30%. Cholestyramine, colestpol và colesevelam là những chất cô lập acid mật thường dùng. Trong quá khứ, những chất này dùng để thay thế statins khi bệnh nhân khộng dung nạp được hoặc dùng cho phụ nữ trong độ tuổi sinh đẻ và trẻ em. Một số tác dụng phụ thường gặp của chất này là táo bón, tăng sỏi mật và hạn chế sử dụng ở bệnh nhân có tiền căn tăng triglyceride máu.Colesevelam có tỉ lệ tác dụng phụ thấp và được chứng minh lợi ích trong cải thiện HbA1c ở bệnh nhânđái tháo đường khó kiểm soát.BAS được khuyến cáo hàng thứ 2 trong điều trị giảm LDL và nên dùng phối hợp với thuốc khác.
- Icosapent ethyl (IPE)
Omega-3 không acid béo là thuốc bổ sung vào liệu pháp điều trị giảm triglycerides, nhưng thuốc gần như không tác động lên các lipoproteins khác. Để có lợi ích về tim mạch thì cần dùng liều cao eicosapentaenoic acid (EPA) và docosahexaenoic acid. Icosapent ethyl là một EPA ethyl ester thuần, tác động lên tế bào mỡ và tế bào viêm thông qua peroxisome proliferator-activated receptor (PPAR), kết quả là làm giảm nồng độ triglyceride, tăng nhạy cảm insulin và điều hòa dòng thác viêm.
Gần đây, thử nghiệm REDUCE IT cho kết quả tích cực khi so sánh giữa IPE và giả dược với p<0.001, nhưng người ta cũng quan sát thấy thuốc này làm tăng tỉ lệ nhập viện ở bệnh nhân có rung nhĩ hoặc cuồng nhĩ. IPE là một lựa chọn phối hợp với statins ở bệnh nhân có bệnh lý tim mạch do xơ vữa có tăng triglyceride.
- Bempedoic acid (BA)
Bempedoic acid làm giảm LDL thông qua ức chế cạnh tranh adenosine triphosphate citrate lyase (ACL), một enzyme xúc tác tổng hợp acetyl coenzyme A, mà acetyl coenzyme A lại là chất nên toàn phần trong quá trình tổng hợp cholesterol tại gan. Bempedoic acid (BA) tác động tương tự statins, điều tiết biểu lộ thụ thể LDL tại gan, tăng thanh thải LDL trong máu. Nhiều nghiên cứu ngẫu nhiên cho thấy nồng độ LDL trong máu giảm từ 18-28% khi sử dụng BA đơn trị hoặc phối hợp với statins. Mặc khác, thuốc này được kích hoạt bởi các enzyme tại gan chứ không bởi các enzyme tại cơ nên giảm được các tác dụng phụ liên quan tới cơ vân. Tuy nhiên chất này lại làm tăng nồng độ acid uric và có thể dẫn đến gout.
Một phân tích tổng hợp của 7 nghiên cứu ngẫu nhiên kết luận rằng BA có giá trị trong điều trị bệnh nhân có nguy cơ tim mạch cao không dung nạp với statin hoặc chưa đạt mục tiêu LDL với liều statin và ezetimibe tối ưu.
Một phân tích khác dựa trên 4 RCT với 3623 bệnh nhân ở Bắc Mỹ và Châu Âu cũng cho kết quả tương tự, BA làm giảm thêm từ 12.7%- 24.5% so với giả dược ở nhóm bệnh nhân có nguy cơ tim mạch cao và nhóm tăng cholesterol máu di truyền dị hợp tử. Ngoài ra cũng đưa ra lưu ý tác dụng phụ làm tăng acid uric của thuốc này.
- Inclisiran
Inclisiran là một RNA tổng hợp nhỏ có chức năng can thiệp vào quá trình thoái giáng của mRNA đặc hiệu cho PCSK-9 tại gan, mRNA này làm giảm tổng hợp PCSK-9 tại gan với thời gian tác động kéo dài ( từ nửa đến 1 năm). Điều này giúp làm giảm nồng độ LDL >50%.
Inclisiran khác với các chất ức chế PCSK9 bởi thời gian tác động kéo dài và tác động ở cấp độ nội bào của tế bào gan, còn các chất ức chế PCSK9 tác động ở cấp độ tuần hoàn. Inclisiran làm giảm LDL một cách nhanh chóng, hiệu quả và kéo dài, giúp cải thiện tình trạng xơ vữa và bilan lipid, thêm vào đó đây là một thuốc khá an toàn và dung nạp tốt. Cũng giống các chất ức chế PCSK9 khác, giá thành còn cao nên chưa sử dụng đại trà.Với cách sử dụng 2 lần mỗi năm, thuốc này hứa hẹn nâng cao sự tuân thủ điều trị và đạt mục tiêu LDL gần như tuyệt đối.
- Chất ức chế PCSK9
Chất ức chế PCSK9 hiện tại là 1 bước tiến trong điều trị hạ lipid, bao gồm 2 thuốc nổi bật là evolocumab và alirocumab; cả 2 thuốc đều là kháng thể đơn dòng từ người có thể gắn với enzyme tự do PCSK9. Enzyme này chịu trách nhiệm xúc tiến cho quá trình hủy thụ thể LDL tại gan, do đó việc ức chế quá trình này dẫn đến tăng thanh thải LDL-C tại gan và làm giảm LDL huyết thanh. Thuốc ức chế PCSK9 có đủ dữ liệu an toàn trên bệnh nhânđái tháo đường. Trong khuyến cáo ACC 2018, thuốc này có chỉ định dự phòng thứ phát trên những bệnh nhân nguy cơ tim mạch rất cao và LDL-C ≥70mg/dL (mặc dù đã tối ưu liều statin và ezetimibe), các bệnh nhân có LDL-C ban đầu trên 190 mg/dL hoặc ≥100mg/dL mặc dù đã dùng statin. Trong khuyến cáo này cho thấy lợi ích giảm biến cố tim mạch chính của PCSK9i nhưng không chỉ rõ vai trò của thuốc trong rối loạn lipid máu do đái tháo đường.
Trong RCT FOURIER, các bệnh nhân có bệnh lý tim mạch đang dùng statin, khi thêm evolorumab người ta nhận thấy LDL-C giảm 60% so với ban đầu về mức trung bình là 30mg/dL, qua đó giảm tương đối 15% kết cục chính ( kết hợp của nhồi máu cơ tim, chết do nguyên nhân tim mạch, đột quỵ, tái thông mạch vành hoặc nhập viên do cơn đau thắt ngực không ổn định). Tương tự trong nghiên cứu ODYSSEY, cùng kết cục chính như trên, alirocumab cũng làm giảm đến 15% biến cố tim mạch. Tuy nhiên, evolocumab và alirocumab đều làm trầm trọng đái tháo đường và biến chứng đái tháo đường hơn, nhưng ở mức thấp, khi so sánh với giả dược. Monami và cộng sự tại Ý đã phân tích kết cục tim mạch của thuốc ức chế PCSK9 trong dân số đái tháo đường và đưa ra kết luận rằng: khác với statins có liên quan đến khả năng tăng nguy cơ mắc đái tháo đường, PCSK9i không có tác dụng phụ có hại nào trên chuyển hóa đường, mở ra hướng nghiên cứu trong dân số đái tháo đường. Và mặc dù chưa biết kết quả nghiên cứu tiếp theo ra sao nhưng việc giảm giá thành của evolocumab và alirocumab sẽ mang đến hy vọng mở rộng thị trường của nhóm thuốc này
- Bromodomain extra-terminal protein inhibitors
Một cơ chế mới là ức chế bromodomain và protein cuối của nó ( BET). Apabetalonetác động lên quá trình sinh lý của tiến trình xơ vữa và biến cố tim mạch thông qua ức chế các protein của BET. Apabetalone điều hòa sao chép gen qua đó điều chỉnh các quá trình vận chuyển ngược cholesterol, phản ứng viêm mạch, đông máu và bổ thể ( hình 3). Apabetalone đã được chứng minh có tác dụng điều tiết giảm dòng thác bổ thể, quá trình xơ vữa và nồng độ ApoE trên các loài gặm nhấm. Nghiên cứu BETonMACE tập trung vào tác dụng của apabetalone trong phòng ngừa các biến cố tim mạch chính trên hơn 2400 cá thể có bệnh mạch vành, đái tháo đường type 2 và HDL-C thấp đang dùng sử dụng statins. Đây là nghiên cứu pha 3 đang được tiến hành và sẽ công bố trong thời gian tới.
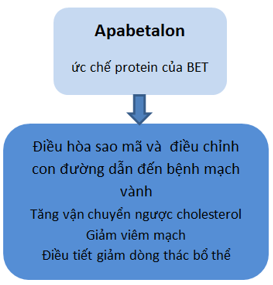
Hình 3.Cơ chế tác động của Apabetalo (3)
- Các thuốc điều trị đái tháo đường
Các nghiên cứu lâm sàng chỉ ra hiệu quả của các thuốc mới điều trị đái tháo đường không chỉ tác động lên glucose máu mà còn giúp giảm cân, hạ huyết áp, hạ lipid máu, giảm viêm, giảm oxi hóa do stress, cải thiện chức năng nội bào và giảm tình trạng xơ vữa. Các thuốc thuộc liệu pháp nội sinh bao gồm: kháng thụ thể glucagon-like peptide-1 (GLP-1RA), ức chế dipeptidyl peptidase-4 (DPP-4is), ức chế đồng vận chuyển natri/ glucose (SGLT2is) đã cho thấy lợi ích, giúp giảm biến cố tim mạch (bảng 3).
BẢNG 3. Tác động của thuốc điều trị đái tháo đường lên bilan lipid (1).
| THUỐC | CHOLESTEROL TOÀN PHẦN | LDL | HDL | TRG |
| Metformin | – /0 | – | 0/+ | – /0 |
| DPP-4 inhibitors | ||||
| Sitagliptin | 0 | 0 | 0/+ | 0 |
| Vildagliptin | 0 | 0 | 0/+ | 0 |
| Saxagliptin | 0 | 0 | 0 | 0 |
| Linagliptin | 0 | 0 | 0 | 0 |
| GLP1 analogues | ||||
| Liraglutide | 0 | 0 | 0 | – |
| Exenatide | -/0 | 0/+ | 0/+ | – |
| SGLT2 inhibitors | ||||
| Empaglifozin | 0/+ | 0/+ | 0/+ | – |
| Dapaglifozin | 0/+ | 0/+ | 0/+ | -/0 |
| Canaglifozin | + | + | + | + |
| Insulin | -/0 | – | 0/+ | – |
DPP-4: dipeptidyl peptidase-4; GLP1: glucagon-like peptide-1; SGLT2: sodium/glucose cotransporter 2; LDL: low-density lipoprotein; HDL: high-density lipoprotein; TRG: triglyceride
0: không có tác động +: tăng –: giảm
0/+: không có tác độnghoặc tăng -/0: không có tác độnghoặc giảm
- Berberine
Berberine cải thiện kiểm soát đường huyết ở các bệnh nhânđái tháo đường bằng cách hoạt hóa activating adenosinemonophosphate-activated kinase. Người ta dùng men gạo lứt kết hợp với sterol thực vật có tác dụng tương tự như nhóm statins và ezetimibe, lảm giảm LDL đến 33% và cholesterol toàn phần đến 19% chỉ trong sáu tuần. Men gạo lứt chứa 9 thành phần hoạt hóa sinh học (monacolins), có công thức giống như lovastatin. Thêm vào đó, việc sử dụng đồng thời các chất chiết xuất từ lá cây và men gạo lứt làm giảm đáng kể LDL-C (21.4 %, p<0.001) và cholesterol toàn phần (14.1 %, p<0.001) sau 16 tuần. Sự kết hợp giữa berberine và men gạo lứt cải thiện rõ các biến số các loại lipid: giảm cholesterol toàn phần, LDL-C và triglyceride (với p< 0.001) và tăng HDL-C ( p<0.001) sau 16 tuần điều trị.
Armolipid Plus® (Rottapharm/Madaus) là một công thức chứa các hợp chất nguồn gốc tự nhiên ( men gạo lứt, policosanol và berberine kết hợp với acid folic, astaxanthin và coenzyme Q10) có đặc tính hỗ trợ giảm lipid máu, hứa hẹn là một giải pháp thay thế hiệu quả và an toàn cho các thuốc tổng hợp. Thuốc này chứa liều thấp các nguyên liệu kể trên, vừa đủ để không gây ra các tác dụng không mong muốn mà vẫn có tác dụng điều trị khi dùng chung với các chất khác.Armolipid Plus® có thể làm giảm 11%-21% cholesterol toàn phần và 15-31% LDL-C, tương đương với liều thấp của statin. Ở các bệnh nhân tăng lipid máu mức độ từ nhẹ tới vừa không dung nạp với statins và không đạt mục tiêu LDL-C với ezetimibe, Armolipid Plus® giúp làm giảm thêm 10% TC và LDL-C. Hơn nữa, Armolipid Plus® cũng giúp cải thiện độ cứng của mạch máu, đây là một biến số độc lập của biến cố tim mạch.
- Chiến lược điều trị
Theo khuyến cáo hiện tại chúng ta nên phối hợp cả phân tầng nguy cơ và mức giảm LDL-C ở bệnh nhânrối loạn lipid do đái tháo đường để lựa chọn phương pháp điều trị tốt nhất cho từng cá thể. Statins là lựa chọn đầu tay và ezetimibe nên được phối hợp khi chưa đạt mục tiêu LDL-C với statin hoăc không dung nạp với statin. Ở bệnh nhân có bệnh lý tim mạch, nguy cơ tim mạch tồn lưu vẫn còn trừ khi đạt được mục tiêu LDL-C và cholesterol với statin. Ở bệnh nhân có bệnh tim mạch do xơ vữa và có LDL <70 mg/dL (1.81 mmol/L), việc thêm Niacin vào không mang lại hiệu quả bổ sung nào mặc dù cải thiện được HDL và TG. PCSK9 đơn trị hoặc phối hợp với statin và ezetimibe nên dành cho bệnh nhân có nguy cơ tim mạch cao và LDL-C trên mục tiêu. Fibrate có thể xem xét ở bệnh nhân nguy cơ timm mạch cao có mức TG cao và HDL-C thấp.
Hiện nay các thuốc đái tháo đường mới ngày càng cho thấy đa tác động trên các yếu tố nguy cơ tim mạch, cùng với hiệu lực lên lipid, các thuốc này hứa hẹn mang đến lợi ích phòng ngừa biến chứng tim mạch ở bệnh nhânđái tháo đường 2. Cuối cùng, thực dưỡng cũng góp phần đạt mục tiêu lipid và giảm nguy cơ tim mạch tồn lưu. Ví dụ như trong nghiên cứu sử dụng gạo lứt, berberine, policosanol, astaxanthin, người ta nhận thấy các thực phẩm này giúp làm giảm lipid và đường huyết, với cholesterol toàn phần giảm 26.15mg/dL (p<0.001), LDL-C(-23.85mg/dL, p<0.001), HDL-C (2.53mg/dL, p<0.001), triglycerides (-13.83mg/dL, p<0.001) và glucose giảm 2.59mg/dL ( p=0.010). Thêm vào đó các loại thực phẩm này còn giúp giảm đáp ứng viêm và tổn thương nội mạch, ảnh hưởng gián tiếp đến quá trình xơ vữa và nguy cơ tim mạch.
Tóm tắt chiến lược và khuyến cáo điều trị hiện nay nêu ở hình 4 và bảng 4. Trong tương lai, có thêm các thuốc mới hơn, có thể chiến lược điều trị sẽ là hình 5 (1,6-8).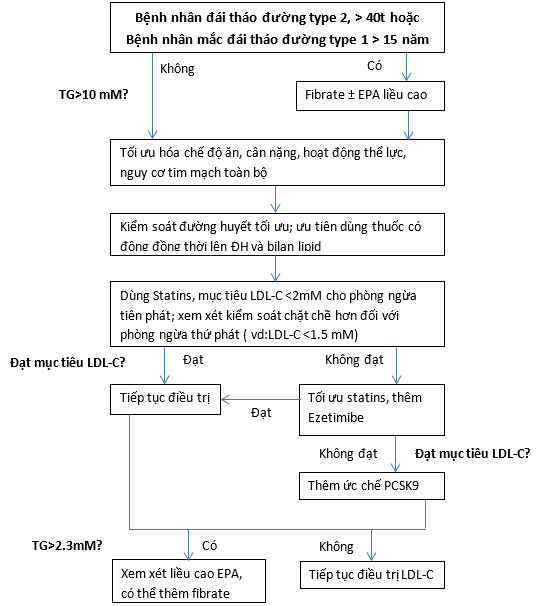
Hình 4. Sơ đồ kiểm soát lipid máu ở BN đái tháo đường hiện nay (6).
EPA, eicosapentanoic acid (omega-3 fatty acids); LDL-C, low-density lipoprotein cholesterol; mM, millimoles per litre; PCSK9, proprotein convertase subtilisin kexin type 9; TG, triglyceride
Bảng 4. Khuyến cáo điều trị rối loạn lipid máu ở bệnh nhân đái tháo đường–ESC 2019 (7)

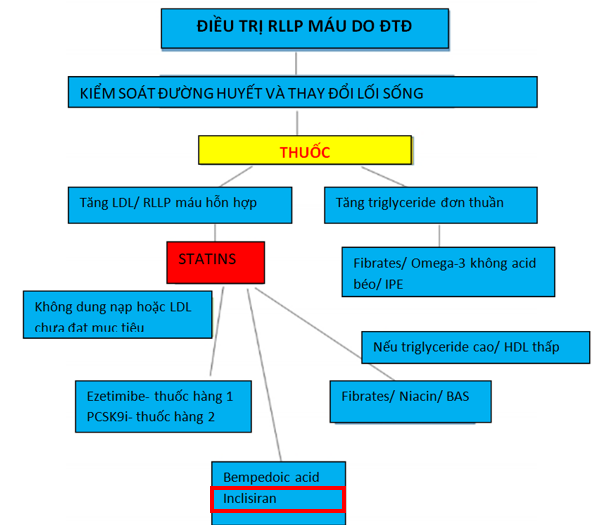
Hình 5. Lưu đồ điều trị rối loạn lipid do đái tháo đường. Statins là nền, phối hợp thuốc có thể xem xét ở bệnh nhân nguy cơ rất cao.(1)
- KẾT LUẬN
Rối loạn lipid do đái tháo đường (bao gồm tăng triglyceride máu, giảm HDL và tăng LDL nhỏ đậm đặc) đại diện cho tình trạng nguy cơ cao dẫn đến bệnh tim mạch do xơ vữa, mà trong đó tình trạng tăng triglyceride là chủ yếu. Kiểm soát tốt rối loạn lipid giúp giảm đáng kể nguy cơ tim mạch.
Cách đánh giá nguy cơ tim mạch dựa trên dân số sống sót không thể áp dụng được cho những bệnh nhân mắc đái tháo đường trẻ tuổi, bởi cách làm đó cho kết quả thấp hơn thực tế.
Các bằng chứng gần đây khuyến cáo áp dụng điều trị hạ lipid máu thường quy cho các bệnh nhân trẻ tuổi mắc đái tháo đường( cả type 1 và 2), trong đó statins là lựa chọn đầu tay. Tổng quát mà nói, statins nên được chỉ định cho tất cả bệnh nhân đái tháo đường với mức LDL >100 mg/dL, bắt đầu với liều trung bình và theo dõi xét nghiệm LDL liên tục.
Ezetimibe kết hợp với statin giúp giảm LDL nhiều hơn và cải thiện kết cục tim mạch trong tương lai. Fibrates có vai trò ở bệnh nhân tăng triglyceride và LDL thấp, fenofibrate nên được cân nhắc cho bệnh nhân đái tháo đường type 2 có bệnh lý võng mạc. Cuối cùng, các thuốc hạ lipid mới ức chế PCSK9 có thể tích hợp sẵn vào điều trị ở bệnh nhânđái tháo đường có rối loạn lipid máu, sử dụng phối hợp với statins, ezetimibe và fibrates. Điều quan trọng cần nhớ là điều trị rối loạn lipid tối ưu giúp giảm biến cố tim mạch đến hơn 50%.
Ngoài ra chúng ta còn có thêm liệu pháp tự nhiên như Armolipid Plus® thay thế các thuốc tổng hợp hiện tại, phù hợp ở những bệnh nhân tăng lipid máu mức độ từ nhẹ với vửa không dung nạp với statins và không đạt mục tiêu LDL-C với ezetimibe, thuốc này còn giúp giảm biến cố tim mạch thông qua giảm độ cứng mạch máu. Các sản phẩm thực dưỡng cũng ngày càng được quan tâm vì chúng vửa tự nhiên lại vừa có tác dụng điều trị, phù hợp với các bệnh nhân có rối loạn lipid máu đơn thuần không kèm bệnh lý tim mạch.
TÀI LIỆU THAM KHẢO
- de Castro.ML: Diabetic dyslipidaemia: which drugs to use. Vol. 19, N° 6 – 02 Dec 2020
- Patti. AM, Giglio. RA, Papanas. N, Rizzo.M & Rizvi. AA: Future perspectives of the pharmacological management of diabetic dyslipidemia. https://www.tandfonline.com/doi/full/10.1080/17512433.2019.1567328
3.Yee-Ming Cheung , O’Brien.R and Ekinci.EI: What is new in lipid-lowering therapies in diabetes?Internal Medicine Journal 49 (2019) 1472–1480.
https://doi.org/10.1111/imj.14291
- Banach.M et al: Association of Bempedoic Acid Administration With AtherogenicLipid Levels in Phase 3 Randomized Clinical Trials of PatientsWith Hypercholesterolemia. JAMA Cardiol. 2020;5(10):1124-1135. doi:10.1001/jamacardio.2020.2314Published online July 1, 2020
- Gupta.M et al: An update on pharmacotherapies in diabetic dyslipidemia. Progress in Cardiovascular Diseases(2019).
https://doi.org/10.1016/j.pcad.2019.07.006
- Lazarte. j, Hegele. Ra: Dyslipidemia Management in Adults With Diabetes
Published: July 12, 2019DOI:https://doi.org/10.1016/j.jcjd.2019.07.003
7. ESC Clinical Practice Guidelines.2019 Guidelines on Dyslipidaemias (Management of)
https://www.escardio.org/Guidelines/Clinical-Practice-Guidelines/Dyslipidaemias-Management-of
- Eun-Jung Rhee: Recent dyslipidemia guidelines for patients with diabetes mellitus. Precision and Future Medicine 2020;4(4):133-140 Published online: September 9, 2020







