8. Rối loạn nhịp thất (VA) ở tim cấu trúc bình thườngggg
TS PHẠM HỮU VĂN
|
Các khuyến cáo cho VA ở tim cấu trúc bình thường Tài liệu tham khảo ủng hộ các khuyến cáo được tóm tắt trong Tư liệu hỗ trợ online 45. |
||
|
COR |
LOE |
Khuyến cáo |
|
I |
B-R |
1. Ở các bệnh nhân có PVCs có triệu chứng ở tim bình thường trong tình trạng khác, điều trị bằng beta blocker hoặc chẹn canxi nondihydropyradine hữu ích để giảm loạn nhịp tái phát và cải thiện triệu chứng (1, 2). |
|
IIa |
B-R |
2. Ở các bệnh nhânVAcó triệu chứng ở tim bình thường ở tình trạng khác, điều trị bằng thuốc chống loạn nhịp là hợp lý để giảm các triệu chứng loạn nhịp tái phát và cải thiện triệu chứng nếu các thuốc chẹn beta và thuốc chẹn kênh canxi nondihydropyradine không có hiệu quả hoặc không dung nạp (3, 4). |
Tóm tắt
Hầu hết VA nguyên phát là do một cơ chế ổ của hoạt động khởi kích hoặc tính tự động bất thường, một số nhịp nhanh vào lại giữa các nhánh bó đã được ghi nhận. Các biểu hiện lâm sàng của VA nguyên phát rất biến đổi và dao động từ lành tính, PVCs không triệu chứng đến VT dai dẳng hoặc thậm chí VF. Trong phát hiện khởi đầu, đánh giá về bệnh tim cấu trúc được bảo đảm bằng khám thực thể, ECG và hình ảnh, thường là siêu âm tim. Trong trường hợp không có bất thường hoặc tiền sử gia đình có SCD, việc đánh giá và điều trị thêm sẽ được hướng dẫn bằng các triệu chứng. Nếu bệnh nhân không có triệu chứng và không có bằng chứng chứng về bệnh kênh tim, cần đảm bảo như đặc tính lành tự nhiên là đủ. Nếu loạn nhịp bị nghi ngờ thường xuyên liên tục gây ra rối loạn chức năng thất theo thời gian, nên theo dõi định kỳ để đánh giá lại chức năng thất (xem Phần 10.8). Đối với các triệu chứng nhẹ, tránh các yếu tố tăng nặng như sử dụng quá nhiều chất caffein hoặc các thuốc giống giao cảm, có thể là đủ. Liệu pháp với thuốc chẹn beta hoặc thuốc chẹn kênh canxi nondihydropyradine làm giảm triệu chứng cho một số bệnh nhân. Thuốc chống loạn nhịp nhóm I có thể có hiệu quả, nhưng thường tránh dùng vì các tác dụng phụ. Đối với những bệnh nhân đòi hỏi ức chế rối loạn nhịp, đối với các trường hợp này các thuốc chống rối loạn nhịp không hiệu quả, không dung nạp, hoặc không mong muốn, triệt phá qua catheter có thể là điều trị có hiệu quả cao (xem Phần 9). Chiến lược triệt phá để nhận biết vị trí nguồn gốc được biểu hiện bằng vị trí hoạt hóa điện học sớm nhất hoặc, khi điều này không khả thi, bằng lập bản đồ tạo nhịp (pace – mapping). Vị trí nguồn gốc thông thường nhất đối với VA nguyên phát là từ đường ra thất phải (RVOT) hoặc hoặc các lỗ nhỏ (ostium) của LV, bao gồm chỗ mở hình bầu dục của LV đến phần động mạch chủ được gắn vào phía trước và nhĩ trái được gắn vào phía sau. Nguồn gốc có thể có thể được dự đoán một cách hợp lý từ hình thái QRS của VA, điều này cung cấp chỉ dẫn tốt về loại phương pháp tiếp cận được đòi hỏi và khả năng thành công và nguy cơ. Triệt phá thất bại thường liên quan đến không có VA cho việc lập bản đồ khi thủ thuật, hoặc nguồn gôc VA ở khi vực của tim không tiếp cận được. Các ổ này đôi khi tạo ra VT đơn hình dai dẳng (5-7).
Văn bản Hỗ trợ Riêng biệt – Khuyến cáo
1. Trong một nghiên cứu đối chứng ngẫu nhiên, mù đôi, giả dược trên 52 bệnh nhân VA có triệu chứng và số lượng PVC trung bình 21.407 ± 1740 nhịp mỗi 24 giờ, atenolol làm giảm đáng kể tần số triệu chứng (p = 0.03) và số lượng PVC (p = 0,001), trong khi giả dược không ảnh hưởng đến số lượng PVC (p = 0,78) hoặc nhịp tim trung bình (p = 0,44) (8). Một so sánh ngẫu nhiên về thuốc chống loạn nhịp với triệt phá qua catheter, metoprolol hoặc propafenone có hiệu quả khiêm tốn để ức chế RVOT-VA mặc dù tỷ lệ tái phát cao hơn rất nhiều so với triệt phá qua catheter (9).
2. Trong một nghiên cứu RCT trên 233 bệnh nhân có ≥30 PVCs mỗi giờ, d-sotalol đã được chứng minh làm giảm lượng PVC thường xuyên, nhưng chỉ có racemic dl-sotalol hiện có sẵn (10). Trong một so sánh ngẫu nhiên ngẫu nhiên các thuốc chống loạn nhịp với triệt phá qua catheter, điều trị metoprolol hoặc propafenone có hiệu quả khi sử dụng để ức chế RVOT PVC mặc dù tỷ lệ tái phát cao hơn rất nhiều so với triệt phá qua catheter (9). Các thuốc chẹn kênh canxi Nydihydropyridine làm giảm loạn nhịp (1, 2, 11, 12).
Tài liệu tham khảo
1. Gill JS, Blaszyk K, Ward DE, et al. Verapamil for the suppression of idiopathic ventricular tachycardia of left bundle branch blốc-like morphology. Am Heart J. 1993;126:1126-33.
2. Gill JS, Ward DE, Camm AJ. Comparison of verapamil and diltiazem in the suppression of idiopathic ventricular tachycardia. Pacing Clin Electrophysiol. 1992;15:2122-6.
3. Kontos MC, Diercks DB, Ho PM, et al. Treatment and outcomes in patients with myocardial infarction treated with acute beta-blocker therapy: results from the American College of Cardiology’s NCDR(R). Am Heart J. 2011;161:864-70.
4. Levine JH, Massumi A, Scheinman MM, et al. Intravenous amiodarone for recurrent sustained hypotensive ventricular tachyarrhythmias. Intravenous Amiodarone Multicenter Trial Group. J Am Coll Cardiol. 1996;27:67-75.
5. Noda T, Shimizu W, Taguchi A, et al. Malignant entity of idiopathic ventricular fibrillation and polymorphic ventricular tachycardia initiated by premature extrasystoles originating from the right ventricular outflow tract. J Am Coll Cardiol. 2005;46:1288-94.
6. Viskin S. Idiopathic polymorphic ventricular tachycardia: a “benign disease” with a touch of bad luck? Korean Circ J. 2017;47:299-306.
7. Viskin S, Rosso R, Rogowski O, et al. The “short-coupled” variant of right ventricular outflow ventricular tachycardia: a not-so-benign form of benign ventricular tachycardia? J Cardiovasc Electrophysiol. 2005;16:912-6.
8. Krittayaphong R, Bhuripanyo K, Punlee K, et al. Effect of atenolol on symptomatic ventricular arrhythmia without structural heart disease: a randomized placebo-controlled study. Am Heart J. 2002;144:e10. efficacy when used to suppress RVOT PVCs although with a far higher rate of recurrence than catheter ablation (9). Nondihydropyridine calcium channel blockers reduce arrhythmias (1, 2, 11, 12).
9. Ling Z, Liu Z, Su L, et al. Radiofrequency ablation versus antiarrhythmic medication for treatment of ventricular premature beats from the right ventricular outflow tract: prospective randomized study. Circ Arrhythm Electrophysiol. 2014;7:237-43.
10.Hohnloser SH, Meinertz T, Stubbs P, et al. Efficacy and safety of d-sotalol, a pure class III antiarrhythmic compound, in patients with symptomatic complex ventricular ectopy. Results of a multicenter, randomized, double-blind, placebo-controlled dose-finding study. The d-Sotalol PVC Study Group. Circulation. 1995;92:1517-25.
11.Badhwar N, Scheinman MM. Idiopathic ventricular tachycardia: diagnosis and management. Curr Probl Cardiol. 2007;32:7-43.
12.Connolly SJ. Meta-analysis of antiarrhythmic drug trials. Am J Cardiol. 1999;84:90R-3R.
8.1. Rối loạn nhịp thất (VA) đường thoát và vòng nhĩ thất
|
Các khuyến cáo cho VA đường thoát Tài liệu tham khảo hỗ trợ các khuyến cáo được tóm tắt trong tư liệu hỗ trợ Online 46. |
||
|
COR |
LOE |
Các khuyến cáo |
|
I |
B-NR |
1. Ở các bệnh nhân VA đường thoát có triệu chứng ở tim bình thường khác đối với họ các thuốc chống loạn nhịp không hiệu quả, không dung nạp, hoặc bệnh nhân không ưa chuộng, triệt phá qua catheter là hữu ích (1-3). |
|
I |
B-NR |
2. Ở các bệnh nhân VT đường thoát có triệu chứng ở tim bình thường khác, beta blocker hoặc chẹn kênh canxi là hữu ích (1-3). |
Văn bản Hỗ trợ Riêng biệt – Khuyến cáo
1. Trong 1 RCT, việc triệt phá qua catheter ưu thế hơn các thuốc chống loạn nhịp trong việc ngăn chặn các PVC thường xuyên phát sinh từ RVOT (4). Các nghiên cứu quan sát đã cho thấy triệt phá qua catheter bằng năng lượng tần số radio có hiệu quả trong điều trị VA nguyên phát phát sinh từ RVOT và đường ra LV (2, 5-16). Vị trí triệt phát có thể là ở dưới hoặc ở trên van phổi trong RVOT (9, 13). Mặc dù hầu hết các RVOT VA có thể được triệt phá trong phạm vi RV, 10% có thể đòi hỏi triệt phá trong phạm vi đỉnh của đường cong (cusp) xoang phổi (9). Các biến chứng nghiêm trọng thường ít. Đối với VA đường ra LV, vị trí triệt phá có thể trong phạm vi xoang đỉnh đường cong (cusp) động mạch chủ (11, 14, 16), dưới van động mạch chủ (2, 6), ở khoảng nối tiếp hai lá động mạch chủ (1-3) hoặc trên bề mặt thượng tâm đỉnh LV (3, 17, 18). Vòng van hai lá và ba lá vị trí ít gặp của VA nguyên phát, nhưng VA này có thể cũng được điều trị có hiệu quả bằng triệt phá qua catheter (1, 19, 20). Khoảng 10% VA nguyên phát có thể phát sinh từ đỉnh của LV. Một số có thể được được triệt phá từ tĩnh mạch tim lớn hoặc bề mặt thượng tâm mạc, nhưng các vị trí khác phát sinh từ khi vực không thể tiếp cận ở sát với động mạch vành trái tháo dỡ khỏi tĩnh mạch tim hoặc trên bề mặt nhĩ, nhưng một số khác lại xuất hiện từ một vùng không thể tiếp cận gần động mạch vành trái, làm mất đi hiệu quả triệt phá (14). Các vị trí nguồn gốc trong cơ ít gặp nhưng có thể đòi hỏi triệt phá trên bề mặt cả hai nội tâm mạc và thượng tâm mạc của các lỗ LV (3). Các biến chứng do triệt phá VA đường thoát ít gặp, nhưng biến chứng chảy máu liên quan đến tiếp cận động mạch và tĩnh mạch, ép ngoại tâm mạc (tamponade), tổn thương đến các động mạch vành có thể xảy ra.
2. Trong một so sánh ngẫu nhiên tiền cứu các thuốc chống loạn nhịp đối lại với triệt phá qua catherter, metoprolol hoặc propafenone tỏ ra có hiệu quả khiêm tốn khi dùng để ức chế RVOT PVC, mặc dù tỷ lệ tái phát cao hơn rất nhiều so với triệt phá qua catheter (4). Các thuốc chẹn kênh canxi nondihydropyradine ngăn chặn loạn nhịp ở một số bệnh nhân (4).
Tài liệu tham khảo
1. Tada H, Ito S, Naito S, et al. Idiopathic ventricular arrhythmia arising from the mitral annulus: a distinct subgroup of idiopathic ventricular arrhythmias. J Am Coll Cardiol. 2005;45:877-86.
2. Yamada T, Litovsky SH, Kay GN. The left ventricular ostium: an anatomic concept relevant to idiopathic ventricular arrhythmias. Circ Arrhythm Electrophysiol. 2008;1:396-404.
3. Yamada -T, Maddox WR, McElderry HT, et al. Radiofrequency catheter ablation of idiopathic ventricular arrhythmias originating from intramural foci in the left ventricular outflow tract: efficacy of sequential versus simultaneous unipolar catheter ablation. Circ Arrhythm Electrophysiol. 2015;8:344-52.
4. Ling Z, Liu Z, Su L, et al. Radiofrequency ablation versus antiarrhythmic medication for treatment of ventricular premature beats from the right ventricular outflow tract: prospective randomized study. Circ Arrhythm Electrophysiol. 2014;7:237-43.
5. Carballeira Pol L, Deyell MW, Frankel DS, et al. Ventricular premature depolarization QRS duration as a new marker of risk for the development of ventricular premature depolarization-induced cardiomyopathy. Heart Rhythm. 2014;11:299-306.
6. Kamioka M, Mathew S, Lin T, et al. Electrophysiological and electrocardiographic predictors of ventricular arrhythmias originating from the left ventricular outflow tract within and below the coronary sinus cusps. Clin Res Cardiol. 2015;104:544-54.
7. Konstantinidou M, Koektuerk B, Wissner E, et al. Catheter ablation of right ventricular outflow tract tachycardia: a simplified remote-controlled approach. Europace. 2011;13:696-700.
8. Latchamsetty R, Yokokawa M, Morady F, et al. Multicenter outcomes for catheter ablation of idiopathic premature ventricular complexes. JACC Clin Electrophysiol. 2015;1:116-23.
9. Liao Z, Zhan X, Wu S, et al. Idiopathic ventricular arrhythmias originating from the pulmonary sinus cusp: prevalence, electrocardiographic/electrophysiological characteristics, and catheter ablation. J Am Coll Cardiol. 2015;66:2633-44.
10.Morady F, Kadish AH, DiCarlo L, et al. Long-term results of catheter ablation of idiopathic right ventricular tachycardia. Circulation. 1990;82:2093-9.
11.Ouyang F, Fotuhi P, Ho SY, et al. Repetitive monomorphic ventricular tachycardia originating from the aortic sinus cusp: electrocardiographic characterization for guiding catheter ablation. J Am Coll Cardiol. 2002;39:500-8.
12.Pedersen CT, Kay GN, Kalman J, et al. EHRA/HRS/APHRS expert consensus on ventricular arrhythmias. Heart Rhythm. 2014;11:e166-96.
13.Tada H, Tadokoro K, Miyaji K, et al. Idiopathic ventricular arrhythmias arising from the pulmonary artery: prevalence, characteristics, and topography of the arrhythmia origin. Heart Rhythm. 2008;5:419-26.
14.Yamada T, McElderry HT, Doppalapudi H, et al. Idiopathic ventricular arrhythmias originating from the aortic root prevalence, electrocardiographic and electrophysiologic characteristics, and results of radiofrequency catheter ablation. J Am Coll Cardiol. 2008;52:139-47.
15.Yamada T, McElderry HT, Doppalapudi H, et al. Idiopathic ventricular arrhythmias originating from the left ventricular summit: anatomic concepts relevant to ablation. Circ Arrhythm Electrophysiol. 2010;3:616-23.
16.Yamada T, McElderry HT, Okada T, et al. Idiopathic left ventricular arrhythmias originating adjacent to the left aortic sinus of valsalva: electrophysiological rationale for the surface electrocardiogram. J Cardiovasc Electrophysiol. 2010;21:170-6.
17.Mountantonakis SE, Frankel DS, Tschabrunn CM, et al. Ventricular arrhythmias from the coronary venous system: prevalence, mapping, and ablation. Heart Rhythm. 2015;12:1145-53.
18.Nagashima K, Choi EK, Lin KY, et al. Ventricular arrhythmias near the distal great cardiac vein: challenging arrhythmia for ablation. Circ Arrhythm Electrophysiol. 2014;7:906-12.
19.Hai JJ, Chahal AA, Friedman PA, et al. Electrophysiologic characteristics of ventricular arrhythmias arising from the aortic mitral continuity-potential role of the conduction system. J Cardiovasc Electrophysiol. 2015;26:158-63.
20.Tada H, Tadokoro K, Ito S, et al. Idiopathic ventricular arrhythmias originating from the tricuspid annulus: prevalence, electrocardiographic characteristics, and results of radiofrequency catheter ablation. Heart Rhythm. 2007;4:7-16.
8.2. VA cơ nhú (Papillary Muscle VA)
|
Khuyến cáo cho VA cơ nhú (PVCs và VT) Tài liệu tham khảo ủng hộ các khuyến cáo được tóm tắt trong tư liệu hỗ trợ online 47. |
||
|
COR |
LOE |
Khuyến cáo |
|
I |
B-NR |
1. Ở các bệnh nhân VA có triệu chứng phát sinh từ cơ nhú đối với những người các thuốc chống loạn nhịp không có hiệu quả, không dung nạp, hoặc không được bệnh nhân ưa thích, triệt phá qua catheter là hữu ích (1-5). |
Văn bản Hỗ trợ Riêng biệt – Khuyến cáo
1. Cơ nhú của LV hoặc RV có thể là vị trí nguồn gốc của VA có thể có hoặc không có bệnh tim cấu trúc (1-5). VA cơ nhú thất trái và thất phải nguyên phát thường nhất là PVCs và NSVT, và thường liên quan đến gắng sức và có thể tạo ra bằng truyền epinephrine hoặc isoproterenol tĩnh mạch (3). Các loạn nhịp này có cơ chế ổ, không phải vào lại. Bất kỳ cơ nhú RV (3) nào cũng có thể là vị trí nguồn gốc và triệt phá qua catheter thường cơ hiệu quả (2). Trong 1 nghiên cứu, triệt phá thành công đã đạt được ở tất cả 8 bệnh nhân với giảm gánh nặng PVC tử 17±20% đến 0.6±0.8% (2). Ở thất trái, vị trí nguồn gốc có thể hoặc cơ nhú sau giữa hoặc trước bên (1, 4, 5). Nhiều hình thái QRS của VA được quan sát ở 47% bệnh nhân, triệt phá ở cả hai mặt của cơ nhú cần thiết ở vài bệnh nhân (4). Đạt được ổn định catheter phù hợp có thể là một thách thức. Thành công cấp thời cao, nhưng tái phát nhiều hơn so với VA đường thoát nguyên phát. Các biến chứng nặng, gồm tổn thương van, thường ít gặp. Các nguy cơ triệt phá qua catheter gồm chảy máu liên quan đến tiếp cận động mạch và tĩnh mạch và nguy cơ thấp của tamponade màng ngoài tim.
Tài liệu tham khảo
1. Ban JE, Lee HS, Lee DI, et al. Electrophysiological characteristics related to outcome after catheter ablation of idiopathic ventricular arrhythmia originating from the papillary muscle in the left ventricle. Korean Circ J. 2013;43:811-8.
2. Crawford T, Mueller G, Good E, et al. Ventricular arrhythmias originating from papillary muscles in the right ventricle. Heart Rhythm. 2010;7:725-30.
3. Doppalapudi H, Yamada T, McElderry HT, et al. Ventricular tachycardia originating from the posterior papillary muscle in the left ventricle: a distinct clinical syndrome. Circ Arrhythm Electrophysiol. 2008;1:23-9.
4. Yamada T, Doppalapudi H, McElderry HT, et al. Electrocardiographic and electrophysiological characteristics in idiopathic ventricular arrhythmias originating from the papillary muscles in the left ventricle: relevance for catheter ablation. Circ Arrhythm Electrophysiol. 2010;3:324-31.
5. Yokokawa M, Good E, Desjardins B, et al. Predictors of successful catheter ablation of ventricular arrhythmias arising from the papillary muscles. Heart Rhythm. 2010;7:1654-9.
8.3. VT vào lại nhánh bó (nhịp nhanh Belhassen)
|
Khuyến cáo cho VT nhánh bó (nhịp nhanh Belhassen) Tài liệu tham khảo hỗ trợ các khuyến cáo được tóm tắt trong phần Bổ sung Dữ liệu online 48. |
||
|
COR |
LOE |
Các khuyến cáo |
|
I |
B-NR |
1. Ở các bệnh nhân nhạy cảm với verapamil, LVT nguyên phát liên quan đến vào lại nhánh bó đối với họ các thuốc chống loạn nhịp không hiệu quả, không dung nạp, hoặc bệnh nhân không ưa thích, triệt phá qua catheter là hữu ích (1-3). |
|
I |
B-NR |
2. Ở các bệnh nhân LVT nhạy cảm với verapamil huyết động ổn định lâu dài liên quan đến vào lại nhánh bó, tiêm tĩnh mạch verapamil để cắt cơn VT được khuyến cáo (3-6). |
|
IIa |
C-LD |
3. Ở các bệnh nhân LVT nguyên phát nhạy cảm với verapamil tái phát tái phát, điều trị lâu dài bằng uống verapamil có thể hữu ích (7-10). |
Văn bản Hỗ trợ Riêng biệt- Khuến cáo
1. Nhịp nhanh thất bên trái (LVT)nguyên phát do vào lại liên quan đến một phần của hệ thống LV Purkinje, thường bó nhánh sau trái khi nhánh dẫn truyền ngược của vòng và được xác định không hoàn toàn một phần tổ chức LV khi nhánh dẫn xuôi, phân chia của nó nhạy cảmvớiverapamil (1-3). Các VT này kéo dài một cách điển hình với QRS có cấu hình blốc nhánh bó phải với trục trên phải với một trục phía trên. Ít gặp hơn là trục VT phía dưới hoặc VT QRS tương đối hẹp xảy ra như là kết quả của các đường vào lại luân phiên, cũng liên quan một phần của hệ thống Purkinje. Thuốc chẹn beta hoặc verapamil thường cắt các cơn rối loạn nhịp này, nhưng thất bại để ngăn ngừa tái phát ở một số bệnh nhân(1-3). Mục tiêu triệt phá cho hình thái phổ biến nhất thường đưa vào đầu xa của nhánh xuôi của hệ thống Purkinje dọc theo phần dưới của váchthất trái(LV)gần chỗ nối của nó với bó sau trái. Triệt phá qua catheter thành công cấp thời ở > 90% bệnh nhân với nguy cơ tái phát khoảng 10%. VT này có thể giống với VA bó do cơ chế ổ ở các bó sau trái hoặc trước trái của hệ thống His-Purkinje LV. Các rối loạn nhịp bó này thường có cơ chế ổ với đích triệt phá qua catheter là vị trí hoạt động điện sớm nhất được ghi với điện thế bó trước tâm thu. Triệt phá qua catheter có hiệu quả cao đối với VA bó và liên bó. Các biến chứng nặng ít gặp và gồm chảy máu ở vị trí tiếp cận động mạch hoặc tĩnh mạch và nguy cơ nhỏ blốc nhánh bó hoặc blốc nhĩ thất.
2. LVT nguyên phát dựa trên cơ sở cơ chế vào lại liên quan đến tổ chức với các đặc tính dẫn truyền chậm dọc theo vách LV khi nhánh xuôi và bó sau trái bình thường của hệ His Purkinje như là nhánh ngược. Vùng dẫn truyền chậm nhậy cảmvớiverapamil (3-6). Các rối loạn nhịp này thường có hình thái blốc nhánh bó phải điển hình với trục trên, mặc dù sự đảo chiều của vòng có thể tạo ra QRS tương đối hẹp trong quá trình VT. Verapamil thường cắt cơn rối loạn nhịp này trong vùng dẫn truyền chậm xuôi (3-6).
3. Mặc dù không có báo cáo RCT đã được công bố nhưng việc sử dụng verapamil kéo dài cho VT nhạy cảm với verapamil đã được báo cáo để kiểm soát nhịp nhanh này ở nhiều bệnh nhân, gồm cả hai người lớn và trẻ em (5, 8-10).
Tài liệu tham khảo
1. Lin D, Hsia HH, Gerstenfeld EP, et al. Idiopathic fascicular left ventricular tachycardia: linear ablation lesion strategy for noninducible or nonsustained tachycardia. Heart Rhythm. 2005;2:934-9.
2. Liu Y, Fang Z, Yang B, et al. Catheter ablation of fascicular ventricular tachycardia: long-term clinical outcomes and mechanisms of recurrence. Circ Arrhythm Electrophysiol. 2015;8:1443-51.
3. Nogami A, Naito S, Tada H, et al. Demonstration of diastolic and presystolic Purkinje potentials as critical potentials in a macroreentry circuit of verapamil-sensitive idiopathic left ventricular tachycardia. J Am Coll Cardiol. 2000;36:811-23.
4. Belhassen B, Rotmensch HH, Laniado S. Response of recurrent sustained ventricular tachycardia to verapamil. Br Heart J. 1981;46:679-82.
5. German LD, Packer DL, Bardy GH, et al. Ventricular tachycardia induced by atrial stimulation in patients without symptomatic cardiac disease. Am J Cardiol. 1983;52:1202-7.
6. Tsuchiya T, Okumura K, Honda T, et al. Effects of verapamil and lidocaine on two components of the re-entry circuit of verapamil-senstitive idiopathic left ventricular tachycardia. J Am Coll Cardiol. 2001;37:1415-21.
7. Anderson JH, Tester DJ, Will ML, et al. Whole-exome molecular autopsy after exertion-related sudden unexplained death in the young. Circ Cardiovasc Genet. 2016;9:259-65.
8. Ohe T, Shimomura K, Aihara N, et al. Idiopathic sustained left ventricular tachycardia: clinical and electrophysiologic characteristics. Circulation. 1988;77:560-8.
9. Snyder C, Bishara J, Darling R, et al. Verapamil-sensitive ventricular tachycardia in an infant. Congenit Heart Dis. 2006;1:124-6.
10.Wang JD, Fu YC, Jan SL, et al. Verapamil sensitive idiopathic ventricular tachycardia in an infant. Jpn Heart J. 2003;44:667-71.
8.4. VT đa hình / VF nguyên phát
|
Các khuyến cáo cho VT đa hình /VF nguyên phát Tài liệu hỗ trợ cho khuyến cáo được tóm tắt trong Tư liệu Hỗ trợ online 49. |
||
|
COR |
LOE |
Các khuyến cáo |
|
I |
B-NR |
1. Ở các bệnh nhân trẻ tuổi (<40 tuổi) với SCA không giải thích được, gần đuối nước không giải thích, hoặc ngất do gắng sức tái phát, những người không bị bệnh tim thiếu máu cục bộ hoặc các bệnh tim cấu trúc khác, nên đánh giá thêm về hội chứng loạn nhịp di truyền được khuyến cáo (1-8). |
|
I |
B-NR |
2. Ở các bệnh nhân được hồi sức từ SCA do VT đa hình hoặc VF, ICD được khuyến cáo nếu sống sót có ý nghĩa > 1 năm được khuyến cáo (9-13). |
|
I |
B-NR |
3. Đối với bệnh nhân có các cơn VF nguyên phát tái phát được khởi đầu bằng PVC có hình thái QRS đồng nhất, triệt phá qua catheter là hữu ích (11, 14). |
Văn bản Hỗ trợ Riêng biệt – Khuyến cáo
1. Khi kết hợp với đánh giá lâm sàng, xét nghiệm di truyền có thể chẩn đoán trong khoảng từ 13% đến 60% trẻ (< 40 tuổi) sống sót của SCA (3), với các kiểu gen phổ biến nhất được nhận biết liên quan với hội chứng QT dài, nhịp nhanh thất đa hình do tiết catecholamine, hội chứng Brugada (8). Các biến cố đuối nước / gần đuối nước đặc biệt liên quan với LQT1 và nhịp nhanh thất đa hình do tiết catecholamine; các đột biến di truyền trong hội chứng QT dài và nhịp nhanh thất đa hình do tiết catecholamine đã được nhận biết ở 23% bệnh nhân với các cơn gần đuối nước không giải thích được (15). Trong một nghiên cứu (6), ngừng tim liên quan đến gắng sức, đặc biệt ở trẻ em, có thể liên quan đến hội chứng QT dài, nhịp nhanh thất đa hình do tiết catecholamine, hoặc hội chứng QT dài qua trung gian calmodulin / triadin / các đột biến nhịp nhanh thất đa hình do tiết catecholamine, có thể đòi hỏi test di truyền chuyên biệt bổ xung (1, 2, 4, 16-18). Các tai nạn lái xe hơi đơn giản nên nỗ lực xem xét các nguyên nhân rối loạn nhịp. Hiệu suất xét nghiệm di truyền cao hơn nếu có tiền sử gia đình về SCD ở người trẻ. Việc giới thiệu đến các trung tâm xét nghiệm di truyền chuyên môn là rất quan trọng nếu chuyên môn địa phương không có.
2. VF khi không có các bệnh tim cấu trúc có thể nhận biết được hoặc các hội chứng rối loạn nhịp di truyền đã biết như nhịp thất trái đa hình, hội chứng QT dài, hội chứng QT ngắn, hội chứng Brugada, hoặc hội chứng sóng J thường là kết quả của các PVC khoảng ghép ngắn phát sinh từ hệ thống Purkinje ở hoặc tâm thất phải hay trái, hoặc ít phổ biến hơn, từ cơ tâm thất (9-13). Nguy cơ tái phát sau hồi sinh VF nguyên phát rất cao (12). Trong số 38 bệnh nhân liên tiếp từ 6 trung tâm khác nhau được triệt phá VF nguyên phát tiên phát khởi đầu bằng PVC khoảng ghép ngắn, 87% đã trải qua ≥ 2 cơn VF trong năm trước (12). Do VF nguyên phát có liên quan đến nguy cơ tái phát VF rất cao, ICD được chỉ định để ngăn ngừa SCD. Triệt phá qua catheter các ổ khởi kích đã chứng minh hiệu quả cao trong việc loại bỏ PVC lắp lại chúng tạo VF ở các bệnh nhân này (11). Trong thời gian theo dõi sau thủ thuật trung bình 63 tháng, có 7 bệnh nhân (18%) trong 38 bệnh nhân được thực hiện triệt phá qua catheter VF nguyên phát được tạo ra do các PVCs có khoảng ghép ngắn bị tái phát VF trong thời gian theo dõi trung bình 4 tháng. Năm trong số 7 bệnh nhân được triệt phá lặp đi lặp lại không có VF tái phát. Vì vậy, mặc dù việc triệt phá qua catheter rất hiệu quả trong VF nguyên phát, nguy cơ tái phát còn rất lớn sau thủ thuật thành công rõ ràng và bệnh nhân nên được bảo vệ với ICD. ICD dưới da có thể không phải là một liệu pháp tốt cho những bệnh nhân này do nguy cơ cao hơn của nhận cảm sóng T được thấy trong quần thể này; tuy nhiên, tư liệu còn hạn chế (10).
3. VF nguyên phát có thể được khởi đầu bằng PVC phát sinh từ các đường thoát hoặc hệ thống His-Purkinje trong phạm vi hoặc thất phải hoặc thất trái (11, 14, 19-21). Một số bệnh nhân có các chùm cơn VF (bão điện) biểu hiện điển hình như các PVCs khởi đầu VT đa hình / VF. PVC thường có hình thái QRS đồng nhất và khoảng ghép ngắn và có thể là đích cho triệt phá để kiểm soát rối loạn nhịp (11). Đối với PVCs từ hệ thống Purkinje, mục tiêu triệt phá là điện thế Purkinje tần số cao đi trước PVCs. Khi các cơn được tạo ra bằng các PVCs khoảng ghép ngắn phát triển từ các đường thoát, đích triệt phá là vị trí hoạt động thất sớm nhất. Các bệnh nhân VF nguyên phát hay có thời kỳ VT / VF thường xuyên xen kẽ với thời kỳ tương đối yên lặng (11, 14). Để tối đa hóa xác suấttriệt pháthành công, thủ thuật được thực hiện tốt nhất trong thời kỳ PVC thường xuyên. Các đợt không thường xuyên của VF có thể thích hợp với việc triệt phá nếu thường xuyên có PVC với các hình thái QRS đồng nhất. Khi PVCs có thể được xác định, triệt phá thành công cao, nhưng sự tái phát trễ xảy ra ở khoảng 10% bệnh nhân do đó việc cấy ICD là quan trọng ngay cả khi việc triệt phá thành công rất lớn. Những nguy cơ triệt phá qua catheter gồm chảy máu ở vị trí tiếp cận động mạch hoặc tĩnh mạch và nguy cơ nhỏdo chènép tim (tamponade). Việc điều trị bằng quinidine cấp thời và kéo dài có thể ngăn chặn tái phát các cơn VF ở một sốbệnh nhân(22).
Tài liệu tham khảo
1. Anderson JH, Tester DJ, Will ML, et al. Whole-exome molecular autopsy after exertion-related sudden unexplained death in the young. Circ Cardiovasc Genet. 2016;9:259-65.
2. Dalal A, Czosek RJ, Kovach J, et al. Clinical presentation of pediatric patients at risk for sudden cardiac arrest. J Pediatr. 2016;
3. Kumar S, Peters S, Thompson T, et al. Familial cardiological and targeted genetic evaluation: low yield in sudden unexplained death and high yield in unexplained cardiac arrest syndromes. Heart Rhythm. 2013;10:1653-60.
4. Linzer M, Pritchett EL, Pontinen M, et al. Incremental diagnostic yield of loop electrocardiographic recorders in unexplained syncope. Am J Cardiol. 1990;66:214-9.
5. Solomon SD, Zelenkofske S, McMurray JJ, et al. Sudden death in patients with myocardial infarction and left ventricular dysfunction, heart failure, or both. N Engl J Med. 2005;352:2581-8.
6. Tester DJ, Medeiros-Domingo A, Will ML, et al. Unexplained drownings and the cardiac channelopathies: a molecular autopsy series. Mayo Clin Proc. 2011;86:941-7.
7. Tzimas I, Zingraf JC, Bajanowski T, et al. The role of known variants of KCNQ1, KCNH2, KCNE1, SCN5A, and NOS1AP in water-related deaths. Int J Legal Med. 2016;1575-9.
8. Wang D, Shah KR, Um SY, et al. Cardiac channelopathy testing in 274 ethnically diverse sudden unexplained deaths. Forensic Sci Int. 2014;237:90-9.
9. Conte G, Caputo ML, Regoli F, et al. True idiopathic ventricular fibrillation in out-of-hospital cardiac arrest survivors in the Swiss Canton Ticino: prevalence, clinical features, and long-term follow-up. Europace. 2017;19:259-66.
10.Frommeyer G, Dechering DG, Kochhauser S, et al. Long-time “real-life” performance of the subcutaneous ICD in patients with electrical heart disease or idiopathic ventricular fibrillation. J Interv Card Electrophysiol. 2016;47:185-8.
11.Haïssaguerre M, Shoda M, Jais P, et al. Mapping and ablation of idiopathic ventricular fibrillation. Circulation. 2002;106:962-7.
12.Knecht S, Sacher F, Wright M, et al. Long-term follow-up of idiopathic ventricular fibrillation ablation: a multicenter study. J Am Coll Cardiol. 2009;54:522-8.
13.Leenhardt A, Glaser E, Burguera M, et al. Short-coupled variant of torsade de pointes. A new electrocardiographic entity in the spectrum of idiopathic ventricular tachyarrhythmias. Circulation. 1994;89:206-15.
14.Haïssaguerre M, Shah DC, Jais P, et al. Role of Purkinje conducting system in triggering of idiopathic ventricular fibrillation. Lancet. 2002;359:677-8.
15.Albertella L, Crawford J, Skinner JR. Presentation and outcome of water-related events in children with long QT syndrome. Arch Dis Child. 2011;96:704-7.
16.Miyake CY, Motonaga KS, Fischer-Colbrie ME, et al. Risk of cardiac disease and observations on lack of potential predictors by clinical history among children presenting for cardiac evaluation of mid-exertional syncope. Cardiol Young. 2016;26:894-900.
17.Gula LJ, Klein GJ, Hellkamp AS, et al. Ejection fraction assessment and survival: an analysis of the Sudden Cardiac Death in Heart Failure Trial (SCD-HeFT). Am Heart J. 2008;156:1196-200.
18.Winkel BG, Yuan L, Olesen MS, et al. The role of the sodium current complex in a nonreferred nationwide cohort of sudden infant death syndrome. Heart Rhythm. 2015;12:1241-9.
19.Noda T, Shimizu W, Taguchi A, et al. Malignant entity of idiopathic ventricular fibrillation and polymorphic ventricular tachycardia initiated by premature extrasystoles originating from the right ventricular outflow tract. J Am Coll Cardiol. 2005;46:1288-94.
20.Sadek MM, Benhayon D, Sureddi R, et al. Idiopathic ventricular arrhythmias originating from the moderator band: electrocardiographic characteristics and treatment by catheter ablation. Heart Rhythm. 2015;12:67-75.
21.Van HH, Zado ES, Haqqani H, et al. Catheter ablation of ventricular fibrillation: importance of left ventricular outflow tract and papillary muscle triggers. Heart Rhythm. 2014;11:566-73.
22.Viskin S, Belhassen B. Idiopathic ventricular fibrillation. Am Heart J. 1990;120:661-71.
9. Bệnh cơ tim do PVC tạo ra (PVC-Induced Cardiomyopathy)
|
Các khuyến cáo cho bệnh cơ tim do PVC tạo ra Tài liệu tham khảo ủng hộ các khuyến cáo được tóm tắt trong tư liệu hỗ trợ online 50. |
||
|
COR |
LOE |
Các khuyến cao |
|
I |
B-NR |
1. Đối với những bệnh nhân cần chấn loại bỏ triệu chứng do rối loạn nhịp hoặc làm giảm chức năng thất nghi ngờ do PVCs thường xuyên (thường > 15% nhịp đập và chủ yếu là 1 hình thái học) và những người thuốc chống loạn nhịp không có hiệu quả, không dung nạp, hoặc bệnh nhân không ưa thích, triệt phá qua catheter là hữu ích (1, 2). |
|
IIa |
B-NR |
2. Ở các bệnh nhân với bệnh cơ tim do PVS tạo ra, điều trị bằng thuốc (ví dụ thuốc chẹn beta, amiodarone) là hợp lý để giảm nhịp tim tái phát và cải thiện triệu chứng và chức năng LV (3, 4). |
Văn bản Hỗ trợ Riêng biệt – Khuyến cáo
1. PVCs thường xuyên (thường> 15% toàn bộ số lượng các nhắt bóp) có thể tạo ra hình thái rối loạn chức năng LV có thể hồi phục (5-18). Tuy nhiên, đôi khi rất khó để xác định xem PVCs có gây rối loạn chức năng LV hay liệu rối loạn chức năng LV tiến triển có gây ra PVC thường xuyên hay không. Rối loạn chức năng LV có liên quan đến gánh nặng PVC lớn hơn (> 10% và thường> 20%), NSVT, sóng P ngược sau PVC, và PVC xen kẽ (interpolated) (6, 15). Trong một nghiên cứu tiền cứu về triệt phá qua catheter cho bệnh cơ tim do PVC gây ra, triệt phá thành công hoàn toàn ở 80% bệnh nhân (19). Chức năng LV bình thường trở lại trong vòng 6 tháng ở 82% trong số 22 bệnh nhân suy chức năng thất lúc đầu. Do đó, PVC thường xuyên là nguyên nhân có thể đảo ngược được của rối loạn chức năng LVvàcó thể được điều trị hiệu quả bằng triệt phá qua catheter. Rất khó để xác định xem liệu chức năng LV rõ ràng có phản ảnh chức năng LV suy hoặc không có khả năng để đánh giá chính xác chức năng thất trái do hoạt động ngoại vị thường xuyên. Ở những bệnh nhân có mật độ PVC cao với chức năng thất bình thường, điều trị tối ưu và giám sát để ngăn ngừa và phát hiện suy giảm chức năng thất.
2. Trong một nghiên cứu mù đôi với 30 bệnh nhân có hoặc không có bệnh tim thiếu máu cục bộ có > 30 PVCs mỗi giờ so sánh sotalol với propranolol, tác dụng thúc đẩy loạn nhịp hiện diện ở 1 bệnh nhân với sotalol. Không có sự khác biệt đáng kể về ức chế PVCs (sotalol 65%, propranolol 44%), với việc giảm trong ngoại tâm thu thất cặp (couplets) là 99% đối với sotalol và 49% đối với propranolol. Có sự gia tăng đáng kể về QTc ở bệnh nhân với sotalol (20). Trong một nghiên cứu đối chứng ngẫu nhiên, mù đôi với 674 bệnh nhân có HF và LVEF < 0.40 do thiếu máu cục bộ hoặc NICM và ≥10 PVCs mỗi giờ, amiodarone làm giảm đáng kể VA, nhịp tim chậm lại và có liên quan đến tăng LVEF 42% trong 2 năm với xu hướng giảm tử suất không có ý nghĩa thông kê (4). VA có bổ xung vào rối loạn chức năng thất ở các bệnh nhân này hay không còn chưa biết rõ.
Tài liệu tham khảo
1. Haïssaguerre M, Shah DC, Jais P, et al. Role of Purkinje conducting system in triggering of idiopathic ventricular fibrillation. Lancet. 2002;359:677-8.
2. Haïssaguerre M, Shoda M, Jais P, et al. Mapping and ablation of idiopathic ventricular fibrillation. Circulation. 2002;106:962-7.
3. Lee GK, Klarich KW, Grogan M, et al. Premature ventricular contraction-induced cardiomyopathy: a treatable condition. Circ Arrhythm Electrophysiol. 2012;5:229-36.
4. Singh SN, Fletcher RD, Fisher SG, et al. Amiodarone in patients with congestive heart failure and asymptomatic ventricular arrhythmia. Survival Trial of Antiarrhythmic Therapy in Congestive Heart Failure. N Engl J Med. 1995;333:77-82.
5. Baman TS, Lange DC, Ilg KJ, et al. Relationship between burden of premature ventricular complexes and left ventricular function. Heart Rhythm. 2010;7:865-9.
6. Ban JE, Park HC, Park JS, et al. Electrocardiographic and electrophysiological characteristics of premature ventricular complexes associated with left ventricular dysfunction in patients without structural heart disease. Europace. 2013;15:735-41.
7. Bogun F, Crawford T, Reich S, et al. Radiofrequency ablation of frequent, idiopathic premature ventricular complexes: comparison with a control group without intervention. Heart Rhythm. 2007;4:863-7.
8. Carballeira Pol L, Deyell MW, Frankel DS, et al. Ventricular premature depolarization QRS duration as a new marker of risk for the development of ventricular premature depolarization-induced cardiomyopathy. Heart Rhythm. 2014;11:299-306.
9. Del Carpio Munoz F, Syed FF, Noheria A, et al. Characteristics of premature ventricular complexes as correlates of reduced left ventricular systolic function: study of the burden, duration, coupling interval, morphology and site of origin of PVCs. J Cardiovasc Electrophysiol. 2011;22:791-8.
10.Deyell MW, Park KM, Han Y, et al. Predictors of recovery of left ventricular dysfunction after ablation of frequent ventricular premature depolarizations. Heart Rhythm. 2012;9:1465-72.
11.Hamon D, Blaye-Felice MS, Bradfield JS, et al. A new combined parameter to predict premature ventricular complexes induced cardiomyopathy: impact and recognition of epicardial origin. J Cardiovasc Electrophysiol. 2016;27:709-17.
12.Hasdemir C, Ulucan C, Yavuzgil O, et al. Tachycardia-induced cardiomyopathy in patients with idiopathic ventricular arrhythmias: the incidence, clinical and electrophysiologic characteristics, and the predictors. J Cardiovasc Electrophysiol. 2011;22:663-8.
13.Kanei Y, Friedman M, Ogawa N, et al. Frequent premature ventricular complexes originating from the right ventricular outflow tract are associated with left ventricular dysfunction. Ann Noninvasive Electrocardiol. 2008;13:81-5.
14.Kawamura M, Badhwar N, Vedantham V, et al. Coupling interval dispersion and body mass index are independent predictors of idiopathic premature ventricular complex-induced cardiomyopathy. J Cardiovasc Electrophysiol. 2014;25:756-2.
15.Niwano S, Wakisaka Y, Niwano H, et al. Prognostic significance of frequent premature ventricular contractions originating from the ventricular outflow tract in patients with normal left ventricular function. Heart. 2009;95:1230-7.
16.Olgun H, Yokokawa M, Baman T, et al. The role of interpolation in PVC-induced cardiomyopathy. Heart Rhythm. 2011;8:1046-9.
17.Yokokawa M, Good E, Crawford T, et al. Recovery from left ventricular dysfunction after ablation of frequent premature ventricular complexes. Heart Rhythm. 2013;10:172-5.
18.Zhong L, Lee YH, Huang XM, et al. Relative efficacy of catheter ablation vs antiarrhythmic drugs in treating premature ventricular contractions: a single-center retrospective study. Heart Rhythm. 2014;11:187-93.
19.Deyell MW, Park KM, Han Y, et al. Predictors of recovery of left ventricular dysfunction after ablation of frequent ventricular premature depolarizations. Heart Rhythm. 2012;9:1465-72.
20.Kubac G, Klinke WP, Grace M. Randomized double blind trial comparing sotalol and propranolol in chronic ventricular arrhythmia. Can J Cardiol. 1988;4:355-9.
10. VA và SCD liên quan đến các quần thể đặc biệt
10.1. Vận động viên thể thao
Ở vận động viên, phạm vi các VA từ PVCs đơn độc, cặp đôi, và NSVT, cho đến VT dai dẳng và SCA đưa đến SCA (1). Các PVCs và các đoạn NSVT lắp lại ngắn, đặc biệt khi không có bệnh tim cấu trúc, phổ biến hơn ở người không phải vận động viên, nhưng nhìn chung chúng lành tính, chỉ cần vận động hạn chế và hiếm khi dẫn tới việc bỏ thể thao (2, 3). Ngược lại, các đoạn NSVT dài hơn, đặc biệt xuất hiện khi gắng sức, VT daidẳng và SCA / SCD thường ít gặp, nhưng chúng có tỷ lệ cao hơn ở vận động viên so với các thông báo ở quần thể nói chung ở các nhóm lứa tuổi tương ứng. Các ước tính đã được báo cáo về SCD từ 1 / 53,703 vận động viên/năm trong cơ sở dữ liệu Hiệp hội Nghiệp đoàn Vận động viên Quốc gia (4) đến < 1 / 200,000 tại các học sinh trung học ở Minnesota (5). Trong số những nghiên cứu được đánh giá có các giao thức dịch tễ tốt hơn, các ước tính nằm trong khoảng 1 / 40.000 đến 1 / 80.000 (6). Những con số này so với nguy cơ chung về dân số là 1.0 đến 1.9 / 100.000 ở thanh thiếu niên và người lớn trẻ (7, 8). Hơn nữa, có vẻ như cả hai sự khác biệt giữa thể thao và giới tính trong mức độ nguy cơ, với nam giới có nguy cơ cao hơn nữ giới ở hầu hết các môn thể thao (7, 9), người da đen có nguy cơ cao hơn người da trắng, và các cầu thủ bóng rổ nam là nguy cơ cao nhất nhóm ở Hoa Kỳ, 1 / 5200 vận động viên-năm (4).
Một nghiên cứu gồm cả hai vận động viên cạnh tranh và giải trí cho thấy cả hai nhóm đều có nguy cơ cao hơn SCD so với dân số chung, với vận động viên giải trí có số lượng tích lũy cao hơn (7), SCD xảy ra ở lớn tuổi hơn và sự phân bố bệnh khác nhau. Dữ liệu về SCD sau khi tử vong ở các vận động viên cho thấy 25% đến 40% giải phẫu tử thi âm tính, cho thấy vai trò của rối loạn phân tử di truyền ở các nạn nhân này (4, 10, 11) và đối với các thành viên trong gia đình (12).
Một hạn chế khác của phân tích dữ liệu SCD ở vận động viên tập trung vào nguyên nhân không phải tim, một số trong đó có các biến cố giống tim. Các nguyên nhân không phải tim gồm rối loạn thần kinh cấp tính, các thuốc ma túy, cơn tấn công tim, tiêu cơ xương (rhabdomyolysis), rối loạn tế bào lưỡi liềm, tự sát và tai nạn (13, 14). Tuy nhiên, loạn nhịp ở vận động viên vẫn là nguyên nhân bệnh lý gây tử vong phổ biến nhất và nhiều trường hợp xảy ra như là biến cố tim đầu tiên.
Nguyên nhân cấu trúc phổ biến nhất của SCAs và SCDs trong các vận động viên ở Hoa Kỳ là bệnh cơ tim phì đại (HCM), tiếp theo là nguồn gốc bất thường của động mạch vành, với viêm cơ tim bổ xung một phần nhỏ hơn nhưng đáng kể (15). Ngoài ra, các chứng rối loạn di truyền khác cũng góp phần phân bố các nguyên nhân gây SCD ở vận động viên, nhiều người trong số đó có thể bị nghi ngờ hoặc xác định bằng tiền sử cẩn thận của gia đình và trước khi đánh giá ECG.
Nói chung, việc điều chỉnh rối loạn nhịp ở vận động viên tiếp theo là ở những người không phải vận động viên. Đối với các can thiệp, hiện nay thường có khuyến cáo sử dụngmáy khử rung ngoài tự động(AED)có khả năng huấn luyện và làm thuận lợi cho các vận động viên cạnh tranh (16), với những tuyên bố ít cụ thể hơn cho khả năng AED tại các tụ điểm về sự sẵn có của AED tại các địa điểm (ví dụ sân tennis) hoặc các tình huống (ví dụ như chạy bộ hoặc chạy nhóm nhỏ) ) trong đó vận động viên giải trí đang xảy ra.
Nhiều vận động viên đã có các thủ thuật sửa chữa (sửa chữa khiếm khuyết bẩm sinh hoặc phát triển như nguồn gốc bất thường của động mạch vành) (17, 18) đang được điều trị cho các rối loạn di truyền (19) hoặc đã cấy ICD (1) và có thể tham gia vận động viên tùy thuộc vào tính chất và mức độ nghiêm trọng của bệnh và với các biện pháp đề phòng và tư vấn thích hợp liên quan đến các nguy cơ tiềm ẩn cón lại (19, 20). Ví dụ, các vận động viên có các rối loạn mắc phải như viêm cơ tim được tư vấn chống lại gắng sức ít nhất 3 đến 6 tháng sau khi giải quyết bệnh.
Tài liệu tham khảo
1. Zipes DP, Link MS, Ackerman MJ, et al. Eligibility and disqualification recommendations for competitive athletes with cardiovascular abnormalities: Task Force 9: arrhythmias and conduction defects: a scientific statement from the American Heart Association and American College of Cardiology. Circulation. 2015;132:e315-25.
2. Biffi A, Pelliccia A, Verdile L, et al. Long-term clinical significance of frequent and complex ventricular tachyarrhythmias in trained athletes. J Am Coll Cardiol. 2002;40:446-52.
3. Verdile L, Maron BJ, Pelliccia A, et al. Clinical significance of exercise-induced ventricular tachyarrhythmias in trained athletes without cardiovascular abnormalities. Heart Rhythm. 2015;12:78-85.
4. Harmon KG, Asif IM, Maleszewski JJ, et al. Incidence, cause, and comparative frequency of sudden cardiac death in national collegiate athletic association athletes: a decade in review. Circulation. 2015;132:10-9.
5. Maron BJ, Haas TS, Ahluwalia A, et al. Incidence of cardiovascular sudden deaths in Minnesota high school athletes. Heart Rhythm. 2013;10:374-77.
6. Harmon KG, Drezner JA, Wilson MG, et al. Incidence of sudden cardiac death in athletes: a state-of-the-art review. Br J Sports Med. 2014;48:1185-92.
7. Marijon E, Tafflet M, Celermajer DS, et al. Sports-related sudden death in the general population. Circulation. 2011;124:672-81.
8. Meyer L, Stubbs B, Fahrenbruch C, et al. Incidence, causes, and survival trends from cardiovascular-related sudden cardiac arrest in children and young adults 0 to 35 years of age: a 30-year review. Circulation. 2012;126:1363-72.
9. Marijon E, Bougouin W, Perier MC, et al. Incidence of sports-related sudden death in France by specific sports and sex. JAMA. 2013;310:642-3.
10.Anderson JH, Tester DJ, Will ML, et al. Whole-exome molecular autopsy after exertion-related sudden unexplained death in the young. Circ Cardiovasc Genet. 2016;9:259-65.
11.Bagnall RD, Weintraub RG, Ingles J, et al. A prospective study of sudden cardiac death among children and young adults. N Engl J Med. 2016;374:2441-52.
12.Semsarian C, Ingles J, Wilde AA. Sudden cardiac death in the young: the molecular autopsy and a practical approach to surviving relatives. Eur Heart J. 2015;36:1290-6.
13.Maron BJ, Haas TS, Ahluwalia A, et al. Demographics and epidemiology of sudden deaths in young competitive athletes: from the United States national registry. Am J Med. 2016;129:1170-7.
14.Yankelson L, Sadeh B, Gershovitz L, et al. Life-threatening events during endurance sports: is heat stroke more prevalent than arrhythmic death? J Am Coll Cardiol. 2014;64:463-9.
15.Maron BJ, Haas TS, Murphy CJ, et al. Incidence and causes of sudden death in U.S. college athletes. J Am Coll Cardiol. 2014;63:1636-43.
16.Link MS, Myerburg RJ, Estes NA 3rd. Eligibility and disqualification recommendations for competitive athletes with cardiovascular abnormalities: Task Force 12: emergency action plans, resuscitation, cardiopulmonary resuscitation, and automated external defibrillators: a scientific statement from the American Heart Association and American College of Cardiology. Circulation. 2015;132:e334-8.
17.Brothers JA, Frommelt MA, Jaquiss RDB, et al. Expert consensus guideline: anomalous aortic origin of a coronary artery – American Association for Thoracic Surgery Clinical Practice Guidelines. J Thorac Cardiovasc Surg. 2017;153:1440-57.
18.Van Hare GF, Ackerman MJ, Evangelista JA, et al. Eligibility and disqualification recommendations for competitive athletes with cardiovascular abnormalities: Task Force 4: congenital heart disease: a scientific statement from the American Heart Association and American College of Cardiology. Circulation. 2015;132:e281-91.
19.Ackerman MJ, Zipes DP, Kovacs RJ, et al. Eligibility and disqualification recommendations for competitive athletes with cardiovascular abnormalities: Task Force 10: the cardiac channelopathies: a scientific statement from the American Heart Association and American College of Cardiology. Circulation. 2015;132:e326-9.
20.Maron BJ, Udelson JE, Bonow RO, et al. Eligibility and disqualification recommendations for competitive athletes with cardiovascular abnormalities: Task Force 3: Hypertrophic cardiomyopathy, arrhythmogenic right ventricular cardiomyopathy and other cardiomyopathies, and myocarditis: a scientific statement from the American Heart Association and American College of Cardiology. Circulation. 2015;132:e273-80.
10.2. Thai nghén
|
Các khuyến cáo cho thai nghén Tài liệu tham khảo hỗ trợ các khuyến cáo được tóm tắt trong phần Tư liệu Hỗ trợ online 51. |
||
|
COR |
LOE |
Các khuyến cáo |
|
I |
B-NR |
1. Ở những bà mẹ có hội chứng QT kéo dài, beta blocker nên được tiếp tục trong thái nghén và suốt giai đoạn sau sinh, kể cả ở phụ nữ đang cho con bú sữa mẹ (1). |
|
I |
C-EO |
2. Ở bệnh nhân thai nghén có VA dai dẳng, chuyển nhịp bằng điện là an toàn và hiệu quả và nên được sử dụng với cấu hình điện tim mạch là an toàn và hiệu quả và nên được sử dụng với cấu hình điện cực tiêu chuẩn (2, 3). |
|
IIa |
B-NR |
3. Ở những bệnh nhân thai nghén cần ICD hoặc triệt phá VT, hợp lý để thực hiện các thủ thuật này trong suốt quá trình thai nghén, tốt nhất là sau tam ca đầu tiên (4, 5). |
Văn bản Hỗ trợ Riêng biệt – Khuyến cáo
1. Phụ nữ có hội chứng QT dài nên được tư vấn về nguy cơ cho mẹ và thai nhi trước khi mang thai để đảm bảo liệu pháp điều trị beta-blocker đang tiếp tục. Nguy cơ SCA hoặc SCD cao hơn đáng kể trong 9 tháng sau sinh, đặc biệt là ở phụ nữ có LQT2 (1, 6, 7). Một phân tích hồi cứu lớn từ đăng ký hội chứng QT kéo dài đã chứng minh tỉ số chênh 40,8 đối với ngất, SCA, hoặc SCD trong số phụ nữ có hội chứng QT kéo dài trong 9 tháng sau sinh; điều trị với beta blockers trong thời kỳ mang thai liên quan một cách độc lập với nguy cơ được giảm xuống (7). Các biến cố loạn nhịp toàn bộ trong quá trình mang thai không tăng lên trong số các phụ nữ nhận được điều trị ức chế beta blockers (1, 6, 7). Trong một nghiên cứu trường hợp đối chứng, các phụ nữ có LQT1 không nhận được beta blockers trong thai kỳ, đặc biệt là những người bị ngất trước đó, đã ở trong nguy cơ SCA hoặc ngất tăng lên một cách có ý nghĩa (8). Tần suất các biến cố đã trở lại với mức độ trước mang thai sau 9 tháng (1). Việc sử dụng beta blockers trong quá trình mang thai được kết hợp với cân nặng trẻ sơ sinh giảm xuống và hạ đường máu (9), nhưng không gây tăng nguy cơ sảy thai (8, 10). Nhịp chậm ở thai nhi có liên quan đến hội chứng QT dài ở thai nhi và có thể không hội tụ để ngừng điều trị beta blockers một cách độc lập (11-14); những trẻ sơ sinh này có nguy cơ tử vong cao hơn và cần được theo dõi và điều trịcẩn thận ởtrẻ sơ sinh (13). Vì 50% trẻ con có thể bị ảnh hưởng do hội chứng QT kéo dài, với nguy cơ các biến cố có hại cao nhất ở trẻ sơ sinh và trẻ nhỏ, tầm soát trẻ sơ sinh khi sinh và khi trẻ sơ sinh bị hội chứng QT dài là rất quan trọng (8).
2. Dữ liệu sẵn có trên các điện trường liên quan đến các bản AED được áp dụng đúng cách cho thấy bào thai là an toàn; không có dữ liệu quan sát có sẵn ngược lại. Vị trí đặt máy khử rung trước bên được ưa thích hơn với tấm đệm bên / bản đặt dưới tổ chức vú, điều này xem xét quan trọng ở bệnh nhân thai nghén.
3. ICD ở phụ nữ mang thai là an toàn và hiệu quả (4). Trong trường hợp hiếm có ở phụ nữ mang thai có chỉ định ICD ngay lập tức, hoặc các chỉ định ít hơn để triệt phá VT trong quá trình thai nghén, nguy cơ phóng xạ đối với thai nhi là tối thiểu (5, 15). Thủ thuật này thường được thực hiện sau tam ca đầu tiên trừ khi có những trường hợp yêu cầu một thủ thuật sớm hơn. Các áo khử rung tim đã được sử dụng trong bệnh cơ tim chu sinh trong khi chờ đợi đánh giá lại sự hồi phục chức năng thất (16). Máy khử rung tim dưới da là một thay thế tiềm năng cho ICD thông thường, mặc dù dữ liệu không có sẵn để hỗ trợ cho một khuyến cáo.
Tài liệu tham khảo
1. Seth R, Moss AJ, McNitt S, et al. Long QT syndrome and pregnancy. J Am Coll Cardiol. 2007;49:1092-8.
2. Jeejeebhoy FM, Zelop CM, Lipman S, et al. Cardiac arrest in pregnancy: a scientific statement from the American Heart Association. Circulation. 2015;132:1747-73.
3. Vanden Hoek TL, Morrison LJ, Shuster M, et al. Part 12: cardiac arrest in special situations: 2010 American Heart Association guidelines for cardiopulmonary resuscitation and emergency cardiovascular care. Circulation. 2010;122(suppl 3):S829-61.
4. Natale A, Davidson T, Geiger MJ, et al. Implantable cardioverter-defibrillators and pregnancy: a safe combination? Circulation. 1997;96:2808-12.
5. Colletti PM, Lee KH, Elkayam U. Cardiovascular imaging of the pregnant patient. Am J Roentgenol. 2013;200:515-21.
6. Khositseth A, Tester DJ, Will ML, et al. Identification of a common genetic substrate underlying postpartum cardiac events in congenital long QT syndrome. Heart Rhythm. 2004;1:60-4.
7. Rashba EJ, Zareba W, Moss AJ, et al. Influence of pregnancy on the risk for cardiac events in patients with hereditary long QT syndrome. LQTS Investigators. Circulation. 1998;97:451-6.
8. Heradien MJ, Goosen A, Crotti L, et al. Does pregnancy increase cardiac risk for LQT1 patients with the KCNQ1-A341V mutation? J Am Coll Cardiol. 2006;48:1410-5.
9. Davis RL, Eastman D, McPhillips H, et al. Risks of congenital malformations and perinatal events among infants exposed to calcium channel and beta-blockers during pregnancy. Pharmacoepidemiol Drug Saf. 2011;20:138-45.
10.Ruys TP, Maggioni A, Johnson MR, et al. Cardiac medication during pregnancy, data from the ROPAC. Int J Cardiol. 2014;177:124-8.
11.Beinder E, Grancay T, Menendez T, et al. Fetal sinus bradycardia and the long QT syndrome. Am J Obstet Gynecol. 2001;185:743-7.
12.Hofbeck M, Ulmer H, Beinder E, et al. Prenatal findings in patients with prolonged QT interval in the neonatal period. Heart. 1997;77:198-204.
13.Cuneo BF, Etheridge SP, Horigome H, et al. Arrhythmia phenotype during fetal life suggests long-QT syndrome genotype: risk stratification of perinatal long-QT syndrome. Circ Arrhythm Electrophysiol. 2013;6:946-51.
14.Cuneo BF, Strasburger JF, Wakai RT. The natural history of fetal long QT syndrome. J Electrocardiol. 2016;49:807-13.
15.Damilakis J, Theocharopoulos N, Perisinakis K, et al. Conceptus radiation dose and risk from cardiac catheter ablation procedures. Circulation. 2001;104:893-7.
16.Duncker D, Haghikia A, Konig T, et al. Risk for ventricular fibrillation in peripartum cardiomyopathy with severely reduced left ventricular function-value of the wearable cardioverter/defibrillator. Eur J Heart Fail. 2014;16:1331-6.
10.3. Các bệnh nhân lớn tuổi với các bệnh đi kèm
|
Khuyến cáo cho các bệnh nhân lớn tuổi với các bệnh đi kèm Xem Báo cáo nhắc lại hệ thống (1). |
||
|
COR |
LOE |
Khuyến cáo |
|
IIa |
B-NRSR |
1. Đối với bệnh nhân lớn tuổi và những bệnh nhân có các bệnh đi kèm có ý nghĩa, người có chỉ định cho ICD ngăn ngừa tiên phát, ICD là phù hợp nếu sống sót có ý nghĩa > 1 năm được dự kiến (1). |
SR chỉ nhắc lại hệ thống.
Tóm tắt
Tham khảo phần “Tổng kết hệ thống cho Hướng dẫn của ACC / AHA / HRS 2017 về Điều chỉnh các Bệnh nhân Rối loạn nhịp Thất và Ngăn ngừa Đột tử Tim cho bằng chứng hệ thống đầy đủ nhắc lại đối với tư liệu bổ xung và phân tích (1). Các kết quả từ câu hỏi “Tác động của cấy ICD đối với dự phòng tiên phát ở các bệnh nhân lớn tuổi và các bệnh nhân có nhiều bệnh kèm theo có ý nghĩa là gì ? (Phần 2) “và sự xem xét tổng thể của ủy ban soạn thảo đã được sử dụng để làm khung quyết định của chúng ta. Khuyến cáo dựa trên cơ sở bằng chứng bao gồm tổng quan hệ thống được thực hiện bằng ERC và được đánh giá bằng SR trên địa chỉ (ví dụ LOE: B-RSR). Các bệnh kèm theo bao gồm sự kết hợp của bệnh thận, bệnh phổi tắc nghẽn mãn tính, rung nhĩ và bệnh tim.
Văn bản Hỗ trợ Riêng biệt – Khuyến cáo
1. Tuổi được xác định khi ≥75 tuổi.
Các phân tích của ERC rất hữu ích trong việc chứng minh rõ ràng không phải tuổi cũng không phải các bệnh kèm theo đơn thuần có thể là loại trừ ICD. Tuy nhiên, dữ liệu đưa vào phân tích còn hạn chế. Thứ nhất, hầu hết các dữ liệu từ các nghiên cứu không ngẫu nhiên và “cả hai lựa chọn và sự không rõ ràng lẫn lộn không thể được điều chỉnh hoàn toàn.”Có thể các bệnh nhân yếu hơn đã không được cung cấp ICDs và do đó không được đưa vào. Thứ hai, do hầu hết các nghiên cứu không phải là ngẫu nhiên, những phát hiện này chỉ biểu hiện mối quan hệ chứ không phải là mối quan hệ nhân quả.
Ngoài ra, người cao tuổi có tỷ lệ biến chứng cao hơn, tuổi thọ ngắn hơn (và do đó ít năm hơn trong thời gian họ có thể thu được lợi ích từ ICD) và sở thích khác nhau (2). Vì những lý do này, điều quan trọng là cần áp dụng phương pháp tiếp cận đặc biệt và mang tính nhân đạo cao để điều trị những bệnh nhân này.
Tài liệu tham khảo
1. Kusumoto FM, Bailey KR, Chaouki AS, et al. Systematic review for the 2017 AHA/ACC/HRS guideline for management of patients with ventricular arrhythmias and the prevention of sudden cardiac death: a report of the American College of Cardiology/American Heart Association Task Force on Clinical Practice Guidelines and the Heart Rhythm Society [published online ahead of print October 30, 2017]. Circulation. doi: 10.1161/CIR.0000000000000550.
2. American Geriatrics Society Expert Panel on the Care of Older Adults with M. Guiding principles for the care of older adults with multimorbidity: an approach for clinicians. J Am Geriatr Soc. 2012;60:E1-25.
10.4. Bệnh thận mạn
Các bệnh nhân bệnh thận mạn tính (CKD) có nguy cơ cao bị SCD so với quần thể dân số nói chung, nhưng nguy cơ so với lợi ích của ICDs dự phòng tiên phát vẫn còn chưa rõ ràng; dữ liệu từ các nghiên cứu quan sát đã mâu thuẫn nhau, cũng như bệnh nhân suy thận trung bình hoặc nặng, đặc biệt những bệnh nhân có bệnh thận giai đoạn cuối (ESRD) chạy thận không được đưa vào các nghiên cứu ngẫu nhiên ICD quan trọng (1-5). Hơn nữa, dữ liệu trước đây có những hạn chế đáng kể cho thấy bệnh nhân nhận ICDs được so sánh không đều với nhóm chứng có CKD không nhận được ICDs dự phòng tiên phát và mức độ suy thận có thể ảnh hưởng đến lợi ích sống còn (6). Các bệnh nhân bị CKD, đặc biệt là ESRD chạy thận, dường như có nguy cơ gia tăng các biến chứng do ICD. Một số lượng đáng kể các ca tử vong đột ngột không có liên quan với VA trong nhóm này (7). Do đó, ERC đã được yêu cầu giải quyết tác động của ICDs đối với tử vong ở bệnh nhân CKD.
ERC tiến hành một phân tích cụ thể của 5 nghiên cứu khám phá rối loạn chức năng thận. Phân tích gộp các nghiên cứu này gợi ý có sự kết hợp giữa cấy ICD và sự sống sót được cải thiện (8). Một giới hạn quan trọng chỉ có 2 nghiên cứu nghiên cứu một cách đặc biệt bệnh nhân với ESRD và hầu hết các dữ liệu được phân tích là từ các nghiên cứu quan sát (8, 9). Vì những hạn chế này, ủy ban biên soạn đã kết luận không có đủ dữ liệu để thông báo cho một khuyến cáo cấy ICD ở bệnh nhân ESRD chạy thận. Các quyết định liên quan đến ICDs ở bệnh nhân CKD, đặc biệt những bệnh nhân ESRD nên được cá thể hoá và xem xét tình trạng chức năng của bệnh nhân, số các bệnh đi kèm và sở thích của bệnh nhân, trong số các yếu tố khác.
Tài liệu tham khảo
1. Bardy GH, Lee KL, Mark DB, et al. Amiodarone or an implantable cardioverter-defibrillator for congestive heart failure. N Engl J Med. 2005;352:225-37.
2. Buxton AE, Lee KL, Fisher JD, et al. A randomized study of the prevention of sudden death in patients with coronary artery disease. Multicenter Unsustained Tachycardia Trial Investigators. N Engl J Med. 1999;341:1882-90.
3. Moss AJ, Hall WJ, Cannom DS, et al. Improved survival with an implanted defibrillator in patients with coronary disease at high risk for ventricular arrhythmia. Multicenter Automatic Defibrillator Implantation Trial Investigators. N Engl J Med. 1996;335:1933-40.
4. Moss AJ, Zareba W, Hall WJ, et al. Prophylactic implantation of a defibrillator in patients with myocardial infarction and reduced ejection fraction. N Engl J Med. 2002;346:877-83.
5. Pun PH, Al-Khatib SM, Han JY, et al. Implantable cardioverter-defibrillators for primary prevention of sudden cardiac death in CKD: a meta-analysis of patient-level data from 3 randomized trials. Am J Kidney Dis. 2014;64:32-9.
6. Charytan DM, Patrick AR, Liu J, et al. Trends in the use and outcomes of implantable cardioverter-defibrillators in patients undergoing dialysis in the United States. Am J Kidney Dis. 2011;58:409-17.
7. Wong MC, Kalman JM, Pedagogos E, et al. Bradycardia and asystole is the predominant mechanism of sudden cardiac death in patients with chronic kidney disease. J Am Coll Cardiol. 2015;65:1263-5.
8. Kusumoto FM, Bailey KR, Chaouki AS, et al. Systematic review for the 2017 AHA/ACC/HRS guideline for management of patients with ventricular arrhythmias and the prevention of sudden cardiac death: a report of the American College of Cardiology/American Heart Association Task Force on Clinical Practice Guidelines and the Heart Rhythm Society [published online ahead of print October 30, 2017]. Circulation. doi: 10.1161/CIR.0000000000000550.
9. Pun PH, Hellkamp AS, Sanders GD, et al. Primary prevention implantable cardioverter defibrillators in end-stage kidney disease patients on dialysis: a matched cohort study. Nephrol Dial Transplant. 2015;30:829-35.
10.5. Bệnh van tim
Bệnh nhân bệnh van tim cần được đánh giá và điều trị theo GDMT cho bệnh van tim, và khi LVEF suy giảm, GDMT áp dụng cho NICM để giảm nguy cơ SCD (23). VA ở bệnh nhân có bệnh van tim có thể do bất kỳ cơ chế nào chịu trách nhiệm cho VA trong các bệnh tim khác gồm bệnh thiếu máu cục bộ, MI, phì đại LV nặng, các rối loạn nhịp phụ thuộc adrenergic, hoặc bất thường phân tử di truyền. Bệnh nhân bị bệnh van tim và VA thường được đánh giá và điều trị bằng các khuyến cáo hiện thời cho mỗi rối loạn (1). Sự hiện diện của VA đơn thuần không thiết lập được chỉ định cho sửa chữa hoặc thay thế van. Nhìn chung, có nhiều hiểu biết hơn về nguy cơ SCD ở các bệnh nhân có hẹp chủ so với tổn thương van khác có nguy cơ từ 1% đến 1,5% mỗi năm (2). Hầu hết các bệnh nhân đột tử đều đã có triệu chứng do bệnh van tim của họ (3, 4). Mặc dù NSV tái phát có thể đặt bệnh nhân bị hẹp động mạch chủ nghiêm trọng có nguy cơ bị ngất, nhưng việc điều chỉnh bệnh nhân như vậy được hướng dẫn bằng sự nghiêm trọng của tổn thương van.
Sa van hai lá là nguyên nhân gây SCD, mặc dù nghiên cứu 18.786 bệnh nhân không thấy tăng nguy cơ SCA đối với bệnh nhân bị sa 2 lá van hai lá so với trường hợp sa một lá van 2 lá đơn thuần hoặc không sa van 2 lá (5). Sự xơ hóa LV ở các cơ nhú đã được mô tả ở một số bệnh nhân sa van 2 lá có VA hoặc SCD (6). Hơn nữa, một hội chứng có thể xảy ra SCD đã được mô tả gồm sa 2 lá van van 2 lá, giới nữ, bất thường sóng T, và ngoại vị phức hợp thất (7). Hướng dẫn điều trị bệnh nhân với NICM, dù bệnh lý van hay nguồn gốc khác, được cung cấp trong hướng dẫn hiện thời (xem Phần 7.2.1 và 7.2.2 về phòng ngừa tiên phát và thứ phát).
10.6. Các sự khác biệt liên quan đến giới tính trong nguy cơ SCD
Thông tin về mối quan hệ giữa giới tính và VA cũng như SCD phần lớn chỉ hạn chế ở các nghiên cứu về dịch tễ học, đoàn hệ và quan sát. Các nghiên cứu về dân số khác nhau, chủ yếu tập trung vào SCD do bệnhtimthiếu máu cục bộ, đã chứng minh sự chênh lệch về tuổi trong nguy cơ SCD trong số nam và nữ (8-10). Những yếu tố này gồm trễ 10 năm trong tỷ lệ SCD ở phụ nữ so với nam giới. Tuy nhiên, gánh nặng các yếu tố nguy cơ ở phụ nữ có cùng hiệu quả như ở nam giới, với nguy cơ tăng 17 lần từ mức thấp nhất đến cao nhất (9). Điều quan trọng là 69% SCD ở phụ nữ là các biến cố tim đầu tiên (8). Nghiên cứu nguy cơ SCD trong giai đoạn 45, 55, 65 và 75 tuổi được xác định thấp hơn thường xuyên và tỉ lệ nguy cơ SCD trong suốt thời gian sống của phụ nữ so với nam giới ở mỗi giai đoạn (10). Sự khác biệt giữa phụ nữ và nam giới có phần nhỏ hơn ở độ tuổi dưới và trên 75 năm, chủ yếu là do giảm nguy cơ ở nam giới. Nguy cơ chung của SCD là 1 trong 9 nam giới và 1 trong 30 phụ nữ (10).
Trong các nghiên cứu về kết cục sau ngừng tim ngoài bệnh viện, phụ nữ lớn tuổi, có SCA ở nhà nhiều hơn, và nhịp có thểđánhsốc (VT/VF) ít hơn nam giới (11, 12). Điều này có liên quan đến khả năng sống sót thấp hơn chút ít; tuy nhiên, phụ nữ có VT / VF và những người có hoạt động điện vô mạch có kết cục tốt hơn so với nam giới (12). Một phân tích hồi cứu ngừng tim ngoài bệnh viện cho thấy tỷ lệ sống sót được cải thiện trong khoảng thời gian 10 năm qua, với kết quả tốt hơn ở nam giới cũng như phụ nữ trẻ hơn (13). Hai nghiên cứu cho thấy những kết cục tốt hơn ở phụ nữ có VT / VF, mặc dù trắc diện yếu tố nguy cơ bất lợi ở nữ giới (14, 15). Một nghiên cứu lớn khác cho thấy mặc dù có sự hồi phục của tuần hoàn tự phát trước nhập viện và sống sót để ra viên, phụ nữ trẻ hơn có tỷ lệ sống sót sau khi xuất viện giống nhau, những phụ nữ trẻ hơn có tỷ lệ sống sót thần kinh nguyên vẹn 1 tháng thấp hơn so với nhóm tuổi từ 50 đến 60 tuổi (16). Một phân tích hồi cứu 17 năm không cho thấy bất kỳ sự khác biệt nào giữa nam giới và nữ giới, mặc dù kết cục toàn bộ được cải thiện (17).
Tỷ lệ bệnh tim thiếu máu cục bộ kết hợp với SCA trong số những phụ nữ sống sót do ngừng tim ngoài bệnh viện thấp hơn đáng kể so với nam giới, nhưng bệnh tim thiếu máu cục bộ vẫn là yếu tố tiên đoán mạnh nhất về nguyên nhân (18) và phụ nữ cũng có khả năng ít hơn đáng kể có rối loạn chức năng LV nặng (LVEF ≤35%) hoặc bệnh tim thiếu máu cục bộ đã được ghi nhận trước đó (19). Phụ nữ dường như ít có cơ hội hưởng lợi từ việc giảm thân nhiệt trị liệu sau ngừng tim; tuy nhiên, ở nhóm trẻ tuổi hơn, hồi phục thần kinh ở phụ nữ tốt hơn so với phụ nữ lớn tuổi hơn (20). Phụ nữ ít có khả năng SCA trong các biến cố vận động viên cạnh tranh. Một nghiên cứu lớn bao gồm cả vận động viên giải trí và thi đấu qua phạm vi tuổi lớn cho thấy SCA ở phụ nữ trong các biến cố 1 trong 20 so với nam giới (21).
Một nghiên cứu tư liệu lớn từ năm 1980 đến năm 1992 đã chứng minh phụ nữ chiếm 70% số trường hợp rối loạn nhịp tim liên quan đến thuốc tim mạch (22). Điều này phù hợp với sự khác biệt khoảng QT giữa nam và nữ. Một phân tích hồi cứu về ngưng quinidin cho thấy có sự khác biệt đáng kể trong việc ngưng dùng thuốc giữa nam giới và phụ nữ (66% so với 84%) chủ yếu là do kéo dài QT (23). Một nghiên cứu về triệt phá qua catheter cho VT đã cho thấy kết cục toàn bộ là giống nhau giữa nam và nữ (24). Sự khác biệt giới tính duy nhất là xác suất cao hơn của phụ nữ có RVOT VT (VT đường thoát thất phải) và xác suất cao hơn nam giới có LVOT VT (VT đường thoát thất trái).
Tài liệu tham khảo
1. Nishimura RA, Otto CM, Bonow RO, et al. 2014 AHA/ACC guideline for the management of patients with valvular heart disease: a report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines. Circulation. 2014;129:e521-643.
2. Genereux P, Stone GW, O’Gara PT, et al. Natural history, diagnostic approaches, and therapeutic strategies for patients with asymptomatic severe aortic stenosis. J Am Coll Cardiol. 2016;67:2263-88.
3. Avierinos JF, Gersh BJ, Melton LJ 3rd, et al. Natural history of asymptomatic mitral valve prolapse in the community. Circulation. 2002;106:1355-61.
4. Grigioni F, Enriquez-Sarano M, Ling LH, et al. Sudden death in mitral regurgitation due to flail leaflet. J Am Coll Cardiol. 1999;34:2078-85.
5. Nordhues BD, Siontis KC, Scott CG, et al. Bileaflet mitral valve prolapse and risk of ventricular dysrhythmias and death. J Cardiovasc Electrophysiol. 2016;27:463-8.
6. Basso C, Perazzolo MM, Rizzo S, et al. Arrhythmic mitral valve prolapse and sudden cardiac death. Circulation. 2015;132:556-66.
7. Sriram CS, Syed FF, Ferguson ME, et al. Malignant bileaflet mitral valve prolapse syndrome in patients with otherwise idiopathic out-of-hospital cardiac arrest. J Am Coll Cardiol. 2013;62:222-30.
8. Albert CM, Chae CU, Grodstein F, et al. Prospective study of sudden cardiac death among women in the United States. Circulation. 2003;107:2096-101.
9. Kannel WB, Wilson PW, D’Agostino RB, et al. Sudden coronary death in women. Am Heart J. 1998;136:205-12.
10.Bogle BM, Ning H, Mehrotra S, et al. Lifetime risk for sudden cardiac death in the community. J Am Heart Assoc. 2016;5:e002398.
11.Kim C, Fahrenbruch CE, Cobb LA, et al. Out-of-hospital cardiac arrest in men and women. Circulation. 2001;104:2699-703.
12.Teodorescu C, Reinier K, Uy-Evanado A, et al. Survival advantage from ventricular fibrillation and pulseless electrical activity in women compared to men: the Oregon Sudden Unexpected Death Study. J Interv Card Electrophysiol. 2012;34:219-25.
13.Wissenberg M, Hansen CM, Folke F, et al. Survival after out-of-hospital cardiac arrest in relation to sex: a nationwide registry-based study. Resuscitation. 2014;85:1212-8.
14.Bray JE, Stub D, Bernard S, et al. Exploring gender differences and the “oestrogen effect” in an Australian out-of-hospital cardiac arrest population. Resuscitation. 2013;84:957-63.
15.Ng YY, Wah W, Liu N, et al. Associations between gender and cardiac arrest outcomes in Pan-Asian out-of-hospital cardiac arrest patients. Resuscitation. 2016;102:116-21.
16.Hagihara A, Onozuka D, Hasegawa M, et al. Resuscitation outcomes of reproductive-age females who experienced out-of-hospital cardiac arrest. Eur Heart J Acute Cardiovasc Care. 2017;6:121-9.
17.Safdar B, Stolz U, Stiell IG, et al. Differential survival for men and women from out-of-hospital cardiac arrest varies by age: results from the OPALS study. Acad Emerg Med. 2014;21:1503-11.
18.Albert CM, McGovern BA, Newell JB, et al. Sex differences in cardiac arrest survivors. Circulation. 1996;93:1170-6.
19.Chugh SS, Uy-Evanado A, Teodorescu C, et al. Women have a lower prevalence of structural heart disease as a precursor to sudden cardiac arrest: The Ore-SUDS (Oregon Sudden Unexpected Death Study). J Am Coll Cardiol. 2009;54:2006-11.
20.Kim MJ, Shin SD, McClellan WM, et al. Neurological prognostication by gender in out-of-hospital cardiac arrest patients receiving hypothermia treatment. Resuscitation. 2014;85:1732-8.
21.Marijon E, Bougouin W, Perier MC, et al. Incidence of sports-related sudden death in France by specific sports and sex. JAMA. 2013;310:642-3.
22.Makkar RR, Fromm BS, Steinman RT, et al. Female gender as a risk factor for torsades de pointes associated with cardiovascular drugs. JAMA. 1993;270:2590-7.
23.Higgins AY, Waks JWJosephson ME. Influence of gender on the tolerability, safety, and efficacy of quinidine used for treatment of supraventricular and ventricular arrhythmias. Am J Cardiol. 2015;116:1845-51.
24.Tanaka Y, Tada H, Ito S, et al. Gender and age differences in candidates for radiofrequency catheter ablation of idiopathic ventricular arrhythmias. Circ J. 2011;75:1585-91.
10.7. Các rối loạn nhịp được tạo ra do thuốc
|
Các khuyến cáo cho các rối loạn nhịp được tạo ra do thuốc Tài liệu tham khảo ủng hộ các khuyến cáo được tóm tắt trong Tư liệu hỗ trợ online 52 – 53. |
||
|
Digoxin |
||
|
COR |
LOE |
Khuyến cáo |
|
I |
B-NR |
1. Việc sử dụng các kháng thể digoxin được khuyến cáo cho những bệnh nhân có VA dai dẳng khả năng do nhiễm độc digoxin (1, 2). |
|
Torsades de pointes và kéo dài QT được tạo ra do thuốc |
||
|
COR |
LOE |
Các khuyến cáo |
|
I |
B-NR |
2. Ở các bệnh nhân có torsades de pointes tái phát kết hợp với kéo dài QT mắc phải và nhịp chậm không thể ngăn chặn được bằng sử dụng magiê tĩnh mạch, tăng nhịp tim bằng tạo nhịp nhĩ hoặc thất hoặc isoproterenol được khuyến cáo để ngăn chặn rối loạn nhịp (3). |
|
I |
C-LD |
3. Đối với các bệnh nhân có kéo dài QT do dùng thuốc, hạ kali máu, hạ magiê máu, hoặc các yếu tố mắc phải khác và torsades de pointes tái phát, sử dụng magiê sulfate tiêm tĩnh mạch để ngăn chặn rối loạn nhịp được khuyến cáo (4, 5). |
|
I |
C-LD |
4. Đối với bệnh nhân có torsades de pointes liên quan đến việc kéo dài QT mắc phải, bù kali đạt đến 4,0 mmol / L hoặc cao hơn và bù magiê đến giá trị bình thường (ví dụ: ≥2 mmol / L) có lợi ích (6, 7). |
|
Blocker kênh natri – Nhiễm độc liên quan |
||
|
COR |
LOE |
Các khuyến cáo |
|
IIa |
C-LD |
5. Ở các bệnh nhân dùng thuốc chẹn kênh natri có biểu hiện ngưỡng tạo nhịp và khử rung tăng lên, ngừng dùng thuốc được giả định có khả năng hoặc lập trình lại thiết bị có thể hữu ích để khôi phục điều trị thiết bị có hiệu quả (8, 9). |
|
III: Harm |
B-NR |
6. Ở những bệnh nhân có hội chứng QT kéo dài mắc phải hoặc bẩm sinh, các thuốc kéo dài QT có thể gây hại (10). |
Văn bản Hỗ trợ Riêng biệt – Khuyến cáo
1. Các rối loạn nhịp điển hình liên quan đến độc tính digoxin gồm tăng tính tự động của tâm nhĩ, bộ nối, hoặc tâm thất (với các nhắt bóp ngoại vị hoặc nhịp tim nhanh) thường kết hợp với blốc nhĩ thất (11). VT nhánh bó hoặc hai chiều về nguồn gốc được gợi ý độc tính digoxin (12). Quá liều digoxin nghiêm trọng làm tăng kali máu và ngừng tim. Chẩn đoán được xác định bằng sự kết hợp của rối loạn nhịp đặc trưng, triệu chứng phụ thuộc (rối loạn thị giác, buồn nôn, thay đổi hành vi) và nồng độ trong huyết thanh tăng lên. Các yếu tố tiềm ẩn có thể gồm suy giáp (hypothyroidism), hạ kali máu, hoặc rối loạn chức năng thận (12). Điều trị độc tính digoxin dựa trên mức độ nghiêm trọng. Trong những trường hợp nhẹ, ngưng dùng thuốc, theo dõi nhịp và duy trì kali huyết thanh bình thường có thể là đủ (11). Magnesium tiêm tĩnh mạch thường được dùng khi có sự hiện diện của VA (12). Đôi khi, tạo nhịp tim tạm thời có thể cần thiết cho blốc nhĩ thất hoặc vô tâm thu (13). Đối với nhiễm độc nghiêm trọng hơn (nồng độ digoxin huyết thanh vượt quá 4ng / ml và loạn nhịp nghiêm trọng như VT), điều trị được lựa chọn là kháng thể Fab đặc hiệu cho digoxin. Trong một loạt 150 bệnh nhân bị nhiễm độc nặng, đáp ứng nhanh (30 phút đến 4 giờ), và 54% bệnh nhân có ngừng tim đã sống sót sau khi nhập viện (1). Tác dụng ngoại ý bao gồm sự gia tăng của bệnh tiềm ẩn (tăng nhịp thất trong AF, làm trầm trọng thêm HF) và hạ kali máu. Liều thấp hơn (và ít tốn kém hơn) so với liều trung hòa đầy đủ là đủ miễn là ngừng tim không phải sắp xảy ra (2). Giám sát nồng độ digoxin không đáng tin cậy sau khi dùng kháng thể antidigoxin.
2. Theo dõi bệnh nhân có nguy cơ cao trong thời gian bắt đầu các thuốc chống loạn nhịp kéo dài QT và ghi nhận hội chứng khi nó xảy ra là bước đầu tiên. Tạo nhịp tạm thời có hiệu quả cao trong việc điều chỉnh torsades de pointes tái phát sau khi bổ sung kali và magiê (3). Isoproterenol cũng có thể được sử dụng để làm tăng nhịp tim và loại bỏ các các khoảng ngừng sau ngoại vị (3).
3. Magiê tiêm tĩnh mạch có thể ngăn chặn các đợtxoắn đỉnh(torsades de pointes)mà không nhất thiết làm QT ngắn lại, ngay cả khi magiê huyết thanh bình thường (4, 5). Liều lặp lại có thể là cần thiết, tăng liều để ngăn chặn các đợt ngoại vị và các cơn VT tạm thời trong khi các yếu tố thúc đẩy đã được sửa chữa (4). Độc tính magnesium (tiến triển dẫn đến ức chế hô hấp) có thể xảy ra ở nồng độ huyết thanh cao, nhưng nguy cơ này rất nhỏ so với liều thường dùng để điều trị torsades de pointes, từ 1 đến 2 g tiêm tĩnh mạch (14).
Các biến thể allen trong các gen bệnh QT dài về lâm sàng đã được xác định ở những bệnh nhân bị torsades de pointes (7, 15-18) do thuốc gây ra. Hơn nữa, toàn bộ quá trình sắp xếp xuất hiện gây ra một gánh nặng gia tăng các biến thể kênh kali hiếm gặp trong nguy cơ torsades de pointes gây ra do thuốc (17, 19). Những phát hiện này vẫn chưa hỗ trợ sàng lọc di truyền tổng quát để dự đoán torsades de pointes do thuốc gây ra. Trong hội chứng QT dài, xét nghiệm di truyền có thể được thực hiện trong trường hợp chỉ số có cảm giác torsades de pointes do thuốc gây ra, và nếu họ không sống sót trong sự kiện đó thì có thể thực hiện sàng lọc điện tâm đồ của người thân thế hệ thứ nhất.
4. Duy trì kali huyết thanh giữa 4,5 mEq / L và 5 mEq / L làm ngắn QT và có thể làm giảm nguy cơ torsades de pointes tái phát (6, 7).
5. Trong các thử nghiệm lâm sàng lớn, thuốc chẹn kênh natri làm tăng tỷ lệ tử vong ở bệnh nhân hồi phục từ MI (20), nhưng những xu hướng tương tự cũng được thấy với các thử nghiệm trước đó của mexiletine (21) và disopyramide (22). Dựa trên CAST, flecainide chống chỉ định ở những bệnh nhân thiếu máu cục bộ, MI trước đó và tránh dùng cho bệnh nhân có bệnh tim cấu trúc khác (20).
Chẹn kênh natri làm tăng đòi hỏi về năng lượng khử rung và ngưỡng ngưỡng tạo nhịp (8, 9); kết quả là bệnh nhân có thể yêu cầu lập trình lại hoặc điều chỉnh các hệ thống định kỳ hoặc ICD hoặc thay đổi phác đồ thuốc của họ (mặc dù các hệ thống định kỳ hiện đại cung cấp việc kiểm tra ngưỡng tự động và điều chỉnh dòng ra của tạo nhịp đã giảm nguy cơ mất dẫn nhịp). Các chất chẹn kênh natri có thể “chuyển” AF sang cuồng nhĩ chậm, có thể nhìn thầy dẫn truyền nhĩ thất 1:1 với các phức hợp QRS rộng có thể nhầm với VT (23).
Các thuốc chẹn kênh natri, như procainamide và flecainide, đôi khi có thể thúc đẩy ECG hội chứng Brugada điển hình (24, 25). Điều này đã được báo cáo không chỉ với thuốc chống loạn nhịp tim mà còn với thuốc chống trầm cảm ba vòng (26) và cocain (27) (www.brugadadrugs.org) (28). Cho dù điều này đại diện cho cá nhân bị che lấp với hội chứng Brugada không có căn cứ lâm sàng (xem Phần 7.9.1.3) hoặc kết thúc của một phỏ rộng các đáp ứng đối với các blockers kênh natri còn chưa rõ.
Trong trạng thái độc tính blocker kênh natri, tư liệu trên động vật bị giới hạn gợi ý sử dụng natri, như natri cloride hoặc natri bicarbonate, có thể cải thiện sự chậm dẫntruyềnhoặc ngăn chặn VT thông thường hoặc kháng chuyển nhịp (29). Điều trị thành công với chất chẹn beta (30) và nhũ tương chất béo và / hoặc oxy hóa màng ngoài cơ thể cũng đã được báo cáo (31).
6. Thuốc kéo dài QT (www.crediblemeds.org) (32) không được sử dụng ở bệnh nhân có hội chứng QT dài mắc phải ngoại trừ không có sự thay thế phù hợp hoặc lợi ích vượt qua nguy cơ. Các đợt torsades de pointes có thể bị thúc đẩy do tiếp xúc với thuốc kéo dài theo QT, và việc kéo dài QT (từ các yếu tố nguy cơ di truyền và lâm sàng) làm tăng nguy cơ này (10). Các loại thuốc có liên quan đến torsades de pointes được tìm thấy trong một số nhóm dược phẩm, bao gồm thuốc chống loạn nhịp, thuốc kháng histamin, thuốc kháng sinh, thuốc chống nấm, thuốc chống trầm cảm, thuốc chống loạn thần, thuốc phiện và thuốc chống ung thư (10) (Bảng 10).
Tài liệu tham khảo
1. Antman EM, Wenger TL, Butler VP Jr, et al. Treatment of 150 cases of life-threatening digitalis intoxication with digoxin-specific Fab antibody fragments. Final report of a multicenter study. Circulation. 1990;81:1744-52.
2. Chan BS, Buckley NA. Digoxin-specific antibody fragments in the treatment of digoxin toxicity. Clin Toxicol. 2014;52:824-36.
3. Keren A, Tzivoni D, Gavish D, et al. Etiology, warning signs and therapy of torsade de pointes. A study of 10 patients. Circulation. 1981;64:1167-74.
4. Tzivoni D, Banai S, Schuger C, et al. Treatment of torsade de pointes with magnesium sulfate. Circulation. 1988;77:392-7.
5. Kannankeril P, Roden DM, Darbar D. Drug-induced long QT syndrome. Pharmacol Rev. 2010;62:760-81.
6. Choy AM, Lang CC, Chomsky DM, et al. Normalization of acquired QT prolongation in humans by intravenous potassium. Circulation. 1997;96:2149-54.
7. Yang T, Roden DM. Extracellular potassium modulation of drug blốc of IKr. Implications for torsade de pointes and reverse use-dependence. Circulation. 1996;93:407-11.
8. Hellestrand KJ, Burnett PJ, Milne JR, et al. Effect of the antiarrhythmic agent flecainide acetate on acute and chronic pacing thresholds. Pacing Clin Electrophysiol. 1983;6:892-9.
9. Echt DS, Black JN, Barbey JT, et al. Evaluation of antiarrhythmic drugs on defibrillation energy requirements in dogs. Sodium channel blốc and action potential prolongation. Circulation. 1989;79:1106-17.
10.Schwartz PJ, Woosley RL. Predicting the unpredictable: drug-induced QT prolongation and torsades de pointes. J Am Coll Cardiol. 2016;67:1639-50.
11.Hauptman PJ, Kelly RA. Digitalis. Circulation. 1999;99:1265-70.
12.Kelly RA, Smith TW. Recognition and management of digitalis toxicity. Am J Cardiol. 1992;69:108G-18G.
13.Osmonov D, Erdinler I, Ozcan KS, et al. Management of patients with drug-induced atrioventricular blốc. Pacing Clin Electrophysiol. 2012;35:804-10.
14.Zipes DP, Camm AJ, Borggrefe M, et al. ACC/AHA/ESC 2006 guidelines for management of patients with ventricular arrhythmias and the prevention of sudden cardiac death: a report of the American College of Cardiology/American Heart Association Task Force and the European Society of Cardiology Committee for Practice Guidelines. Circulation. 2006;114:e385-484.
15.Behr ER, Ritchie MD, Tanaka T, et al. Genome wide analysis of drug-induced torsades de pointes: lack of common variants with large effect sizes. PloS One. 2013;8:e78511.
16.Kaab S, Crawford DC, Sinner MF, et al. A large candidate gene survey identifies the KCNE1 D85N polymorphism as a possible modulator of drug-induced torsades de pointes. Circ Cardiovasc Genet. 2012;5:91-9.
17.Strauss DG, Vicente J, Johannesen L, et al. A common genetic variant risk score is associated with drug-induced QT prolongation and torsade de pointes risk: a pilot study. Circulation. 2017;135:1300-10.
18.Yang P, Kanki H, Drolet B, et al. Allelic variants in long-QT disease genes in patients with drug-associated torsades de pointes. Circulation. 2002;105:1943-8.
19.Weeke P, Mosley JD, Hanna D, et al. Exome sequencing implicates an increased burden of rare potassium channel variants in the risk of drug-induced long QT interval syndrome. J Am Coll Cardiol. 2014;63:1430-7.
20.Echt DS, Liebson PR, Mitchell LB, et al. Mortality and morbidity in patients receiving encainide, flecainide, or placebo. The Cardiac Arrhythmia Suppression Trial. N Engl J Med. 1991;324:781-8.
21.Chamberlain DA, Jewitt DE, Julian DG, et al. Oral mexiletine in high-risk patients after myocardial infarction. Lancet. 1980;2:1324-7.
22.UK Rythmodan Multicentre Study Group. Oral disopyramide after admission to hospital with suspected acute myocardial infarction. U. K. Rythmodan Multicentre Study Group. Postgrad Med J. 1984;60:98-107.
23.Crijns HJ, Van Gelder IC, Lie KI. Supraventricular tachycardia mimicking ventricular tachycardia during flecainide treatment. Am J Cardiol. 1988;62:1303-6.
24.Alings M, Wilde A. “Brugada” syndrome: clinical data and suggested pathophysiological mechanism. Circulation. 1999;99:666-73.
25.Konigstein M, Rosso R, Topaz G, et al. Drug-induced Brugada syndrome: clinical characteristics and risk factors. Heart Rhythm. 2016;13:1083-7.
26.Tada H, Sticherling C, Oral H, et al. Brugada syndrome mimicked by tricyclic antidepressant overdose. J Cardiovasc Electrophysiol. 2001;12:275.
27.Littmann L, Monroe MH, Svenson RH. Brugada-type electrocardiographic pattern induced by cocaine. Mayo Clin Proc. 2000;75:845-9.
28.Brugada drugs. Available at: http://www.brugadadrugs.org. Accessed October 6, 2016.
29.Bajaj AK, Woosley RL, Roden DM. Acute electrophysiologic effects of sodium administration in dogs treated with O-desmethyl encainide. Circulation. 1989;80:994-1002.
30.Myerburg RJ, Kessler KM, Cox MM, et al. Reversal of proarrhythmic effects of flecainide acetate and encainide hydrochloride by propranolol. Circulation. 1989;80:1571-9.
31.Brumfield E, Bernard KR, Kabrhel C. Life-threatening flecainide overdose treated with intralipid and extracorporeal membrane oxygenation. Am J Emerg Med. 2015;33:1840-5.
32.Credible meds. Available at: http://www.crediblemeds.org. Accessed December 26, 2016.
10.8. Bệnh tim bẩn sinh người lớn
|
Các khuyến cáo cho bệnh tim bẩm sinh người lớn Tài liệu tham khảo ủng hộ các khuyến cáo được tóm tắt trong tư liệu hỗ trợ online 54. |
||
|
COR |
LOE |
Các khuyến cáo |
|
I |
B-NR |
1. Bệnh nhân người lớn bị bệnh tim bẩm sinh phức hợp đã được sửa chữa có VA thường xuyên, phức tạp hoặc dai dẳng, hoặc ngất không giải thích được nên đánh giá về các giải phẫu còn sót lại hoặc các bất thường về động mạch vành (1-6). |
|
I |
B-NR |
2. Ở các bệnh nhân mắc bệnh tim bẩm sinh người lớn và VA phức tạp hoặc dai dẳng với tổn thương huyết động tồn dư quan trọng, điều trị các bất thường huyết động bằng can thiệp qua catheter hoặc ngoại khoa khi khả thi được chỉ định trước khi xem xét triệt phá hoặc ICD (3, 7-12 ). |
|
I |
B-NR |
3. Ở các bệnh nhân bị bệnh tim bẩm sinh người lớn và VT không ổn định về huyết động, ICD được khuyến cáo sau khi đánh giá và điều trị phù hợp đối với các tổn thương tôn dư / rối loạn chức năng thất trái nếu có sống sót > 1 năm có ý nghĩa được dự báo (13-17). |
|
I |
B-NR |
4. Ở các bệnh nhân bị bệnh tim bẩm sinh người lớn có SCA do VT hoặc VF khi không có nguyên nhân có thể đảo ngược, ICD được khuyến cáo nếu sống sót có ý nghĩa hơn 1 năm được dự kiến (13-17). |
|
IIa |
B-NR |
5. Ở người lớn có tứ chứng sinh lý Fallot đã được sửa chữa có các đặc tính nguy cơ cao và VA thường xuyên, nghiên cứu điện sinh lý có thể hữu ích để đánh giá nguy cơ VT/VF dai dẳng (18, 19). |
|
IIa |
B-NR |
6. Ở người lớn có tứ chuwnbgs sinh lý Fallot đã được sửa chữa vf có VT/VF có thể được tạo ra hoặc VT dai dẳng sinh lý, cấy ICD là phù hợp (1, 19, 20). |
|
IIa |
B-NR |
7. Ở các bệnh nhân bị bệnh tim bẩm sinh ở người trưởng thành có VT đơn hình dai dẳng tái phát hoặc sốc ICD cho VT tái phát, triệt phá qua catheter có thể có hiệu quả (21-25). |
|
IIa |
B-NR |
8. Ở các bệnh nhân có bệnh tim bẩm sinh người lớn phức tạp trung bình hoặc nặng có ngất không giải thích được và ít nhất có rối loạn chức năng thất trung bình hoặc phì đại đáng kể, hoặc cấy ICD hoặc nghiên cứu điện sinh lý với cấy ICD đối với VA dai dẳng có thể tại ra là phù hợp nếu sống sót có ý nghĩa > 1 năm được dự kiến (26). |
|
IIa |
B-NR |
9. Ở những bệnh nhân mắc bệnh tim bẩm sinh phức tạp trung bình hoặc nặng ở người trưởng thành đã được sửa chữa có ngất không giải thích được và ít nhất có rối loạn chức năng thất trung bình hoặc nghiên cứu điện sinh lý với cấy ICD cho VA dai dẳng có thể tạo ra là phù hợp nếu sống sót có ý nghĩa > 1 năm được dự kiến (5, 16, 27-29). |
|
IIb |
B-NR |
10. Ở những bệnh nhân có bệnh tim bấm sinh người lớn và rối loạn chức năng thất nặng (LVEF <35%) và triệu chứng suy tim mặc dù GDMT hoặc các yếu tố nguy cơ bổ xung, việc cấy ghép ICD có thể được xem xét nếu sống sót có ý nghĩa hơn 1 năm được dự kiến (14-16 , 20). |
|
III: Harm |
B-NR |
11. Ở các bệnh nhân bị bệnh tim bẩm sinh ở người lớn, những người có VA không triệu chứng, điều trị chống loạn nhịp dự phòng với thuốc cấp Ic (nghĩa là flecainide, propafenone) hoặc amiodarone có khả năng gây hại (30-32). |
Bảng 11 và hình 16
Tóm tắt
Từ chừng Fallot (Tetralogy of Fallot: TOF) được định nghĩa, bệnh tim bẩm sinh với tắc nghẽn đường ra thất phải (RVOT) và khiếm khuyết vách liên thất, thường đòi hỏi phải phải đặt ông từ thất phải sang động mạch phổi hoặc thay van đông mạch phổi; gồm TOF và tâm thất phải hai đường ra. Bệnh tim bẩm sinh phức tạp mức trung bình được định nghĩa là bệnh tim bẩm sinh cần phải được sửa chữa ngoại khoa trong tim, ngoại trừ các khiếm khuyết về tâm thất và nhĩ thất; bao gồm TOF, hẹp động mạch chủ, hẹp eo động mạch chủ, và bất thường Ebstein của van ba lá. Bệnh tim bẩm sinh phức tạp nghiêm trọng được định nghĩa là bệnh tim bẩm sinh có tim đòi hỏi sửa chữa trong tim, thường với các thu thuật theo giai đoạn; gồm chuyển vị các động mạch lớn, các động mạch truncus, và các giải phẫu thất đơn thuần (Hình 16).
Văn bản Hỗ trợ Riêng biệt – Khuyến cáo
1. Sự kết hợp VT với các bất thường về huyết động học RV (thất phải) đã được tính toàn đầu tiên ở các bệnh nhân TOF được sửa chữa (33). Nhiều nghiên cứu từ thời điểm đó đã cho thấy sự tương quan của tồn dư huyết động học và rối loạn chức năng thất với nguy cơ VT hoặc SCD ở bệnh nhân bị bệnh tim bẩm sinh (1, 3-6, 18, 34-36). Thể hiện với VA thường xuyên hoặc phức tạp có thể chỉ ra chức năng huyết động xấu, tổn thương động mạch vành, hoặc tưới máu giảm trong trạng thái phì đại thất. Đánh giá cũng có thể gồm test gắng sức để đánh giá dự trữ chức năng (35). Đánh giá cẩn thận tình trạng huyết động học để tối ưu điều chỉnh là quan trọng (9). Các vấn đề về huyết động tồn dư có khả năng điều trị được có thể được nhận biết trong quá trình đánh giá huyết động, như hẹp đường ra thất hoặc hở đáng kể, có thể có lợi ích từ hoặc can thiệp qua catheter hoặc ngoại khoa (3, 7, 10, 12, 37). Bệnh nhân có chức năng thất giảm rõ rệt, áp lực cuối tâm trương tăng lên, hoặc cao áp động mạch phổi nên được điều trị các vấn đề cơ bàn về huyết động học như một phần của điều chỉnh rối loạn nhịp của chúng.
2. Sự tương quan của các bất thường tồn dư huyết động động học với VA đã được nghiên cứu rộng rãi nhất ở những bệnh nhân có TOF đã được sửa chữa, trong đó tăng áp RV, tắc nghẽn đường ra động mạch phổi tồn dư hoặc hở van, cả giãn RV là những nguy cơ cho VT/SCD (1, 2, 8, 33, 34, 36). Trong các nghiên cứu này, các PVC thường xuyên có tương quan với nguy cơ VT lâm sàng hoặcVT dai dẳng có thể tạo ra. Một cách tiếp cận phối hợp ngoại khoa đối với các bất thường câu trúc với ngoại khoa rối loạn nhipju được hướng dẫn của lập bản đồ đã được sử dụng thành công (3, 8, 10, 12), nhưng việc loại bỏ các vòng VT có thể bị hạn chế do nguồn gốc VT ở LV hoặc nội tâm mạc sâu và các hạn chế của lập bản đồ có hiệu quả; tiếp cận theo kinh nghiệm với phẫu thuật VT thường không được khuyến cáo do hiệu quả bị giới hạn và đưa đến nguy cơ thúc đẩy rối loạn nhịp thất (38). Thay van phổi ở bệnh nhân có TOF có thể cải thiện huyết động học và trạng thái chức năng, nhưng nó cũng có thể không loại trừ được nguy cơ VT (3, 12); đánh giá lại sau phẫu thuật cho nhu cầu ICD được thực hiện sau giai đoạn hồi phục sớm.
3. Sử chữa các bất thường tồn dư huyết động / cấu trúc thúc đẩy VT có thể cải thiện chức năng thất và giảm triệu chứng, nhưng nó có thể ngăn chặn nguy cơ VT hoặc SCA tiếp theo một không đầy đủ. Việc sử dụng ICDs ở bệnh nhân mắc bệnh tim bẩm sinh ở người lớn cho việc dự phòng thứ phát chiếm khoảng 50% số cấy ICD hiện nay, ở tuổi trung bình từ 36 đến 41 tuổi (13-17). Bệnh nhân có bệnh tim bẩm sinh ở người trưởng thành có tỷ lệ sốc phù hợp từ 3% đến 6% mỗi năm, với tần suất sốc phù hợp tăng lên nhẹ đối với các chỉ định phòng ngừa thú phát (14, 15, 17). Bệnh nhân có bệnh tim bẩm sinh ở người trưởng thành có tỷ lệ biến chứng và sốc không phù hợp cao hơn so với các quần thể người lớn khác (13-17, 39).
4. Thách thức của việc cấy ICD ở bệnh nhân bị bệnh tim bẩm sinh ở người trưởng thành có thể gồm phức tạp về giải phẫu, các shunts trong tim, cũng như tiếp cận mạch máu bị hạn chế đến thất. Bệnh nhân bị bệnh tim bẩm sinh ở người lớn nhận được ICD có tỷ lệ biến chứng tăng 26% -45%, cũng như các sốc không thích hợp từ 15% đến 25% bệnh nhân (13-16, 40). Các nghiên cứu hạn chế về việc sử dụng cấy ICD dưới da (41), báo cáo thành công được cải thiện bằng cách sử dụng bên phải thêm vào vị trí dây cạnh ức trái cho việc che dấu (42). Bệnh nhân với tâm thất độc nhất hoặc thất phải hệ thống có thể không chịu đựng được test ngưỡng khử rung, làm suy yếu hệ thống đa hệ. Những bệnh nhân có giải phẫu phức tạp, như những bệnh nhân cao tuổi sinh lý tâm thất độc nhất, hoặc các bệnh nhân có chức năng thất giảm đáng kể, phì đại rõ, hoặc phẫu thuật trước nhiều lần, có thể có lợi từ việc xem xét ghép tim trước khi tiến triển rối loạn chức năng thận và gan.
5. Các bệnh nhân TOF được sửa chữa có nguy cơ tăng lên cho tạo ra VT dai dẳng với hệ thống giảm bớt trước đó đến các shunts phổi, ngất không giải thích được, PVC thường xuyên, nhịp nhanh nhĩ, khoảng QRS >= 180ms, LVEF giảm hoặc rối loạn chức năng tâm trương, thất phải giãn, hở hoặc hép phổi nặng, hoặc mức độ BNP tăng lên. Các bệnh nhân có sinh lý TÒ và trạng thái huyết động dưới tối ưu nhiều khả năng hơn để có VT dai dẳng có thể tạo ra (18, 19, 33, 35), và VT dai dẳng có thể tạo ra được sửa chữa có nguy cơ SCA tăng lên trong nghiên cứu đoàn hệ đa trung tâm (19). Đánh giá huyết động học đối với những bất thường tồn dư là quan trọng, điều trị với catheter hoặc phẫu thuật các tổn thương quan trọng trước khi xem xét cấy ICD.
6. Trong một nghiên cứu đoàn hệ đa trung tâm, VT dai dẳng có thể tạo ra ở bệnh nhân TOF là nguy cơ độc lập cho VT lâm sàng tiếp theo hoặc SCD (19); các bệnh nhân trong nghiên cứu sớm đã có tim giãn lớn và các shunts sửa chữa nhẹ trước đó. Các bệnh nhân TOF được sửa chữa chiếm 50% các ICD được cấy ở bệnh tim bẩm sinh người lớn (13-16, 40). Các sốc ICD phù hợp xảy ra lên tới 7,7% mỗi năm với TOF được cấy ICD để dự phòng tiên phát, so với 9,8% mỗi năm ở bệnh nhân có ICD dự phòng thứ phát (20). Trong một nghiên cứu khác gồm các bệnh nhân bị TOF cũng như các tổn thương khác, VT dai dẳng có thể tạo ra không tương quan với sốc ICD thích hợp tiếp theo (14). Do có tỷ lệ cao các sốc không thích hợp ở mức 20% đến 30% và các biến chứng ít nhất 30% bệnh nhân bị bệnh tim bẩm sinh người lớn (14-17, 39, 40, 43), ngoài những gánh nặng về tài chính và tâm lý, thực hiện quyết định chia sẽ liên quan đến ICD dự phòng tiên phát là cơ bản.
7. Ở các bệnh nhân VT đơn hình dai dẳng tái phát, triệt phá VT qua catheter có thể có hiệu quả (21-25). Sửa chữa huyết động học, vào thời điểm loạn nhịp đã được triệt phá bằng ngoại khoa, nên được xem xét. Đối với các bệnh nhân bệnh tim bẩm sinh người lớn phức tạp, nên chăm sóc tại các trung tâm có kinh nghiệm. Sau khi triệt phá VT qua catheter thành công, cấy ICD cho những người không có ICD được quyết định mang tính cá thể dựa trên cơ sở trạng thái chức năng và sinh lý và thực hiện các quyết định chia sẻ. Theo dõi cẩn thận trong thời gian theo dõi đối với rối loạn nhịp tái phát là điều cơ bản.
8. Nguy cơ SCD cao nhất liên quan đến bệnh tim bẩm sinh đã được sửa chữa được thông báo từ các đoàn hệ lớn đồng thời ở các bệnh nhân chuyển vị đại động mạch có sửa chữa can trở nhĩ, bất thường Ebstein của van ba lá, hẹp động mạch chủ, và sinh lý tâm thất độc nhất (44-47). Bệnh nhân với sửa chữa cản trở nhĩ Senning hoăc Mustard có nguy cơ cáo cho SCD, đặc biệt khi gắng sức (48). Vách ngăn tâm nhĩ là khả năng hạn chế không phù hợp với tăng khối lượng và có thể liên quan đến hẹp tĩnh mạch phổi và áp lực cuối tâm trương tăng lên. Thiếu máu cục bộ và nhồi máu RV xảy ra, với các khiếm khuyết tười máu được xác định do các nghiên cứu tười máu cơ tim ở > 40% bệnh nhân trong quần thể này (49, 50). Các yếu tố nguy cơ ngưng tim ở bệnh nhân có sự chuyển vị và sửa chữa vách ngăn tâm nhĩ gồm đóng khiếm khuyết vách liên thất trước đó, các triệu chứng HF, loạn nhịp, RVEF <30% đến 35%, và thời gian QRS > 140 ms (48, 51). Trong một nghiên cứu đa trung tâm duy nhất đánh giá kết cục sau khi cấy ICD ở bệnh nhân có sửa chữa vách ngăn nhĩ của chuyển vị đại động mạch trước đó, thiếu beta blockers được kết hợp với nguy cơ cao của trị liệu ICD (26). Các rối loạn nhịp nhĩ thường đi trước VT ở những bệnh nhân chuyển vị, và điều trị nhịp nhanh nhĩ gồm triệt phá qua catheter, thuật toán chống nhịp nhanh, cũng như beta blockers là quan trọng để giảm sốc ICD (26, 52, 53).
9. Nguy cơ SCD tăng lên trong số các bệnh nhân bệnh tim bẩm sinh ở người lớn so với các quần thể chung, với tuổi tử vong trung bình phạm vi từ 30 đến 49 (27, 44, 47, 54, 55). Nguy cơ SCD cao nhất trong số các bệnh nhân bệnh tim bẩm sinh phức tạp ở mức vừa hoặc nặng và chiếm khoảng 25% nguyên nhân tử vong do tim (5, 27, 28, 44-46, 55, 56). Bệnh nhân có khiếm khuyết vách và bệnh sử gia đình về khiếm khuyến vách dương tính, bệnh cơ tim, hoặc blốc nhánh bó / khiếm khuyết dẫn truyền có thể có đột biến gene NKX2.5, chúng báo trước nguy cơ tăng lên cho SCD sớm; test di truyền và xem xét sớm cấy ICD nếu dương tính được xác định (57-59). Bệnh nhân có các hình thái tim bẩm sinh phức tạp đã được sửa chữa đã trải qua ngoại khoa trong tim nhiều lần trong vài thập niên đầu tiên của đời sống với sự phì đại kết hợp và nguy cơ cho thiếu máu dười nội tâm mạc cũng như các hình thái góp phần vào VT/VF. Các yếu tố nguy cơ đối với SCD gồm sự phức tạp của bệnh tim tăng lên, VA, SVT, sự tăng lên tiến triển của khoảng thời gian QRS, rối loạn chức năng hệ thống thất và rối loạn chức năng thất dưới phổi (subpulmonary) (1, 5, 6, 14, 28, 29, 36, 45-47, 55) . Ngoại suy từ các dữ liệu liên quan đến các biện pháp cụ thể của chức năng thất bảo đảm việc cấy ICD dự phòng tiên phát từ các bệnh nhân lớn tuổi bị NICM là không thực tế. Sự phát triển của ngất không giải thích được ở những bệnh nhân mắc bệnh tim bẩm sinh phức tạp trung bình đến nặng ở người lớn có thể là điềm báo trước về nguy cơ SCD; nghiên cứu điện sinh lý với việc xem xét ICD cho ngăn ngừa tiên phát có thể có lợi ích.
10. ICDs được cấy ở bệnh nhân bị bệnh tim bẩm sinh người lớn, những người ở độ tuổi 40 và 50, đối với các chỉ định dự phòng tiên phát hiện nay chiếm từ 40% đến 67% số thiết bị cấy ở bệnh nhân bị bệnh tim bẩm sinh ở người trưởng thành (13, 15, 16, 41). Ở những bệnh nhân này, các sốc thích hợp được phóng ra từ 14% đến 22% ở bệnh nhân trong 3 đến 5 năm đầu theo dõi (13, 15, 16). Ở những bệnh nhân bị bệnh tim bẩm sinh và chức năng thất trái giảm nghiêm trọng, hoặc phẫu thuật thất đơn, test ngưỡng khử rung có thể gây ra nguy cơ quá cao. Ở những bệnh nhân không tiếp cận được mạch máu hoặc sử chữa Fontan trước đó, nguy cơ phẫu thuật lại xương ức cho cấy ICD thượng tâm mạc có thể vướt quá những lợi ích tiềm ẩn và việc xem xét đánh giá ghép tạng có thể được ưa chuộng. Cấy ICD dưới da có thể là lựa chọn phù hợp cho các bệnh nhân tương tự (42, 53).
11. Bệnh nhân người lớn có bệnh tim bẩm sinh người lớn phức tạp thường có phì đại và rối loạn chức năng thất ở các mức độ khác nhau, nguy cơ của họ cho chức năng thất trái xấu đi tăng lên với các thuốc chống loạn nhịp. Trong nghiên cứu lớn duy nhất của thuốc chống loạn nhịp cho bệnh tim bẩm sinh, sử dụng flecainide có liên quan đến thúc đẩy loạn nhịp ở 5,8% bệnh nhân và SCA ở 3,9% bệnh nhân (30). Việc sử dụng amiodarone thường được dành riêng cho VA có triệu chứng trơ hoặc VA không triệu chứng có thể làm trầm trọng thêm rối loạn chức năng tâm thất, do nguy cơ cao có thể xảy ra các phản ứng bất lợi gồm rối loạn tuyến giáp, đặc biệt ở nữ giới và bệnh nhân với sinh lý tâm thất độc nhất (31, 32).
Bảng 11. Bệnh tim bẩm sinh: Các yếu tố nguy cơ cho VA/SCD
|
Bệnh tim bẩm sinh |
Tỷ lệ VA |
Tỷ lệ SCD |
Các đặc tính nguy cơ cao |
|
Phức tạp đơn |
|||
|
ASD (44, 47, 57-62) |
2%–6% |
<1.5% |
Tạo nhịp thất Giãn thất phải Tăng áp phổi NKX2.5 gene |
|
VSD (27, 44, 47, 57-63) |
3%–18% |
<3% |
|
|
Phức tạp trung bình |
|||
|
Tứ chứng Fallot (Tetralogy of Fallot) (1, 2, 5, 6, 28, 34, 36, 44, 46, 47, 54-56, 62-65) |
14%–31% |
1.4%–8.3% |
Ngất không giải thích được VA thường xuyên hoặc phức tạp VT dai dẳng Khoảng thời gian QRS ≥180 ms VT dai dẳng có thể tạo ra Nhịp nhanh nhĩ LVEF giảm Thất phải giãn PR nghiêm trọng PS nghiêm trọng |
|
Hẹp động mạch (27, 44, 56) |
10%–34% |
3%–20% |
Ngất không giải thích được Phì đại LV nặng Độ chênh áp lực hẹp động mạch chủ >40 mm Hg Rồi loạn chức năng thất |
|
Hẹp eo động mạch chủ (28, 29, 44, 46, 56, 62) |
2% |
2% |
Phình vị trí sửa chữa Hẹp động mạch chủ Tăng huyết áp hệ thống Bệnh động mạch vành sớm |
|
Bất thường Ebstein (45, 47, 55) |
2% |
3%–6% |
Giãn lớn tim Rung nhĩ Nhịp nhanh phức hợp rộng Hở hai lá RVOT giãn |
|
Phức tạp nặng |
|||
|
Chuyển vị đại động mạch (27, 44-48, 51, 55, 56, 62) Xoay nhĩ Xoay động mạch cc-TGA |
2% 2% 10% |
3%–9.5% 1% 17%–25% |
Xoay nhĩ Sửa chữa Mustard Đóng VSD trước đó Ngất không giải thích được Nhịp nhanh nhĩ Hẹp miệng mạch vành Rối loạn chức năng hệ thống thất Hở 3 lá nặng |
|
Thân chung động mạch (Truncus arteriosus) (66, 67) |
10% |
4% |
Sửa chữa ngoại khoa nhiều lần Các bất thường động mạch vành Rối loạn chức năng thất và/hoặc phì đại |
|
Sửa chữa Fontan cho sinh lý tâm thất độc nhất * (27, 37, 44, 45, 47, 55, 68) |
5%–17% |
2.8%–5.4% |
Nhịp nhanh nhĩ Khoảng thời gian theo dõi dài hơn Cổ chướng Bệnh ruột mất Protein |
* Sinh lý tâm thất độc nhất gồm: Không van 3 lá, Thất trái 2 đường vào, Không van 2 lá, Tim trái giản chun giãn, Khiếm khuyết vách liên thất mất cân bằng.
ASD: khiếm khuyết vách liên nhĩ; cc-TGA: chuyển vị đại động mạch có sửa chữa bẩm sinh; LV: thất trái; LVEF: phân suất tống máu; PR: hở phổi; PS: hẹp phổi; RV: thất phải; RVOT: đường ra thất phải; SCD: đột tử tim; VA: rối loạn nhịp thất; VSD: khiếm khuyết vách liên thất; và VT: nhịp nhanh thất.
Hình 16. Ngăn ngừa SCD ở bệnh nhân có tim bẩm sinh ở người lớn
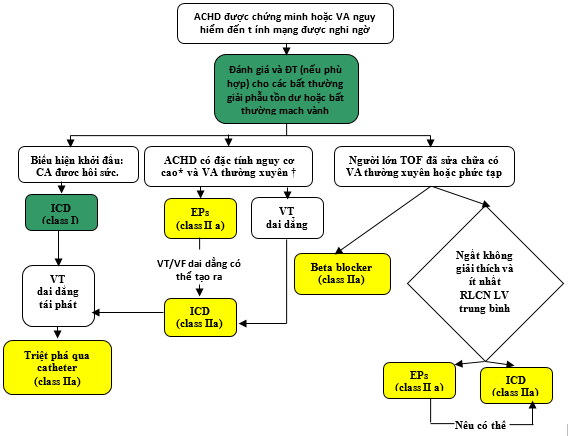
Các màu tương ứng với Classs của khuyến cáo ở bảng 1.
Xem phần 10.8 cho thảo luận.
*Đặc tính nguy cơ cao:Hệ thống giảm bớt trước kia đối với shunts phổi, ngất không giải thích được, PVC thường xuyên, nhịp nhanh nhĩ, khoảng thời gian QRS > 180 ms, LVEF giảm hoặc rối loạn chức năng tâm trương, tâm thất phải giãn, hở hoặc hẹp phổi nặng, hoặc mức độ BNP tăng.
†VA thường xuyên đề cập đến PVC thường xuyên và / hoặc VT tạm thời. ACHD: bệnh tim bẩm sinh người lớn; BNP: peptide natriuretic type B; EPs: nghiên cứu điện sinh lý; ICD: máy khử rung tim có thể cấy; LVEF: phân suất tống máu thất trái; PVC: phức hợp thất sớm; SCD: đột tử tim; TOF: tứ chứng Fallot; VA: loạn nhịp thất; và VT: nhịp nhanh thất.VF: rung thất. RLCNLV: rối loạn chức năng thất trái.
Tài liệu tham khảo
1. Diller GP, Kempny A, Liodakis E, et al. Left ventricular longitudinal function predicts life-threatening ventricular arrhythmia and death in adults with repaired tetralogy of fallot. Circulation. 2012;125:2440-6.
2. Gatzoulis MA, Till JA, Somerville J, et al. Mechanoelectrical interaction in tetralogy of Fallot. QRS prolongation relates to right ventricular size and predicts malignant ventricular arrhythmias and sudden death. Circulation. 1995;92:231-7.
3. Harrison DA, Harris L, Siu SC, et al. Sustained ventricular tachycardia in adult patients late after repair of tetralogy of Fallot. J Am Coll Cardiol. 1997;30:1368-73.
4. Knauth AL, Gauvreau K, Powell AJ, et al. Ventricular size and function assessed by cardiac MRI predict major adverse clinical outcomes late after tetralogy of Fallot repair. Heart. 2008;94:211-6.
5. Koyak Z, de Groot JR, Bouma BJ, et al. Sudden cardiac death in adult congenital heart disease: can the unpredictable be foreseen? Europace. 2017;19:401-6.
6. Koyak Z, Harris L, de Groot JR, et al. Sudden cardiac death in adult congenital heart disease. Circulation. 2012;126:1944-54.
7. Adamson L, Vohra HA, Haw MP. Does pulmonary valve replacement post repair of tetralogy of Fallot improve right ventricular function? Interact Cardiovasc Thorac Surg. 2009;9:520-7.
8. Deal BJ, Scagliotti D, Miller SM, et al. Electrophysiologic drug testing in symptomatic ventricular arrhythmias after repair of tetralogy of Fallot. Am J Cardiol. 1987;59:1380-5.
9. Khairy P, Van Hare GF, Balaji S, et al. PACES/HRS Expert consensus statement on the recognition and management of arrhythmias in adult congenital heart disease: developed in partnership between the Pediatric and Congenital Electrophysiology Society (PACES) and the Heart Rhythm Society (HRS). Heart Rhythm. 2014;11:e102-65.
10.Sabate Rotes A, Connolly HM, Warnes CA, et al. Ventricular arrhythmia risk stratification in patients with tetralogy of Fallot at the time of pulmonary valve replacement. Circ Arrhythm Electrophysiol. 2015;8:110-6.
11.Therrien J, Provost Y, Merchant N, et al. Optimal timing for pulmonary valve replacement in adults after tetralogy of Fallot repair. Am J Cardiol. 2005;95:779-82.
12.Therrien J, Siu SC, Harris L, et al. Impact of pulmonary valve replacement on arrhythmia propensity late after repair of tetralogy of Fallot. Circulation. 2001;103:2489-94.
13.Kella DK, Merchant FM, Veledar E, et al. Lesion-specific differences for implantable cardioverter defibrillator therapies in adults with congenital heart disease. Pacing Clin Electrophysiol. 2014;37:1492-8.
14.Koyak Z, de Groot JR, Van Gelder IC, et al. Implantable cardioverter defibrillator therapy in adults with congenital heart disease: who is at risk of shocks? Circ Arrhythm Electrophysiol. 2012;5:101-10.
15.Santharam S, Hudsmith L, Thorne S, et al. Long-term follow-up of implantable cardioverter-defibrillators in adult congenital heart disease patients: indications and outcomes. Europace. 2017;19:407-13.
16.Vehmeijer JT, Brouwer TF, Limpens J, et al. Implantable cardioverter-defibrillators in adults with congenital heart disease: a systematic review and meta-analysis. Eur Heart J. 2016;37:1439-48.
17.Yap SC, Roos-Hesselink JW, Hoendermis ES, et al. Outcome of implantable cardioverter defibrillators in adults with congenital heart disease: a multi-centre study. Eur Heart J. 2007;28:1854-61.
18.Chandar JS, Wolff GS, Garson A Jr, et al. Ventricular arrhythmias in postoperative tetralogy of Fallot. Am J Cardiol. 1990;65:655-61.
19.Khairy P, Landzberg MJ, Gatzoulis MA, et al. Value of programmed ventricular stimulation after tetralogy of fallot repair: a multicenter study. Circulation. 2004;109:1994-2000.
20.Khairy P, Harris L, Landzberg MJ, et al. Implantable cardioverter-defibrillators in tetralogy of Fallot. Circulation. 2008;117:363-70.
21.Kapel GF, Reichlin T, Wijnmaalen AP, et al. Re-entry using anatomically determined isthmuses: a curable ventricular tachycardia in repaired congenital heart disease. Circ Arrhythm Electrophysiol. 2015;8:102-9.
22.Kapel GF, Reichlin T, Wijnmaalen AP, et al. Left-sided ablation of ventricular tachycardia in adults with repaired tetralogy of Fallot: a case series. Circ Arrhythm Electrophysiol. 2014;7:889-97.
23.Kapel GF, Sacher F, Dekkers OM, et al. Arrhythmogenic anatomical isthmuses identified by electroanatomical mapping are the substrate for ventricular tachycardia in repaired tetralogy of Fallot. Eur Heart J. 2017;38:268-76.
24.van Zyl M, Kapa S, Padmanabhan D, et al. Mechanism and outcomes of catheter ablation for ventricular tachycardia in adults with repaired congenital heart disease. Heart Rhythm. 2016;13:1449-54.
25.Zeppenfeld K, Schalij MJ, Bartelings MM, et al. Catheter ablation of ventricular tachycardia after repair of congenital heart disease: electroanatomic identification of the critical right ventricular isthmus. Circulation. 2007;116:2241-52.
26.Khairy P, Harris L, Landzberg MJ, et al. Sudden death and defibrillators in transposition of the great arteries with intra-atrial baffles: a multicenter study. Circ Arrhythm Electrophysiol. 2008;1:250-7.
27.Engelings CC, Helm PC, Abdul-Khaliq H, et al. Cause of death in adults with congenital heart disease – an analysis of the German National Register for Congenital Heart Defects. Int J Cardiol. 2016;211:31-6.
28.Gallego P, Gonzalez AE, Sanchez-Recalde A, et al. Incidence and predictors of sudden cardiac arrest in adults with congenital heart defects repaired before adult life. Am J Cardiol. 2012;110:109-17.
29.Tutarel O, Kempny A, Alonso-Gonzalez R, et al. Congenital heart disease beyond the age of 60: emergence of a new population with high resource utilization, high morbidity, and high mortality. Eur Heart J. 2014;35:725-32.
30.Fish FA, Gillette PC, Benson DW Jr. Proarrhythmia, cardiac arrest and death in young patients receiving encainide and flecainide. The Pediatric Electrophysiology Group. J Am Coll Cardiol. 1991;18:356-65.
31.Stan MN, Sathananthan M, Warnes C, et al. Amiodarone-induced thyrotoxicosis in adults with congenital heart disease-clinical presentation and response to therapy. Endocr Pract. 2014;21:33-40.
32.Thorne SA, Barnes I, Cullinan P, et al. Amiodarone-associated thyroid dysfunction: risk factors in adults with congenital heart disease. Circulation. 1999;100:149-54.
33.Garson A Jr, Porter CB, Gillette PC, et al. Induction of ventricular tachycardia during electrophysiologic study after repair of tetralogy of Fallot. J Am Coll Cardiol. 1983;1:1493-502.
34.Khairy P, Aboulhosn J, Gurvitz MZ, et al. Arrhythmia burden in adults with surgically repaired tetralogy of Fallot: a multi-institutional study. Circulation. 2010;122:868-75.
35.Tsai SF, Chan DP, Ro PS, et al. Rate of inducible ventricular arrhythmia in adults with congenital heart disease. Am J Cardiol. 2010;106:730-6.
36.Valente AM, Gauvreau K, Assenza GE, et al. Contemporary predictors of death and sustained ventricular tachycardia in patients with repaired tetralogy of Fallot enrolled in the INDICATOR cohort. Heart. 2014;100:247-53.
37.Sakamoto T, Nagashima M, Hiramatsu T, et al. Fontan circulation over 30 years. What should we learn from those patients? Asian Cardiovasc Thorac Ann. 2016;24:765-71.
38.Harrild DM, Berul CI, Cecchin F, et al. Pulmonary valve replacement in tetralogy of Fallot: impact on survival and ventricular tachycardia. Circulation. 2009;119:445-51.
39.Berul CI, Van Hare GF, Kertesz NJ, et al. Results of a multicenter retrospective implantable cardioverter-defibrillator registry of pediatric and congenital heart disease patients. J Am Coll Cardiol. 2008;51:1685-91.
40.Khanna AD, Warnes CA, Phillips SD, et al. Single-center experience with implantable cardioverter-defibrillators in adults with complex congenital heart disease. Am J Cardiol. 2011;108:729-34.
41.Moore JP, Mondesert B, Lloyd MS, et al. Clinical experience with the subcutaneous implantable cardioverter-defibrillator in adults with congenital heart disease. Circ Arrhythm Electrophysiol. 2016;9:e004338.
42.Okamura H, McLeod CJ, DeSimone CV, et al. Right parasternal lead placement increases eligibility for subcutaneous implantable cardioverter defibrillator therapy in adults with congenital heart disease. Circ J. 2016;80:1328-35.
43.Witte KK, Pepper CB, Cowan JC, et al. Implantable cardioverter-defibrillator therapy in adult patients with tetralogy of Fallot. Europace. 2008;10:926-30.
44.Raissadati A, Nieminen H, Haukka J, et al. Late causes of death after pediatric cardiac surgery: a 60-year population-based study. J Am Coll Cardiol. 2016;68:487-98.
45.Diller GP, Kempny A, Alonso-Gonzalez R, et al. Survival prospects and circumstances of death in contemporary adult congenital heart disease patients under follow-up at a large tertiary centre. Circulation. 2015;132:2118-25.
46.Nieminen HP, Jokinen EV, Sairanen HI. Causes of late deaths after pediatric cardiac surgery: a population-based study. J Am Coll Cardiol. 2007;50:1263-71.
47.Zomer AC, Vaartjes I, Uiterwaal CS, et al. Circumstances of death in adult congenital heart disease. Int J Cardiol. 2012;154:168-72.
48.Lange R, Horer J, Kostolny M, et al. Presence of a ventricular septal defect and the Mustard operation are risk factors for late mortality after the atrial switch operation: thirty years of follow-up in 417 patients at a single center. Circulation. 2006;114:1905-13.
49.Lubiszewska B, Gosiewska E, Hoffman P, et al. Myocardial perfusion and function of the systemic right ventricle in patients after atrial switch procedure for complete transposition: long-term follow-up. J Am Coll Cardiol. 2000;36:1365-70.
50.Millane T, Bernard EJ, Jaeggi E, et al. Role of ischemia and infarction in late right ventricular dysfunction after atrial repair of transposition of the great arteries. J Am Coll Cardiol. 2000;35:1661-8.
51.Schwerzmann M, Salehian O, Harris L, et al. Ventricular arrhythmias and sudden death in adults after a Mustard operation for transposition of the great arteries. Eur Heart J. 2009;30:1873-9.
52.Buber J, Ackley TJ, Daniels CJ, et al. Outcomes following the implantation of cardioverter-defibrillator for primary prevention in transposition of the great arteries after intra-atrial baffle repair: a single-centre experience. Europace. 2016;18:1016-22.
53.Backhoff D, Kerst G, Peters A, et al. Internal cardioverter defibrillator indications and therapies after atrial baffle procedure for d-transposition of the great arteries: a multicenter analysis. Pacing Clin Electrophysiol. 2016;39:1070-76.
54.Oechslin EN, Harrison DA, Connelly MS, et al. Mode of death in adults with congenital heart disease. Am J Cardiol. 2000;86:1111-6.
55.Verheugt CL, Uiterwaal CS, van der Velde ET, et al. Mortality in adult congenital heart disease. Eur Heart J. 2010;31:1220-9.
56.Silka MJ, Hardy BG, Menashe VD, et al. A population-based prospective evaluation of risk of sudden cardiac death after operation for common congenital heart defects. J Am Coll Cardiol. 1998;32:245-51.
57.Abou Hassan OK, Fahed AC, Batrawi M, et al. NKX2-5 mutations in an inbred consanguineous population: genetic and phenotypic diversity. Sci Rep. 2015;5:8848.
58.El Malti R, Liu H, Doray B, et al. A systematic variant screening in familial cases of congenital heart defects demonstrates the usefulness of molecular genetics in this field. Eur J Human Genet. 2016;24:228-36.
59.Ellesoe SG, Johansen MM, Bjerre JV, et al. Familial atrial septal defect and sudden cardiac death: identification of a novel NKX2-5 mutation and a review of the literature. Congenit Heart Dis. 2016;11:283-90.
60.Cuypers JA, Opic P, Menting ME, et al. The unnatural history of an atrial septal defect: longitudinal 35 year follow up after surgical closure at young age. Heart. 2013;99:1346-52.
61.Kuijpers JM, van der Bom T, van Riel AC, et al. Secundum atrial septal defect is associated with reduced survival in adult men. Eur Heart J. 2015;36:2079-86.
62.Verheugt CL, Uiterwaal CS, Grobbee DE, et al. Long-term prognosis of congenital heart defects: a systematic review. Int J Cardiol. 2008;131:25-32.
63.Engelfriet P, Boersma E, Oechslin E, et al. The spectrum of adult congenital heart disease in Europe: morbidity and mortality in a 5 year follow-up period. The Euro Heart Survey on adult congenital heart disease. Eur Heart J. 2005;26:2325-33.
64.Arya S, Kovach J, Singh H, et al. Arrhythmias and sudden death among older children and young adults following tetralogy of Fallot repair in the current era: are previously reported risk factors still applicable? Congenit Heart Dis. 2014;9:407-14.
65.Wu MH, Lu CW, Chen HC, et al. Arrhythmic burdens in patients with tetralogy of Fallot: a national database study. Heart Rhythm. 2015;12:604-9.
66.Baraona F, Valente AM, Porayette P, et al. Coronary arteries in childhood heart disease: implications for management of young adults. J Clin Exp Cardiolog. 2012;(suppl 8):006.
67.Naimo PS, Fricke TA, Yong MS, et al. Outcomes of truncus arteriosus repair in children: 35 years of experience from a single institution. Semin Thorac Cardiovasc Surg. 2016;28:500-11.
68.Pundi KN, Pundi KN, Johnson JN, et al. Sudden cardiac death and late arrhythmias after the Fontan operation. Congenit Heart Dis. 2017;12:17-23.
11.Máy khử rung tim khác với ICD qua đường tĩnh mạch
11.1. Máy khử rung tim có thể cấy dưới da
|
Các khuyến cáo cho máy khử rung tim cấy dưới da Điều ủng hộ các khuyến cáo được tóm tắt trong Tư liệu Hỗi trợ Online 55. |
||
|
COR |
LOE |
Khuyến cáo |
|
I |
B-NR |
1. Ở những bệnh nhân đáp ứng được các tiêu chuẩn cho ICD nhưng tiếp cận mạch máu không phù hợp hoặc nguy cơ cao cho nhiễm trùng, cũng như ở họ việc tạo nhịp cho nhịp chậm hoặc cắt cơn VT hoặc như một phần của CRT hoặc không cần thiết hoặc không được dự đoán, máy khử rung dưới da được khuyến cáo (1-5). |
|
IIa |
B-NR |
2. Ở các bệnh nhân đáp ứng chỉ định cho ICD, việc cấy máy khử rung tim dưới da có thể là hợp lý nếu nhịp tim chậm hoặc chấm dứt VT hoặc như là một phần của CRT là không cần thiết và cũng không được dự đoán (1-4). |
|
III: Harm |
B-NR |
3. Ở những bệnh nhân có chỉ định tạo nhịp cho nhịp chậm hoặc CRT, hoặc cho những người tạo nhịp chống nhịp nhanh cho việc cắt VT được đòi hỏi, máy khử rung tim dưới da không nên được cấy (1-4, 6-8). |
Tóm tắt
Ở bệnh nhân đang được xem xét cho máy khử rung tim dưới da, ECG trước khi cấy để tính toán hình thể học sóng QRS-T là cần thiết để giảm nguy cơ nhận cảm thấp của VT / VF và nguy cơ sốc không phù hợp (9-11). Máy khử rung tim dưới da được cấy bằng cách sử dụng các mốc giải phẫu chủ yếu, do đó giảm thiểu nhu cầu sử dụng soi quang tuyến. Máy khử rung tim cấy dưới da gồm một máy phát xung đặt ở đường giữa của khe liên sườn thứ năm và thứ sáu và một dây điện cực với 2 điện cực nhận cảm và cuộn sốc, đặt ngay sát vào xương ức ngay dưới da. Cũng giống như ICD đường tĩnh mạch, máy phát xung hoạt động như điện cực khử rung nhưng thêm vào, nó có thể cũng đóng vai trò như điện cực lựa chọn cho nhận cảm. Máy khử rung tim dưới da có thể cấy dưới da không thể đạt được nhận cảm rối loạn nhịp phù hợp cho tất cả các bệnh nhân, và kiểm tra điện tim để đánh giá nhận cảm đòi hỏi trước khi cấy (10, 11). Một số đòi hỏi test gắng sức sau cấy dụng cụ để chắc chắn nhận cảm cho test gắng sức sau cấy dụng cụ để chắc chắn nhận cảm phù hợp với gắng sức.
Cả hai máy khử rung tim cấy qua đường tĩnh mạch và dưới da đều có bộ phân biệt SVT-VT có thể được lập trình để tạo sự phân biệt SVT với VT; tuy nhiên, những phân biệt này không phải lúc nào cũng hiệu quả. Nếu VT dai dẳng được xác nhận, điều trị cắt cơn loạn nhịp được phóng ra. Tất cả các ICDs cung cấp sốc để cắt các VT hoặc VF, nhưng các sốc trong bệnh nhân tỉnh táo làm đau đớn và liên quan đến chất lượng sống. ICDs qua tĩnh mạch có khả năng tạo nhịp cho nhịp chậm cũng như tạo nhịp chống nhịp nhanh để các nhiều cơn VT mà không đau đớn. Máy khử rung tim cấy dưới da cung cấp nhịp tim nhịp tim giới hạn ở posthock nhưng không cung cấp tạo nhịp cho nhịp chậm sau sốc bị hạn chế không cung cấp hoặc tạo nhịp cho nhịp chậm cũng không tạo nhịp chống nhịp nhanh.
Khử rung tim dưới da được khuyến cáo có thể cấy, Các khuyến cáo thay thế, nhưng không thể loại bỏ, sự cần thiết trong một giai đoạn chờ đợi và các dụng cụ khác để được tính toán cho cấy ICD/CRT được về khử rung tim dưới da có thể cấy ghép được, nhưng không làm mất hiệu lực, sự cần thiết phải chờ đợi thời gian và các yêu cầu khác để đáp ứng cho việc cấy ICD / CRT được xác định trong các phần khác của tài liệu này.
Văn bản Hỗ trợ Riêng biệt – Khuyến cáo
1. Máy khử rung tim cấy dưới da được thiết kế để tránh việc cần thiết tiếp cận tĩnh mạch và một số biến chứng của điện cực đưa vào tĩnh mạch (1-4) gồm tràn khí màng phổi, tràn dịch màng phổi và ép tim). Những khó khăn trong việc tiếp cận tĩnh mạch có thể kéo dài quá trình cấy và đôi khi dẫn đến cấy ICD thất bại. Những khó khăn này có nhiều khả năng gặp phải ở những bệnh nhân có tiếp cận tĩnh mạch hạn chế như bệnh nhân bệnh thận giai đoạn cuối (ESRD). Trong một nghiên cứu của 27 bệnh nhân ESRD, máy khử rung tim dưới da không gắn với tăng nguy cơ biến chứng thủ thuật hoặc các cú sốc không thích hợp (5). Nguy cơ nhiễm trùng huyết thấp hơn so với ICDs qua đường tĩnh mạch (1-4). Do đó, một máy khử rung tim cấy dưới da có thể được ưa chuộng ở những bệnh nhân có nguy cơ cao bị nhiễm trùng, như những người có nhiễm trùng dụng cụ trước đó, ESRD, tiểu đường, hoặc những người bị suy giảm miễn dịch mạn tính.
2. Các nghiên cứu không ngẫu nhiên cho thấy máy khử rung tim cấy dưới da phát hiện và đảo ngược VF trong test ngưỡng khử rung và cắt thành công các VT dai dẳng tự phát xẩy ra trong quá trình theo dõi (1, 13). Trong 1 nghiên cứu 314 bệnh nhân, tỷ lệ không biến chứng 180 ngày 99% và thành công của việc cắt VF bằng sốc đầu tiên > 90% (2). Tất cả các cơn VT/VF tự phát ở 21 bệnh nhân (6,7%) đã được đảo ngược thành công, và không có sai lệch điện cực, viêm nội tâm mạc hay nhiễm trùng máu, chèn ép tim, thủng tim, tràn khí màng phổi hoặc tràn máu phổi liên quan đến máy khử rung tim cấy ghép dưới da (2) . Trong số 472 bệnh nhân tham gia vào đăng ký EFFORTLESS (Evaluation of Factors Impacting Clinical Outcome and Cost Effectiveness of the S-ICD) (3), tỷ lệ không biến chứng 94%, trong 360 ngày. Hiệu quả chuyển nhịp của sốc đầu tiên 88% và chuyển nhịp lâm sàng thành công 100% sau tối đa 5 cú sốc. Trong 882 bệnh nhân tham gia trong nghiên cứu miễn phí khám phá thiết bị và đăng ký EFFORTLESS (4), 111 trường hợp VT / VF tự phát được điều trị ở 59 bệnh nhân; 90,1% đã cắt cơn với 1 sốc, và 98,2% đã cắt cơn trong phạm vi 5 sốc có khả năng. Tỷ lệ sốc không phù hợp được tính toán 3 năm 13,1% đại đa số do quá nhạy cảm với các tín hiệu của tim, và tử suất 4,7%. Các biến chứng liên quan đến thiết bị xảy ra ở 11,1% bệnh nhân. Một thử nghiệm đang tiến hành sẽ so sánh hiệu quả của máy khử rung tim cấy dưới da với ICD qua đường tĩnh mạch về kết quả của sốc không phù hợp, biến chứng, hiệu quả sốc, và tử suất (13).
3. Máy khử rung tim cấy dưới da không có khả năng tạo nhịp cho chậm, tạo nhịp hai buồng thất, hoặc tạo nhịp chống nhịp nhanh. Do đó, những bệnh nhân cần bất kỳ loại nào của tạo nhịp từ ICD không nên được cung cấp máy khử rung cấy dưới da (6). Một số tình huống lâm sàng có thể xuất hiện trong đó một máy tạo nhịp tim đường tĩnh mạch cho tạo nhịp chậm ở bệnh nhân có khử rung tim cấy dưới da – nó là cần thiết; điều này có thể được thực hiện miễn tạo nhịp không phải đơn cực. Thiết bị tạo nhịp không dây cho các bệnh nhân người đòi hỏi tạo nhịp sẽ được đánh giá với máy khử rung tim cấy dưới da trong tương lai gần.
Tài liệu tham khảo
1. Bardy GH, Smith WM, Hood MA, et al. An entirely subcutaneous implantable cardioverter-defibrillator. N Engl J Med. 2010;363:36-44.
2. Weiss R, Knight BP, Gold MR, et al. Safety and efficacy of a totally subcutaneous implantable-cardioverter defibrillator. Circulation. 2013;128:944-53.
3. Lambiase PD, Barr C, Theuns DA, et al. Worldwide experience with a totally subcutaneous implantable defibrillator: early results from the EFFORTLESS S-ICD Registry. Eur Heart J. 2014;35:1657-65.
4. Burke MC, Gold MR, Knight BP, et al. Safety and efficacy of the totally subcutaneous implantable defibrillator: 2-year results from a pooled analysis of the IDE study and EFFORTLESS registry. J Am Coll Cardiol. 2015;65:1605-15.
5. El-Chami MF, Levy M, Kelli HM, et al. Outcome of subcutaneous implantable cardioverter defibrillator implantation in patients with end-stage renal disease on dialysis. J Cardiovasc Electrophysiol. 2015;26:900-4.
6. de Bie MK, Thijssen J, van Rees JB, et al. Suitability for subcutaneous defibrillator implantation: results based on data from routine clinical practice. Heart. 2013;99:1018-23.
7. Olde Nordkamp LR, Dabiri AL, Boersma LV, et al. The entirely subcutaneous implantable cardioverter-defibrillator: initial clinical experience in a large Dutch cohort. J Am Coll Cardiol. 2012;60:1933-9.
8. Köbe J, Reinke F, Meyer C, et al. Implantation and follow-up of totally subcutaneous versus conventional implantable cardioverter-defibrillators: a multicenter case-control study. Heart Rhythm. 2013;10:29-36.
9. Groh CA, Sharma S, Pelchovitz DJ, et al. Use of an electrocardiographic screening tool to determine candidacy for a subcutaneous implantable cardioverter-defibrillator. Heart Rhythm. 2014;11:1361-6.
10.Olde Nordkamp LR, Warnaars JL, Kooiman KM, et al. Which patients are not suitable for a subcutaneous ICD: incidence and predictors of failed QRS-T-wave morphology screening. J Cardiovasc Electrophysiol. 2014;25:494-9.
11.Randles DA, Hawkins NM, Shaw M, et al. How many patients fulfil the surface electrocardiogram criteria for subcutaneous implantable cardioverter-defibrillator implantation? Europace. 2014;16:1015-21.
12.Al-Khatib SM, Greiner MA, Peterson ED, et al. Patient and implanting physician factors associated with mortality and complications after implantable cardioverter-defibrillator implantation, 2002-2005. Circ Arrhythm Electrophysiol. 2008;1:240-9.
13.Olde Nordkamp LR, Knops RE, Bardy GH, et al. Rationale and design of the PRAETORIAN trial: a Prospective, RAndomizEd comparison of subcuTaneOus and tRansvenous ImplANtable cardioverter-defibrillator therapy. Am Heart J. 2012;163:753-60.
11.2. Áo khử rung tim
|
Các khuyến cáo cho áo khử rung tim Tài liệu tham khảo ủng hộ khuyến cáo được tóm tắt trong tài liệu hỗ trợ online 56. |
||
|
COR |
LOE |
Các khuyến cáo |
|
IIa |
B-NR |
1. Ở các bệnh nhân ICD và bệnh sử SCA hoặc VA dai dẳng ở họ đã lấy bỏ ICD do đòi hỏi (nhiễm trùng), áo khử rung tim mặc là phù hợp cho dự phòng SCD (1-4). |
|
IIb |
B-NR |
2. Ở các bệnh nhân có nguy cơ SCD tăng lên nhưng họ không đủ điều kiện cho ICD, như đang đợi ghép tim, có LVEF 35% hoặc ít hơn trong phạm vi 40 ngày từ khi MI, hoặc NICM mới được chẩn đoán, tái tuần hoàn trong phạm vi 90 ngày, viên cơ tim hoặc bệnh cơ tim thứ phát hoặc nhiễm trùng hệ thống, áo khử rung tim là phù hợp (1-5). |
Tóm tắt
Máy khử rung tim có thể mặc là một dụng cụ giống chiệc áo nỉ được mặc dưới ào thường, nó theo dõi liên tục nhịp tim và phóng ra tự động sốc điện khi có VF hoặc VT được phát hiện. Dụng cụ này được dùng để mặc liên tục, 24 giờ mỗi ngày, trừ khi người mặc đang bồn tắm hoặc vòi sen. Thiết bị khử rung tim có thể mặc được phê duyệt tại Hoa Kỳ do Cơ quan Quản lý Thực phẩm và Dược phẩm Hoa Kỳ dành cho những bệnh nhân “có nguy cơ SCA và không phải là ứng cử viên hoặc từ chối máy khử rung” (6). Tư vấn khoa học từ AHA tóm tắt các dữ liệu và khuyến cáo cho việc sử dụng áo khử rung tim (4). Hiệu quả của áo khử rung tim ghi nhận và khử rung VF được chứng minh trong một số nghiên cứu, mặc dù không có RTCs hỗ trợ sử dụng áo khử rung tim. Trong số 3569 bệnh nhân nhận được thiết bị cho các lý do khác nhau, có ít nhất 1 ngày trong đăng ký nhà sản xuất hở Hoa Kỳ, có 59 trường hợp VT / VF ở 59 bệnh nhân, với tần suất 1,7% / bệnh nhân / năm. Hiệu quả sốc lần đầu tiên là 99%, với tỉ lệ sống sót sau sốc là 90%. Nhìn chung, 2% bệnh nhân đã nhận được sốc không phù hợp (1).
Văn bản Hỗ trợ Riêng biệt – Khuyến cáo
1. Loại bỏ ICD trong một khoảng thời gian, thông thường nhất do nhiễn trùng, làm bệnh nhân đến nguy cơ VT/SCD không được điều trị ngoài trừ theo dõi và tiếp cận khử rung ngoài cấp cứu được duy trì. Trong 1 loạt 354 bệnh nhân nhận được áo khử rung tim, chỉ định do nhiễm trùng 10% (3). Đối với bệnh nhân có bệnh sử SCA hoặc VA kéo dài, áo khử rung tim có thể cho phép bệnh nhân xuất viện về nhà với việc ngăn ngừa VT/SCA đến tận khi tình huống lâm sàng cho phép cấy lại ICD.
2. Các bệnh nhân được liệt kê trong các khuyến cáo này đã đại diện cho các loạt lâm sàng và các đăng ký chứng minh sự an toàn và hiệu quả của áo máy khử rung tim. Bệnh nhân MI mới xẩy ra, NICM mới được chẩn đoán, mới tái tuần hoàn, viêm cơ tim và bệnh cơ tim thứ phát có nguy cơ tăng VT / SCA tăng lên. Tuy nhiên, áo khử rung tim có thể chưa chứng minh lợi ích trong các trạng thái này, một phần do tình hướng lâm sàng có thể chứng minh với điều trị và thởi gian. Ở các bệnh nhân chờ đợi ghép tim, thậm chí với sống sót được mong đợi <1 năm không cần ghép tạng, và phụ thuộc vào các yếu tố lâm sàng như sử dụng thuốc inotrop tĩnh mạch, áo khử rung tim có thể là một sự thay thế cho một ICD.
Tài liệu tham khảo
1. Chung MK. The role of the wearable cardioverter defibrillator in clinical practice. Cardiol Clin. 2014;32:253-70.
2. Chung MK, Szymkiewicz SJ, Shao M, et al. Aggregate national experience with the wearable cardioverter-defibrillator: event rates, compliance, and survival. J Am Coll Cardiol. 2010;56:194-203.
3. Klein HU, Meltendorf U, Reek S, et al. Bridging a temporary high risk of sudden arrhythmic death. Experience with the wearable cardioverter defibrillator (WCD). Pacing Clin Electrophysiol. 2010;33:353-67.
4. Piccini JP Sr, Allen LA, Kudenchuk PJ, et al. Wearable cardioverter-defibrillator therapy for the prevention of sudden cardiac death: a science advisory from the American Heart Association. Circulation. 2016;133:1715-27.
5. Ellenbogen KA, Koneru JN, Sharma PS, et al. Benefit of the wearable cardioverter-defibrillator in protecting patients after implantable-cardioverter defibrillator explant. Results from the National Registry. JACC Clin Electrophysiol. 2017;3:243-50.
6. LifeVest Wearable Cardioverter Defibrillator. Available at: http://www.fda.gov/MedicalDevices/ ProductsandMedicalProcedures/DeviceApprovalsandClearances/Recently-ApprovedDevices/ucm458494.htm. Accessed August 26, 2016.
11.3 Máy khử rung tự động ngoài
Khử rung tim ngoài (AED) có thể cứu sống khi sử dụng trong phạm vi vài phút khởi phát VF. AED là phương pháp có hiệu quả để khử rung cho những người bị ngừng tim ngoài bệnh viện, và do những người đáp ứng đầu tiên sử dụng máy là an toàn và hiệu quả (1-3). Các nỗ lực của chính phủ liên bang đã có hiệu quả trong việc đưa AED vào các sân bay / máy bay và các tòa nhà liên bang, trong khi nhiều nỗ lực khác nhau ở cấp bang và cộng đồng đã có hiệu quả trong việc đặt AED ở nhiều nơi. nhưng không phải tất cả, trường học, các sự kiện thể thao, các khu dân cư mật độ cao, và các sân bay cũng như trong các xe cảnh sát và xe cứu hỏa (4-7). Các giao thức hồi sức có hoặc không có đặt AED được yêu cầu ở hầu hết các tiểu bang dành cho câu lạc bộ thể dục, mặc dù các cơ sở tập luyện thay thế trong nhà có thể có tỷ lệ ngưng tim cao hơn và tăng khả năng sống sót hơn ở các địa điểm công cộng trong nhà khác (8). Trong quần thể nghiên cứu 21 triệu người, sống sót để xuất viện cao gần hai lần khi AED được áp dụng cho ngừng tim ngoài bệnh viện (9). Đặt AED được mởi rộng và phối hợp trong cộng đồng, gồm ở các khu vực địa lý nguy cơ cao như trường hợp và các khu vực thể thao được tổi chức, có thể làm tăng đáng kể tỷ lệ bệnh nhân ngừng tim ngoài bệnh viện họ sẽ nhận được điều trị AED (10). Cơ quan Quản lý Thực phẩm và Dược phẩm Hoa Kỳ đã phê duyệt việc bán lẻ AEDs. Khoảng 70% SCAs xảy ra ở nhà, và tỷ lệ sống sót sau khi xuất viện sau đặt AED bằng các dịch vụ cấp cứu y tế đã thấp hơn một cách có ý nghĩa cho ngừng tim tại nhà (12%) so với các tình huống công cộng (34%) (11). Tuy nhiên, trong một RCT của AEDS, đặt AED ở nhà không cải thiện sự sống còn của bệnh nhân hồi phục từ MI thành trước (12). Khu vực đặt thiết bị phù hợp để giảm thời gian chậm trễ sau khởi phát SCA là rất quan trọng. Ngoài việc phòng ngừa, các thành phần quan trọng của sự sống còn từ SCA gồm sự nhận biết ngay lập tức và hoạt động của hệ đáp ứng cấp cứu, CPR (hồi sức tim phổi) chất lượng cao và sớm, khử rung nhanh chóng đối với nhịp có khả năng đánh sốc (13).
Tài liệu tham khảo
1. Marenco JP, Wang PJ, Link MS, et al. Improving survival from sudden cardiac arrest: the role of the automated external defibrillator. JAMA. 2001;285:1193-200.
2. Priori SG, Bossaert LL, Chamberlain DA, et al. ESC-ERC recommendations for the use of automated external defibrillators (AEDs) in Europe. Eur Heart J. 2004;25:437-5.
3. Blom MT, Beesems SG, Homma PC, et al. Improved survival after out-of-hospital cardiac arrest and use of automated external defibrillators. Circulation. 2014;130:1868-75.
4. Koster RW. Automatic external defibrillator: key link in the chain of survival. J Cardiovasc Electrophysiol. 2002;13:S92-5.
5. Valenzuela TD, Roe DJ, Nichol G, et al. Outcomes of rapid defibrillation by security officers after cardiac arrest in casinos. N Engl J Med. 2000;343:1206-9.
6. Caffrey SL, Willoughby PJ, Pepe PE, et al. Public use of automated external defibrillators. N Engl J Med. 2002;347:1242-7.
7. Page RL, Joglar JA, Kowal RC, et al. Use of automated external defibrillators by a U.S. airline. N Engl J Med. 2000;343:1210-6.
8. Page RL, Husain S, White LY, et al. Cardiac arrest at exercise facilities: implications for placement of automated external defibrillators. J Am Coll Cardiol. 2013;62:2102-9.
9. Weisfeldt ML, Sitlani CM, Ornato JP, et al. Survival after application of automatic external defibrillators before arrival of the emergency medical system: evaluation in the resuscitation outcomes consortium population of 21 million. J Am Coll Cardiol. 2010;55:1713-20.
10.Hansen CM, Lippert FK, Wissenberg M, et al. Temporal trends in coverage of historical cardiac arrests using a volunteer-based network of automated external defibrillators accessible to laypersons and emergency dispatch centers. Circulation. 2014;130:1859-67.
11.Weisfeldt ML, Everson-Stewart S, Sitlani C, et al. Ventricular tachyarrhythmias after cardiac arrest in public versus at home. N Engl J Med. 2011;364:313-21.
12.Bardy GH, Lee KL, Mark DB, et al. Home use of automated external defibrillators for sudden cardiac arrest. N Engl J Med. 2008;358:1793-804.
13.Travers AH, Perkins GD, Berg RA, et al. Part 3: adult basic life support and automated external defibrillation: 2015 International Consensus on Cardiopulmonary Resuscitation and Emergency Cardiovascular Care Science With Treatment Recommendations. Circulation. 2015;132:S51-83.
12. Xem xét chuyên biệt cho triệt phá qua catheter
|
Khuyến cáo cho triệt phá qua catheter Tài liệu tham khảo ủng hộ khuyến cáo được tóm tắt trong tư liệu hỗ trợ onlien 57. |
||
|
COR |
LOE |
Các khuyến cáo |
|
I |
C-LD |
1. Ở các bệnh nhân có VT vào lại nhánh bó, triệt phá qua catheter rất hữu ích để giảm nguy cơ tái phát VT và sốc ICD (1-3). |
|
IIa |
B-NR |
2. Ở các bệnh nhân bệnh tim cấu trúc đã triệt phá dưới nội tâm mạc qua catheter thất bại, triệt phá qua catheter thượng tâm mạc có thể hữu ích để giảm nguy cơ VT đơn hình tái phát (4-6). |
Tóm tắt
VT vào lại nhánh bó do liên quan đến vào lại các nhánh bó. Triệt phá qua catheter là điều trị được ưa thích cho VT này, đã gặp ở < 10% các bệnh nhân với VT đơn hình dai dẳng tái phát và bệnh tim cấu trúc (xem phần 7.2.3).
Văn bản Hỗ trợ Riêng biệt – Khuyến cáo
1. VT vào lại nhánh bỏ có thế xẩy ra ở bất kỳ hình thái nào của bệnh tim kết hợp với dẫn truyền nội His chậm. Cơ chế phổ biến nhất liên quan đến dẫn truyền xuôi qua bó nhánh phải và dẫn ngược qua bó nhánh trái, bằng cách đó tạo ra hình thái QRS blốc nhánh bó trái trong quá trình VT, nó thường nhanh và dung nạp kém. Triệt phá qua catheter nhánh bó phải hoặc trái làm ngắt vòng và thường chữa khỏi (1-3). Sau triệt phá, dẫn truyền nhĩ thất bị suy yếu nặng có thể bị, đòi hỏi phải tạo nhịp vĩnh viễn, có thể có các hậu quả huyết động (4, 6). Nhiều bệnh nhân có VT khác liên quan đến sẹo có thể tạo ra hoặc đáp ứng đủ cho ICD do mức độ nặng của bệnh tim kết hợp.
2. Thất bại trong việc triệt phá qua catheter có thể do khu vực nền rối loạn nhịp ở giữa cơ tim hoặc thượng tâm mạc, và điều này nhiều khả năng hơn ở các bệnh nhân có bệnh cơ tim không do thiếu máu so với bệnh cơ tim thiếu máu cục bộ, và trong bệnh cơ tim thất phải gây loạn nhịp (7-9). Trong thử nghiệm HELP-VT (4), triệt phá thượng tâm mạc đòi hỏi ở 30% bệnh nhân có VT liên quan đến bệnh cơ tim không do thiếu máu cục bộ (NICM) so với 1.2% bệnh nhân có bệnh cơ tim bị thiếu máu cục bộ. QRS rộng với sự líu ríu rõ ràng của phần QRS khởi đầu và phức bộ QS ở các chuyển đạo bên hoặc dưới trong quá trình VT gợi ý vòng ở thượng tâm mạc trong NICM, nhưng ECG không dự báo chính xác khu vực VT thượng tâm mạc ở các bệnh nhân MI trước đó. MRI tim trước thủ thuật và lập bản đồ điện giải phẫu trong khi thủ thuật là công cụ hữu ích để hướng dẫn định khu sẹo thượng tâm mạc có thể là nguồn gốc VT vào lại (8, 10). Sự liên kết thượng tâm mạc ngăn chặn tiếp cận của thu thuật ở một số bệnh nhân, đáng chú ý với nhiều phẫu thuật tim trước đó. Tiếp cận thượng tâm mạc qua da cho lập bản đồ và triệt phá được kết hợp với tần số biến chứng nặng khoảng 5% và chèn ép tim do việc đâm hoặc rách thất phải có thể đòi hỏi ngoại khoa cấp cứu hoặc tổn thương động mạch vành nguy hiểm tính mạng và tổn thương thần kinh hoành có thể xảy ra (11, 12). Kinh nghiệm đã được báo cáo từ các trung tâm tư vấn hạng ba.
Tài liệu tham khảo
1. Blanck Z, Dhala A, Deshpande S, et al. Bundle branch reentrant ventricular tachycardia: cumulative experience in 48 patients. J Cardiovasc Electrophysiol. 1993;4:253-62.
2. Lopera G, Stevenson WG, Soejima K, et al. Identification and ablation of three types of ventricular tachycardia involving the his-purkinje system in patients with heart disease. J Cardiovasc Electrophysiol. 2004;15:52-8.
3. Mehdirad AA, Keim S, Rist K, et al. Long-term clinical outcome of right bundle branch radiofrequency catheter ablation for treatment of bundle branch reentrant ventricular tachycardia. Pacing Clin Electrophysiol. 1995;18:2135-43.
4. Dinov B, Fiedler L, Schonbauer R, et al. Outcomes in catheter ablation of ventricular tachycardia in dilated nonischemic cardiomyopathy compared with ischemic cardiomyopathy: results from the Prospective Heart Centre of Leipzig VT (HELP-VT) study. Circulation. 2014;129:728-36.
5. Tanner H, Hindricks G, Volkmer M, et al. Catheter ablation of recurrent scar-related ventricular tachycardia using electroanatomical mapping and irrigated ablation technology: results of the prospective multicenter Euro-VT-study. J Cardiovasc Electrophysiol. 2010;21:47-53.
6. Marchlinski FE, Haffajee CI, Beshai JF, et al. Long-term success of irrigated radiofrequency catheter ablation of sustained ventricular tachycardia: post-approval THERMOCOOL VT trial. J Am Coll Cardiol. 2016;67:674-83.
7. Assomull RG, Prasad SK, Lyne J, et al. Cardiovascular magnetic resonance, fibrosis, and prognosis in dilated cardiomyopathy. J Am Coll Cardiol. 2006;48:1977-85.
8. Bogun FM, Desjardins B, Good E, et al. Delayed-enhanced magnetic resonance imaging in nonischemic cardiomyopathy: utility for identifying the ventricular arrhythmia substrate. J Am Coll Cardiol. 2009;53:1138-45.
9. Roberts WC, Siegel RJ, McManus BM. Idiopathic dilated cardiomyopathy: analysis of 152 necropsy patients. Am J Cardiol. 1987;60:1340-55.
10.Piers SR, Tao Q, van Huls van Taxis CFB, et al. Contrast-enhanced MRI-derived scar patterns and associated ventricular tachycardias in nonischemic cardiomyopathy: implications for the ablation strategy. Circ Arrhythm Electrophysiol. 2013;6:875-83.
11.Sacher F, Roberts-Thomson K, Maury P, et al. Epicardial ventricular tachycardia ablation a multicenter safety study. J Am Coll Cardiol. 2010;55:2366-72.
12.Della Bella P, Brugada J, Zeppenfeld K, et al. Epicardial ablation for ventricular tachycardia: a European multicenter study. Circ Arrhythm Electrophysiol. 2011;4:653-9.
Xem tiếp trong kỳ sau…







