Ts. Bs. Võ Tuấn Anh1
Bs. Nguyễn Thị Lệ Trang2
Bs. Nguyễn Thanh Hiền
(1) Phụ trách khoa Ngoại lồng ngực tim mạch BV ĐK Đồng nai.
(2) Khoa nội tim mạch tổng quát BV Nhân dân 115
Danh mục viết tắt:
| ACC | American College of Cardiology: trường môn tim mạch Mỹ |
| AHA | American Heart Association: hội tim mạch Mỹ |
| ASE | American Society of Echocardiography: hội siêu âm Mỹ |
| COAPT | Cardiovascular Outcomes Assessment of the MitraClip Percutaneous Therapy for Heart Failure Patients With Functional Mitral Regurgitation: đánh giá kết cục tim mạch của phương pháp điều trị can thiệp qua da MitraClip cho bệnh nhân suy tim với hở 2 lá chức năng. |
| DSA | Digital Subtraction Angiography: chụp mạch máu xóa nền. |
| EAE | European Association of Echocardiography: hội siêu âm châu Âu |
| ERO
ESC |
Effective Regurgitation Orifice: diện tích hở 2 lá hiệu quả
European Society of Cardiology: hội tim mạch châu Âu |
| GDMT | Guideline – Directed Medical Therapy: điều trị nội khoa theo hướng dẫn |
| LVIDs | Left Ventricular Internal Diameter end systole: đường kính thất trái cuối tâm thu |
| MITRA-FR | Multicentre Study of Percutaneous Mitral Valve Repair MitraClip Device in Patients With Severe Secondary Mitral Regurgitation: nghiên cứ đa trung tâm sửa van 2 lá qua da dụng cụ MitraClip ở bệnh nhân hở 2 lá chức năng nặng. |
| MSCT | Multislice Computer Tomography: CT đa lát cắt |
| P3 | Posteromedial scallop: phần mép sau giữa. |
| PAPs | Pulmonary Artery Systolic Pressure: áp lực tâm thu động mạch phổi |
| RF | Regurgitation Fraction: phân suất phụt ngược (dòng hở) |
| RVol | Regurgitation Volume: thể tích hở |
| SAM | Systolic Anterior Motion: vận động ra trước thì tâm thu |
| STICH | Surgical Treatment for Ischemic Heart Failure trial: thử nghiệm điều trị ngoại khoa bệnh tim thiếu máu cục bộ. |
| VC | Vena Contracta: eo luồng màu |
Mở đầu:
Hở van 2 lá thứ phát (chức năng) trung bình và nặng kèm suy tim chiếm khoảng 1/3 bệnh nhân suy tim và nó làm nặng thêm tình trạng lâm sàng, ảnh hưởng tiên lượng. Hở 2 lá thứ phát là do quá trình tái cấu trúc thất trái hậu quả của bệnh cơ tim thiếu máu cục bộ hay không thiếu máu cục bộ cơ tim dẫn tới không áp sát của các lá van 2 lá bình thường thông qua một s cơ chế. Vì hở hở 2 lá thứ phát về cơ bản là bệnh của thất trái, không phải của van, nên chiến lược điều trị là hướng tới những rối loạn của thất trái. Tuy nhiên, hở 2 lá thứ phát làm nặng thêm tình trạng tái cấu trúc thất trái do quá tải thể tích và điều trị nội khoa theo guideline (GDMT) là bắt buộc để cải thiện triệu chứng và tiên lượng. Điều trị can thiệp bệnh nhân suy tim và hở van 2 lá thứ phát đang thay đổi. Ngược với hở van 2 lá tiên phát, lợi ích của phẫu thuật sửa van 2 lá ở bệnh nhân hở 2 lá thứ phát đơn độc hay kèm phẫu thuật bắc cầu vẫn là một dấu hỏi. Gần đây, kỹ thuật sửa hở van 2 lá thứ phát qua ống thông (Transcatheter) được thực hiện trên một phổ rộng bệnh nhân và mang lại lợi ích, mặc dù vẫn cần nghiên cứu thêm. Với nhiều tiến bộ về hiểu biết sinh lý bệnh của bệnh, các phương pháp đánh giá và các phương pháp điều trị can thiệp mới, cũng như xác định những nhóm bệnh nhân có lợi nhất để lựa chọn can thiệp điều trị, chiến lược điều trị hở van 2 lá cũng đã có nhiều thay đổi. Bài viết này sẽ cập nhật những quan điểm mới nhất trong chẩn đoán và điều trị hở van 2 lá thứ phát hiện nay [3].
- Đại cương:
- Định nghĩa:
Hở van hai lá thứ phát được định nghĩa là khi có sự hiện diện của tình trạng hở van hai lá nhưng các lá van và dây chằng của van hai lá có cấu trúc bình thường.[9]
- Tần suất:
Hở van hai lá là bệnh lý phổ biến nhất trong số các bệnh van tim. Hở van hai lá nói chung có tần suất dưới 1% trên dân số dưới 55 tuổi, nhưng tần suất này sẽ tăng lên với mỗi mười tuổi và lên đến 9% trên dân số trên 75 tuổi (Hình 1.1)[6].
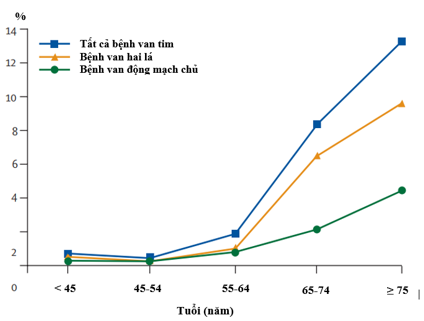
Hình 1.1: Tần suất bệnh van tim trung bình và nặng theo tuổi.
“Nguồn: Vuyisile T Nkomo, 2006” [6]
Trong một nghiên cứu thực hiện trên dân số Mỹ năm 2020 về tỉ lệ hở van hai lá dựa trên bảng phân loại của Carpentier, hở van hai lá thứ phát được xếp vào nhóm IIIb. Kết quả nghiên cứu cho thấy có từ 2 triệu đến 2,5 triệu dân bị hở van hai lá. Hở van hai lá thứ phát do rối loạn chức năng thất trái nói chung chiếm 16.250 người trong mỗi triệu dân, trong đó hở van hai lá thứ phát do bệnh cơ tim thiếu máu chiếm từ 7.500 đến 9.000 người trong mỗi triệu dân, hở van hai lá thứ phát do bệnh cơ tim giãn nở chiếm 160 người trong mỗi triệu dân.[4]
- Nguyên nhân và cơ chế:
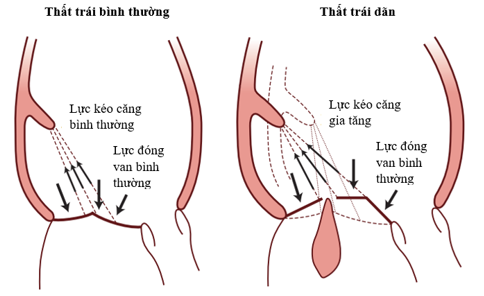
Hình1.2: Cơ chế gây hở van hai lá thứ phát.
“Nguồn: Grayburn, 2020” [5]
Bộ máy van hai lá bao gồm lá van, vòng van, dây chằng van, cơ nhú. Trong thì tâm thu, thất trái co, đẩy dòng máu ra khỏi đường thoát thất trái vào động mạch chủ, đồng thời đẩy van hai lá về phía nhĩ. Lực đẩy này được gọi là lực đóng van. Cùng lúc đó, cơ nhú bám vào thất trái làm điểm tựa kéo căng các dây chằng van, tạo nên lực đối trọng với lực đóng van hai lá, gọi là lực kéo căng. Bình thường, lực kéo căng và lực đóng van hai lá cân bằng nhau, giúp van hai lá đóng kín trong thì tâm thu (Hình1.2). Vòng van hai lá là điểm bám của các lá van, cũng đóng vai trò quan trọng trong việc giữ cho van hai lá đóng kín. Bất kỳ nguyên nhân gì gây ra rối loạn sự cân bằng trên cũng sẽ gây hở van hai lá.[5]
Hở van hai lá thứ phát có thể gặp trong những trường hợp sau:[5]
- Bệnh cơ tim thiếu máu.
- Bệnh cơ tim không thiếu máu:
- Bệnh cơ tim giãn nở.
- Bệnh cơ tim phì đại.
- Bệnh cơ tim hạn chế.
- Rung nhĩ.
Trong bệnh cơ tim thiếu máu, hình dáng và vận động của thất trái bị thay đổi khu trú hoặc toàn bộ, dẫn đến sự thay đổi vị trí các cơ nhú và hướng của lực kéo, khiến một phần hoặc toàn bộ các lá van bị kéo căng, đồng thời vòng van bị giãn khiến các lá van không áp tốt [9]. Thất trái trong bệnh cơ tim giãn nở giãn dạng hình cầu, vòng van giãn và các cơ nhú bị đưa ra xa làm toàn bộ van hai lá bị kéo căng, điểm áp của lá van lúc này nằm xa về phía thất thay vì ngay dưới vòng van như bình thường, dẫn đến hở van hai lá. Trong trường hợp bệnh cơ tim hạn chế và rung nhĩ, chức năng tâm thu thất trái thường được bảo tồn, hở van hai lá gây ra chủ yếu do giãn nhĩ trái kèm theo giãn vòng van hai lá. Hở van hai lá trong bệnh cơ tim phì đại do một cơ chế đặc biệt. Dòng máu đi ra khỏi đường thoát thất trái bị uốn cong về phía buồng nhận do phì đại của đường thoát thất trái đã đẩy lá van hai lá về phía đường thoát thất trái, gây ra hiện tượng SAM và hở van hai lá.[5]
- Lượng giá:
- Chẩn đoán:
Về lâm sàng, bệnh nhân bị hở van hai lá thứ phát thường có biểu hiện mệt mỏi, khó thở khi gắng sức, giảm khả năng gắng sức. Tuy nhiên những triệu chứng này khó có thể kết luận là do bệnh tim nền, hở van hai lá thứ phát, hay các bệnh đi kèm như bệnh phổi tắc nghẽn mạn tính, suy nhược gây ra. Khi thăm khám, âm thổi toàn tâm thu điển hình thường cũng không hiện diện.[5]
Siêu âm tim qua thành ngực là công cụ đầu tay giúp chẩn đoán hở van hai lá thứ phát, lượng giá độ nặng, xác định nguyên nhân và theo dõi điều trị. Trên siêu âm tim sẽ thấy các lá van và dây chằng van bình thường hoặc dày nhẹ. Một phần hoặc toàn bộ lá van bị kéo căng về phía thất trái, nhất là lá sau khiến diện áp lá van bị đưa ra xa khỏi vòng van về phía thất. Lá sau bị kéo căng nhiều hơn lá trước, khiến cho vùng diện áp của lá trước chồm lên lá sau tạo hình ảnh giả sa lá trước, cần lưu ý để tránh nhầm lẫn khi siêu âm. Dòng hở có thể trung tâm hoặc lệch tâm. Kèm theo là những hình ảnh cho thấy sự biến đổi cấu trúc, chức năng của thất trái, vòng van, nhĩ trái.[11]
Hở van hai lá thứ phát trên siêu âm tim được chia làm hai dạng: Đối xứng (symetric) và không đối xứng (asymetric).[5, 11]
- Dạng đối xứng gặp trong nhồi máu cơ tim vùng trước rộng, nhồi máu cơ tim đa vùng, bệnh cơ tim thiếu máu. Vòng van giãn và phẳng, thất trái giãn dạng cầu, chỉ số cầu thất trái tăng. Cả hai lá van đều bị kéo căng về phía thất trái. Có thể thấy lá trước dạng cánh chim hải âu (Seagull sign). Dòng hở thường ở vị trí trung tâm lá van (hình 2.1).
- Dạng không đối xứng gặp trong nhồi máu cơ tim vùng sau dưới hoặc thành bên. Vòng van giãn ít, không đối xứng. Thất trái giãn khu trú tại thành sau dưới hoặc thành bên, thường chỉ giãn phần đáy. Lá van bị kéo căng chủ yếu ở lá sau, thường khu trú tại P3 hoặc nặng nhất tại P3. Dòng hở chủ yếu nằm tại vị trí P3. Một số trường hợp có thể ghi nhận hai dòng hở riêng biệt, bắt chéo nhau (hình 2.2).
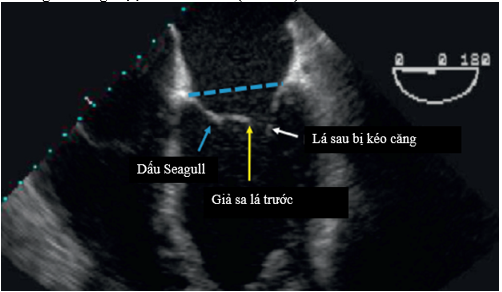
Hình 2.1: Những đặc điểm siêu âm của hở van hai lá thứ phát.
“Nguồn: Grayburn, 2020” [5]
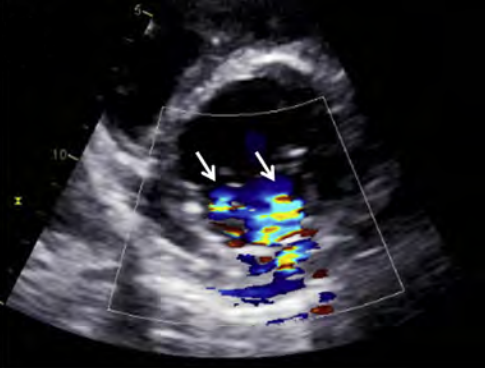
Hình 2.2: Hở van hai lá thứ phát, hai dòng hở nằm tại P3 và trung tâm.
“Nguồn: ASE, 2017”[11]
- Đánh giá độ nặng:
Tiêu chuẩn để lượng giá độ nặng hở van hai lá thứ phát cho đến thời điểm này vẫn còn là vấn đề tranh cãi. Nếu so sánh với hở van hai lá nguyên phát, hở van 2 lá thứ phát có thể có tiên lượng xấu hơn mặc dù diện tích hở van hiệu quả (ERO) thấp hơn. Phương pháp đo ERO cũng có thể đưa ra trị số đo đạc thấp hơn so với ERO thực tế vì trong hở van hai lá thứ phát, ERO thường không có dạng tròn (hình 2.3). Tuy nhiên theo khuyến cáo mới nhất của ACC/AHA (2020), các tiêu chuẩn định nghĩa hở van hai lá thứ phát nặng trùng với tiêu chuẩn định nghĩa hở van hai lá nguyên phát nặng.[9]
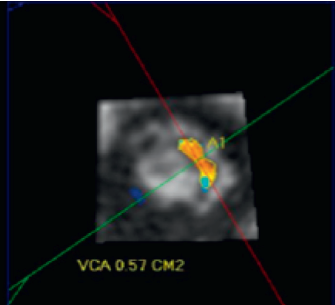
Hình 2.3: ERO không có dạng tròn của hở van hai lá thứ phát.
“Nguồn: Grayburn, 2020”[5]
Trên lâm sàng, bệnh nhân bị hở van hai lá thứ phát được phân giai đoạn dựa theo khuyến cáo của ACC/AHA 2020 như bảng 2.1.[9]
Bên cạnh đó, để tiên lượng khả năng sửa van thành công, khi chuẩn bị bệnh nhân cần đo đạc thêm các chỉ số sau:
- Diện tích lều (Tenting area): Đo trên mặt cắt 3 buồng từ mỏm hoặc mặt cắt trục dọc cạnh ức vào giữa tâm thu. Được tính bằng diện tích hình tạo bởi lá trước, lá sau và đoạn thẳng nối hai điểm vòng van (Hình 2.4).
- Khoảng cách cơ nhú sau – vòng sợi (Posterior papillary – fibrosa distance): Đo trên mặt cắt 3 buồng từ mỏm vào giữa tâm thu. Được tính bằng khoảng cách giữa đỉnh cơ nhú sau trong và vòng van lá trước (Hình 2.5).
- Chiều cao lều (Tenting height)/Khoảng cách diện áp (Coaptation distance): Đo trên mặt cắt 4 buồng từ mỏm vào giữa tâm thu. Được tính bằng chiều cao của điểm áp hai lá van khi hạ vuông góc xuống đường thẳng nối hai điểm vòng van (Hình 2.6).
- Góc sau bên (Posterolateral angle): Đo trên mặt cắt 4 buồng từ mỏm vào giữa thì tâm thu. Được tính bằng góc tạo bởi lá sau và đường thẳng nối hai điểm vòng van (Hình 2.7).
- Chỉ số cầu tâm thu (Systolic sphericity index): Đo trên mặt cắt 4 buồng từ mỏm vào cuối tâm thu. Là tỉ số đường kính ngang lớn nhất với chiều dài thất trái (đoạn thẳng nối mỏm tim – điểm giữa đoạn thẳng nối hai điểm vòng van) (Hình 2.8).
- Khoảng cách hai cơ nhú (Interpapillary muscle distance): Đo trên mặt cắt trục ngang qua hai cơ nhú vào đầu tâm thu. Được tính bằng khoảng cách giữa hai cơ nhú (Hình 2.9).
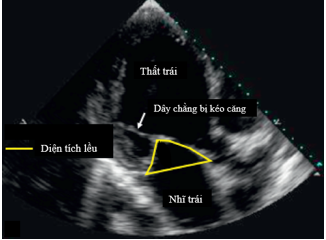
Hình 2.4: Cách đo diện tích lều.
“Nguồn: Grayburn, 2020”[5]
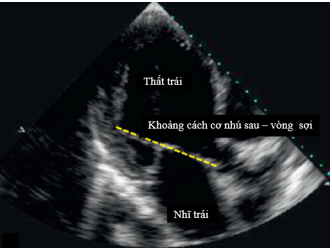
Hình 2.5: Cách đo khoảng cách cơ nhú sau – vòng sợi.
“Nguồn: Grayburn, 2020”[5]
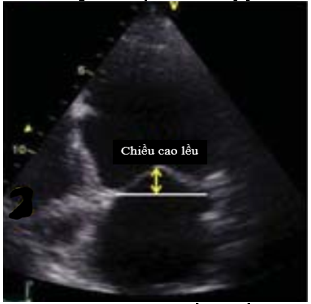
Hình 2.6: Cách đo chiều cao lều.
“Nguồn: EAE, 2010”[13]
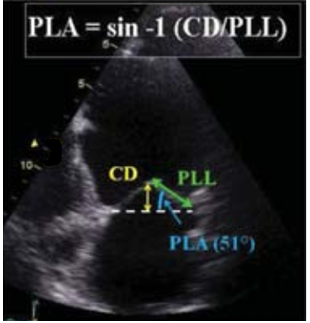
Hình 2.7: Cách đo góc sau bên. (CD: Coaptation distance, PLL: Posterolateral Leaflet, PLA: Posterolateral Area)
“Nguồn: EAE,2010”[13]
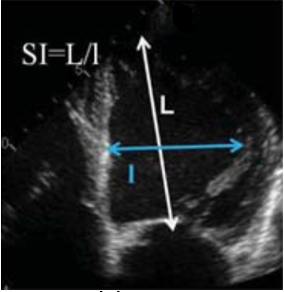
Hình 2.8: Cách đo chỉ số cầu tâm thu. (SI: Sphericity Index)
“Nguồn: EAE, 2010”[13]
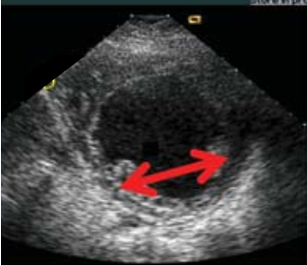
Hình 2.9: Cách đo khoảng cách hai cơ nhú.
“Nguồn: EAE, 2010”[13]
Các yếu tố tiên lượng sửa van khó bao gồm [13]:
- Khoảng cách diện áp ≥
- Diện tích lều > 2,5 – 3 cm2.
- Dòng hở phức tạp.
- Góc sau bên > 450.
- Khoảng cách hai cơ nhú > 20 mm.
- Khoảng cách cơ nhú sau – vòng sợi > 40mm
- Bất thường vận động vùng thành bên thất trái.
- Đường kính thất trái cuối tâm trương> 65 mm, đường kính thất trái cuối tâm thu > 51 mm, thể tích thất trái cuối tâm thu> 140 mL.
- Chỉ số cầu tâm thu > 0,7.
Bảng 2.1: Phân giai đoạn của bệnh nhân bị hở van hai lá thứ phát.
“Nguồn: ACC/AHA, 2020”[9]
| Giai đoạn | Định nghĩa | Giải phẫu van | Huyết động qua van | Tổn thương tim đi kèm | Triệu chứng |
| A | Có nguy cơ hở van hai lá | Lá van, dây chằng, vòng van bình thường.
Bệnh nhân có bệnh mạch vành hoặc bệnh cơ tim. |
Không có dòng hở van hai lá hoặc hiện diện dòng hở trung tâm có diện tích < 20% diện tích nhĩ trái, VC < 0,3 cm. | Thất trái không giãn hoặc giãn nhẹ hoặc có rối loạn vận động vùng.
Bệnh cơ tim nguyên phát có thất trái giãn và chức năng tâm thu thất trái giảm. |
Suy tim hoặc các triệu chứng liên quan đến thiếu tưới máu mạch vành, đáp ứng với điều trị tái thông mạch máu và điều trị nội khoa thích hợp. |
| B | Hở van hai lá tiến triển | Có rối loạn vận động vùng, lá van bị kéo căng nhẹ.
Giãn vòng van, mất diện áp trung tâm của van mức độ nhẹ. |
ERO < 0,4 cm2
RVol< 60 mL RF < 50% |
Rối loạn vận động vùng kèm theo chức năng tâm thu thất trái giảm.
Thất trái giãn và giảm chức năng tâm thudo bệnh cơ tim nguyên phát |
Suy tim hoặc các triệu chứng liên quan đến thiếu tưới máu mạch vành, đáp ứng với điều trị tái thông mạch máu và điều trị nội khoa thích hợp. |
| C | Hở van hai lá nặng không triệu chứng | Có rối loạn vận động vùng và/hoặc giãn thất trái, van hai lá bị kéo căng nặng.
Giãn vòng van, mất diện áp trung tâm của van mức độ nặng. |
ERO ≥ 0,4 cm2
RVol≥ 60 mL RF ≥ 50% |
Rối loạn vận động vùng kèm theo chức năng tâm thu thất trái giảm.
Thất trái giãn và giảm chức năng tâm thudo bệnh cơ tim nguyên phát |
Suy tim hoặc các triệu chứng liên quan đến thiếu tưới máu mạch vành, đáp ứng với điều trị tái thông mạch máu và điều trị nội khoa thích hợp. |
| D | Hở van hai lá nặng có triệu chứng | Có rối loạn vận động vùng và/hoặc giãn thất trái, van hai lá bị kéo căng nặng.
Giãn vòng van, mất diện áp trung tâm của van mức độ nặng. |
ERO ≥ 0,4 cm2
RVol≥ 60 mL RF ≥ 50% |
Rối loạn vận động vùng kèm theo chức năng tâm thu thất trái giảm.
Thất trái giãn và giảm chức năng tâm thudo bệnh cơ tim nguyên phát |
Triệu chứng suy tim liên quan đến hở van hai lá, vẫn tồn tại sau điều trị tái thông mạch máu và nội khoa thích hợp.
Giảm khả năng gắng sức. Khó thở khi gắng sức. |
- Điều trị:
Cho đến nay, vẫn chưa có phương án nào là tối ưu trong điều trị hở van hai lá thứ phát bởi vì trong trường hợp này, hở van 2 lá chỉ là một phần trong phức hợp bệnh lý và sự phục hồi chức năng van hai lá trong trường hợp này không đóng vai trò điều trị nguyên nhân[9]. Quyết định lựa chọn phương pháp điều trị tối ưu nên được đưa ra sau khi đã có sự hội chẩn đội nhóm tim mạch bao gồm bác sĩ Nội Tim mạch, bác sĩ Can thiệp Tim mạch, bác sĩ Ngoại Tim mạch [3, 7].
- Điều trị nội khoa:
Hở van hai lá thứ phát thường là hậu quả của rối loạn chức năng tâm thu thất trái, do đó điều trị theo phác đồ hướng dẫn điều trị suy tim tiêu chuẩn (GDMT) vẫn giữ vai trò chính trong điều trị hở van hai lá thứ phát.
Khuyến cáo điều trị hở van 2 lá thứ phát dựa trên nhiều yếu tố, bao gồm phân loại (từ thất hay từ nhĩ), mức độ nặng, tình trạng huyết động; bệnh kèm theo, kinh nghiệm và chuyên môn của đội ngũ bác sĩ. Guideline hướng dẫn ưu tiên điều trị nội khoa trên bệnh nhân suy tim có chức năng thất trái giảm và hở 2 lá thứ phát, và cần được theo dõi bởi bác sĩ tim mạch. Những thử nghiệm ngẫu nhiên bao gồm những bệnh nhân suy tim có EF giảm cho thấy có cải thiện về chức năng và tỉ lệ sống còn khi dùng beta-blockers, ACEI, ức chế thụ thể Aldosterone, ARNI, SGLT-2i. Việc điều chỉnh liều lượng và kết hợp các thuốc trên tuỳ thuộc vào đáp ứng lâm sàng có thể diễn ra từ vài tuần đến vài tháng.
Tái đồng bộ thất có thể cải thiện chức năng thất trái, giảm kích thước thất trái, và giảm mức độ hở 2 lá chọn lọc trên một số bệnh nhân có suy tim EF giảm và block nhánh trái hoàn toàn, QRS ≥ 150 msc. Trên bệnh nhân hở 2 lá liên quan đến rung nhĩ, chuyển nhịp và duy trì xoang có thể cải thiện độ lớn nhĩ, vòng van, và mức độ hở van. Mặt khác cũng cần điều trị giảm lipid máu, giảm nguy cơ đột tử (đặt ICD), và giảm nguy cơ đột quỵ (dùng kháng đông trên bệnh nhân rung nhĩ).
- Can thiệp nội mạch:
Đối với bệnh nhân hở van hai lá thứ phát, nếu triệu chứng lâm sàng không cải thiện sau khi đã tối ưu điều trị nội khoa theo GDMT, can thiệp hoặc phẫu thuật van hai lá sẽ được đặt ra nhằm mục đích cải thiện triệu chứng và kéo dài thời gian sống còn (14, 15). Chỉ định can thiệp hay phẫu thuật sẽ dựa trên từng trường hợp cụ thể và được tóm tắt trong sơ đồ 1. [9].
Can thiệp nội mạch được chỉ định khi bệnh nhân hở van hai lá nặng có triệu chứng không cải thiện với điều trị suy tim tối ưu và nguy cơ phẫu thuật cao đồng thời có giải phẫu van phù hợp để thực hiện can thiệp. Có nhiều phương pháp và dụng cụ can thiệp nội mạch được áp dụng cho van hai lá như: Thu nhỏ vòng van trực tiếp (Mitralign, Guidant, Guided delivery system, Millipede, ValtechCardio), thu nhỏ vòng van gián tiếp (I-Coapsys, Ample PS3), tạo hình xoang vành (Monarc, Viacor, ReCor, Carillon), sửa van hai lá qua da (MitraClip, Mobius, Neochord, Thermocool, Percu-Pro), thay van hai lá qua da (Endovalve-Herrmann, CardiaAQ, Mitraltech, Lutter, Medtronic). Phương pháp được sử dụng phổ biến hiện nay và đã được áp dụng tại Việt Nam là sửa van hai lá qua da sử dụng dụng cụ MitraClip [3].
Có hai thử nghiệm lâm sàng ngẫu nhiên lớn về MitraClip đã được công bố là MITRA-FR và COAPT. Kết quả của thử nghiệm MITRA-FR cho thấy MitraClip kết hợp với điều trị nội khoa không giảm tiên lượng tử vong so với điều trị nội khoa đơn thuần. Ngược lại kết quả của thử nghiệm COAPT cho thấy MitraClip kết hợp với điều trị nội khoa làm giảm tỉ lệ nhập viện và tử vong so với điều trị nội khoa đơn thuần. Tuy nhiên đặc điểm bệnh nhân của hai thử nghiệm có một số khác biệt, những bệnh nhân trong thử nghiệm COAPT có thể tích thất trái trung bình nhỏ hơn và mức độ hở van hai lá nặng hơn so với những bệnh nhân trong thử nghiệm MITRA-FR. Điều đó gợi ý rằng việc lựa chọn bệnh nhân đóng vai trò nhất định trong hiệu quả can thiệp.[8, 10]
- Phẫu thuật:
Phẫu thuật là phương án được ưu tiên nếu bệnh lý tim nền dẫn đến hở van hai lá có thể giải quyết bằng phẫu thuật như bệnh lý mạch vành, rung nhĩ, bệnh cơ tim phì đại. Khi đó, phẫu thuật sửa hoặc thay van hai lá sẽ là phẫu thuật đi kèm với các phẫu thuật trên.
Marek A. Deja và cộng sự tiến hành thử nghiệm đa trung tâm (STICH trial) so sánh tiên lượng tử vong giữa nhóm bệnh nhân được phẫu thuật van hai lá kèm theo phẫu thuật bắc cầu mạch vành so với nhóm không được phẫu thuật van hai lá kèm theo phẫu thuật bắc cầu mạch vành (van hai lá hở trung bình hoặc hở nặng). Với thời gian theo dõi trung vị là 56 tháng với tổng thời gian theo dõi là 6 năm, kết quả cho thấy nhóm được phẫu thuật van hai lá đi kèm với phẫu thuật bắc cầu mạch vành có tỉ lệ tử vong thấp hơn có ý nghĩa thống kê.[12]
Anthony W. Castleberry tiến hành phân tích hồi cứu từ cơ sở dữ liệu của trung tâm y khoa đại học Duke, Hoa Kỳ về những bệnh nhân bị hở van hai lá trung bình hoặc nặng và có hẹp mạch vành nặng từ năm 1990 đến năm 2009. Các bệnh nhân được chia làm 3 nhóm: Điều trị nội khoa, can thiệp mạch vành, phẫu thuật bắc cầu mạch vành không kèm phẫu thuật van hai lá và phẫu thuật bắc cầu mạch vành kèm theo phẫu thuật van hai lá. Kết quả cho thấy, nhóm phẫu thuật có tỉ lệ sống còn cao hơn có ý nghĩa thống kê so với nhóm điều trị nội khoa và nhóm can thiệp mạch vành. Tuy nhiên trong nhóm phẫu thuật thì việc phẫu thuật van 2 lá đi kèm phẫu thuật mạch vành chưa chứng minh được khả năng làm tăng tỉ lệ sống còn có ý nghĩa thống kê so với nhóm không phẫu thuật van hai lá đi kèm.[2]
Thông thường van hai lá sẽ được sửa bằng cách đặt vòng van. Sự lựa chọn loại vòng van phụ thuộc vào vòng van giãn đối xứng hay không đối xứng. Tuy nhiên, trong tất cả các trường hợp, nguyên tắc xác định kích thước vòng van nhân tạo không thay đổi, đều dựa trên việc đo kích thước bề mặt của lá trước. Việc khâu vòng van tự nhiên vào vòng van nhân tạo đòi nhiều lưu ý kỹ thuật phức tạp để có thể đạt được kết quả như ý (hình 3.1)[1].
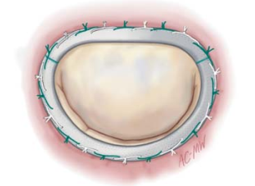
Hình 3.1: Phương pháp đặt vòng van hai lá.
“Nguồn: Carpentier, 2010” [1]
Bên cạnh việc tạo hình lại vòng van, trong một số trường hợp, bác sĩ phẫu thuật còn phải thực hiện thêm một số kỹ thuật khác như mở rộng lá sau, cắt dây chằng thứ cấp, tạo hình lại thất trái và cơ nhú, di chuyển vị trí cơ nhú để cải tạo tốt hơn độ kín của van (hình 3.2).[1]
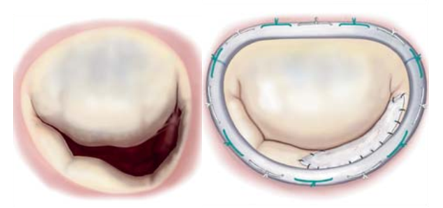
Hình 3.2: Tạo hình vòng van hai lá kèm mở rộng lá sau bằng màng ngoài tim (Trái: Trước khi sửa van; Phải: Sau khi sửa van).
“Nguồn: Carpentier, 2010”[1]
Lựa chọn sửa van hai lá hay thay van hai lá phụ thuộc nhiều vào quyết định và kinh nghiệm của bác sĩ phẫu thuật tim. Các thông tin về yếu tố ảnh hưởng đến tiên lượng sửa van khó trên siêu âm tim sẽ góp phần định hướng cho bác sĩ phẫu thuật tim về quyết định sửa van hay thay van. Thông thường sửa van được ưu tiên lựa chọn vì có thể bảo tồn được hệ thống dây chằng van, giúp giảm nguy cơ suy tim nặng thêm sau phẫu thuật. Trong trường hợp phải thay van, các bác sĩ phẫu thuật cũng sẽ cố gắng giữ lại tối đa lượng dây chằng có thể.
Đối với những bệnh lý tim nền dẫn đến hở van hai lá không thể giải quyết bằng phẫu thuật (hở hai lá thứ phát không do bệnh tim thiếu máu cục bộ), phẫu thuật van hai lá trong trường hợp này vẫn chưa có bằng chứng có thể cải thiện tiên lượng tử vong. Phẫu thuật van hai lá đơn thuần có thể được đặt ra để giúp cải thiện triệu chứng khi phân suất tống máu còn bảo tồn và triệu chứng nặng không đáp ứng với điều trị nội khoa tối ưu.[5]
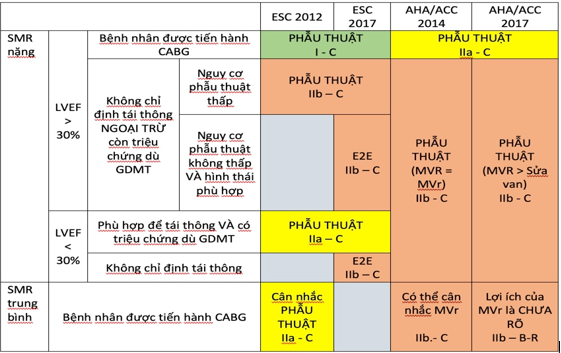
Hình 3.3 và 3.4 giới thiệu hướng dẫn điều trị mới hở van hai lá thứ phát từ hội tim mạch châu Âu và Mỹ.
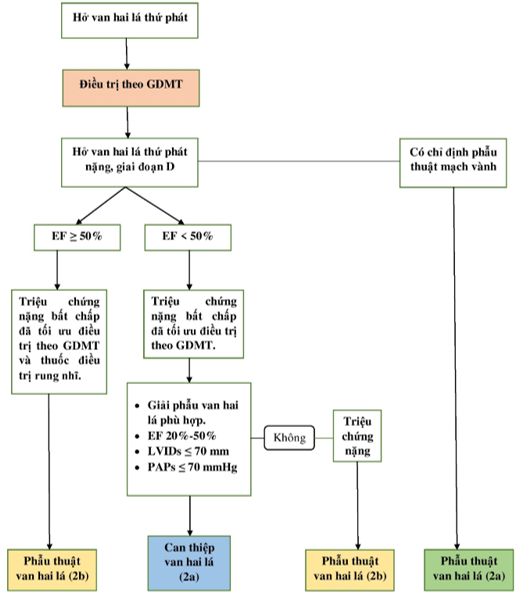
Sơ đồ 3.1: Chỉ định điều trị hở van hai lá thứ phát.
“ Nguồn: ACC/AHA, 2020”[9]
Hình 3.3. Tiến triển hướng dẫn điều trị hở 2 lá thứ phát của hội tim mạch Mỹ và Châu Âu. CABG: phẫu thuật bắc cầu mạch vành. GDMT, điều trị nội khoa theo hướng dẫn. LVEF, phân suất tống máu thất trái. MR, hở van 2 lá. MVR, thay van 2 lá. OMM, đều trị nội khoa tối ưu. SMR, hở 2 lá thứ phát [16].
- Kết luận
Trong vài thập niên qua, chúng ta đã có nhiều tiến bộ trong hiểu biết về hở van 2 lá thứ phát cũng như xác định được những phân nhóm bệnh nhân có lợi trong điều trị hơn. Hở 2 lá thứ phát có tiên lượng xấu và có liên quan trực tiếp với độ nặng của hở van. Vai trò của điều trị phẫu thuật vẫn còn nhiều tranh cãi vì các nghiên cứu gần đây chưa đủ chứng minh hiệu quả. Ngược lại, điều trị can thiệp đã được xác định có vai trò trong điều trị hở van 2 lá nặng thứ phát. Các thử nghiệm ngẫu nhiên đối đầu có kiểm soát cho thấy rằng lợi ích chỉ có ở quần thể bệnh nhân lựa chọn chính xác.
Trong khi chờ các kết quả nghiên cứu mới, các hướng dẫn mới đây của Mỹ 2020 và châu Âu 2021 rất được kỳ vọng và tập trung vào những điểm chính sau:
- Suy tim với hở 2 lá thứ phát là bệnh lý nặng kèm tiên lượng xấu với tiến triển xấu đi theo độ nặng của hở 2 lá.
- GDMT bao gồm tái đồng bộ thất và tái tưới máu cơ tim phải là bước điều trị đầu tiên ở bất kỳ bệnh nhân hở van 2 lá.
- Phẫu thuật van 2 lá cùng với tái tưới máu bằng phẫu thuật (CABG) được đề nghị bởi guideline hiện nay, nhưng chúng ta cần hiểu rằng, chưa có nghiên cứu nào đủ mạnh về chỉ định này.
- Với bệnh nhân ở 2 lá không do bệnh tim thiếu máu cục bộ, lợi ích của điều trị ngoại khoa hở 2 lá thứ phát còn chưa được khẳng định, vì vậy, nó chỉ hạn chế rất ít trong các trường hợp: (i) khi kết hợp với thủ thuật ngoại khoa khác ở bệnh nhân hở 2 lá có ý nghĩa hay (ii) khi các thủ thuật khác không thể thực hiện được và chức năng thất trái không quá thấp hoặc (iii) như là biện pháp thay thế cho ghép tim hay dùng hỗ trợ cơ học dài hạn.
- Ở bệnh nhân chống chỉ định ngoại khoa, COAPT cho thấy điều trị hở 2 lá thứ phát có thể cứu sống và cải thiện chất lượng cuộc sống ở nhóm bệnh nhân hở 2 lá nhất định. COAPT và MITRA.FR khẳng định rằng, kỹ thuật MitraClip là an toàn và hiệu quả làm giảm độ nặng hở van và tốt hơn hầu hết các phẫu thuật ngoại khoa với kỹ thuật góc-tới-góc (the edge-to-edge) và là kỹ thuật đặc biệt thích hợp cho điều trị bệnh này.
Tài liệu tham khảo
- Carpentier Alain (2010), “Techniques in Type IIIb: Systolic Restricted Leaflet Motion“, Carpentier’s Reconstructive Valve Surgery. Saunders Elsevier. 149-156.
- Castleberry A. W., J. B. Williams, M. A. Daneshmand, et al. (2014), “Surgical revascularization is associated with maximal survival in patients with ischemic mitral regurgitation: a 20-year experience”, Circulation, 129 (24), 2547-56.
- Coats A. J. S., S. D. Anker, A. Baumbach, et al. (2021), “The management of secondary mitral regurgitation in patients with heart failure: a joint position statement from the Heart Failure Association (HFA), European Association of Cardiovascular Imaging (EACVI), European Heart Rhythm Association (EHRA), and European Association of Percutaneous Cardiovascular Interventions (EAPCI) of the ESC”, Eur Heart J, 42, 1254–1269.
- de Marchena E., A. Badiye, G. Robalino, et al. (2011), “Respective prevalence of the different carpentier classes of mitral regurgitation: a stepping stone for future therapeutic research and development”, J Card Surg, 26 (4), 385-92.
- Grayburn Paul A. (2020), “Secondary (Funtional) Mitral Regurgitation in Ischemic and Dilated Cardiomyopathy“, Valvular heart disease – a companion to Braunwald’s heart disease, C.M. Otto and R.O. Bonow, Editors., Elsevier. 354-369.
- Nkomo V. T., J. M. Gardin, T. N. Skelton, et al. (2006), “Burden of valvular heart diseases: a population-based study”, Lancet, 368 (9540), 1005-11.
- O’Gara P. T., P. A. Grayburn, V. Badhwar, et al. (2017), “2017 ACC Expert Consensus Decision Pathway on the Management of Mitral Regurgitation: A Report of the American College of Cardiology Task Force on Expert Consensus Decision Pathways”, J Am Coll Cardiol, 70 (19), 2421-2449.
- Obadia J. F., D. Messika-Zeitoun, G. Leurent, et al. (2018), “Percutaneous Repair or Medical Treatment for Secondary Mitral Regurgitation”, N Engl J Med, 379 (24), 2297-2306.
- Otto C. M., R. A. Nishimura, R. O. Bonow, et al. (2021), “2020 ACC/AHA Guideline for the Management of Patients With Valvular Heart Disease: A Report of the American College of Cardiology/American Heart Association Joint Committee on Clinical Practice Guidelines”, Circulation, 143 (5), e72-e227.
- Stone G. W., J. Lindenfeld, W. T. Abraham, et al. (2018), “Transcatheter Mitral-Valve Repair in Patients with Heart Failure”, N Engl J Med, 379 (24), 2307-2318.
- Zoghbi W. A., D. Adams, R. O. Bonow, et al. (2017), “Recommendations for Noninvasive Evaluation of Native Valvular Regurgitation: A Report from the American Society of Echocardiography Developed in Collaboration with the Society for Cardiovascular Magnetic Resonance”, J Am Soc Echocardiogr, 30 (4), 303-371.
- Deja M. A., P. A. Grayburn, B. Sun, et al. (2012), “Influence of mitral regurgitation repair on survival in the surgical treatment for ischemic heart failure trial”, Circulation, 125 (21), 2639-48.
- Lancellotti P., L. Moura, L. A. Pierard, et al. (2010), “European Association of Echocardiography recommendations for the assessment of valvular regurgitation. Part 2: mitral and tricuspid regurgitation (native valve disease)”, Eur J Echocardiogr, 11 (4), 307-32.
- Cammertoni. F et al: The treatment of mitral insufficiency in refractory heart failure. European Heart Journal Supplements (2020) 22 (Supplement L), L93–L96
15 Patrick T. O’Gara, M.D., and Michael J. Mack: Secondary Mitral Regurgitation. N Engl J Med 2020;383:1458-67.
- Grinberg. D , Uhlrich. W , Thivolet. S et al: The unfinished saga of invasive procedures for secondary mitral regurgitation. Ann Cardiothorac Surg 2021;10(1):66-74.







