Tăng huyết áp là một bệnh rất phổ biến. Tỷ lệ người bị tăng huyết áp rất cao. Ở các nước phương Tây tỷ lệ người bị tăng huyết áp ở độ tuổi ≥ 35 tuổi là vào khỏang 35 – 50%. Tỷ lệ này ở châu Á có thấp hơn nhưng cũng đạt con số 25 – 35 % [1].
PGS.TS Trương Quang Bình
1. Đặt vấn đề
Tăng huyết áp là một bệnh rất phổ biến. Tỷ lệ người bị tăng huyết áp rất cao. Ở các nước phương Tây tỷ lệ người bị tăng huyết áp ở độ tuổi ≥ 35 tuổi là vào khỏang 35 – 50%. Tỷ lệ này ở châu Á có thấp hơn nhưng cũng đạt con số 25 – 35 % [1]. Số người bị tăng huyết áp nhiều như vậy sẽ là một gánh nặng cho ngành y tế. Những biến chứng của bệnh tăng huyết áp cũng rất trầm trọng như tai biến mạch máu não, nhồi máu cơ tim, suy tim, suy thận, bệnh mắt do tăng huyết áp, bệnh động mạch ngọai biên [2]. Chính vì quan trọng như vậy cho nên quốc gia nào, khu vực nào cũng có chiến lược kiểm sóat tình trạng tăng huyết áp.
Biện pháp chính trong kiểm sóat tình trạng tăng huyết áp là biện pháp điều trị hạ áp. Các nhà y học đã chứng minh rất rõ ràng rằng khi giảm được trị số huyết áp thì sẽ giảm được các biến cố tim mạch, tử vong tim mạch do tăng huyết áp gây ra. Cứ làm giảm được 2mmHg trị số huyết áp tâm thu thì sẽ làm giảm đuợc 7% nguy cơ tử vong do bệnh mạch vành và làm giảm được 10% nguy cơ tử vong do đột quị [3].
Rất nhiều lọai thuốc điều trị hạ áp đã được nghiên cứu trong điều trị tăng huyết áp. Cho đến nay, chúng ta có trong tay 5 nhóm thuốc hạ áp. Đó là: nhóm thuốc lợi tiểu, nhóm thuốc ức chế bêta giao cảm, nhóm thuốc chẹn kênh canxi, nhóm thuốc ức chế men chuyển, nhóm thuốc ức chế thụ thể angiotensine. Ngòai 5 nhóm thuốc vừa kể trên chúng ta cũng còn có những nhóm thuốc hạ áp khác như nhóm thuốc hạ áp tác dụng trên thần kinh trung ương, nhóm thuốc tác dụng ức chế thụ thể alpha giao cảm.
Đã có rất nhiều nghiên cứu về hiệu quả của các lọai thuốc hạ áp. Kết quả của những nghiên cứu này đã tạo ra được các khuyến cáo điều trị tăng huyết áp. Thầy thuốc trên tòan thế giới đã sử dụng những khuyến cáo trên trong thực hành lâm sàng của mình và đã đạt được những kết quả rất tốt. Tuy nhiên, không phải bất cứ nhóm đối tượng bệnh nhân nào cũng có đủ bằng chứng thông qua các công trình nghiên cứu khoa học đã công bố. Cụ thể là đối tượng nghiên cứu chính của những công trình nghiên cứu về điều trị hạ áp chủ yếu là người ở các quốc gia phương Tây, còn người phương Đông ít có tham gia vào những công trình nghiên cứu như vậy. Là thầy thuốc ở quốc gia phương Đông, mà cụ thể là quốc gia châu Á, chúng ta cần có những chứng cứ về điều trị hạ áp cho bệnh nhân chúng ta. Vì vậy, những công trình nghiên cứu về điều trị tăng huyết áp được thực hiện trên đối tượng bệnh nhân người châu Á luôn luôn có sự hấp dẫn với chúng ta.
2. Đặc điểm về bệnh tăng huyết áp và điều trị tăng huyết áp ở các quốc gia châu Á
Người châu Á chúng ta có những đặc điểm về bệnh tim mạch khác với người phương Tây:
– Người châu Á có cơ địa dễ mắc bệnh đái tháo đường hơn người châu Âu. Tỷ lệ mắc đái tháo đường của người chúng ta có thể tăng gấp 3,5 lần so với người Châu Âu. Đây là một yếu tố nguy cơ tim mạch quan trọng cho chúng ta và nhất là cho những người có tăng huyết áp [4].
– Những biến cố tim mạch xảy ra cũng khác nhau giữa người châu Á và người phương Tây: tỷ lệ biến cố nhồi máu cơ tim và biến cố tai biến mạch máu não của người phương Tây là tương đương nhau, còn ở người châu Á thì biến cố tai biến mạch máu não cao hơn biến cố nhồi máu cơ tim và cao hơn biến cố tai biến mạch máu não ở người châu Âu [5].
– Đáp ứng điều trị tăng huyết áp cũng khác nhau giữa người châu Á so với người phương Tây: bệnh nhân chúng ta đáp ứng tốt hơn với thuốc hạ áp, tỷ lệ người đạt được huyết áp mục tiêu cao hơn so với bệnh nhân phương Tây [6].
3. Số lượng bệnh nhân Châu Á trong các công trình nghiên cứu ở phương Tây về điều trị tăng huyết áp
Các nghiên cứu ở phương tây về điều trị tăng huyết áp như ASCOT – BPLA, ALLHAT, LIFE, VaLHeFT, VALUE, HOT, PROGRESS là những công trình nghiên cứu lớn, mang lại những kết luận quan trọng cho thực hành lâm sàng hàng ngày của bác sỹ. Dù có những đối tượng người châu Á tham gia trong nghiên cứu nhưng số lượng đối tượng nghiên cứu này còn rất hạn chế. Cụ thể thì trong nghiên cứu ASCOT –BPLA chỉ có < 5% đối tượng nghiên cứu là người châu Á [7]; nghiên cứu ALLHAT cũng chỉ có < 5% người tham gia nghiên cứu là người châu Á [8]; nghiên cứu VaL HeFT và VALUE chỉ có <3% là người châu Á [10]; và ít nhất là trong nghiên cứu LIFE (<0,5%) [9]. Trong nghiên cứu HOT thì chỉ có 205 bệnh nhân người châu Á, và trong nghiên cứu PROGRESS cũng chỉ có 2335 bệnh nhân người châu Á [11].
Như vậy, có thể nói rằng số bệnh nhân người châu Á tham gia vào các công trình nghiên cứu về điều trị tăng huyết áp rất ít. Và như thế, những kết luận từ những công trình nghiên cứu này chưa chắc đã có thể áp dụng đúng hòan tòan vào thực hành trên bệnh nhân châu Á. Chúng ta đã có nhiều công trình nghiên cứu về điều trị tăng huyết áp thực hiện đơn thuần trên bệnh nhân người châu Á chưa ?
4. Các nghiên cứu về điều trị tăng huyết áp được thực hiện trên người châu Á
Những công trình nghiên cứu về điều trị tăng huyết áp tương đối lớn ở người châu Á có thể kể đến: STONE (Shanghai Trial Of Nifedipine in the Elderly), SYST-China (Systolic hypertension in China), HOT China, FEVER, JIKEI, KYOTO.
Trong công trình STONE (1632 bệnh nhân người Trung Quốc) thuốc được sử dụng là Nifedipine [12], trong công trình SYST – China (2394 bệnh nhân người Trung Quốc) thuốc được sử dụng là Nitrendipine [13], trong công trình nghiên cứu HOT China (>50.000 bệnh nhân người Trung Quốc) thuốc được sử dụng là Felodipine, trong nghiên cứu FEVER (>10.000 bệnh nhân người Trung Quốc) thuốc được sử dụng cũng là Felodipine [14], trong nghiên cứu JIKEI (>3000 bệnh nhân người Nhật) thuốc được sử dụng là Valsartan [15] và trong nghiên cứu KYOTO (>3000 bệnh nhân người Nhật) thì Valsartan cũng là thuốc được sử dụng [16].
Như vậy, thuốc ức chẹn kênh can xi và thuốc ức chế thụ thể angiotensin đã có được những nghiên cứu trên bệnh nhân người châu Á và cho những kết quả rất đáng khích lệ. Tuy nhiên, những công trình nghiên cứu này cũng chưa có kết quả về điều trị kết hợp thuốc ngay từ đầu, nhất là việc sử dụng viên thuốc kết hợp với liều cố định. Vì vậy, một nghiên cứu điều trị hạ áp bằng thuốc phối hợp liều cố định trên bệnh nhân chấu Á là điều trong mong đợi của các thầy thuốc châu Á.
5. Nghiên cứu HEAALTH trên bệnh nhân người châu Á
Giới thiệu nghiên cứu
Losartan là hợp chất đầu tiên trong nhóm ƯCTT có tác dụng hạ áp. Tính hiệu quả và an toàn của Losartan đơn độc và khi kết hợp với HCTZ đã được nghiên cứu nhiều ở các bệnh nhân không phải người Châu Á [17,18] . Hiệu quả lâu dài của việc phối hợp Losartan/HCTZ nhờ vào hạ được HA và giảm thiểu nguy cơ mắc các biến chứng của THA như phì đại thất trái [19], đạm niệu [20], và các kết cục lâm sàng như bệnh thận mạn giai đoạn cuối [21] và đột quỵ [22].
Phần lớn các bằng chứng lâm sàng của Losartan/HCTZ đều không được nghiên cứu trên các BN Châu Á. Có rất ít nghiên cứu với Losartan 100 mg/HCTZ 12,5 mg. Bằng chứng cho việc phát triển viên phối hợp này là liều tối ưu của Losartan để giảm đạm niệu là 100 mg mỗi ngày [23-25]. Thêm vào đó, vì các tác dụng không mong muốn của lợi tiểu thường thấy khi dùng liều cao (ví dụ, HCTZ> 50 mg) [26], nên các BS thích dùng HCTZ 12,5 mg. Nghiên cứu này, Asian Hypertension Evaluation of Angiotensin II Antagonist Losartan+HCTZ (HEAALTH), được thực hiện để đánh giá tính hiệu quả và an toàn của việc phối hợp Losartan/HCTZ, đặc biệt ở liều Losartan 100 mg/HCTZ 12,5 mg, ở các BN người Châu Á đang được điều trị với ƯCMC hoặc ƯCTT với liều thông thường mà chưa đạt được HA mục tiêu.
Phương pháp nghiên cứu
Chọn lựa bệnh nhân
Các BN có THA vô căn (HA tâm trương khi ngồi (SiDBP) ≥ 90 đến < 110 mm Hg ở các BN không có đái tháo đường và SiDBP ≥ 80 đến < 100 mm Hg ở các BN có đái tháo đường), trên 18 tuổi và là người Châu Á. Các BN bị loại khỏi nghiên cứu nếu có bất kỳ bằng chứng lâm sàng của các vấn đề về huyết học, thận, gan hoặc đường tiêu hóa; đã biết nhạy cảm với thuốc; hoặc các bệnh lý liên quan đến hệ mạch máu não, hệ miễn dịch hoặc hệ tim mạch, bao gồm nhồi máu cơ tim hoặc suy chức năng thất trái (phân suất tống máu ≤ 50%). Các BN có sử dụng các thuốc hạ áp khác cùng lúc, lithium, các thuốc hướng tâm thần hoặc chống trầm cảm; kháng viêm không steroid, thuốc ức chế men COX II hoặc aspirin liều cao mỗi ngày; astemizole, terfenadine hoặc bất kỳ thuốc nào khác có ảnh hưởng đến HA đều bị loại khỏi nghiên cứu. Phụ nữ có thai hoặc cho con bú cũng không được nhận vào.
Qui trình nghiên cứu
Đây là một nghiên cứu nhãn mở, đa trung tâm bao gồm 1 tuần sàng lọc/giai đoạn nền với đơn trị liệu hạ HA (lần khám 1 và 2) và giai đoạn 12 tuần điều trị với Losartan/HCTZ. Khởi đầu với liều Losartan 50 mg/HCTZ 12,5 mg và chỉnh đến liều Losartan 100 mg/HCTZ 12,5 mg ở thời điểm 4 tuần và Losartan 100 mg/HCTZ 25 mg ở thời điểm 8 tuần nếu HA mục tiêu chưa đạt được. Trong 512 BN được sàng lọc, 437 BN thỏa tiêu chuẩn nhận và có mức HA chưa kiểm soát được với đơn trị liệu (SiDBP ≥ 90 mm Hg ở các BN không có đái tháo đường và SiDBP ≥ 80 mm Hg ở các BN có đái tháo đường) được đưa vào nghiên cứu sau lần thăm khám thứ 2 và chuyển sang sử dụng viên phối hợp liều cố định Losartan 50 mg/HCTZ 12,5 mg. Tất cả các xét nghiệm trong mỗi lần thăm khám được thực hiện bởi các phòng xét nghiệm tại địa phương, và ngoại trừ lần thăm khám sàng lọc, tất cả các lần khám sau đều được thực hiện trước 12 giờ trưa để chắc rằng việc đo HA diễn ra trong khoảng đáy 22-26 giờ sau liều thuốc uống cuối cùng.
Thuốc dùng trong nghiên cứu
Tất cả thuốc dùng trong nghiên cứu đều lấy từ nguồn của địa phương và được cung cấp nguyên nhãn. Các BN được hướng dẫn dùng thuốc trong nghiên cứu đều đặn mỗi ngày từ 6 giờ đến 10 giờ sáng, sau bữa điểm tâm, trừ ngày hẹn được thăm khám. Vào ngày thăm khám, thuốc sẽ được cấp sau khi có kết luận của buổi khám. Số viên thuốc sẽ được đếm ở mỗi lần thăm khám để kiểm tra sự tuân thủ của BN.
Phương pháp quan sát
Nhịp tim, HA khi ngồi, HA khi đứng được đo ngay đầu buổi thăm khám, sử dụng huyết áp kế thủy ngân. BN ngồi nghỉ ít nhất 5 phút trước khi được đo HA. HA tư thế ngồi được đo 3 lần cách nhau 1-2 phút và lấy giá trị trung bình. Không giá trị SiDBP nào được lớn hơn 5 mmHg so với trị số trung bình của 3 lần đo. BN đứng ít nhất 1 phút trước khi đo HA tư thế đứng. Một điện tâm đồ 12 chuyển đạo được đo khi khởi đầu nghiên cứu.
Tất cả các biến cố ngoại ý được phát hiện hoặc khai báo được ghi nhận ở mỗi lần thăm khám. Các xét nghiệm cơ bản được thực hiện ở tất cả các lần thăm khám.
Kế hoạch phân tích và phương pháp thống kê
Biến số chính là phần trăm số BN đạt được HA mục tiêu sau 8 tuần điều trị với viên kết hợp Losartan/HCTZ (vì thời điểm 8 tuần được xem là cột mốc chính của nghiên cứu). BN được xem như đạt HA mục tiêu nếu SiDBP ở lần thăm khám sau cùng trước cột mốc chính < 90 mmHg ở nhóm không đái tháo đường và < 80 mmHg ở nhóm có đái tháo đường. Đây là một nghiên cứu ước lượng, vì vậy không có giả thiết nào được kiểm định. Giả định rằng, tỷ lệ phần trăm các BN đạt HA mục tiêu dự kiến trong khoảng 50-60%, nghiên cứu này với 400 bệnh nhân ước lượng tỷ lệ bệnh nhân đạt được HA mục tiêuvới độ chính xác vào khoảng 5% (nghĩa là KTC 95% cho phép kiểm 2 đuôi). Biến số chính về hiệu quả, là tỷ lệ phần trăm BN đạt HA mục tiêu sau 8 tuần điều trị với liều Losartan 50 mg/HCTZ 12,5 mg, được tính toán kèm với KTC 95%.
Toàn bộ dân số nghiên cứu được đưa vào để phân tích về hiệu quả, bao gồm tất cả các BN đã dùng ít nhất 1 liều thuốc trong nghiên cứu và có đầy đủ dữ liệu về các biến số cần thiết. Mỗi BN đều phải có các thông số nền để phân tích sự thay đổi so với ban đầu. Sau lần thăm khám thứ 2 (cuối giai đoạn sàng lọc), các thông số được ghi nhận và dùng làm giá trị nền. Trong suốt thời gian điều trị, giá trị cuối cùng đo đạc được trước khi đến cột mốc chính được dùng để đánh giá hiệu quả; tất cả các giá trị đo được đều được dùng, bao gồm cả các thông tin khi BN ngừng tham gia hoặc các lần thăm khám không hẹn trước. Một cách khác để phân tích tiêu chí chính về hiệu quả là chỉ phân tích trên nhóm các BN tham gia trọn thời gian nghiên cứu.
Tiêu chí phụ bao gồm mức độ thay đổi trung bình so với nền của SiDBP (tiêu chí phụ quan trọng) và SiSBP, tỷ lệ đáp ứng (phần trăm số BN đạt HA mục tiêu hoặc SiDBP giảm ít nhất 10 mmHg) sau 8 tuần điều trị và tỷ lệ phần trăm số BN đạt HA mục tiêu sau 12 tuần điều trị. Các biến số thứ cấp khác được ghi nhận ở tuần thứ 8 bao gồm tỷ lệ phần trăm đạt HA mục tiêu và tỷ lệ đáp ứng ở các phân nhóm BN đái tháo đường, phì đại thất trái trên ECG và béo phì (BMI > 25 kgm-2); thay đổi trung bình của albumin vi lượng nước tiểu; và thay đổi điểm số nguy cơ đột quị Framingham. Biến số phụ quan trọng, mức độ thay đổi trung bình so với nền của SiDBP ở tuần thứ 8, được tính toán kèm với KTC 95%. Các biến số phụ khác liên quan đến sự thay đổi so với nền được phân tích theo cách tương tự như trên. Các biến số phụ liên quan đến tỷ lệ phần trăm hoặc tỷ lệ đáp ứng được phân tích theo cách tương tự với biến số chính.
Chỉ số về tuân thủ được định nghĩa là tổng số của ngày BN sử dụng thuốc nghiên cứu chia cho tổng số ngày BN tham gia vào nghiên cứu.
Việc đánh giá tính an toànvà sự dung nạp của liệu pháp phối hợp Losartan/HCTZ là một mục tiêu chuyên biệt thứ phát của nghiên cứu. Dân số nghiên cứu về tính an toàn bao gồm tất cả các bệnh nhân tham gia nhận được ít nhất một liều thuốc trong nghiên cứu. Tất cả các biến cố ngoại ý xảy ra sau khi dùng liều thuốc đầu tiên và đến 14 ngày sau khi ngưng điều trị đều được ghi nhận trong phân tích tính an toàn.
Kết quả nghiên cứu
Đặc điểm bệnh nhân
Trong 512 BN được sàng lọc, 75 BN bị loại với các lý do: không đạt tiêu chuẩn đo HA (n=57), tự rút lui (n=13), mất dấu (n=4), không tuân theo đề cương (n=1). 437 (85,4%) BN còn lại thỏa tiêu chuẩn và được nhận vào tại 1 trong 32 trung tâm ở 7 quốc gia. Đa số BN thuộc Trung Quốc và Hàn Quốc (khoảng 60%): Trung Quốc 24%, Hong Kong 4%, Hàn Quốc 35%, Malaysia 11%, Philippine 12%, Đài Loan 9% và Thái Lan 4%. Tổng cộng 391 BN (89,5%) hoàn thành đủ thời gian nghiên cứu.
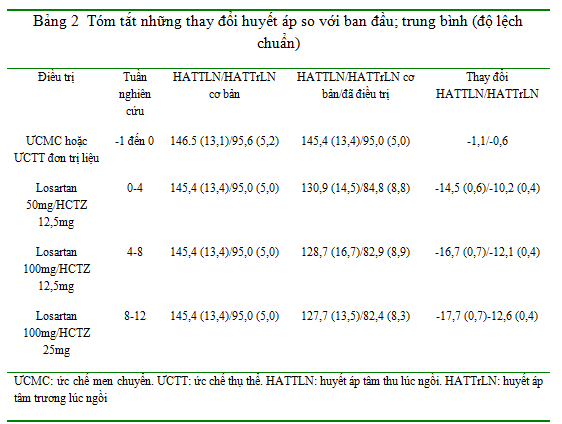
Đặc điểm cơ bản của tất cả BN tham gia nghiên cứu được trình bày trong Bảng 1. Tuổi trung bình là 53,0 (± 10.1) năm và thời gian biết THA là 5,2 (± 7.3) năm. Trong 437 BN, 313 (71,6%) có ít nhất 1 chẩn đoán bệnh khác kèm theo, chiếm tỷ lệ cao nhất là tăng lipid máu (14%), rối loạn lipid máu (6%), phì đại thất trái (9%), đái tháo đường (11%), mãn kinh (10%), đau đầu (7%) và chóng mặt (6%). SiSBP nền trung bình là 145,3 (± 13,5) mmHg và SiDBP là 95,0 (± 5,0) mmHg.
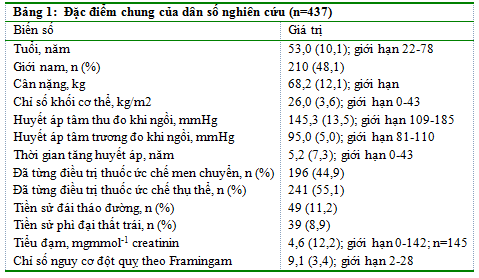
55% BN đã được điều trị THA trước đó với 1 loại thuốc ƯCTT và 45% với ƯCMC.Các loại thuốc ƯCTT đã dùng trước đó (số BN, liều trung bình (độ lệch chuẩn) là: candesartan (n=11, 8 (0) mg), eprosartan (n=11, 572 (90) mg), irbesartan (n=26, 150 (0) mg), losartan (n=125, 49 (9) mg), olmesartan (n=3, 23 (15) mg), telmisartan (n=23, 40 (0) mg) và valsartan (n=42, 93 (38) mg).Các loại thuốc ƯCMC đã dùng trước đó: benazepril (n=18, 10 (0) mg), captopril (n=24, 40 (19) mg), cilazapril (n=8, 3 (1) mg), enalapril (n=49, 9 (3) mg), fosinopril (n=7, 10 (0) mg), imidapril (n=14, 9 (2) mg), lisinopril (n=10, 10 (5) mg), moexipril (n=4, 7.5 (0) mg), perindopril (n=39, 4 (1) mg) và ramipril (n=23, 4 (5) mg).
Liệu pháp điều trị trong nghiên cứu
Sau 4 tuần đầu của nghiên cứu, tất cả 437 BN đều được dùng Losartan 50 mg/HCTZ 12,5 mg. Sau 8 tuần, 250 BN (57,2%) vẫn còn dùng Losartan 50 mg/HCTZ 12,5 mg, 163 BN (37,3%) dùng Losartan 100 mg/HCTZ 12,5 mg, và có 1 BN (0,2%) dùng Losartan 100 mg/HCTZ 25 mg. Khi kết thúc nghiên cứu (12 tuần), 232 BN (53,1%) vẫn còn dùng Losartan 50 mg/HCTZ 12,5 mg, 96 BN (22,0%) dùng Losartan 100 mg/HCTZ 12,5 mg, và 65 BN (14,9%) dùng Losartan 100 mg/HCTZ 25 mg. Các BN tuân thủ tốt với trị liệu của nghiên cứu (dữ liệu không công bố).
Đạt được HA mục tiêu và tỷ lệ đáp ứng
Biến số chính, tỷ lệ phần trăm BN đạt được HA mục tiêu (SiDBP < 90 mmHg ở nhóm BN không đái tháo đường và < 80 mmHg ở nhóm có đái tháo đường) sau 8 tuần dùng liệu pháp phối hợp Losartan/HCTZ (liều lên đến Losartan 100 mg/HCTZ 12.5 mg), là 73.5% (KTC 95%: 69,0 –77,6) (Hình 1). Kết quả phân tích riêng ở nhóm các BN tham gia trọn thời gian nghiên cứu củng cố thêm cho kết quả phân tích toàn bộ dân số nghiên cứu. Sau 4 tuần và 12 tuần, HA mục tiêu đạt được lần lượt ở 63,4% và 78,1% số BN (Hình 1).Các kết quả tương tự được tìm thấy khi phân tích các dưới nhóm, bao gồm giới, phân nhóm tuổi, quốc gia, SiDBP nền, SiSBP nền và sử dụng các thuốc điều trị tăng HA sớm (dữ liệu không công bố).
Tỷ lệ đáp ứng (tỷ lệ phần trăm BN đạt HA mục tiêu, hoặc giảm SiDPB ít nhất 10 mm Hg) sau 8 tuần điều trị là 78,1% (KTC 95%: 73,9–82,0). Sau 4 và 12 tuần, tỷ lệ đáp ứng lần lượt là 67,8% và 83,3% (Hình 1).
Kết quả tương tự đối với HA mục tiêu và tỷ lệ đáp ứng được tìm thấy sau 8 tuần điều trị đối với các nhóm BN có nền tảng phì đại thất trái và béo phì. Trong nhóm BN đái tháo đường, HA mục tiêu đạt được ở 47,9%, trong khi tỷ lệ đáp ứng là 64,6%. Khi nghiên cứu kết thúc (tuần 12), có 94/430 BN (22%) là những người không đáp ứng (không đạt được HA mục tiêu), trong đó có 21 BN đái tháo đường (ở tuần 12, 27/48 BN đái tháo đường đạt HA mục tiêu).
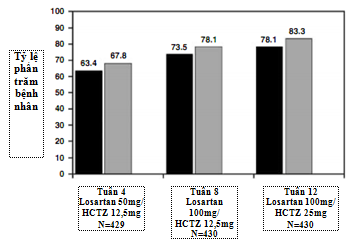
Hình 1: Bệnh nhân Châu Á không kiểm soát được huyết áp với liều đơn trị liệu thông thường của ức chế men chuyển hoặc ức chế thụ thể, những người đạt được huyết áp mục tiêu (thanh đen; đo huyết áp tâm trương lúc ngồi <90mmHg ở người không bị đái tháo đường và <80 mmHg ở người đái tháo đường) hoặc có đáp ứng (thanh màu xám; đo huyết áp tâm trương lúc ngồi <90mmHg ở người không bị đái tháo đường và <80 mmHg ở người đái tháo đường hoặc giảm giảm huyết áp tâm trương lúc ngồi ≥ 10 mmHg) sau đơn trị liệu đã được đổi qua dùng losartan/hydrochlorothiazide dạng phối hợp.
Sự thay đổi HA ở tuần 4, 8, 12 và các chỉ số khác
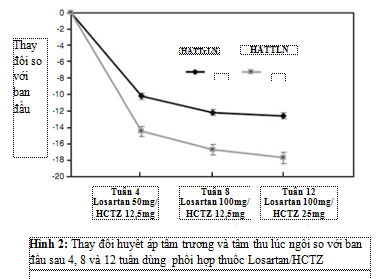
SBP/DBP tư thế ngồi giảm có ý nghĩa thống kê (thay đổi trung bình so với nền, P<0,001) ở tuần 4 (-14,5/-10,2 mmHg, với liều Losartan 50 mg/HCTZ 12,5 mg), tuần 8 (-16,7/-12,1 mmHg, chỉnh liều đến Losartan 100 mg/HCTZ 12,5 mg) và tuần 12 (-17,7/-12,6 mmHg, chỉnh liều đến Losartan 100 mg/HCTZ 25 mg) (Bảng 2, Hình 2). StSBP và StDBP giảm so với nền từ sau 8 tuần điều trị với liệu pháp phối hợp Losartan/HCTZ; thay đổi trung bình so với nền của StSBP và StDBP lần lượt là -15,8 và -10,8 mmHg.
Albumin niệu vi lượng giảm so với nền từ sau 8 tuần điều trị với Losartan/HCTZ; thay đổi trung bình so với nền -1,43 mgmmol-1creatinine (KTC 95%: -2,82 đến -0,05). Điểm nguy cơ đột quỵ Framingham cũng giảm sau 8 tuần điều trị; thay đổi trung bình so với nền là -2,28 (KTC 95%: -2,46 đến -2,11). Sau 4 và 12 tuần, thay đổi trung bình so với nền lần lượt là -1,98 và -2,44. Sau 12 tuần, điểm nguy cơ đột quỵ Framingham thay đổi so với nền là -2,22 ở nam và -2,65 ở nữ.
Tính an toàn
Tất cả 437 BN đều được khảo sát về tính an toàn. Số ngày dùng thuốc trung bình là 81 ngày. Trong suốt khoảng thời gian điều trị, các biến cố ngoại ý trên lâm sàng và cận lâm sàng xảy ra lần lượt ở 120 (27,5%) và 88 (21%). Nhiễm trùng hô hấp trên (n=15, 3,4%), chóng mặt (n=15, 3,4%) và đau đầu (n=12, 2,7%) là những biến cố ngoại ý ghi nhận nhiều nhất trên lâm sàng. 37 BN (8,5%) được ghi nhận có các biến cố ngoại ý lâm sàng có thể hoặc chắc chắn có liên quan đến thuốc. biến cố nghiêm trọng gặp ở 7 BN (2,5%). 1 BN bị 2 biến cố nghiêm trọng, chóng mặt và bệnh thận, được cho là có liên quan đến thuốc vì sau khi rút khỏi nghiên cứu BN đã hồi phục hoàn toàn. Không ghi nhận trường hợp tử vong nào.
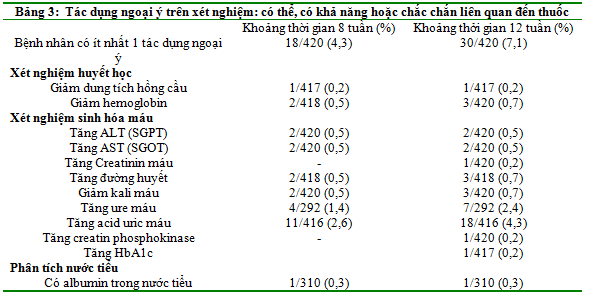
Trong suốt quá trình điều trị, các biến cố ngoại ý trên cận lâm sàng gặp ở 88 BN (21,0%). Không có biến cố nghiêm trọng và chỉ có 2 BN cần phải dừng điều trị (1 BN bị tăng AST và ALT, 1 BN bị tăng ALT).Các biến cố ngoại ý trên cận lâm sàng thường gặp nhất là tăng ALT (n=18, 4,3%), uric acid (n=21, 5,0%), HbA1c (n=21, 5,0%), glucose (n=14, 3,3%) và tăng albumin niệu (n=9, 2,9%). 30 BN (7,1%) được ghi nhận các biến cố ngoại ý trên cận lâm sàng được cho là có liên quan đến thuốc (Bảng 3). Chủ yếu là tăng uric acid (n=18) và urea máu (n=7). Không ghi nhận thay đổi nào đáng kể về các chỉ số huyết học.
Bàn luận
Kết quả nghiên cứu cho thấy đa số các BN Châu Á (73,5%), trước đây không đạt được HA mục tiêu với liều thông thường ƯCMC hoặc ƯCTT đơn trị liệu, đã đạt được HA mục tiêu DBP < 90 mmHg ở nhóm không đái tháo đường và DBP < 80 mmHg ở nhóm có đái tháo đường khi chuyển sang dùng liệu pháp phối hợp Losartan 50-100 mg/HCTZ 12.5 mg trong vòng 8 tuần. Thêm vào đó, 78,1% BN có đáp ứng với liệu pháp phối hợp sau 8 tuần, nghĩa là DBP < 90 mmHg ở nhóm không đái tháo đường và DBP < 80 mmHg ở nhóm có đái tháo đường hoặc DBP giảm hơn 10 mmHg. Đa số các kinh nghiệm sử dụng phối hợp Losartan/HCTZ là với liều Losartan 50 mg/HCTZ 12,5 mg là trên đối tượng không phải người Châu Á. Chỉ có 1 nghiên cứu vừa công bố về liệu pháp phối hợp Losartan 100 mg/HCTZ 12,5 mg trên đối tượng không phải người Châu Á [27]. Các BN có HA chưa kiểm soát tốt (DBP 95-120 mmHg) khi điều trị với Losartan 100 mg, được chia ngẫu nhiên tiếp tục điều trị với Losartan 100 mg hoặc Losartan 100 mg/HCTZ 12,5 mg. Sau 6 tuần theo dõi, 55% BN ở nhóm dùng viên phối hợp và 42,4% BN nhóm đơn trị liệu đã đạt được HA mục tiêu (SiDBP < 90 mmHg), trong khi có đến 63% BN ở nhóm dùng viên phối hợp có đáp ứng (trung bình DBP < 90 mmHg hoặc trung bình DBP giảm hơn 10 mmHg), và 44,4% BN ở nhóm đơn trị liệu có đáp ứng.
Trong nghiên cứu này, 63,4% BN Châu Á đạt được HA mục tiêu với liều Losartan 50 mg/HCTZ 12,5 mg sau 4 tuần, trong khi có 67,8% BN có đáp ứng. Kết quả này phù hợp với 2 nghiên cứu trước đây trên nhóm BN không phải người Châu Á, được điều trị 6 tuần với Losartan 50 mg và chỉnh liều (nếu DBP > 90 mmHg) thành Losartan 100 mg hoặc Losartan 50 mg/HCTZ 12,5 mg trong 6 tuần tiếp theo [28,29]. Trong nghiên cứu thứ nhất, 70% BN có đáp ứng với viên phối hợp Losartan 50 mg/HCTZ 12,5 mg (DBP < 90 mmHg hoặc ≥ 90 mmHg mà có giảm DBP > 10 mmHg) và 60% có đáp ứng với Losartan 50–100 mg đơn trị liệu [28]. Trong nghiên cứu thứ hai, 76,8% BN có đáp ứng với viên phối hợp và 73,1% đáp ứng với đơn trị liệu [29]. Trong một nghiên cứu ở các BN gốc Châu Á với DBP nền 95-115 mmHg và SBP < 190 mmHg, 26,8% BN đạt HA mục tiêu sau 4 tuần đơn trị liệu với Valsartan 80 mg. Các BN không đạt HA mục tiêu được chuyển sang Losartan 50 mg/HCTZ 12,5 mg và sau 4 tuần 72% BN đạt HA mục tiêu [30]. Trong một nghiên cứu gần đây ở các BN Nhật Bản có HA không được kiểm soát (HA theo dõi 24 giờ ≥ 135/80 mmHg) sau hơn 2 tháng điều trị Candesartan 8 mg hoặc Amlodipine 5 mg được chuyển sang Losartan 50 mg/HCTZ 12,5 mg. HA theo dõi 24 giờ giảm có ý nghĩa thống kê ở cả 2 nhóm sau thời gian điều trị từ 3 đến 12 tháng. SBP cũng giảm có ý nghĩa ở cả 2 nhóm trong khoảng thời gian ngày (6 giờ – 21 giờ 30), đêm (22 giờ – 5 giờ 30) và sáng sớm (6 giờ – 8 giờ) sau 12 tháng điều trị với Losartan/HCTZ [31].
Losartan 100 mg/HCTZ 25 mg là liều phối hợp cao nhất trong nghiên cứu này và có hiệu quả nâng tỷ lệ phần trăm BN đạt HA mục tiêu lên 78,1% và tăng tỷ lệ đáp ứng lên 83,3%. Một nghiên cứu trên những BN không phải người Châu Á với HA không được kiểm soát (DBP > 90 mmHg) với điều trị phối hợp với ít nhất 2 loại thuốc được chuyển sang dùng Losartan 100 mg/HCTZ 25 mg. Tỷ lệ HA được kiểm soát (DBP ≤ 90 mmHg) và tỷ lệ đáp ứng (DBP < 90 mmHg hoặc DBP giảm ≥ 10 mmHg) lần lượt là 63,0% và 82,1% sau 12 tuần [32]. Trong một nghiên cứu về những BN THA trung bình đến nặng chưa điều trị hoặc các BN THA chưa kiểm soát dù đã được điều trị với một loại thuốc hoặc viên kết hợp liều thấp, tỷ lệ đáp ứng với Losartan 100 mg/HCTZ 25 mg là 87,8% (trị số trung bình của SBP và DBP đều giảm > 5mmHg qua theo dõi 24 giờ) sau 8 tuần điều trị [33].
Kinh nghiệm điều trị hiện nay và trước đây đều cho thấy sự phối hợp Losartan/HCTZ có thể làm giảm HA có ý nghĩa trên lâm sàng ở các BN người Châu Á, và mức độ hạ HA cũng tương đồng với những nghiên cứu trên các BN không phải người Châu Á. HA thấp hơn có liên quanvới giảm nguy cơ các biến cố tim mạch [34]; tuy nhiên chưa có các nghiên cứu đơn thuần với Losartan có theo dõi kết cuộc ở các BN người Châu Á.
Xét nghiệm tìm đạm niệu quan trọng để đánh giá nguy cơ của BN và sự cần thiết thay đổi điều trị [35]. Lấy nước tiểu tại 1 thời điểm và dùng tỷ lệ albumin/creatinine cho phép đánh giá hiệu quả của điều trị [36]. Đạm niệu nền trong nghiên cứu này thấp (4,65 mg mmol-1creatinine) có khả năng do số lượng BN đái tháo đường thấp (11%) và tuổi BN trẻ hơn (trung bình 53 tuổi). Đạm niệu giảm còn 1,43 mg mmol-1creatinine sau 8 tuần (khi đã nâng liều lên Losartan 100 mg/HCTZ 12.5 mg). Trong một nghiên cứu gần đây trên nhóm BN Châu Á có bệnh lý thận, mối liên hệ giữa liều thuốc và sự đáp ứng có khác nhau giữa HA so với mức giảm đạm niệu [35]. Losartan 50 và 100 mg có hiệu quả hạ HA tương tự nhưng Losartan 100 mg cho thấy làm giảm đạm niệu tốt hơn ở các BN với tất cả các kiểu hình của men chuyển angiotensin.
Nghiên cứu này có một số hạn chế. Đây là một nghiên cứu nhãn mở mà không có nhóm chứng. Có thể tác dụng hạ HA quan sát thấy được là do hiệu ứng placebo. Để giảm thiểu khả năng này, các BN được yêu cầu tiếp tục đơn trị liệu đã có trong ít nhất 4 tuần trước khi vào tầm soát và tiếp tục dùng thêm 1 tuần nữa trước khi bắt đầu nghiên cứu. Các BN có DBP chênh lệch > 5 mmHg qua 2 lần thăm khám đầu tiên thì không được nhận vào nghiên cứu.Độ khác biệt trung bình của HA đo giữa 2 lần khám của các BN được nhận vào là < 1 mmHg (DBP 95,6 (± 5,2) mmHg ở lần khám 1 và DBP 95,0 (± 5,0) mmHg ở lần khám 2), cho thấy rằng HA ổn định ở giai đoạn sàng lọc. Qua việc các nghiên cứu viên đếm số viên thuốc ở mỗi lần thăm khám, cho thấy sự tuân thủ của BN rất tốt trong nghiên cứu này, điều này có thể góp phần vào sự giảm HA. Cũng cần nhắc lại rằng, HA được đo ở vùng đáy của liều thuốc (22-26 giờ sau liều cuối cùng). Nghiên cứu viên gọi điện thoại trước mỗi lần thăm khám và nhắc nhở BN không uống thuốc vào ngày thăm khám, và lịch khám thường được hẹn vào buổi sáng. Quy trình này có lẽ làm tăng tính tuân thủ và vì vậy tăng đáp ứng điều trị.
Kết luận của nghiên cứu
Việc thay đổi điều trị ở các BN người Châu Á chưa đạt HA mục tiêu khi đơn trị liệu với ƯCTT hoặc ƯCMC sang liệu pháp phối hợp Losartan/HCTZ làm HA giảm có ý nghĩa, đạt được HA mục tiêu ở phần lớn các BN. Kết quả này cũng phù hợp với các nghiên cứu trước đây trên nhóm BN không phải người Châu Á. Viên kết hợp Losartan/HCTZ nhìn chung được các BN người Châu Á dung nạp tốt, tương tự hợp với các nghiên cứu trước đây trên nhóm BN không phải người Châu Á.
6. Kết luận
Chúng ta vừa có thêm một công trình nghiên cứu về điều trị tăng huyết áp ở người châu Á. Kết quả của nghiên cứu này giúp chúng ta có thêm chứng cứ về việc dùng viên thuốc phối hợp liều cố định giữa Losartan/HCTZ sẽ giúp kiểm sóat huyết áp tốt cho bệnh nhân đã thất bại với điều trị bằng thuốc ƯCMC hoặc ƯCTT đơn trị liệu.
Tài liệu tham khảo
1. Wolf-Maier K, et al. Hypertension prevalence and blood pressure levels in 6 European countries, Canada, and the United States. JAMA 2003;289:2363–9.
2. Joint National Committee on Detection, Evaluation and treatment of high blood pressure. Arch Intern Med. 1993; 153: 154 – 183
3. Lewington S et al. Lancet 2002;360:1903-1913.
4. Mather HM, Keen H. The Southall Diabetes Survey: prevalence of known diabetes in Asians and Europeans. Br Med J 1985;291:1081–4
5. Bhopal R, et al. Predicted and observed CV disease in South Asians: application of FINRISK, Framingham and SCORE models to Newcastle Heart Project data. J Public Health 2005;27:93–100
6. Zhu JR, et al. Implication of clinical studies for the Asian population: focus on Chinese/Asian population. Int J Clin 2006;60(Suppl. 150):14–16
7. Dahlöf et al. Prevention of cardiovascular events with an antihypertensive regimen of amlodipine adding perindopril as required versus atenolol adding bendroflumethiazide as required, in the Anglo-Scandinavian Cardiac Outcomes Trial-Blood Pressure Lowering Arm (ASCOT-BPLA): a multicentre randomised controlled trial. Lancet 2005;366:895–906
8.ALLHAT Collaborative Group. Major outcomes in high-risk hypertensive patients randomised to angiotensin-converting enzyme inhibitor or calcium channel blocker vs diuretic: The Antihypertensive and Lipid-Lowering Treatment to Prevent Heart Attack Trial (ALLHAT). JAMA 2002;288:2981–97
9. Dahlöf et al. Cardiovascular morbidity and mortality in the Losartan Intervention For Endpoint reduction in hypertension study (LIFE): a randomised trial against atenolol. Lancet 2002; 359:995–1003
10. Cohn et al. Baseline demographics of the Valsartan Heart Failure Trial. Val-HeFT Investigators. Eur J Heart Fail 2000;2:439–46
11.Rodgers A, et al. Perindopril-based BP lowering in individuals with cerebrovascular disease: consistency of benefits by age, sex and region (PROGRESS).
J Hypertens 2004;22:653–9
12. Gong L, Zhang W, Zhu Y, Zhu J, Kong D, Pagé V, Ghadirian P, LeLorier J, Hamet P. Shanghai trial of nifedipine in the elderly (STONE). J Hypertens. 1996 Oct;14(10):1237-45.
13. Ji-Guang Wang, MD; Jan A. Staessen, MD, PhD; Lansheng Gong, MD; Lisheng Liu, MD; for the Systolic Hypertension in China (Syst-China) Collaborative Group. Arch Intern Med. 2000;160:211-220.
14. Liu L, Zhang Y, Liu G, Li W, Zhang X, Zanchetti A; FEVER Study Group. The Felodipine Event Reduction (FEVER) Study: a randomized long-term placebo-controlled trial in Chinese hypertensive patients. J Hypertens. 2005 Dec;23(12):2157-72.
15. Original Text
15. Seibu Mochizuki et al for the Jikei Heart Study group. Valsartan in a Japanese population with hypertension and other cardiovascular disease (Jikei Heart Study): a randomised, open-label, blinded endpoint morbidity-mortality study. The Lancet, Volume 369, Issue 9571, Pages 1431 – 1439, 28 April 2007.
16.T Sawada1, T Takahashi1, H Yamada1, B Dahlo¨ f2 and H Matsubara1, KYOTO HEART study: effects of valsartan on morbidity and mortality in uncontrolled hypertensive patients with high risk of cardiovascular events. Journal of Human Hypertension (2009) 23, 188–195.
17. Goa KL, Wagstaff AJ. Losartan potassium: a review of its pharmacology, clinical ef?cacyand tolerability in the management of hypertension. Drugs 1996; 51:820–845.
18. Benedict CR. Safe and effective management of hypertension with ?xed-dose combinationtherapy: focus on losartan plus hydrochlorothiazide. Int J Clin Pract 2000; 54:48–54.
19. Dahlof B, Zanchetti A, Diez J, Nicholls MG, Yu CM, Barrios V, Aurup P, Smith RD,Johansson M. Effects of losartan and atenolol on left ventricular mass and neurohormonalpro?le in patients with essential hypertension and left ventricular hypertrophy.J Hypertens 2002; 20: 1855–1864, J Hypertens 2002; 20: 2315.
20. Hou FF, Xie D, Zhang X, Chen PY, Zhang WR, Liang M, Guo ZJ, Jiang JP. Renoprotectionof Optimal Antiproteinuric Doses (ROAD) study: a randomized controlled study ofbenazepril and losartan in chronic renal insuf?ciency. J Am Soc Nephrol 2007; 18:1889–1898.
21. Brenner BM, Cooper ME, de Zeeuw D, Keane WF, Mitch WE, Parving HH, Remuzzi G,Snapinn SM, Zhang Z, Shahinfar S. Effects of losartan on renal and cardiovascularoutcomes in patients with type 2 diabetes and nephropathy. NEnglJMed2001; 345:861–869.
22. Dahlof B, Devereux RB, Kjeldsen SE, Julius S, Beevers G, de Faire U, Fyhrquist F, IbsenH, Kristiansson K, Lederballe-Pedersen O, Lindholm LH, Nieminen MS, Omvik P,Oparil S, Wedel H. Cardiovascular morbidity and mortality in the Losartan InterventionFor Endpoint reduction in hypertension study (LIFE): a randomised trial againstatenolol. Lancet 2002; 359: 995–1003.
23. Andersen S, Rossing P, Juhl TR, Deinum J, Parving HH.Optimal dose of losartan forrenoprotection in diabetic nephropathy. Nephrol Dial Transplant 2002; 17:1413–1418.
24. Laverman GD, Henning RH, de Jong PE, Navis G, de Zeeuw D. Optimal antiproteinuricdose of losartan in nondiabetic patients with nephrotic range proteinuria. Am J KidneyDis 2001; 38: 1381–1384.
25. Park HC, Choi HY, Kim BS, Kang SW, Choi KH, Ha SK, Lee HY, Han DS.effect oflosartan in non-diabetic renal disease is not dependent on ACE insertion/deletionpolymorphism. Kidney Blood Press Res 2006; 29: 216–224.
26 Fukuda M, Kimura G. Pathophysiology of antihypertensive therapy with diuretics.Hypertens Res 2006; 29:645–653.
27. Gleim GW, Rubino J, Zhang H, Shahinfar S, Soffer BA, Lyle PA, Littlejohn III TW,Feig PU. A multicenter, randomized, double-blind, parallel-group trial of the antihypertensiveef?cacy and tolerability of a combination of once-daily losartan100 mg/hydrochlorothiazide 12.5mg compared with losartan 100 mg monotherapy inthe treatment of mild to severe essential hypertension. Clin Ther 2006; 28:1639–1648.
28. Dahlof B, Lindholm LH, Carney S, Pentikainen PJ, Ostergren J. Main results of thelosartan versus amlodipine (LOA) study on drug tolerability and psychological generalwell-being. LOA Study Group. J Hypertens 1997; 15: 1327–1335.
29. Manolis AJ, Grossman E, Jelakovic B, Jacovides A, Bernhardi DC, Cabrera WJ,Watanabe LA, Barragan J, Matadamas N, Mendiola A, Woo KS, Zhu JR, Mejia AD,Bunt T, Dumortier T, Smith RD. Effects of losartan and candesartan monotherapyand losartan/hydrochlorothiazide combination therapy in patients with mild to moderatehypertension. Losartan Trial Investigators. Clin Ther 2000; 22: 1186–1203.
30. Watanabe LA, Wei M, Sun N, Kim D, Chiang CE, Ke Y, Tseng CD, Coloma R, Vala M,Massaad R, Feig P, Guptha S. Effect on blood pressure control of switching fromvalsartan monotherapy to losartan/hydrochlorothiazide in Asian patients with hypertension:results of a multicentre open-label trial. Curr Med Res Opin 2006; 22:1955–1964.
31. Minami J, Abe C, Akashiba A, Takahashi T, Kameda T, Ishimitsu T, Matsuoka H. Longtermef?cacy of combination therapy with losartan and low-dose hydrochlorotiazide inpatients with uncontrolled hypertension. Int Heart J 2007; 48: 177–186.
32. Naidoo DP, Sareli P, Marin F, Aroca-Martinez G, Maritz FJ, Jardim PC, Guerrero AA,Thompson CA, Bero T, Drazka J, Kosmalova V, Dumortier T, Smith RD. Increasedef?cacy and tolerability with losartan plus hydrochlorothiazide in patients withuncontrolled hypertension and therapy-related symptoms receiving two monotherapies.Adv Ther 1999; 16: 187–199.
33. Coca A, Sobrino J, Soler J, Felip A, PelegrưA, MưnguezA,VilaJ,delaSierraA,PlanaJ.Trough-to-peak ratio, smoothness index, and circadian blood pressure pro?le aftertreatment with once-daily ?xed combination of losartan 100 and hydrochlorothiazide in essential hypertension. J Cardiovasc Pharmacol 2002; 39:824–833.
34. Lawes CM, Rodgers A, Bennett DA, Parag V, Suh I, Ueshima H, MacMahon S. Bloodpressure and cardiovascular disease in the Asia Paci?c region. J Hypertens 2003; 21:707–716.
35. Bramlage P, Thoenes M, Paar WD, Bramlage CP, Schmieder RE. Albuminuria: anindicator of cardiovascular risk. Med Klin (Munich) 2007; 102: 833–843.
36. Jafar TH, Chaturvedi N, Hatcher J, Levey AS.Use of albumin creatinine ratio and urinealbumin concentration as a screening test for albuminuria in an Indo-Asian population.Nephrol Dial Transplant 2007; 22: 2194