Bệnh viện Nhân dân 115
Summary
Objective. The aim of this study was to assess the ability of low-dose dobutamine echocardiography (LDDE) to predict recovery of dysfuctional but viable myocardial regions in post uncomplicated acute myocardial infarction (AMI) patients after sucessful coronary revascularization.
Background. Dobutamine echocardiography is a well established evaluation method for myocardial viability assessement in European and American countries but Vietnam.
Methods. Sixty-one patients with first aMI and two or more abnormal wall motion segments at rest underwent LDDE 12 ± 5 days after AMI to evaluate myocardial viability. Revascularization was performed after LDDE 3 ± 4 days by percutaneous coronary intervention (PCI). 2D echocardiography was a reference for left ventricular functional regional improvement, repeated 3 months and 6 months after PCI.
Results. Sensitivity and specificity of LDDE for predicting regional functional recovery after revascularization were 80% and 89%. LDDE show a high accuracy in predicting regional functional recovery at 3 months and 6 months after PCI (79% and 84%, respectively). Left ventricular ejection fraction incrseased from 41% ± 10% at baseline to 52% ± 14% at 6 months (p < 0.0005) in patients with 4 or more viable segments, whereas less although significant improvement was found in less than 4 viable segment patients (from 46% ± 10% to 52% ± 11%, p <0.01). Left ventricular end diastolic volume was also decreased more in 4 or more viable segment group than in less than 3 viable segment one (14 ± 14 mL/m2 vesus 6 ± 12 mL/m2, p < 0.05).
Conclusion. Low -dose dobutamine echocardiography was reliable to predict recovery of viable myocardium after revascularization in post infarction patients.
Chữ viết tắt: bn = bệnh nhân, ĐMV = động mạch vành, ĐCB = độ chuyên biệt, ĐN = độ nhạy, GTTĐA = giá trị tiên đoán âm, GTTĐD = giá trị tiên đoán dương, SATD = siêu âm tim dobutamine, LVEF = phân suất tống máu thất trái, NMCT = nhồi máu cơ tim. PCI = can thiệp mạch vành qua da, RLVĐ = rối loạn vận động.
ĐẶT VẤN ĐỀ
Sau nhồi máu cơ tim (NMCT) cấp, vùng cơ tim rối loạn chức năng co bóp có thể đã bị hoại tử hoặc còn sống. Khác với vùng cơ tim đã bị hoại tử, vùng cơ tim còn sống được chi phối bởi động mạch vành hẹp tới hạn có khả năng hồi phục chức năng sau điều trị tái thông mạch vành. Siêu âm tim dobutamine (SATD) liều thấp là một kỹ thuật đánh giá sống còn cơ tim dựa trên nguyên lý phát hiện bảo tồn dự trữ co bóp của vùng cơ tim còn sống và do đó có thể tiên đoán sự hồi phục chức năng của các vùng này sau tái thông vành. Nhiều nghiên cứu trước đây đã cho thấy giá trị của SATD trong tiên đoán hồi phục chức năng vùng thất trái sau NMCT cấp [1-6]. Tại Hà nội và TP HCM, SATD được sử dụng ở một số bệnh viện, chủ yếu để chẩn đoán BĐMV trên quần thể bệnh nhân đau ngực và ít được dùng trong khảo sát sống còn cơ tim. Vì vậy, chúng tôi thực hiện đề tài nghiên cứu này nhằm đánh giá khả năng của SATD liều thấp trong tiên đoán cải thiện chức năng vùng thất trái (regional LV function) sau điều trị tái thông mạch vành bằng can thiệp mạch vành qua da trên quần thể các bệnh nhân (bn) sau NMCT cấp không biến chứng tại khoa tim mạch bệnh viện Nhân dân 115. Kèm theo chúng tôi cũng đánh giá tính an toàn của kỹ thuật này trên các bn sau NMCT cấp không biến chứng trong nhóm nghiên cứu.
ĐỐI TƯỢNG VÀ PHƯƠNG PHÁP NGHIÊN CỨU
Dân số nghiên cứu. Có 61 bn trong nhóm nghiên cứu được thu thập từ tháng 02/2007 đến tháng 10/2009 (20 tháng) theo trình tự thời gian. Tiêu chuẩn chọn bệnh khi đáp ứng đủ mọi điều kiện sau:
– NMCT cấp lần đầu tiên, chẩn đoán NMCT cấp khi có men tim(CK-MB, Troponin I) tăng trên 2 lần giá trị bình thường kèm theo một hoặc hai biểu hiện: đau thắt ngực kéo dài trên 20 phút, biến đổi trên ECG chứng tỏ có thiếu máu cục bộ (ST chênh lên hoặc chênh xuống) [7].
– Có rối loạn vận động vùng (RLVĐ) ít nhất là 2 vùng thấy được trên siêu âm tim khi nghỉ.
– Đã lên kế hoạch điều trị tái thông mạch vành bằng can thiệp mạch vành qua da (PCI) và được tái thông mạch vành thành công sau đó.
Tiêu chuẩn loại trừ ra khỏi nhóm nghiên cứu khi có một trong các tiêu chuẩn sau:
– NMCT có biến chứng: shock tim, suy tim, loạn nhịp quan trọng như rung thất, nhịp nhanh thất xuất hiện sau nhồi máu ³ 48 giờ, tái đau ngực.
– Đã tái thông mạch vành cấp cứu hoặc có tiền sử điều trị tái thông mạch vành trước đây.
– Có tiền sử NMCT trước đây.
– Hẹp ³ 50% nhánh chính động mạch vành trái
– Có bệnh lý van tim quan trọng (hở van hai lá hoặc van ĐM chủ độ ³ 3)
– Tăng huyết áp quan trọng chưa được điều trị ổn định (>160/90 mmHg)
– Huyết khối nhô vào lòng thất trái (protruding thrombus)
– Cửa sổ siêu âm không thích hợp.
Quy trình nghiên cứu. SATD đánh giá sống còn cơ tim được thực hiện trong vòng 7 – 21 ngày sau NMCT cấp. Can thiệp mạch vành qua da (PCI) được thực hiện sau khi làm SATD. SATD có thể được làm trước hoặc sau chụp mạch vành Tiêu chuẩn vàng cho đánh giá sống còn cơ tim là sự hồi phục chức năng vùng sau PCI. Chức năng vùng được đánh giá bằng siêu âm tim 2D và được thực hiện 3 lần, lần đầu trước PCI (cùng thời điểm với làm SATD), hai lần sau là ở thời điểm 3 tháng và 6 tháng sau PCI. Ở thời điểm 3 và 6 tháng sau PCI, gọi bn lên làm siêu âm tim qua điện thoại.
Quy trình nghiên cứu chính được tóm tắt trong sơ đồ (SĐ).
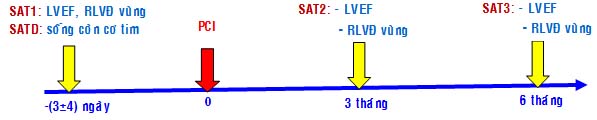
Quy trình siêu âm tim gắng sức bằng dobutamine. Không ngưng các thuốc ức chế beta và dãn vành trước làm SATD. Siêu âm được thực hiện bằng máy siêu âm doppler màu Phillip Envisor C HD có bộ phận xử lý bằng kỹ thuật điện toán chuyên dùng cho SAT gắng sức với đầu dò điện tử có tần số tự động thay đổi trong khoảng 2 – 4 MHz, có áp dụng tính năng thu nh?n hòa âm (Tissue Harmonic Imaging) giúp th
ấy rõ hơn ranh giới của lớp nội mạc với buồng thất trái, thuận lợi cho đánh giá rối loạn vận động vùng và đo phân suất tống máu thất trái trên siêu âm 2D. Dobutamine được truyền tĩnh mạch bằng bơm tiêm điện với liều khởi đầu 5 mg/kg/phút, sau đó tăng lên 10 mg/kg/phút với mỗi giai đoạn kéo dài 5 phút. Bệnh nhân nằm ở tư thế nghiêng trái. Đánh giá vận động vùng trên các mặt cắt cạnh ức trọc dọc, cạnh ức trục ngang, bốn buồng và 2 buồng ở mỏm trên siêu âm 2D. Sau khi kết thúc, đánh giá lại hình ảnh lưu trữ bởi kỹ thuật số: hình ảnh mỗi mặt cắt ở 3 giai đoạn được sắp sếp trên cùng một màn hình chia 4 phần (quad-screen format): trước truyền dobutamine, cuối giai đoạn dobutamine liều 5mg/kg/phút (phút thứ 5) và cuối giai đoạn dobutamine liều 10mg/kg/phút (phút thứ 10). Huyết áp và ECG 12 chuyển đạo được đo ngay trước truyền dobutamine và lặp lại mỗi 2 phút. ECG monitor được theo dõi sát trong suốt quá trình tiến hành nghiệm pháp. Ngưng nghiệm pháp nếu có một trong các biểu hiện sau: rối loạn vận động vùng mới xuất hiện ³ 2 vùng, ST chênh xuống ³ 2 mm, đau ngực, huyết áp tâm thu giảm > 20 mmHg so với ban đầu hoặc huyết áp tăng > 220/120 mmHg.
Phân tích kết quả siêu âm tim. SATD được đánh giá bởi 2 bác sĩ có kinh nghiệm làm SATD trên 5 năm, đánh giá trực tiếp trong quá trình làm và trên hình ảnh lưu trữ bằng kỹ thuật số sau khi kết thúc, lấy ý kiến đồng thuận.
Thành thất trái được chia làm 17 vùng vùng theo khuyến cáo của Hiệp hội siêu âm tim Mỹ [8]. Vận động vùng được chia làm 5 mức [9]: bình thường (normal) = 1 điểm, giảm động (hypokinetic) = 2 điểm, giảm động nặng (severely hypokinetic) = 3 điểm, vô động (akinetic) = 4 điểm, loạn động (dyskinetic) = 5 điểm. Một phân vùng được xếp vào loại giảm động nặng trong thì tâm thu, bề dầy thành tăng rất ít và vận động hướng tâm rất hạn chế. Vô động nếu bề dầy thành mỏng và thì tâm thu không tăng. Loạn động nếu bề dầy thành mỏng, không dầy lên và vận động hướng ra ngoài trong thì tâm thu. Điểm vận động thành (WMS: Wall Motion Score) là tổng số điểm 17 vùng cộng lại và chỉ số điểm vận động thành (WMSI: Wall Motion Score Index) được tính bằng WMS chia cho 17. Vùng cơ tim được động mạch vành (ĐMV) chi phối được tính như sau: ĐMV xuống trước trái nuôi phần giữa và mỏm vách liên thất, toàn bộ thành trước vách và thành trước. Nếu ĐMV phải chiếm ưu thế, nó sẽ nuôi phần đáy dưới vách, thành dưới và thành dưới bên, ĐMV mũ sẽ cung cấp máu cho thành trước bên. Nếu ĐMV trái chiếm ưu thế, ĐMV mũ sẽ nuôi cả thành trước bên và dưới bên, ĐMV phải chỉ nuôi thành dưới và đáy vách liên thất [10].
Khảo sát sống còn cho những vùng cơ tim có rối loạn vận động khi nghỉ từ mức ³ 2 điểm. Các kiểu đáp ứng của vùng rối loạn vận động khi nghỉ với dobutamine liều thấp được phân định như sau: 1/ Cải thiện co bóp từ 1 mức trở lên (theo 5 mức vận động vùng nói trên) dưới dobutamine liều thấp: cơ tim còn sống; 2/ Vận động thành xấu đi trong quá trình truyền dobutamine so với lúc nghỉ: cơ tim còn sống nhưng bị TMCB, gọi là cơ tim tổn thương (jeopardized myocardium); 3/ Không thay đổi: không cải thiện cũng không xấu đi trong quá trình làm là kiểu đáp ứng của vùng cơ tim không còn sống hay vùng bị hoại tử (sẹo).
Được xem là hồi phục chức năng vùng trong thời gian theo dõi 3 – 6 tháng sau PCI nếu vùng rối loạn vận động khi nghỉ trước PCI cải thiện WMS ³ 1 mức, không tính trường hợp loạn động thành vô động.
Phân suất tống máu thất trái được đo theo phương pháp Simpson bốn buồng trên siêu âm 2D và lấy giá trị trung bình cộng của 3 lần đo.
Chụp động mạch vành và can thiệp mạch vành. Có thể can thiệp cùng một lần ngay sau chụp mạch vành hoặc chụp và can thiệp hai lần riêng biệt. ĐMV được xem là hẹp đáng kể khi hẹp ³ 70% đường kính lòng. Dòng chảy tính theo phân độ TIMI (TIMI flow grade) từ 0 đến 3 [11]. Kết quả của can thiệp được dùng để đối chứng xem ĐMV nào đã được can thiệp tốt và từ đó suy ra những vùng cơ tim tương ứng được tái tưới máu sau can thiệp. Chỉ lấy các BN can thiệp tái thông mạch vành thành công. Tiêu chuẩn can thiệp tái thông thành công gồm thành công về kỹ thuật và thành công về lâm sàng. Về mặt kỹ thuật là tốt nếu hẹp tồn lưu sau can thiệp dưới 20%, dòng chảy TIMI 3, không bóc tách hay huyết khối, không mất nhánh bên quan trọng (đường kính lòng mạch ³ 2mm). Về lâm sàng, các bn được theo dõi tại phòng cấp cứu khoa tim mạch trong vòng 24 giờ sau can thiệp. Lâm sàng là tốt nếu bn không đau ngực, khó thở hay tụt huyết áp. Điện tâm đồ và men tim được làm lại ngay sau thủ thuật, 6 giờ và 24 giờ sau thủ thuật hoặc khi có biểu hiện bất thường trên lâm sàng như đau ngực, khó thở, tụt huyết áp không giải thích được. Kết quả can thiệp là tốt nếu trên ECG 12 chuyển đạo, ST không thay đổi so với trước can thiệp; CK – MB và troponin I tăng dưới 3 lần sau can thiệp nếu men tim đã về bình thường ho?c không tăng quá 25% giá trị của lần thử trước can thiệp nếu men tim còn tăng [12].
Phương pháp xử lý thống kê. Số liệu nghiên cứu được xử lý bằng phần mềm thống kê SPSS phiên bản 16.01. Các biến số liên tục được biểu diễn dưới dạng trung bình ± độ lệch chuẩn. Các biến số định tính được ghi nhận bằng tỉ lệ %. Dùng t-test cho các biến định lượng. So sánh 2 tỉ lệ bằng phép kiểm Z. So sánh các biến định tính hoặc bán định lượng bằng phép kiểm Chi bình phương. Tính toán độ nhạy, độ chuyên biệt, giá trị tiên đoán dương và giá trị tiên đoán âm theo định nghĩa chuẩn. Ngưỡng có ý nghĩa thống kê là p < 0.05.
KẾT QUẢ NGHIÊN CỨU
Một số đặc điểm của nhóm bệnh nhân nghiên cứu.
61 bệnh nhân (bn) thỏa tiêu chuẩn chọn bệnh thuộc các khoa nội tim mạch Bệnh viện Nhân dân 115, với các đặc điểm được thể hiện ở Bảng 1.
|
Bảng 1. Một số đặc điểm nền của nhóm BN nghiên cứu |
|
|
Tuổi |
58 ± 11 |
|
Tỉ lệ nam / nữ |
48/13 |
|
Tăng huyết áp |
29 (48%) |
|
Đái tháo đường |
11 (18%) |
|
Hút thuốc lá |
29 (48%) |
|
Rối loạn lipid máu |
48 (12%) |
|
NMCT không ST chênh lên |
11 (18%) |
|
NMCT thành trước |
32 (52%) |
|
NMCT thành dưới |
18 (30%) |
|
Chỉ số thể tích thất trái cuối tâm trương (EDVI) (Ml/ m2) |
56 ± 24 |
|
Chỉ số thể tích thất trái cuối tâm thu (ESVI) (Ml/ m2) |
32 ± 19 |
|
Phân suất tống máu thất trái (LVEF) (%) |
45 ± 10 |
|
Chỉ số điểm vận động thành (WMSI) |
1.77 ± 0.42 |
|
Tắc LAD / LAD liên quan nhồi máu hẹp ≥ 70% |
11/38 |
|
Tắc RCA / RCA liên quan nhồi máu hẹp ≥ 70% |
9/22 |
|
Tắc LCX / LCX liên quan nhồi máu hẹp ≥ 70% |
1/1 |
LAD = nhánh ĐMV xuống trước trái, LCX = nhánh ĐMV mũ, RCA = nhánh ĐMV phải
Siêu âm tim dobutamine: SATD được thực hiện sau NMCT cấp 12 ± 5 ngày và trước PCI 3 ± 4 ngày.
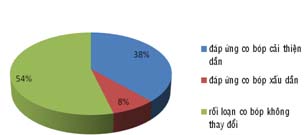
Ơ thời điểm 6 tháng sau PCI, trong số 61 bn nghên cứu có 1 bn bị mất theo dõi do thay đổi số điện thoại không liên lạc được, 1 bn đột tử lúc 5 tháng tại nhà không rõ nguyên nhân. Khảo sát trên 1003 vùng trên 59 bn có 338 vùng RLVĐ khi nghỉ (34%), với 309 vùng (31% tổng số vùng) được điều trị tái tưới máu sau đó bằng phương pháp PCI, trong đó gồm 40 vùng giảm động, 108 vùng giảm động nặng, 156 vùng vô động và 5 vùng loạn động. Số vùng không được điều trị tái tưới máu là 29 vùng. Các kiểu đáp ứng của 307 vùng RLVĐ với dobutamine liều thấp gồm 118 vùng (38%) đáp ứng kiểu co bóp cải thiện dần, 25 vùng (8%) đáp ứng kiểu co bóp xấu dần và 166 vùng (54%) co bóp không thay đổi (biểu đồ 1).
Trong 61 bn nghiên cứu, chỉ có 1 bn xuất hiện cơn nhịp nhanh trên thất không kéo dài (NSVT) ở cuối liều dobutamine 10 mg/kg/phút, tự hết ngay sau ngưng truyền dobutamine.
Theo dõi bằng siêu âm tim 2D sau PCI 3 – 6 tháng. 61 bn được PCI thành công sau SATD 3 ± 4 ngày với 63 stent thường và 26 stent phủ thuốc. Trên 61 bn nghiên cứu, ở thời điểm 3 tháng có 10 bn không đến tái khám vì lý do riêng. Ơ thời điểm 6 tháng có 1 bn đột tử tại nhà 5 tháng sau PCI không rõ nguyên nhân và 1 bn thay đổi số điện thoại không liên lạc được. Như vậy chỉ còn 49 bn được theo dõi siêu âm tim đủ cả hai thời điểm 3 tháng và 6 tháng và 59 bn được làm siêu âm tim ở thời điểm 6 tháng.
Số vùng cơ tim còn sống và hoại tử (không còn sống) xác định trên SATD hồi phục chức năng co bóp sau PCI 6 tháng được thể hiện ở sơ đồ 2.A và bảng 2. Tỷ lệ hồi phục chức năng vùng ở nhóm vùng đáp ứng kiểu còn sống cao hơn nhiều so với ở nhóm vùng đáp ứng kiểu hoại tử trên SATD ( 89% so với 19%, p < 0.0001). Trong số 157 vùng hồi phục chức năng, có 135 vùng hồi phục hoàn toàn chức năng co bóp (85%). Tỉ lệ hồi phục chức năng sau PCI ở nhóm vùng giảm động và giảm động nặng cũng cao h
ơn ở nhóm vùng vô động và loạn động (80% của 148 vùng so với 25% của 161 vùng, p < 0.0001). Tuy nhiên, khi xem xét chỉ trên những vùng còn sống, tỷ lệ hồi phục chức năng vùng giữa các vùng giảm động – giảm động nặng (111/124 vùng) với các vùng vô động – loạn động (16/19 vùng) không khác biệt có ý nghĩa (90% so với 84%).
Sơ đồ 2. Hồi phục chức năng vùng trong khoảng thời gian 3 – 6 tháng sau PCI (vg = vùng, HP = hồi phục)
Trên 49 bn khảo sát được siêu âm tim ở cả hai thời điểm 3 tháng và 6 tháng sau PCI (sơ đồ 2.B) có 246 vùng RLVĐ với 128 vùng hồi phục sau 6 tháng (52%). Ơ thời điểm 3 tháng có 115 vùng (90%) hồi phục chức năng (25 vùng giảm động, 62 vùng giảm động nặng, 28 vùng vô động) trong đó 88 vùng hồi phục hoàn toàn (69%). Ơ thời điểm 6 tháng có 128 vùng hồi phục chức năng (35 vùng giảm động, 62 vùng giảm động nặng và 31 vùng vô động); như vậy chỉ có thêm 13 vùng mới hồi phục (10%), nhưng có đến 102 vùng hồi phục hoàn toàn (80%).
Bảng 2. Phân bố các vùng hồi phục và không hồi phục chức năng sau PCI 6 tháng trên 59 bn theo các mức độ RLVĐ vùng khác nhau
|
Giảm động |
Giảm động nặng |
Vô động |
Loạn động |
||||||||
|
viable |
viable |
nonviable |
viable |
nonviable |
nonviable |
||||||
|
HP |
KHP |
HP |
KHP |
HP |
KHP |
HP |
KHP |
HP |
KHP |
HP |
KHP |
|
37 |
3 |
74 |
10 |
7 |
17 |
16 |
3 |
25 |
112 |
0 |
5 |
Viable = còn sống, nonviable = không còn sống (xác định trên SATD)
HP = hồi phục, KHP = không hồi phục
Khả năng của SATD liều thấp trong tiên đoán hồi phục chức năng vùng thất trái sau PCI trên bn sau NMCT cấp. Số vùng hồi phục và không hồi phục chức năng sau PCI 3 – 6 tháng của các nhóm vùng còn sống hoặc hoại tử / SATD được thể hiện trong bảng 3.
– Từ kết quả ở bảng 3, tính ra khả năng của SATD liều thấp trong tiên đoán cải thiện chức năng vùng sau tái thông mạch vành (bảng 4 và biểu đồ 2, 3).
Chỉ có khác biệt về GTTĐD giữa 2 thời điểm 3 và 6 tháng trên 49 bn là có ý nghĩa
(77% so với 87%, p < 0.05); ĐN, ĐCB, GTTĐA không khác biệt có ý nghĩa (biểu đồ 3).
Bảng 3. Hồi phục chức năng vùng sau PCI 3 – 6 tháng
|
|
Hồi phục (+) |
Hồi phục (-) |
Tổng số vùng |
|
|
3 tháng/ 49 bn |
Số vùng còn sống / SATD |
91 |
28 |
119 |
|
Số vùng hoại tử / SATD |
24 |
103 |
127 |
|
|
Tổng số vùng |
115 |
131 |
246 |
|
|
6 tháng/ 49 bn |
Số vùng còn sống / SATD |
104 |
15 |
119 |
|
Số vùng hoại tử / SATD |
24 |
103 |
127 |
|
|
Tổng số vùng |
128 |
118 |
246 |
|
|
6 tháng/ 59 bn |
Số vùng còn sống / SATD |
127 |
16 |
143 |
|
Số vùng hoại tử / SATD |
32 |
134 |
166 |
|
|
Tổng số vùng |
159 |
150 |
309 |
|
– Từ kết quả ở bảng 3, tính ra khả năng của SATD liều thấp trong tiên đoán cải thiện chức năng vùng sau tái thông mạch vành (bảng 4 và biểu đồ 2, 3).
Bảng 4. Khả năng của SATD liều thấp trong tiên đoán cải thiện chức năng vùng của các vùng cơ tim rối loạn vận động khi nghỉ sau PCI
|
|
3 tháng / 49 bn n = 246 |
6 tháng / 49 bn n = 246 |
6 tháng / 59 bn n = 309 |
|
ĐN % |
79 (91/115) |
81 (104/128) |
80 (127/159) |
|
ĐCB % |
79 (103/131) |
87 (103/118) |
89 (134/150) |
|
GTTĐD % |
77 (91/119) |
87 (104/119) |
89 (127/143) |
|
GTTĐÂ % |
81 (103/127) |
81 (103/127) |
81 (134/166) |
|
ĐCX % |
79% (194/246) |
84 (207/246) |
84 (261/309) |
Chỉ có khác biệt về GTTĐD giữa 2 thời điểm 3 và 6 tháng trên 49 bn là có ý nghĩa
(77% so với 87%, p < 0.05); ĐN, ĐCB, GTTĐA không khác biệt có ý nghĩa (biểu đồ 3).
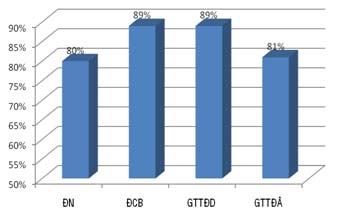
Biểu đồ 2. Khả năng của SATD tiên đoán hồi phục chức năng vùng sau PCI 6 tháng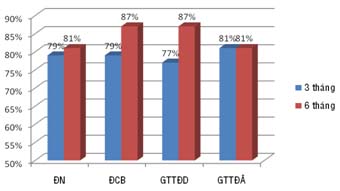
Biểu đồ 3. So sánh khả năng của SATD tiên đoán hồi phục chức năng vùng giữa hai thời điểm 3 và 6 tháng sau PCI
Sự thay đổi các thông số thất trái sau PCI so với trước PCI giữa 2 nhóm có và không có cơ tim còn sống. Các nghiên cứu trước đây đã xác định LVEF có khả năng cải thiện sau tái thông vành nếu có một lượng nhất định số vùng cơ tim RLVĐ nhưng còn sống, số vùng này thay đổi trong khoảng 2 – 4 vùng tùy nghiên cứu trong đó ³ 4 vùng được nhiều nghiên cứu xác định nhất [16]. Dựa trên kết quả này, chúng t
ôi chia các 59 bn trong nhóm nghiên cứu được theo dõi ở thời điểm sau PCI 6 tháng thành 2 phân nhóm: nhóm A có ³ 4 vùng cơ tim còn sống và nhóm B có < 4 vùng cơ tim còn sống, sau đó so sánh một số đặc điểm nền và sự thay đổi các thông số thất trái sau PCI giữa hai phân nhóm này. Kết quả thể hiện trong bảng 4. Các đặc điểm nền không khác biệt giữa hai nhóm. Mức giảm thể tích thất trái cuối tâm trương, mức tăng LVEF và mức giảm WMSI ở phân nhóm có cơ tim còn sống ³ 4 vùng đều nhiều hơn ở phân nhóm có cơ tim còn sống < 4 vùng có ý nghĩa.
Bảng 4. So sánh một số đặc điểm nền và sự thay đổi các thông số của thất trái sau PCI giữa hai phân nhóm bệnh nhân có số vùng RLVĐ còn sống ≥ 4 và < 4 vùng
|
|
Phân nhóm A (n = 16) |
Phân nhóm B (n = 43) |
p |
|
|
Tuổi |
59 ± 6 |
58 ± 12 |
NS |
|
|
Phái (nam / nữ) |
12/4 |
32/9 |
NS |
|
|
Đái tháo đường |
7/16 |
20/43 |
NS |
|
|
Tăng huyết áp |
7/16 |
21/22 |
NS |
|
|
Hút thuốc lá |
3/16 |
7/36 |
NS |
|
|
Rối loạn lipid máu |
12/16 |
31/43 |
NS |
|
|
NMCT cấp thành trước |
9/16 |
21/22 |
NS |
|
|
EDVI trước PCI (mL/m2) |
59 ± 21 |
55 ± 25 |
NS |
|
|
ESVI trước PCI (mL/m2) |
36 ± 18 |
31 ± 19 |
NS |
|
|
LVEF trước PCI (%) |
41 ± 10 |
46 ± 10 |
NS |
|
|
WMSI trước PCI |
1.9 ± 0.4 |
1.7 ± 0.4 |
NS |
|
|
EDVI sau PCI 6 tháng (mL/m2) |
45 ± 16 |
48 ± 21 |
NS |
|
|
ESVI sau PCI 6 tháng (mL/m2) |
22 ± 14 |
23 ± 14 |
NS |
|
|
LVEF sau PCI 6 tháng(%) |
52 ± 14 |
52 ± 11 |
NS |
|
|
WMSI sau PCI 6 tháng |
1.4 ± 0.5 |
1.6 ± 0.5 |
NS |
|
|
Mức giảm EDVI sau PCI 6 tháng (mL/m2) |
14 ± 14 |
6 ± 12 |
0.048* |
|
|
Mức giảm ESVI sau PCI 6 tháng (mL/m2) |
13 ± 12 |
7 ± 13 |
NS |
|
|
Mức tăng LVEF sau PCI 6 tháng |
11 ± 9 |
6 ± 5 |
0.005* |
|
|
Mức giảm WMSI sau PCI 6 tháng |
0.5 ± 0.4 |
0.1 ± 0.2 |
0.004* |
|
Các biến cố trong thời gian theo dõi 6 tháng sau PCI. Trong thời gian theo dõi 6 tháng sau PCI, có 1 bn đột tử tại nhà không rõ nguyên nhân, 1 bn nhập viện 1 đợt 3 ngày lúc 5 tháng do suy tim NYHA III không chụp mạch vành sau đó và 1 bn nhập viện một đợt 6 ngày do đau ngực không đặc hiệu.
BÀN LUẬN
Một thực tế tại bệnh viện Nhân dân 115, bn nhiều bn bị NMCT cấp đến nhập viện muộn vài ngày sau NMCT trong tình trạng đã ổn định, hết đau ngực và quá thời gian thích hợp cho can thiệp tái thông mạch vành sớm (tỉ lệ bn NMCT cấp được PCI cấp cứu chỉ là 7.5%) [22]. Lúc này, ngoài đánh giá thiếu máu cục bộ tồn lưu, đánh giá sống còn của vùng cơ tim RLVĐ khi nghỉ cũng là một yếu tố quan trọng giúp chọn lựa các bn có được lợi ích từ điều trị tái thông mạch vành muộn trong giai đoạn NMCT bán cấp.
Kết quả nghiên cứu này của chúng tôi đã chứng tỏ trên các
bn NMCT cấp lần đầu không biến chứng, SATD liều thấp có thể tiên đoán tốt khả năng cải thiện chức năng vùng của các vùng RLVĐ khi nghỉ sau can thiệp tái thông mạch vành các ĐMV thủ phạm còn hẹp quan trọng (³ 70%).
Thời điểm làm SATD: Trong các nghiên cứu về SATD đánh giá sống còn cơ tim sau NMCT cấp không biến chứng, bn được làm SATD trong vòng 3 – 21 ngày sau NMCT cấp [1 – 6]. Các bn trong nhóm nghiên cứu của chúng tôi được làm SATD trong vòng 7 – 21 ngày sau NMCT cấp. Chúng tôi chọn thời điểm sớm nhất là 7 ngày sau NMCT cấp không biến chứng để bn hoàn toàn ổn định với điều trị nội khoa và hạn chế tối đa các tai biến có thể xảy ra khi làm SATD trên nhóm đối tượng này.
Phương thức tiêm truyền dobutamine và tính an toàn: Có hai phương thức tiêm truyền dobutamine chủ yếu được sử dụng trong kỹ thuật SATD đánh giá sống còn cơ tim gồm phương thức liều thấp và phương thức liều cao. Dobutamine liều thấp (5 – 10 µg/kg/ph) làm tăng co bóp cơ tim, ít gây tăng nhịp tim và huyết áp, do đó giúp phát hiện dự trữ co bóp của vùng RLVĐ khi nghỉ nhưng còn sống và thường không gây TMCB. Dobutamine liều cao ³ 20 µg/kg/ph giúp phát hiện TMCB do gắng sức. Hơn nữa, đáp ứng hai pha (biphasic response: cải thiện co bóp ở dobutamine liều thấp và xấu lại ở dobutamine liều cao) theo kết quả của một số nghiên cứu có độ tin cậy cao hơn trong tiên đoán hồi phục chức năng vùng [13], [14]. Tuy nhiên, nguy cơ xuất hiện các tai biến nghiêm trọng gây ra do TMCB (như NMCT, nhịp nhanh thất, rung thất, thậm chí tử vong) sẽ tăng, nhất là ở nhóm các bn sau NMCT cấp. Trong một nghiên cứu sổ bộ đa trung tâm, tần suất tử vong của phương thức chuẩn (liều cao) khoảng 1/5000 và tần suất các tai biến nghiêm trọng khoảng 3/1000 [15]. Vì lý do an toàn cho bn và kinh nghiệm làm SATD liều cao trên nhóm bn sau NMCT cấp chưa có nhiều, chúng tôi chọn phương thức dobutamine liều thấp. Tỉ lệ các tai biến nghiêm trọng của kỹ thuật trong nghiên cứu của chúng tôi thấp, chỉ có 1/64 bn bị cơn nhịp nhanh trên thất ngắn (NSVT) ở liều dobutamine 10 µg/kg/ph, tự hết khi ngưng truyền dobutamine.
Khả năng của SATD liều thấp trong tiên đoán hồi phục chức năng vùng: Trong 309 vùng RLVĐ khi nghỉ được điều trị tái tưới máu trong nghiên cứu của chúng tôi có 143 vùng đáp ứng kiểu còn sống và 166 vùng đáp ứng kiểu hoại tử trên SATD. Tỉ lệ hồi phục chức năng vùng sau PCI 6 tháng ở nhóm vùng đáp ứng kiểu còn sống cao hơn nhiều so với nhóm vùng đáp ứng kiểu hoại tử (89% so với 19%, p < 0.0001). Như vậy rõ ràng đáp ứng kiểu cơ tim còn sống xác định bằng SATS có khả năng tiên đoán tốt hồi phục chức năng vùng sau điều trị tái thông vành cho các vùng RLVĐ khi nghỉ trước đó. Tính toán từ dữ liệu nghiên cứu của chúng tôi, SATD có độ nhậy 80%, độ chuyên biệt 89%, giá trị tiên đoán dương 89%, giá trị tiên đoán âm 81% và độ chính xác 84% trong tiên đoán hồi phục chức năng vùng của các vùng RLVĐ khi nghỉ sau điều trị tái thông mạch vành 6 tháng. Trong tổng kết của Schinkel và cộng sự [16] phân tích các nghiên cứu từ năm 1980 – 2007 của tất cả các kỹ thuật chẩn đoán hình ảnh đánh giá sống còn cơ tim, có 41 nghiên cứu (1411 bn) về SATD trong đó 33 nghiên cứu (1121 bn) sử dụng dobutamine liều thấp, cho thấy SATD là một kỹ thuật có độ chính xác cao trong tiên đoán hồi phục chức năng vùng với trung bình độ nhậy, độ chuyên biệt, giá trị tiên đoán dương, giá trị tiên đoán âm của các nghiên cứu lần lượt là 79%, 78%, 76% và 82%. độ nhậy dao động trong khoảng 57 – 91%, độ chuyên biệt dao động trong khoảng 44 – 85%, giá trị tiên đoán dương dao động trong khoảng 60 – 88% và giá trị tiên đoán âm dao động trong khoảng 55 – 94%. Kết quả nghiên cứu của chúng tôi nằm trong khoảng thay đổi này. Độ nhậy và độ chuyên biệt của các nghiên cứu về SATD trong tiên đoán hồi phục chức năng vùng sau tái thông mạch vành có thể thay đổi phụ thuộc vào một số yếu tố như tỉ lệ mức độ nặng của rối loạn vận động vùng, hay nói cách khác, mức độ thay đổi cấu trúc cũng như số lượng tế bào cơ tim còn sống trong các vùng RLVĐ của dân số nghiên cứu hay thời gian theo dõi của các nghiên cứu. Nghiên cứu của Baumgarner và cs cho thấy ở các vùng có số lượng tế bào còn sống > 50% độ nhạy và độ chuyên biệt của SATD lần lượt là 76% và 82%, nếu tính ở các vùng có số lượng tế bào còn sống > 25% thì độ nhạy giảm xuống còn 66% và độ chuyên biệt vẫn ở mức 81% [17].
Có 8% vùng còn sống (17/219 vùng) xác định trên SATD không hồi phục chức năng trong nghiên cứu của chúng tôi. Nhiều nghiên cứu đã đưa ra một số lý do có thể làm vùng cơ tim còn sống không hồi phục chức năng sau PCI [3], [16]. Các yếu tố trước tái thông mạch gồm: 1/ tổn thương tế bào quá nặng làm cơ tim không hồi phục được chức năng co bóp; 2/ sẹo NMCT dưới nội mạc: vùng cơ tim còn sống một phần nhưng có sẹo ở lớp cơ dưới nội mạc sẽ không cải thiện chức năng sau tái thông mạch vành; 3/ sẹo lớn gần vùng còn sống có thể ngăn cản vùng này hồi phục chức năng. Các yếu tố trong và sau tái thông mạch gồm: 1/ tái thông mạch không hoàn toàn; 2/ tổn thương TMCB gây ra trong lúc tái thông mạch có thể làm cơ tim còn sống chuyển dạng thành mô sẹo, 3/ tái hẹp trong stent.
Tỉ lệ vùng rối loạn vận động khi nghỉ không còn sống xác định trên SATD vẫn hồi phục chức năng sau tái thông vành trong nghiên cứu của chúng tôi là 19%. Ngoài hạn chế của kỹ thuật, hạn chế của bác sĩ đánh giá kết quả, chúng tôi nghĩ hiện tượng tái cấu trúc sau NMCT có thể là một nguyên nhân đáng kể trong nghiên cứu của chúng tôi. Hiện tượng tái cấu trúc sau NMCT (hoặc vùng rối loạn chức năng bị biến đổi cấu trúc nặng) gây dãn vùng nhồi máu làm cho việc phân định tính sống còn của vùng kề cận có thể bị nhầm lẫn, ví dụ vùng mỏm vách bị nhồi máu sẽ dãn rộng ra lấn sang vị trí của vùng giữa vách kề cận làm chẩn đoán nhầm cả vùng giữa lẫn vùng mỏm vách đều không còn sống trong khi thực chất chỉ có vùng mỏm bị. Sau điều trị tái thông vành, tình trạng tái cấu trúc của vùng mỏm vách được cải thiện làm vùng này thu hẹp lại, và vùng giữa vách lúc này được diễn giải lầm là hồi phục. Lý luận này của chúng tôi cũng dựa trên và kết quả của các nghiên cứu về tính sống còn có đối chứng với giải phẫu bệnh, kết quả này cho thấy ngay cả trong NMCT xuyên thành, hiếm khi toàn bộ các tế bào cơ tim bị phá hủy ở vùng nhồi máu. Hầu như luôn có một số lượng tế bào được để dành, phần lớn ở vùng dưới t
hượng mạc [18]. Sự hiện diện của cơ tim còn sống ở lớp ngoài của thành thất không giúp hồi phục chức năng vùng khi nghỉ nhưng có thể góp phần chống tái cấu trúc, duy trì hình dạng và kích thước thất trái nhờ ngăn cản vùng nhồi máu dãn rộng[19]. Các chỉ số về sự thay đổi kích thước thất trái sau PCI trong nghiên cứu của chúng tôi cũng ủng hộ lý luận này, ở 43 bn có số vùng cơ tim còn sống không đáng kể (< 4 vùng) thể tích thất trái cuối tâm trương và tâm thu sau PCI 6 tháng vẫn giảm có ý nghĩa so với trước PCI với chỉ số thể tích thất trái cuối tâm trương trước và sau PCI lần lượt là 55 ± 25 mL/m2 và 48 ± 21 mL/m2, p < 0.005; chỉ số thể tích thất trái cuối tâm thu trước và sau PCI lần lượt là 31 ± 20 mL/m2 và 23 ± 14 mL/m2, p < 0.005.
Một tỉ lệ cải thiện co bóp cũng được ghi nhận ở những vùng RLVĐ không được tái thông trong một số nghiên cứu và được lý giải do 2 khả năng [20]: 1/ Hồi phục tự phát của cơ tim choáng váng sau NMCT; 2/ Cải thiện dần tưới máu do tuần hoàn bàng hệ phát triển. Tỉ lệ này trong nghiên cứu của chúng tôi là 7% (2/29 vùng).
So sánh sự hồi phục chức năng vùng của các vùng RLVĐ ở các mức độ khác nhau: nghiên cứu của Bolognese và cs cho thấy vùng giảm động có nhiều khả năng còn dự trữ co bóp hơn vùng vô động và loạn động, hồi phục chức năng vì thế cũng thường gặp ở các vùng RLVĐ ở mức độ nhẹ hơn so với các vùng RLVĐ nặng [1]. Kết quả nghiên cứu của chúng tôi cũng thống nhất với kết quả của nghiên cứu này: 84% của nhóm vùng giảm động và giảm động nặng còn dự trữ co bóp so với chỉ có 12% của nhóm vùng vô động và loạn động còn dự trữ co bóp; với tần suất hồi phục ở các vùng giảm động và giảm động nặng cao hơn đáng kể tần suất này ở các vùng vô động và loạn động (80% so với 25%, p < 0.0001). Có thể lý giải điều này dựa trên giả thuyết: vùng giảm động chứa hỗn hợp mô cơ tim bình thường, cơ tim còn sống và mô sẹo trong khi đó mô sẹo nổi trội ở vùng vô động và loạn động. Tuy nhiên, khi xem xét chỉ trên những vùng còn sống xác định bằng SATD, không thấy khác biệt đáng kể về tỷ lệ hồi phục chức năng vùng giữa các vùng giảm động – giảm động nặng so với các vùng vô động – loạn động (nghiên cứu của Bolognese và cs là 87% so với 91% [1], nghiên cứu của chúng tôi là 90% so với 84%). Nói cách khác, những vùng cơ tim đáp ứng tăng co bóp dưới tác dụng của dobutamine liều thấp chứng tỏ bộ phận co bóp (contractile apparatus) còn nguyên vẹn và có khả năng hồi phục chức năng tâm thu bất chấp mức độ RLVĐ vùng khi nghỉ.
Bàn luận về thời gian hồi phục chức năng vùng: Trên 49 bn trong nghiên cứu của chúng tôi được theo dõi ở cả 2 thời điểm 3 tháng và 6 tháng, trong số 119 vùng còn sống xác định trên SATD, 77% số vùng hồi phục ở thời điểm 3 tháng và có thêm 10% số vùng hồi phục muộn hơn ở thời điểm 6 tháng, tương tự nghiên cứu của Bolognese và cs với tỉ lệ vùng còn sống hồi phục ở thời điểm 3 tháng là 74% và vùng hồi phục thêm ở thời điểm 6 tháng là 15% (n = 127) [1]. Ơ các nghiên cứu trên nhóm bn sau NMCT cấp, khả năng tỉ lệ vùng RLVĐ do cơ tim choáng váng cao hơn cơ tim ngủ đông và do đó hồi phục chức năng sớm hơn so với nhóm bn bị BĐMV mạn.
So sánh sự thay đổi một số thông số thất trái sau PCI giữa phân nhóm có số vùng cơ tim còn sống ³ 4 vùng với phân nhóm có số vùng cơ tim còn sống < 4 vùng: nhóm các bn có số vùng cơ tim còn sống ³ 4 vùng cho thấy cải thiện các thông số về chức năng co bóp thất trái sau PCI 6 tháng so với nhóm các bn có số vùng cơ tim còn sống < 4 vùng, bao gồm trung bình mức tăng LVEF là 11 ± 9 so với 6 ± 5, p < 0.01 và trung bình mức giảm WMSI là 0.5 ± 0.4 so với 0.1 ± 0.2, p < 0.01. Ngoài ra, trung bình mức giảm thể tích thất trái cuối tâm trương cũng giảm nhiều hơn ở nhóm có số vùng cơ tim còn sống = 4 vùng so với nhóm có số vùng cơ tim còn sống < 4 vùng (14 ± 14 mL/m2 so với 6 ± 2 mL/m2, p < 0.05). Như vậy, ngoài ích lợi trên chức năng co bóp thất trái, một số nghiên cứu trước đây đã đưa ra nhận xét kích thước thất trái giảm sau PCI ở nhóm bn có số vùng cơ tim còn sống nhiều hơn gợi ý lượng cơ tim còn sống được điều trị tái tưới máu có thể là một yếu tố chống lại quá trình tái cấu trúc thất trái trên các bn bị BĐMV có rối loạn chức năng tâm thu thất trái, đặc biệt là các bn sau NMCT [21]. Tuy nhiên để có câu trả lời rõ ràng cho vấn đề này, cần có những nghiên cứu với cỡ mẫu lớn so sánh 2 nhóm có và không có cơ tim còn sống đáng kể được phân ngẫu nhiên vào điều trị tái thông cơ học hoặc điều trị nội khoa tối ưu.
HẠN CHẾ CỦA ĐỀ TÀI
Phân tích chức năng vùng trong đánh giá sống còn bằng SATD là phương pháp định tính và bán định lượng do đó mang tính chủ quan phụ thuộc vào kinh nghiệm của người đánh giá, nhưng giá trị của phương pháp đánh giá này của SATD trong phát hiện cơ tim còn sống đã được công nhận một cách rộng rãi và đến nay vẫn còn là phương pháp đánh giá chuẩn. Các bn trong nghiên cứu của chúng tôi không được chụp mạch vành lại đánh giá sự thông thương của stent và biết chắc tất cả các vùng được tưới máu đầy đủ. Tái hẹp sau PCI có thể ngăn cản hồi phục chức năng của một số vùng còn sống và do đó ảnh hưởng đến kết quả nghiên cứu. Tuy nhiên, các bn trong nhóm nghiên cứu của chúng tôi khá ổn định trong thời gian theo dõi 6 tháng sau PCI và các biến cố mạch vành ghi nhận được có tỷ lệ rất thấp. Một hạn chế nữa là cỡ mẫu trong nghiên cứu của chúng tôi còn nhỏ nên chưa có tính đại diện cao.
KẾT LUẬN
Trong những năm gần đây, xác định sự hiện diện và mức độ cơ tim còn sống nhưng rối loạn chức năng co bóp đã trở thành một phần quan trọng trong đánh giá lâm sàng các bn bị BĐMV có rối loạn chức năng thất trái trong đó có một số lượng đáng kể các bn sau NMCT cấp, giúp chọn lựa các bn được nhiều lợi ích từ điều trị tái thông vành. Kết quả nghiên cứu của chúng tôi cho thấy SATD liều thấp là kỹ thuật có độ chính xác cao trong tiên đoán hồi phục chức năng vùng vùng thất trái sau điều trị tái thông mạch vành bằng PCI trên quần thể các bn sau NMCT cấp không biến chứng. SATD cũng là một phương tiện chẩn đoán xác định sống còn cơ tim đơn giản, ít tốn kém và có tính khả thi cao, có thể triển khai ở nhiều bệnh viện trong các thành phố và bệnh viện tỉnh.
TÀI LIỆU THAM KHẢO
1. Bolognese L, Buonamici P, Santini A, et al. Early dobutamine echocardiography predicts improvemment in regional and global left ventricular function after reperfused acute myocardial infarction without residual stenosis of the infacrt-related artery. Am Heart J 2000;139:153-63.
2. Leclerccq F, Messner-Pellenc P, Morague C, et al. Myocardial viability assessed by dobutamine echocardiography in acute myocardial infarction after successful primary coronary angioplasty. Am J Cardiol 1997;80:6-10.
3. Monin JL, Garot J, Scherrer-Crosbie M, et al. Prediction of functional recovery of viable myocardium after delayed revascularization in postinfarction patients. J Am Coll Cardiol 1999;34:1012-9.
4. Galli M, Marcassa C, Bolli R, et al. Spontaneous delayed recovery of perfusion and contraction after the first 5 weeks after anterior infarction: Evidence for the presence of hibernating myocardium in the infarcted area. Circulation 1994;90:1386-97.
5. Poli A, Previtali M, Lanzarini L, et al. Comparison of dobutamine stress echocardiography with dipyridamole stress echocardiography for detection of viable myocardium after myocardial infarction treated with thrombolysis. Heart 1996;75:240-246.
6. Smart SC, Sawada S, Ryan T, et al. Low-dose dobutamine echocardiography detects reversible dysfunction after throbolytic therapy on acute myocardial infarction. Circulation 1993;88:405-415.
7. Thygesen K, Alpert JS, White HD. Universal definition of myocardial infartion: Kristian Thygesen, Joseph S. Alpert and Harvey D. White on behalf of the Joint ESC/ACCF/AHA/WHF Task force for the redefinition of myocardial infartion. Eur Heart J 2007;28:2525-2538.
8. Cerqueira MD; Weissman NJ; Dilsizian V, et al. Standardized myocardial segmentation and nomenclature for tomographic imaging of the heart: a statement for healthcare professionals from the Cardiac Imaging Committee of the Council on Clinical Cardiology of the American Heart Association. Circulation 2002:105(4):539-42.
9. Feigenbaum H, Amstrong Wf, Ryan T (2005). Feigenbaum’s echocardiography. Lippincott Williams & Wilkins, USA, 6th edition, pp 437 – 487.
10. Lang RM; Bierig M; Devereux RB, et al. Recommendations for chamber quantification: a report from the American Society of Echocardiography’s Guidelines and Standards Committee and the Chamber Quantification Writing Group, developed in conjunction with the European Association of Echocardiography, a branch of the European Society of Cardiology. J Am Soc Echocardiogr. 2005;18(12):1440-63.
11. Popma JJ (2008). Braunwald’s heart disease, a textbook of cardiovascular medicine. Elsevier, USA, 8th edition, pp 423-456.
12. ACC/AHA/SCAI 2005 Guideline Update for Percutaneous Coronary Intervention. A Report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines (ACC/AHA/SCAI Writing Committee to Update the 2001 Guidelines for Percutaneous Coronary Intervention).
13. Afridi I, Kleiman NS, Raizner AE, et al. Dobutamine echocardiography in myocardial hibernation. Optimal dose and accuracy in predicting recovery of ventricular function after coronary angioplasty. Circulation 1995;91: 663 – 70.
14. Cornel JH, Bax JJ, Elhendy A, et al. Biphasic response to dobutamine predicts improvement of global left ventricular function after surgical revascularization in patients with stable coronary artery disease: implications of time course of recovery on diagnostic accuracy. J Am Coll Cardiol 1998 ;31:1002-10.
15. Sicari R, Nihoyannopoulos P, Evangeliste A, et al. Stress echocardiography expert consensus statement. European Journal of Echocardiography 2008;9:415-437.
16. Schinkel FL, Bax JJ, Poldermans D, Elhendy A, Ferrari R, Rahimtoola SH. Hibernating myocardium: diagnosis and patient outcomes. Curr Probl Cardiol 2007;32:375-410.
17. Baumgartner H, Porenta G, Lau YK, et al. Assessment of myocardial viability by dobutamine echocardiography, positron emission tomography and thallium-201 SPECT: correlation with histopathology in explanted hearts. J Am Coll Cardiol 1998;32:1701-8.
18. Carluccio E, Biagioli P, Alunni G, et al. Patients with hibernating myocardium show altered lelf ventricular volumes and shape, which revert after revarsculavization . J Am Col Cardiol 2006; 47 :969 -977.
19. Bonow RO. Identification of viable myocardium. Circulation 1996; 94:2674.
20. Paolo G, Camici, Sanjay KP, et al. Stunning, hibernation, and assessment of myocardial viability. Circulation 2008;117:103-114.
21. Diopisopoulos P, Smart SC, Sagar KB. Dobutamine stress echocardiography predict left ventricular remodeling after acute myocardial infarction. J Am Soc Echocardiogr 1999;12:777-84.
22. Trần lệ diễm Thúy, Trần thị thanh Phương, Nguyễn thị Tuyết, Trương phan thu Loan, Nguyễn thanh Hiền. Khảo sát một số đặc điểm lâm sàng, cận lâm sàng và phương pháp điều trị bệnh nhân hội chứng mạch vành cấp từ 01-01-2004 đến 31-12-2006. Kỷ yếu hội nghị tim mạch miền Nam tháng 11 – 2007.









