Biên dịch: BS. CKII. Nguyễn Hoàng Dũng
Khoa Hồi sức Phẫu thuật tim, BV Chợ Rẫy
Hiệu đính: TS. BS. Ngô Minh Hùng
Khoa Tim mạch can thiệp, BV Chợ Rẫy
Chia-Te Liao1,2, Jin-Long Huang3,4, Huai-Wen Liang5, Fa-Po Chung4,6, Ying-Hsiang Lee7,8, Po-Lin Lin7,9, Wei-Ru Chiou7,10, Wen-Yu Lin11, Chien-Yi Hsu4,12,13 and Hung-Yu Chang4,14
TÓM TẮT
Mục tiêu Ivabradine đã được sử dụng ở những bệnh nhân suy tim mạn tính (ST) với phân suất tống máu giảm (HFrEF) và đồng thời có nhịp xoang ≥70 lần/phút. Việc sử dụng thuốc này trong HFrEF cấp vẫn còn lo ngại. Nghiên cứu này sử dụng cơ sở dữ liệu đa trung tâm thực tế để khảo sát tác dụng của ivabradine ở những bệnh nhân HFrEF mất bù cấp trước khi xuất viện.
Phương pháp và kết quả Những bệnh nhân HFrEF mất bù cấp được xác định qua hồi cứu của nghiên cứu này đã được dùng ivabradine lúc xuất viện từ hai cơ sở dữ liệu ST đa trung tâm. Phương pháp ghép điểm xu hướng đã được thực hiện để điều chỉnh các yếu tố gây nhiễu. Tỷ lệ tử vong do tim mạch, tử vong do mọi nguyên nhân và nguy cơ tái nhập viện do ST tái phát sau đó được so sánh giữa những bệnh nhân có và không điều trị ivabradine. Sau khi ghép điểm xu hướng 1:2, 876 bệnh nhân (tuổi, 60,7 ± 14,6 tuổi; nữ, 23,2%; phân suất tống máu thất trái, 28,2% ± 7,8%; và tần số tim lúc xuất viện, 84,3 ± 13,8 lần/phút) được đưa vào phân tích cuối cùng, tương ứng bao gồm 292 và 584 bệnh nhân có và không có điều trị ivabradine khi xuất viện. Không thấy có sự khác biệt đáng kể nào về đặc điểm cơ bản giữa hai nhóm. Tại thời điểm theo dõi 1 năm, bệnh nhân trong nhóm ivabradine có tần số tim thấp hơn đáng kể (77,6 ± 14,7 so với 81,1 ± 16,3 l/p P = 0,005) và triệu chứng cơ năng ST mức độ nặng thấp hơn (Phân độ chức năng của Hiệp hội Tim mạch New York, 2,1 ± 0,7 so với 2,3 ± 0,9; P <0,001) so với nhóm không dùng ivabradine. Những bệnh nhân sử dụng Ivabradine có nguy cơ tử vong do tim mạch trong 1 năm thấp hơn đáng kể (5,8 so với 12,2 trên 100 người năm; P = 0,003), tử vong do mọi nguyên nhân (7,2 so với 14,0 trên 100 người; P = 0,003) và tổng tái nhập viện do ST (42,3 so với 72,6 trên 100 người năm; P <0,001) so với người không sử dụng ivabradine. Sau khi phân tích đa biến, việc kê đơn ivabradine trước khi xuất viện vẫn liên quan độc lập với tỷ lệ tử vong do mọi nguyên nhân trong 1 năm thấp hơn (tỷ số nguy cơ 0,45; khoảng tin cậy 95%, 0,28–0,74; P = 0,002) và tử vong do tim mạch (tỷ số nguy cơ 0,41; khoảng tin cậy 95%, 0,24–0,72; P = 0,002).
Kết luận Kết quả nghiên cứu hiện tại cho thấy điều trị bằng ivabradine có liên quan đến giảm nguy cơ tử vong do tim mạch, tử vong do mọi nguyên nhân và tái nhập viện do ST trong vòng 1 năm ở những bệnh nhân HFrEF mất bù cấp trong dân số thực tế.
Từ khoá Suy tim; Nhập viện; Ivabradine; Tỷ lệ tử vong; Thực tế
LỜI MỞ ĐẦU
Suy tim (ST) là một vấn đề sức khỏe cộng đồng toàn cầu do tiêu tốn nguồn lực đáng kể. Ngoài việc gây tử vong cao, ST còn tác động bất lợi đến chất lượng cuộc sống.1 Tái nhập viện vì ST xảy ra ngay sau khi xuất viện đã trở thành một vấn đề đặc biệt rắc rối.2 Mặc dù có những tiến bộ trong điều trị ST, tỷ lệ tái nhập viện và tử vong vẫn còn cao, dẫn đến gánh nặng lớn cho kinh tế và xã .hội3–5 Dữ liệu gần đây cho thấy tỷ lệ mắc ST ở Đông Nam Á tương tự như ở các nước phương Tây, với tỷ lệ tái nhập viện trong 30 ngày dao động từ 3% đến 15%.6 Ngoài ra, tỷ lệ tử vong do mọi nguyên nhân trong 1 năm sau nhập viện do ST mất bù cấp dao động khoảng 9,2% đến 37,5%.7 Trong Sổ bộ Hoa Kỳ được công bố gần đây tuyển chọn > 10.000 bệnh nhân, 56% bệnh nhân tái nhập viện trong vòng 30 ngày vì các biến cố HF nặng hơn. Tuy nhiên, việc sử dụng các liệu pháp chăm sóc tiêu chuẩn cả trước và sau khi khởi phát ST nặng hơn còn thấp.8 Những phát hiện này nhấn mạnh tầm quan trọng của việc giáo dục bệnh nhân đầy đủ, tối ưu hóa hơn nữa liệu pháp theo hướng dẫn hiện có và các chiến lược dược lý mới.
Liệu pháp giảm nhẹ ST đường uống, bao gồm thuốc ức chế men chuyển (ACEi), thuốc ức chế thụ thể angiotensin (ARB), thuốc ức chế beta và thuốc đối kháng thụ thể mineralocorticoid (MRA) nên được tiếp tục và/hoặc khởi đầu sau khi đạt được sự ổn định huyết động trong thời gian nhập viện vì ST cấp, dựa theo hướng dẫn khuyến cáo9. Thử nghiệm SHIFT (Thử nghiệm Điều trị suy tim Tâm thu bằng chất ức chế kênh If ivabradine) đã chứng minh ivabradine góp phần vào tác dụng có lợi ở những bệnh nhân có nhịp xoang và tần số tim ≥70 nhịp mỗi phút10. Tuy nhiên, nghiên cứu SHIFT tuyển chọn những bệnh nhân đã nhập viện vì ST trong vòng 12 tháng trước đó nhưng không phải trong vòng 4 tuần trước đó. Khoảng 73% bệnh nhân nhập viện vì ST và phân suất tống máu giảm (HFrEF) có nhịp tim ≥70 l/p khi xuất viện và tỷ lệ tử vong do mọi nguyên nhân trong 1 năm, tỷ lệ tái nhập viện và chi phí y tế tương ứng cao hơn đáng kể11. Do đó, việc tối ưu hóa việc kiểm soát tần số tim sau giai đoạn cấp của HFrEF là một vấn đề quan trọng. Bởi vì thử nghiệm SHIFT không bao gồm những bệnh nhân đã xuất viện kể từ lần đầu nhập viện vì ST mất bù cấp, lợi ích lâm sàng của ivabradine trên những bệnh nhân này ít rõ ràng hơn. Trong bối cảnh đó, hai đoàn hệ đa trung tâm của bệnh nhân ST ở Đài Loan đã được sử dụng để đánh giá tác dụng của ivabradine được kê đơn trước khi xuất viện ở những bệnh nhân nhập viện vì HFrEF mất bù cấp.
PHƯƠNG PHÁP
Thiết kế nghiên cứu và đặc điểm bệnh nhân
Nghiên cứu này trích xuất và phân tích dữ liệu từ hai đoàn hệ ST đa trung tâm ở Đài Loan: (1) sổ bộ TSOC-HFrEF khởi đầu bởi Hiệp hội Tim mạch Đài Loan chứa dữ liệu nghiên cứu quan sát, đa trung tâm, tiến cứu của 1.509 bệnh nhân HFrEF đã nhập viện gần đây vì ST tại 21 bệnh viện ở Đài Loan từ năm 2013 đến năm 2014,12 và (2) một nghiên cứu ST hồi cứu, đa trung tâm khởi đầu bởi điều tra viên chính, bao gồm 1.845 bệnh nhân HFrEF từ 10 bệnh viện từ năm 2016 đến năm 2018.13 Khái niệm ST mất bù cấp đề cập đến sự khởi phát nhanh chóng hoặc nặng hơn của các triệu chứng cơ năng và/hoặc thực thể của ST (ví dụ: ứ dịch và/hoặc giảm cung lượng tim với giảm tưới máu ngoại vi).9 Tiêu chuẩn chọn bệnh cho nghiên cứu này gồm (i) bệnh nhân nam hoặc nữ >20 tuổi với HFrEF có triệu chứng, (ii) bệnh nhân được xuất viện sau nhập viện vì ST mất bù cấp, và (iii) bệnh nhân có nhịp xoang với tần số tim khi nghỉ ngơi ≥70 l/p lúc xuất viện. Tiêu chuẩn loại trừ bao gồm những bệnh nhân từ chối tư vấn y tế hoặc mất theo dõi và không phải nhịp xoang (tạo nhịp nhĩ, rung nhĩ hoặc cuồng nhĩ) hoặc nhịp xoang với tần số tim khi nghỉ ngơi <70 l/p. Các bệnh nhân đủ điều kiện được chia thành hai nhóm tuỳ theo đơn thuốc ivabradine khi xuất viện (nhóm dùng ivabradine và nhóm không dùng ivabradine). Sơ đồ của nghiên cứu này được thể hiện trong Hình 1. Các quy trình của hai đoàn hệ ST tương tự nhau và 50 biến số trên mỗi bệnh nhân trong cả hai đoàn hệ được thu thập trong quá trình lần đầu nhập viện vì ST, bao gồm tuổi, giới tính, chỉ số khối cơ thể, nguyên nhân ST, huyết áp tâm thu, tần số tim, nhóm chức năng của Hiệp hội Tim mạch New York (NYHA), phân suất tống máu thất trái (LVEF), mức lọc cầu thận ước tính (eGFR), bệnh đồng mắc, thuốc điều trị, dữ liệu xét nghiệm và sử dụng thiết bị tim. Nghiên cứu này tuân thủ các nguyên tắc đạo đức của Tuyên bố Helsinki và đã được phê chuẩn bởi cơ quan ủy ban đạo đức của mỗi bệnh viện.
Kết quả nghiên cứu
Ba kết cục lâm sàng được xác định trong nghiên cứu trong suốt 1 năm theo dõi như sau: tỷ lệ tử vong do nguyên nhân tim mạch, tử vong do mọi nguyên nhân và tái nhập viện do ST. Dữ liệu về tái nhập viện do ST được thu thập trong vòng 6 tháng và từ 6 đến 12 tháng sau khi xuất viện. Tần suất tái nhập viện do ST được phân loại thành 0, 1, 2 và ≥3 lần.
Phân tích thống kê
Các biến liên tục và biến phân loại được biểu thị tương ứng bằng các giá trị trung bình ± độ lệch chuẩn và tỷ lệ phần trăm. Ghép điểm xu hướng được thực hiện để điều chỉnh các yếu tố gây nhiễu. Xu hướng được ước tính bằng cách sử dụng mô hình hồi quy logistic với các biến số sau: tuổi, giới tính, chỉ số khối cơ thể, huyết áp tâm thu, tần số tim và nhóm chức năng NYHA khi xuất viện, LVEF, eGFR, nguyên nhân ST, và 13 bệnh đồng mắc (tăng huyết áp, đái tháo đường, rối loạn lipid máu, bệnh động mạch ngoại vi, rung nhĩ, bệnh phổi tắc nghẽn mạn tính (COPD) hoặc hen suyễn, bệnh thận mạn, ngưng thở khi ngủ, tiền sử đột quỵ, rối loạn chức năng tuyến giáp, tiền sử nhồi máu cơ tim, bệnh ác tính và trầm cảm). Bởi vì có nhiều bệnh nhân không dùng ivabradine, mỗi bệnh nhân trong nhóm ivabradine được ghép với hai bệnh nhân trong nhóm không dùng ivabradine (ghép 1: 2). Trong quá trình ghép, phương pháp cận lân, xâm nhập nhưng không thay thế và với thước cặp 0,01 của điểm xu hướng đã được sử dụng.
Hình 1 Sơ đồ nghiên cứu
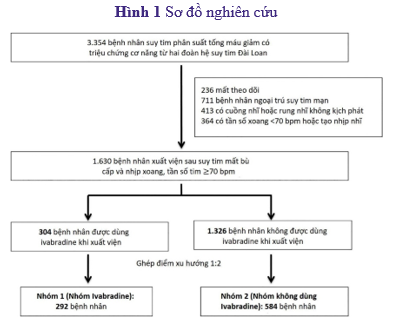
Sự khác biệt về các đặc điểm cơ bản và các thông số lâm sàng đã được kiểm định bằng cách sử dụng kiểm định χ2 cho các biến phân loại, và dữ liệu liên tục được so sánh bằng kiểm định t Student’s hoặc kiểm định Mann – Whitney U. Nguy cơ tử vong do tim mạch và tử vong do mọi nguyên nhân được phân tích bằng phân tích sống cònvới phương pháp Kaplan-Meier và kiểm định log-rank. Bởi vì điều trị ST ban đầu giữa hai nhóm khác nhau đáng kể, các phân tích hồi quy Cox phân nhóm và đa biến được thực hiện để đánh giá tính nhất quán về tác dụng điều trị của ivabradine và đánh giá ảnh hưởng của mỗi phương pháp điều trị trên kết cục lâm sàng. Giá trị P <0,05 được coi là có ý nghĩa thống kê, và các phân tích thống kê được thực hiện bằng phần mềm IBM SPSS Statistics 24.0 (IBM SPSS, IBM Corp., Armonk, NY, USA).
KẾT QUẢ
Các đặc điểm cơ bản
Nghiên cứu này bao gồm 1.630 bệnh nhân HFrEF xuất viện sau nhập viện vì ST mất bù cấp với tần số xoang ≥70 l/p. Trong số những bệnh nhân này, 304 bệnh nhân được dùng ivabradine khi xuất viện (nhóm ivabradine), trong khi 1.326 bệnh nhân không được dùng ivabradine khi xuất viện (nhóm không sử dụng ivabradine). Bệnh nhân trong nhóm không dùng ivabradine già hơn đáng kể, có số đo tần số tim cao hơn khi xuất viện và khuynh hướng có tiền sử liên quan đến rung nhĩ kịch phát trước khi ghép điểm xu hướng. Ngược lại, bệnh nhân trong nhóm ivabradine có tiền sử nhồi máu cơ tim và rối loạn lipid máu nhiều hơn. Sau khi ghép điểm xu hướng 1:2,876 bệnh nhân được đưa vào phân tích cuối cùng. Tuổi trung bình của đối tượng nghiên cứu và LVEF trung bình lần lượt là 60,7 tuổi và 28,2%. Nhìn chung, hai đoàn hệ được ghép khá cân bằng. Bảng 1 cho thấy chi tiết các đặc điểm cơ bản của cả hai đoàn hệ trước và sau khi ghép điểm xu hướng.
Thuốc và thiết bị điều trị suy tim khi xuất viện
Tỷ lệ kê đơn thuốc chẹn beta (70,2% so với 68,2%, P = 0,536), thuốc lợi tiểu quai (68,8% so với 73,1%, P = 0,185) và thuốc chống đông (15,4% so với 15,2%, P = 0,947) là tương tự giữa hai nhóm khi xuất viện. Bệnh nhân trong nhóm ghép ivabradine có vẻ thích sử dụng ACEi, ARB, hoặc sacubitril/valsartan (80,5% so với 71,1%, P = 0,003); sacubitril/valsartan (38,0% so với 18,0%, P <0,001); hoặc MRA (71,6% so với 51,9%, P <0,001) hơn, trong khi bệnh nhân ở nhóm không dùng ivabradine có vẻ thích được dùng ACEi/ARB (53,1% so với 42,5%, P = 0,003), digoxin (24,0% so với 16,1%, P = 0,007) và amiodarone (14,2% so với 8,9%, P = 0,025) hơn. So với những bệnh nhân ở nhóm không dùng ivabradine, bệnh nhân trong nhóm ivabradine có nhiều khả năng được cấy thiết bị trợ tim hơn, bao gồm liệu pháp tái đồng bộ tim (7,2% so với 2,4%, P = 0,001) và cấy máy phá rung chuyển nhịp (11,0% so với 4,1 %, P <0,001). Mặc dù có sự khác biệt trong các phác đồ giảm tần số tim khi xuất viện, bệnh nhân ở cả hai nhóm đều có số đo tần số tim tương đương khi xuất viện (83,5 ± 15,0 so với 84,7 ± 13,1 l/p P = 0,248).
Bảng 1 Đặc điểm cơ bản của các bệnh nhân ở các nhóm khác nhau
| Trước khi ghép điểm xu hướng
|
Giá trị P |
Sau khi ghép điểm xu hướng | ||||
| Nhóm IVA
(n=304) |
Nhóm Không IVA (n=1326) | Nhóm IVA (n = 292) | Nhóm Không IVA
(n = 584) |
Giá trị p | ||
| Tuổi (năm)
Giới nam, (%) BMI (kg/m2) Thời gian nằm viện (ngày) HATT nhập viện (mmHg) TST nhập viện (lần/phút) HATT xuất viện (mmHg) TST xuất viện (lần/phút) Nhóm chức năng NYHA xuất viện LVEF (%) eGFR (ml/phút/m2) Bệnh cơ tim TMCB, n (%) |
60,1 ± 14,9
226 (76,9) 25,4 ± 5,6 13,6 ± 24,4 129,1 ± 21,2 92,9 ± 16,1 119,5 ± 20,7 83,7 ± 14,7 2,6 ± 0,7 28,2 ± 7,2 65,7 ± 47,4 152 (50,0) |
62,4 ± 15,3
967 (72,9) 25,3 ± 4,9 12,7 ± 13,1 130,6 ± 25,2 94,7 ± 19,9 120,4 ± 19,0 86,0 ± 12,2 2,6 ± 0,7 28,5 ± 8,1 61,4 ± 35,1 628 (47,4) |
0,018
0,165 0,659 0,437 0,286 0,092 0,487 0,010 0,101 0,488 0,073 0,406 |
60,5 ± 14,9
224 (76,7) 25,4 ± 5,6 13,6 ± 24,6 129,2 ± 21,2 92,8 ± 16,1 119,6 ± 20,7 83,5 ± 15,0 2,6 ± 0,7 28,2 ± 7,3 65,5 ± 48,0 140 (47,9) |
60,8 ± 14,4
449 (76,9) 25,1 ± 5,1 12,4 ± 11,9 129,9 ± 25,5 93,4 ± 20,0 119,7 ± 20,2 84,7 ± 13,1 2,6 ± 0,7 28,2 ± 8,1 63,9 ± 32,6 280 (47,9) |
0,764
0,955 0,433 0,342 0,675 0,622 0,967 0,248 0,225 0,930 0,573 1,000 |
| Bệnh đồng mắc, n (%) | ||||||
| Đái tháo đường | 156 (51,3) | 611 (46,1) | 0,099 | 150 (51,4) | 301 (51,5) | 0,962 |
| Tăng huyết áp | 166 (54,6) | 719 (54,3) | 0,904 | 160 (54,8) | 312 (53,4) | 0,701 |
| Tiền sử nhồi máu cơ tim | 103 (33,9) | 364 (27,5) | 0,025 | 97 (33,2) | 173 (29,6) | 0,277 |
| Bệnh động mạch ngoại vi | 24 (7,9) | 99 (75) | 0,799 | 24 (8,2) | 45 (7,7) | 0,790 |
| Tiền sử đột quỵ | 27 (8,9) | 128 (9,7) | 0,679 | 27 (9,2) | 51 (8,7) | 0,801 |
| Rung nhĩ kịch phát | 40 (13,2) | 249 (18,8) | 0,019 | 40 (13,7) | 89 (15,2) | 0,544 |
| Rối loạn lipid máu | 141 (46,4) | 519 (39,2) | 0,020 | 129 (44,2) | 269 (46,1) | 0,598 |
| COPD | 36 (11,8) | 157 (11,8) | 0,999 | 36 (12,3) | 84 (14,4) | 0,404 |
| Bệnh thận mạn | 113 (37,2) | 456 (34,4) | 0,359 | 107 (36,6) | 219 (37,5) | 0,805 |
| Tiền sử bệnh lý tuyến giáp | 21 (6,9) | 69 (5,2) | 0,241 | 21 (7,2) | 42 (7,2) | 1,000 |
| Ngưng thở khi ngủ | 10 (3,3) | 36 (2,7) | 0,585 | 10 (3,4) | 17 (2,9) | 0,678 |
| Tiền sử bệnh ác tính | 21 (6,9) | 62 (4,7) | 0,110 | 19 (6,5) | 40 (6,8) | 0,849 |
| Trầm cảm | 9 (3,0) | 28 (2,1) | 0,370 | 9 (3,1) | 10 (1,7) | 0,189 |
| RASi | 241 (79,3) | 943 (71,1) | 0,004 | 235 (80,5) | 415 (71,1) | 0,003 |
| ACEi/AR B | 125 (41,1) | 713 (53,8) | <0,001 | 124 (42,5) | 310 (53,1) | 0,003 |
| Sacubitril/Valsartan | 116 (38,2) | 230 (17,3) | <0,001 | 111 (38,0) | 105 (18,0) | <0,001 |
| Chẹn beta | 209 (68,8) | 856 (64,6) | 0,124 | 205 (70,2) | 398 (68,2) | 0,536 |
| MRA | 215 (70,7) | 689 (52,0) | <0,001 | 209 (71,6) | 303 (51,9) | <0,001 |
| Digoxin | 47 (15,5) | 310 (23,4) | 0,003 | 47 (16,1) | 140 (24,0) | 0,007 |
| CRT | 21 (6,9) | 33 (2,5) | <0,001 | 21 (7,2) | 14 (2,4) | 0,001 |
| ICD | 32 (10,5) | 48 (3,6) | <0,001 | 32 (11,0) | 24 (4,1) | <0,001 |
Viết tắt: ACEi, thuốc ức chế men chuyển angiotensin; ARB, thuốc chẹn thụ thể angiotensin; BMI, chỉ số khối cơ thể; COPD, bệnh phổi tắc nghẽn mạn tính; CRT, liệu pháp tái đồng bộ tim; eGFR, mức lọc cầu thận ước tính; TST, tần số tim; ICD, cấy máy tạo nhịp; TMCB, bệnh cơ tim thiếu máu cục bộ; IVA, ivabradine; LVEF, phân suất tống máu thất trái; MRA, thuốc đối kháng thụ thể mineralocorticoid; NYHA Fc, Nhóm chức năng Hiệp hội Tim mạch New York; PAD, bệnh động mạch ngoại vi; RASi, thuốc ức chế hệ renin-angiotensin; HATT, huyết áp tâm thu.
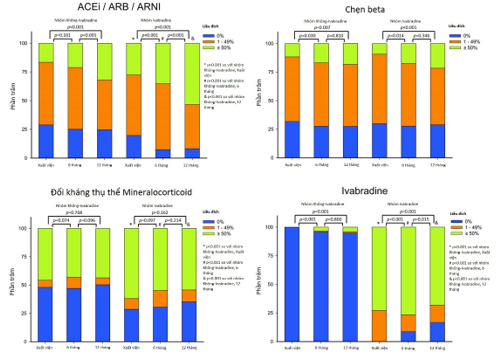
Hình 2. Các loại và liều lượng của các thuốc điều trị suy tim ở các bệnh nhân nghiên cứu theo thời gian. ACEi, thuốc ức chế men chuyển; ARB, thuốc chẹn thụ thể angiotensin; ARNI, thuốc ức chế neprilysin thụ thể angiotensin.
Tỷ lệ kê đơn và liều lượng của thuốc ức chế hệ thống renin-angiotensin, thuốc chẹn beta, MRA và ivabradine khi xuất viện, 6 tháng và 12 tháng sau khi nhập viện được trình bày trong Hình 2. Tăng chỉnh liều thuốc ức chế hệ renin- angiotensin và thuốc chẹn beta có khác biệt đáng kể ở cả hai nhóm khi theo dõi 1 năm (tất cả các giá trị P <0,01). Không có sự thay đổi đáng kể trong các mô hình kê đơn của MRA tại thời điểm theo dõi 1 năm ở cả hai nhóm. Ivabradine được khởi đầu ở 5,3% bệnh nhân trong nhóm không sử dụng ivabradine và ngừng sử dụng ở 16,8% bệnh nhân trong nhóm ivabradine sau 1 năm theo dõi.
KẾT CỤC LÂM SÀNG
Tỷ lệ tử vong tim mạch chung là 10,0 trên 100 người năm tại thời điểm theo dõi 1 năm. Tỷ lệ tử vong do tim mạch tương ứng là 5,8 và 12,2 trên 100 người năm đối với nhóm ivabradine và không dùng ivabradine, [tỷ số nguy cơ (HR), 0,45; Khoảng tin cậy 95% (KTC); 0,26-0,76; P = 0,003; Hình 3A. Tỷ lệ tử vong do bất kỳ nguyên nhân nào ở bệnh nhân trong nhóm ghép dùng ivabradine và không dùng ivabradine lần lượt là 7,2 và 14,0 trên 100 người năm (HR, 0,48; CI 95%, 0,30–0,77; P = 0,003; Hình 3B).
Trong 6 tháng đầu tiên sau lần đầu nhập viện vì ST, 319 lần tái nhập viện vì ST đã xảy ra ở 221 bệnh nhân. Hơn nữa, 20,3% và 27,7% bệnh nhân tương ứng trong nhóm ivabradine và không dùng ivabradine tái nhập viện vì ST ít nhất một lần trong vòng 6 tháng sau lần đầu nhập viện (P = 0,004). Từ 6 đến 12 tháng sau nhập viện lần đầu vì ST, đã có 187 lần tái nhập viện vì ST ở 132 bệnh nhân. Hơn nữa, 12,2% và 19,5% bệnh nhân tương ứng trong nhóm ghép ivabradine và nhóm không dùng ivabradine phải tái nhập viện vì ST ít nhất một lần trong khoảng thời gian từ 6 đến 12 tháng sau lần đầu nhập viện (P = 0,007). Hình 4A cho thấy tỷ lệ tái nhập viện lần đầu tiên và lặp lại vì ST ở bệnh nhân trong nhóm ghép ivabradine thấp hơn đáng kể so với bệnh nhân trong nhóm không sử dụng ivabradine (tỷ số chênh cho lần đầu tiên tái nhập viện ngoài ý muốn vì ST trong vòng 1 năm là 0,65; CI 95%, 0,48–0,89; P = 0,006).
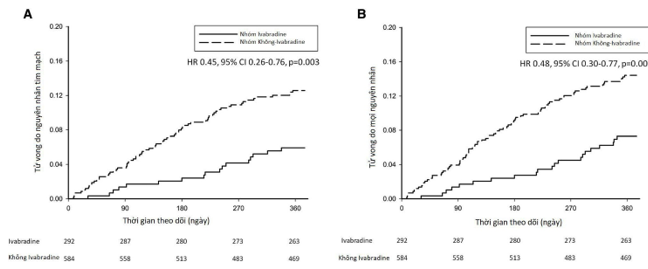
Hình 3. Đường cong Kaplan – Meier tử vong do nguyên nhân tim mạch (A) và tử vong do bất kỳ nguyên nhân nào (B) trong vòng 1 năm ở bệnh nhân nghiên cứu. CI, khoảng tin cậy; HR, tỷ số rủi ro.
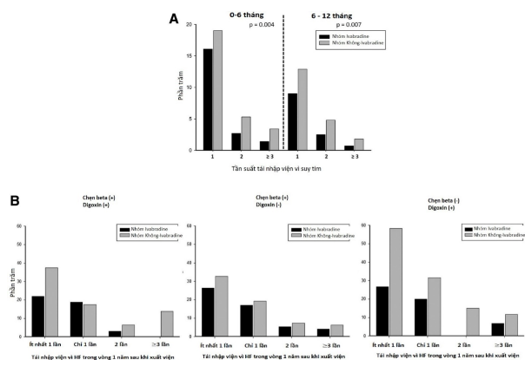
Hình 4. Tần suất tái nhập viện vì suy tim (ST) sau lần đầu nhập viện trong vòng 1 năm (A), và phân loại theo kê đơn ban đầu của thuốc chẹn beta và digoxin (B).
Kết cục lâm sàng của các liệu pháp ST nền khác nhau
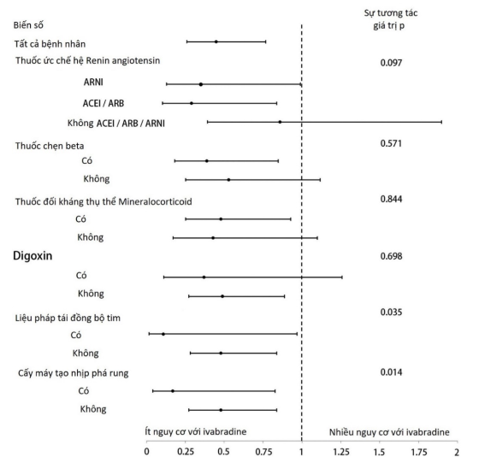
Trong số những bệnh nhân được điều trị nền đồng thời với thuốc chẹn beta, bệnh nhân được điều trị bằng ivabradine có nguy cơ tử vong do tim mạch thấp hơn đáng kể so với những người không dùng ivabradine (3,9 so với 9,5 trên 100 người năm; HR, 0,39; CI 95%, 0,18 –0,83; P = 0,011). Kết cục có lợi của ivabradine trong tỷ lệ tử vong do tim mạch là nhất quán giữa các phân nhóm được khảo sát khác nhau của các thuốc và các thiết bị cấy ghép điều trị ST nền khác nhau (Hình 5). Tỷ lệ tử vong do tim mạch là tương tự ở những bệnh nhân không điều trị bằng ivabradine trong đoàn hệ 2013–2014 và 2016–2018 (P = 0,540).
Bảng 2 trình bày các phân tích hồi quy Cox đơn biến và đa biến cho các điều trị ST ban đầu liên quan đến kết cục 1 năm. Việc kê đơn ivabradine khi xuất viện có liên quan độc lập với nguy cơ tử vong do mọi nguyên nhân trong 1 năm thấp hơn (HR, 0,45; CI 95%, 0,28–0,74; P = 0,002). Sử dụng thuốc chẹn beta và ức chế hệ renin-angiotensin khi xuất viện cũng liên quan độc lập với khả năng sống sót tốt hơn (HR, 0,59; CI 95%, 0,40–0,88; P = 0,009 đối với thuốc chẹn beta và HR, 0,58; CI 95%, 0,38– 0,86; P = 0,008 đối với thuốc ức chế hệ renin- angiotensin). Hơn nữa, việc kê đơn ivabradine, thuốc ức chế hệ renin-angiotensin và thuốc chẹn beta khi xuất viện có liên quan độc lập với nguy cơ tử vong do tim mạch trong 1 năm thấp hơn (Bảng 2).
Hình 5. Tỷ số rủi ro tử vong do tim mạch theo các phân nhóm điều trị suy tim trong hai đoàn hệ. ACEi, thuốc ức chế men chuyển; ARB, thuốc chẹn thụ thể angiotensin; ARNI, thuốc ức chế neprilysin thụ thể angiotensin.
Bảng 2. Phân tích đa biến cho các phương pháp điều trị suy tim liên quan đến kết cục một năm sau lần đầu nhập viện vì suy tim
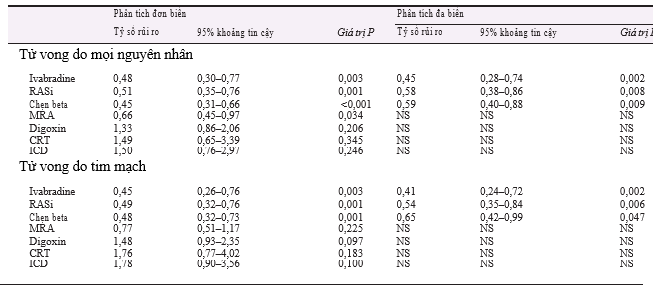
Phân tích đa biến được điều chỉnh theo tuổi, giới tính, nguyên nhân suy tim, chỉ số khối cơ thể, thời gian nằm viện, phân suất tống máu thất trái, huyết áp tâm thu, tần số tim, mức lọc cầu thận ước tính, nhóm chức năng của Hiệp hội Tim mạch New York khi xuất viện, tiền sử nhập viện vì suy tim, rung nhĩ, tăng huyết áp, đái tháo đường, bệnh phổi tắc nghẽn mạn tính, bệnh động mạch ngoại vi, tiền sử đột quỵ, tiền sử bệnh lý tuyến giáp, ngưng thở khi ngủ, tiền sử bệnh ác tính, trầm cảm, liệu pháp thiết bị và kê đơn thuốc điều trị suy tim khi xuất viện.
Viết tắt: CRT, liệu pháp tái đồng bộ tim; ICD, cấy máy tạo nhịp phá rung; MRA, thuốc chẹn thụ thể mineralocorticoid; NS, không có ý nghĩa thống kê; RASi, thuốc ức chế hệ renin-angiotensin.
Hình 4B cho thấy tỷ lệ phần trăm tổng số tái nhập viện vì ST 1 năm sau khi xuất viện, được phân loại theo các điều trị giảm tần số tim khác nhau. Bất kể sự kết hợp khác nhau của thuốc chẹn beta và digoxin khi xuất viện, bổ sung ivabradine cho thấy giảm nguy cơ tái nhập viện lần đầu và/hoặc lặp lại vì ST trong vòng 1 năm sau khi xuất viện kể từ lần đầu nhập viện.
Sự thay đổi của huyết áp, tần số tim và phân suất tống máu thất trái
Bảng 3 cho thấy sự thay đổi của các dấu hiệu sinh tồn và kết cục lâm sàng trong vòng 1 năm. Tại thời điểm theo dõi 1 năm, bệnh nhân trong nhóm ivabradine có tần số tim thấp hơn đáng kể (77,6 ± 14,7 so với 81,1 ± 16,3 l/p P = 0,005) và mức độ nặng của các triệu chứng cơ năng ST thấp hơn (nhóm chức năng NYHA, 2,1 ± 0,7 so với 2,3 ± 0,9; P <0,001) so với nhóm không dùng ivabradine. Hơn nữa, bệnh nhân trong nhóm ivabradine có số đo LVEF cao hơn so với nhóm không dùng ivabradine, mặc dù không có ý nghĩa thống kê (39,2% ± 14,0% so với 37,3% ± 15,2%; P = 0,104).
BÀN LUẬN
Các biến cố bất lợi thường xảy ra sau khi xuất viện kể từ lần đầu nhập viện do ST mất bù cấp. Trong nghiên cứu hiện tại, 1/4 số bệnh nhân phải tái nhập viện vì ST trong vòng 6 tháng và 1/10 tử vong do các nguyên nhân tim mạch trong vòng 1 năm sau lần đầu nhập viện vì ST, cho thấy cần phải điều trị kịp thời và thích hợp cho những bệnh nhân có nguy cơ cao này.
Những bệnh nhân nhập viện vì ST cấp thường yếu ớt do có nhiều bệnh đồng mắc, ví dụ, suy thận và COPD, huyết động không ổn định, và cần dùng thuốc vận mạch và tăng co bóp cơ tim. Những tình trạng này thường hạn chế việc khởi đầu và chuẩn độ các liệu pháp theo hướng dẫn, đó là MRA, thuốc ức chế hệ renin-angiotensin và thuốc chẹn beta.14 Tuy nhiên, khác với các loại thuốc trên, ivabradine có tác dụng đặc hiệu và ở mức độ cao vào dòng If trong nút xoang nhĩ và không ảnh hưởng bất lợi đến thận và hệ thống phế quản. Phân tích phân nhóm của thử nghiệm SHIFT đã tạo ra bằng chứng đầy hứa hẹn về những lợi ích tim mạch nhất quán và tính an toàn ở bệnh nhân ST và rối loạn chức năng thận hoặc COPD.14,15 Đối với việc điều trị những bệnh nhân ST và hạ huyết áp hoặc huyết động không ổn định, sử dụng ivabradine (so với thuốc chẹn beta) có thể thích hợp hơn trong những trường hợp này vì đặc trưng khác biệt của nó là giảm tần số tim mà không gây hạ huyết áp hoặc ức chế co bóp cơ tim.16–18 Một báo cáo loạt ca đã cho thấy tính an toàn và hiệu quả của ivabradine ở năm bệnh nhân bị sốc tim.18 Một nghiên cứu khác tuyển chọn 10 bệnh nhân ST tiến triển với áp lực mao mạch phổi bít ≥15 mmHg và nhịp nhanh xoang đã cho thấy ivabradine tiêm tĩnh mạch làm giảm đáng kể tần số tim và thể tích tống máu và công tâm thu thấttrái .16 Tương tự, 52 bệnh nhân ST mất bù điều trị với dobutamine được phát hiện có tần số tim thấp hơn và thể tích tống máu tốt hơn sau khi điều trị bằng ivabradine.17 Ngoài những ưu điểm này, ivabradine còn có tác dụng đặc biệt khác là cải thiện chức năng co bóp và tưới máu mạch vành mà không ảnh hưởng đến các thụ thể adrenergic.19 Một phân tích hậu kiểm của nghiên cứu SHIFT cho thấy bệnh nhân trong nhóm ivabradine và không dùng ivabradine có sự gia tăng huyết áp tương ứng 12 và 11 mmHg sau 24 tháng, và huyết áp ban đầu không ảnh hưởng đến tác động của việc giảm nhịp tim đối với các kết cục lâm sàng.20 Kết quả của chúng tôi lặp lại nghiên cứu nói trên và cho thấy không có sự khác biệt về huyết áp tâm thu khi theo dõi 1 năm giữa hai nhóm. Những ưu điểm và đặc tính dược lý đặc biệt này của ivabradine có thể hỗ trợ việc sử dụng nó ở những bệnh nhân ST cấp với gánh nặng bệnh đồng mắc cao và huyết động không ổn định và thậm chí cho phép bắt đầu hoặc chỉnh liều sớm thuốc chẹn beta trong thực hành thực tế.21
Tăng tần số tim làm tăng tiêu thụ oxy cơ tim, làm trầm trọng thêm tổn thương cơ tim, và dẫn đến tái cấu trúc thất tiêu cực.19 Hơn nữa, trái ngược với sự gia tăng lực co bóp kèm theo tần số khử cực cơ tăng lên ở tim bình thường, mối quan hệ tần số – lực âm được ghi nhận trong cơ tim suy do giảm tưới máu mạch vành, khiếm khuyết canxi thoáng qua và hoạt tính mạng lưới cơ tương, và tăng stress oxy hóa.19,22,23 Do đó, khi xử trí bệnh nhân bị ST mất bù cấp, sự xuất hiện của nhịp tim nhanh được coi là dấu hiệu cảnh báo vì tần số tim tăng cao có liên quan đến kết cục tim mạch bất lợi ở các giai đoạn khác nhau trong thời gian nhập viện vì ST.11,24–26 Lưu ý, mặc dù dữ liệu của chúng tôi cho thấy sự khác biệt tuyệt đối về tần số tim giữa hai nhóm nhỏ hơn so với quan sát trong nghiên cứu SHIFT (3,5 so với 8 lần/phút),10 bổ sung điều trị bằng ivabradine vẫn liên quan với tỷ lệ tử vong do tim mạch trong 1 năm thấp hơn đáng kể và số lần tái nhập viện vì ST ít hơn. Hiện tượng này có thể ngụ ý các tác dụng bảo vệ tim khác của ivabradine ngoài tác dụng làm giảm tần số tim.
Bảng 3. Đặc điểm của bệnh nhân khi xuất viện và ở những người sống sót tại thời điểm 12 tháng sau khi xuất viện.
| Nhóm IVA
(n = 292) |
Nhóm Không-IVA
(n = 584) |
Giá trị P | |
| Ban đầu | |||
| Huyết áp tâm thu (mmHg) | 129,2 ± 21,2 | 129,9 ± 25,5 | 0,675 |
| Tần số tim (lần/phút) | 83,5 ± 15,0 | 84,7 ± 13,1 | 0,248 |
| LVEF (%) | 28,2 ± 7,3 | 28,2 ± 8,1 | 0,930 |
| NYHA Fc | 2,6 ± 0,7 | 2,6 ± 0,7 | 0,225 |
| Tại thời điểm 12 thánga | |||
| Huyết áp tâm thu (mmHg) | 120,4 ± 19,4 | 121,5 ± 21,5 | 0,489 |
| Tần số (lần/phút) | 77,6 ± 14,7 | 81,1 ± 16,3 | 0,005 |
| LVEF (%) | 39,2 ± 14,0 | 37,3 ± 15,2 | 0,104 |
| NYHA Fc | 2,1 ± 0,7 | 2,3 ± 0,9 | <0,001 |
| Tử vong do tim mạch, n (%) | 17 (5,8%) | 71 (12,2%) | 0,002 |
| Tử vong do mọi nguyên nhân, n (%) | 21 (7,2%) | 82 (14,0%) | 0,002 |
| Tái nhập viện ít nhất 1 lần vì ST, n (%) | 79 (27,1%) | 212 (36,3%) | <0,001 |
aHuyết áp tâm thu, tần số tim và phân suất tống máu thất trái được thu thập từ những người sống sót tại thời điểm 12 tháng sau khi xuất viện (nhóm IVA n = 271, nhóm không-IVA n = 502).
Viết tắt: ST, suy tim; IVA, ivabradine; LVEF, phân suất tống máu thất trái; NYHA Fc, nhóm chức năng của Hiệp hội Tim mạch New York.
Đầu tiên, khi việc giảm tần số tim liên quan đến chẹn beta bị ngăn chặn bởi tạo nhịp, co thắt mạch vành do alpha- adrenergic được bộc lộ, điều này có thể làm suy giảm tưới máu mạch vành và chức năng tim.27 Khác với thuốc chẹn beta, ivabradine có thể đồng thời làm giảm tần số tim và cải thiện tưới máu mạch vành và chức năng tim bằng cách duy trì sự giãn mạch qua trung gian nội mô và không gây co thắt mạch vành liên quan đến alpha-adrenergic hoặc ức chế hoạt động co bóp cơ tim.28,29 Điều này sẽ cho phép chức năng tim hoạt động tốt hơn trong hoạt động hàng ngày hoặc tập thể dục.30 Thứ hai, lợi ích của ivabradine chống lại nhồi máu cơ tim ngoài việc giảm tần số tim.31 Các nghiên cứu cho thấy ivabradine có thể làm giảm kích thước nhồi máu cơ tim và duy trì khả năng sống sót của tế bào cơ tim nhiều hơn sau thiếu máu cục bộ hoặc tái tưới máu bằng cách giảm sự hình thành các loại oxy phản ứng của ty thể và tăng sản xuất adenosine triphosphate và khả năng giữ canxi.31,32 Ngoài ra, ivabradine được quan sát thấy làm giảm tái cấu trúc tim bất lợi và cải thiện sự tạo mạch sau nhồi máu cơ tim.33 Những tác dụng bảo vệ tim theo nhiều hướng này có thể cung cấp những giải thích hợp lý tại sao những bệnh nhân được điều trị bằng ivabradine cải thiện đáng kể kết cục lâm sàng ngay cả khi tần số tim giảm không nhiều.
Cho đến nay, tỷ lệ sử dụng ivabradine vẫn còn thấp trong thực tế, mặc dù sổ bộ dài hạn ESC-HF báo cáo rằng tỷ lệ kê đơn ivabradine tăng từ 1,2% lên 3,2% trước khi nhập viện vì ST và khi xuất viện.34 Về lý thuyết, người ta cho rằng ivabradine được sử dụng như một điều trị bổ sung làm giảm tần số tim sau một thuốc chẹn beta. Tuy nhiên, mặc dù các nghiên cứu có liên quan cho rằng nên tiếp tục điều trị bằng thuốc chẹn beta ở những bệnh nhân ST mất bù cấp nếu tình trạng lâm sàng của họ cho phép,35 tác dụng ức chế co bóp cơ tim của thuốc chẹn beta trên huyết động tim mạch gây ra sự miễn cưỡng của một số bác sĩ khi kê đơn chúng, đặc biệt là trong giai đoạn mất bù cấp.
Trong bối cảnh thực tế, việc sử dụng thuốc chẹn beta giảm đáng kể từ 89,9% xuống 69,1% sau 6 tháng kể từ khi ST nặng hơn xảy ra.8 Do đó, sẽ không thực tế nếu cho rằng tất cả bệnh nhân nhập viện vì HFrEF có thể sử dụng và dung nạp liệu pháp chẹn beta đầu tiên và dần dần đưa vào sử dụng ivabradine trong những tháng tiếp theo vì nhiều bệnh nhân vẫn có nguy cơ cao tái nhập viện trong giai đoạn dễ bị tổn thương. Trở ngại này có thể hạn chế việc sử dụng ivabradine kịp thời. Một phân tích hậu kiểm từ nghiên cứu SHIFT cho thấy duy trì điều trị ivabradine có liên quan đến nhập viện do mọi nguyên nhân ít hơn sau 1, 2 và 3 tháng.36 Hơn nữa, thử nghiệm ETHIC-AHF đã cho thấy những bệnh nhân được điều trị bằng ivabradine và thuốc chẹn beta khi xuất viện có tần số tim thấp hơn đáng kể và LVEF tốt hơn sau 4 tháng so với những bệnh nhân được điều trị bằng thuốc chẹn beta đơn thuần.37 Tương tự như vậy, một nghiên cứu từ các quốc gia hậu Xô Viết cho thấy việc bổ sung ivabradine vào liệu pháp chẹn beta cho bệnh nhân ST cấp trong thời gian nhập viện đã góp phần làm giảm tỷ lệ tử vong do mọi nguyên nhân và tái nhập viện vì ST trong vòng 1 năm so với chỉ sử dụng thuốc chẹn beta đơn thuần.38 Theo đó, do tác dụng có lợi của sự kết hợp ivabradine và thuốc chẹn beta ở những bệnh nhân ST mất bù cấp, một số bác sĩ lâm sàng bắt đầu ủng hộ tiếp cận không theo từng bước thay vì sử dụng từng nhóm thuốc theo kiểu bậc thang.39 Nghiên cứu thực tế này ủng hộ cách tiếp cận này và cung cấp kết quả có lợi rằng ivabradine có thể được sử dụng hiệu quả trong bất kỳ trường hợp lâm sàng nào miễn là bệnh nhân ST đã được xuất viện với nhịp xoang và tần số tim ≥70 l/p.
Một số hạn chế vốn có trong thiết kế hồi cứu của nghiên cứu này cần được đề cập. Đầu tiên, các quyết định điều trị dựa trên thực hành trong thực tế của các bác sĩ tim mạch tham gia. Loại nghiên cứu hồi cứu này có thể tiềm ẩn những sai lệch không thể đo lường được. Tuy nhiên, nghiên cứu này nhằm mục đích bao gồm phạm vi rộng những bệnh nhân phản ánh thực tế hiện tại về thực hành sau giai đoạn cấp đối với ivabradine và không bao gồm quần thể ST bị bó hẹp trong các thử nghiệm lâm sàng.
Thứ hai, số lượng bệnh nhân tương đối nhỏ. Một thử nghiệm ngẫu nhiên, có đối chứng với giả dược đang được tiến hành đánh giá hiệu quả và tính an toàn của ivabradine trên 674 bệnh nhân ST cấp có thể xác định vai trò của việc giảm tần số tim sớm bởi ivabradine ở những bệnh nhân này.40
Kết luận, trong số những quần thể Châu Á thực tế với ST mất bù cấp và giảm LVEF, điều trị bằng ivabradine có liên quan với giảm nguy cơ tử vong do tim mạch, tử vong do mọi nguyên nhân và tái nhập viện vì ST trong vòng 1 năm. Những lợi ích này của ivabradine nhất quán với các loại thuốc điều trị ST nền khác nhau. Cần có thêm các thử nghiệm lâm sàng quy mô lớn để xác định lợi ích của ivabradine ở những bệnh nhân HFrEF mất bù cấp.
Tài liệu tham khảo (xem đầy đủ tại www.timmachhoc.vn)
- Mosterd A, Hoes AW. Clinical epidemiology of heart failure. Heart 2007; 93: 1137–1146.
- Gheorghiade M. Rehospitalization for heart failure: problems and perspectives. J Am Coll Cardiol 2013; 61: 391–403.
- Sakata Y, Shimokawa H. Epidemiology of heart failure in Asia. Circ J 2013; 77: 2209–2217.
- Cleland JG, Swedberg K, Follath F, Komajda M, Cohen-Solal A, Aguilar JC, Dietz R, Gavazzi A, Hobbs R, Korewicki J, Madeira HC, Moiseyev VS, Preda I, van Gilst WH, Widimsky J, Freemantle N, Eastaugh J, Mason J, Study Groupon Diagnosis of the Working Group on Heart Failure of the European Society of Cardiology. The EuroHeart Failure survey programme– a survey on the quality of care among patients with heart failure in Europe. Part 1: patient characteristics and diagnosis. Eur Heart J 2003; 24: 442–463.
- Shimokawa H, Miura M, Nochioka K, Sakata Y. Heart failure as a general pan- demic in Asia. Eur J Heart Fail 2015; 17: 884–892.
- Reyes EB, Ha JW, Firdaus I, Ghazi AM, Phrommintikul A, Sim D, Vu QN, Siu CW, Yin WH, Cowie MR. Heart failureacross Asia: Same healthcare burden but differences in organization of care. Int J Cardiol 2016; 223: 163–167.
- Wang CC, Wu CK, Tsai ML, Lee CM, Huang WC, Chou HH, Huang JL, Chi NH, Yen HW, Tzeng BH, Chang WT, Chang HY, Wang CH, Lu YY, Tsai JP, Su CH, Cherng WJ, Yin WH, Tsai CT, Wu YW, Lin JL, Hwang JJ. 2019 Focused Up- date of the Guidelines of the Taiwan So- ciety of Cardiology for the Diagnosis and Treatment of Heart Failure. Acta Cardiol Sin 2019; 35: 244–283.
- Butler J, Yang M, Manzi MA, Hess GP, Patel MJ, Rhodes T, Givertz MM. Clinical course of patients with worsen- ing heart failure with reduced ejection fraction. J Am Coll Cardiol 2019; 73: 935–944.
- Ponikowski P, Voors AA, Anker SD, Bueno H, Cleland JG, Coats AJ, Falk V, González-Juanatey JR, Harjola VP, Jankowska EA, Jessup M, Linde C, Nihoyannopoulos P, Parissis JT, Pieske B, Riley JP, Rosano GM, Ruilope LM, Ruschitzka F, Rutten FH, van der Meer P, Authors/Task Force Members; Docu- ment Reviewers. 2016 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure: The Task Force for the diagnosis and treatment of acute and chronic heart failure of the European Society of Cardiology (ESC). Developed with the special con- tribution of the Heart Failure Associa- tion (HFA) of the ESC. Eur J Heart Fail 2016; 18: 891–975.
- Swedberg K, Komajda M, Böhm M, Borer JS, Ford I, Dubost-Brama A, Lerebours G, Tavazzi L, SHIFT Investiga- tors. Ivabradine and outcomes in chronic heart failure (SHIFT): a randomised placebo-controlled study. Lancet 2010; 376: 875–885.
- DeVore AD, Schulte PJ, Mentz RJ, Hardy NC, Kelly JP, Velazquez EJ, Maya JF, Kielhorn A, Patel HK, Reed SD, Hernandez AF. Relation of elevated heart rate in patients with heart failure with reduced ejection fraction to one-year outcomes and costs. Am J Cardiol 2016; 117: 946–951.
- Wang CC, Chang HY, Yin WH, Wu YW, Chu PH, Wu CC, Hsu CH, Wen MS, Voon WC, Lin WS, Huang JL, Chen SM, Yang NI, Chang HC, Chang KC, Sung SH, Shyu KG, Lin JL, Mar GY, Chan KC, Kuo JY, Wang JH, Chen ZC, Tseng WK, Cherng WJ. TSOC-HFrEF registry: a reg- istry of hospitalized patients with de- compensated systolic heart failure: description of population and manage- ment. Acta Cardiol Sin 2016; 32: 400–411.
- Lee YH, Lin PL, Chiou WR, Huang JL, Lin WY, Liao CT, Chung FP, Liang HW, Hsu CY, Chang HY. Combination of ivabradine and sacubitril/valsartan in patients with heart failure and reduced ejection fraction. ESC Heart Fail 2021; 8: 1204–1215.
- Tavazzi L, Swedberg K, Komajda M, Böhm M, Borer JS, Lainscak M, Robertson M, Ford I, SHIFT Investiga- tors. Clinical profiles and outcomes in patients with chronic heart failure and chronic obstructive pulmonary disease: an efficacy and safety analysis of SHIFT study. Int J Cardiol 2013; 170: 182–188.
- Voors AA, van Veldhuisen DJ, Robertson M, Ford I, Borer JS, Böhm M, Komajda M, Swedberg K, Tavazzi L, SHIFT inves- tigators. The effect of heart rate reduc- tion with ivabradine on renal function in patients with chronic heart failure: an analysis from SHIFT. Eur J Heart Fail 2014; 16: 426–434.
- De Ferrari GM, Mazzuero A, Agnesina L, Bertoletti A, Lettino M, Campana C, Schwartz PJ, Tavazzi L. Favourable ef- fects of heart rate reduction with intra- venous administration of ivabradine in patients with advanced heart failure. Eur J Heart Fail 2008; 10: 550–555.
- Porcile R, Levin R, Fridman O, Baztarrica GP, Villeco S, Salvaggio F, Blanco N. Safety, tolerability and efficacy of ivabradine for control of sinus tachycar- dia in patients undergoing inotropic therapy. Curr Res Cardiol 2016; 3: 13–16.
- Chiu MH, Howlett JG, Sharma NC. Initi- ation of ivabradine in cardiogenic shock. ESC Heart Fail 2019; 6: 1088–1091.
- Heusch G. Heart rate in the pathophysi- ology of coronary blood flow and myo- cardial ischaemia: benefit from selective bradycardic agents. Br J Pharmacol 2008; 153: 1589–1601.
- Komajda M, Böhm M, Borer JS, Ford I, Robertson M, Manolis AJ, Tavazzi L, Swedberg K, SHIFT Investigators. Effi- cacy and safety of ivabradine in patients with chronic systolic heart failure ac- cording to blood pressure level in SHIFT. Eur J Heart Fail 2014; 16: 810–816.
- Barry AE, Schukina EV, Samoilova OV, Pricolota OA, Malovichko SI, Pricolota AV, Bagriy EA. The addition of ivabradine to beta-blocker improves ex- ercise capacity in systolic heart failure patients in a prospective, open-label study. Adv Ther 2015; 32: 108–119.
- Hasenfuss G, Holubarsch C, Hermann HP, Astheimer K, Pieske B, Just H. Influ- ence of the force–frequency relationship on haemodynamics and left ventricular function in patients with nonfailing hearts and in patients with dilated car- diomyopathy. Eur Heart J 1994; 15: 164–170.
- Heusch G. Heart rate and heart failure. Not a simple relationship. Circ J 2011; 75: 229–236.
- Claret PG, Stiell IG, Yan JW, Clement CM, Rowe BH, Calder LA, Perry JJ. Hemody- namic, management, and outcomes of patients admitted to emergency depart- ment with heart failure. Scand J Trauma Resusc Emerg Med 2016; 24: 132.
- Bui AL, Grau-Sepulveda MV, Hernandez AF, Peterson ED, Yancy CW, Bhatt DL, Fonarow GC. Admission heart rate and in-hospital outcomes in patients hospi- talized for heart failure in sinus rhythm and in atrial fibrillation. Am Heart J 2013; 165: 567–574.e6.
- Lan WR, Lin SI, Liao FC, Chang HY, Tsai CT, Wu YJ, Liu PY, Chen CH, Lee YH. Ef- fect of reducing heart rate on outcomes in patients with reduced ejection frac- tion. Am J Cardiol 2021; 150: 77–81.
- Seitelberger R, Guth BD, Heusch G, Lee JD, Katayama K, Ross J Jr. Intracoronary alpha 2-adrenergic receptor blockade at- tenuates ischemia in conscious dogs dur- ing exercise. Circ Res 1998; 62: 436–442.
- Simon L, Ghaleh B, Puybasset L, Giudicelli J-F, Berdeaux A. Coronary and hemodynamic effects of S 16257, a new bradycardic agent, in resting and exercising conscious dogs. J Pharmacol Exp Ther 1995; 275: 659–666.
- Monnet X, Ghaleh B, Colin P, Parent De Curzon O, Giudicelli J-F, Berdeaux A. Effects of heart rate reduction with ivabradine on exercise induced myocardial ischemia and stunning. J Pharmacol Exp Ther 2001; 299: 1133–1139.
- Colin P, Ghaleh B, Monnet X, Hittinger L, Berdeaux A. Effect of graded heart rate reduction with ivabradine on myocardial oxygen consumption and diastolic time in exercising dogs. J Pharmacol Exp Ther 2004; 308: 236–240.
- Heusch G, Skyschally A, Gres P, van Caster P, Schilawa D, Schulz R. Improve- ment of regional myocardial blood flow and function and reduction of infarct size with ivabradine: Protection beyond heart rate reduction. Eur Heart J 2008; 29: 2265–2275.
- Heusch G. Pleiotropic action(s) of the bradycardic agent ivabradine: Cardio- vascular protection beyond heart rate reduction. Br J Pharmacol 2008; 155: 970–971.
- Mulder P, Barbier S, Chagraoui A, Richard V, Henry JP, Lallemand F, Renet S, Lerebours G, Mahlberg-Gaudin F, Thuillez C. Long-term heart rate reduc- tion induced by the selective If current inhibitor ivabradine improves left ventricular function and intrinsic myo- cardial structure in congestive heart fail- ure. Circulation 2004; 109: 1674–1679.
- Crespo-Leiro MG, Anker SD, Maggioni AP, Coats AJ, Filippatos G, Ruschitzka F, Ferrari R, Piepoli MF, Delgado Jimenez JF, Metra M, Fonseca C, Hradec J, Amir O, Logeart D, Dahlström U, Merkely B, Drozdz J, Goncalvesova E, Hassanein M, Chioncel O, Lainscak M, Seferovic PM, Tousoulis D, Kavoliuniene A, Fruhwald F, Fazlibegovic E, Temizhan A, Gatzov P, Erglis A, Laroche C, Mebazaa A, Heart Failure Association (HFA) of the European Society of Cardi- ology (ESC). European Society of Cardi- ology Heart Failure Long-Term Registry (ESC-HF-LT): 1-year follow-up out- comes and differences across regions. Eur J Heart Fail 2016; 18: 613–625.
- Komajda M, Tavazzi L, Swedberg K, Böhm M, Borer JS, Moyne A, Ford I, Investigators SHIFT. Chronic exposure to ivabradine reduces readmissions in the vulnerable phase after hospitaliza- tion for worsening systolic heart failure: a post-hoc analysis of SHIFT. Eur J Heart Fail 2016; 18: 1182–1189.
- Hidalgo FJ, Anguita M, Castillo JC, Rodríguez S, Pardo L, Durán E, Sánchez JJ, Ferreiro C, Pan M, Mesa D, Delgado M, Ruiz M. Effect of early treatment with ivabradine combined with beta-blockers versus beta-blockers alone in patients hospitalised with heart fail- ure and reduced left ventricular ejection fraction (ETHIC-AHF): A randomised study. Int J Cardiol 2016; 217: 7–11.
- Lopatin YM, Cowie MR, Grebennikova AA, Sisakian HS, Pagava ZM, Hayrapetyan HG, Abdullaev TA, Voronkov LG, Chesnikova AI, Tseluyko VI, Tarlovskaya EI, Dadashova GM, Berkinbaev SF, Glezer MG, Koziolova NA, Rakisheva AG, Kipiani ZV, Kurlyanskaya AK. Optimization of heart rate lowering therapy in hospitalized patients with heart failure: Insights from the Optimize Heart Failure Care Program. Int J Cardiol 2018; 260: 113–117.
- Prins KW, Neill JM, Tyler JO, Eckman PM, Duval S. Effects of Beta-Blocker withdrawal in acute decompensated heart failure: A systematic review and meta-analysis. JACC Heart failure 2015; 3: 647–653.
- Lam CSP, Butler J. Victims of Success in Failure. Circulation 2020; 142: 1129–1131.
- Su Y, Ma T, Wang Z, Dong B, Tai C, Wang H, Zhang F, Yan C, Chen W, Xu Y, Ye L, Tye GJ, Ong SB, Zhang J, Xu D. Efficacy of early initiation of ivabradine treatment in patients with acute heart failure: rationale and design of SHIFT-AHF trial. ESC Heart Fail 2020; 7: 4465–4471.
—————————————————————————————————————————
* Chú thích:
1Division of Cardiology, Chi-Mei Medical Center, Tainan, Taiwan; 2Department of Public Health, College of Medicine, National Cheng Kung University, Tainan, Taiwan; 3Cardiovascular Center, Taichung Veterans General Hospital, Taichung, Taiwan; 4Faculty of Medicine, School of Medicine, National Yang Ming Chiao Tung University, Taipei, Taiwan; 5Division of Cardiology, Department of Internal Medicine, E-Da hospital, I-Shou University, Kaohsiung, Taiwan; 6Division of Cardiology, Department of Medicine, Taipei Veterans General Hospital, Taipei, Taiwan; 7Department of Medicine, Mackay Medical College, New Taipei, Taiwan; 8Cardiovascular Center, MacKay Memorial Hospital, Taipei, Taiwan; 9Division of Cardiology, Department of Internal Medicine, Hsinchu MacKay Memorial Hospital, Hsinchu, Taiwan; 10Division of Cardiology, Taitung MacKay Memorial Hospital, Taitung, Taiwan; 11Division of Cardiology, Department of Medicine, Tri-Service General Hospital, National Defense Medical Center, Taipei, Taiwan; 12Division of Cardiology and Cardiovascular Research Center, Department of Internal Medicine, Taipei Medical University Hospital, Taipei, Taiwan; 13Taipei Heart Institute, Division of Cardiology, Department of Internal Medicine, School of Medicine, College of Medicine, Taipei Medical University, Taipei, Taiwan; and 14Heart Center, Cheng Hsin General Hospital, No.45 Cheng-Hsin Street, 112 Beitou, Taipei, Taiwan.







