BS. NGUYỄN THANH HIỀN
* Khoa Nội Tim Mạch Bệnh viện Đại học Y Dược
Mặc dù có những tiến bộ trong điều trị, bệnh nhân suy tim vẫn có tỷ lệ tiến triển nặng và tử vong cao, do đó rất cần thiết phải tìm các phương pháp điều trị mới nhằm cải thiện kết cục lâm sàng của bệnh nhân. Bệnh nhân suy tim có tình trạng tăng đông và tăng nguy cơ bị huyết khối thuyên tắc, kể cả những bệnh nhân suy tim nhịp xoang. Do đó, điều trị thuốc kháng đông đường uống đã nổi lên như một chiến lược khả thi để cải thiện kết cục cho bệnh nhân. Trước đây, có các thử nghiệm lâm sàng ngẫu nhiên so sánh tác dụng của warfarin với kháng kết tập tiểu cầu ở bệnh nhân suy tim nhịp xoang. Mặc dù không nghiên cứu nào cho thấy kết cục chính cải thiện đáng kể, tuy nhiên biến cố thuyên tắc do huyết khối lại có dấu hiệu giảm đi cùng vớinguy cơ chảy máu gia tăng.Với những kết quả này, các hướng dẫn hiện nay không khuyến cáo sử dụng kháng đông uống ở bệnh nhân suy tim nhịp xoang mà không có tiền sử các biến cố huyết khối thuyên tắc hoặc thuyên tắc từ tim. Tuy nhiên, trong thời gian gần đây, các thử nghiệm ngẫu nhiên có đối chứng sử dụng kháng đông đường uống tác dụng trực tiếp, có cơ chế tác động khác và an toàn hơn warfarin, đã báo cáo những tác dụng có lợi ở bệnh nhân suy tim nhịp xoang.Bài viết nhằm mục đích thảo luận về cơ sở lý luận cho kháng đông uống ở bệnh nhân suy tim nhịp xoang, tóm tắt dữ liệu có sẵn và khoảng trống của kiến thức nền tảng, cung cấp thời điểm các kháng đông đường uống có thể được xem xét.
TAM GIÁC VIRCHOW VÀ SUY TIM LÀ MỘT TÌNH TRẠNG TĂNG ĐÔNG
Tam giác Virchow, trong đó ứ trệ tuần hoàn, rối loạn chức năng nội mô và tình trạng tăng đônghội tụ thúc đẩy hình thành huyết khối, giải thích khuynh hướng bệnh nhân suy tim dễ bị các biến cố huyết khối thuyên tắc (hình 1) (1, 56).
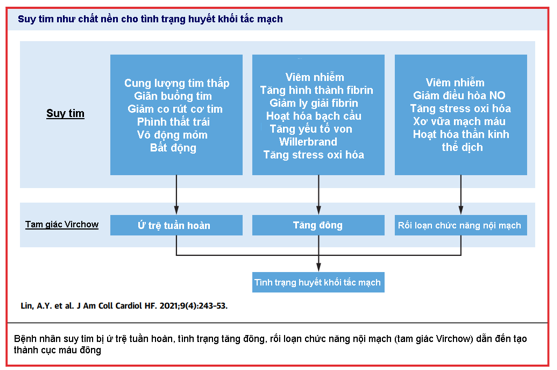
Hình 1. Khuynh hướng của bệnh nhân HF đối với các biến cố huyết khối thuyên tắc (56)
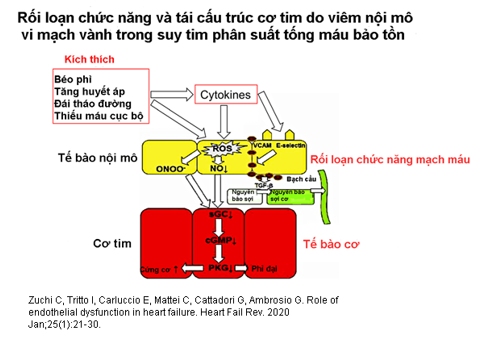
Hình 2. Các cơ chế liên quan đến rối loạn chức năng mạch máu và tế bào cơ tim gây ra bởi các tác nhân gây viêm và stress oxy hóa trong vi tuần hoàn mạch vành (4)
Ở bệnh nhân suy tim, cung lượng tim thấp và tăng áp suất đổ đầy bên phải trở nên trầm trọng hơn bởi bệnh nhân giảm khả năng vận động, dẫn đến dòng máu di chuyển chậm và tăng đông trong toàn bộ hệ thống mạch máu. Tim dãn lớn, giảm co bóp cơ tim ở cả tâm nhĩ và tâm thất,và áp lực trongbuồng tim tăng cao làm trầm trọng thêm tình trạng này và dẫn đến hình thành huyết khối.Rối loạn chức năng nội mô ở bệnh nhân suy tim dẫn đến giảm giải phóng nitric oxit (NO) (2-4). Tình trạng viêm và tăng stress oxy hóa càng làm giảm NO (hình 2). Sụt giảm NO dẫn đến co mạch ngoại vi và thúc đẩy sự kết dính của bạch cầu đơn nhân và tiểu cầu vào bề mặt nội mô của mạch máu và tim(5).Tăng mức độ dimethylarginine không đối xứng(6),một chất ức chế tổng hợp NO nội sinh, làm giảm hoạt động của superoxide dismutase ngoại bào liên kết với nội mô, một loại enzyme loại bỏ mảnh vụn sau phản ứng oxy hóa (7), và thay đổi biểu hiện của microRNA,đóng vai trò quan trọng trong việc duy trì tính toàn vẹn và điều chỉnh sự phát triển mạch máu (8),góp phần vào rối loạn chức năng nội mô. Không có gì đáng ngạc nhiên khi chức năng nội mô bị suy giảm ở những bệnh nhân suy tim có liên quan độc lập với các biến cố lâm sàng (3,9-11).
Tăng hình thành thrombin kết hợp với suy giảm tiêu sợi huyết do kích hoạt các con đường viêm và thần kinh thể dịch dẫn đến tình trạng tăng đông trong suy tim(12,13). Kích hoạt tiểu cầu do yếu tố Von Willebrand lưu hành trong máu cao cũng góp phần vào quá trình tăng đông (14). Nhìn chung, các con đường liên quan đến thrombin góp phần vào biến cố tim mạch vì gây ra tổn thương tế bào cơ tim, viêm nhiễm, rối loạn chức năng nội mô và vi huyết khối (15).
BẰNG CHỨNG TĂNG NGUY CƠ THUYÊN TẮC HUYẾT KHỐI Ở BỆNH NHÂN SUY TIM NHỊP XOANG
Tình trạng tăng đông ở bệnh nhân suy tim làm tăng nguy cơ mắc các biến cố huyết khối thuyên tắc bao gồm đột quỵ, huyết khối trong tim, huyết khối tĩnh mạch sâu, thuyên tắc phổi và nhồi máu cơ tim.
Đột quỵ: Tỷ lệ đột quỵ ở người lớn ởHoa Kỳ là 2,5% (16).Theo phân tích hồi cứu từ nghiên cứu CORONA và GISSI-HF,đột quỵ xảy ra ở 3,4% bệnh nhân bị suy tim không có rung nhĩ(17). Báo cáo theo dõi 289.353 bệnh nhân tại Đan Mạch mắc suy tim trong 30 năm chỉ ra có mối liên quan đáng kể giữa suy tim và đột quỵ do thiếu máu cục bộ(18). Người bệnh suy tim mới khởi phát đặc biệt dễ bị tổn thương, nguy cơ đột quỵ do thiếu máu cục bộ tăng hơn 5 lần trong tháng đầu tiên sau khi chẩn đoán(19). Những đột quỵ thầm lặngthường gặp ở những bệnh nhân bị suy tim, xảy ra ở khoảng 35% bệnh nhân bị bệnh cơ tim giãn nở so với 3% trong nhóm không bị suy tim(20). Mặc dù nguy cơ đột quỵ tăng lênở bệnh nhân suy tim với phân suất tống máu giảm và bảo tồn, tỉ lệ này cao hơn ở bệnh nhân suy tim phân suất tống máu giảm (21).Ở những bệnh nhân nhập viện gần đây cho thấy mức peptide lợi niệu natri cao và đột quỵ có liên quan với độ nặng của suy tim. Nguy cơ đột quỵ tái phát tăng lên gấp 2 lần ở bệnh nhân suy tim (22,23); trong mộtkhảo sát, tỉ lệ được báo cáo là 12%/năm (24) ở bệnh nhân suy tim nhịp xoang, tỷ lệ tương tự như ở bệnh nhân rung nhĩ (25). Ngoài ra,biến cố đột quỵ ở bệnh nhân suy tim có tỷ lệ tử vong cao hơn, triệu chứng thần kinh nghiêm trọng hơn và thời gian nằm viện lâu hơn so với những bệnh nhân không có suy tim (26).
Huyết khối tiểu nhĩ trái: Tiểu nhĩ trái là vị trí phổ biến để hình thành huyết khối ở bệnh nhân suy tim vì đặc trưng giải phẫu của nó.Tỷ lệ huyết khối tiểu nhĩ trái dao động trong khoảng 40-68% bệnh nhân suy tim nhịp xoang (27-29). Yếu tố tiên đoán huyết khối tiểu nhĩ trái bao gồm hình dạng tiểu nhĩ trái, EF giảm, tăng đường kính tâm trương thất trái.
Huyết khối thất trái: Huyết khối trong thất trái đã được báo cáo khoảng 11% đến 44% bệnh nhân suy tim (30),tỉ lệ nghịch với phân suất tống máu thất trái (31). Hở van hai lá nặng có thể có tác dụng bảo vệ vì làm giảm ứ trệ trong tâm thất trái(32).Tăng áp lực thất trái cuối tâm trương và rối loạn vận động vùng có liên quan đếnhình thành huyết khối thất trái (33), giải thích tại sao huyết khối thường xuất hiện trong bệnh cảnh nhồi máu cơ tim thành trước rộng, phình thất trái và bệnh cơ tim giãn (34,35).
Huyết khối tĩnh mạch sâu và thuyên tắc phổi: Sung huyết và ứ trệ tĩnh mạch là yếu tố nguy cơ của huyết khối tĩnh mạch sâu. Trong một phân tích gộp của 71 nghiên cứu, huyết khối tĩnh mạch có triệu chứng được báo cáo ở 3,7% trường hợp bệnh nhân suy tim nhập viện không được điều trị dự phòng huyết khối(36). Sự hiện diện của huyết khối tĩnh mạch ở bệnh nhân bị suy tim có tác động quan trọng đến diễn biến lâm sàng vì thuyên tắc phổi đã được xác định là nguyên nhân gây tử vong phổ biến ở nhóm bệnh nhân này (37,38).
Nhồi máu cơ tim cấp: Cải thiện khả năng sống sót sau NMCT cấp đã góp phần làm tăng tỉ lệ suy tim do bệnh mạch vành. Ngược lại, một khi suy tim được chẩn đoán, nhồi máu cơ tim cấp là biến cố thường gặp. Trong nghiên cứu OPTIMAAL ở bệnh nhân suy tim, 57% trong số 180 bệnh nhân có bằng chứng của NMCT cấp khi tử thiết (39). Trong một nghiên cứu trên 884.931 bệnh nhân Medicare, suy tim là một yếu tố nguy cơ độc lập đối với NMCT tái phát (40). Suy tim làm nguy cơ NMCT tái phát hoặc tử vong do bệnh mạch vanh ở nam giới cao gấp 2 lần theo chương trình dịch tễ học tim mạch tại Stockholm( 41).
TÁC DỤNG CỦA KHÁNG ĐÔNG Ở BỆNH NHÂN SUY TIM NHỊP XOANG
Mặc dù các nghiên cứu trước đây về warfarin không cho thấybằng chứng thuyết phục về lợi ích lâm sàng ở bệnh nhân suy tim nhịp xoang, một số báo cáo tỷ lệ đột quỵ thiếu máu giảm. Những nghiên cứu này cũng như một số nghiên cứu mới gần đây cho thấy lợi ích của kháng đông đường uống tác dụng trực tiếp liều thấp ở bệnh nhân suy tim nhịp xoang.
THỬ NGHIỆM SỬ DỤNG WARFARIN
Thử nghiệm lâm sàng WARCEF: so sánh giữa warfarin và aspirin liều 325mg/ ngày ở 2.305 bệnh nhân suy tim phân suất tống máu giảm có nhịp xoang. Không có sự khác biệt về kết cục của đột quỵ do thiếu máu, xuất huyết não, hoặc tử vong do mọi nguyên nhân giữa các nhóm điều trị. Tỉ lệ đột quỵ thiếu máu ở nhóm sử dụng warfarin giảm đáng kể so với nhóm sử dụngaspirin (2.5% vs. 4.7%; p=0.005) bị lu mờ bởi tỉ lệ xuất huyết nặng tăng gấp 2 lần.
Thử nghiệm WATCH(5): thực hiện sau các thử nghiệm nhỏ hơn như WASH và HELAS. Trong nghiên cứu này, 1.587 bệnh nhân suy tim còn nhịp xoang có triệu chứng (LVEF <35%) được điều trị warfarin nhãn mở hoặc điều trị mù đôi bằng aspirin (162mg/ngày) với giả dược hoặc clopidogrel (75mg/ngày) với giả dược. Không có sự khác biệt trong kết quả của lần xuất hiện biến cố đầu tiên gồm tử vong, nhồi máu cơ tim cấp không tử vong, hoặc đột quỵ không tử vong giữa các nhóm điều trị; đột quỵ không tử vong xảy ra ít hơn trong nhóm điều trị warfarin so với nhóm điều trị aspirin hoặc clopidogrel (warfarin vs aspirin vs clopidogrel lần lượt: 0,2% vs 1,7% vs 2,1%). Tỉ lệ nhập viện do suy tim ở nhóm dùng warfarin thấp hơn so với aspirin (16,5% vs 22,2%; p = 0,02). Biến cố xuất huyết cao hơn khi dùng warfarin so với dung kháng kết tập tiểu cầu.
NGHIÊN CỨU SỬ DỤNG KHÁNG ĐÔNG ĐƯỜNG UỐNG TÁC DỤNG TRỰC TIẾP
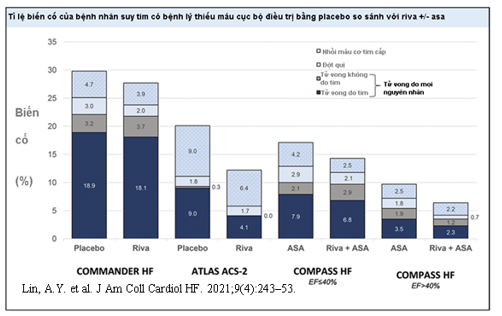
Hình 3. Các nghiên cứu sử dụng kháng đông đường uống tác dụng trực tiếp (56)
ATLAS ACS 2 – TIMI51: thử nghiệm ngẫu nhiên ở 15.526 bệnh nhân bị hội chứng vành cấp xảy ra trong thời gian gần được điều trị Rivaroxaban liều 2,5mg hoặc 5 mg hai lần mỗi ngày hoặc giả dược cùng với liệu pháp kháng kết tập tiểu cầu nền (42). Nhóm Rivaroxaban 2,5mg và 5mg giảm biến cố chính như tử vong do nguyên nhân tim mạch, NMCT cấp, hoặc đột quỵ so với giả dược (9,1% vs 10,7% [p = 0,02] và 8,8% vs 10,7% [p = 0,03]). Rivaroxaban tăng tỷ lệ chảy máu nặng không liên quan đến bắc cầu mạch vành (2,1% vs 0,6%;p <0,001) và xuất huyết nội sọ (0,6% vs 0,2%; p = 0,009), không tăng đáng kể chảy máu gây tử vong (0,3% vs 0,2%; p = 0,66). Liều 2,5mg gây chảy máu tử vong ít hơn đáng kể so với liều 5mg. Trong 1.694 bệnh nhân suy tim ở thời điểm phân chia ngẫu nhiên, phân tích cho thấy rằng liều 2,5mg (HR 0,42; KTC 95%: 0,59 đến 0,81;p = 0,001) và liều 5mg (HR: 0,44; KTC 95%: 0,61 đến 0,84; p = 0,002) của rivaroxaban làm giảm đáng kể kết cục chính, tỷ lệ tử vong do tim mạch và tử vong do mọi nguyên nhân mà không làm tăng nguy cơ chảy máu nặng (43).
COMPASS: là thử nghiệm lâm sàng ngẫu nhiên mù đôi có đối chứng, trong đó 27.395 bệnh nhân bệnh mạch vành ổn định hoặc động mạch ngoại biên có nhịp xoang được điều trị rivaroxaban (2,5mg x 2 lần/ngày) cộng với aspirin (100 mg/ngày), rivaroxaban (5mg x 2 lần/ngày), hoặc aspirin (100 mg/ngày)(44). Các kết cục chính: tử vong do tim mạch, đột quỵ, hoặc NMCT cấp xảy ra ít hơn ở nhóm bệnh nhân dùng 2,5mg rivaroxaban cộng với aspirin so với nhóm aspirin đơn độc (4,1% vs 5,4%; HR 0,76; KTC 95%; 0,66 đến 0,86; p <0,001). Mặc dù xuất huyết nặng xảy ra ở nhóm này nhiều hơn so với chỉ dùng aspirin (3,1% vs 1,9%; HR: 1,70; KTC 95%: 1,40 đến 2,05;p <0,001) nhưng không có sự khác biệt đáng kể về chảy máu nội sọ hoặc tử vong. Trong một phân tích hậu kỳ về 5.902 bệnh nhân bị suy tim, liều 2,5mg rivaroxaban với aspirin có liên quan đến mức giảm nguy cơ tuyệt đối lớn hơn (2,4% so với 1,0%) và giảm rủi ro tương đối tương tự bệnh nhân không suy tim về các biến cố tim mạch nghiêm trọng(45). Những tác động có lợi này thấy được ở những bệnh nhân có LVEF ≤ 40% hoặc LVEF> 40% (hình 3). Nguy cơ xuất huyết như nhau ở bệnh nhân có hay không có suy tim.
COMMANDER-HF: khả năng liều thấp rivaroxaban có thể cải thiện kết quả ở bệnh nhân suy tim nhịp xoang đã được thử nghiệm trong COMMANDER HF (Nghiên cứu đánh giá tính hiệu quả và an toàn của Rivaroxaban trong việc giảm nguy cơ tử vong, nhồi máu cơ tim hoặc đột quỵ ở những người tham gia bị suy tim và bệnh động mạch vành sau một đợt suy tim mất bù)(46). Trong COMMANDER-HF, hiệu quả của liều 2,5mg rivaroxaban trên tử vong do mọi nguyên nhân, NMCT cấp,và đột quỵ được đánh giá ở 5.022 bệnh nhân bệnh mạch vành có nhịp xoang với LVEF <40% sau đợt mất bù cấp gần đây. Tuy nhiên, rivaroxaban không thể giảm tiêu chí chính hay nhập viện do suy tim, cũng như các tiêu chí phụ. Quan sát tỷ lệ tử vong, yếu tố kết cục chính, COMMANDERHF cao hơn đáng kể so với ATLAS ACS 2 – TIMI 51 hoặc COMPASS và các ca nhập viện do suy tim thường xuyên xảy ra gợi ý rằng kết quả của nghiên cứu không hiệu quả bởi vì sự thật là các kết cục này được thúc đẩy bởi các sự kiện liên quan đến nguyên nhân suy bơm hơn là huyết khối thuyên tắc. Tuy nhiên, trong dân số nghiên cứu của COMMANDER-HF, các biến cố huyết khối thuyên tắc không phải là hiếm gặp với sự kết hợp của NMCT cấp, đột quỵ do thiếu máu, đột tử do tim, huyết khối tĩnh mạch sâu có triệu chứng, và thuyên tắc phổi xảy ra ở 15,5% bệnh nhân sử dụng giả dược(47). Hơn nữa, rivaroxaban liên quan đến việc giảm đáng kể 17% kết cục huyết khối thuyên tắc (hình 4). Trong 150 trường hợp đột quỵ xảy ra trong COMMANDER-HF, hầu hết là thiếu máu cục bộ và kết quả rất xấu, với gần một nửa số bệnh nhân tử vong hoặc bị mất khả năng vận động nặng (48). Rivaroxaban giảm đáng kể nguy cơ đột quỵ hoặc cơn thoáng thiếu máu não khoảng 33% mà không tăng nguy cơ xuất huyết.
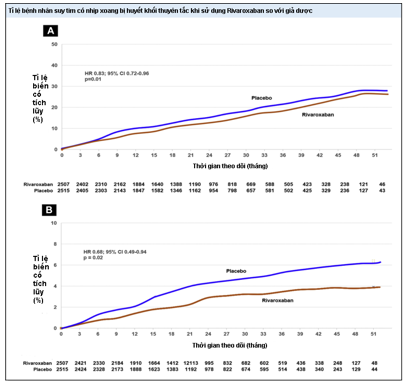
Hình 4. Xuất hiện các biến cố huyết khối thuyên tắc ở bệnh nhân suy tim và bệnh mạch vành có nhịp xoang được điều trị bằng rivaroxaban so với giả dược từ thử nghiệm COMMANDER HF.
(A) Bệnh nhânđược điều trị bằng rivaroxaban đã làm giảm các biến cố huyết khối thuyên tắc tổng hợp, được định nghĩa là nhồi máu cơ tim, đột quỵ do thiếu máu cục bộ, tử vong đột ngột / không mong muốn,thuyên tắc phổi có triệu chứng, hoặc huyết khối tĩnh mạch sâu có triệu chứng, so với bệnh nhân dùng giả dược.
(B) Giảm đột quỵ do mọi nguyên nhân hoặc thiếu máu não thoáng qua ở bệnh nhân được điều trị bằng rivaroxaban so với giả dược (56).
CÂN NHẮC TRƯỚC KHI ĐIỀU TRỊ KHÁNG ĐÔNG
Dù nguy cơ biến cố huyết khối thuyên tắc tăng cao ởbệnh nhân suy tim nhịp xoang, chỉ định kháng đông đường uống nóng lên trong thời gian gần đây bởi các nghiên cứu thực tế cho thấy giảm nguy cơ tuy rằng không được thiết kế tốt cũng như không mạnh để đưa ra khuyến cáo. Bác sĩ lâm sàng phải quyết định xem có nên chỉ định kháng đông uống cho những bệnh nhân này hay không. Dự đoán chính xác nguy cơ đột quỵ có thể giúp giải quyết tình trạng tiến thoái lưỡng nan về vấn đề này; phương pháp tiếp cận sẽ được thảo luận tiếp theo đây.
ĐIỂM CHA2DS2-VASc DÙNG ĐỂ TIÊN LƯỢNG
Thang điểm CHA2DS2-VASc, bao gồm 7 đặc điểm lâm sàng (suy tim sung huyết, tăng huyết áp, 75 tuổi trở lên, đái tháo đường, đột quỵ / cơn thoáng thiếu máu não, bệnh mạch máu, tuổi từ 65 đến 74, giới tính) có liên quan đến nguy cơ huyết khối thuyên tắc được sử dụng rộng rãi để dự đoán đột quỵ ở bệnh nhân rung nhĩ. Một số nghiên cứu cho thấy thang điểm này có thể hữu ích ở bệnh nhân suy tim nhịp xoang. Trong 136.545 bệnh nhân nhập viện vì suy tim, CHA2DS2-VASc dự báo biến chứng huyết khối thuyên tắc (đột quỵ do thiếu máu cục bộ, cơn thoáng thiếu máu não và thuyên tắc động mạch ngoại vi) ở bệnh nhân nhịp xoang tốt như đã được báo cáo ở bệnh nhân rung nhĩ(49). Một nghiên cứu quan sát mô tả (registry study) ở Đan Mạch trên 42.987 bệnh nhân suy tim báo cáo rằng mặc dù điểm CHA2DS2-VASc tăng có liên quan đến nguy cơ đột quị do thiếu máu, huyết khối tắc mạch và tử vong cao hơn, tuy nhiên thang điểm này chỉ có giá trị dự đoán khiêm tốn về đột quỵ do thiếu máu (thống kê C trong 1 năm là 0,64)(50). Ở những bệnh nhân trong thử nghiệm WARCEF,điểm CHA2DS2-VASc có giá trị dự đoán mức độ trung bình (51), được cải thiện bằng cách thêm thông tin về bệnh tim thiếu máu cục bộ và bệnh thận mạn (52). Tương tự, thang điểm CHA2DS2-VASc thể hiện độ chính xác mức độ trung bình để dự đoán rủi ro đột quỵ / thiếu máu não thoáng qua trong nghiên cứu COMMANDER HF(48).
CÁC YẾU TỐ NGUY CƠ KHÁC
Bệnh nhân trong nhóm có mức D-dimer cao nhất ở nghiên cứu COMMANDER HF có nguy cơ đột quỵ cao nhất cũng như khả năng giảm đột quị cao nhất với rivaroxaban (53, 54). Dấu hiệu khi siêu âm tim bao gồm EF thấp, dòng chảy chậm, giảm strain toàn thể và hạn chế đổ đầy thất trái cũng có liên quan đến rủi ro đột quỵ do thiếu máu cục bộ (55). Rối loạn nhịp kịch phát, có thể không được phát hiện bằng cách sử dụng các thiết bị theo dõi thông thường, có thể là một yếu tố rủi ro đối với biến cố huyết khối tắc mạch. Rung nhĩ kịch phát đôi khi khó phát hiện do đó tìm kiếm rối loạn nhịp kịch phát bằng thiết bị theo dõi tiêu chuẩn hoặc những thiết bị cấy ghép mới có sẵn cũng có thể được xem xét.
ĐỀ NGHỊ XEM XÉT DÙNG KHÁNG ĐÔNG Ở BỆNH NHÂN SUY TIM NHỊP XOANG
Sơ đồ xem xét sử dụng kháng đông ở bệnh nhân suy tim có nhịp xoang được thể hiện ở hình 5. Mặc dù các khuyến cáo phần lớn không đề cập sử dụng kháng đông ở bệnh nhân suy tim nhịp xoang, nhưng các hướng dẫn đề nghị chiến lược điều trị kháng đông cho các tình trạng cụ thể sau:
– Phình thất trái,
– Các biến cố huyết khối thuyên tắc trước đây,
– Sau nhồi máu cơ tim cấp ST chênh lên kèm loạn động hoặc vô động vùng mỏm thành trước thất trái).
– Ngoài ra, dựa trên kết quả nghiên cứu ATLAS, ACS 2 – TIMI 51 và COMPASS, các hướng dẫn điều trị khuyến cáo sử dụng rivaroxaban 2,5mg hai lần mỗi ngày cùng với aspirin và clopidogrel ở bệnh nhân hội chứng vành cấp có nguy cơ xảy ra biến cố thiếu máu cục bộ cao (khuyến cáo nhóm IIb) và rivaroxaban 2,5 mg hai lần mỗi ngày cùng với aspirin ở bệnh nhân hội chứng mạch vành mạn có nguy cơ xảy ra biến cố thiếu máu cục bộ trung bình đến cao (khuyến cáo nhóm IIa), nguy cơ xuất huyết không cao.
Vì lợi ích của kháng đông uống trong những nghiên cứu này đã được chỉ ra ở những bệnh nhân suy tim nhịp xoang. Do đó, việc sử dụng chúng nên được cân nhắc ở những bệnh nhân nằm trong nhóm này sau hội chứng vành cấp hoặc có hội chứng mạch vành mạn.
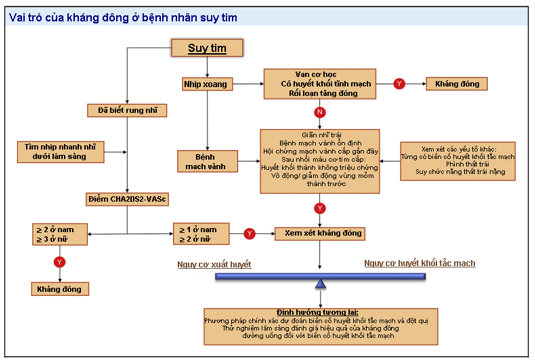
Hình 5. Sơ đồ hướng dẫn sử dụng kháng đông ở bệnh nhân suy tim có nhịp xoang (56)
TÀI LIỆU THAM KHẢO1. Lip GY, Gibbs CR. Does heart failure confer ahypercoagulable state? Virchow’s triad revisited.J Am Coll Cardiol 1999;33:1424–6.2. Chong AY, Blann AD, Patel J, Freestone B,Hughes E, Lip GY. Endothelial dysfunction and damage in congestive heart failure: relation offlow-mediated dilation to circulating endothelial cells, plasma indexes of endothelial damage, andbrain natriuretic peptide. Circulation 2004;110:1794–8.3. Heitzer T, Baldus S, von Kodolitsch Y,Rudolph V, Meinertz T. Systemic endothelial dysfunction as an early predictor of adverseoutcome in heart failure. Arterioscler Thromb VascBiol 2005;25:1174–9.4. Zuchi C, Tritto I, Carluccio E, Mattei C,Cattadori G, Ambrosio G. Role of endothelialdysfunction in heart failure. Heart Fail Rev 2020;25:21–30.5. Kim W, Kim EJ. Heart failure as a risk factor forstroke. J Stroke 2018;20:33–45.6. Usui M, Matsuoka H, Miyazaki H, Ueda S,Okuda S, Imaizumi T. Increased endogenous nitricoxide synthase inhibitor in patients with congestive heart failure. Life Sci 1998;62:2425–30.7. Landmesser U, Spiekermann S, Dikalov S, et al.Vascular oxidative stress and endothelial dysfunction in patients with chronic heart failure:role of xanthine-oxidase and extracellular superoxide dismutase. Circulation 2002;106:3073–8.8. Santulli G. MicroRNAs and endothelial (dys)function. J Cell Physiol 2016;231:1638–44.9. Fischer D, Rossa S, Landmesser U, et al. Endothelial dysfunction in patients with chronic heartfailure is independently associated with increasedincidence of hospitalization, cardiac transplantation, or death. Eur Heart J 2005;26:65–9.10. Katz SD, Hryniewicz K, Hriljac I, et al. Vascularendothelial dysfunction and mortality risk in patients with chronic heart failure. Circulation 2005;111:310–4.11. de Berrazueta JR, Guerra-Ruiz A, GarcíaUnzueta MT, et al. Endothelial dysfunction,measured by reactive hyperaemia using straingauge plethysmography, is an independent predictor of adverse outcome in heart failure. Eur JHeart Fail 2010;12:477–83.12. Yamamoto K, Ikeda U, Furuhashi K, Irokawa M,Nakayama T, Shimada K. The coagulation system isactivated in idiopathic cardiomyopathy. J Am CollCardiol 1995;25:1634–40.13. Jafri SM, Ozawa T, Mammen E, Levine TB,Johnson C, Goldstein S. Platelet function,thrombin and fibrinolytic activity in patients withheart failure. Eur Heart J 1993;14:205–12.14. Sbarouni E, Bradshaw A, Andreotti F,Tuddenham E, Oakley CM, Cleland JG. Relationship between hemostatic abnormalities andneuroendocrine activity in heart failure. Am HeartJ 1994;127:607–12.15. Zannad F, Stough WG, Regnault V, et al. Isthrombosis a contributor to heart failure pathophysiology? Possible mechanisms, therapeuticopportunities, and clinical investigation challenges. Int J Cardiol 2013;167:1772–82.16. Benjamin EJ, Muntner P, Alonso A, et al. Heartdisease and stroke statistics—2019 update: areport from the American Heart Association. Circulation 2019;139:e56–528.17. Abdul-Rahim AH, Perez AC, Fulton RL, et al.Risk of stroke in chronic heart failure patients without atrial fibrillation: analysis of theControlled Rosuvastatin in Multinational TrialHeart Failure (CORONA) and the Gruppo Italianoper lo Studio della Sopravvivenza nell’InsufficienzaCardiaca-Heart Failure (GISSI-HF) Trials. Circulation 2015;131:1486–94.18. Adelborg K, Szépligeti S, Sundbøll J, et al. Riskof stroke in patients with heart failure: a population-based 30-year cohort study. Stroke 2017;48:1161–8.19. Alberts VP, Bos MJ, Koudstaal P, et al. Heartfailure and the risk of stroke: the Rotterdam Study.Eur J Epidemiol 2010;25:807–12.20. Kozdag G, Ciftci E, Ural D, et al. Silent cerebralinfarction in chronic heart failure: ischemic andnonischemic dilated cardiomyopathy. Vasc HealthRisk Manag 2008;4:463–9.21. Greenberg B, Peterson ED, Berger JS, et al.Ejection fraction, B-type natriuretic peptide andrisk of stroke and acute myocardial infarctionamong patients with heart failure. Clin Cardiol2019;42:277–84.22. Petty GW, Brown RD Jr., Whisnant JP, Sicks JD,O’Fallon WM, Wiebers DO. Survival and recurrenceafter first cerebral infarction: a population-basedstudy in Rochester, Minnesota, 1975 through1989. Neurology 1998;50:208–16.23. Gage BF, van Walraven C, Pearce L, et al.Selecting patients with atrial fibrillation for anticoagulation: stroke risk stratification in patientstaking aspirin. Circulation 2004;110:2287–92.24. Witt BJ, Brown RD Jr., Jacobsen SJ, et al.Ischemic stroke after heart failure: a communitybased study. Am Heart J 2006;152:102–9.25. Katsanos AH, Parissis J, Frogoudaki A, et al.Heart failure and the risk of ischemic strokerecurrence: a systematic review and meta-analysis. J Neurol Sci 2016;362:182–7.26. Haeusler KG, Laufs U, Endres M. Chronic heartfailure and ischemic stroke. Stroke 2011;42: 2977–82.27. Bakalli A, Georgievska-Ismail L, Koçinaj D,et al. Left ventricular and left atrial thrombi insinus rhythm patients with dilated ischemic cardiomyopathy. Med Arch 2012;66:155–8.28. Bakalli A, Georgievska-Ismail L, Koçinaj D,Musliu N, Krasniqi A, Pllana E. Prevalence of leftchamber cardiac thrombi in patients with dilatedleft ventricle at sinus rhythm: the role of transesophageal echocardiography. J Clin Ultrasound2013;41:38–45.29. Bakalli A, Georgievska-Ismail LJ, ZantevaNaumoska M, et al. Predictors of left atrialappendage thrombus in heart failure patients atsinus rhythm. Eur Heart J 2013;34.30. Sivri N, Yetkin E, Tekin GO, Yalta K,Waltenberger J. Anticoagulation in patients withleft ventricular systolic dysfunction and sinusrhythm: when? Clin Appl Thromb Hemost 2014;20:729–34.31. Dries DL, Rosenberg YD, Waclawiw MA,Domanski MJ. Ejection fraction and risk ofthromboembolic events in patients with systolicdysfunction and sinus rhythm: evidence for genderdifferences in the studies of left ventriculardysfunction trials. J Am Coll Cardiol 1997;29:1074–80.32. Kalaria VG, Passannante MR, Shah T, Modi K,Weisse AB. Effect of mitral regurgitation on leftventricular thrombus formation in dilated cardiomyopathy. Am Heart J 1998;135:215–20.33. Choi UL, Park JH, Sun BJ, et al. Impaired leftventricular diastolic function is related to theformation of left ventricular apical thrombus inpatients with acute anterior myocardial infarction.Heart Vessels 2018;33:447–52.34. Asinger RW, Mikell FL, Elsperger J, Hodges M.Incidence of left-ventricular thrombosis after acute transmural myocardial infarction. Serialevaluation by two-dimensional echocardiography. N Engl J Med 1981;305:297–302.35. Lee GY, Song YB, Hahn JY, et al. Anticoagulation in ischemic left ventricular aneurysm.Mayo Clin Proc 2015;90:441–9.36. Tang L, Wu YY, Lip GY, Yin P, Hu Y. Heartfailure and risk of venous thromboembolism: asystematic review and meta-analysis. LancetHaematol 2016;3:e30–44.37. Bounameaux H, Agnelli G. Symptoms andclinical relevance: a dilemma for clinical trials onprevention of venous thromboembolism. ThrombHaemost 2013;109:585–8.38. Garg R, Yusuf S. Overview of randomized trialsof angiotensin-converting enzyme inhibitors on mortality and morbidity in patients with heartfailure. Collaborative Group on ACE Inhibitor Trials. JAMA 1995;273:1450–6.39. Orn S, Cleland JG, Romo M, Kjekshus J,Dickstein K. Recurrent infarction causes the mostdeaths following myocardial infarction with leftventricular dysfunction. Am J Med 2005;118:752–8.40. Wang Y, Leifheit E, Normand ST,Krumholz HM. Association between subsequenthospitalizations and recurrent acute myocardialinfarction within 1 year after acute myocardialinfarction. J Am Heart Assoc 2020;9:e014907.41. Leander K, Wiman B, Hallqvist J, Andersson T,Ahlbom A, de Faire U. Primary risk factors influence risk of recurrent myocardial infarction/deathfrom coronary heart disease: results from the Stockholm Heart Epidemiology Program (SHEEP).Eur J Cardiovasc Prev Rehabil 2007;14:532–7.42. Mega JL, Braunwald E, Wiviott SD, et al.Rivaroxaban in patients with a recent acute coronary syndrome. N Engl J Med 2012;366:9–19.43. Korjian S, Braunwald E, Daaboul Y, et al.Usefulness of rivaroxaban for secondaryprevention of acute coronary syndrome in patientswith history of congestive heart failure (from theATLAS-ACS-2 TIMI-51 Trial). Am J Cardiol 2018;122:1896–90144. Eikelboom JW, Connolly SJ, Bosch J, et al.Rivaroxaban with or without aspirin in stable cardiovascular disease. N Engl J Med 2017;377:1319–30.45. Branch KR, Probstfield JL, Eikelboom JW,et al. Rivaroxaban with or without aspirin in patients with heart failure and chronic coronary orperipheral artery disease. Circulation 2019;140:529–37.46. Zannad F, Anker SD, Byra WM, et al. Rivaroxaban in patients with heart failure, sinus rhythm,and coronary disease. N Engl J Med 2018;379:1332–42.47. Greenberg B, Neaton JD, Anker SD, et al. Association of rivaroxaban with thromboembolic eventsin patients with heart failure, coronary disease, andsinus rhythm: a post hoc analysis of the COMMANDER HF trial. JAMA Cardiol 2019;4:515–23.48. Mehra MR, Vaduganathan M, Fu M, et al.A comprehensive analysis of the effects ofrivaroxaban on stroke or transient ischaemicattack in patients with heart failure, coronaryartery disease, and sinus rhythm: the COMMANDER HF trial. Eur Heart J 2019;40:3593–602.49. Wolsk E, Lamberts M, Hansen ML, et al.Thromboembolic risk stratification of patientshospitalized with heart failure in sinus rhythm: anationwide cohort study. Eur J Heart Fail 2015;17:828–36.50. Melgaard L, Gorst-Rasmussen A, Lane DA,Rasmussen LH, Larsen TB, Lip GY. Assessment ofthe CHA2DS2-VASc score in predicting ischemicstroke, thromboembolism, and death in patientswith heart failure with and without atrial fibrillation. JAMA 2015;314:1030–8.
51. Ye S, Qian M, Zhao B, et al. CHA(2)DS(2)-VAS cscore and adverse outcomes in patients with heartfailure with reduced ejection fraction and sinusrhythm. Eur J Heart Fail 2016;18:1261–652. Hai JJ, Chan PH, Chan YH, et al. Prediction ofthromboembolic events in heart failure patients insinus rhythm: the Hong Kong Heart Failure Registry. PLoS One 2016;11:e0169095.53. Freudenberger RS, Cheng B, Mann DL, et al.The first prognostic model for stroke and death inpatients with systolic heart failure. J Cardiol 2016;68:100–3.54. Ferreira JP, Lam CSP, Anker SD, et al. PlasmaD-dimer concentrations predicting stroke risk andrivaroxaban benefit in patients with heart failureand sinus rhythm: an analysis from theCOMMANDER-HF trial. Eur J Heart Fail 2020 Sep21.55. Loh E, Sutton MS, Wun CC, et al. Ventriculardysfunction and the risk of stroke aftermyocardial infarction. N Engl J Med 1997;336:251–7.56. Lin AY, Dinatolo E, Metra M, Sbolli M, Dasseni N, Butler J, Greenberg BH. Thromboembolism in Heart Failure Patients in Sinus Rhythm: Epidemiology, Pathophysiology, Clinical Trials, and Future Direction. JACC Heart Fail. 2021 Apr;9(4):243-253.







