BS. NGUYỄN THANH HIỀN
BS. LÊ NGỌC CÁT TƯỜNG
Một số thuật ngữ viết tắt:
ACS: Hội chứng vành cấp; ASCVD: Bệnh tim mạch do xơ vữa; AF: Rung nhĩ; CHK: chống huyết khối; DAPT: Liệu pháp kháng kết tập tiểu cầu kép; DOACs: Thuốc kháng đông đường uống trực tiếp; ESC: Hiệp hội Tim mạch Châu Âu; HK: huyết khối; KĐ: kháng đông; INR: Tỷ lệ chuẩn hóa quốc tế; NSAIDs: Thuốc kháng viêm không steroid; OACs: Thuốc kháng đông đường uống; PCI: Can thiệp mạch vành qua da; PK/PD: Dược động học/dược lực học; PPIs: Thuốc ức chế bơm proton. RCT: thử nghiệm lâm sàng ngẫu nhiên có đối chứng; SAPT: Liệu pháp kháng kết tập tiểu cầu đơn; STEMI: Nhồi máu cơ tim cấp có ST chênh lên; TIMI Score: Thang điểm tiên lượng cho bệnh nhân mắc Hội chứng vành cấp; VTE: Thuyên tắc tĩnh mạch do huyết khối; XHTH: Xuất huyết đường tiêu hóa;
* GIỚI THIỆU
Việc cân bằng hiệu quả và độ an toàn của liệu pháp CHK là một vấn đề phức tạp, đặc biệt ở những bệnh nhân mắc đồng thời các bệnh lý tim mạch và đường tiêu hóa, do bệnh lý này có thể ảnh hưởng đến các đặc tính dược động học và/hoặc dược lực học (PK/PD) của thuốc hoặc làm thay đổi nguy cơ XHTH. Do đó, cần làm sáng tỏ về một số khía cạnh trong việc quản lý liệu pháp CHK ở nhóm bệnh nhân này. Thứ nhất, nhiều tình huống lâm sàng khác nhau, chẳng hạn như hội chứng kém hấp thu, phẫu thuật giảm cân, hội chứng ruột ngắn hoặc nuôi ăn qua ống thông, có thể ảnh hưởng đến sự hấp thu và sinh khả dụng của các thuốc CHK dùng đường uống. Thứ hai, việc sử dụng các thuốc CHK ở bệnh nhân có nguy cơ XHTH cao cần được xem xét kỹ lưỡng. Các biến cố chảy máu là một yếu tố tiên lượng quan trọng ở bệnh nhân mắc bệnh tim mạch, và đôi khi chúng có thể quan trọng tương đương với các biến cố HK. Việc xác định bệnh nhân có nguy cơ XHTH cao, điều chỉnh nguy cơ chảy máu bằng cách sử dụng các thuốc bảo vệ đường tiêu hóa, và chọn lựa phác đồ CHK phù hợp đóng vai trò cực kỳ quan trọng trong việc ngăn ngừa XHTH. Thứ ba, sau một đợt XHTH cấp tính, việc xác định thời gian gián đoạn liệu pháp CHK và phác đồ tái khởi động đòi hỏi phải cân nhắc kỹ lưỡng sự cân bằng giữa mức độ nghiêm trọng của chảy máu và nguy cơ các biến cố HK (1-8). Trong bài viết này, chúng tôi tóm tắt các bằng chứng về việc áp dụng liệu pháp CHK ở bệnh nhân mắc đồng thời các bệnh lý tim mạch và đường tiêu hóa.
1. ẢNH HƯỞNG CỦA BỆNH LÝ ĐƯỜNG TIÊU HÓA ĐẾN PK/PD
Một số tình trạng lâm sàng có thể ảnh hưởng đến PK/PD của các thuốc CHK (xem Hình 1). Những thay đổi phổ biến nhất bao gồm hoạt động của hệ tiêu hóa, pH dạ dày-ruột, diện tích bề mặt hấp thu của đường tiêu hóa (do bệnh lý hoặc phẫu thuật) và đường dùng thuốc. Đường uống có thể không phù hợp cho bệnh nhân có tình trạng rối loạn tri giác, những người bị buồn nôn hoặc nôn dữ dội, hoặc những người có vấn đề về nhu động đường tiêu hóa hay tắc ruột có thể cản trở việc thuốc được đưa đến đường ruột một cách hiệu quả. Việc lựa chọn đường dùng cũng phụ thuộc vào đặc tính PK/PD của thuốc (xem Hình 2) (9). Rất ít RCT đã so sánh PK/PD hoặc hiệu quả lâm sàng giữa đường uống và các đường dùng thay thế của thuốc CHK (hình 3) (10).
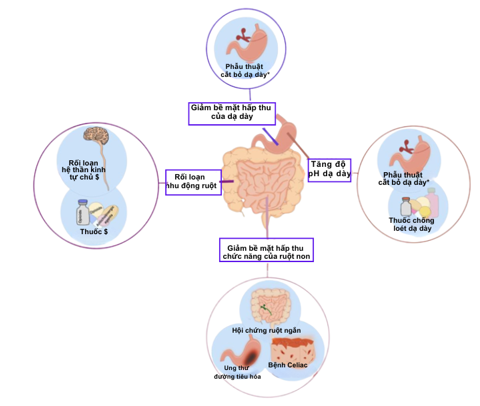
Hình 1. Các yếu tố làm thay đổi sự hấp thu thuốc CHK qua đường tiêu hóa. Các phẫu thuật cắt dạ dày có thể làm giảm sự hấp thu của thuốc CHK thông qua nhiều cơ chế, ngoài việc giảm diện tích hấp thu và tăng pH dạ dày, còn bao gồm tăng tốc độ làm rỗng dạ dày và sự trộn kém của dịch ruột với mật và các men tiêu hóa. †Tăng pH dạ dày có thể làm giảm sự hấp thu phụ thuộc pH của các thuốc kháng huyết khối. ‡Bệnh Parkinson, đa xơ cứng, xơ cứng bì, đái tháo đường, nhiễm HIV, suy giáp, cũng như một số thuốc, có thể làm tăng thời gian vận chuyển qua ống tiêu hóa và làm chậm thời gian đạt nồng độ đỉnh của các thuốc CHK (9)
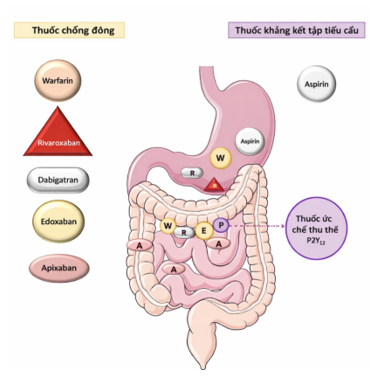
Hình 2. Vị trí hấp thu của các thuốc CHK. Nhóm thuốc KĐ: Warfarin được hấp thu ở dạ dày và đoạn gần ruột non, Rivaroxaban chủ yếu được hấp thu ở dạ dày, Dabigatran được hấp thu ở dạ dày và đoạn gần ruột non, Edoxaban được phân rã tại dạ dày và hấp thu ở ruột non, Apixaban được hấp thu ở ruột non và đại tràng lên. Nhóm thuốc kháng kết tập tiểu cầu: Aspirin chủ yếu được hấp thu ở dạ dày, Các thuốc ức chế P2Y₁₂ được hấp thu ở đoạn gần ruột non (9).
Đối với liệu pháp kháng tiểu cầu, aspirin không bao tan trong ruột có thể được nghiền nát và dùng qua ống thông dạ dày (hoặc dùng đường trực tràng dưới dạng thuốc đạn) với liều lượng và hiệu quả dự kiến tương tự như khi dùng đường uống. Aspirin dạng tiêm tĩnh mạch hiện có ở các nước châu Âu dành cho bệnh nhân mắc ACS không thể dùng thuốc bằng đường uống. Đối với các thuốc ức chế P2Y12, dữ liệu dược động học từ những người tình nguyện khỏe mạnh cho thấy clopidogrel có thể được nghiền nát và dùng qua ống thông dạ dày, mang lại thời gian khởi phát tác dụng nhanh hơn và sinh khả dụng cao hơn so với viên nguyên vẹn. Ở những bệnh nhân không thể dùng liệu pháp kháng tiểu cầu bằng đường uống, cangrelor đường tiêm tĩnh mạch đã được sử dụng thành công.
Đối với các thuốc OACs, các thuốc đối kháng vitamin K có thể được dùng qua đường nuôi ăn qua ống thông. Tuy nhiên, sinh khả dụng có thể khó dự đoán do khả năng thuốc đối kháng vitamin K bám vào thành ống thông, điều này đòi hỏi phải theo dõi chặt chẽ chỉ số INR. Đối với các thuốc DOACs, viên nang dabigatran không nên bẻ hoặc nghiền nát vì công thức thuốc có một lớp bao phủ lên lõi axit tartaric để tạo thành các hạt nhỏ nhằm giảm sự thay đổi trong hấp thu. Apixaban, edoxaban và rivaroxaban có thể được nghiền nát và pha trong 60ml nước (hoặc nước ép táo hoặc sốt táo) (10).
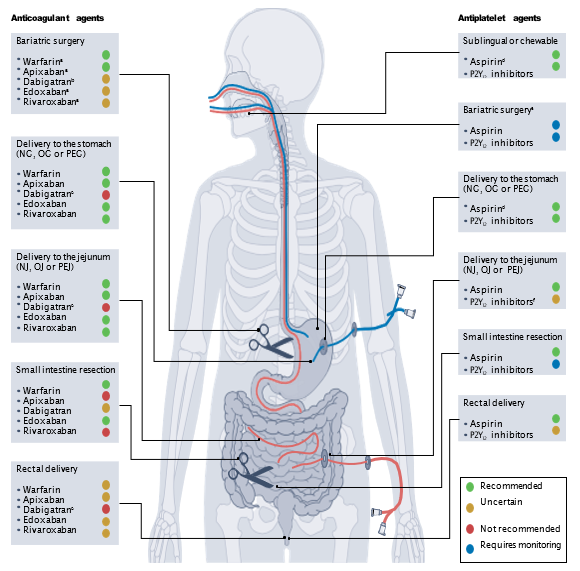
Hình 3. Dược động học và Dược lực học của Thuốc CHK ở Bệnh nhân có Rối loạn Tiêu hóa Các thuốc CHK có thể được nghiền nát và sử dụng qua ống thông ở những bệnh nhân không thể dùng thuốc theo đường uống thông thường. aNăm 2021, Hiệp hội Huyết khối và Cầm máu Quốc tế[66] đã đề xuất không sử dụng thuốc DOACs để điều trị hoặc dự phòng thuyên tắc huyết khối tĩnh mạch trong giai đoạn cấp tính sau phẫu thuật giảm cân, và đề xuất chuyển các thuốc đường tiêm sang thuốc kháng vitamin K. Họ khuyên rằng DOACs có thể được xem xét sau ít nhất 4 tuần điều trị bằng đường tiêm, với việc theo dõi nồng độ DOAC đáy để xác định sự hấp thu. Tuy nhiên, dựa trên bằng chứng gần đây còn hạn chế hơn, ảnh hưởng của phẫu thuật cắt dạ dày hình ống và nối tắt dạ dày hình chữ Y lên dược động học và dược lực học của apixaban được cho là khá nhỏ và rất có thể không có ý nghĩa lâm sàng. bVì dabigatran được hấp thu chủ yếu ở dạ dày và tá tràng, sự hấp thu có thể bị giảm sau phẫu thuật giảm cân. cViên nang dabigatran không được bẻ hoặc nghiền nát. dCác công thức aspirin không bọc ruột. eSau phẫu thuật giảm cân, sự hấp thu của aspirin và thuốc ức chế thụ thể P2Y12 có thể tăng lên, cần phải theo dõi chảy máu. fVì thuốc ức chế P2Y12 được hấp thu chủ yếu ở đoạn gần ruột non, sự hấp thu của chúng có thể bị giảm khi đưa thuốc vào các phần xa của ruột non. NG, đặt ống thông dạ dày qua mũi; NJ, đặt ống thông hỗng tràng qua mũi; OG, đặt ống thông dạ dày qua miệng; OJ, đặt ống thông hỗng tràng qua miệng; PEG, mở thông dạ dày qua da bằng nội soi; PEJ, mở thông hỗng tràng qua da bằng nội soi hoặc qua ống thông (10).
1.1 Rối loạn nhu động ruột do opioid
Các loại thuốc giảm đau opioid, bao gồm cả morphine (với liều thấp tới 5mg) và fentanyl, có thể làm chậm quá trình làm rỗng dạ dày và giảm nhu động ruột. Điều này dẫn đến việc làm chậm hấp thu thuốc ức chế P2Y12 và làm giảm đáp ứng chống kết tập tiểu cầu (11). Dựa trên dữ liệu hạn chế hiện có, Hiệp hội Tim mạch Canada không khuyến khích việc sử dụng opioid một cách thường quy ở bệnh nhân STEMI. Tuy nhiên, ESC chỉ ra rằng không có sự gia tăng rõ rệt về nguy cơ các kết quả lâm sàng bất lợi do bất kỳ tương tác nào giữa morphine và thuốc chống kết tập tiểu cầu trong bối cảnh hội chứng vành cấp (12,13).
1.2 Hấp Thu Thuốc Sau Phẫu Thuật Cắt Bỏ Đường Tiêu Hóa
Phẫu thuật cắt bỏ đường tiêu hóa có thể tác động đáng kể đến cách cơ thể hấp thu thuốc CHK. Việc hiểu rõ những thay đổi này là rất quan trọng để đảm bảo thuốc phát huy hiệu quả và an toàn tối đa cho bệnh nhân. Aspirin dường như không bị ảnh hưởng nhiều về mặt hấp thu ở bệnh nhân đã cắt dạ dày hoặc mắc hội chứng ruột ngắn. Các thuốc ức chế P2Y12 chủ yếu được hấp thu ở đoạn gần ruột non. Do đó, các thủ thuật hay phẫu thuật liên quan đến vùng này, hoặc tình trạng hội chứng ruột ngắn, có thể làm giảm sự hấp thu của chúng. Đối với những bệnh nhân có nguy cơ huyết khối cao nên theo dõi chức năng tiểu cầu cho đến khi có thêm dữ liệu (14).
VKAs được hấp thu ở dạ dày và đoạn gần ruột non. Tuy nhiên, hệ vi sinh vật đường ruột có thể ảnh hưởng đến quá trình tổng hợp và hấp thu vitamin K, từ đó tác động đến đáp ứng của cơ thể với VKAs. Trong hội chứng ruột ngắn, bệnh nhân có thể gặp tình trạng đáp ứng kém hoặc đáp ứng quá mức với VKAs. Điều này đòi hỏi phải theo dõi chặt chẽ INR. Phẫu thuật cắt đại tràng dường như không ảnh hưởng đến sinh khả dụng của VKAs (15,16).
Sinh khả dụng của DOACs phụ thuộc vào vị trí hấp thu cụ thể của từng loại thuốc, cũng như sự hiện diện và phân bố của enzyme cytochrome P450 3A4 (CYP3A4) trong ruột, đặc biệt là ở hồi tràng. CYP3A4 rất quan trọng đối với quá trình chuyển hóa của apixaban và rivaroxaban, nhưng ít quan trọng hơn đối với edoxaban. Tương tự, P-glycoprotein 1 (P-gp 1) ở hồi tràng và đại tràng đóng vai trò quan trọng trong việc thải trừ dabigatran và edoxaban, nhưng ít tác động hơn đến apixaban và rivaroxaban. Dabigatran chủ yếu hấp thu ở dạ dày và tá tràng. Sự hấp thu của nó bị suy giảm sau phẫu thuật cắt dạ dày hoặc trong hội chứng ruột ngắn, nhưng không bị ảnh hưởng sau phẫu thuật cắt đại tràng. Rivaroxaban có thể bị ảnh hưởng hấp thu sau phẫu thuật cắt dạ dày, nhưng không bị ảnh hưởng bởi các phẫu thuật cắt bỏ ruột non hoặc cắt đại tràng. Apixaban hấp thu chủ yếu ở ruột non và đoạn gần ruột già. Do đó, việc cắt bỏ ruột non (nhưng không phải cắt dạ dày) có thể làm cho sinh khả dụng trở nên khó dự đoán. Edoxaban có độ hòa tan phụ thuộc vào pH và phân rã trong dạ dày. Do đó, hấp thu edoxaban có thể giảm sau phẫu thuật cắt dạ dày hoặc phẫu thuật nối tắt dạ dày, nhưng không bị giảm sau phẫu thuật cắt bỏ ruột đoạn xa hoặc cắt đại tràng (xem Hình 3) (10).
1.3 Phẫu thuật giảm cân (Bariatric surgery)
Phẫu thuật cắt dạ dày hình ống (Sleeve gastrectomy) và nối tắt dạ dày hình chữ Y chiếm >90% các ca phẫu thuật giảm cân hiện đại. Trong phẫu thuật cắt dạ dày hình ống, gần 80% dạ dày được cắt bỏ mà không chuyển hướng đường tiêu hóa. Trong phẫu thuật nối tắt dạ dày hình chữ Y, phần lớn dạ dày đoạn giữa – cuối, toàn bộ tá tràng và đoạn gần hỗng tràng sẽ không tiếp xúc với thức ăn và thuốc. Trong khi cả hai phẫu thuật đều làm giảm bề mặt hấp thu trong lòng dạ dày, đoạn gần ruột non còn bị cắt bỏ thêm sau phẫu thuật nối tắt dạ dày hình chữ Y. Những thay đổi này có thể ảnh hưởng đến PK/PD của các thuốc CHK (17-21). Béo phì có thể liên quan đến việc giảm tác dụng của aspirin, và phẫu thuật có thể khôi phục hoàn toàn sự ức chế tiểu cầu . Giai đoạn sớm, sau phẫu thuật cắt dạ dày hình ống hoặc nối tắt dạ dày hình chữ Y, sự hấp thu và đáp ứng với aspirin có thể tăng lên Việc liệu sự gia tăng đáp ứng aspirin này có chuyển thành nguy cơ chảy máu quá mức trong giai đoạn sớm sau phẫu thuật hay không đòi hỏi phải nghiên cứu thêm. Chảy máu quá mức tiềm ẩn đã được báo cáo với các thuốc ức chế P2Y12 sau phẫu thuật nối tắt dạ dày hình chữ Y (22,23). Cần có thêm các nghiên cứu để hiểu rõ lý do của việc tăng nguy cơ chảy máu này.
Đối với bệnh nhân đang dùng warfarin, cần kiểm tra INR thường xuyên hơn trong 3 tháng đầu. Chỉ một vài nghiên cứu nhỏ đã xem xét PK/PD của DOACs sau phẫu thuật giảm cân. Một nghiên cứu đã báo cáo những thay đổi lớn về sinh khả dụng của dabigatran, edoxaban và rivaroxaban sau phẫu thuật giảm cân, và đề xuất theo dõi nồng độ thuốc sau phẫu thuật. Một tổng quan hệ thống đã nhấn mạnh sự thiếu hụt dữ liệu về việc sử dụng DOACs ở bệnh nhân sau phẫu thuật giảm cân. Dựa trên bằng chứng hạn chế hiện có, tác dụng của phẫu thuật cắt dạ dày hình ống hoặc nối tắt dạ dày hình chữ Y lên PK/PD của apixaban có lẽ không có ý nghĩa lâm sàng. Mặc dù Hiệp hội Huyết khối và Cầm máu Quốc tế đã khuyến cáo không sử dụng DOACs trong 4 tuần đầu sau phẫu thuật nối tắt dạ dày hình chữ Y. Việc kiểm tra nồng độ anti-factor Xa trong huyết tương ở những bệnh nhân này để phát hiện nồng độ thuốc kháng đông thấp có thể cần thiết. Ở những bệnh nhân nằm trong ngưỡng dưới điều trị mặc dù dùng DOAC thường xuyên, việc chuyển sang một tác nhân thay thế (như heparin trọng lượng phân tử thấp) để quản lý ngắn hạn có thể là hợp lý (10,24).
2. CHIẾN LƯỢC BẢO VỆ ĐƯỜNG TIÊU HÓA
2.1 Nguy cơ XHTH khi sử dụng liệu pháp CHK
Việc tăng liều hoặc tăng cường độ của liệu pháp CHK hoặc sử dụng liệu pháp CHK kết hợp sẽ làm tăng nguy cơ XHTH. Nguy cơ XHTH cũng bị ảnh hưởng bởi việc sử dụng đồng thời các thuốc NSAIDs hoặc corticosteroid. Những bệnh nhân có nguy cơ cao bị XHTH thường bị loại khỏi hầu hết các thử nghiệm về liệu pháp kháng đông. Do đó, phần lớn kiến thức của chúng ta đến từ các nghiên cứu quan sát (25,26).
Trong một phân tích tổng hợp các thử nghiệm ngẫu nhiên có đối chứng ở những bệnh nhân được điều trị bằng aspirin (75–325 mg mỗi ngày) so với nhóm giả dược, nguy cơ XHTH nặng tăng khi sử dụng aspirin (OR 1,55, 95% CI 1,27–1,90). Nguy cơ XHTH với aspirin dường như có liên quan đến liều lượng. Một thử nghiệm lâm sàng ngẫu nhiên khác trên bệnh nhân hội chứng vành cấp cho thấy những bệnh nhân dùng aspirin 300–325 mg/ngày có sự gia tăng nhỏ nhưng có ý nghĩa về XHTH nặng trong 30 ngày theo dõi so với những bệnh nhân dùng aspirin 75–100 mg/ngày (0.4% so với 0.2%; P = 0.04). Nguy cơ XHTH tăng lên đáng kể hơn nữa khi aspirin được kết hợp với clopidogrel, so với đơn trị liệu aspirin (OR 1.86, 95% CI 1.49–2.31) (27).
Khoảng một nửa số biến cố chảy máu nặng liên quan đến liệu pháp OAC xuất phát từ đường tiêu hóa. Tỷ lệ XHTH nặng trong các RCT của OAC để điều trị thuyên tắc huyết khối tĩnh mạch hoặc để phòng ngừa đột quỵ ở bệnh nhân AF lần lượt là 0.5–1.6 và 0.8–1.9 biến cố trên 100 bệnh nhân-năm. Chúng ta cần phân tầng nguy cơ XHTH cho mọi bệnh nhân sử thuốc CHK. Các RCT ở bệnh nhân AF cho thấy, so với warfarin, tỷ lệ XHTH cao hơn ở dabigatran 150 mg hai lần mỗi ngày (1.9 so với 1.3 biến cố trên 100 bệnh nhân-năm), edoxaban 60 mg mỗi ngày (1.5 so với 1.3 biến cố trên 100 bệnh nhân-năm) và rivaroxaban (2.0 so với 1.2 biến cố trên 100 bệnh nhân-năm) nhưng thấp hơn với apixaban (0.8 so với 0.9 biến cố trên 100 bệnh nhân-năm) (28,29).
2.2 Phân tầng nguy cơ XHTH
Các thang điểm khác nhau để ước đoán nguy cơ chảy máu nặng (như PRECISE-DAPT và định nghĩa của ARC-HBR đã được sử dụng ở bệnh nhân dùng thuốc kháng tiểu cầu. Tuy nhiên, các mô hình này không đặc biệt ước đoán nguy cơ XHTH. Thang điểm (ABC) 2D (tuổi >65, tiền sử thiếu máu, chảy máu nặng gần đây, tiền sử XHTH, sử dụng thuốc PPI, sử dụng kết hợp OACs và liệu pháp DAPT) đã được phát triển như một thang điểm nguy cơ để dự đoán XHTH ở bệnh nhân dùng thuốc kháng tiểu cầu (xem Hình 4) (9,10).

Hình 4. Thang điểm (ABC) 2D đánh giá nguy cơ xuất huyết tiêu hóa
(a) Thiếu máu: được định nghĩa là nồng độ hemoglobin < 13 g/dL ở nam hoặc < 12 g/dL ở nữ. (b) Chảy máu nặng gần đây: chảy máu nặng xảy ra trong vòng < 30 ngày trước khi sử dụng thuốc kháng kết tập tiểu cầu.
Hiện tại, chúng ta chưa tìm thấy một mô hình cụ thể nào để đánh giá nguy cơ XHTH ở bệnh nhân dùng thuốc OACs để điều trị AF. Điều đáng chú ý là các biến cố chảy máu có thể có các yếu tố dự đoán khác nhau tùy thuộc vào vị trí chảy máu. Đối với bệnh nhân bị VTE, các nhà nghiên cứu của RIETE đã xác định các yếu tố nguy cơ sau cho XHTH nặng: giới tính nam, tuổi ≥ 70, khởi phát VTE ban đầu là thuyên tắc phổi, ung thư đang hoạt động, tiền sử VTE, chảy máu tiêu hóa gần đây, giãn tĩnh mạch thực quản, thiếu máu, thời gian prothrombin bất thường, suy thận, sử dụng corticosteroid là yếu tố nguy cơ đáng kể gây XHTH. Tỷ lệ XHTH nặng ở những người có nguy cơ thấp là 0.2%, trong khi ở những người có nguy cơ cao là 6.1%. Tuy nhiên, mô hình này vẫn cần được đồng thuận từ các nghiên cứu độc lập bên ngoài (30).
2.3 Liệu pháp bảo vệ đường tiêu hóa bằng thuốc (bảng 1)
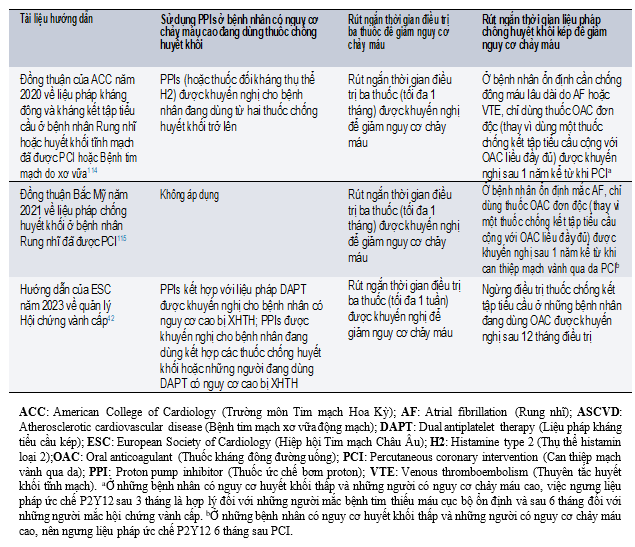
Trong một phân tích tổng hợp các RCT ở bệnh nhân dùng aspirin (<325 mg mỗi ngày), việc sử dụng PPI có liên quan đến việc giảm nguy cơ XHTH so với nhóm đối chứng (OR 0.27, KTC 95% 0.16–0.43). Trong thử nghiệm COGENT RCT86 trên 3.873 bệnh nhân mắc ACS hoặc trải qua PCI và được điều trị bằng DAPT nền clopidogrel, sự kết hợp của clopidogrel (75 mg) và omeprazole (20 mg) so với chỉ dùng clopidogrel đã giảm đáng kể tỷ lệ biến cố tiêu hóa trong 180 ngày — bao gồm chảy máu rõ rệt hoặc tiềm ẩn và loét hoặc xói mòn dạ dày tá tràng có triệu chứng, tắc nghẽn hoặc thủng (HR 0.34, KTC 95% 0.18–0.63, P < 0.001). Mặc dù có tương tác giữa omeprazole và clopidogrel, dẫn đến việc chuyển đổi clopidogrel thành chất chuyển hóa giảm hoạt tính, không quan sát thấy sự gia tăng có ý nghĩa lâm sàng nào về các biến cố thiếu máu cục bộ. Trong một RCT riêng biệt trên bệnh nhân dùng DAPT, esomeprazole 40 mg mỗi ngày có liên quan đến tỷ lệ XHTH thấp hơn famotidine 20 mg mỗi ngày (HR 0.095, KTC 95% 0.005–0.504). Các hướng dẫn của Trường môn Tim mạch Hoa Kỳ/Hiệp hội Tim mạch Hoa Kỳ khuyến cáo sử dụng PPI ở những bệnh nhân dùng DAPT có nguy cơ XHTH, bao gồm những người đang dùng OAC, người cao tuổi, giới tính nữ, cân nặng thấp, bệnh thận mạn tính, đái tháo đường, thiếu máu hoặc đang dùng NSAID. Tương tự, các hướng dẫn của ESC khuyến cáo sử dụng PPI với DAPT ở những bệnh nhân có nguy cơ XHTH cao (được định nghĩa là những người có tiền sử loét hoặc xuất huyết tiêu hóa, sử dụng kháng đông, sử dụng NSAID hoặc corticosteroid mạn tính) hoặc có từ hai yếu tố nguy cơ trở lên trong số: tuổi ≥ 65, khó tiêu, bệnh trào ngược dạ dày thực quản, nhiễm Helicobacter pylori hoặc nghiện rượu. Thử nghiệm COMPASS đã so sánh vai trò của pantoprazole (40 mg mỗi ngày) so với giả dược ở những bệnh nhân không bị loại trừ vì có nguy cơ chảy máu cao và đang dùng aspirin liều thấp cùng rivaroxaban 2.5 mg hai lần mỗi ngày hoặc đơn trị liệu aspirin. Kết cục chính là thời gian đến khi xuất hiện biến cố đường tiêu hóa trên đầu tiên, được định nghĩa là một tổng hợp các triệu chứng chảy máu rõ ràng, XHTH trên, chảy máu ẩn, loét hoặc xói mòn dạ dày tá tràng có triệu chứng, hoặc tắc nghẽn hoặc thủng đường tiêu hóa trên. Việc sử dụng pantoprazole không làm giảm đáng kể nguy cơ biến cố đường tiêu hóa trên (kết cục chính) so với giả dược (HR 0.88, KTC 95% 0.67–1.15) nhưng có liên quan đến việc giảm nguy cơ chảy máu rõ ràng được xác nhận có nguồn gốc từ dạ dày tá tràng (HR 0.52, KTC 95% 0.28–0.94, P = 0.03). Trong hướng dẫn của ESC năm 2023, việc sử dụng omeprazole hoặc esomeprazole không được khuyến cáo ở những người đang dùng clopidogrel. Ở bệnh nhân đang dùng ticagrelor hoặc prasugrel, việc sử dụng PPI không liên quan đến các kết cục tim mạch bất lợi vì quá trình chuyển hóa của các thuốc này không phụ thuộc vào CYP2C19 (31-33).
Bảng 1. Khuyến cáo về các chiến lược bảo vệ đường tiêu hóa ở bệnh nhân đang dùng thuốc kháng đông
2.4 Giảm nguy cơ XHTH bằng các thủ thuật tim mạch
Các chiến lược sử dụng thiết bị để rút ngắn thời gian điều trị kháng đông ở bệnh nhân AF bao gồm các thiết bị bít hoặc loại bỏ túi thừa nhĩ trái. Các thiết bị này đã được chứng minh trong một số RCT là không thua kém liệu pháp chống đông trong việc giảm tỷ lệ đột quỵ và thuyên tắc hệ thống. Bít túi thừa nhĩ trái qua da cho phép giảm liều hoặc ngừng liệu pháp kháng đông, từ đó làm giảm các biến cố chảy máu.
Thiết kế stent mạch vành với polymer tương thích sinh học hoặc stent không polymer là một trong những chiến lược để cho phép rút ngắn thời gian và/hoặc cường độ của liệu pháp chống tiểu cầu, từ đó giảm nguy cơ chảy máu. Sự phân hủy của polymer, vốn được cho là gây viêm nội mạc và hỏng stent, có thể cho phép rút ngắn thời gian DAPT sau đặt stent một cách an toàn.
Việc đặt lưới lọc tĩnh mạch chủ dưới nhằm giảm nguy cơ thuyên tắc phổi tái phát và được chỉ định ở những bệnh nhân có huyết khối tĩnh mạch sâu chi dưới đoạn gần hoặc thuyên tắc phổi cấp tính có chống chỉ định tuyệt đối với liệu pháp kháng đông. Một đánh giá hệ thống của sáu RCT và năm nghiên cứu quan sát tiền cứu kiểm tra các chỉ định khác nhau cho việc đặt lưới lọc tĩnh mạch chủ dưới không tìm thấy sự khác biệt đáng kể về các biến cố chảy máu nghiêm trọng giữa những bệnh nhân được điều trị và không được điều trị bằng lưới lọc tĩnh mạch chủ dưới (OR 0,90, 95% CI 0,58–1,38). Những phát hiện này đã được đồng thuận trong một phân tích cập nhật bao gồm 13 nghiên cứu (10,34-38).
2.5 Xuống thang phác đồ chống HK
Việc lựa chọn phác đồ CHK tốt nhất cho bệnh nhân cần OAC cùng với một hoặc hai thuốc kháng tiểu cầu là một thách thức. Liệu pháp ba loại CHK (triple antithrombotic therapy) ở bệnh nhân AF hoặc VTE đã mắc ACS gần đây hoặc đang trải qua PCI có liên quan đến tăng nguy cơ chảy máu. Các RCT cho thấy rằng, sau một thời gian tối thiểu của liệu pháp ba loại CHK (thường là 1 tuần đến 1 tháng), việc giảm cường độ xuống một thuốc KĐ cộng với một thuốc ức chế P2Y12 (thường là clopidogrel) có liên quan đến nguy cơ chảy máu thấp hơn, so với tiếp tục liệu pháp ba thuốc CHK, mà không có sự khác biệt đáng kể về các biến cố thiếu máu cục bộ. Những dữ liệu này đã được đưa vào một số hướng dẫn lâm sàng (Bảng 1,2). Liệu pháp 2 thuốc CHK cũng nên được kê đơn trong một khoảng thời gian giới hạn, nếu có thể. Việc liệu pháp kháng tiểu cầu có nên tiếp tục ở bệnh nhân đang dùng thuốc KĐ dài hạn hay không nên được tham khảo bởi các chuyên gia về HK. Bằng chứng cho thấy nhiều bệnh nhân đang dùng thuốc KĐ có thể ngừng liệu pháp kháng tiểu cầu một cách an toàn. Ở bệnh nhân AF và ASCVD ổn định (không ACS hoặc PCI trong một năm gần đây), đơn trị liệu KĐ có liên quan đến nguy cơ chảy máu tổng thể thấp hơn so với một thuốc KĐ cộng với một thuốc kháng tiểu cầu, mà không quan sát thấy sự gia tăng nguy cơ các biến cố thiếu máu cục bộ. Trong AFIRERCT, bệnh nhân AF và ASCVD ổn định (bao gồm cả những người đã trải qua PCI >1 năm trước đó) được phân ngẫu nhiên để nhận rivaroxaban hoặc rivaroxaban cộng với đơn trị liệu kháng tiểu cầu. Đơn trị liệu rivaroxaban không kém hơn liệu pháp kết hợp về hiệu quả (một tổng hợp đột quỵ, thuyên tắc hệ thống, nhồi máu cơ tim, đau thắt ngực không ổn định cần tái thông mạch hoặc tử vong do mọi nguyên nhân) (HR 0.72, KTC 95% 0.55–0.95, P < 0.001 cho không kém hơn) và vượt trội về an toàn (chảy máu nặng) (HR 0.59, KTC 95%, 0.39–0.89, P = 0.01) (10, 39,40).
Bảng 2. Các khuyến nghị về việc ngừng và tiếp tục sử dụng các thuốc chống huyết khối ở BN bị xuất huyết tiêu hóa cấp tính
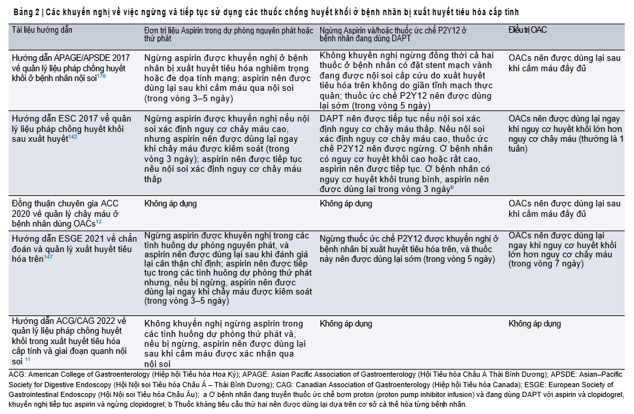
3. ÁP DỤNG THỰC HÀNH SỬ DỤNG THUỐC CHK Ở BỆNH NHÂN BỆNH ĐƯỜNG TIÊU HÓA
3.1. Bệnh nhân có nguy cơ cao bị XHTH (hình 5)
3.1.1 Liệu pháp kháng tiểu cầu
Trong thử nghiệm CAPRIE với bệnh nhân có nguy cơ biến cố thiếu máu cục bộ, nguy cơ XHTH trên cao hơn khi dùng aspirin 325 mg/ngày so với clopidogrel 75 mg/ngày (2,7% so với 2,0%; P = 0,05), tương tự, tỷ lệ nhập viện do XHTH cũng cao hơn (1,1% so với 0,7%; P = 0,012). Trong một phân tích tổng hợp của 22 RCT về phòng ngừa tiên phát và thứ phát bệnh tim mạch, aspirin (75–325 mg mỗi ngày) làm tăng nguy cơ XHTH so với giả dược (RR 2,07, 95% CI 1,61–2,66). Trong một phân tích tổng hợp của các RCT ở bệnh nhân có bệnh động mạch vành xác định, đơn trị liệu với chất ức chế P2Y12 (ticagrelor 90 mg hai lần mỗi ngày hoặc clopidogrel 75 mg mỗi ngày) có liên quan đến nguy cơ XHTH bất kỳ thấp hơn (HR 0,75, 95% CI 0,57–0,97, P = 0,027) và các biến cố thiếu máu cục bộ thấp hơn (HR 0,88, 95% CI 0,79–0,97, P = 0,012) so với đơn trị liệu aspirin (75–325 mg/ngày). Nguy cơ XHTH thấp hơn có thể chủ yếu do clopidogrel, dựa trên kết quả của các thử nghiệm quan trọng. Trong một phân tích dưới nhóm các RCT ở bệnh nhân sử dụng các thuốc ức chế P2Y₁₂ thế hệ thứ ba (bao gồm cả các thử nghiệm dùng đơn trị hoặc phối hợp DAPT với aspirin), nguy cơ XHTH cao hơn ở nhóm dùng prasugrel (RR 1,40; KTC 95%: 1,10–1,77) so với nhóm dùng ticagrelor (RR 1,15; KTC 95%: 0,94–1,39), khi mỗi thuốc được so sánh với clopidogrel. Mặc dù bằng chứng còn hạn chế, các dữ liệu hiện có cho thấy clopidogrel có thể liên quan đến nguy cơ XHTH thấp hơn so với aspirin hoặc prasugrel ở bệnh nhân có nguy cơ thiếu máu cục bộ ổn định. Mặc dù clopidogrel có thể liên quan đến số biến cố XHTH ít hơn so với ticagrelor, nhưng các dữ liệu hiện có chưa đủ thuyết phục, và trong một nghiên cứu còn ghi nhận mối lo ngại về tỷ lệ tử vong sau biến cố cao hơn ở nhóm dùng clopidogrel so với ticagrelor. Do đó, hiện chưa thể đưa ra kết luận về sự so sánh giữa hai thuốc này. Phân tích từ dự án hợp tác PANTHER— một phân tích gộp ở mức độ bệnh nhân từ các thử nghiệm ngẫu nhiên có đối chứng (RCTs) so sánh đơn trị liệu thuốc ức chế P2Y₁₂ với đơn trị liệu aspirin trong phòng ngừa các biến cố tim mạch ở bệnh nhân đã có bệnh động mạch vành cho thấy, đơn trị liệu bằng thuốc ức chế P2Y₁₂ có liên quan đến nguy cơ thấp hơn về tử vong tim mạch, nhồi máu cơ tim và đột quỵ so với đơn trị liệu aspirin ở bệnh nhân bệnh động mạch vành (CAD), chủ yếu nhờ giảm nguy cơ nhồi máu cơ tim, từ đó dẫn đến giảm nguy cơ biến cố tim mạch bất lợi thuần (NACE). Tỷ lệ xuất huyết nặng tương đương nhau giữa hai nhóm, tuy nhiên XHTH và đột quỵ xuất huyết thấp hơn ở nhóm đơn trị liệu P2Y₁₂. Dựa trên các bằng chứng ngẫu nhiên hiện có, đơn trị liệu P2Y₁₂ dài hạn có thể được ưu tiên thay thế cho đơn trị liệu aspirin dài hạn trong phòng ngừa thứ phát ở bệnh nhân CAD (5,10,41-44).
3.1.2 Liệu pháp kháng đông (KĐ)
Hiện nay, có rất ít nghiên cứu chất lượng cao về việc sử dụng thuốc KĐ ở những bệnh nhân có nguy cơ cao bị XHTH nhưng chưa có biến cố XHTH gần đây. Ở bệnh nhân AF, dựa trên kết quả của các thử nghiệm quan trọng, edoxaban 60 mg/ngày (HR 1,23, 95% CI 1,02–1,50, P = 0,03), dabigatran 150 mg hai lần/ngày (HR 1,50, 95% CI 1,19–1,89, P < 0,001) và rivaroxaban 20 mg/ngày (HR 1,42, 95% CI 1,22–1,66, P < 0,001) có liên quan đến nguy cơ XHTH cao hơn so với warfarin. Ngược lại, edoxaban 30 mg mỗi ngày có liên quan đến nguy cơ XHTH thấp hơn so với warfarin (HR 0,67, 95% CI 0,57–0,83, P < 0,001), trong khi nguy cơ XHTH với dabigatran 110 mg hai lần mỗi ngày không khác biệt đáng kể so với warfarin (HR 1,10, 95% CI 0,86–1,41, P = 0,43). Apxaban liều điều trị (5mg 2 lần/ngày) có tỉ lệ XHTH thấp nhất. Ở bệnh nhân VTE, các biến cố XHTH xảy ra thường xuyên hơn với dabigatran so với warfarin (4,2% so với 2,8% trong thử nghiệm RE-COVER I RCT và 3,7% so với 2,6% trong thử nghiệm RE-COVER II RCT), trong khi các biến cố XHTH ít gặp hơn với apixaban so với warfarin (0,3% so với 0,7% trong thử nghiệm AMPLIFY. Ở bệnh nhân ung thư và VTE, các biến cố XHTH có số lượng cao hơn (nhưng không có ý nghĩa thống kê) với rivaroxaban so với dalteparin (4,4% so với 1,5% trong thử nghiệm SELECT-D RCT và với edoxaban so với dalteparin (3,8% so với 1,1% trong thử nghiệm Hokusai VTE Cancer RCT. Số lượng biến cố XHTH không khác biệt đáng kể giữa bệnh nhân dùng apixaban và những người dùng dalteparin (1,9% so với 1,7%) (10, 45).
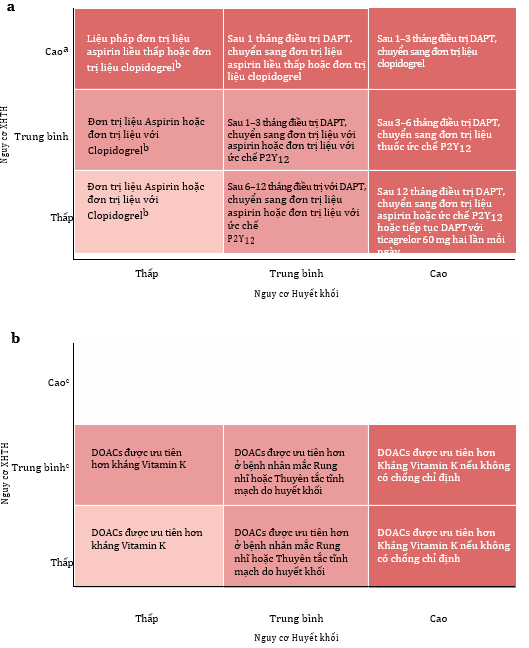
Hình 5. Quản lý các thuốc CHK ở bệnh nhân có nguy cơ XHTH. Việc quản lý các thuốc CHK ở mỗi bệnh nhân phải được cá thể hóa, và phần tóm tắt trong hình này chỉ mang tính hướng dẫn chung. Bệnh nhân có nguy cơ XHTH cao bao gồm những người có ung thư đường tiêu hóa trong lòng ruột. Bệnh nhân có nguy cơ XHTH trung bình bao gồm những người có tiền sử bệnh loét dạ dày tá tràng và những người đang sử dụng NSAID. Bệnh nhân có nguy cơ XHTH thấp bao gồm những người có tiền sử bệnh trĩ chảy máu. a, Bệnh nhân có nguy cơ HK cần liệu pháp kháng tiểu cầu. Bệnh nhân có nguy cơ HK thấp bao gồm những người đang dùng liệu pháp kháng tiểu cầu để dự phòng tiên phát hoặc có ASCVD không triệu chứng mà không có các đặc điểm nguy cơ cao. Bệnh nhân có nguy cơ HK trung bình bao gồm những người mắc ASCVD không có ACS hoặc PCI gần đây và có các đặc điểm nguy cơ cao, những người đã trải qua PCI và những người được quản lý y tế đối với ACS không ST chênh lên. Bệnh nhân có nguy cơ HK cao bao gồm những người bị STEMI, đột quỵ thiếu máu cục bộ, HK trong stent hoặc PCI trong ACS. b, Bệnh nhân có nguy cơ HK cần liệu pháp kháng đông. Bệnh nhân có nguy cơ HK thấp bao gồm những người mắc AF (với điểm CHA2DS2-VASc từ 2–4), huyết khối tĩnh mạch sâu chi đoạn xa đơn độc, thuyên tắc phổi nhánh nhỏ, hoặc thuyên tắc huyết khối tĩnh mạch xảy ra hơn 3 tháng trước. Bệnh nhân có nguy cơ HK trung bình bao gồm những người bị PE nguy cơ trung bình–thấp, và những người có van cơ học không ở vị trí hai lá, AF nguy cơ cao, hoặc VTE từ 1–3 tháng trước. Bệnh nhân có nguy cơ HK cao bao gồm những người bị PE nguy cơ cao gần đây hoặc những người bị PE nguy cơ trung bình–cao, hoặc những người có van hai lá cơ học, hội chứng kháng phospholipid HK, hoặc VTE trong tháng trước. aỞ bệnh nhân có nguy cơ XHTH cao, clopidogrel là thuốc ức chế P2Y12 được lựa chọn. bClopidogrel có liên quan đến nguy cơ chảy máu thấp hơn aspirin. cBít tiểu nhĩ trái có thể được xem xét ở bệnh nhân AF. dDabigatran 110 mg hai lần mỗi ngày có thể là một lựa chọn ở bệnh nhân AF (theo Cơ quan Dược phẩm Châu Âu), và rivaroxaban 15 mg mỗi ngày cũng có thể là một lựa chọn ở bệnh nhân AF cần thuốc kháng tiểu cầu.
4. Bệnh nhân có XHTH đang hoạt động
Bất chấp nguy cơ HK cơ bản ở bệnh nhân mắc bệnh tim mạch, liệu pháp CHK thường được tạm dừng trong các giai đoạn có XHTH lâm sàng đáng kể. Tùy thuộc vào bối cảnh lâm sàng, các tác nhân đảo ngược có thể được xem xét nếu có chỉ định (Bảng 2).
4.1 Liệu pháp kháng tiểu cầu
Một số hướng dẫn khuyến cáo tiếp tục liệu pháp aspirin để phòng ngừa thứ phát vào cùng ngày nếu cầm máu được xác nhận qua nội soi, trong khi có thể tiếp tục trì hoãn ở những bệnh nhân dùng thuốc kháng tiểu cầu khác để phòng ngừa tiên phát. Ngay cả khi aspirin được sử dụng để phòng ngừa thứ phát, cần cân nhắc sự cân bằng giữa nguy cơ HK và nguy cơ tái phát chảy máu. Sau khi nhập viện vì xuất huyết túi thừa, việc tiếp tục aspirin để phòng ngừa thứ phát cũng được khuyến cáo sau khi tình trạng ổn định (3,10,46,47).
Ở bệnh nhân có XHTH trên và có chỉ định rõ ràng cho liệu DAPT, chẳng hạn như vừa đặt stent hoặc nhồi máu cơ tim gần đây, tuyên bố đồng thuận của ESC và hướng dẫn của Hội Nội soi Tiêu hóa Châu Âu khuyến cáo tiếp tục DAPT nếu nội soi cho thấy các đặc điểm nguy cơ thấp, trong khi nếu có chảy máu đang hoạt động và các đặc điểm nội soi nguy cơ cao, hướng dẫn khuyến cáo ngừng aspirin hoặc DAPT trong ngắn hạn dựa trên mức độ nghiêm trọng của chảy máu và nguy cơ HK, với ít nhất một thuốc (thường là aspirin) được tái sử dụng sớm và thuốc thứ hai được tạm ngừng đến 5 ngày sau khi cầm máu. Liều cao của thuốc PPI được khuyến cáo ở tất cả bệnh nhân có loét dạ dày tá tràng chảy máu. Ở bệnh nhân vừa đặt stent và có XHTH dưới khi đang dùng DAPT, aspirin nên được tiếp tục nếu có thể, trong khi chất ức chế P2Y12 được ngừng trong tối đa 5 ngày (3,10,46,47)
4.2 Liệu pháp kháng đông
Ở bệnh nhân có XHTH đang hoạt động, thuốc KĐ cần được ngưng. Các khuyến cáo về thời điểm khởi động lại kháng đông còn khác nhau, từ ngay khi đã đạt được cầm máu, đến trong vòng 3–7 ngày ở bệnh nhân có nguy cơ thuyên tắc huyết khối cao, hoặc 7–15 ngày sau khi đã cầm máu. Việc tiếp tục liệu pháp kháng đông trong vòng 7 ngày sau biến cố XHTH dưới cũng được khuyến cáo trong hướng dẫn của Trường Môn Tiêu hóa Hoa Kỳ (3,10,46,47).
5. Bệnh nhân có xuất huyết tiêu hóa gần đây (trong vòng 3 ngày, hình 6)
5.1 Liệu pháp kháng tiểu cầu
Bằng chứng ủng hộ việc tiếp tục liệu pháp kháng tiểu cầu sau khi ổn định XHTH ở bệnh nhân có bệnh mạch máu có triệu chứng. Trong một thử nghiệm ngẫu nhiên có đối chứng với giả dược trên 156 bệnh nhân dùng aspirin bị xuất huyết do bệnh loét dạ dày tá tràng, việc tiếp tục aspirin liều thấp sau khi ổn định xuất huyết có liên quan đến giảm đáng kể tỷ lệ tử vong sau 8 tuần (1,3% so với 12,9%; P = 0,005), với chi phí là tăng không đáng kể về tái xuất huyết loét sau 30 ngày (10,3% so với 5,4%; P = 0,25). Ở bệnh nhân có nguy cơ HK cao (như những người vừa bị nhồi máu cơ tim, đột quỵ thiếu máu cục bộ hoặc can thiệp mạch vành qua da) và có các đặc điểm nội soi nguy cơ thấp (không xác định được nguồn xuất huyết, loét có nền sạch hoặc không có chảy máu đang hoạt động), việc tiếp tục aspirin liều thấp và các chất ức chế P2Y12 (nếu được chỉ định) được ủng hộ ngay sau khi đạt được cầm máu. Hướng dẫn của ESC đề xuất chuyển từ ticagrelor hoặc prasugrel sang clopidogrel sau XHTH. Ở bệnh nhân có nguy cơ HK thấp hơn (như những người có bệnh tim mạch xơ vữa ổn định) hoặc nguy cơ tái xuất huyết cao (chảy máu đang hoạt động hoặc có mạch máu nhìn thấy không chảy máu), việc trì hoãn tiếp tục liệu pháp chống tiểu cầu được ưu tiên. Thời gian trì hoãn phụ thuộc vào mức độ nghiêm trọng và nguồn gốc xuất huyết, và nên được xác định thông qua tham vấn với một đội ngũ đa chuyên khoa (29, 47-52).
5.2 Liệu pháp kháng đông
Dữ liệu từ thực hành lâm sàng thường quy cho thấy OAC bị ngừng vô thời hạn ở tới 50% bệnh nhân sau XHTH nặng cấp tính. Mặc dù bằng chứng chủ yếu đến từ các nghiên cứu quan sát còn tồn tại hạn chế về phương pháp luận và nguy cơ nhiễu có thể ảnh hưởng đến quyết định tái khởi động hoặc ngừng KĐ, những bệnh nhân được tái dùng KĐ có nguy cơ tương đối thấp hơn rõ rệt đối với HK (giảm 40–70%) và tử vong (giảm 40–50%), nhưng đồng thời có nguy cơ tương đối tái xuất huyết cao hơn tới khoảng gấp đôi.
Nguy cơ chảy máu, nguy cơ HK, thời gian đã trôi qua kể từ biến cố chảy máu, và tình trạng chức năng của bệnh nhân là những yếu tố quan trọng nhất cần được cân nhắc khi quyết định thời điểm tối ưu để khởi động lại kháng đông.
Do thiếu dữ liệu chất lượng cao, việc cân nhắc nguy cơ tuyệt đối, khả năng áp dụng các biện pháp dự phòng (cho cả chảy máu và HK), cũng như nguy cơ dài hạn của chảy máu và HK, là then chốt để xác định lợi ích lâm sàng ròng, thông qua quyết định chung với sự tham gia của nhóm đa chuyên khoa.Quản lý KĐ dài hạn ở các bệnh nhân này cần bao gồm đánh giá định kỳ nhằm bảo đảm lựa chọn thuốc và liều phù hợp với chỉ định và đặc điểm người bệnh (như tuổi, cân nặng, creatinin huyết thanh), đồng thời phát hiện và xử trí các yếu tố nguy cơ chảy máu có thể thay đổi, kể cả những yếu tố phát sinh trong quá trình theo dõi.
Ngày càng có nhiều bằng chứng (dù chủ yếu từ các nghiên cứu hồi cứu hoặc cải thiện chất lượng) cho thấy các chương trình quản lý KĐ (stewardship programmes) là những sáng kiến hệ thống có tính phối hợp, hiệu quả và bền vững, giúp tối ưu hóa việc kê đơn thuốc KĐ ở bệnh nhân nội trú.
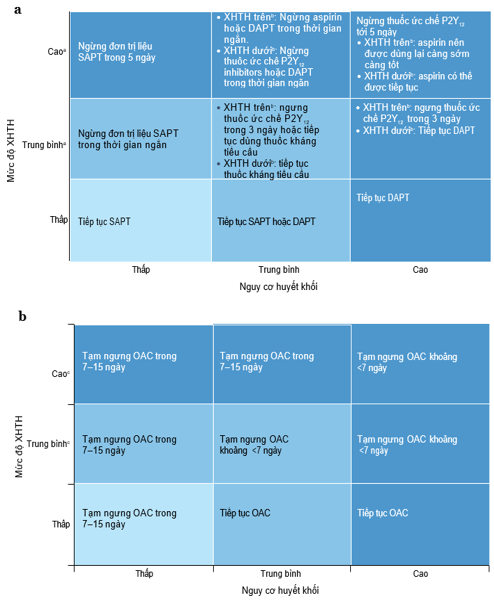
Hình 6. Quản lý các thuốc CHK ở bệnh nhân bị XHTH gần đây, được phân tầng theo nguy cơ HK và mức độ nghiêm trọng của chảy máu. Bệnh nhân có XHTH gần đây nguy cơ cao bao gồm những người bị sốc mất máu hoặc XHTH nặng. Bệnh nhân có XHTH gần đây nguy cơ trung bình bao gồm những người bị XHTH không nặng nhưng có ý nghĩa lâm sàng. Bệnh nhân có XHTH gần đây nguy cơ thấp bao gồm những người bị chảy máu trĩ nhỏ hoặc rách Mallory–Weiss. a, Bệnh nhân có nguy cơ HK cần liệu pháp kháng tiểu cầu. Bệnh nhân có nguy cơ HK thấp bao gồm những người có ASCVD ổn định mà không có các đặc điểm nguy cơ cao. Bệnh nhân có nguy cơ HK trung bình bao gồm những người có ASCVD không có ACS hoặc PCI gần đây và có các đặc điểm nguy cơ cao, những người đã trải qua PCI chọn lọc hoặc những người được quản lý y tế đối với ACS không ST chênh lên. Bệnh nhân có nguy cơ HK cao bao gồm những người bị nhồi máu cơ tim ST chênh lên, đột quỵ, huyết khối stent hoặc PCI trong ACS. Sự phân biệt giữa quản lý XHTH trên và XHTH dưới đến từ hướng dẫn của Trường môn Tiêu hóa Hoa Kỳ về XHTH dưới10. b, Bệnh nhân có nguy cơ HK cần liệu pháp KĐ. Bệnh nhân có nguy cơ HK thấp bao gồm những người bị AF (điểm CHA2DS2-VASc là 2), HK tĩnh mạch sâu chi đoạn xa đơn độc, thuyên tắc phổi nhánh nhỏ, hoặc VTE hơn 6 tháng trước do một yếu tố nguy cơ khởi phát chính mà không có bất kỳ yếu tố nguy cơ nào khác. Bệnh nhân có nguy cơ HK trung bình bao gồm những người bị PE nguy cơ trung bình–thấp, van cơ học không ở vị trí van hai lá, AF nguy cơ cao, hoặc VTE từ 1–6 tháng trước. Bệnh nhân có nguy cơ HK cao bao gồm những người bị PE nguy cơ cao, PE nguy cơ trung bình–cao, van hai lá cơ học, VTE trong tháng trước, hoặc hội chứng kháng phospholipid, HK ở bệnh nhân chảy máu cấp tính. aỞ những bệnh nhân bị XHTH đang hoạt động, có ý nghĩa lâm sàng, việc điều trị bằng các thuốc KĐ nên được tạm ngừng cho đến khi đạt được sự ổn định cầm máu và ngừng chảy máu; clopidogrel là thuốc ức chế P2Y12 được lựa chọn sau một biến cố chảy máu. bỞ những bệnh nhân bị XHTH trên, điều trị bằng aspirin nên được tạm ngừng khi sử dụng cùng với thuốc ức chế P2Y12. Ở những bệnh nhân bị XHTH dưới, điều trị bằng thuốc ức chế P2Y12 nên được tạm ngừng khi sử dụng cùng với aspirin. cỞ tất cả bệnh nhân bị XHTH có ý nghĩa lâm sàng, điều trị bằng thuốc KĐ nên được tạm ngừng.
* KẾT LUẬN
Việc duy trì độ an toàn mà không làm ảnh hưởng đến hiệu quả của các tác nhân CHK ở bệnh nhân có rối loạn tim mạch và tiêu hóa là một vấn đề phổ biến và quan trọng. Việc điều chỉnh liệu pháp CHK và quản lý bệnh nhân có XHTH đang hoạt động hoặc gần đây, cũng như những người có nguy cơ XHTH cao, thường đòi hỏi sự tham gia của một đội ngũ đa chuyên khoa.
Các điểm chính:
- Việc cân bằng giữa tính an toàn và hiệu quả của liệu pháp CHK ở bệnh nhân rối loạn tiêu hóa là một thách thức, do khả năng cản trở sự hấp thu của thuốc CHK hoặc làm tăng nguy cơ chảy máu.
- Nhiều bối cảnh lâm sàng khác nhau, bao gồm hội chứng kém hấp thu, phẫu thuật giảm cân, hội chứng ruột ngắn hoặc nuôi ăn qua ống thông, có thể ảnh hưởng đến sự hấp thu và sinh khả dụng của các thuốc CHK dùng đường uống.
- Các biến cố chảy máu là một yếu tố tiên lượng quan trọng ở bệnh nhân mắc bệnh tim mạch – đôi khi quan trọng ngang với các biến cố HK – và việc sử dụng các thuốc CHK ở bệnh nhân có nguy cơ cao bị XHTH là rất thách thức.
- Hầu hết các mô hình hiện có để dự đoán nguy cơ chảy máu ở bệnh nhân mắc bệnh động mạch vành không đánh giá cụ thể nguy cơ XHTH.
- Xác định bệnh nhân có nguy cơ XHTH cao, điều chỉnh nguy cơ chảy máu bằng cách sử dụng các thuốc bảo vệ đường tiêu hóa và lựa chọn phác đồ CHK phù hợp có vai trò quan trọng trong việc ngăn ngừa XHTH.
- Sau một đợt XHTH cấp tính, việc xác định thời gian gián đoạn liệu pháp CHK và phác đồ tái khởi động đòi hỏi phải cân nhắc giữa mức độ nghiêm trọng của chảy máu và nguy cơ các biến cố HK.
TÀI LIỆU THAM KHẢO
- Mitrov-Winkelmolen, L. et al. The effect of Roux-en-Y gastric bypass surgery in morbidly obese patients on pharmacokinetics of (acetyl) salicylic acid and omeprazole: the ERY-PAO study. Obes. Surg. 26, 2051–2058 (2016).
- Miedziaszczyk, M., Ciabach, P. & Szałek, E. The effects of bariatric surgery and gastrectomy on the absorption of drugs, vitamins, and mineral elements. Pharmaceutics 13, 2111 (2021).
- Abraham, N. S. et al. American College of Gastroenterology-Canadian Association of Gastroenterology Clinical Practice Guideline: management of anticoagulants and antiplatelets during acute gastrointestinal bleeding and the periendoscopic period. J. Can. Assoc. Gastroenterol. 5, 100–101 (2022).
- Mehran, R. et al. Associations of major bleeding and myocardial infarction with the incidence and timing of mortality in patients presenting with non-ST-elevation acute coronary syndromes: a risk model from the ACUITY trial. Eur. Heart J. 30, 1457–1466 (2009).
- Yasuda, H. et al. Treatment and prevention of gastrointestinal bleeding in patients receiving antiplatelet therapy. World J. Crit. Care Med. 4, 40–46 (2015).
- Abrignani, M. G. et al. Gastroprotection in patients on antiplatelet and/or anticoagulant therapy: a position paper of National Association of Hospital Cardiologists and the Italian Association of Hospital Gastroenterologists and Endoscopists. Eur. J. Intern. Med. 85, 1–13 (2021).
- Kido, K. & Scalese, M. J. Management of oral anticoagulation therapy after gastrointestinal bleeding: whether to, when to, and how to restart an anticoagulation therapy. Ann. Pharmacother. 51, 1000–1007 (2017).
- Scott, M. J., Veitch, A. & Thachil, J. Reintroduction of anti‐thrombotic therapy after a gastrointestinal haemorrhage: if and when? Br. J. Haematol. 177, 185–197 (2017).
- AH. Et al. Optimizing antithrombotic therapy in patients with coexisting cardiovascular and gastrointestinal disease. Số bổ sung. https://doi.org/10.1038/s41569-024-01003-3
- AH. Et al. Optimizing antithrombotic therapy in patients with coexisting cardiovascular and gastrointestinal disease. Nature reviews cardiology. doi.org/10.1038/s41569-024-01003-3
- Hobl, E. L. et al. Morphine decreases clopidogrel concentrations and effects: a randomized, double-blind, placebo-controlled trial. J. Am. Coll. Cardiol. 63, 630–635 (2014).
- Wong, G. C. et al. 2019 Canadian Cardiovascular Society/Canadian Association of Interventional Cardiology guidelines on the acute management of ST-elevation myocardial infarction: focused update on regionalization and reperfusion. Can. J. Cardiol. 35, 107–132 (2019).
- Byrne, R. A. et al. 2023 ESC Guidelines for the management of acute coronary syndromes. Eur. Heart J. 44, 3720–3826 (2023).
- Droppa, M. et al. Individualised dual antiplatelet therapy in a patient with short bowel syndrome after acute myocardial infarction with coronary artery stenting. BMJ Case Rep. 2015, bcr2014205227 (2015).
- Yan, H. et al. The relationship among intestinal bacteria, vitamin K and response of vitamin K antagonist: a review of evidence and potential mechanism. Front. Med. 9, 829304 (2022).
- Sobieraj, D. M., Wang, F. & Kirton, O. C. Warfarin resistance after total gastrectomy and Roux-en-Y esophagojejunostomy. Pharmacotherapy 28, 1537–1541 (2008).
- Hakeam, H. A. & Al-Sanea, N. Effect of major gastrointestinal tract surgery on the absorption and efficacy of direct acting oral anticoagulants. J. Thromb. Thrombolysis 43, 343–351 (2017).
- Colquitt, J. et al. Surgery for weight loss in adults. Cochrane Database Syst. Rev. 2014, D003641
- Angrisani, L. et al. Bariatric surgery and endoluminal procedures: IFSO worldwide survey 2014. Obes. Surg. 27, 2279–2289 (2017).
- Kingma, J. S. et al. Oral drug dosing following bariatric surgery: general concepts and specific dosing advice. Br. J. Clin. Pharmacol. 87, 4560–4576 (2021).
- Azran, C. et al. Oral drug therapy following bariatric surgery: an overview of fundamentals, literature and clinical recommendations. Obes. Rev. 17, 1050–1066 (2016).
- Norgard, N. B. et al. Aspirin responsiveness changes in obese patients following bariatric surgery. Cardiovasc. Ther. 35, e12268 (2017).
- Caruana, J. A, et al. Risk of massive upper gastrointestinal bleeding in gastric bypass patients taking clopidogrel. Surg. Obes. Relat. Dis. 3, 443–445 (2007).
- Martin, K. A. et al. Use of direct oral anticoagulants in patients with obesity for treatment and prevention of venous thromboembolism: updated communication from the ISTH SSC Subcommittee on Control of Anticoagulation. J. Thromb. Haemost. 19, 1874–1882 (2021).
- Sostres, C., Gargallo, C. J. & Lanas, A. Nonsteroidal anti-inflammatory drugs and upper and lower gastrointestinal mucosal damage. Arthritis Res. Ther. 15, S3 (2013).
- Masclee, G. M. et al. Risk of upper gastrointestinal bleeding from different drug combinations. Gastroenterology 147, 784–792.e9 (2014).
- Lanas, A. et al. Low doses of acetylsalicylic acid increase risk of gastrointestinal bleeding in a meta-analysis. Clin. Gastroenterol. Hepatol. 9, 762–768.e6 (2011).
- Carnicelli, A. P. et al. Direct oral anticoagulants versus warfarin in patients with atrial fibrillation: patient-level network meta-analyses of randomized clinical trials with interaction testing by age and sex. Circulation 145, 242–255 (2022).
- Xu, Y. & Siegal, D. M. Anticoagulant-associated gastrointestinal bleeding: framework for decisions about whether, when and how to resume anticoagulants. J. Thromb. Haemost. 19, 2383–2393 (2021).
- Catella, J. et al. Major gastrointestinal bleeding in patients receiving anticoagulant therapy for venous thromboembolism. Thromb. Res. 214, 29–36 (2022).
- Mo, C. et al. Proton pump inhibitors in prevention of low-dose aspirin-associated upper gastrointestinal injuries. World J. Gastroenterol. 21, 5382–5392 (2015).
- Levine, G. N. et al. 2016 ACC/AHA guideline focused update on duration of dual antiplatelet therapy in patients with coronary artery disease: a report of the American College of Cardiology/American Heart Association task force on clinical practice guidelines: an update of the ACCF/AHA/SCAI guideline for percutaneous coronary intervention,
- Virani, S. S. et al. 2023 AHA/ACC/ACCP/ASPC/NLA/PCNA guideline for the management of patients with chronic coronary disease. Circulation 148, e9–e119.
- M et al. Left Atrial Appendage Occlusion vs Standard of Care After Ischemic Stroke Despite Anticoagulation. JAMA Neurol. doi:10.1001/jamaneurol.2024.2882.
- J et al. SCAI/HRS expert consensus statement on transcatheter left atrial appendage closure. Heart Rhythm 2023;20: e1–e16.
- Holmes, D. R. Jr. et al. Prospective randomized evaluation of the Watchman left atrial appendage closure device in patients with atrial fibrillation versus long-term warfarin therapy: the PREVAIL trial. J. Am. Coll. Cardiol. 64, 1–12 (2014).
- Costa, R. A. et al. Polymer-free biolimus A9-coated stents in the treatment of de novo coronary lesions: 4- and 12-month angiographic follow-up and final 5-year clinical outcomes of the prospective, multicenter biofreedom FIM clinical trial. JACC Cardiovasc. Interv. 9, 51–64, 2016.
- Bikdeli B. et al. Developmental or procedural vena cava interruption and venous thromboembolism: a review. Semin. Thromb. Hemost. doi.org/ 10.1055/s-0043-1777991 (2024).
- De Caterina, R. et al. Great debate: triple antithrombotic therapy in patients with atrial fibrillation undergoing coronary stenting should be limited to 1 week. Eur. Heart J. 43, 3512–3527 (2022).
- Gargiulo, G. et al. Safety and efficacy outcomes of double vs. triple antithrombotic therapy in patients with atrial fibrillation following percutaneous coronary intervention: a systematic review and meta-analysis of non-vitamin K antagonist oral anticoagulant-based randomized clinical trials. Eur. Heart J. 40, 3757–3767 (2019).
- Gragnano, F. et al. P2Y12 inhibitor or aspirin monotherapy for secondary prevention of coronary events. J. Am. Coll. Cardiol. 82, 89–105 (2023).
- Guo, C. G. et al. Systematic review with meta-analysis: the risk of gastrointestinal bleeding in patients taking third-generation P2Y12 inhibitors compared with clopidogrel. Aliment. Pharmacol. Ther. 49, 7–19 (2019).
- F et al. P2Y12 Inhibitor or Aspirin Monotherapy for Secondary Prevention of
Coronary Events. J Am Coll Cardiol 2023; 82:89–105. - M et al. Clopidogrel vs aspirin for secondary prevention of coronary artery disease: a systematic review and individual patient data meta-analysis. Lancet 2025; 406: 1091–102.
- Zhu W, et al. Comparative Effectiveness and Safety of Non–Vitamin K Antagonist Oral Anticoagulants in Atrial Fibrillation Patients. Stroke. 2021;52(4):1225-1233
- Sengupta, N. et al. Management of patients with acute lower gastrointestinal bleeding:
an updated ACG guideline. J. Gastroenterol. 118, 208–231 (2023) - Halvorsen, S. et al. Management of antithrombotic therapy after bleeding in patients with coronary artery disease and/or atrial fibrillation: expert consensus paper of the European Society of Cardiology Working Group on Thrombosis. Eur. Heart J. 38, 1455–1462 (2017).
- Sung, J. J. et al. Asia-Pacific working group consensus on non-variceal upper gastrointestinal bleeding: an update 2018. Gut 67, 1757–1768 (2018).
- Qureshi, W. et al. Restarting anticoagulation and outcomes after major gastrointestinal bleeding in atrial fibrillation. Am. J. Cardiol. 113, 662–668 (2014).
- Little, D. et al. Resumption of anticoagulant therapy after anticoagulant-related gastrointestinal bleeding: a systematic review and meta-analysis. Thromb. Res. 175, 102–109 (2019).
- Candeloro, M. et al. Recurrent bleeding and thrombotic events after resumption of oral anticoagulants following gastrointestinal bleeding: communication from the ISTH SSC Subcommittee on Control of Anticoagulation. J. Thromb. Haemost. 19, 2618–2628 (2021).
- Little, D. H. W. et al. Management of antithrombotic therapy after gastrointestinal bleeding: a mixed methods study of health-care providers. J. Thromb. Haemost. 19, 153–160 (2021).







