1. ĐẠI CƯƠNG
Từ khi xuất hiện vào thập niên 1930 đến nay, heparin đã được sử dụng phổ biến trong thực hành lâm sàng với nhiều chỉ định từ phòng ngừa huyết khối, lọc máu đến điều trị các bệnh do thuyên tắc huyết khối
BS. TRẦN CÔNG DUY
BỘ MÔN NỘI TỔNG QUÁT
ĐẠI HỌC Y DƯỢC TP. HỒ CHÍ MINH
1. ĐẠI CƯƠNG
Từ khi xuất hiện vào thập niên 1930 đến nay, heparin đã được sử dụng phổ biến trong thực hành lâm sàng với nhiều chỉ định từ phòng ngừa huyết khối, lọc máu đến điều trị các bệnh do thuyên tắc huyết khối. Khoảng 1/3 bệnh nhân nhập viện có sử dụng heparin hàng năm. Tuy nhiên, heparin có thể dẫn đến các tác dụng phụ nghiêm trọng. Một trong những tác dụng phụ nặng nổi tiếng của heparin là giảm tiểu cầu.
Giảm tiểu cầu do heparin (heparin-induced thrombocytopenia – HIT) là một biến chứng quan trọng và đe dọa tính mạng của điều trị heparin. Có 2 loại HIT: HIT týp I không do cơ chế miễn dịch và HIT týp II do cơ chế miễn dịch (Bảng 1). Trong thực hành y khoa, khi nói đến HIT, chúng ta đề cập đến HIT týp II. Việc điều trị HIT cần ngưng heparin và sử dụng các thuốc kháng đông thay thế. Bài tổng quan này nhằm mục tiêu tổng kết lại các thông tin về HIT từ sinh lý bệnh đến cách tiếp cận chẩn đoán và điều trị để các bác sĩ hiểu rõ hơn về một tác dụng phụ quan trọng của một loại thuốc được sử dụng phổ biến trên trong thực hành lâm sàng hàng ngày, tránh bỏ sót chẩn đoán và có thái độ xử trí phù hợp.
2. ĐỊNH NGHĨA
Giảm tiểu cầu do heparin (heparin-induced thrombocytopenia – HIT) là một tình trạng rối loạn sau sử dụng heparin, trong đó bệnh nhân biểu hiện giảm số lượng tiểu cầu (< 150.000/mm3) hoặc giảm tương đối lớn hơn hoặc bằng 50% so với số lượng tiểu cầu ban đầu (một số bệnh nhân có thể giảm số lượng tiểu cầu ít hơn 50%), có thể có hoặc không các biến chứng huyết khối [2].
Qua định nghĩa trên, chúng ta lưu ý một số vấn đề: thời điểm xuất hiện HIT, mức độ giảm số lượng tiểu cầu, loại heparin sử dụng và nguy cơ huyết khối.
♦ Thời điểm bắt đầu giảm tiểu cầu sau sử dụng heparin thay đổi theo tiền sử sử dụng heparin. Khoảng 5 đến 14 ngày là điển hình ở các bệnh nhân chưa từng sử dụng hoặc đã sử dụng heparin cách hơn 100 ngày, trong khi sự giảm tiểu cầu đáng kể (trong vòng vài giờ) xảy ra ở các bệnh nhân có tiền sử dùng heparin gần đây và nồng độ kháng thể kháng PF4-heparin lưu hành có thể phát hiện được.
♦ Số lượng tiểu cầu hiếm khi giảm dưới 10.000/mm3, ít khi xuất huyết và điển hình hồi phục trong 4 đến 14 ngày sau khi ngừng heparin mặc dù sự hồi phục có thể lâu hơn ở một số bệnh nhân.
♦ Ở các bệnh nhân HIT, nguy cơ huyết khối gấp 30 lần dân số chứng. Các biến chứng huyết khối xuất hiện ở khoảng 20 đến 50% bệnh nhân. Nguy cơ huyết khối vẫn còn cao trong vài ngày đến vài tuần sau khi ngừng heparin, thậm chí khi số lượng tiểu cầu đã về bình thường. Huyết khối xảy ra ở cả tĩnh mạch và động mạch. Các biểu hiện không điển hình bao gồm hoại tử da do heparin, hoại thư tĩnh mạch chi và phản ứng dạng phản vệ sau bolus tĩnh mạch heparin.
♦ HIT được mô tả ở các bệnh nhân được điều trị với tất cả các loại heparin và bất kỳ liều lượng, bao gồm cả các trường hợp bệnh nhân có catheter tráng heparin và bệnh nhân được bolus liều thấp 250 đơn vị heparin. Tỉ lệ HIT ở bệnh nhân được điều trị heparin không phân đoạn (unfrationated heparin – UFH) gấp 10 lần bệnh nhân được điều trị với heparin trọng lượng phân tử thấp (low molecular weight heparin – LMWH). Tỉ lệ HIT tăng cũng được mô tả ở các bệnh nhân sử dụng lại heparin trong vòng 100 ngày. Ở các bệnh nhân được điều trị với UFH, tỉ lệ HIT được báo cáo ở những người sử dụng heparin nguồn gốc từ bò cao hơn những người sử dụng heparin nguồn gốc từ heo. Fondaparinux là một thuốc kháng đông mới xúc tác sự ức chế yếu tố Xa thông qua antithrombin, dẫn đến ức chế hình thành thrombin. Fondaparinux có thể liên quan với sự hình thành các kháng thể kháng PF4-heparin nhưng không gây ra HIT bởi vì phản ứng yếu của kháng thể kháng PF4-fondaparinux.
Dựa vào cơ chế miễn dịch, có 2 loại giảm tiểu cầu do heparin (heparin-induced thrombocytopenia – HIT) (Bảng 1):
♦ HIT týp I: xảy ra trong vòng 1-4 ngày sau sử dụng heparin. HIT týp 1 là một rối loạn không qua cơ chế miễn dịch và xảy ra do tác dụng trực tiếp của heparin đối với hoạt hóa tiểu cầu. Giảm tiểu cầu thường nhẹ (số lượng tiểu cầu > 100.000 mm3), không tiến triển và không gây ra xuất huyết hoặc huyết khối. HIT týp 1 dần dần hồi phục mà không cần ngừng heparin và số lượng tiểu cầu trở về bình thường trong vòng vài ngày mà không cần điều trị đặc hiệu [17].
♦ HIT týp II: là một rối loạn do cơ chế miễn dịch xảy ra điển hình 5-14 ngày sau khi sử dụng heparin, và có thể gây ra các biến chứng huyết khối đe dọa tính mạng (life-threating) và đe dọa chi (limb-threating), có thể dẫn đến phản ứng huyết khối toàn thân (cả tĩnh mạch và động mạch) hơn là xuất huyết [17].
Bảng 1. So sánh HIT miễn dịch và HIT không do miễn dịch [4]
|
Đặc điểm |
HIT miễn dịch (HIT týp II) |
HIT không do miễn dịch (HIT týp I) |
|
Tần suất |
2 – 3 % |
10 – 30 % |
|
Giảm số lượng tiểu cầu |
Trung bình hoặc nặng |
Nhẹ |
|
Thời gian từ khi bắt đầu điều trị heparin |
>5 ngày (có thể ngắn hơn nếu sử dụng heparin gần đây) |
<5 ngày |
|
Kháng thể HIT |
Có |
Không |
|
Nguy cơ huyết khối |
Cao |
Thấp |
|
Điều trị |
Ngừng heparin; sử dụng các thuốc kháng đông thay thế |
Theo dõi |
3. DỊCH TỄ HỌC
Tần suất
Các nghiên cứu trong y văn ghi nhận tần suất của HIT khoảng 1-5% [1], [18], [23]. Nhiều nghiên cứu báo cáo tần suất HIT 5% ở các bệnh nhân sau phẫu thuật chỉnh hình được dùng UFH phòng ngừa huyết khối trong 10-14 ngày. Một nghiên cứu của Smythe và các đồng nghiệp [19] ước tính tần suất HIT là 0,76% bệnh nhân nhận liều điều trị UFH và < 0,1% bệnh nhân được phòng ngừa chống huyết khối với UFH, nguy cơ toàn thể của HIT khoảng 0,2% trong tất cả bệnh nhân sử dụng heparin. Trong cùng nghiên cứu, 49% các trường hợp HIT mới xảy ra ở bệnh nhân phẫu thuật bắc cầu động mạch vành và/hoặc thay thế van. Bảng 2 ghi nhận tần suất HIT theo dân số bệnh nhân và loại heparin sử dụng.
Tử suất / bệnh suất
HIT miễn dịch là một biến chứng nặng có 20-50% nguy cơ xuất hiện các biến cố thuyên tắc huyết khối mới [22]. Tỉ lệ tử vong khoảng 20%, và khoảng 10% bệnh nhân cần đoạn chi hoặc chịu bệnh suất chính khác [3],[15],[21].
Huyết khối liên quan HIT có thể ảnh hưởng hệ động mạch, hệ tĩnh mạch hoặc cả hai. Các biến chứng huyết khối có thể bao gồm tai biến mạch máu não, nhồi máu cơ tim, thiếu máu cục bộ chi, huyết khối tĩnh mạch sâu và hiếm gặp thiếu máu các cơ quan khác. Các biến chứng huyết khối gây tử vong ở khoảng 29% bệnh nhân, và 21% bệnh nhân phải đoạn chi [11]. Một nghiên cứu với 108 bệnh nhân nhập viện được chẩn đoán HIT cho thấy các biến chứng huyết khối xảy ra ở khoảng 29% bệnh nhân, và sự giảm tiểu cầu nặng, sớm ở các bệnh nhân lớn tuổi có vẻ liên quan với sự xuất hiện các biến chứng huyết khối [15].
Bảng 2. Tần suất HIT theo dân số bệnh nhân và loại heparin [2]
|
Điều trị |
Nguy cơ |
Dân số nguy cơ |
Tỉ lệ kháng thể kháng PF4-heparin (%) |
Tỉ lệ HIT (%) |
|
UFH (mới sử dụng hoặc >100 ngày) |
Cao |
Bệnh nhân phẫu thuật chỉnh hình |
14 |
3 – 5 |
|
|
Trung bình |
Người lớn phẫu thuật tim |
25 – 50 |
1 – 2 |
|
|
Trung bình |
Bệnh nhân nội tổng quát |
8 – 20 |
0,8 – 3,0 |
|
|
Thấp đến hiếm |
Bệnh nhân nhi khoa tổng quát |
0 – 2,3 |
0 – 0,1 |
|
LMWH (mới sử dụng hoặc >100 ngày) |
Trung bình |
Bệnh nhân nội khoa |
2 – 8 |
0 – 0,9 |
|
|
Hiếm |
Phụ nữ mang thai |
Chưa rõ |
0 – 0,1 |
|
UFH hoặc LMWH (sử dụng trong vòng 100 ngày) |
Chưa rõ |
Tất cả dân số lâm sàng |
Chưa rõ |
Chưa rõ |
Chủng tộc
Một nghiên cứu của Lewis và cộng sự báo cáo người Da trắng có ít nguy cơ biến cố huyết khối hơn chủng tộc khác bất kể biểu hiện HIT. Nghiên cứu này cho thấy rằng các chủng tộc khác tiến triển đến kết cục huyết khối liên quan HIT đặc biệt các huyết khối mới gấp khoảng 2-3 lần người Da trắng [12].
Giới tính
Nam có ít nguy cơ đáng kể bị huyết khối hơn nữ trong nhóm các bệnh nhân HIT có huyết khối. Nữ bị huyết khối gấp 1,7 lần so với nam có biến cố huyết khối liên quan HIT [12]. Tần suất HIT gia tăng ở nữ được phát hiện nhiều nhất ở các bệnh nhân được điều trị với UFH. Không có mối liên quan giữa giới tính và nguy cơ HIT ở các bệnh nhân được điều trị với LMWH. LMWH trong phòng ngừa HIT có thể có lợi ích tuyệt đối lớn nhất ở các bệnh nhân nữ được phòng ngừa huyết khối sau phẫu thuật [28].
Tuổi
Một nghiên cứu có tổng số 408 bệnh nhân được chẩn đoán HIT cho thấy 66% bệnh nhân lớn hơn 60 tuổi [6].
4. SINH LÝ BỆNH
HIT là một biến chứng nặng của điều trị heparin gây ra bởi các kháng thể kháng phức hợp heparin và yếu tố tiểu cầu 4 (platelet factor 4 – PF4). Các kháng thể này hiện diện gần như ở tất cả bệnh nhân có chẩn đoán lâm sàng HIT. Tuy nhiên, các kháng thể này cũng hiện diện ở nhiều bệnh nhân sử dụng heparin nhưng không có biểu hiện lâm sàng HIT. Huyết tương từ hơn 90% bệnh nhân HIT chứa các kháng thể kháng PF4-heparin.
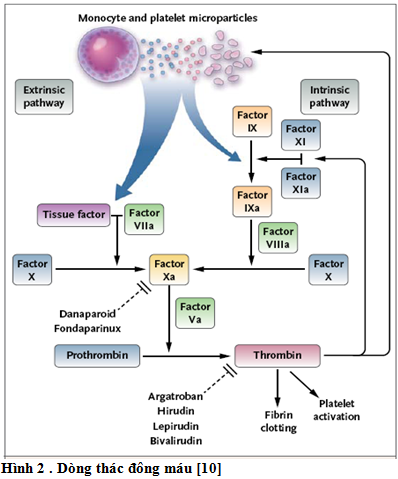
Các kháng thể IgG gắn với các vị trí biểu lộ cấu trúc trên PF4, một yếu tố gắn heparin được phóng thích bởi sự hoạt hóa tiểu cầu. Các phức hợp miễn dịch này tập trung trên bề mặt của các tế bào bao gồm tiểu cầu, tế bào đơn đơn nhân và có thể tế bào nội mô, cũng như trong huyết tương, gắn với thụ thể Fc¥RIIA (Hình 1). Các phức hợp miễn dịch gắn kết với bề mặt của tiểu cầu, hoạt hóa tiểu cầu và phóng thích các vi phần tử tiền đông. Các tiểu cầu được hoạt hóa bởi immunoglobulin G (IgG) HIT tăng phóng thích và biểu lộ PF4 trên bề mặt. Do đó, vòng phản hồi dương tính được tạo ra, dẫn đến sự phóng thích thêm PF4 với sự hoạt hóa tiểu cầu. Các vi phần tử tiểu cầu và tế bào đơn nhân hoạt hóa dòng thác đông máu bằng cách phóng thích yếu tố mô, gắn với yếu tố Xa, dẫn đến hoạt hóa yếu tố IX và X. Các vi phần tử này cũng thúc đẩy đông máu bằng cách cung cấp bề mặt màng phospholipid. Bề mặt này tăng cường sự tập trung của các phức hợp dòng thác đông máu, bao gồm phức hợp khởi động (yếu tố mô, yếu tố VIIa, Ixa và X) và phức hợp prothrombinase (yếu tố Va, Xa và prothrombin) (Hình 2).
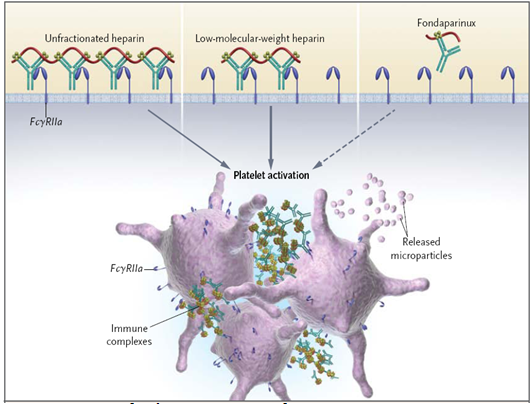
Hình 1 . Hoạt hóa tiểu cầu bởi các kháng thể kháng phức hợp PF4-heparin [10]
UFH và PF4 hình thành các phức hợp siêu lớn (> 670 kDa) với tỉ số tối ưu của PF4 với heparin khoảng 1:1. Các phức hợp này ổn định và có thể nhìn thấy dưới kính hiển vi điện tử. Các phức hợp siêu lớn ít được hình thành khi dùng LMWH và không hình thành với pentasacharide fondaparinux sodium. Khả năng PF4 hình thành các phức hợp siêu lớn bao gồm nhiều phân tử PF4 sắp xếp thành lưới với các phân tử UFH được xem là đóng vai trò cơ bản trong sự hình thành tự kháng thể, sự hoạt hóa tiểu cầu phụ thuộc kháng thể, và xu hướng tạo huyết khối ở các bệnh nhân HIT.
Có mối liên quan giữa sự xuất hiện kháng thể kháng PF4-heparin và nguy cơ HIT. Mặc dù gần như tất cả bệnh nhân HIT có kháng thể kháng PF4-heparin nhưng đa số bệnh nhân với kháng thể kháng PF4-heparin không có HIT. Điều gì làm một số kháng thể gây bệnh và các kháng thể khác không gây bệnh chưa được hiểu rõ nhưng có thể liên quan nồng độ kháng thể hoặc kích cỡ của các phức hợp PF4-heparin. Hơn nữa, một số bệnh nhân dễ xuất hiện kháng thể kháng PF4-heparin gây bệnh hơn các người khác. Điều này có lẽ dễ thấy ở các bệnh nhân phẫu thuật bắc cầu mạch vành; kháng thể kháng PF4-heparin xuất hiện ở 20 đến 50% bệnh nhân sau phẫu thuật, với nguy cơ toàn thể của HIT khoảng 1%. Ngược lại, kháng thể kháng PF4-heparin hình thành ở chỉ khoảng 10% bệnh nhân phẫu thuật chỉnh hình, nhưng HIT xảy ra ở một nửa các bệnh nhân đó [24].
Từ sinh lý bệnh của HIT, điều trị HIT bao gồm sử dụng thay thế thuốc kháng đông nonheparin không phản ứng chéo và có thể ngăn cản dòng thác đông máu được hoạt hóa ở mức thrombin hoặc yếu tố X (Hình 2). Các thuốc được sử dụng nhằm mục đích này bao gồm thuốc ức chế trực tiếp thrombin đường tĩnh mạch như argatropan, hirudin tái tổ hợp, lepirudin, desirudin, bivalirudin; và các thuốc ức chế yếu tố Xa đường tĩnh mạch như danaparoid và fondaparinux.
5. LÂM SÀNG
Mặc dù giảm số lượng tiểu cầu nhưng xuất huyết không phổ biến ở HIT; đặc điểm lâm sàng cơ bản của HIT là huyết khối [21],[22]. Ở các bệnh nhân này, tỉ lệ tương đối của huyết khối (OR=20-40) và tỉ lệ tuyệt đối của huyết khối (nguy cơ huyết khối, 30-75%) tăng có ý nghĩa. Ở các bệnh nhân HIT được điều trị chỉ bằng ngừng heparin, tỉ lệ huyết khối là 38-76%. Ở các bệnh nhân HIT không có huyết khối tại thời điểm chẩn đoán, nguy cơ huyết khối trong những ngày sau khi ngừng heparin là 19-52%; nguy cơ này kéo dài thậm chí khi số lượng tiểu cầu trở về trị số bình thường.
Các biến chứng thuyên tắc huyết khối có thể xuất hiện ở động mạch, tĩnh mạch hoặc cả hai. Huyết khối ở những bệnh nhân này gây ra bệnh suất và tử suất cao: đến 9-11% cần đoạn chi và tử vong đến 8-20% mặc dù được điều trị. Lý do tại sao một số bệnh nhân HIT xảy ra huyết khối và những người khác không có vẫn chưa rõ. Trong các nghiên cứu cắt ngang, các biểu hiện huyết khối tương quan với các dấu ấn hóa sinh của hoạt hóa tiểu cầu và tăng sản xuất thrombin, và trong các nghiên cứu tiến cứu, nguy cơ huyết khối cao hơn ở các bệnh nhân có nồng độ kháng thể kháng PF4-heparin cao hơn và ở những bệnh nhân giảm tiểu cầu tương đối hơn 70%.
Các biến chứng huyết khối tim mạch sau đã được mô tả: tắc các mảnh ghép tĩnh mạch (không phải động mạch), huyết khối tĩnh mạch ở các bệnh nhân có catheter trung tâm, hình thành huyết khối tâm nhĩ hoặc tâm thất, huyết khối van nhân tạo, nhồi máu cơ tim, và thuyên tắc phổi. Sự hiện diện bất kỳ các biến chứng này ở các bệnh nhân sử dụng heparin bắt buộc phải loại trừ HIT.
Các biến chứng ít gặp hơn của HIT là hoại thư chi, nhồi máu xuất huyết thượng thận hai bên, tổn thương da và phản ứng toàn thân cấp. Có đến 20% bệnh nhân có kháng thể biểu hiện tổn thương hoại tử hoặc hồng ban tại vị trí tiêm heparin. Các phản ứng toàn thân cấp như nhịp tim nhanh, sốt, lạnh run, tăng huyết áp, khó thở hoặc đau ngực xảy ra sau tiêm mạch heparin lặp lại ở 25% bệnh nhân có kháng thể lưu hành. Bệnh nhân HIT cũng có thể biểu hiện huyết khối tĩnh mạch sâu, có thể tiến triển đến đoạn chi nếu sử dụng coumarin dẫn đến giảm nặng protein C (hoại thư chi do coumarin).
Bảng 3. Các biểu hiện của HIT[7]
|
Huyết khối tĩnh mạch sâu Thuyên tắc phổi Huyết khối động mạch: đột quỵ, hội chứng mạch vành cấp, huyết khối động mạch ngoại biên Tổn thương da Xuất huyết thượng thận Hoại thư chi (venous limb gangrene) Phản ứng toàn thân cấp: ớn lạnh, lạnh run Khởi phát cấp với hôn mê và tử vong Hoại tử da do warfarin |
2. CẬN LÂM SÀNG
2.1 Đếm tiểu cầu
Cùng với nghi ngờ lâm sàng, số lượng tiểu cầu giảm là yếu tố quyết định trong chẩn đoán HIT ở phần lớn bệnh nhân. Trong HIT, giảm tiểu cầu thường dưới 150.000/mm3 hoặc giảm ≥ 50%, và điển hình trở về bình thường một tuần sau khi nghi ngờ điều trị với heparin. Nhìn chung có khuyến cáo sử dụng trị số giảm tương đối hơn trị số tuyệt đối để đánh giá giảm tiểu cầu.
Giảm tiểu cầu xảy ra điển hình vào 5 đến 14 ngày sau khi bắt đầu điều trị heparin, nhưng có thể sớm hơn hoặc muộn hơn. Ở các bệnh nhân có kháng thể PF4-heparin do sử dụng heparin gần đây, giảm tiểu cầu có thể xảy ra vài phút sau khi sử dụng lại heparin. Giảm tiểu cầu cũng có thể xảy ra vào 3 tuần sau khi ngưng điều trị heparin. Theo dõi số lượng tiểu cầu có thể được chỉ định ở tất cả bệnh nhân điều trị heparin nhưng tần suất theo dõi sẽ phụ thuộc vào nguy cơ (Bảng 4)
Bảng 4 . Tỉ lệ HIT theo loại dân số và khuyến cáo theo dõi số lượng tiểu cầu [8]
|
Loại dân số |
Ví dụ |
Tần suất theo dõi |
|
Sử dụng heparin gần đây |
Bệnh nhân được điều trị heparin trong vòng 100 ngày qua hoặc không rõ có sử dụng trước đó |
Ban đầu và trong 24 giờ đầu |
|
Phản ứng toàn thân cấp |
Bệnh nhân biểu hiện phản ứng toàn thân trong 30 phút đầu sau điều trị UFH |
Ngay lập tức và so sánh với trị số trước đó |
|
Nguy cơ HIT >1% |
Bệnh nhân được điều trị UFH với liều điều trị hoặc LMWH với liều chống huyết khối |
Ban đầu và ít nhất mỗi 2 ngày trong 14 ngày sau sử dụng hoặc đến khi ngừng heparin |
|
Nguy cơ HIT 0,1-1% |
Bệnh nhân nội khoa hoặc phụ nữ có thai được điều trị UFH với liều phòng ngừa hoặc LMWH sau bolus UFH; bệnh nhân ngoại khoa được điều trị LMWH với liều phòng ngừa; bệnh nhân được điều trị bolus UFH (catheter nội mạch) |
Ban đầu và mỗi 2-3 ngày trong 14 ngày sau sử dụng hoặc đến khi ngừng heparin |
|
Nguy cơ HIT <0,1% |
Bệnh nhân được điều trị LMWH liều phòng ngừa |
Không cần thiết (theo biểu hiện lâm sàng) |
2.2 Xét nghiệm kháng thể kháng PF4-heparin
Xét nghiệm phát hiện kháng thể ở tất cả bệnh nhân được điều trị heparin không được khuyến cáo vì độ nhạy và độ đặc hiệu tiên đoán sự xuất hiện của HIT thấp. Chỉ định các xét nghiệm kháng thể nên dựa vào nghi ngờ lâm sàng và không làm trì hoãn điều trị thích hợp. Các xét nghiệm phát hiện kháng thể PF4-heparin được khuyến cáo ở các bệnh nhân nghi ngờ HIT dựa vào đặc điểm thời gian của sự giảm tiểu cầu hoặc sự xuất hiện huyết khối.
Nhiều xét nghiệm khác nhau được dùng để phát hiện kháng thể HIT nhưng không có xét nghiệm nào có độ nhạy và độ đặc hiệu 100%. Có 2 nhóm xét nghiệm kháng thể kháng PF4-heparin: xét nghiệm huyết thanh (hoặc gọi là xét nghiệm miễn dịch) và xét nghiệm chức năng.
v Xét nghiệm huyết thanh (serologic assay) hoặc miễn dịch (immunologic assay): có ở nhiều các phòng xét nghiệm và có thể phát hiện các kháng thể IgG, IgA, IgM lưu hành. Mặc dù xét nghiệm miễn dịch có độ nhạy cao (lớn hơn 97%) nhưng độ đặc hiệu (74 đến 86%) bị giới hạn vì xét nghiệm có thể phát hiện các kháng thể kháng PF4-heparin ở các bệnh nhân không có HIT [16],[24],[27]. Vì vậy, giá tri tiên đoán dương của xét nghiệm miễn dịch có thể thấp (10 đến 93%, phụ thuộc vào dân số nghiên cứu)[16],[20], nhưng giá trị tiên đoán âm cao (lớn hơn 95%) [9],[16]. Độ đặc hiệu của xét nghiệm có thể được cải thiện nếu chỉ đo kháng thể IgG [27].
v Xét nghiệm chức năng (functional assay): đánh giá sự hoạt hóa tiểu cầu và phát hiện các kháng thể kháng PF4-heaprin có thể gắn kết và hoạt hóa các thụ thể Fc trên các tiểu cầu. Độ nhạy của xét nghiệm đánh giá sự ngưng tập tiểu cầu lớn hơn 90% tại các phòng xét nghiệm có kinh nghiệm[ 25]. Độ đặc hiệu của xét nghiệm từ 77 đến 100%, phụ thuộc vào bệnh cảnh lâm sàng sử dụng heparin. Xét nghiệm đo sự phóng thích 14C-serotonin từ tiểu cầu được hoạt hóa có độ nhạy cao (89 đến 100%) nhưng không được áp dụng rộng rãi. Do sự biến đổi của phản ứng ở các người cho tiểu cầu đối với kháng thể kháng PF4-heparin, giá trị tiên đoán dương của các xét nghiệm chức năng có khuynh hướng cao hơn (89 đến 100%) giá trị tiên đoán âm (81%).
v Xét nghiệm huyết thanh được khuyến cáo ở các bệnh nhân khi nghi ngờ lâm sàng HIT cao hoặc trung bình, bởi vì ở các bệnh nhân đó, kết quả âm tính có giá trị tiên đoán âm cao và gợi ý chẩn đoán thay thế khác. Xét nghiệm kháng thể không được khuyến cáo ở các bệnh nhân nghi ngờ lâm sàng HIT thấp. Tình huống khó khăn xảy ra khi bệnh nhân với xác suất HIT trung bình có kết quả xét nghiệm huyết thanh dương tính. Trong tình huống này, xét nghiệm chức năng có thể hữu ích vì kết quả dương tính sẽ tăng xác suất HIT thực sự.
Bảng 5. Các xét nghiệm phát hiện kháng thể kháng PF4-heparin [8]
|
Phương pháp |
Kỹ thuật |
Thuận lợi |
Bất lợi |
|
Xét nghiệm chức năng |
|||
|
Phóng thích serotonin |
Xác định số lượng serotonin phóng thích bởi các hạt tiểu cầu thông qua phát hiện phóng xạ hoặc hóa học |
Độ nhạy cao (> 95%) |
Cần người cho tiểu cầu. Kỹ thuật phóng xạ. Sử dụng hạn chế ở các phòng xét nghiệm nghiên cứu |
|
Hoạt hóa tiểu cầu |
Quan sát trực tiếp sự ngưng kết tiểu cầu |
|
|
|
Phóng thích adenosine triphosphate |
Phát hiện bằng huỳnh quang |
|
|
|
Vi phần tử tiểu cầu |
Phát hiện bằng đo dòng chảy tế bào (flow cytometry) |
|
Sử dụng hạn chế ở các phòng xét nghiệm nghiên cứu |
|
Xét nghiệm ngưng kết |
Đo sự ngưng kết tiểu cầu bằng máy đo ngưng kết quy ước |
|
Độ nhạy và độ đặc hiệu giới hạn; cần người cho tiểu cầu |
|
Găn kết annexin V |
Xác định số lượng annexin V gắn kết với các tiểu cầu được hoạt hóa |
|
|
|
Xét nghiệm miễn dịch |
|||
|
Xét nghiệm điện di miễn dịch PF4/polyanion |
Phát hiện PF4 polyvinyl sulfate |
Độ nhạy cao |
Độ đặc hiệu thấp |
|
Xét nghiệm điện di miễn dịch PF4/heparin |
Phát hiện phức hợp PF4-heparin |
Độ nhạy cao và độ đặc hiệu cao hơn (chỉ phát hiện IgG) |
Tính sẵn có ít (các phòng xét nghiệm nghiên cứu) |
Chỉ một tỉ lệ nhỏ bệnh nhân có kháng thể HIT sẽ bị HIT, và một tỉ lệ nhỏ hơn sẽ bị huyết khối do HIT. Không phải tất cả kháng thể được phát hiện bởi xét nghiệm miễn dịch có thể gây ra HIT biểu hiện lâm sàng, vì vậy độ đặc hiệu của xét nghiệm ở mức trung bình. Ngược lại, xét nghiệm chức năng nhạy và đặc hiệu đối với HIT vì chúng chỉ phát hiện các kháng thể có thể hoạt hóa tiểu cầu. Ở các bệnh nhân HIT hồi phục, có một thời gian đi chậm vài tuần giữa hồi phục số lượng tiểu cầu và sự biến mất kháng thể HIT (HIT bán cấp), nhất là khi sử dụng xét nghiệm huyết thanh. Các bệnh nhân này vẫn còn nguy cơ xảy ra HIT khởi phát nhanh (rapid- onset HIT) khi sử dụng lại heparin.
2.3 Chẩn đoán hình ảnh
Vấn đề lâm sàng chính liên quan HIT là huyết khối, cả tĩnh mạch và động mạch. Các xét nghiệm hình ảnh mạch máu khác nhau có thể được sử dụng để chứng minh các tổn thương huyết khối: siêu âm Doppler, CT-scan, xạ hình thông khí tưới máu… Khi nghi ngờ HIT, nên thực hiện siêu âm Doppler để tầm soát huyết khối tĩnh mạch sâu.
2.4 Xét nghiệm khác
Các xét nghiệm khác trong chẩn đoán HIT bao gồm các xét nghiệm thường quy và xét nghiệm chẩn đoán phân biệt nguyên nhân giảm tiểu cầu được chỉ định tùy tình huống lâm sàng như phết máu ngoại biên, tủy đồ, xét nghiệm tìm nguyên nhân nhiễm trùng, bệnh tự miễn…
3. TIẾP CẬN CHẨN ĐOÁN
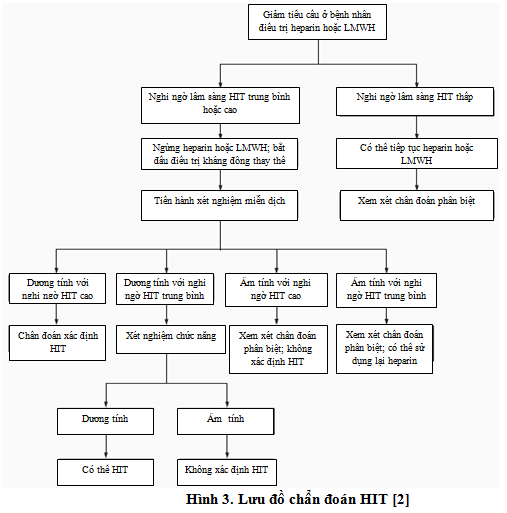
Xác định chẩn đoán HIT ở các bệnh nhân được điều trị heparin có thể là một thử thách. Tiếp cận chẩn đoán HIT bắt đầu từ nghi ngờ lâm sàng, thang điểm 4T’s (Bảng 6) giúp đánh giá xác suất tiền nghiệm lâm sàng trước khi xét nghiệm các kháng thể kháng PF4-heparin. Lưu đồ ở hình 3 giúp tiến hành các bước chẩn đoán HIT.
Thang điểm 4T’s có 4 đặc điểm đặc biệt hữu ích trong ước đoán xác suất HIT: mức độ giảm tiểu cầu, thời điểm khởi phát, sự hiện diện của huyết khối mới hoặc tiến triển và có nguyên nhân khác của giảm tiểu cầu hay không. Thang điểm 4T’s được đưa ra để đánh giá xác suất tiền nghiệm. Nếu điểm số thấp, HIT có thể được loại trừ mà không cần xét nghiệm kháng thể. Nếu xác suất tiền nghiệm không thấp, nên ngừng heparin và điều trị kháng đông thay thế trong lúc thực hiện các xét nghiệm.
Bảng 6. Thang điểm 4T’s [7]
|
Điểm (0,1 hoặc 2 đối với mỗi mục: điểm tối đa có thể = 8) |
|||
|
|
2 |
1 |
0 |
|
Thrombocytopenia (giảm tiểu cầu) |
Giảm > 50% và mức tiểu cầu thấp nhất ≥ 20 x 109/l |
Giảm 30-50% hoặc mức tiểu cầu thấp nhất 10-19 x 109/l |
Giảm <30% hoặc mức tiểu cầu thấp nhất < 10 x 109/l |
|
Timing* of platelet count fall or other sequelae(Thời điểm giảm số lượng tiểu cầu hoặc các biến cố khác) |
Bắt đầu rõ ràng giữa ngày 5 và 10; hoặc ≤ 1 ngày (nếu sử dụng heparin trong vòng 30 ngày) |
Phù hợp với miễn dịch nhưng không rõ (như thiếu số lượng tiểu cầu) hoặc bắt đầu giảm tiểu cầu sau ngày 10; hoặc giảm ≤ 1 ngày (nếu sử dụng heparin cách 30-100 ngày) |
Giảm số lượng tiểu cầu ≤ 4 ngày (không sử dụng heparin gần đây) |
|
Thrombosis or other sequelae(huyết khối hoặc các biến cố khác) |
Huyết khối mới; hoại tử da; phản ứng toàn thân sau bolus heparin |
Huyết khối hiện tại hoặc tiến triển; tổn thương da hồng ban; huyết khối nghi ngờ chưa được chứng minh |
Không |
|
oTher cause for thrombocytopenia not evident(nguyên nhân khác của giảm tiểu cầu không rõ ràng) |
Không có nguyên nhân khác của giảm tiểu cầu rõ ràng |
Nguyên nhân khác có thể rõ ràng |
Nguyên nhân khác xác định rõ ràng |
Điểm xác suất tiền nghiệm: 6-8 = Cao; 4-5 = Trung bình; 0-3 = Thấp
*Ngày đầu tiên sử dụng heparin được xem là ngày 0; ngày mà số lượng tiểu cầu bắt đầu giảm được xem là ngày khởi phát giảm tiểu cầu (nhìn chung mất hơn 1-3 ngày đến khi đạt bất kỳ ngưỡng giảm tiểu cầu).
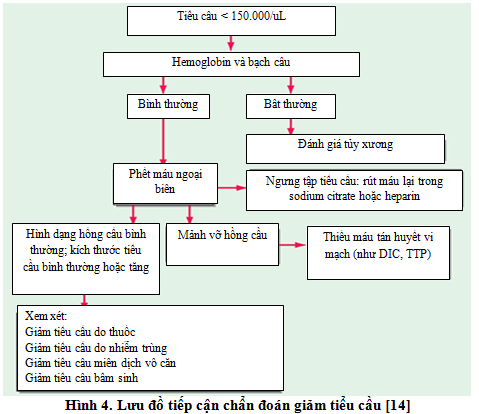
Giảm tiểu cầu có thể xuất hiện ở nhiều tình huống lâm sàng khác nhau như bệnh lý tủy xương, nhiễm trùng, bệnh tự miễn… Do đó, để tránh bỏ sót chẩn đoán, chúng ta cần khai thác tiền căn, bệnh sử, khám lâm sàng cẩn thận, sau đó chỉ định các xét nghiệm cần thiết để chẩn đoán phân biệt các nguyên nhân gây giảm tiểu cầu (Bảng 7) trước khi kết luận giảm tiểu cầu ở bệnh nhân do heparin. Có nhiều loại thuốc (Bảng 8) có thể gây ra giảm tiểu cầu qua cơ chế miễn dịch, do đó cần khai thác tiền sử, bệnh sử chi tiết để chẩn đoán phân biệt. Một cách tiếp cận chẩn đoán toàn diện từ tình trạng giảm số lượng tiểu cầu (Hình 4) sẽ giúp chúng ta chẩn đoán xác định nguyên nhân giảm tiểu cầu ở bệnh nhân sử dụng heparin có thực sự do thuốc này hay không.
Bảng 7. Các nguyên nhân của giảm tiểu cầu [5]
|
Giảm sản xuất tiểu cầu |
Tăng phá hủy tiểu cầu |
|
Tăng bắt giữ ở lách |
Nhiễm trùng |
Bảng 8 . Các thuốc liên quan với giảm tiểu cầu miễn dịch do thuốc [5]
|
Tương đối phổ biến |
Ít phổ biến hơn |
|
Thuốc ức chế Glycoprotein IIb/IIIa (abciximab, eptifibatide, tirofiban); quinine, quinidine, kháng sinh sulfa, carbamazepine, vancomycin |
Actinomycin, amitriptyline, amoxicillin /piperacillin/nafcillin, cephalosporin (cefazolin, ceftazidime, ceftriaxone), celecoxib, ciprofloxacin, esomeprazole, fexofenadine, fentanyl, fucidic acid, furosemide, muối vàng, levofloxacin, metronidazol, naproxen, oxaliplatin, phenytoin, propanolol, propoxyphene, ranitidine, rifampin, suramin, trimethoprime. |
8. ĐIỀU TRỊ
Các phương pháp điều trị được đề cập trong bài tổng quan này dựa trên các hướng dẫn của Trường Môn Các Bác Sĩ Lồng Ngực Hoa Kỳ (American College of Chest Physicians) năm 2012 [13], Hiệp Hội Huyết Học Anh Quốc (British Society for Haematology) năm 2012 [7] và nhiều tài liệu cập nhật khác.
Mục tiêu điều trị
Mục tiêu của điều trị HIT là giảm nguy cơ huyết khối bằng cách giảm hoạt hoá tiểu cầu và hình thành thrombin.
Nguyên tắc điều trị
Nên ngưng tất cả các nguồn heparin, bao gồm cả dung dịch heparin duy trì thông các catheter tĩnh mạch, khi nghi ngờ lâm sàng HIT trung bình hoặc cao và khởi động điều trị kháng đông thay thế. Khi nghi ngờ lâm sàng HIT thấp, quyết định ngừng heparin và điều trị kháng đông thay thế nên được điều chỉnh theo tình trạng bệnh nhân.
Các bệnh nhân giảm tiểu cầu do heparin không phân đoạn không nên được điều trị với LMWH vì các thuốc này có tính phản ứng chéo cao với các kháng thể PF4-heparin lưu hành. Đơn trị liệu warfarin ở bệnh nhân HIT cũng chống chỉ định dựa trên các báo cáo về hoại tử da do warfarin và hoại thư chi. Nếu bệnh nhân đang được điều tri warfarin khi chẩn đoán HIT, sử dụng vitamin K được khuyến cáo để đảo ngược tác dụng của thuốc. Aspirin và đặt lưới lọc tĩnh mạch chủ dưới không được xem là các điều trị hiệu quả.
Điều trị HIT cần kháng đông thay thế với một trong hai nhóm kháng đông (Bảng 9): ức chế trực tiếp thrombin hoặc heparinoid. Thuốc ức chế trực tiếp thrombin gắn kết trực tiếp và bất hoạt thrombin không thông qua antithrombin như heparin. Ức chế trực tiếp thrombin có thời gian bán hủy ngắn và không có phản ứng chéo với heparin. Heparinoid có tác dụng giảm sự hình thành thrombin. Không có các nghiên cứu so sánh trực tiếp các loại kháng đông thay thế khác nhau. Hiện tại, chưa có kinh nghiệm lâm sàng và in vitro để đánh giá chứng cớ về việc sử dụng các thuốc ức chế thrombin hoặc yếu tố Xa đường uống trong điều trị HIT. Sự lựa chọn kháng đông thay thế nên dựa vào tính sẵn có, kinh nghiệm sử dụng, phương pháp theo dõi có sẵn và tình trạng lâm sàng của bệnh nhân đặc biệt là tình trạng chức năng gan, thận.
Bảng 9. Nguyên tắc điều trị khi nghi ngờ HIT nhiều hoặc đã chẩn đoán xác định [25]
|
1 |
Ngừng và tránh sử dụng tất cả heparin |
|
2 |
Điều trị kháng đông thay thế |
|
3 |
Trì hoãn warfarin đến khi số lượng tiểu cầu hồi phục đáng kể (cho vitamin K nếu warfarin đã được sử dụng) |
|
4 |
Xét nghiệm các kháng thể HIT |
|
5 |
Theo dõi huyết khối tĩnh mạch sâu chi dưới |
|
6 |
Tránh truyền tiểu cầu dự phòng |
Bảng 10. Các thuốc kháng đông không phải heparin được dùng trong điều trị HIT [10]
|
Thuốc |
Liều lượng |
Theo dõi |
|
Argatroban |
Truyền tĩnh mạch liên tục 2,0 ug/kg/ph (không bolus); giảm còn 0,5-1,2 ug/kg/ph ở bệnh nhân bệnh gan, bệnh nặng hoặc sau phẫu thuật tim |
Chỉnh liều để duy trì aPTT 1,5-3,0 lần trị số ban đầu (tối đa 10 ug/kg/ph) |
|
Desirudin |
Tiêm dưới da 15-30 mg mỗi 12 giờ (liều thích hợp nhất để điều trị nếu HIT không được xác định) |
Không cần |
|
Bivalirudin |
Liều chưa được xác lập; 0,15-2,0 ug/kg/giờ (không bolus) được đề nghị |
Chỉnh liều để duy trì aPTT 1,5-2,5 lần trị số ban đầu |
|
Daparanoid |
Bolus tĩnh mạch (1500 U nếu <60 kg; 2250 U nếu 60 – <75 kg; 3000 U nếu 75 – 90 kg; 3750 U nếu > 90 kg), tiếp theo truyền tĩnh mạch 400 U/giờ trong 4 giờ, 300 U/giờ trong 4 giờ, sau đó 150-200 U/giờ |
Chỉnh liều để hoạt tính anti-Xa 0,5-0,8 U/ml (sử dụng đường cong chuẩn daparanoid) |
|
Fondaparinux |
5,0 mg tiêm dưới da 1 lần/ngày (<50 kg); 7,5 mg (50-100 kg); 10,0 mg (>100 kg) |
Không cần |
Bảng 11. Đặc điểm của các thuốc kháng đông được dùng để điều trị HIT [13]
|
Đặc điểm |
Lepirudin |
Argatroban |
Daparanoid |
Bivalirudin |
Fondaparinux |
|
Mục tiêu |
Thrombin |
Thrombin |
Yếu tố Xa (ưu thế) |
Thrombin |
Yếu tố Xa |
|
Thời gian bán hủy |
80 phút |
40-50 phút |
24 giờ |
25 phút |
17-20 giờ |
|
Thải trừ |
Thận |
Gan mật |
Thận |
Enzym (80%), thận (20%) |
Thận |
|
Được chấp thuận đối với bệnh nhân HIT |
Điều trị |
Điều trị/PCI |
Điều trị |
PCI/phẫu thuật tim |
Không |
|
Phương pháp điều trị |
TM, TDD |
TM |
TM, TDD |
TM |
TDD |
|
Theo dõi |
aPTT |
aPTT |
Nồng độ anti-Xa |
aPTT |
Nồng độ anti-Xa |
|
ECT (liều cao) |
ACT |
|
ACT hoặc ECT (liều cao) |
|
|
|
Tác dụng trên INR |
+ |
+++ |
0 |
++ |
0 |
|
Đặc điểm miễn dịch |
40-60% |
Không |
5% phản ứng chéo với kháng thể HIT |
Có thể phản ứng chéo với kháng thể kháng lepirudin |
Có thể có HIT |
|
Thuốc đối kháng |
Không |
Không |
Không |
Không |
Không |
|
Qua nhau thai |
Không rõ |
Không rõ |
Không |
Không rõ |
Có |
|
Có thể thẩm tách |
Máy thẩm tách lưu lượng cao |
20% |
Có |
25% |
20% |
ACT: activated clotting time; ECT: ecarin clotting time
THUỐC ỨC CHẾ TRỰC TIẾP THROMBIN ĐƯỜNG TĨNH MẠCH
Các thuốc ức chế trực tiếp thrombin đường tĩnh mạch được sử dụng rộng rãi để điều trị HIT. Argatroban được FDA ở Hoa Kỳ chấp thuận điều trị HIT và bilivarudin được chấp thuận ở Hoa Kỳ trong can thiệp mạch vành qua da ở các bệnh nhân có nguy cơ HIT. Desirudin không được chấp thuận sử dụng trong HIT nhưng được chấp thuận phòng ngừa huyết khối tĩnh mạch sâu sau phẫu thuật khớp háng. Lepirudin được chấp thuận sử dụng HIT nhưng ngừng sản xuất vì những lý do thương mại ở Châu Âu vào 2011 và ở Bắc Mỹ vào 2012. Ức chế trực tiếp thrombin gây ra sự tăng aPTT phụ thuộc liều, cho phép theo dõi đơn giản; tuy nhiên, theo dõi aPTT của các thuốc này có thể bị nhiễu bởi bệnh đông máu tiêu thụ, điều trị warfarin, và bệnh gan.
Argatrobanlà thuốc ức chế trực tiếp thrombin tổng hợp có nguồn gốc từ acid amin L-arginine, gắn kết có hồi phục với vị trí hoạt động của thrombin, ức chế hoạt động xúc tác của nó. Thuốc có thời gian khởi phát tác dụng trung bình và tác dụng kháng đông ổn định trong 1 đến 3 giờ. Chế độ chuẩn là truyền tĩnh mạch 2 ug/kg/phút. Giảm liều truyền tĩnh mạch được khuyến cáo ở các bệnh nhân rối loạn chức năng gan, bệnh nặng hoặc phẫu thuật tim (Bảng 10). Vì thời gian bán hủy ngắn, tác dụng kháng đông kết thúc sớm sau khi ngừng thuốc, và sự tăng đông dội ngược có thể xảy ra nếu ngừng thuốc trong khi tình trạng tiền đông vẫn còn.
Bivalirudin là đồng phân hirudin gắn kết với cả vị trí hoạt động và vị trí gắn kết fibrin của thrombin lưu hành và thrombin gắn huyết khối. Thuốc có thời gian bán hủy ngắn (khoảng 25 phút) và được thải trừ bởi thận và sự phân hủy của enzym. Thuốc được truyền tĩnh mạch liên tục. Bivalirudin đã được sử dụng như thuốc kháng đông trong phẫu thuật tim ở các bệnh nhân HIT hoặc tiền sử HIT gần đây. Liều điều trị HIT chưa được xác lập, mặc dù chế độ 0,15 đến 2 mg/kg/giờ, điều chỉnh theo aPTT, được đề nghị (Bảng 10).
Lepirudin và desirudin là các dẫn xuất hirudin tái tổ hợp cũng ức chế trực tiếp thrombin tự do và thrombin gắn fibrin. Hai hirudin tái tổ hợp này khác ít với hirudin tự nhiên ở chuỗi acid amin. Lepirudin được nghiên cứu rộng rãi và chấp thuận sử dụng trong HIT nhưng không còn sản xuất nữa. Dữ liệu liên quan việc sử dụng desirudin trong HIT còn hạn chế, nhưng liều 15 hoặc 30 mg tiêm dưới da mỗi 12 giờ được đề nghị.
HEPARINOIDS
Danaparoidlà hỗn hợp các glycosaminoglycan sulfate trọng lượng phân tử thấp, không có heparin, bao gồm heparan sulfate, dermatan sulfate và chondroititn sulfate. Danaparoid ức chế yếu tố Xa phụ thuộc antithrombin tác dụng dài. Thuốc bị rút ra khỏi thị trường Hoa Kỳ bởi nhà sản xuất vào 2002 do thiếu nguồn cung cấp, nhưng có thể sử dụng và được chấp thuận điều trị HIT ở Canada, Nhật Bản, Châu Âu và Úc. Phản ứng chéo in vitro của danaparoid với một số kháng thể gây ra HIT đã được báo cáo, nhưng thường ít có ý nghĩa lâm sàng. Theo dõi hoạt tính Xa nên được thực hiện ở các bệnh nhân có cân nặng ngoài phạm vi 55 đến 90 kg và ở các bệnh nhân suy thận cấp (Bảng 10). Danaparoid có thể được tiêm dưới da và tĩnh mạch và không qua nhau thai.
Fondaparinux là pentasaccharide sulfate tổng hợp gắn kết antithrombin, làm ức chế yếu tố Xa kéo dài. Fondaparinux được hấp thu nhanh ( < 30 phút) sau khi tiêm dưới da và thời gian bán hủy của nó cho phép sử dụng 1 lần mỗi ngày (Bảng 10). Liều điều trị (5 đến 10 mg tiêm dưới da) hiếm khi làm aPTT kéo dài. Mặc dù có thể đo nồng độ anti-Xa huyết tương nhưng không cần theo dõi anti-Xa thường quy. Sử dụng fondaparinux điều trị HIT trong thai kỳ đã được báo cáo nhưng kinh nghiệm còn hạn chế. Fondaparinux có thể hình thành kháng thể kháng PF4, tuy nhiên không gây ra sự hoạt hóa tiểu cầu bởi các phức hợp miễn dịch mới.
NHỮNG VẤN ĐỀ KHÁC LIÊN QUAN ĐIỀU TRỊ
Truyền tiểu cầukhông được sử dụng phòng ngừa trong HIT. HIT là một hiện tượng tự miễn và sự tăng số lượng kháng nguyên có thể làm tăng tình trạng tăng đông và gây ra các biến cố huyết khối.
Thuốc ức chế Glycoprotein IIb/IIIa không có tác dụng kháng đông trực tiếp và không ức chế sự hoạt hóa tiểu cầu thông qua các kháng thể HIT; do đó, chúng không hiệu quả khi sử dụng đơn độc trong điều trị HIT. Tuy nhiên, sự phối hợp của thuốc ức chế glycoprotein IIb/IIIa và kháng đông thay thế được sử dụng hiệu quả trong bệnh cảnh tạo hình mạch vành và làm giảm gián tiếp sự hình thành thrombin và ức chế sự ngưng tập tiểu cầu, cho phép chỉ định như điều trị bổ sung ở những trường hợp chọn lọc.
Chuyển sang thuốc kháng vitamin K
HIT được xem là yếu tố nguy cơ đối với thuyên tắc huyết khối tĩnh mạch. Vì nguy cơ này hồi phục và thoáng qua nên kháng đông thay thế nên được tiếp tục trong 4 đế 6 tuần ở các bệnh nhân HIT đơn thuần và 3 tháng ở các bệnh nhân có huyết khối. Nên tránh việc sử dụng sớm thuốc kháng vitamin K (như warfarin) vì điều này có thể làm nặng hơn tình trạng tiền đông thông qua sự giảm nhanh protein C, một chất kháng đông tự nhiên. Khi tiểu cầu trở về nồng độ bình thường sau một đợt HIT cấp, warfarin nên được sử dụng từ liều thấp 5 mg hoặc ít hơn và tăng dần để đạt INR 2 đến 3. Warfarin nên gối đầu với thuốc kháng đông thay thế đường tĩnh mạch trong ít nhất 5 ngày và đến khi INR đạt mục tiêu. Với các thuốc ức chế trực tiếp thrombin, liều thuốc kháng vitamin K trong thời gian gối đầu có thể làm tăng INR.
HIT trong thai kỳ
HIT không phổ biến trong thai kỳ, nhất là tỉ lệ HIT ở các bệnh nhân điều trị LMWH rất thấp đến mức đến việc theo dõi thường quy dân số này không được chỉ định. Có ít dữ liệu về quá trình chẩn đoán trong thai kỳ, do đó tiếp cận lâm sàng chung sử dụng thang điểm như 4T’s, kết hợp với xét nghiệm kháng thể có vẻ hợp lý. Ở các bệnh nhân nghi ngờ HIT nhiều hoặc đã xác định HIT, nên ngừng heparin và bắt đầu kháng đông thay thế. Có các dữ liệu về sử dụng danaparoid, argatroban và fondaparinux trong HIT ở bệnh nhân mang thai. Số lượng lớn nhất của các báo cáo là về sử dụng danaparoid (Lindhoff-Last et al, 2005). Trong 51 bệnh nhân mang thai điều trị danaparoid vì không dung nạp heparin hoặc HIT (n=32), 37 sơ sinh khỏe mạnh được sinh ra từ các bà mẹ điều trị danaparoid đủ thời gian và danaparoid ngừng ở 14 bệnh nhân khác trước sinh vì nhiều lý do khác nhau không liên quan điều trị danaparoid. Có 4 biến cố xuất huyết ở mẹ trong thai kỳ; 2 trong số này tử vong do các vấn đề nhau thai. Có 3 trường hợp chết thai không do danaparoid. Có một số ít báo cáo hàng loạt ca ghi nhận sử dụng argatroban trong thai kỳ (Young et al, 2008; Ekbatani et al, 2010; Tanimura et al, 2012). Trong 2 báo cáo, argatroban được sử dụng phối hợp với fondaparinux với các kết quả thai kỳ thành công (Ekbatani et al, 2010; Tanimura et al, 2012), và trong một nghiên cứu khác, argatroban được dùng liên tục trong 6 tháng với kết quả thai kỳ tốt (Young et al, 2008).
Điều trị bệnh nhân với tiền sử HIT: Các bệnh nhân với tiền sử HIT không luôn luôn xảy ra HIT lặp lại khi sử dụng lại heparin, mặc dù nguy cơ gia tăng. Vì những biến chứng nặng tiềm năng liên quan HIT, việc sử dụng các kháng đông thay thế được khuyến cáo bất kỳ khi nào có thể ở các bệnh nhân này.
TÓM TẮT CÁC KHUYẾN CÁO ĐIỀU TRỊ VÀ PHÒNG NGỪA HIT [13]
♦ Đối với các bệnh nhân điều trị heparin mà bác sĩ đánh giá nguy cơ HIT > 1%, theo dõi số lượng tiểu cầu mỗi 2 hoặc 3 ngày từ ngày 4 đến 14 (hoặc đến khi ngừng heparin) (Mức độ 2C).
♦ Đối với các bệnh nhân điều trị heparin mà bác sĩ đánh giá nguy cơ HIT < 1%, không theo dõi số lượng tiểu cầu (Mức độ 2C).
♦ Ở các bệnh nhân HIT có huyết khối, khuyến cáo sử dụng các thuốc kháng đông thay thế nonheparin, đặc biệt là lepirudin, argatroban và danaparoid, hơn sử dụng heparin hoặc LMWH hoặc bắt đầu/tiếp tục thuốc kháng vitamin K (Mức độ 1C).
♦ Ở các bệnh nhân HIT có huyết khối với chức năng thận bình thường, đề nghị sử dụng argatropan hoặc lepirudin hoặc danaparoid hơn các kháng đông nonheparin khác (Mức độ 2C).
♦ Ở các bệnh nhân HIT có huyết khối và suy thận, đề nghị sử dụng argatropan hơn các kháng đông nonheparin khác (Mức độ 2C).
♦ Ở các bệnh nhân HIT và giảm tiểu cầu nặng, đề nghị truyền tiểu cầu chỉ khi xuất huyết hoặc trong khi thực hiện một thủ thuật xâm lấn với nguy cơ xuất huyết gia tăng (Mức độ 2C).
♦ Ở các bệnh nhân nghi ngờ nhiều hoặc đã xác định HIT, khuyến cáo không bắt đầu kháng vitamin K đến khi tiểu cầu hồi phục đáng kể (ví dụ, thường đến ít nhất 150 x 109/L) hơn bắt đầu kháng vitamin K ở mức số lượng tiểu cầu thấp hơn và thuốc kháng vitamin K nên được khởi đầu ở liều thấp (tối đa 5 mg warfarin hoặc 6 mg phenprocoumon) hơn sử dụng liều cao (Mức độ 1C).
♦ Nếu thuốc kháng vitamin K đã được sử dụng khi bệnh nhân được chẩn đoán HIT, nên điều trị với vitamin K (Mức độ 2C).
♦ Ở các bệnh nhân đã xác định HIT, khuyến cáo gối đầu thuốc kháng vitamin K với một thuốc kháng đông nonheparin trong ít nhất 5 ngày và đến khi INR trong phạm vi mục tiêu hơn khoảng thời gian gối đầu ngắn hơn và kiểm tra INR sau khi tác dụng kháng đông của thuốc kháng đông nonheparin biến mất (Mức độ 2C).
♦ Ở các bệnh nhân HIT đơn thuần (HIT không có huyết khối), khuyến cáo sử dụng lepirudin hoặc argatroban hoặc danaparoid hơn sử dụng heparin hoặc LMWH hoặc bắt đầu/tiếp tục thuốc kháng vitamin K (Mức độ 1C).
♦ Ở các bệnh nhân HIT đơn thuần (HIT không có huyết khối) với chức năng thận bình thường, khuyến cáo sử dụng argatroban hoặc lepirudin hoặc danaparoid hơn các thuốc kháng đông nonheparin khác (Mức độ 2C).
♦ Ở các bệnh nhân HIT cấp (giảm tiểu cầu, kháng thể HIT dương tính) hoặc HIT bán cấp (tiểu cầu bình thường nhưng kháng thể HIT dương tính) cần phẫu thuật tim khẩn, đề nghị sử dụng bivalirudin hơn các thuốc kháng đông thay thế khác và hơn heparin cùng với truyền tiểu cầu (Mức độ 2C).
♦ Ở các bệnh nhân HIT cấp cần phẫu thuật tim không khẩn, khuyến cáo ngừng phẫu thuật (nếu có thể) đến khi HIT biến mất và các kháng thể HIT âm tính (Mức độ 2C).
♦ Ở các bệnh nhân HIT cấp hoặc bán cấp cần can thiệp mạch vành qua da, đề nghị sử dụng bivalirudin (Mức độ 2B) hoặc argatroban (Mức độ 2C) hơn các thuốc kháng đông nonheparin khác .
♦ Ở các bệnh nhân HIT cấp hoặc bán cấp cần điều trị thay thế thận, đề nghị sử dụng argatropan hoặc danaparoid hơn các thuốc kháng đông nonheparin khác (Mức độ 2C).
♦ Ở các bệnh nhân với tiền sử HIT cần điều trị thay thế thận tiếp tục hoặc khóa catheter, đề nghị sử dụng citrate tại chỗ hơn sử dụng heparin hoặc LMWH (Mức độ 2C).
♦ Ở các bệnh nhân mang thai với HIT cấp hoặc bán cấp, đề nghị sử dụng danaparoid hơn các thuốc kháng đông thay thế khác (Mức độ 2C). Đề nghị sử dụng lepirudin hoặc fondaparinux chỉ khi danaparoid không có sẵn (Mức độ 2C).
♦ Ở các bệnh nhân có tiền sử HIT mà kháng thể heparin âm tính, cần phẫu thuật tim, đề nghị sử dụng heparin (chỉ sử dụng ngắn hạn) hơn các thuốc kháng đông nonheparin khác (Mức độ 2C).
♦ Ở các bệnh nhân có tiền sử HIT mà kháng thể heparin vẫn còn, cần phẫu thuật tim, đề nghị sử dụng các thuốc kháng đông nonheparin hơn heparin hoặc LMWH (Mức độ 2C).
♦ Ở các bệnh nhân có tiền sử HIT mà kháng thể heparin âm tính, cần thông tim hoặc can thiệp mạch vành qua da, đề nghị sử dụng bivalirudin (Mức độ 2B) hoặc argatroban (Mức độ 2C) hơn các thuốc kháng đông nonheparin khác.
♦ Ở các bệnh nhân với tiền sử HIT có huyết khối cấp (không liên quan HIT) và chức năng thận bình thường, đề nghị sử dụng fondaparinux với liều điều trị đầy đủ đến khi có thể chuyển sang thuốc kháng vitamin K (Mức độ 2C).
Bảng 12. Hệ thống mức độ theo hướng dẫn của Trường Môn Các Bác Sĩ Lồng Ngực Hoa Kỳ [13]
|
1 |
Khuyến cáo mạnh |
|
2 |
Khuyến cáo yếu |
|
A |
Chứng cớ chất lượng cao |
|
B |
Chứng cớ chất lượng trung bình |
|
C |
Chứng cớ chất lượng yếu |
9. KẾT LUẬN
HIT là một biến chứng nặng của một loại thuốc điều trị phổ biến. HIT thường bị bỏ sót chẩn đoán và nên nghi ngờ ở tất cả bệnh nhân điều trị heparin xuất hiện giảm tiểu cầu hoặc huyết khối. Chúng ta nên nhớ rằng mặc dù tỉ lệ HIT dao động lớn nhưng bệnh nhân ở bất kỳ lứa tuổi với bất kỳ tình trạng bệnh và sử dụng bất kỳ loại heparin (UFH hay LMWH) với bất kỳ liều lượng và qua bất kỳ đường nào cũng có thể xuất hiện HIT. Các nguyên nhân khác của giảm tiểu cầu nên được loại trừ trước khi chẩn đoán HIT. Khi nghi ngờ lâm sàng HIT, nên ngừng ngay lập tức heparin và xem xét điều trị kháng đông thay thế như ức chế trực tiếp thrombin thay thế hoặc heparinoid. Nhìn chung, chẩn đoán và điều trị HIT là một thử thách tiếp diễn. Các nghiên cứu trong tương lai đánh giá tính hiệu quả và an toàn của các thuốc kháng đông mới trong điều trị HIT sẽ có giá trị to lớn đối với cộng đồng y khoa.
TÀI LIỆU THAM KHẢO
1. Arepally G, Cines DB. Heparin-induced thrombocytopenia and thrombosis. Clin Rev Allergy Immunol. Fall 1998;16(3):237-47.
2. Arepally GM, Ortel TL. Heparin-induced thrombocytopenia. N Eng J Med 2006; 355: 809-17.
3. Boshkov LK, Warkentin TE, Hayward CP, Andrew M, Kelton JG. Heparin-induced thrombocytopenia and thrombosis: clinical and laboratory studies. Br J Haematol. Jun 1993;84(2):322-8.
4. Eduard Shantsila, et al. Heparin-induced thrombocytopenia, a contemporary clinical approach to diagnosis and management. Chest 2009; 135: 1651-64
5. Foster, et al. Platelet disorders. The Washington Manual of Medical Therapeutics 2007; 32rd edition: 514-21.
6. Greinacher A, et al. Clinical features of heparin-induced thrombocytopenia including risk factors for thrombosis. A retrospective analysis of 408 patients. Thromb Haemost. Jul 2005;94(1):132-5.
7. Henry Watson, et al. Guidelines on the diagnosis and management of heparin-induced thrombocytopenia: second edition.British Journal of Haematology 2012.
8. Ignacio Cruz-Gonzalez, et al. Heparin-induced thrombocytopenia. Rev Esp Cardiol 2007; 60 (10): 1071-82
9. Lo GK, et al. Evaluationb of pretest clinical score (4T’s) for the diagnosis of heparin-induced thrombocytopenia in two clinical settings. J Thromb Haemost 2006; 4: 759-65.
10. Kelton JG. Nonheparin anticoagulants for heparin-induced thrombocytopenia. N Engl J Med 2013;368:737-44
11. King DJ, Kelton JG. Heparin-associated thrombocytopenia. Ann Intern Med. Apr 1984;100(4):535-40.
12. Lewis BE, et al. Effects of argatroban therapy, demographic variables, and platelet count on thrombotic risks in heparin-induced thrombocytopenia. Chest. Jun 2006;129(6):1407-16.
13. Linkins LA, et al. Treatment and prevention of heparin-induced thrombocytopenia. Antithrombotic therapy and prevention of thrombosis, 9th ed: American College of Chest Physicians Evidence-Based Clinical Practice Guidelines. Chest 2012; 141 (2) (Suppl):e 495S-e530S.
14. Longo DL, et al. Disorders odf platelets and vessel wall. Harrison’s Principle of Internal Medicine 2011; 18th edition.
15. Nand S, Wong W, Yuen B, et al. Heparin-induced thrombocytopenia with thrombosis: incidence, analysis of risk factors, and clinical outcomes in 108 consecutive patients treated at a single institution. Am J Hematol. Sep 1997;56(1):12-6.
16. Pouplard C, et al. Decision analysis for use of platelet aggregation test, carbon 14-serotonin release assay, and heparin-platelet factor 4 enzyme-linked immunosorbent assay for diagnosis of heparin-induced thrombocytopenia. Am J Clin Patho 1999;111:700-6.
17. Sancar Eke. Heparin-induced thrombocytopenia. http://emedicine.medscape.com/article/1357846-overview
18. Schmitt BP, Adelman B. Heparin-associated thrombocytopenia: a critical review and pooled analysis. Am J Med Sci. Apr 1993;305(4):208-15.
19. Smythe MA, Koerber JM, Mattson JC. The incidence of recognized heparin-induced thrombocytopenia in a large, tertiary care teaching hospital. Chest. Jun 2007;131(6):1644-9.
20. Verma AK, et al. Frequency of heparin-induced thrombocytopenia in critical care patients. Pharmacotherapy 2003;23:745-53.
21. Warkentin TE, Levine MN, Hirsh J, et al. Heparin-induced thrombocytopenia in patients treated with low-molecular-weight heparin or unfractionated heparin. N Engl J Med. May 18 1995;332(20):1330-5.
22. Warkentin TE, Kelton JG. A 14-year study of heparin-induced thrombocytopenia. Am J Med. Nov 1996;101(5):502-7.
23. Warkentin TE. Heparin-induced thrombocytopenia: a ten-year retrospective. Annu Rev Med. 1999;50:129-47.
24. Warkentin TE, et al. Impact of the patient population on the risk for heparin-induced thrombocytopenia. Blood 2000; 96: 1703-8
25. Warkentin TE. Heparin-induced thrombocytopenia: diagnosis and management. Ciculation 2004; 110: e454-e458.
26. Warkentin TE, et al. Heparin-induced thrombocytopenia: recognition, treatment and prevention: the Seventh ACCP Conference on Anti thrombotic and Thrombolytic Therapy. Chest 2004; 126: Suppl: 311S-337S
27. Warkentin TE, et al. Laboratory testing for the antibodies that cause heparin-induced thrombocytopenia: how much class do we need? J Lab Clin Med 2005;146:341-6.
28. Warkentin TE, Sheppard JA, et al. Gender imbalance and risk factor interactions in heparin-induced thrombocytopenia. Blood. Nov 1 2006;108(9):2937-41.
29. Warkentin TE, Eikelboom JW. Who is (still) getting HIT?. Chest. Jun 2007;131(6):1620-2.







