TS.BS. TRẦN CÔNG DUY
PGS.TS.BS. HOÀNG VĂN SỸ
Bộ môn Nội Tổng quát, Trường Y, ĐH Y Dược TP.HCM
Khoa Nội Tim Mạch, Bệnh viện Chợ Rẫy TPHCM
TÓM TẮT
Tăng cholesterol máu gia đình (Familial Hypercholesterolemia – FH) là rối loạn lipid máu di truyền phổ biến, đặc trưng bởi tăng cao nồng độ LDL-C ở giai đoạn sớm của cuộc đời và nguy cơ cao bệnh tim mạch do xơ vữa. Trong khi phân tích đơn gen truyền thống (LDLR, APOB, PCSK9) là nền tảng chẩn đoán FH, một tỷ lệ đáng kể bệnh nhân có biểu hiện lâm sàng nghi ngờ FH nhưng không phát hiện được đột biến đơn gen. Sự phát triển của thang điểm nguy cơ đa gen LDL-C cho phép định lượng gánh nặng di truyền tích lũy từ nhiều biến thể gen làm tăng LDL-C. Các bằng chứng gần đây cho thấy bệnh nhân có điểm nguy cơ đa gen LDL-C cao có thể làm gia tăng thêm nguy cơ ngay cả trong nhóm FH đơn gen hoặc xuất hiện ở các bệnh nhân có chẩn đoán lâm sàng FH nhưng xét nghiệm đơn gen âm tính. Việc phối hợp thang điểm nguy cơ đa gen LDL-C và phân tích đơn gen giúp tối ưu hóa chẩn đoán nguyên nhân về cơ chế di truyền, phân tầng nguy cơ, cá thể hóa điều trị theo hướng y học chính xác và tư vấn di truyền cho bệnh nhân và thân nhân. Bài tổng quan này phân tích cơ sở di truyền, bằng chứng lâm sàng và ý nghĩa thực hành của mô hình tích hợp đơn gen và đa gen trong quản lý bệnh nhân nghi ngờ FH.
1. ĐẶT VẤN ĐỀ
Tăng cholesterol máu gia đình là nguyên nhân di truyền thường gặp nhất của bệnh tim mạch với tần suất khoảng 1/220 người và thậm chí phổ biến hơn ở một số chủng tộc và nhóm dân số nhất định [1]. Bệnh đặc trưng bởi tăng LDL-C kéo dài từ giai đoạn sớm của cuộc đời và nguy cơ cao bệnh tim mạch do xơ vữa, đặc biệt là bệnh mạch vành sớm [1-2]. Nếu không điều trị, nam giới mắc FH có nguy cơ biến cố mạch vành lên tới 50% trước 50 tuổi và nữ giới khoảng 30% trước 60 tuổi [1]. Tỉ lệ FH ở những bệnh nhân nhồi máu cơ tim cấp khởi phát sớm ở dân số Việt Nam là 14,7% [3].
Hiện nay, chẩn đoán FH chủ yếu dựa trên tiêu chuẩn lâm sàng như Dutch Lipid Clinic Network (DLCN), Simon Broome hoặc tiêu chuẩn của Tổ Chức Y Tế Thế Giới [4]. Tuy nhiên, các tiêu chuẩn này phụ thuộc vào mức LDL-C, tiền sử gia đình và các dấu hiệu thực thể (u vàng ở gân, vòng giác mạc) nên có thể độ nhạy không cao. Một thách thức lớn trong thực hành là nhóm bệnh nhân có kiểu hình nghi ngờ FH (LDL-C rất cao, tiền sử gia đình bệnh tim mạch sớm) nhưng xét nghiệm đơn gen âm tính (kiểu gen âm tính). Khoảng trống chẩn đoán “kiểu hình dương tính, kiểu gen âm tính” này đặt ra câu hỏi về vai trò của cơ chế di truyền đa gen.
Trong những thập kỷ qua, sự phát triển của nghiên cứu liên quan toàn bộ hệ gen (GWAS) đã xác định nhiều biến thể đơn nucleotide (single nucleotide polymorphisms – SNP) có ảnh hưởng đến nồng độ LDL-C. Từ đó, thang điểm nguy cơ đa gen (Polygenic Risk Score – PRS) ra đời, cho phép định lượng gánh nặng di truyền tích lũy do nhiều biến thể gen làm tăng LDL-C. Việc phối hợp phân tích đơn gen truyền thống với thang điểm nguy cơ đa gen mở ra hướng tiếp cận mới trong chẩn đoán và phân tầng nguy cơ ở bệnh nhân nghi ngờ FH [1]. Mục tiêu của bài tổng quan này là phân tích cơ sở khoa học và giá trị lâm sàng của việc tích hợp thang điểm nguy cơ đa gen LDL-C với phân tích đơn gen ở bệnh nhân nghi ngờ tăng cholesterol máu gia đình.
2. CƠ SỞ DI TRUYỀN CỦA TĂNG CHOLESTEROL MÁU
Tăng cholesterol máu gia đình là một rối loạn di truyền đặc trưng bởi tình trạng tăng LDL-C suốt đời, dẫn đến xơ vữa động mạch tiến triển sớm và tăng nguy cơ bệnh tim mạch do xơ vữa. Về mặt di truyền học, tăng cholesterol máu không phải là một thực thể đồng nhất mà bao gồm một phổ liên tục từ cơ chế đơn gen có tính thấm cao đến cơ chế đa gen tích lũy nhiều biến thể nguy cơ nhỏ. Hiểu rõ nền tảng di truyền này là cơ sở cho việc tích hợp phân tích đơn gen và thang điểm nguy cơ đa gen trong thực hành lâm sàng.
2.1. Cơ chế đơn gen
FH cổ điển bị gây ra bởi các đột biến trong các gen liên quan trực tiếp đến chuyển hóa LDL-C, chủ yếu bao gồm LDLR, APOB và PCSK9. Hơn 90% các đột biến gây FH đã được báo cáo nằm trên gen LDLR; khoảng 5–10% trên gen APOB và <1% trên gen PCSK9 [1]. Hơn 2.000 biến thể khác nhau đã được mô tả trong các gen này, với khoảng 1.000 biến thể đủ bằng chứng để phân loại là “gây bệnh” hoặc “có khả năng gây bệnh” theo hướng dẫn của Trường Môn Di Truyền Y Khoa và Hệ Gen Hoa Kỳ (ACMG).
Gen LDLR mã hóa thụ thể LDL ở bề mặt tế bào gan, có vai trò thu nhận và thanh thải LDL-C khỏi tuần hoàn. Các biến thể gây mất chức năng làm giảm số lượng hoặc chức năng thụ thể LDL, dẫn đến tăng LDL-C máu kéo dài suốt đời. Các biến thể này có thể là đột biến vô nghĩa, sai nghĩa, đột biến vị trí cắt, chèn/xóa nhỏ hoặc tái sắp xếp lớn của DNA. Mức độ nặng của kiểu hình phụ thuộc vào tính chất biến thể: đột biến không có thụ thể thường gây tăng LDL-C cao hơn và nguy cơ bệnh mạch vành sớm hơn so với biến thể khiếm khuyết thụ thể [1]. Gen APOB mã hóa apolipoprotein B-100, thành phần chính của hạt LDL. Các biến thể sai nghĩa trong vùng gắn kết với LDLR (đặc biệt p.Arg3527Gln) làm giảm ái lực giữa LDL và thụ thể, gây giảm thanh thải LDL. Kiểu hình thường nhẹ hơn so với đột biến không có thụ thể LDLR. Gen PCSK9 mã hóa protein PCSK9 điều hòa thoái hóa thụ thể LDL. Các biến thể tăng chức năng làm tăng phân hủy thụ thể LDL, dẫn đến giảm số lượng thụ thể trên bề mặt tế bào gan và tăng LDL-C [1].
FH đồng hợp tử (HoFH) xảy ra khi có hai alen gây bệnh, thường trên gen LDLR. Tần suất HoFH ước tính khoảng 1/200.000 – 1/300.000 dân [1]. Bệnh nhân HoFH có LDL-C rất cao từ thời thơ ấu và có thể xuất hiện xơ vữa động mạch nặng trước 20 tuổi. FH dị hợp tử (HeFH) có tần suất khoảng 1/200 – 1/250 trong dân số chung, cao hơn nhiều so với ước tính trước đây [4].
Kiểu hình FH có thể do các biến thể gây bệnh chưa được phát hiện, biến thể ở các gen khác và/hoặc biến thể ở các gen chưa được khám phá [5]. Các biến thể gây bệnh ở các gen khác cũng có thể gây kiểu hình FH. Tăng cholesterol máu di truyền lặn trên nhiễm sắc thể thường có thể xảy ra do các biến thể gây bệnh ở cả hai alen của LDLRAP1, gen mã hóa protein adaptor 1 của LDLR [6]. Ngoài ra còn có các căn nguyên tiềm tàng khác cho kiểu hình FH. Một biến thể gây bệnh ở gen mã hóa apolipoprotein E, APOE (p.Leu167del), được báo cáo gây kiểu hình trội trên nhiễm sắc thể thường, bao gồm nhồi máu cơ tim sớm, u vàng ở gân, u vàng mí mắt và tăng LDL-C [7]. Các rối loạn lipid máu di truyền Mendel khác có biểu hiện kiểu hình chồng lấp với FH và cần được xem xét. Sitosterolemia (do các biến thể gây bệnh di truyền lặn trên nhiễm sắc thể thường ở gen ABCG5 hoặc ABCG8) có thể biểu hiện với u vàng và tăng cholesterol máu [8]. Thiếu hụt lysosomal acid lipase, do các biến thể gây bệnh lặn trên nhiễm sắc thể thường ở gen LIPA, cũng có thể biểu hiện với tăng LDL-C, thường kèm theo bệnh gan nhiễm mỡ [9]. Ngoài ra, tăng lipoprotein (a) cao, do yếu tố di truyền tại gen LPA, cũng có thể góp phần tạo kiểu hình tương tự FH và làm tăng nguy cơ tim mạch độc lập, cần được xem xét trong đánh giá toàn diện [1]. Tuy nhiên, tỷ lệ phát hiện đột biến đơn gen gây bệnh trong nhóm được chẩn đoán lâm sàng chắc chắn FH dao động khoảng 60–80%, còn ở nhóm có thể FH thấp hơn đáng kể (khoảng 21–44%) [1]. Điều này phản ánh sự tồn tại của các cơ chế di truyền khác như đa gen ngoài đơn gen cổ điển.
2.2. Cơ chế đa gen
Không phải tất cả bệnh nhân có kiểu hình FH (LDL-C cao, tiền sử gia đình) đều mang biến thể gây bệnh trên gen LDLR, APOB hoặc PCSK9. Nghiên cứu GWAS quy mô lớn đã xác định hàng trăm đến hàng nghìn biến thể đơn nucleotide phổ biến có tác động nhỏ nhưng tích lũy lên mức LDL-C huyết tương [5]. Sự kết hợp của nhiều SNP tăng LDL-C có thể tạo nên kiểu hình tăng LDL-C đáng kể, được gọi là tăng cholesterol máu do đa gen. Martin-Campos JM và cộng sự nhấn mạnh rằng phần lớn tính di truyền chưa được đánh giá (missing heritability) của LDL-C có thể được giải thích bởi cơ chế đa gen thay vì các đột biến hiếm có tác động lớn [5].
Khái niệm thang điểm nguy cơ đa gen LDL-C được xây dựng bằng cách cộng có trọng số các alen nguy cơ của nhiều SNP liên quan đến LDL-C. Mỗi SNP đóng góp một phần nhỏ vào tăng LDL-C; khi tích lũy đủ số lượng, tổng hiệu ứng có thể tương đương hoặc gần tương đương với FH dị hợp tử nhẹ. Dữ liệu từ các nghiên cứu đa sắc tộc trên hơn 300.000 cá thể đã xác nhận vai trò rộng rãi của các biến thể phổ biến trong điều hòa lipid máu và sự khác biệt về tần suất theo chủng tộc [10]. Điều quan trọng là cơ chế đơn gen và đa gen không loại trừ lẫn nhau mà có thể tương tác. Một bệnh nhân mang biến thể LDLR gây bệnh đồng thời có điểm nguy cơ đa gen cao có thể có nồng độ LDL-C cao hơn và nguy cơ tim mạch lớn hơn so với người chỉ mang một trong hai yếu tố. Ngược lại, điểm nguy cơ đa gen thấp có thể làm nhẹ biểu hiện kiểu hình của đột biến đơn gen. Mô hình tích hợp đột biến đơn gen và nguy cơ đa gen phản ánh tốt hơn phổ nguy cơ tim mạch trong dân số [11]. Từ góc độ sinh học phân tử, FH và tăng điểm nguy cơ đa gen LDL-C di truyền không nên được xem là hai thực thể tách biệt mà là một phổ liên tục. Ở một đầu phổ là các đột biến hiếm, tác động lớn với tính thấm cao và nguy cơ bệnh tim mạch do xơ vữa sớm; ở đầu kia là tích lũy nhiều biến thể phổ biến có hiệu ứng nhỏ. Giữa hai cực này là nhiều kiểu hình trung gian, trong đó đơn gen và đa gen có thể cùng tồn tại. Sự hiểu biết về cơ sở di truyền này là nền tảng để ứng dụng phối hợp phân tích đơn gen truyền thống và thang điểm nguy cơ đa gen trong tiếp cận bệnh nhân nghi ngờ tăng cholesterol máu gia đình, hướng tới y học chính xác trong quản lý bệnh nhân rối loạn lipid máu.
3. THANG ĐIỂM NGUY CƠ ĐA GEN LDL-C
Sự phát triển của các nghiên cứu di truyền học quần thể trong những thập kỷ qua đã làm thay đổi căn bản cách tiếp cận tăng cholesterol máu. Nếu trước đây trọng tâm chủ yếu đặt vào các đột biến hiếm có hiệu ứng lớn (các đột biến đơn gen), thì các nghiên cứu GWAS đã chứng minh rằng nồng độ LDL-C trong dân số chịu ảnh hưởng đồng thời của hàng trăm đến hàng nghìn biến thể phổ biến có hiệu ứng nhỏ nhưng cộng gộp lại tạo thành tác động sinh học đáng kể [1]. Từ nền tảng đó, thang điểm nguy cơ đa gen LDL-C đã được xây dựng nhằm định lượng khuynh hướng di truyền tích lũy đối với tăng nồng độ LDL-C ở từng cá thể.
3.1. Nguyên lý xây dựng thang điểm nguy cơ đa gen
Nguyên lý cốt lõi của thang điểm nguy cơ đa gen là tổng hợp ảnh hưởng của nhiều biến thể đơn nucleotide liên quan đến LDL-C thành một chỉ số duy nhất phản ánh gánh nặng di truyền. Các SNP này được xác định thông qua nghiên cứu GWAS quy mô lớn, tiêu biểu như Global Lipids Genetics Consortium và UK Biobank với hàng trăm nghìn cá thể tham gia [1],[5].
Quy trình xây dựng thang điểm nguy cơ đa gen bao gồm ba bước chính. Thứ nhất, lựa chọn biến thể gen SNP dựa trên ngưỡng ý nghĩa thống kê (thường p < 5×10⁻⁸) và loại bỏ các SNP có tương quan liên kết cao nhằm tránh trùng lặp tín hiệu. Một số thang điểm nguy cơ đa gen chỉ sử dụng vài chục SNP mạnh nhất trong khi các mô hình thế hệ mới có thể tích hợp hàng triệu SNP với phương pháp hiệu chỉnh Bayes.
Thứ hai, mỗi SNP được gán một trọng số (hệ số beta) phản ánh mức thay đổi LDL-C tương ứng với mỗi alen nguy cơ, ước tính từ mô hình hồi quy trong GWAS. Thang điểm nguy cơ đa gen được tính bằng tổng có trọng số của số alen nguy cơ mà cá thể mang tại mỗi locus:
PRS = Σ (βᵢ × số alen nguy cơ tại SNPᵢ)
Cách tiếp cận này tạo thành một thang điểm cho phép định lượng xu hướng tăng LDL-C dựa trên toàn bộ nền tảng di truyền phổ biến của cá thể.
Thứ ba, điểm nguy cơ đa gen được chuẩn hóa theo phân bố trong quần thể tham chiếu và phân tầng theo phân vị. Martin-Campos JM và cộng sự nhấn mạnh rằng thang điểm nguy cơ đa gen phản ánh phần lớn tính di truyền chưa được đánh giá trong tăng LDL-C tức là phần di truyền không được giải thích bởi các đột biến hiếm có tác động lớn [5]. Hội Tim Hoa Kỳ cũng khẳng định thang điểm nguy cơ đa gen đại diện cho bước tiến quan trọng trong phân tầng nguy cơ tim mạch dựa trên nền tảng di truyền toàn bộ hệ gen [11].
3.2. Giá trị chẩn đoán của thang điểm nguy cơ đa gen LDL-C
Các biến thể di truyền thường gặp khi được cộng gộp thành thang điểm nguy cơ đa gen có thể dự đoán nồng độ lipid. Ví dụ, nhóm trên bách phân vị thứ 95 của thang điểm nguy cơ đa gen LDL-C có mức tăng LDL-C (≈ 30 mg/dL) tương đương với những người mang đột biến gen gây tăng cholesterol máu gia đình (FH) ở người gốc châu Âu. Trong số các cá nhân bị tăng cholesterol máu nặng, khoảng 2% mang biến thể FH đơn gen trong khi 23% thuộc nhóm trên bách phân vị thứ 95 của thang điểm nguy cơ đa gen LDL-C [12]. Ngoài ra, thang điểm nguy cơ đa gen LDL-C còn giải thích một phần biến thiên nồng độ LDL-C ở những người mang biến thể FH [13].
Trong thực hành lâm sàng, một vấn đề thường gặp là bệnh nhân có LDL-C ≥ 190 mg/dL và tiền sử gia đình dương tính nhưng không phát hiện được đột biến gen LDLR, APOB hay PCSK9. Nhóm bệnh nhân này thường được mô tả là “kiểu hình FH nhưng kiểu gen âm tính”. Thang điểm nguy cơ đa gen đóng vai trò đặc biệt quan trọng trong việc giải thích cơ chế sinh bệnh ở nhóm này. Talmud P và cộng sự tuyển chọn những bệnh nhân FH tại Vương quốc Anh và so sánh với nhóm chứng khỏe mạnh từ nghiên cứu Whitehall II (WHII) tại Anh và thẩm định trên một nhóm bệnh nhân tại phòng khám Lipid ở Bỉ (Hôpital de Jolimont, Haine St-Paul, Bỉ) [14]. Những người tham gia được xác định kiểu gen đối với 12 alen phổ biến làm tăng LDL-C đã được xác định bởi Global Lipid Genetics Consortium, và một thang điểm nguy cơ đa gen có trọng số làm tăng LDL-C được xây dựng. Phân bố thang điểm đa gen được so sánh giữa các bệnh nhân FH không xác định được đột biến, các bệnh nhân có đột biến đã xác định, và nhóm chứng từ WHII. Nghiên cứu này chọn được 321 bệnh nhân Vương quốc Anh không có đột biến (451 bệnh nhân Bỉ), 319 bệnh nhân Vương quốc Anh có đột biến (273 bệnh nhân Bỉ), và 3.020 đối tượng chứng từ WHII. Giá trị trung bình của điểm nguy cơ đa gen LDL-C có trọng số ở nhóm WHII (0,90 [SD 0,23]) có liên quan mạnh với nồng độ LDL-C (p = 1,4 × 10⁻⁷⁷; R² = 0,11). Bệnh nhân Vương quốc Anh không có đột biến đơn gen có điểm nguy cơ đa gen LDL-C trung bình cao hơn có ý nghĩa (1,0 [SD 0,21]) so với nhóm chứng WHII (p = 4,5 × 10⁻¹⁶), tương tự ở nhóm bệnh nhân Bỉ không có đột biến đơn gen (0,99 [0,19]; p = 5,2 × 10⁻²⁰). Điểm nguy cơ đa gen cũng cao hơn ở nhóm bệnh nhân có đột biến tại Vương quốc Anh (0,95 [0,20]; p = 1,6 × 10⁻⁵) và Bỉ (0,92 [0,20]; p = 0,04) so với nhóm chứng WHII. 167/321 (52%) bệnh nhân Vương quốc Anh không có đột biến đơn gen nằm trong ba thập phân vị cao nhất của phân bố thang điểm nguy cơ đa gen LDL-C của WHII, trong khi chỉ 35 bệnh nhân (11%) thuộc ba thập phân vị thấp nhất. Talmud P và cộng sự đã chứng minh rằng một tỷ lệ đáng kể bệnh nhân được chẩn đoán lâm sàng FH nhưng không phát hiện đột biến đơn gen có điểm nguy cơ đa gen cao hơn so với dân số chung, ủng hộ giả thuyết tăng LDL-C do đa gen [12]. Điều này chứng minh rằng cơ chế đa gen có thể tạo nên kiểu hình tăng LDL-C nghiêm trọng tương tự FH dị hợp tử nhẹ. Như vậy, thang điểm nguy cơ đa gen giúp phân biệt giữa tăng LDL-C do đột biến đơn gen (FH) và tăng LDL-C do tích lũy đa gen (tăng cholesterol máu do đa gen). Sự phân biệt này có ý nghĩa không chỉ về mặt sinh học mà còn về tư vấn di truyền. Trong khi FH do đơn gen mang nguy cơ di truyền 50% cho thân nhân bậc một, tăng LDL-C do đa gen không tuân theo mô hình Mendel rõ ràng và nguy cơ ở thân nhân phụ thuộc vào phân bố alen trong gia đình. Ngoài ra, thang điểm nguy cơ đa gen còn có thể hỗ trợ diễn giải các biến thể chưa rõ ý nghĩa (Variant of Uncertain Significance). Nếu bệnh nhân mang biến thể chưa rõ ý nghĩa nhưng có điểm nguy cơ đa gen cao, khả năng cơ chế đa gen chiếm ưu thế có thể được xem xét; ngược lại, điểm nguy cơ đa gen thấp gợi ý vai trò lớn hơn của biến thể hiếm.
Thang điểm nguy cơ đa gen LDL-C cũng được ghi nhận liên quan đến nguy cơ các bệnh tim mạch khác như hẹp van động mạch chủ, phình động mạch chủ bụng, bệnh động mạch ngoại biên và huyết khối tĩnh mạch. Tuy nhiên, khả năng tiên lượng độc lập với LDL-C đo được cho các bệnh lý này vẫn chưa được nghiên cứu đầy đủ [11].
3.3. Giá trị tiên lượng của thang điểm nguy cơ đa gen LDL-C
Bên cạnh giá trị chẩn đoán, thang điểm nguy cơ đa gen còn có ý nghĩa tiên lượng tim mạch độc lập. Trinder M và cộng sự phân tích nguy cơ bệnh tim mạch sớm (cơn đau thắt ngực không ổn định, nhồi máu cơ tim, tái thông mạch vành hoặc đột quỵ ở tuổi < 55) ở dân số sổ bộ British Columbia FH có chẩn đoán lâm sàng nghi ngờ, có thể hoặc chắc chắn FH theo tiêu chuẩn DLCN và phát hiện rằng mang đột biến đơn gen gây FH làm tăng nguy cơ đáng kể so với tăng LDL-C do đa gen ở cùng mức LDL-C [15]. Quan trọng hơn, khi điểm nguy cơ đa gen cao kết hợp với đột biến đơn gen, nguy cơ tim mạch tăng mạnh khoảng 3 lần (tỉ số nguy hại HR hiệu chỉnh: 3,06; khoảng tin cậy 95%: 1,56–5,99; p = 0,001) so với nhóm tham chiếu gồm các bệnh nhân không có điểm nguy cơ đa gen LDL-C tăng và cũng không mang đột biến đơn gen (Hình 1) [15]. Điều này chứng minh sự tương tác cộng gộp giữa cơ chế đơn gen và đa gen, củng cố quan điểm rằng FH và tăng LDL-C do đa gen tồn tại trên một phổ liên tục, chứ không phải hai thực thể tách biệt.
Một nghiên cứu khác của Trinder M và cs trên gần 49.000 cá thể từ 40 đến 69 tuổi được tuyển chọn từ UK Biobank trên toàn Vương quốc Anh trong giai đoạn từ ngày 13 tháng 3 năm 2006 đến ngày 1 tháng 10 năm 2010 và được theo dõi đến ngày 31 tháng 3 năm 2017 [16]. Dữ liệu kiểu gen và giải trình tự exome từ đoàn hệ UK Biobank được sử dụng để xác định các cá thể bị tăng cholesterol máu do đơn gen (LDLR, APOB và PCSK9) hoặc tăng cholesterol máu do đa gen (thang điểm nguy cơ đa gen LDL-C > bách phân vị thứ 95 dựa trên 223 biến thể đơn nucleotide trong toàn bộ đoàn hệ). Các cá thể với nguồn gốc tổ tiên khác nhau có sự khác biệt đáng kể trong phân bố thang điểm nguy cơ đa gen LDL-C (Hình 2A). Thang điểm nguy cơ đa gen LDL-C có mối liên quan rõ rệt với mức LDL-C nền ở các cá thể có nguồn gốc châu Phi (multiple R² = 0,04; β [SE] = 17,40 [1,91]; P < 0,001) (n = 4.680), Đông Á (multiple R² = 0,06; β [SE] = 21,73 [1,25]; P < 0,001) (n = 10.640), và châu Âu (multiple R² = 0,09; β [SE] = 28,01 [0,18]; P < 0,001) (n = 439.871) (Hình 2B). Sự gia tăng bách phân vị của thang điểm nguy cơ đa gen LDL-C có liên quan với sự gia tăng nguy cơ bệnh tim mạch theo kiểu phụ thuộc liều lượng trong toàn bộ đoàn hệ (kiểm định xu hướng, P < 0,001) (Hình 2C). Cụ thể, nhóm thập phân vị thứ 10 của thang điểm đa gen LDL-C có nguy cơ bệnh tim mạch cao nhất so với nhóm thập phân vị thứ nhất (HR hiệu chỉnh [aHR] 1,35; KTC 95%: 1,30–1,40; P < 0,001). Nghiên cứu này đánh giá mối liên quan giữa kiểu gen với nguy cơ tái thông mạch vành và động mạch cảnh, nhồi máu cơ tim, đột quỵ thiếu máu cục bộ và tử vong do mọi nguyên nhân trong toàn bộ quần thể nghiên cứu cũng như ở các nhóm tham gia có FH do đơn gen (n = 277), tăng cholesterol máu do đa gen (n = 2379) hoặc tăng cholesterol máu chưa xác định nguyên nhân (n = 2232) tại các mức LDL-C tương đương được đo tại thời điểm tuyển chọn. Trong số 48.741 cá thể có dữ liệu kiểu gen và giải trình tự exome, tuổi trung bình (độ lệch chuẩn) là 56,6 (8,0) tuổi và 54,5% là nữ (26.541/48.741). Đột biến đơn gen gây FH được phát hiện ở 277 cá thể (0,57%, tương đương 1/176 người). Những người mang đơn gen FH có nguy cơ cao hơn trải qua một biến cố bệnh tim mạch do xơ vữa ở tuổi ≤55 so với những người không mang đột biến đơn gen FH (17/277 [6,1%] so với 988/48.464 [2,0%]; P < 0,001). So với dân số chung, cả tăng cholesterol máu do đơn gen và đa gen đều liên quan với nguy cơ gia tăng các biến cố tim mạch. Hơn nữa, trong nhóm có mức LDL-C tương đương, cả tăng cholesterol máu do đơn gen (HR 1,93; KTC 95%: 1,34–2,77; P < 0,001) và đa gen (HR 1,26; KTC 95%: 1,03–1,55; P = 0,03) đều liên quan có ý nghĩa với nguy cơ tăng các biến cố tim mạch so với nhóm tăng cholesterol máu không xác định được nguyên nhân di truyền [16].
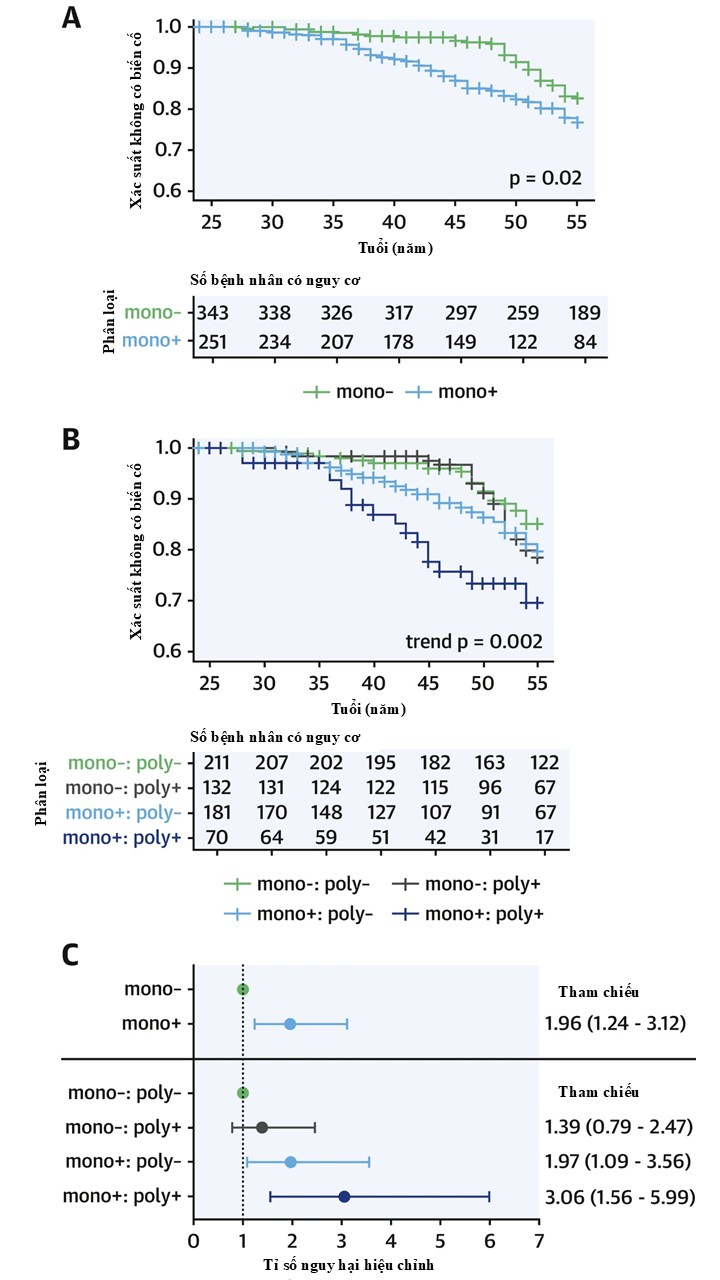
Hình 1. Ảnh hưởng của kiểu gen đối với biến cố tim mạch sớm ở bệnh nhân có chẩn đoán lâm sàng nghi ngờ, có thể hoặc chắc chắn FH [15].
Phân tích thời gian đến biến cố đầu tiên đối với các biến cố tim mạch sớm (tuổi ≤ 55) gồm đau thắt ngực không ổn định, nhồi máu cơ tim, tái thông mạch vành và đột quỵ, được thực hiện trên toàn bộ dân số sổ bộ FH British Columbia (n = 626) [13]. Bệnh nhân được phân tầng dựa trên: (A) tình trạng có hoặc không có đột biến đơn gen gây FH; (B) trong nhóm mang đột biến đơn gen và nhóm có thang điểm nguy cơ đa gen LDL-C tăng cao, sử dụng thiết kế giai thừa 2×2; và (C) tỷ số nguy hại kèm khoảng tin cậy 95% cho biến cố tim mạch sớm được hiệu chỉnh theo tuổi, giới tính, LDL-C, đái tháo đường và tăng huyết áp. mono = đột biến đơn gen gây tăng cholesterol máu gia đình; poly = thang điểm nguy cơ đa gen LDL-C ≥ bách phân vị 80.
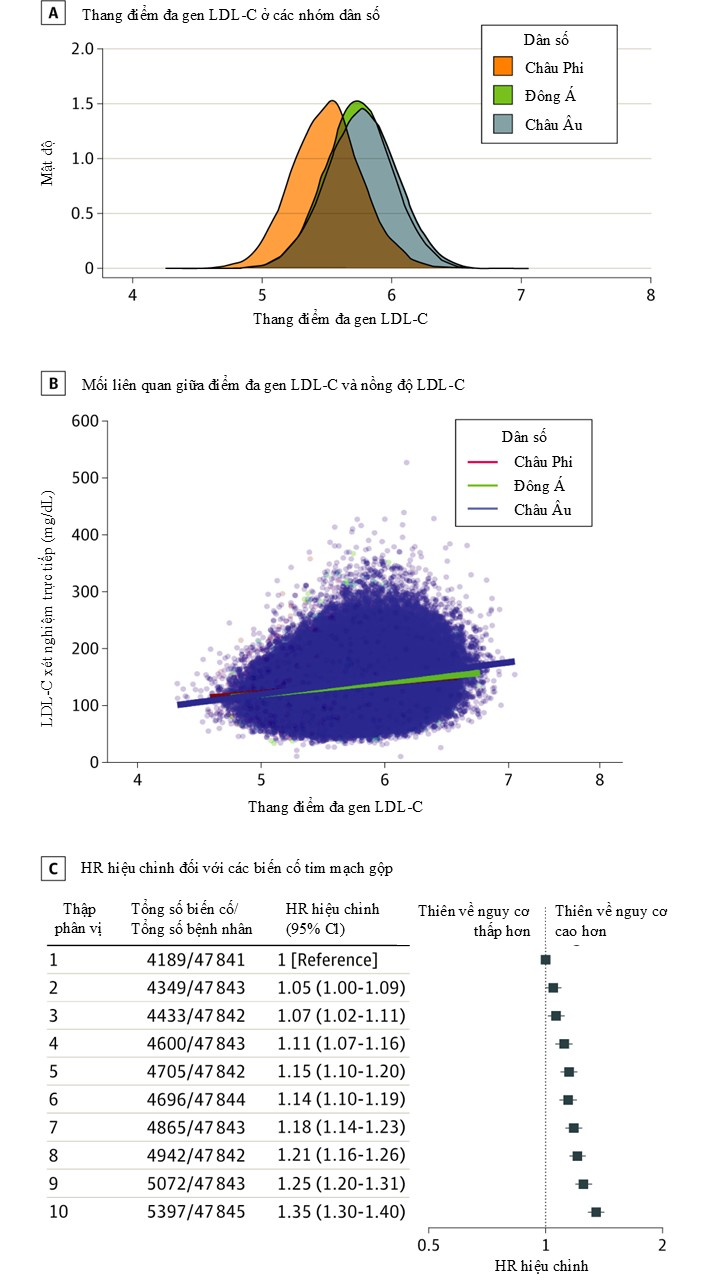
Hình 2. Thang điểm nguy cơ đa gen LDL-C và nồng độ LDL-C với nguy cơ bệnh tim mạch trong dân số UK Biobank [16].
(A) Phân bố thang điểm nguy cơ đa gen LDL-C được trình bày theo các nhóm nguồn gốc di truyền châu Phi, Đông Á và châu Âu. (B) Mối liên quan tuyến tính giữa thang điểm nguy cơ đa gen LDL-C và mức LDL-C. (C) Tỉ số nguy hại hiệu chỉnh (aHR) kèm khoảng tin cậy 95% đối với biến cố tim mạch gộp gồm nhồi máu cơ tim, tái thông mạch vành hoặc động mạch cảnh, đột quỵ thiếu máu cục bộ hoặc tử vong do mọi nguyên nhân được trình bày cho từng thập phân vị của bách phân vị thang điểm nguy cơ đa gen LDL-C. Tỉ số nguy hại đã được hiệu chỉnh theo tuổi, giới tính, kiểu gen và/hoặc lô xét nghiệm, cùng với nguồn gốc di truyền.
Từ góc độ lâm sàng, giá trị tiên lượng của thang điểm nguy cơ đa gen có ý nghĩa trong cả dự phòng tiên phát và thứ phát. Ở những cá thể trẻ chưa có bệnh tim mạch do xơ vữa nhưng thuộc nhóm điểm nguy cơ đa gen cao, can thiệp sớm bằng thay đổi lối sống hoặc statin có thể làm giảm đáng kể nguy cơ tích lũy. Ở bệnh nhân đã có bệnh tim mạch do xơ vữa, điểm nguy cơ đa gen cao có thể xác định nhóm nguy cơ rất cao cần mục tiêu LDL-C thấp hơn và liệu pháp tích cực hơn (statin hoạt lực cao, ezetimibe, ức chế PCSK9). Hội Tim Hoa Kỳ nhấn mạnh rằng thang điểm nguy cơ đa gen có thể bổ sung cho các mô hình dự báo nguy cơ truyền thống, nhưng cần thận trọng khi áp dụng ở các quần thể ngoài châu Âu do khác biệt về cấu trúc di truyền [11].
4. ỨNG DỤNG PHỐI HỢP THANG ĐIỂM NGUY CƠ ĐA GEN LDL-C VÀ PHÂN TÍCH ĐƠN GEN Ở BỆNH NHÂN NGHI NGỜ TĂNG CHOLESTEROL MÁU GIA ĐÌNH
4.1. Mô hình tích hợp phân tích đơn gen và đa gen
Phân tích đơn gen đóng vai trò nền tảng trong chẩn đoán FH, đặc biệt trong việc xác nhận các trường hợp mang đột biến gây bệnh trên gen LDLR, APOB hoặc PCSK9 và triển khai sàng lọc theo phả hệ (cascade screening) cho thân nhân. Tuy nhiên, nhiều dữ liệu cho thấy cách tiếp cận này chưa đủ để giải thích toàn bộ phổ kiểu hình tăng LDL-C trong thực hành lâm sàng. Tỷ lệ phát hiện biến thể gây bệnh ở nhóm chắc chắn FH chỉ đạt khoảng 60–80%, và giảm đáng kể ở nhóm có thể FH [1]. Điều này đồng nghĩa với việc một tỷ lệ đáng kể bệnh nhân có biểu hiện lâm sàng rất điển hình của FH nhưng không phát hiện được đột biến đơn gen bằng các phương pháp hiện tại.
Sự phát triển của thang điểm nguy cơ đa gen tăng cholesterol máu đã mở ra khả năng tích hợp giữa phân tích đột biến hiếm có hiệu ứng lớn và nền tảng đa gen phổ biến có hiệu ứng nhỏ. FH nên được xem như một phổ liên tục giữa cơ chế đơn gen và đa gen thay vì một thực thể nhị nguyên “có hoặc không có đột biến” [1]. Trong mô hình tích hợp này, mỗi bệnh nhân nghi ngờ FH được đánh giá đồng thời về sự hiện diện của đột biến đơn gen gây bệnh và thang điểm nguy cơ đa gen.
4.2. Tiềm năng ứng dụng lâm sàng
Việc tích hợp thang điểm nguy cơ đa gen LDL-C vào đánh giá bệnh nhân nghi ngờ FH có nhiều ứng dụng lâm sàng quan trọng. Trước hết, thang điểm nguy cơ đa gen giúp chẩn đoán nguyên nhân về cơ chế di truyền ở các bệnh nhân tăng cholesterol máu, tinh chỉnh phân tầng nguy cơ tim mạch vượt ra ngoài mức LDL-C tuyệt đối (Hình 3) [1]. Thang điểm nguy cơ đa gen có thể cải thiện dự báo nguy cơ tim mạch độc lập với các yếu tố truyền thống, đặc biệt ở những cá thể có LDL-C cao từ sớm trong đời. Điều này có ý nghĩa khi đánh giá bệnh nhân trẻ tuổi có tiền sử gia đình bệnh mạch vành sớm nhưng không phát hiện đột biến đơn gen.
Thứ hai, thang điểm nguy cơ đa gen hỗ trợ cá thể hóa mục tiêu điều trị LDL-C. Theo khuyến cáo của Hội Tim Châu Âu/Hội Xơ Vữa Động Mạch Châu Âu (ESC/EAS) 2019, mục tiêu LDL-C phụ thuộc vào phân tầng nguy cơ tim mạch tổng thể [4]. Trong tương lai gần, bệnh nhân FH mang đột biến đơn gen kết hợp điểm nguy cơ đa gen cao có thể được xem là nhóm nguy cơ rất cao, cần mục tiêu LDL-C thấp hơn và chiến lược điều trị tích cực hơn, bao gồm statin hoạt lực cao, phối hợp ezetimibe và sớm cân nhắc ức chế PCSK9. Ngược lại, ở bệnh nhân tăng LDL-C với điểm nguy cơ đa gen cao nhưng không có đột biến đơn gen, chiến lược điều trị có thể được điều chỉnh dựa trên nguy cơ toàn diện thay vì mô hình di truyền Mendel.
Thứ ba, thang điểm nguy cơ đa gen có thể có vai trò trong hướng dẫn điều trị hạ lipid máu. Điểm nguy cơ đa gen cao liên quan với nguy cơ bệnh mạch vành tăng đáng kể, ngay cả khi không có đột biến đơn gen, và hiệu ứng này độc lập với nồng độ LDL-C. Điều này cho thấy thang điểm nguy cơ đa gen có thể giúp xác định nhóm bệnh nhân cần can thiệp sớm hơn, ngay cả khi mức LDL-C chưa đạt ngưỡng chẩn đoán FH cổ điển. Thang điểm nguy cơ đa gen có vai trò thiết lập kế hoạch quản lý sớm hơn và tăng liều sớm hơn các liệu pháp hạ lipid tương tự như FH theo tuyên bố khoa học của Hội Tim Hoa Kỳ vào năm 2022 [11].
Thứ tư, việc phối hợp giữa phân tích đơn gen và đa gen có ý nghĩa trong tư vấn di truyền cho bệnh nhân và thân nhân. FH do đơn gen mang đặc điểm di truyền trội nhiễm sắc thể thường với nguy cơ 50% cho thân nhân bậc một, trong khi tăng LDL-C do đa gen không tuân theo quy luật Mendel đơn giản. Do đó, việc tích hợp thang điểm nguy cơ đa gen giúp tránh gán nhãn FH do đơn gen không cần thiết cho gia đình bệnh nhân kiểu gen âm tính. Ở bệnh nhân mang đột biến đơn gen nhưng điểm nguy cơ đa gen thấp, sự hiện diện của nền tảng đa gen thuận lợi có thể giải thích mức LDL-C thấp hơn dự kiến và tiên lượng thuận lợi hơn. Ngược lại, điểm nguy cơ đa gen cao ở bệnh nhân kiểu gen âm tính giúp giải thích cơ chế tăng LDL-C và giảm bớt lo âu liên quan đến việc không tìm thấy đột biến trong bối cảnh lâm sàng rất điển hình [1].
Như vậy, phối hợp thang điểm nguy cơ đa gen tăng cholesterol máu với phân tích đơn gen giúp chuyển đổi cách tiếp cận FH từ mô hình chẩn đoán nhị nguyên sang đánh giá nguy cơ tích hợp, phản ánh chính xác hơn bản chất phổ liên tục của di truyền lipid máu. Đây là bước tiến quan trọng hướng tới cá thể hóa điều trị rối loạn lipid máu dựa trên nền tảng di truyền toàn diện.
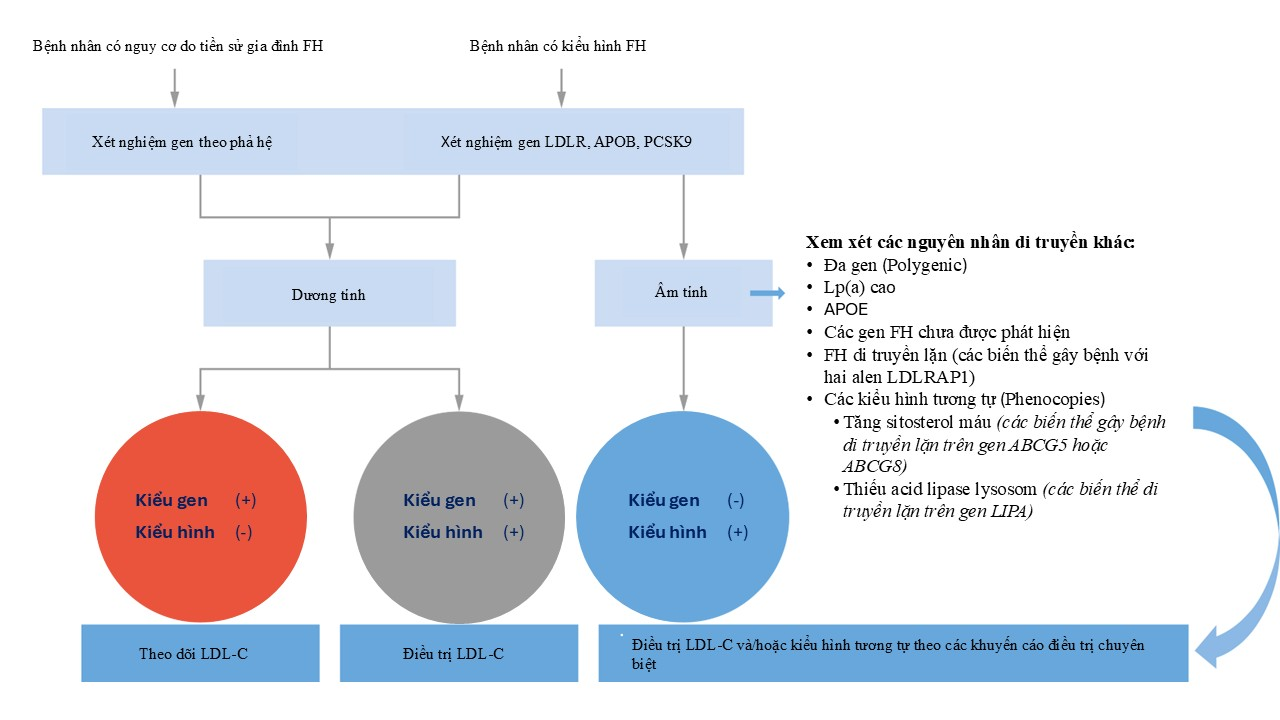
Hình 3. Xét nghiệm gen ở bệnh nhân nghi ngờ tăng choleseterol máu gia đình [1]
5. KẾT LUẬN
Tăng cholesterol máu gia đình là một tình trạng di truyền phổ biến nhưng còn chưa được chẩn đoán đầy đủ, với nguy cơ cao gây bệnh tim mạch do xơ vữa sớm và tử vong do tim mạch nếu không được điều trị kịp thời. Trong nhiều năm, cách tiếp cận chẩn đoán và quản lý FH chủ yếu dựa trên tiêu chuẩn lâm sàng kết hợp phân tích đột biến đơn gen. Tuy nhiên, những tiến bộ trong di truyền học quần thể đã cho thấy rằng tăng LDL-C tồn tại trên một phổ liên tục giữa cơ chế đơn gen và đa gen, trong đó nhiều bệnh nhân mang kiểu hình điển hình nhưng không phát hiện được đột biến gây bệnh xác định. Thang điểm nguy cơ đa gen LDL-C cung cấp một công cụ định lượng gánh nặng di truyền tích lũy, giúp giải thích các trường hợp kiểu hình dương tính nhưng kiểu gen âm tính, đồng thời tinh chỉnh phân tầng nguy cơ tim mạch ở bệnh nhân đã xác định có đột biến đơn gen. Khi phối hợp thang điểm nguy cơ đa gen với phân tích đơn gen truyền thống, khả năng chẩn đoán chính xác được cải thiện, nguy cơ tim mạch được đánh giá toàn diện hơn và chiến lược điều trị có thể được cá thể hóa theo nền tảng di truyền riêng biệt của từng bệnh nhân. Sự tích hợp này đại diện cho một bước tiến quan trọng trong thời đại y học chính xác, trong đó quyết định lâm sàng không chỉ dựa trên mức LDL-C tuyệt đối mà còn phản ánh bối cảnh di truyền phức tạp. Trong tương lai, với sự phát triển của công nghệ giải trình tự, dữ liệu di truyền đa sắc tộc và các nghiên cứu can thiệp tiến cứu, mô hình tích hợp này có tiềm năng trở thành tiêu chuẩn thực hành mới trong đánh giá và điều trị rối loạn lipid máu di truyền.
TÀI LIỆU THAM KHẢO
- Sturm AC, Knowles JW, Gidding SS, et al. Clinical Genetic Testing for Familial Hypercholesterolemia: JACC Scientific Expert Panel. J Am Coll Cardiol. 2018;72(6):662-680. doi: 10.1016/j.jacc.2018.05.044.
- Nguyen KM, Hoang SV, Nguyen TN, et al. Complex Coronary Artery Lesions in a Young Woman With an Acute Myocardial Infarction and Genetically Confirmed Familial Hypercholesterolemia: A Case Report and Literature Review From a Developing Country. Cureus. 2024 Aug 30;16(8):e68212. doi: 10.7759/cureus.68212.
- Nguyen KM, Hoang SV. Prevalence of genetically diagnosed familial hypercholesterolemia in Vietnamese patients with premature acute myocardial infarction. Medicine (Baltimore). 2024 Sep 27;103(39):e39939. doi: 10.1097/MD.0000000000039939.
- Mach F, Baigent C, Catapano AL, et al. 2019 ESC/EAS Guidelines for the management of dyslipidaemias: lipid modification to reduce cardiovascular risk. Eur Heart J. 2020;41(1):111-188. doi: 10.1093/eurheartj/ehz455.
- Martín-Campos JM. Genetic Determinants of Plasma Low-Density Lipoprotein Cholesterol Levels: Monogenicity, Polygenicity, and “Missing” Heritability. Biomedicines. 2021;9(11):1728. doi: 10.3390/biomedicines9111728.
- D’Erasmo L, Minicocci I, Nicolucci A, et al. Autosomal recessive hypercholesterolemia: long-term cardiovascular outcomes. J Am Coll Cardiol 2018;71:279–88.
- Awan Z, Choi HY, Stitziel N, et al. APOE p. Leu167del mutation in familial hypercholester olemia. Atherosclerosis 2013;231:218–22.
- Berge KE, Tian H, Graf GA, et al. Accumula tion of dietary cholesterol in sitosterolemia caused by mutations in adjacent ABC transporters. Sci ence 2000;290:1771–5.
- Chora JR, Alves AC, Medeiros AM, et al. Lysosomal acid lipase deficiency: a hidden disease among cohorts of familial hypercholesterolemia? J Clin Lipidol 2017;11:477–84.e2.
- Klarin D, Damrauer SM, Cho K, et al. Genetics of blood lipids among ~300,000 multi-ethnic participants of the Million Veteran Program. Nat Genet. 2018;50(11):1514-1523. doi: 10.1038/s41588-018-0222-9.
- O’Sullivan JW, Raghavan S, Marquez-Luna C, et al. Polygenic Risk Scores for Cardiovascular Disease: A Scientific Statement From the American Heart Association. Circulation. 2022;146(8):e93-e118. doi: 10.1161/CIR.0000000000001077.
- Natarajan P, Peloso GM, Zekavat SM, et al. Deep-coverage whole genome sequences and blood lipids among 16,324 individuals. Nat Commun. 2018;9(1):3391. doi: 10.1038/s41467-018-05747-8.
- Oetjens MT, Kelly MA, Sturm AC, et al. Quantifying the polygenic contribution to variable expressivity in eleven rare genetic disorders. Nat Commun. 2019;10(1):4897. doi: 10.1038/s41467-019-12869-0.
- Talmud PJ, Shah S, Whittall R, et al. Use of low-density lipoprotein cholesterol gene score to distinguish patients with polygenic and monogenic familial hypercholesterolaemia: a case-control study. Lancet. 2013;381(9874):1293-301. doi: 10.1016/S0140-6736(12)62127-8.
- Trinder M, Li X, DeCastro ML, et al. Risk of Premature Atherosclerotic Disease in Patients With Monogenic Versus Polygenic Familial Hypercholesterolemia. J Am Coll Cardiol. 2019;74(4):512-522. doi: 10.1016/j.jacc.2019.05.043.
- Trinder M, Francis GA, Brunham LR. Association of Monogenic vs Polygenic Hypercholesterolemia With Risk of Atherosclerotic Cardiovascular Disease. JAMA Cardiol. 2020;5(4):390-399. doi: 10.1001/jamacardio.2019.5954.







