Cơ chế bệnh sinh của hội chứng mạch vành cấp là sự tạo lập huyết khối gây tắc động mạch vành. Huyết khối trong động mạch vành ban đầu được tạo nên từ khối tiểu cầu kết tập lại, sau đó có sự hình thành mạng fibrin chồng lên trên.
TS.BS. Hồ Huỳnh Quang Trí
Viện Tim TP.HCM
Cơ chế bệnh sinh của hội chứng mạch vành cấp là sự tạo lập huyết khối gây tắc động mạch vành. Huyết khối trong động mạch vành ban đầu được tạo nên từ khối tiểu cầu kết tập lại, sau đó có sự hình thành mạng fibrin chồng lên trên. Xuất phát từ cơ chế bệnh sinh này, điều trị chống huyết khối trong hội chứng mạch vành cấp bao gồm 2 thành phần là điều trị chống tiểu cầu và điều trị chống đông (chống lại sự hình thành mạng fibrin). Trong thời gian gần đây, cả 2 thành phần của liệu pháp chống huyết khối đã đạt nhiều tiến bộ quan trọng. Trong điều trị chống tiểu cầu, 2 thuốc mới có hiệu quả cao đã được chấp thuận cho sử dụng trong lâm sàng là ticagrelor và prasugrel 1,2. Trong điều trị chống đông, bên cạnh các thuốc cổ điển là heparin không phân đoạn (KPĐ) và heparin trọng lượng phân tử thấp (TLPTT), đã có thêm một số thuốc được chấp thuận dùng cho bệnh nhân hội chứng mạch vành cấp là fondaparinux và bivalirudin 3. Nhân dịp fondaparinux được hãng dược phẩm Glaxo SmithKline đưa vào thị trường Việt Nam trong tháng 7/2011 với tên biệt dược là Arixtra, tác giả bài viết muốn giới thiệu với các đồng nghiệp trong ngành tim mạch học và hồi sức cấp cứu tính năng và các chỉ định đã được công nhận của thuốc này.
CẤU TẠO, CƠ CHẾ TÁC DỤNG VÀ ĐẶC ĐIỂM DƯỢC ĐỘNG HỌC CỦA FONDAPARINUX
Cấu tạo và cơ chế tác dụng của heparin KPĐ, heparin TLPTT và fondaparinux được minh họa trên hình 1. Heparin KPĐ là một hỗn hợp không đồng nhất những chuỗi mucopolysaccharide có chiều dài khác nhau, ở đầu mỗi chuỗi có gốc pentasaccharide (tức là 5 saccharide nối với nhau) đặc hiệu. Phân tử heparin KPĐ kết hợp với antithrombin (AT) hiện diện trong huyết tương tại vị trí pentasaccharide đặc hiệu này và hoạt hóa AT. Sau khi được hoạt hóa, AT cùng với phân tử heparin KPĐ (chuỗi dài) sẽ bất hoạt hóa các yếu tố đông máu như yếu tố Xa và thrombin (hình 1, hàng trên cùng).
Heparin TLPTT được bào chế bằng cách khử polyme heparin KPĐ (bằng tác nhân hóa học hoặc bằng enzym). Sự khử polyme tạo ra những chuỗi mucopolysaccharide ngắn, có trọng lượng phân tử trung bình 4000-5000 Da. Ở đầu mỗi chuỗi cũng có pentasaccharide đặc hiệu. Phân tử heparin TLPTT cũng kết hợp với AT tại vị trí pentasaccharide đặc hiệu và hoạt hóa AT. Tuy nhiên vì heparin TLPTT có chuỗi ngắn hơn heparin KPĐ nên phức hợp heparin TLPTT – AT có tác dụng bất hoạt hóa yếu tố Xa mạnh hơn là bất hoạt hóa thrombin (hình 1, hàng giữa).
Gần đây các nhà khoa học đã tổng hợp được fondaparinux là một đồng dạng của pentasaccharide đặc hiệu. Fondaparinux kết hợp với AT và hoạt hóa AT. Phức hợp fondaparinux – AT chỉ bất hoạt hóa yếu tố Xa và hoàn toàn không có ảnh hưởng trên thrombin (hình 1, hàng dưới cùng). Như vậy, có thể gọi fondaparinux là một thuốc ức chế chọn lọc Xa 3,4. Sau khi bất hoạt hóa một phân tử Xa, phân tử fondaparinux tách ra khỏi phức hợp AT – Xa để tiếp tục gắn với một phân tử AT khác, do đó một phân tử fondaparinux có thể bất hoạt hóa nhiều phân tử Xa. Một phân tử Xa có thể có thể kích hoạt sự tổng hợp của 50 phân tử thrombin 4. Điều này giải thích vì sao fondaparinux tuy ức chế chọn lọc Xa nhưng có hiệu lực chống đông mạnh.
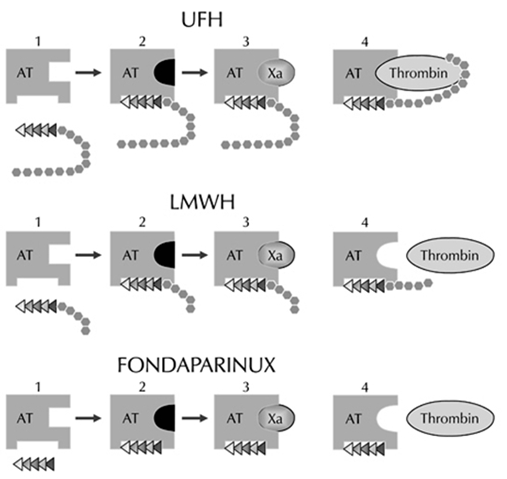
Hình 1: Cấu tạo và cơ chế tác dụng của heparin không phân đoạn (UFH), heparin trọng lượng phân tử thấp (LMWH) và fondaparinux (đọc chú thích trong bài viết).
Fondaparinux được dùng với liều thông thường là 2,5 mg tiêm dưới da một lần duy nhất trong ngày. Fondaparinux chống chỉ định đối với bệnh nhân suy thận nặng có độ thanh thải creatinin < 30 ml/phút 3.
VỊ TRÍ CỦA FONDAPARINUX TRONG ĐIỀU TRỊ HỘI CHỨNG MẠCH VÀNH CẤP KHÔNG CÓ ST CHÊNH LÊN
Vị trí của fondaparinux trong điều trị hội chứng mạch vành cấp không có ST chênh lên đã được xác định bởi nghiên cứu OASIS-5 (The Fifth Organization to Assess Strategies in Acute Ischemic Syndromes) 11. OASIS-5 là một thử nghiệm lâm sàng phân nhóm ngẫu nhiên, mù đôi, đa trung tâm. Mục tiêu nghiên cứu là so sánh hiệu quả và tính an toàn của fondaparinux và enoxaparin (là một heparin TLPTT) trong điều trị hội chứng mạch vành cấp không có ST chênh lên. Đối tượng lànhững người bị đau thắt ngực không ổn định hoặc nhồi máu cơ tim (NMCT) cấp không có ST chênh lên trong vòng 24 giờ đầu sau đau ngực và có ít nhất 2 trong số 3 tiêu chuẩn sau: tuổi từ 60 trở lên, tăng troponin hoặc CK-MB và thay đổi điện tim chứng tỏ có thiếu máu cục bộ tim. Những người có chống chỉ định với heparin TLPTT, mới bị đột quị dạng xuất huyết, có chỉ định dùng kháng đông ngoài chỉ định do hội chứng mạch vành cấp hoặc có creatinin/huyết thanh ≥ 3 mg/dl (265 mmol/l) bị loại khỏi nghiên cứu. Tiêu chí đánh giá (TCĐG) chính về hiệu quả là phối hợp các biến cố chết, NMCT và thiếu máu cục bộ kháng trị sau 9 ngày. TCĐG chính về tính an toàn là chảy máu nặng (chảy máu gây chết, chảy máu trong hộp sọ, sau phúc mạc hoặc trong nhãn cầu, hemoglobin tụt ≥ 3 g/dl hoặc phải truyền máu hơn 2 đơn vị) sau 9 ngày. TCĐG về tương quan lợi ích/nguy cơ là phối hợp các biến cố chết, NMCT, thiếu máu cục bộ kháng trị và chảy máu nặng sau 9 ngày. Các TCĐG phụ gồm từng biến cố chết, NMCT, thiếu máu cục bộ kháng trị và phối hợp các biến cố này cũng như đột quị sau 30 ngày và vào cuối nghiên cứu (sau 6 tháng).
Bệnh nhân nhóm fondaparinux được cho dùng fondaparinux tiêm dưới da 2,5 mg/ngày, thời gian dùng là cho đến khi xuất viện, không quá 8 ngày. Bệnh nhân nhóm enoxaparin được cho dùng enoxaparin tiêm dưới da 1 mg/kg 2 lần/ngày, thời gian dùng 2-8 ngày hoặc cho đến khi bệnh nhân có tình trạng lâm sàng ổn định. Thông tim có thể được thực hiện bất cứ lúc nào. Ở nhóm enoxaparin, bệnh nhân không được dùng thêm thuốc chống đông nếu liều enoxaparin cuối được tiêm trong vòng 6 giờ trước thông tim và được dùng thêm heparin KPĐ nếu liều enoxaparin cuối được tiêm hơn 6 giờ trước thông tim (liều heparin KPĐ là 0,013 ml/kg nếu có dùng một thuốc kháng thụ thể glycoprotein IIb/IIIa hoặc 0,02 ml/kg nếu không dùng). Ở nhóm fondaparinux, bệnh nhân được dùng thêm 2,5 mg fondaparinux tiêm tĩnh mạch nếu liều fondaparinux cuối được tiêm trong vòng 6 giờ trước thông tim và 2,5-5 mg fondaparinux tiêm tĩnh mạch nếu liều fondaparinux cuối được tiêm hơn 6 giờ trước thông tim (liều fondaparinux tiêm tĩnh mạch là 2,5 mg nếu có dùng một thuốc kháng thụ thể glycoprotein IIb/IIIa hoặc 5 mg nếu không dùng).
Tổng cộng có 20.078 bệnh nhân được tuyển vào nghiên cứu. Các đặc điểm và điều trị của bệnh nhân được nêu trên bảng 1.
Bảng 1: Các đặc điểm và điều trị của bệnh nhân tham gia OASIS-5.
|
|
Enoxaparin (n = 10.021) |
Fondaparinux (n = 10.057) |
|
Tuổi – năm |
66,6 ± 11,0 |
66,6 ± 10,8 |
|
Giới nam – số (%) |
6148 (61,4) |
6231 (62,0) |
|
Thời gian từ lúc đau ngực đến lúc phân nhóm – giờ |
12,7 ± 6,8 |
12,7 ± 6,8 |
|
Chẩn đoán lúc vào nghiên cứu – số (%) Đau thắt ngực không ổn định Nghi NMCT |
4517 (45,1) 5502 (54,9) |
4581 (45,6) 5474 (54,4) |
|
Tiền sử NMCT Mổ bắc cầu hoặc can thiệp mạch vành qua da Đột quị Suy tim Đái tháo đường |
2580 (25,7) 1953 (19,5) 647 (6,5) 1386 (13,8) 2503 (25,0) |
2584 (25,7) 2022 (20,1) 597 (5,9) 1402 (13,9) 2575 (25,6) |
|
Thuốc dùng sau khi phân nhóm – số (%) Aspirin Clopidogrel hoặc ticlopidine Heparin KPĐ Ức chế men chuyển hoặc chẹn thụ thể AT Chẹn bêta Hạ lipid máu |
9767 (97,5) 6735 (67,2) 3131 (31,2) 7630 (76,1) 8792 (87,7) 7856 (78,4) |
9809 (97,5) 6797 (67,6) 2211 (22,0) 7535 (74,9) 8766 (87,2) 7988 (79,4) |
|
Thủ thuật trong bệnh viện – số (%) Chụp mạch vành Can thiệp mạch vành qua da Mổ bắc cầu mạch vành |
6325 (63,1) 3435 (34,3) 897 (9,0) |
6390 (63,5) 3454 (34,3) 965 (9,6) |
Các biến cố thuộc TCĐG chính xảy ra ở 579 người trong nhóm fondaparinux (tỉ lệ 5,8%) và 573 người trong nhóm enoxaparin (tỉ lệ 5,7%). Sự khác biệt giữa 2 nhóm không có ý nghĩa thống kê (tỉ số nguy cơ 1,01; khoảng tin cậy 95% 0,90 đến 1,13). Tỉ lệ từng biến cố chết, NMCT và thiếu máu cục bộ kháng trị sau 9 ngày của 2 nhóm cũng khác biệt không có ý nghĩa thống kê. Sau 30 ngày phối hợp các biến cố chết, NMCT và thiếu máu cục bộ kháng trị của 2 nhóm tương đương nhau, tuy nhiên phối hợp các biến cố chết, NMCT và đột quị của nhóm fondaparinux thấp hơn có ý nghĩa so với nhóm enoxaparin (6,7% so với 7,5%; p = 0,02). Sau 180 ngày phối hợp các biến cố chết, NMCT và đột quị của nhóm fondaparinux cũng thấp hơn rất có ý nghĩa so với nhóm enoxaparin (11,3% so với 12,5%; p = 0,007) (hình 2). Tử vong sau 30 ngày và sau 180 ngày của nhóm fondaparinux đều thấp hơn so với nhóm enoxaparin (bảng 2). Khác biệt rõ nhất giữa 2 nhóm chính là tỉ lệ chảy máu nặng: Tỉ lệ này sau 9 ngày, 30 ngày và 180 ngày đều thấp hơn rất có ý nghĩa (p < 0,001) ở nhóm fondaparinux (bảng 2). Tỉ lệ các biến cố chết, NMCT, thiếu máu cục bộ kháng trị và chảy máu nặng sau 9 ngày (TCĐG về tương quan lợi ích/nguy cơ) là 7,3% ở nhóm fondaparinux và 9,0% ở nhóm enoxaparin (tỉ số nguy cơ 0,81; khoảng tin cậy 95% 0,73 đến 0,89; p < 0,001).
Bệnh nhân bị chảy máu nặng trong thời gian nằm viện có tỉ lệ tử vong sau 30 ngày và vào cuối nghiên cứu (sau 180 ngày) cao hơn đáng kể so với bệnh nhân không có chảy máu. Vào cuối nghiên cứu số người chết ở nhóm enoxaparin nhiều hơn số người chết ở nhóm fondaparinux là 64. Trong số 64 người này có 41 người đã từng bị chảy máu nặng và 20 người đã từng bị chảy máu nhẹ trong thời gian nằm viện. Điều này chứng tỏ chảy máu trong thời gian nằm viện có ảnh hưởng rất quan trọng đối với tử vong vào cuối nghiên cứu.
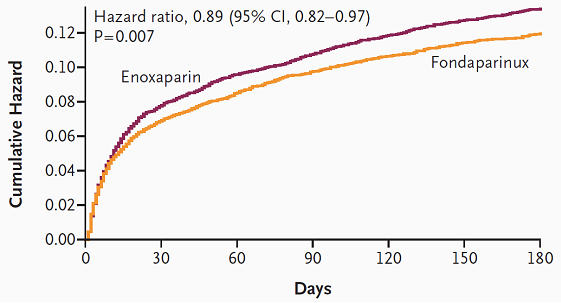
Hình 2: Tần suất dồn các biến cố chết, NMCT và đột quị sau 180 ngày ở nhóm enoxaparin (đường trên) và nhóm fondaparinux (đường dưới).
Bảng 2: Các biến cố lâm sàng ở 2 nhóm trong nghiên cứu OASIS-5.
|
|
Enoxaparin (n = 10.021) |
Fondaparinux (n = 10.057) |
Tỉ số nguy cơ (KTC 95%) |
Trị số p |
|
SAU 9 NGÀY Chết, NMCT, TMCB kháng trị Chết NMCT TMCB kháng trị Đột quị Chảy máu nặng Chết, NMCT, TMCB kháng trị hoặc chảy máu nặng |
573 (5,7) 186 (1,9) 264 (2,7) 188 (1,9) 45 (0,5) 412 (4,1) 905 (9,0) |
579 (5,8) 177 (1,8) 263 (2,6) 194 (1,9) 37 (0,4) 217 (2,2) 737 (7,3) |
1,01 (0,90-1,13) 0,95 (0,77-1,17) 0,99 (0,84-1,18) 1,03 (0,84-1,26) 0,82 (0,53-1,27) 0,52 (0,44-0,61) 0,81 (0,73-0,89) |
< 0,001 < 0,001 |
|
SAU 30 NGÀY Chết, NMCT, TMCB kháng trị Chết NMCT TMCB kháng trị Đột quị Chảy máu nặng Chết, NMCT, đột quị Chết, NMCT, TMCB kháng trị hoặc chảy máu nặng |
864 (8,6) 352 (3,5) 411 (4,1) 222 (2,2) 95 (1,0) 494 (5,0) 752 (7,5) 1238 (12,4) |
805 (8,0) 295 (2,9) 387 (3,9) 220 (2,2) 74 (0,7) 313 (3,1) 671 (6,7) 1025 (10,2) |
0,93 (0,84-1,02) 0,83 (0,71-0,97) 0,94 (0,82-1,08) 0,99 (0,82-1,19) 0,77 (0,57-1,05) 0,62 (0,54-0,72) 0,89 (0,80-0,98) 0,82 (0,75-0,89) |
0,13 0,02
< 0,001 0,02 < 0,001 |
|
SAU 180 NGÀY Chết, NMCT, TMCB kháng trị Chết NMCT TMCB kháng trị Đột quị Chảy máu nặng Chết, NMCT, đột quị Chết, NMCT, TMCB kháng trị hoặc chảy máu nặng |
1308 (13,2) 638 (6,5) 635 (6,6) 238 (2,4) 161 (1,7) 569 (5,8) 1234 (12,5) 1698 (17,1) |
1222 (12,3) 574 (5,8) 606 (6,3) 231 (2,3) 127 (1,3) 417 (4,3) 1113 (11,3) 1493 (15,0) |
0,93 (0,86-1,00) 0,89 (0,80-1,00) 0,95 (0,85-1,06) 0,97 (0,81-1,16) 0,78 (0,62-0,99) 0,72 (0,64-0,82) 0,89 (0,82-0,97) 0,86 (0,81-0,93) |
0,06 0,05
0,04 < 0,001 < 0,001 < 0,001 |
Ghi chú: NMCT: nhồi máu cơ tim; TMCB: thiếu máu cục bộ; Trong dấu ngoặc đơn là tỉ lệ phần trăm.
Nói tóm lại, nghiên cứu OASIS-5 chứng tỏ ở bệnh nhân hội chứng mạch vành cấp không có ST chênh lên: (1) Fondaparinux giảm tử vong, NMCT và thiếu máu cục bộ kháng trị tương đương enoxaparin và ít gây chảy máu nặng hơn so với enoxaparin trong 9 ngày đầu; (2) Fondaparinux giảm tử vong nhiều hơn enoxaparin sau 30 ngày và sau 6 tháng (có liên quan với việc thuốc ít gây chảy máu nặng hơn trong 9 ngày đầu), đồng thời giảm có ý nghĩa phối hợp các biến cố chết, NMCT và đột quị sau 30 ngày và sau 6 tháng so với enoxaparin; (3) Ở bệnh nhân được can thiệp mạch vành qua da, huyết khối ca-tê-te thường gặp hơn trong nhóm fondaparinux, tuy nhiên có thể ngừa biến cố này bằng cách tiêm tĩnh mạch bổ sung heparin KPĐ khi làm thủ thuật.
Việc dùng fondaparinux điều trị bệnh nhân hội chứng mạch vành cấp không có ST chênh lên đã được cả Trường Môn Tim mạch/Hiệp hội Tim Hoa Kỳ lẫn Hội tim mạch Châu Âu công nhận. Trên bảng 3 là hướng dẫn của các tổ chức này về việc dùng fondaparinux trong hội chứng mạch vành cấp không có ST chênh lên.
Bảng 3: Hướng dẫn của các hội chuyên khoa về điều trị chống đông bằng fondaparinux trong hội chứng mạch vành cấp không có ST chênh lên 13,14.
|
Hội Tim mạch Châu Âu (2007) |
Trường Môn Tim mạch/Hiệp hội Tim Hoa Kỳ (cập nhật 2011) |
|
Thuốc chống đông được khuyến cáo cho mọi bệnh nhân (I-A). Ở bệnh nhân hội chứng mạch vành cấp không có ST chênh lên không phải can thiệp mạch vành qua da khẩn (< 2 giờ), fondaparinux được khuyến cáo dùng như là thuốc chống đông có tương quan hiệu quả/an toàn tốt nhất (I-A). Liều dùng: 2,5 mg tiêm dưới da 1 lần/ngày. Nếu cần can thiệp mạch vành qua da: thêm heparin KPĐ 50-100 IU/kg (IIa-C). Có thể ngưng kháng đông 24 giờ sau can thiệp mạch vành qua da (IIa-C). Ở bệnh nhân được điều trị nội khoa, tiếp tục thuốc chống đông cho đến khi xuất viện (I-B). |
Thuốc chống đông được chỉ định sớm cho mọi bệnh nhân (I-A). Trong cả 2 chiến lược điều trị (can thiệp sớm hoặc nội khoa), fondaparinux là một trong các thuốc chống đông có thể chọn (I-B). Liều dùng: 2,5 mg tiêm dưới da 1 lần/ngày. Không dùng nếu độ thanh thải creatinin < 30 ml/phút. Nếu quyết định điều trị nội khoa và bệnh nhân có nguy cơ chảy máu cao, fondaparinux được ưu tiên chọn (I-B). Dùng fondaparinux trong thời gian nằm viện, không quá 8 ngày (I-A). Nếu can thiệp mạch vành qua da: thêm heparin KPĐ 50-60 IU/kg. Ngưng thuốc kháng đông sau thủ thuật nếu không có biến chứng (I-B). Nếu quyết định mổ bắc cầu sau chụp mạch vành: ngưng fondaparinux 24 giờ trước mổ (I-B). |
Ghi chú: I: Theo chứng cứ và/hoặc ý kiến chung, liệu pháp có lợi và hiệu quả; IIa: Chứng cứ/ý kiến chung thiên về lợi ích/hiệu quả của liệu pháp; A: Có số liệu từ nhiều thử nghiệm lâm sàng phân nhóm ngẫu nhiên hoặc phân tích gộp; B: Có số liệu từ một thử nghiệm lâm sàng phân nhóm ngẫu nhiên hoặc từ những nghiên cứu không phân nhóm ngẫu nhiên lớn.
VỊ TRÍ CỦA FONDAPARINUX TRONG ĐIỀU TRỊ NHỒI MÁU CƠ TIM CẤP VỚI ST CHÊNH LÊN
Vị trí của fondaparinux trong điều trị nhồi máu cơ tim cấp với ST chênh lên đã được xác định bởi nghiên cứu OASIS-6 (Organization for the Assessment of Strategies for Ischemic Syndromes-6) 15. OASIS-6 là một thử nghiệm lâm sàng phân nhóm ngẫu nhiên, mù đôi, đa trung tâm. Mục tiêu nghiên cứu là so sánh hiệu quả ngừa tử vong và tái NMCT của fondaparinux và tiếp cận chống đông chuẩn trong NMCT cấp với ST chênh lên. Đối tượng là bệnh nhân NMCT cấp với ST chênh lên trong vòng 24 giờ đầu sau đau ngực. Những người có chống chỉ định với liệu pháp chống đông, bao gồm những người có nguy cơ chảy máu cao, đang dùng thuốc chống đông uống hoặc có creatinin/huyết thanh ≥ 3 mg/dl (265 mmol/l) bị loại khỏi nghiên cứu. Tiêu chí đánh giá (TCĐG) chính về hiệu quả là phối hợp các biến cố chết và tái NMCT sau 30 ngày, sau 9 ngày và vào cuối nghiên cứu (3-6 tháng). TCĐG chính về tính an toàn là chảy máu nặng sau 9 ngày, 30 ngày và vào cuối nghiên cứu. TCĐG về tương quan lợi ích/nguy cơ là phối hợp các biến cố chết, tái NMCT và chảy máu nặng sau 9 ngày, 30 ngày và vào cuối nghiên cứu.
Bệnh nhân nhóm fondaparinux được cho dùng fondaparinux tiêm dưới da 2,5 mg/ngày (liều đầu tiêm tĩnh mạch), thời gian dùng là cho đến khi xuất viện, không quá 8 ngày. Đối với bệnh nhân được chuẩn bị can thiệp mạch vành qua da tiên phát, liều đầu fondaparinux là 5 mg nếu không có dùng một thuốc kháng thụ thể glycoprotein IIb/IIIa. Bệnh nhân nhóm chứng được phân tầng thành phân nhóm 1 (không có chỉ định dùng heparin KPĐ) và phân nhóm 2 (có chỉ định dùng heparin KPĐ, ví dụ bệnh nhân được điều trị bằng thuốc tiêu sợi huyết chọn lọc fibrin, bệnh nhân thích hợp cho điều trị chống đông hoặc bệnh nhân được chuẩn bị can thiệp mạch vành qua da tiên phát). Ở phân nhóm 2 liều heparin KPĐ là 60 IU bolus, sau đó truyền tĩnh mạch 12 IU/kg/giờ trong 24-48 giờ, vận tốc truyền được điều chỉnh để đạt aPTT gấp 1,5-2,0 lần chứng.
Tổng cộng có 12.092 bệnh nhân được tuyển vào nghiên cứu. Các đặc điểm và điều trị của bệnh nhân được nêu trên bảng 4.
Bảng 4: Các đặc điểm và điều trị của bệnh nhân tham gia OASIS-6.
|
|
Chứng (n = 6056) |
Fondaparinux (n = 6036) |
|
Tuổi – năm |
61,5 ± 12,2 |
61,6 ± 12,3 |
|
Giới nam – số (%) |
4353 (71,9) |
4393 (72,8) |
|
Thời gian từ lúc đau ngực đến lúc phân nhóm – giờ |
4,8 |
4,8 |
|
Điện tim lúc nhập viện – số (%) ST chênh > 2 mm ST chênh > 1 mm Bloc nhánh trái mới xuất hiện Chỉ điểm NMCT thành sau |
3728 (61,6) 2183 (36,0) 60 (1,0) 74 (1,2) |
3610 (59,8) 2282 (37,8) 58 (1,0) 80 (1,3) |
|
Tiền sử Tăng huyết áp Đái tháo đường Suy tim NMCT Đột quị |
3307 (54,6) 1064 (17,6) 840 (13,9) 746 (12,3) 385 (6,4) |
3274 (54,3) 1088 (18,0) 844 (14,0) 772 (12,8) 416 (6,9) |
|
Thuốc dùng sau khi phân nhóm – số (%) Aspirin Clopidogrel hoặc ticlopidine Heparin KPĐ Ức chế men chuyển hoặc chẹn thụ thể AT Chẹn bêta Hạ lipid máu |
5839 (96,4) 3540 (58,5) 681 (11,2) 4847 (80,0) 5074 (83,8) 4529 (74,8) |
5841 (96,8) 3481 (57,7) 651 (10,8) 4795 (79,4) 5092 (84,4) 4494 (74,5) |
|
Thủ thuật trong bệnh viện – số (%) Chụp mạch vành Can thiệp mạch vành qua da tiên phát Thuốc tiêu sợi huyết |
2625 (43,3) 1903 (31,4) 2744 (45,3) |
2656 (44,0) 1886 (31,2) 2692 (44,6) |
Trên bảng 5 là số biến cố thuộc TCĐG chính (kèm tỉ lệ phần trăm) ở 2 nhóm sau 9 ngày, 30 ngày và vào cuối nghiên cứu. Phối hợp các biến cố chết và tái NMCT và từng biến cố riêng biệt ở nhóm fondaparinux luôn thấp hơn có ý nghĩa so với nhóm chứng trong suốt thời gian nghiên cứu. Trên hình 3 là các đường Kaplan-Meier biểu diễn tử vong dồn cho đến 180 ngày của 2 nhóm. Số ca thiếu máu cục bộ kháng trị sau 9 ngày của 2 nhóm không khác biệt (26 so với 27). Số ca đột quị ở nhóm fondaparinux ít hơn so với nhóm chứng (43 so với 55). Số ca bị suy tim hoặc choáng tim của nhóm fondaparinux ít hơn so với nhóm chứng (563 so với 599).
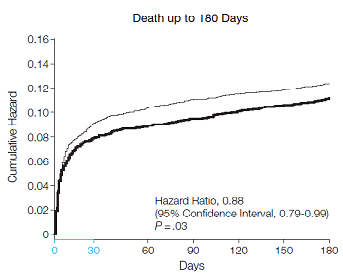
Hình 3: Tử vong dồn cho đến 180 ngày của nhóm fondaparinux (đường dưới) và nhóm chứng (đường trên).
Bảng 5: Các biến cố lâm sàng ở 2 nhóm trong nghiên cứu OASIS-6.
|
|
Chứng (n = 6056) |
Fondaparinux (n = 6036) |
Tỉ số nguy cơ (KTC 95%) |
Trị số p |
|
CHẾT HOẶC TÁI NMCT Ngày 9 Ngày 30 Cuối nghiên cứu (3-6 tháng) |
537 (8,9) 677 (11,2) 857 (14,8) |
444 (7,4) 585 (9,7) 756 (13,4) |
0,83 (0,73-0,94) 0,86 (0,77-0,96) 0,88 (0,79-0,97) |
0,003 0,008 0,008 |
|
CHẾT Ngày 9 Ngày 30 Cuối nghiên cứu (3-6 tháng) |
425 (7,0) 540 (8,9) 674 (11,6) |
368 (6,1) 470 (7,8) 598 (10,5) |
0,87 (0,75-1,00) 0,87 (0,77-0,98) 0,88 (0,79-0,99) |
0,04 0,03 0,03 |
|
TÁI NMCT Ngày 9 Ngày 30 Cuối nghiên cứu (3-6 tháng) |
136 (2,3) 175 (3,0) 245 (4,6) |
92 (1,6) 142 (2,5) 200 (3,8) |
0,67 (0,52-0,88) 0,81 (0,65-1,01) 0,81 (0,67-0,97) |
0,004 0,06 0,03 |
Ghi chú: NMCT: nhồi máu cơ tim; Trong dấu ngoặc đơn là tỉ lệ phần trăm.
Số ca chảy máu nặng của nhóm fondaparinux ít hơn so với nhóm chứng (61 so với 79). Số ca chết, tái NMCT hoặc chảy máu nặng sau 9 ngày (TCĐG về tương quan lợi ích/nguy cơ) là 464 ở nhóm fondaparinux và 559 ở nhóm enoxaparin (tỉ số nguy cơ 0,83; khoảng tin cậy 95% 0,73 đến 0,94; p = 0,003).
Trong số bệnh nhân tham gia OASIS-6 có 2867 bệnh nhân không được tái thông mạch vành bằng bất cứ biện pháp nào (cả thuốc tiêu sợi huyết lẫn can thiệp mạch vành qua da tiên phát). Ở những đối tượng này, fondaparinux giảm có ý nghĩa chết/tái NMCT (tỉ số nguy cơ 0,80; khoảng tin cậy 95% 0,65 đến 0,98) và không tăng nguy cơ chảy máu nặng (tỉ số nguy cơ 0,82; khoảng tin cậy 95% 0,44 đến 1,55).
Có 5436 người được điều trị bằng thuốc tiêu sợi huyết. Ở phân nhóm này fondaparinux giảm có ý nghĩa phối hợp các biến cố chết và tái NMCT sau 30 ngày (tỉ số nguy cơ 0,79; khoảng tin cậy 95% 0,68 đến 0,92)16. Lợi ích của fondaparinux đặc biệt rõ ở những bệnh nhân được điều trị bằng thuốc tiêu sợi huyết không chọn lọc (chủ yếu là streptokinase). Ở những đối tượng này, fondaparinux giảm có ý nghĩa cả chết/tái NMCT (tỉ số nguy cơ 0,76; khoảng tin cậy 95% 0,64 đến 0,90) lẫn chảy máu nặng (tỉ số nguy cơ 0,60; khoảng tin cậy 95% 0,37 đến 0,97)16.
Có 3789 người được can thiệp mạch vành qua da tiên phát. Ở phân nhóm này fondaparinux có khuynh hướng tăng chết/tái NMCT sau 30 ngày tuy là không có ý nghĩa thống kê (tỉ số nguy cơ 1,2; khoảng tin cậy 95% 0,91 đến 1,57; p = 0,19).
Nói tóm lại, nghiên cứu OASIS-6 chứng tỏ trong NMCT cấp với ST chênh lên: (1) Fondaparinux giảm có ý nghĩa nguy cơ chết/tái NMCT so với tiếp cận chống đông chuẩn; (2) Ở bệnh nhân không được tái thông mạch vành, fondaparinux giảm có ý nghĩa nguy cơ chết/tái NMCT và không tăng nguy cơ chảy máu nặng; (3) Ở bệnh nhân được điều trị bằng thuốc tiêu sợi huyết, fondaparinux giảm có ý nghĩa tử vong, tái NMCT và chảy máu nặng (lợi ích đặc biệt rõ ở những bệnh nhân được điều trị bằng thuốc tiêu sợi huyết không chọn lọc); (4) Ở bệnh nhân được can thiệp mạch vành qua da tiên phát, fondaparinux không mang lại lợi ích.
Hiện nay cả Hội Tim mạch Châu Âu lẫn Trường Môn Tim mạch/Hiệp hội Tim Hoa Kỳ đều công nhận việc dùng fondaparinux trong NMCT cấp với ST chênh lên 17,18. Bảng 6 tóm tắt hướng dẫn của các tổ chức này về việc dùng fondaparinux trong NMCT cấp với ST chênh lên. Tuy cùng dựa vào kết quả của nghiên cứu OASIS-6, hướng dẫn của Hoa Kỳ và của Châu Âu không giống nhau. Đối với bệnh nhân được điều trị bằng thuốc tiêu sợi huyết, các chuyên gia Châu Âu giới hạn việc dùng fondaparinux cho những người được điều trị bằng streptokinase, trong khi các chuyên gia Hoa Kỳ không đưa ra giới hạn này. Đối với bệnh nhân được can thiệp mạch vành qua da tiên phát, các chuyên gia Châu Âu khuyên không dùng fondaparinux, trong khi các chuyên gia Hoa Kỳ vẫn cho phép dùng với điều kiện phải tiêm tĩnh mạch bổ sung một thuốc có hoạt tính chống thrombin, ví dụ heparin KPĐ hoặc bivalirudin, trước thủ thuật.
Năm 2008 Trường Môn các thầy thuốc lồng ngực Hoa Kỳ (American College of Chest Physicians) đưa ra hướng dẫn thực hành lần thứ 8 về điều trị chống huyết khối, trong đó có đề cập đến điều trị chống huyết khối trong NMCT cấp với ST chênh lên 19. Nội dung hướng dẫn này ở vị trí trung gian giữa hướng dẫn của Hội Tim mạch Châu Âu và hướng dẫn của Trường Môn Tim mạch/Hiệp hội Tim Hoa Kỳ: (1) Đối với bệnh nhân được điều trị bằng thuốc tiêu sợi huyết, fondaparinux được khuyến cáo dùng kèm bất kể thuốc tiêu sợi huyết đó là chọn lọc hay không chọn lọc fibrin; (2) Đối với bệnh nhân được can thiệp mạch vành qua da tiên phát, fondaparinux không được khuyên dùng 19. Nói chung, hiện nay heparin KPĐ vẫn là thuốc chống đông được ưa chuộng trong can thiệp mạch vành qua da tiên phát.
Bảng 6: Hướng dẫn của các hội chuyên khoa về điều trị chống đông bằng fondaparinux trong NMCT cấp với ST chênh lên 17,18.
|
Hội Tim mạch Châu Âu (2008) |
Trường Môn Tim mạch/Hiệp hội Tim Hoa Kỳ (2007) |
|
Fondaparinux được chỉ định cho bệnh nhân NMCT cấp với ST chênh lên được điều trị bằng streptokinase (IIa-B) hoặc không được tái thông mạch vành (I-B). Fondaparinux không được chỉ định cho bệnh nhân NMCT cấp với ST chênh lên được can thiệp mạch vành qua da tiên phát (III-B). Liều dùng: 2,5 mg tiêm tĩnh mạch, 24 giờ sau tiêm dưới da 2,5 mg 1 lần/ngày (nếu creatinin/huyết thanh ≤ 3 mg/dl (265 mmol/l). Thời gian dùng: cho đến khi xuất viện, không quá 8 ngày. |
Bệnh nhân NMCT cấp với ST chênh lên được tái thông mạch vành bằng thuốc tiêu sợi huyết cần được điều trị chống đông ít nhất 48 giờ (I-C). Fondaparinux là một lựa chọn (với điều kiện creatinin/huyết thanh < 3 mg/dl); Liều khởi đầu 2,5 mg tiêm tĩnh mạch, sau đó 2,5 mg tiêm dưới da 1 lần/ngày; Dùng trong thời gian nằm viện, không quá 8 ngày (I-B). Bệnh nhân NMCT cấp với ST chênh lên không được tái thông mạch vành nên được điều trị chống đông (không dùng heparin KPĐ) trong thời gian nằm viện, không quá 8 ngày (IIa-B). Fondaparinux là một lựa chọn, liều giống liều dùng cho bệnh nhân được điều trị bằng thuốc tiêu sợi huyết (IIa-B). Nếu cần can thiệp mạch vành qua da cho một bệnh nhân đã dùng fondaparinux: tiêm tĩnh mạch bổ sung một thuốc chống đông có hoạt tính chống thrombin (I-C). Không được dùng fondaparinux như thuốc chống đông duy nhất khi can thiệp mạch vành qua da (III-C). |
Ghi chú: I: Theo chứng cứ và/hoặc ý kiến chung, liệu pháp có lợi và hiệu quả; IIa: Chứng cứ/ý kiến chung thiên về lợi ích/hiệu quả của liệu pháp; III: Theo chứng cứ/ý kiến chung, liệu pháp không có lợi/hiệu quả, trong một số trường hợp có thể có hại; A: Có số liệu từ nhiều thử nghiệm lâm sàng phân nhóm ngẫu nhiên hoặc phân tích gộp; B: Có số liệu từ một thử nghiệm lâm sàng phân nhóm ngẫu nhiên hoặc từ những nghiên cứu không phân nhóm ngẫu nhiên lớn; C: Ý kiến đồng thuận của các chuyên gia và/hoặc những nghiên cứu nhỏ, nghiên cứu hồi cứu.
TÀI LIỆU THAM KHẢO
1) European Commission approves BriliqueTM (Ticagrelor tablets). http://www.astrazeneca.com/Media/press-releases/Article/European-Commission-Approves-Brilique
2) Wiviott SD, Antman EM, Braunwald E. Prasugrel. Circulation 2010;122:394-404.
3) Hirsh J, Bauer KA, Donati M, et al. Parenteral anticoagulants. American College of Chest Physicians evidence-based clinical practice guidelines (8th edition). Chest 2008;133:141S-159S.
4) Paolucci F, Clavies M, Donat F, et al. Fondaparinux sodium mechanism of action: identification of specific binding to purified and human plasma-derived proteins. Clin Pharmacokinet 2002;41:11-18.
5) Donat F, Duret J, Santoni A, et al. The pharmacokinetics of fondaparinux sodium in healthy volunteers. Clin Pharmacokinet 2002;41:1-9.
6) Lieu C, Shi J, Donat F, et al. Fondaparinux sodium is not metabolised in mammalian liver fractions and does not inhibit cytochrom P450-mediated metabolism of concomitant drugs. Clin Pharmacokinet 2002;41:19-26.
7) Kuo K, Kovacs M. Fondaparinux: a potential new therapy for HIT. Hematology 2005;10:271-275.
8) Papadopoulos S, Flynn JD, Lewis DA. Fondaparinux as a treatment option for heparin-induced thrombocytopenia. Pharmacotherapy 2007;27:921-926.
9) Smogorzewska A, Brandt JT, Chandler WL, et al. Effect of fondaparinux on coagulation assays. Results of College of American Pathologists proficiency testing. Arch Pathol Lab Med 2006;130:1605-1611.
10) Bijsterveld N, Moons A, Boekholdt S, et al. Ability of recombinant factor VIIa to reverse the anticoagulant effect of the pentasaccharide fondaparinux in healthy volunteers. Circulation 2002;106:2550-2554.
11) The Fifth Organization to Assess Strategies in Acute Ischemic Syndromes Investigators. Comparison of fondaparinux and enoxaparin in acute coronary syndromes. N Engl J Med 2006;354:1464-1476.
12) Mehta SR, Granger CB, Eikelboom JW, et al. Efficacy and safety of fondaparinux versus enoxaparin in patients with acute coronary syndromes undergoing percutaneous coronary intervention. Results from the OASIS-5 trial. J Am Coll Cardiol 2007;50:1742-1751.
13) Guidelines for the diagnosis and treatment of non-ST-segment elevation acute coronary syndromes. The Task Force for the diagnosis and treatment of non-ST-segment elevation acute coronary syndromes of the European Society of Cardiology. Eur Heart J 2007;28:1598-1660.
14) 2011 ACCF/AHA Focused update incorporated into the ACC/AHA 2007 guidelines for the management of patients with unstable angina/non-ST-elevation myocardial infarction. A report of the American College of Cardiology Foundation/American Heart Association Task Force on practice guidelines. J Am Coll Cardiol 2011;57:e215-367.
15) The OASIS-6 Trial Group. Effects of fondaparinux on mortality and reinfarction in patients with acute ST-segment elevation myocardial infarction. The OASIS-6 randomized trial. JAMA 2006;295:1519-1530.
16) Peters RJG, Joyner C, Bassand P, et al, for the OASIS-6 investigators. The role of fondaparinux as an adjunct to thrombolytic therapy in acute myocardial infarction: a subgroup analysis of the OASIS-6 trial. Eur Heart J 2008;29:324-331.
17) Management of acute myocardial infarction in patients presenting with persistent ST-segment elevation. The Task Force on the management of ST-segment elevation acute myocardial infarction of the European Society of Cardiology. Eur Heart J 2008;29:2909-2945.
18) 2007 Focused update of the ACC/AHA 2004 guidelines for the management of patients with ST-elevation myocardial infarction. A report of the American College of Cardiology/American Heart Association Task Force on practice guidelines. Circulation 2008;117:296-329.
19) Goodman SG, Menon V, Cannon CP, et al. Acute ST-segment elevation myocardial infarction. American College of Chest Physicians evidence-based clinical practice guidelines (8th edition). Chest 2008;133:708S-775S.







