(Combination therapy in the extended cardiovascular continuum: a focus on perindopril and amlodipine * J Cardiovas Med 2015, 16:000-000)
Sự tiến triển của bệnh lí tim mạch là hậu quả của con đường xơ vữa và tuổi tác.
Tác giả: Borghi Claudio, Morbini Martino và Arrigo F.G.Cicero
Người dịch: BS. Nguyễn Việt Hoài
Hiệu đính: BS. Nguyễn Thanh Hiền
Điểm xuất phát của hai con đường này khác nhau- những yếu tố nguy cơ hoặc lão hóa động mạch chủ- nhưng chúng đều dẫn đến tình trạng cuối cùng – bệnh tim giai đoạn cuối. Cùng với nhau, những con đường này đan xen gây nên chuỗi bệnh lí tim mạch tích hợp. Ức chế hệ thống Renin-angiotensin-aldosteron (RAAS) cho thấy làm chậm, cắt đứt sự tiến triển bệnh tim mạch theo con đường xơ vữa. Bảo vệ tim mạch bằng ức chế RAAS rất đa dạng; những thuốc ức chế RAAS khác nhau cho ra mức bảo vệ khác nhau . Tương tự, thuốc chẹn kênh canxi (CCBs) cũng cho thấy hiệu quả bảo vệ tim mạch rất rõ ràng, đặc biệt là yếu tố nguy cơ bệnh mạch máu não. Nghiên cứu AngloScandinavian Cardiac Outcome Trial (ASCOT) cho thấy sự kết hợp Ức chế men chuyển (ACE) perindopril và chẹn canxi amlodipine cho hiệu quả bảo vệ tim mạch tốt hơn so với Chẹn beta và Thiazid ở bệnh nhân tăng huyết áp nguy cơ. Bằng cách làm giảm những hậu quả xấu xảy ra ở nhiều giai đoạn của chuỗi bệnh tim mạch tích hợp trong khi hạ huyết áp, perindopril và Amlodipine có thể cắt đứt hoặc làm chậm sự tiến triển của bệnh tim mạch. Những thuốc hạ áp này có hiệu quả bổ sung trên mạch máu: tăng cường bảo vệ mạch máu và giảm tác dụng phụ. Bằng chứng từ ASCOT cho thấy hiệu quả hạ áp và bảo vệ mạch máu của amlodipine ± perindopril đi kèm đã cho thấy hiệu quả thực tế trong lâm sàng. Chiến lược sử dụng ức chế men chuyển và ức chế canxi như perindopril và amlodipine nhắm vào nhiều giai đoạn ở cả 2 con đường dẫn đến bệnh tim mạch có thể làm giảm một cách hiệu quả nguy cơ tim mạch và hạ huyết áp
Giới thiệu
Yếu tố nguy cơ lớn nhất của bệnh tim mạch là tăng huyết áp, kiểm soát huyết áp là công việc rất quan trọng để phòng chống những tổn thương về tim mạch. Nghiên cứu dịch tễ học gần đây cho thấy dân số tăng huyết áp có nguy cơ tim mạch tổng cộng suốt đời ở tuổi 30 là 63.3%[độ tin cậy 95% (CI) 62.9-63.8 ]so với 46.1% (45.5-46.8) ở dân số có huyết áp bình thường, và xuất hiện bệnh tim mạch sớm hơn 5 năm (95% CI 4.8-5.2). Do vậy việc tìm kiếm những nguyên nhân gây tăng huyết áp không kiểm soát có thể điều chỉnh là rất quan trọng, và điều trị khi có thể. Hạ huyết áp do vậy cũng làm giảm một cách hiệu quả những nguy cơ này. Tuy nhiên một số bệnh nhân dù đã huyết áp kiểm soát tốt rồi vẫn còn những nguy cơ tim mạch. Do vậy điều trị huyết áp một cách tối ưu nên đồng thời vừa hạ huyết áp, vừa giảm những hậu quả xấu của bệnh tim mạch. Thấy được hậu quả xấu của việc vừa có những yếu tố nguy cơ tồn lưu và bệnh kèm theo ở bệnh nhân tăng huyết áp, Guideline mới nhất của Châu Âu đã khuyến cáo công cụ đánh giá nguy cơ như lão hóa mạch máu nên được sử dụng để đánh giá nguy cơ tim mạch toàn bộ trước khi điều trị tăng huyết áp
Bệnh tim mạch tiến triển theo con đường một chuỗi các sự kiện xơ vữa từ các yếu tố nguy cơ không liên quan, đa dạng cho đến bệnh tim giai đoạn cuối. Theo mô hình này – vòng xoắn bệnh lý tim mạch- đã được nhắc đến lần đầu tiên cách đây hơn 20 năm. Gần đây, chuỗi các sự kiện bệnh học khác – vòng xoắn bệnh tim mạch do lão hóa đã được nhắc đến. Hậu quả xấu của bệnh tim mạch do lão hóa là do dãn từ từ và xơ cứng động mạch chủ đoạn gần, gây ảnh hưởng tim, thận và não. Mô hình sau này cùng với giai đoạn sau của bệnh tim mạch xơ vữa cổ điển hình thành nên vòng xoắn bệnh lí tim mạch tích hợp (hình 1). Mô hình kết hợp này cho cái nhìn tổng quan về bệnh tim mạch tiến triển như thế nào và giải thích tại sao điều chỉnh huyết áp ở bệnh nhân bệnh tim mạch rất khó khăn. Nghiên cứu đã được tiến hành về hiệu quả của ức chế RAAS ở bệnh tim mạch xơ vữa. Những phân tích gộp gần đây so sánh thuốc ức chế RAAS với điều trị khác hoặc ức chế RAAS và giả dược về hiểu quả giảm tỉ lệ tử vong ở bệnh nhân tăng huyết áp kết luận rằng ức chế men chuyển(ACE) có ưu thế hơn ức chế thụ thể (ARB) trong việc làm giảm tỉ lệ tử vong do tim mạch và mọi nguyên nhân khác, do vậy tránh được tiến triển của vòng xoán bệnh lý.
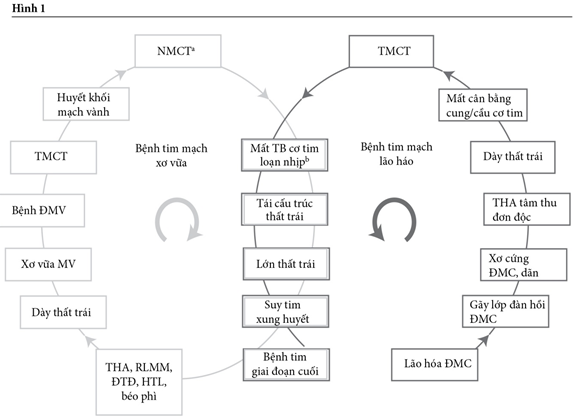
Hình 1: Các giai đoạn của vòng xoắn bệnh lí tim mạch tích hợp, xuất phát từ bệnh tim mạch do xơ vữa và bệnh tim mạch lão hóa; Cả ức chế men chuyển và ức chế thụ thể đều cho hiệu quả tốt ở hầu hết các giai đoạn. Phần xám trung tâm chỉ ra điểm giao thoa của 2 con đường bệnh. a dẫn đến hoạt hóa thần kinh-thể dịch, b dẫn đến đột tử do tim, c dẫn đến bệnh vi mạch máu, bệnh thận và bệnh não sóng phản hồi, và bệnh thận giai đoạn cuối và sa sút trí tuệ
Nhiều BN cần hơn 2 loại thuốc huyết áp để đạt HA mục tiêu. Trong trường hợp này, sự kết hợp 2 thuốc theo nghiên cứu ASCOT chẹn canxi amlodipine và ƯCMC perindopril cho hiệu quả bảo vệ tim mạch tốt hơn ở BN THA có yếu tố nguy cơ tim mạch so với chiến lược cũ là lợi tiểu thiazid và ức chế beta mặc dù hiệu quả giảm áp là giống nhau. Tỉ lệ tử vong cũng giảm đi nhiều. Amlodipine ± perindopril tốt hơn so với atenolol ± thiazid trong việc ngăn ngừa tiến triển tăng huyết áp kháng trị. Giống như những phối hợp ức chế canxi và ức chế hệ RAA khác, sự kết hợp liều cố định perindopril-amlodipine cho thấy hiệu quả cao trong hạ huyết áp ở BN THA giai đoạn 2 hoặc THA nặng (hình 2). Guideline hội THA Châu Âu đang ủng hộ việc kết hợp ƯCMC và ức chế Canxi. Mục tiêu của chuyên đề này là khám phá những phương thức kết hợp điều trị THA giữa ƯCMC và ức chế canxi, và đặc biệt là phối hợp amlodipine ± perindopril trong nghiên cứu ASCOT, để làm giảm yếu tố nguy cơ tim mạch bằng cách hạ huyết áp và có thể làm giảm đi hậu quả xấu của bệnh tim mạch ở mức mạch máu
Sinh bệnh học trong vòng xoắn bệnh lí tim mạch tích hợp
Trong mô hình bệnh tim mạch do xơ vữa, đa yếu tố nguy cơ như: tăng huyết áp (THA), rối loạn mỡ máu (RLMM), đái tháo đường (ĐTĐ), hút thuốc lá, béo phì dẫn đến dày thất trái, xơ vữa mạch vành và bệnh động mạch vành (hình 1). Những thay đổi sớm này trong tiến triến bệnh tim mạch lâm sàng được giải thích bằng những thay đổi sinh lí bệnh: trong trường hợp này, việc sinh ra những yếu tố viêm và stress oxít hóa/ cơ học đã dẫn đến giảm nitric oxid sinh học và tổn thương mô
Sự gia tăng angiotensinII làm rối loạn chức năng nội mạc dẫn đến gia tăng sản phẩm phân tử hoạt hóa mạch máu, cytokines, yếu tố phát triển, và những chất tiền đông, đóng vai trò như là yếu tố thúc đẩy xơ vữa và xơ cứng mạch máu
Ở mức độ tổn thương mạch vành, sự xấu đi về sinh lí bệnh được cho rằng xảy ra nhiều nhất trong tổn thương mô, biểu hiện bằng nhồi máu cơ tim (NMCT), loạn nhịp, mất tế bào cơ tim
Tái cấu trúc bệnh học ở tim xảy ra đặc trưng bằng tái cấu trúc và lớn thất cho đến suy tim xung huyết, bệnh tim giai đoạn cuối và tử vong. Cắt đứt hoặc làm chậm quá trình bệnh học của các giai đoạn tim mạch này sẽ làm chậm hoặc dừng sự tiến triển của bệnh tim mạch.
Không giống như phương thức bệnh tim mạch do xơ vữa, phương thức bệnh tim mạch do lão hóa chỉ có một điểm khởi đầu: lão hóa động mạch chủ (ĐMC)(hình 1). Sự suy yếu ĐMC do lão hóa làm cho lớp đàn hồi bị thoái sản và cuối cùng là đứt, dẫn đến giãn thành ĐM. Phản ứng lại việc thành ĐM mỏng, ứ đọng collagen cũng như là lắng đọng canxi tại chỗ tăng lên; điều này dẫn đến xơ cứng ĐMC . Những yếu tố nguy cơ như ĐTĐ tham gia vào quá trình này bằng cách thúc đẩy kết nối chéo với phân tử protein bằng phản ứng kết nối đường.
Xơ cứng ĐMC làm gia tăng HA tâm thu và giảm HA tâm trương, dẫn đến THA tâm thu đơn độc và rối loạn nhu cầu oxy cơ tim. Nhu cầu oxy cơ tim tăng vì tim hoạt động nhiều hơn để bơm máu chống lại áp lực ĐMC tâm thu cao hơn, và cung cấp oxy cho cơ tim sẽ giảm vì sự xơ cứng làm giảm áp lực tâm trương ĐMC, thời gian tâm trương giảm và tưới máu cơ tim giảm. Hậu quả sự phá vỡ cung cầu oxy gây nên thiếu máu cơ tim không phụ thuộc vào xơ vữa ĐM.
Xơ cứng ĐM cũng gây tăng trở kháng và sóng phản hồi sớm, điều này nghĩa là một người 80 tuổi có hiệu áp cao lớn hơn ba lần so với người 20 tuổi (60-70 so với 20mmHg). Sự điều hòa chống đỡ những cơn áp lực mạch dẫn đến những áp lực này được chuyển vào những ĐM nhỏ ở cơ quan nội tạng với lưu lượng máu lúc nghỉ cao. Hậu quả của áp lực cao (xé và căng) ở ĐM nhỏ ở não và thận gây huyết khối, vi nhồi máu và rách mạch máu nhỏ, việc này theo thời gian dài sẽ dẫn đến dễ bị sa sút trí tuệ và bệnh thận giai đoạn cuối.
Ở giai đoạn sau cùng của bệnh tim mạch, bệnh tim mạch do xơ vữa và do lão hóa tích hợp với nhau; hình thành chuỗi tim mạch tích hợp gắn kết. Mất cơ tim, tái cấu trúc tim, lớn thất, suy tim xung huyết và bệnh tim giai đoạn cuối là những giai đoạn cuối cùng của cả 2 con đường. Dày thất trái, thiếu máu cơ tim, loạn nhịp cũng là những giai đoạn tìm thấy ở cả 2 con đường nhưng nguyên nhân của chúng ở mỗi con đường thì khác nhau (hình 1).
THA sẽ làm thúc đẩy nhanh tiến trình này, và cả ĐM lớn và nhỏ đều bị ảnh hưởng: tăng tỉ lệ thành/lòng mạch và mất đi các động mạch nhỏ làm gia tăng huyết áp trung bình; huyết áp trung bình cao hơn thúc đẩy xơ cứng các mạch máu lớn; xơ cứng các mạch máu lớn càng nhiều làm gia tăng độ chênh áp tâm thu tâm trương, dẫn đến phá hủy các mạch máu nhỏ, dày thất trái, dày lớp nội-trung mạc ĐM cảnh và bong mảng xơ vữa.
Các biến cố tim mạch cho thấy có liên quan đến những dạng phá hủy cơ quan đích khác nhau, sự khác biệt giữa ĐM lớn và nhỏ làm nặng hơn tình trạng phá hủy ĐM. Điều trị THA tác động trên cả ĐM lớn và nhỏ không chỉ cắt đứt quá trình phá hủy mà còn có thể tạo điều kiện cho con đường tái cấu trúc bằng thuốc ở cả ĐM lớn và nhỏ. Kết quả của hiệu quả mức đôi này là giảm áp lực trung tâm, giảm phá hủy cơ quan đích và các biến cố tim mạch.
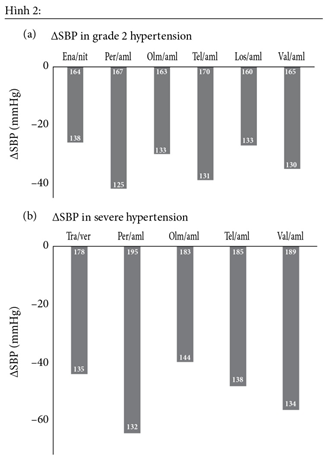
Hình 2: Giảm HA tâm thu trong 8-18 tuần với giá trị HA ban đầu và cuối trung bình[(màu trắng(mmHg)]của dạng kết hợp ức chế hệ RAA/ ức hế canxi ở BN THA độ 2(a) và ở BN THA nặng (b)Aml:Amlodipine;Ena,enalapril;Los,Losartan;Nit,nitrendipine;Olm,olmesartan;Per,Perindopril;Tel,telmisartan;Val,valsartan;Ver,verapamil
Ức chế men chuyển và ức chế canxi trong vòng xoán bệnh lý tim mạch tích hợp
Lợi ích của điều trị THA
Kết hợp ức chế RAAS với ức chế canxi là chiến lược hiệu quả giảm HA ở BN THA (hình 2). Nó cho thấy giảm HA một cách hiệu quả hơn so với điều trị riêng lẻ từng loại. Guideline THA Châu Âu đã khằng định cả ƯCMC và ức chế canxi là sự chọn lựa hiệu quả trong việc khởi đầu và duy trì trong điều trị THA dù là đơn trị liệu hay điều trị kết hợp. ƯCMC hạ HA bằng cách không cho men chuyển chuyển Angiotensin I sang Angiotensin II – chất co mạch mạnh và giới hạn sự thoái hóa bradykinin . Ức chế canxi hạ HA bằng cách chống co thắt cơ trơn của lớp áo giữa ĐM dẫn đến giãn mạch thụ động và hiệu quả này dường như có hiệu quả rất lớn trong việc hạ HA. Mặt khác một số nghiên cứu thử nghiệm so sánh giữa các ức chế RAAS cùng giảm mức HA giống nhau ở các nhóm thuốc khác nhau cho thấy kết quả khác biệt rõ ràng (bảng 1) và thấy rằng ƯCMC có hiệu quả tốt hơn ARB trong việc giảm những hậu quả THA.
Lợi ích ngoài giảm HA
Ức chế RAAS cho thấy có ích lợi trong nhiều giai đoạn xuyên suốt bệnh tim do xơ vữa. Chúng ngăn ngừa không cho Angiotensin II đóng vai trò cơ bản trong việc sinh ra bệnh mạch máu xơ vữa ở mức độ tại chỗ và hệ thống
ƯCMC còn có ưu thế hơn so với ƯCTT vì ngăn thoái hóa bradykinin, chất này tích tụ lại ở tế bào nội mạc, gia tăng hoạt động tổng hợp và thể hiện Nitric oxid (NO) tế bào. Nitric oxid có đặc tính giãn mạch, chống kết tụ, và chống tăng sản và ức chế sự di cư của TB cơ trơn do Angiotensin II
ƯCTT không giữ lại bradykinin và làm gia tăng nhiều Angiotensin II, gắn vào nhiều loại thụ thể. Do vậy nó không cho hiệu quả bảo vệ tim mạch giống như ƯCMC . Trong khi đó, ức chế canxi cho hiệu quả bảo vệ tim mạch tương ứng với khả năng giảm HA của nó, chúng cho thấy giảm đáng kể việc tái tưới máu, nhập viện do đau ngực, NMCT không tử vong, đột quỵ và cơn thoáng thiếu máu não ở BN HA bình thường có bệnh mạch vành
Lợi ích bổ sung
Về phương diện bệnh lí tim mạch, hiệu quả, giảm tác dụng phụ, ƯCMC và ức chế canxi phối hợp với nhau rất tốt. Hiệu quả điều trị phối kết hợp ƯCMC và ức chế canxi được mô tả trong nghiên cứu phân tích gộp 179 222 bệnh nhân THA hoặc nguy cơ cao cho thấy ƯCMC cho hiệu quả bảo vệ bệnh mạch vành và ức chế canxi phòng chống đột quỵ không phụ thuộc vào mức giảm huyết áp. Những nghiên cứu khác cũng cho thấy rằng sự kết hợp 2 nhóm thuốc này cho hiệu quả cũng cho hiệu quả bảo vệ mạch máu rất tốt. ƯCMC và ức chế canxi cho hiệu quả bảo vệ mạch máu bổ sung ở nhiều giai đoạn của chuỗi tim mạch tích hợp như được tóm tắt ở bảng 2. Khi những hiệu quả này kết hợp lại, chúng cho ra hiệu quả tốt trên lâm sàng như bằng chứng được báo cáo ở bảng 3.
Lợi ích tổng hợp của kết hợp liều cố định THA so phối hợp rời (phối hợp hai thuốc riêng rẻ) bao gồm đáp ứng nhanh hơn, hạ HA tốt hơn, kiểm soát HA tốt hơn và tuân thủ điều trị. Nhưng kết hợp ƯCMC và ức chế canxi còn có thể cho ưu thế bổ sung hơn nữa so với kết hợp những nhóm thuốc khác. Trong nghiên cứu phân tích gộp tiền cứu ngẫu nhiên kiểm soát đối chứng, ƯCMC dường như tốt hơn ƯCTT trong việc giảm phù ngoại biên ở BN dùng ức chế canxi (giảm nguy cơ 0.74;95%Cl 0.64-0.84;p<0.0001). Điều này dường như cũng được làm rõ trong nghiên cứu lâm sàng điều trị hạ HA tối ưu SYMBIO với liều kết hợp cố định perindopril/amlodipine thực hiện ở 2 132 BN HA không kiểm soát được, dung nạp kém với ƯCMC và ức chế canxi trước đó, trong đó điều trị kết hợp perindopril và amlodipine giảm 58% BN phù mắc cá chân do amlodipine.
Bảng 1: Nghiên cứu với độ giảm HA giống nhau, cho thấy những nhóm thuốc ức chế hệ RAA khác nhau cho hiệu quả mạch máu khác nhau
|
Nghiên cứu |
Dân số |
Điều trị |
HA ban đầu (mmHg) |
Độ chênh HA ΔBP(mmHg) |
Kết quả |
|
HOPE28 |
Bệnh tim mạch/nguy cơ |
Ramipril vs giả dược |
139/79 |
-3/-1 |
Ít tử vong do tim mạch, ít NMCT và đột quỵ |
|
EUROPA29 |
Bệnh tim mạch |
Perindopril vs giả dược |
137/82 |
-5/-2 |
Ít tử vong do tim mạch, ít NMCT |
|
ACCOMPLISH30 |
THA/nguy cơ tim mạch |
Benazepril/amlodipine vs benazepril/HCTZ |
145/80 |
-1/-1 |
Ít tử vong do tim mạch, ít NMCT và đột quỵ |
|
ASCOT-BPLA10 |
THA/nguy cơ tim mạch |
Perindopril/amlodipine vs atenolol/bendroflumethiazide |
164/95 |
-3/-2 |
Ít tử vong do tim mạch, ít NMCT và đột quỵ |
|
PEACE31 |
Bệnh tim mạch |
Trandolapril vs giả dược |
133/78 |
-3/-1 |
Không ý nghĩa |
|
PRoFESS32 |
Đột quỵ gần đây |
Telmisartan vs giả dược |
144/84 |
-4/-2 |
Không ý nghĩa |
|
ACTIVE 133 |
Nguy cơ đột quỵ/rung nhĩ |
Irbesartan vs giả dược |
138/83 |
-3/-2 |
Không ý nghĩa |
|
TRANSCEND34 |
Nguy cơ tim mạch |
Telmisartan vs giả dược |
141/82 |
-4/-2 |
Không ý nghĩa |
|
ONTARGET35 |
Nguy cơ tim mạch |
Telmisartan/ramipril vs ramipril |
142/82 |
-2/-1 |
Suy thận nhiều hơn |
|
ROADMAP36 |
ĐTĐ |
Olmesartan vs giả dược |
136/81 |
-3/-2 |
Ít tiểu microalbumin niệu, nhiều tử vong tim mạch với ARB |
|
ORIENT37 |
ĐTĐ |
Olmesartan vs giả dược |
141/78 |
-3/-2 |
Nhiều tử vong tim mạch với ARB |
|
ALTITUDE38 |
ĐTĐ |
Aliskiren vs giả dược |
137/74 |
-1/-0.5 |
Ít tiểu albumin niệu, nhiều biến cố tim thận |
Perindopril-amlodipine trong chuỗi tim mạch tích hợp
Lợi ích của điều trị THA
Perindopril hoạt động dựa trên ức chế tạo sản phẩm angiotensin II cho thấy rất hiệu quả trong việc hạ HA trong phần lớn dân số. So với những ƯCMC khác, perindopril có thời gian hoạt động kéo dài, và hiệu quả càng tăng khi tăng liều. ƯCTT mặc dù theo dõi HA di động 24 giờ cho thấy hiệu quả hạ áp có tăng lên khi tăng liều, tuy nhiên không nhiều. Perindopril còn có tác dụng bảo tồn tưới máu cơ quan
ƯCMC khác nhau có ái lực gắn vị trí men chuyển nội mạc người khác nhau; perindopril có tính chọn lọc cao nhất cho vị trí bám vào bradykinin so với các các ức chế men chuyển khác, điều này giải thích tại sao nó hiệu quả trong việc phòng chống tự hủy nội mạc. Những ƯCMC ái mỡ cao như là perindopril và ramipril còn hoạt động trên men chuyển mô, điều này giải thích sự khác nhau về tính chất xơ vữa giữa các thuốc ƯCMC.
Tương tự, ức chế canxi amlodipine là loại thuốc được dung nạp tốt trong đơn trị liệu hoặc điều trị kết hợp và cũng cho thấy là loại thuốc hạ áp hiệu quả, an toàn trong 24 giờ, đặc biệt trong THA tâm thu đơn độc. THA tâm thu đơn độc là bước mấu chốt trong bệnh tim mạch do lão hóa (hình 1). Bên cạnh làm chậm tiến triển bệnh tim mạch, điều trị THA còn tác động đến THA tâm thu đơn độc làm chậm tiến triển bệnh thận và bệnh não sa sút trí tuệ.
Kết hợp perindoril và amlodipine cho thấy giảm HA hiệu quả hơn là điều trị từng loại một, điều này được giải thích bằng bằng chứng là hai thuốc này có cơ chế tác động bổ sung cho nhau. Bảng 2 cho thấy những cơ chế hoạt động thông thường của hai nhóm này: ví dụ perindopril và amlodipine là những chất giãn mạch và làm tăng tổng hợp NO nội mô và NO. Bên cạnh chẹn kênh canxi, amlodipine còn cho ra hiệu quả hạ áp kèm theo qua việc kích thích tổng hợp NO điều hòa kinin. Tương phản với perindopril, amlodipine kích hoạt hoặc phóng thích kallikrein, chất này kích thích tổng hợp kinin. Perindopril phòng chống phân hủy kinin.
Hiệu quả lâm sàng của điều trị THA kết hợp giữa perindopril và amlodipine đã được nghiên cứu ở nhiều công trình, và những kết quả được tóm tắt ở bảng 3. Hiệu quả hạ áp của perindopril và amlodipine trong nghiên cứu ASCOT: amlodipine ± perindopril đi kèm hạ HA cánh tay ở BN THA có nguy cơ tim mạch khoảng 27.5/17.7 mmHg trong 5.5 năm . Amlodipine ± perindopril đi kèm có tác dụng một phần trong việc hạ HA cánh tay nhiều hơn mong đợi trong nghiên cứu quan sát so sánh với atenolol ± thiazid đi kèm. Để làm rõ điều này, một số nghiên cứu sâu ASCOT đã được thực hiện để xem làm thế nào Perindopril và amlodipine ảnh hưởng mục tiêu HA ngoài HA cánh tay như là HA trung tâm, sóng phản hồi HA, HA 24 giờ, HA ban đêm và dao động HA. Chúng cho thấy perindopril và amlodipine thực sự có tác động hiệu quả lên những thông số HA này.
Trong 2 199 BN trong nghiên cứu lượng giá chức năng động mạch chủ CAFE, khi dùng amlodipine ± perindopril đi kèm có một sư khác biệt rõ về giảm HA tâm thu ĐMC trung tâm (4.3mmHg;95% CI 3.3-5.4mmHg;p<0.0001) và hiệu áp ĐMC trung tâm (3.0mmHg;95% CI 2.1-3.9mmHg;p<0.0001), mặc dù sự giảm HA cánh tay là giống nhau khi dùng với atenolol ± thiazid đi kèm. Trong nghiên cứu về sóng phản hồi ĐM ở 259 BN, amlodipine ± perindopril giảm chỉ số sóng phản hồi nhiều hơn so với atenolol ± thiazide (20±11% so với 23±13%;p=0.02), bên cạnh hạ HA tâm thu ĐM cảnh , gần với HA tâm thu trung tâm một cách hiệu quả (127±12 so với 133± 15mmHg;p<0.0001). HA tâm thu ban đêm, yếu tố chỉ điểm cho những diễn tiến tim mạch và đột quỵ, đã được giảm nhiều hơn khi dùng amlodipine ± perindopril (Δ=2.2mmHg;95% CI-3.4 đến 0.9 mmHg) ở mỗi nghiên cứu riêng lẻ ASCOT trong 1 905 BN. Sự giảm HA ban đêm là 1 yếu tố dự đoán các biến cố tim mạch tốt hơn HA đo tại bệnh viện. Tuy nhiên cũng có ngoại lệ về sự giảm HA ban đêm: ví dụ thử nghiệm điểm cuối toàn bộ telmisartan một mình hoặc kết hợp với ramipril ONTARGET , trong đó HA tâm thu ban đêm giảm nhiều hơn bởi telmisartan hơn là so với ramipril (Δ -4.1mmHg;p<0.011), nhưng hiệu quả bảo vệ tim mạch của telmisartan lại không tốt hơn. Điều này minh họa sự khác nhau nhiều hơn về bảo vệ tim mạch giữa ƯCMC và ƯCTT . Phân tích sự thay đổi HA trong ASCOT cho thấy sự biến động HA trong thời gian dài ngắn và thời gian dài được giảm nhiều khi dùng amlodipine ± perindopril
Trong thực hành lâm sàng sự kết hợp trong một viên thuốc perindopril arginin-amlodipine đã khẳng định hiệu quả hoạt động bổ sung của perindopril và amlodipine bằng cách hạ HA một cách hiệu quả những trường hợp chưa đạt HA đích mặc dù đã điều trị trước đó với nhiều loại nhóm HA khác nhau (bảng 3). Viên thuốc kết hợp perindopril và amlodipine giảm HA di động trong 24 giờ đến 18.5/8.4mmHg từ 146.1/84.3mmHg ở BN ngoại trú THA nguyên phát không kiểm soát được (≥140/90 hoặc≥130/80mmHg vơi nguy cơ tim mạch cao hoặc rất cao) sau 3 tháng (p<0.0001) với 100% HA giảm ban ngày duy trì suốt đêm. Sự giảm HA với perindopril- amlodipine rất nhanh: sau 4 tuần, perindopril- amlodipine giảm HA được 26.8/16.1mmHg từ 159.5/99.mmHg (p<0.0001) ở 2 845 BN THA không điều trị(>160/100mmHg) hoặc THA không kiểm soát được bằng đơn trị liệu (>140/90mmHg). Kiểm soát HA (<140/90mmHg) đạt được ở 2 091 BN(73%)
Theo SYMBIO đã nêu ở trên, nghiên cứu bao gồm BN uống ƯCMC(77% BN) và ức chế canxi (59%), hoặc là từng viên riêng lẽ hoặc trong dạng kết hợp được chuyển qua trị liệu bằng viên phối hợp cố định perindopril-amlodipin (5/5, 5/10, 10/5 hoặc 10/10). Liều thuốc được xác định bởi những BS riêng biệt và được tăng liều cho đến khi tối ưu được điều trị THA. HA giảm đến 25.5/12.9mmHg từ 158.3/95mmHg sau 3 tháng; BN THA nặng nhất (giai đoạn 3) HA giảm đến 45.4/20mmHg. Kết quả tương tự cũng đạt được với liều cố định trong nghiên cứu STRONG- đánh giá tính an toàn và hiệu quả của perindopril- amlodipine ở bệnh nhán tăng huyết áp mới chẩn đoán hoặc chưa kiểm soát huyết áp, được thực hiện ở 1250 BN THA. Perindopril- amlodipine cũng cho thấy cải thiện huyết áp ở BN có nhiều bệnh tật đi kèm như là bệnh thận, ĐTĐ, tăng cholesterol máu
Bảng 2: Hiệu quả có lợi mạch máu của perindopril và amlodipine trong chuỗi tim mạch tích hợp 27,48-59
|
Giai đoạn xảy ra tác động lên mạch máu |
Hiệu quả có lợi trên mạch máu |
|
|
Perindopril |
Amlodipine |
|
|
Vòng xoắn bệnh lý tim mạch |
|
|
|
Yếu tố nguy cơ (THA)48 |
Tăng/giảm giãn mạch |
Tăng/giảm giãn mạch |
|
Giảm co mạch |
Tăng hoạt hóa tổng hợp NO nội mạc |
|
|
Tăng tổng hợp NO nội mạc |
Tăng tổng hợp NO |
|
|
Tăng tổng hợp NO |
|
|
|
Xơ vữa mạch vành 27,48,49 |
Giảm kết dính bạch cầu đơn nhân |
Giảm oxit hóa LDL |
|
Bệnh ĐM vành 27,48 |
Tăng chống tái cấu trúc |
Giảm kết tụ LDL thay đổi |
|
Tăng chức năng nội mạc |
Giảm tổng hợp metalloproteinase nền 1 |
|
|
Giảm tự tiêu |
|
|
|
Huyết khối mạch vành 27,48 |
Giảm tăng sản TB cơ trơn |
Giảm tăng sản TB cơ trơn |
|
Nhồi máu cơ tim 27,48 |
Giảm phát triển TB cơ trơn |
Giảm di nhập TB cơ trơn |
|
Giảm di nhập TB cơ trơn |
Tăng hoạt động yếu tố hoạt hóa plasminogen mô |
|
|
Thoái sản chất nền |
|
|
|
Tăng hoạt động yếu tố hoạt hóa plasminogen mô (tPA) |
||
|
Giảm những chất ức chế 1 hoạt hóa plasminogen mô (PAI-1) |
||
|
Vòng xoắn bệnh lý lão hóa |
|
|
|
THA tâm thu đơn độc 50,58 |
Giảm HA tâm thu ĐMC trung tâm |
Giảm HA tâm thu ĐMC trung tâm |
|
Giảm độ chênh áp lực mạch ĐMC trung tâm |
Giảm độ chênh áp lực mạch ĐMC trung tâm |
|
|
|
Giảm mạnh HA tâm thu |
|
|
Mất cân bằng cung/cầu oxy cơ tim |
Tăng dự trữ mạch vành |
Giảm kháng lực mạch vành |
|
Tăng tối đa lưu lượng máu mạch vành |
|
|
|
Vòng tim mạch xơ vữa/lão hóa tích hợp |
|
|
|
Dày thất trái 52,58 |
Giảm chỉ số khối cơ thất trái |
Giảm chỉ số khối cơ thất trái |
|
Thiếu máu cơ tim 48,53,59 |
Giảm điểm vận động vùng thất trái |
Tăng lưu lượng mạch vành |
|
|
Giảm độ thay đổi ST chênh |
Giảm ST chênh xuống |
|
Tái cấu trúc thất 54 |
Giảm tái cấu trúc thất |
|
|
Suy tim xung huyết 55 |
Giảm tỉ lệ tim lồng ngực |
|
Bảng 3 : Lợi ích của phối hợp perindopril và amlodipine10,16,29,59-65
|
Nghiên cứu |
n |
Dân số |
Thời gian nghiên cứu |
Điều trị |
Kết quả quan trọng của perindopril và amlodipine |
|
DIAMOND50 |
2845 |
THA không kiểm soát được bằng đơn trị liệu hoặc THA chưa điều trị |
4 tuần |
FDC perindopril/amlodipinea |
HA giảm từ 159.5/99.3 xuống 132.7/83.2 mmHg(p<0.001);gần ¾(73%) đạt HA mục tiêu |
|
STRONG16 |
1250 |
THA |
60 ngày |
FDC perindopril/amlodipine 4/5mg |
HA giảm đến 41.9/23.2 mmHg từ 167.4/101.4 mmHg(p<0.0001);HA mục tiêu đạt được 2/3 (66.1%) |
|
Makani et al.61 |
17206 |
Phân tích gộp THA có phù ngoại biên do dùng ức chế canxi |
9 tuần |
Ức chế RAAS/ức chế canxi vs ức chế canxi |
Ức chế RAAS/ức chế canxi giảm nguy cơ phù do ức chế canxi so với ức chế canxi đơn độc, ƯCTT ít hiệu quả hơn ƯCMC về hiệu quả giảm phù |
|
CAPE59 |
250 |
Đau thắt ngực ổn định |
10 tuần |
Amlodipine 5/10mg |
ST chênh xuống giảm 60% so với 44% dùng giả dược(p=0.025);đau ngực(p=0.042) và sử dụng nitroglycerine(p=0.0006) cũng giảm |
|
SYMBIO62 |
2132 |
THA không kiểm soát được bằng ƯCMC và/hoặc ức chế canxi |
3 tháng |
FDC perindopril/amlodipinea |
HA giảm từ 158.5/93.6 xuống còn 132.9/80.7 mmHg(p<0.0001);hầu hết ¾ (74%) đạt được HA mục tiêu; ban đầu,15% BN điều trị amlodipine có phù mắt cá;sau 3 tháng phù giảm 58%(6%;p<0.001) |
|
PRORYV63 |
2249 |
THA |
3 tháng |
FDC perindopril/amlodipinea |
HA giảm từ 168.97 xuống 132/80mmHg(p<0.001);80% đạt HA mục tiêu |
|
PEAR64 |
262 |
THA |
3 tháng |
FDC perindopril/amlodipinea |
HA 24 giờ giảm từ 146.1/84.3xuo61ng 127.6/75.9 mmHg(p<0.001);HA bệnh viện giảm từ 159.8/94.3 xuống 131.1/80.0 mmHg(p<0.001) |
|
EUROPA29 |
12218 |
Bệnh tim mạch vành mạn |
4 năm |
Perindopril 8mg vs giả dược |
Điểm cuối nguyên phát c giảm20% so với giả dược(p=0.0003); perindopril giảm NMCT không tử vong 22%(p=0.001) |
|
EUROPA CCB65 |
2122 |
Bệnh tim mạch vành mạn |
4 năm |
Perindopril/ức chế canxi vs giả dược/ức chế canxi |
Điểm cuối nguyên phát c giảm 35% (p<0.05) thêm perindopril vào amlodipine giảm tỉ lệ tử vong do mọi nguyên nhân 46%(p<0.01) |
|
ASCOT-BPLA10 |
19257 |
THA nguy cơ cao với ≥3 yếu tố nguy cơ |
5 năm |
Amlodipine 5/10mg± perindopril 4/8mg |
Tỉ lệ tử vong do tim mạch giảm 24% so với atenolol±lợi tiểu (p=0.007); tỉ lệ tử vong do mọi nguyên nhân giảm 11%(p=0.0247) |
Lợi ích ngoài điều trị THA
Trong vòng xoắn bệnh lý tim mạch xơ vữa, perindopril giảm thoái hóa và kết dính của TB bạch cầu đơn nhân, có hiệu quả chống tái cấu trúc và cải thiện chức năng nội mạc. Perindopril cũng cho thấy làm giảm kích thước mảng xơ vữa không vôi hóa ở BN bệnh mạch vành. Amlodipine có hiệu quả mạch máu bổ sung trong xơ vữa mạch vành và bệnh mạch vành, giảm LDL oxi hóa, kết tụ LDL và metalloproteinase . Trong nghiên cứu PREVENT lượng giá ngẩu nhiên tiền cứu ảnh hưởng mạch máu, amlodipine giảm sự tiến triển xơ vữa ở ĐM cảnh và nhóm BN có HA tâm thu lớn hơn trung bình. Trong nghiên cứu NORMALISE đánh giá amlodipine làm thoái lui sang thương xơ vữa bằng siêu âm nội mạch máu khi so sánh amlodipine và enalapril trong việc ngăn ngừa huyết khối CAMELOT, sự thay đổi về thể tích mảng xơ vữa được đo bằng siêu âm nội mạch thì thấp hơn khi dùng amlodipine so với giả dược. Bằng cách ngăn ngừa phản ứng gốc tự do xảy ra ở tế bào màng cơ trơn mạch máu, amlodipine ngăn ngừa oxi hóa LDL và phospholipid màng, qua đó cản trở hình thành tết bào bọt, rối loạn chức năng nội mạc và phản ứng viêm. Cực dương của amlodipine cắt đứt hình thành TB bọt bằng cách không cho LDL đã điều chỉnh kết tụ lại.
Huyết khối mạch vành và NMCT được hạn chế bởi peridopril và amlodipine bằng con đường làm giảm sự tăng sản và di cư của tế bao cơ trơn , và gia tăng hoạt động yếu tố hoạt hóa plasminogen mô. Perindopril cũng làm chậm sư tăng trưởng tế bào cơ trơn , phòng chống thoái hóa nền và làm chậm ức chế hoạt hóa plasminogen.
Trong vòng xoắn bệnh lý tim mạch do lão hóa (hình 1), sự giảm tương đối về sóng phản hồi áp lực khi uống amlodipine ± perindopril đi kèm đóng vai trò trong việc phòng chống THA tâm thu đơn độc và dày thất trái. Hơn nữa cả amlodipine và perindopril làm mất đi sự mất cân bằng cung cầu oxy cơ tim: perindopril tăng lượng dự trữ mạch vành và tối ưu lưu lượng máu mạch vành và amlodipine giảm kháng lực mạch máu mạch vành.
Perindopril và amlodipine còn có thể làm chậm tiến triển bệnh tim mạch. Cả perindopril và amlodipine đều làm giảm dày thất trái và thiếu máu cơ tim (bảng 2). Trong thiếu máu cơ tim, perindopril làm giảm số điểm vận động vùng thất trái và biên độ thay đổi ST chênh, trong khi đó amlodipine cải thiện lưu lượng mạch vành và giảm tỉ lệ ST chênh xuống 48,53,59. Perindopril còn có thể làm giảm tiến triển của bệnh tim nặng bằng cách giảm tái cấu trúc thất và tỉ lệ tim thành ngực trong suy tim xung huyết.
Những ích lợi trên cho thấy đơn trị liệu perindopril hoặc amlodipine làm giảm nguy cơ tim mạch. Nghiên cứu của châu Âu 4 năm về giảm các biến cố tim mạch khi dùng perindopril ở bệnh ĐM vành ổn định(EUROPA) thực hiện ở 12 218 BN nguy cơ thấp không có suy tim, điều trị đơn trị liệu perindopril liều cao làm giảm điểm cuối nguyên phát tử vong kết hợp, NMCT không tử vong và ngưng tim hồi sức 20% so với giả dược (p<0.0003 bảng 3). Đơn trị liệu amlodipine giảm nguy cơ tim mạch ở BN bệnh mạch vành ổn định: ở 1991 BN với HA bình thường (HA tâm trương <100mm Hg) và bệnh mạch vành (hẹp >20%), BN uống amlodipine ngày 1 lần(n=663) hơn 2 năm ít có biến cố tim mạch hơn so với giả dược[n=655;16.6 so với 23.1%, hazard ratio(HR) 0.69; 95% CI 0.54-0.88;p=0.003]. Điều này thấy rõ qua giảm 42% nhập viện do đau ngực (HR 0.58;95% CI 0.41-0.82;p=0.002) và giảm 27% tái tưới máu mạch vành (HR 0.73;95% CI 0.54 – 0.98;p=0.03).
Yếu tố nguy cơ tim mạch giảm khi perindopril dùng kết hợp với ức chế canxi dihydropidine. Sự so sánh giữa EUROPA bệnh mạch vành ổn định uống perindopril – ức chế canxi (n=1022) hoặc giả dược- ức chế canxi (n=1100), ở mỗi lần thăm khám đều thấy perinndopril-ức chế canxi giảm tử vong do mọi nguyên nhân 46% (p<0.01) và những điểm cuối nguyên phát- tử vong tim mạch, NMCT không tử vong và ngưng tim hồi sức 35% (p<0.05). Những nhà nghiên cứu kết luận rằng bởi vì kê toa chẹn beta phổ biến chiếm hơn một nữa số bệnh nhân, nên chẹn canxi dihydropyridine như amlodipine hoặc nifedipine là loại thuốc thường được cho nhiều nhất đi kèm. Đương nhiên phải luôn nhớ kĩ là kết quả tốt thấy được với perindopril và amlodipine rút ra từ phân tích hậu định; do vậy ức chế canxi không thể xác định được và sự sử dụng thường xuyên dihydropyridine là có lí nhưng chưa được chứng minh. Kết quả từ ASCOT đã bảo vệ những kết luận này và đề nghị rằng amlodipine ± perindopril có thể làm giảm biến cố ở BN THA có nhiều yếu tố nguy cơ.Trong nghiên cứu so sánh với atenolol ± thiazide, amlodipine ± thiazide giảm các biến cố tim mạch tổng cộng và thủ thuật 16% (HR 0.84; 95% CI 0.78-0.90;p<0.0001) và tử vong tim mạch, NMCT, đột quỵ 16%(HR 0.84; 95% CI 0.76-0.92;p=0.0003).
Việc giảm tỉ lệ tử vong do tim mạch và mọi nguyên nhân trong nghiên cứu ASCOT khi dùng amlodipine ± perindopril so với atenolol ± lợi tiểu thiazide thúc đẩy cho ra viên thuốc kết hợp perindopril và amlodipine(bảng 3)10
Lợi ích đi kèm
Cùng với việc đáp ứng nhanh, hạ HA, kiểm soát HA tốt và tuân thủ điều trị, liều cố định perindopril-amlodipine có hiệu quả tích cực trong nhiều giai đoạn của chuỗi tim mạch tích hợp hơn là đơn trị liệu amlodipine (hình 2). Phối hợp này còn mang lại hiệu quả bảo vệ cộng thêm chống lại tái cấu trúc thất và suy tim sung huyết. Điều trị kết hợp thường luôn cho kết cục tốt, mặc dù nó cũng tác động cùng một số giai đoạn giống như đơn trị liệu perindopril. Kê toa thuốc perindopril và amlodipine sớm rất quan trọng bởi vì hầu hết ích lợi điều trị 2 nhóm thuốc này thường xảy ra ở giai đoạn sớm hoặc giữa của chuỗi tim mạch tích hợp (hình 2)
Tóm lại, sử dụng sớm perindopril –amlodipine có nhiều ưu thế ích lợi quan trọng so với đơn trị liệu về mặt điều trị THA, đáp ứng nhanh với điều trị, độ bao phủ bệnh tim mạch, hiệu quả bổ sung về dược lí và giảm tác dụng phụ
Kết luận
Kết hợp vòng xoắn bệnh lý lão hóa và bệnh tim mạch do xơ vữa đã có trước đây là một cách mới để hiểu về bệnh tim mạch. Chiến lược dựa trên sự kết hợp ƯCMC và ức chế canxi (ASCOT kết hợp amlodipine ± perindopril) nhằm vào nhiều giai đoạn của chuỗi tim mạch tích hợp, cho thấy làm chậm tiến triển bệnh học bệnh tim mạch và có hiệu quả trên lâm sàng . Chiến lược này không chỉ kiểm soát huyết áp hiệu quả mà còn làm giảm các ảnh hưởng của bệnh ở nhiều giai đoạn trong vòng xoắn tim mạch tích hợp.
Tài liệu tham khảo
1 Mancia G, Fagard R, Narkiewicz K, et al. 2013 ESH/ESC Guidelines for the management of arterial hypertension: the Task Force for the management of arterial hypertension of the European Society of Hypertension (ESH) and of the European Society of Cardiology (ESC). Eur Heart J 2013; 34:2159– 2219.
2 Rapsomaniki E, Timmis A, George J, et al. Blood pressure and incidence of twelve cardiovascular diseases: lifetime risks, healthy life-years lost, and age-specific associations in 1.25 million people. Lancet 2014; 383:1899–1911.
3 Conroy RM, Pyorala K, Fitzgerald AP, et al. Estimation of ten-year risk of fatal cardiovascular disease in Europe: the SCORE project. Eur Heart J 2003; 24:987–1003.
4 Blacher J, Evans A, Arveiler D, et al. Residual cardiovascular risk in treated hypertension and hyperlipidaemia: the PRIME Study. J Hum Hypertens 2010; 24:19–26.
5 Dzau VJ, Antman EM, Black HR, et al. The cardiovascular disease continuum validated: clinical evidence of improved patient outcomes. Part I. Pathophysiology and clinical trial evidence (risk factors through stable coronary artery disease). Circulation 2006; 114:2850–2870.
6 Dzau VJ, Antman EM, Black HR, et al. The cardiovascular disease continuum validated: clinical evidence of improved patient outcomes. Part II. Clinical trial evidence (acute coronary syndromes through renal disease) and future directions. Circulation 2006; 114:2871–2891.
7 O’Rourke MF, Safar ME, Dzau V. The Cardiovascular Continuum extended: aging effects on the aorta and microvasculature. Vasc Med 2010; 15:461– 468.
8 Gupta M, Honos GN, Velazquez EJ, Chung N, Oigman W, Maggioni AP. Evidence for the efficacy of ARBs across the cardiovascular continuum. Curr Med Res Opin 2010; 26:1203–1218.
9 Ferrari R, Boersma E. The impact of ACE inhbition on all-cause and cardiovascular mortality in contemporary hypertension trials: a review. Expert Rev Cardiovasc Ther 2013; 11:705–717.
10 Dahlof B, Sever PS, Poulter NR, et al. Prevention of cardiovascular events with an antihypertensive regimen of amlodipine adding perindopril as required versus atenolol adding bendroflumethiazide as required, in the Anglo-Scandinavian Cardiac Outcomes Trial-Blood Pressure Lowering Arm (ASCOT-BPLA): a multicentre randomised controlled trial. Lancet
2005; 366:895–906.
11 Gupta AK, Nasothimiou EG, Chang CL, Sever PS, Dahlof B, Poulter NR. Baseline predictors of resistant hypertension in the Anglo-Scandinavian Cardiac Outcome Trial (ASCOT): a risk score to identify those at high-risk. J Hypertens 2011; 29:2004–2013.
12 Rubio-Guerra AF, Lozano-Nuevo JJ, Vargas-Ayala G, Rodriguez-Lopez L, Ramos-Brizuela LM, Escalante-Acosta BA. Efficacy of a fixed-dose combination of trandolapril–verapamil in obese hypertensive patients resistant to monotherapy. Clin Exp Hypertens 2006; 28:619–624.
13 Oparil S, Melino M, Lee J, Fernandez V, Heyrman R. Triple therapy with olmesartan medoxomil, amlodipine besylate, and hydrochlorothiazide in adult patients with hypertension: The TRINITY multicenter, randomized, double-blind, 12-week, parallel-group study. Clin Ther 2010; 32:1252–1269.
14 Neutel JM, Mancia G, Black HR, et al. Single-pill combination of telmisartan/amlodipine in patients with severe hypertension: results from the TEAMSTA severe HTN study. J Clin Hypertens (Greenwich) 2012; 14:206–215.
15 Chazova IE, Dongre N, Vigdorchik AV. Real-life safety and effectiveness of amlodipine/valsartan combination in the treatment of hypertension. Adv Ther 2011; 28:134–149.
16 Bahl VK, Jadhav UM, Thacker HP. Management of hypertension with the fixed combination of perindopril and amlodipine in daily clinical practice: results from the STRONG prospective, observational, multicenter study. Am J Cardiovasc Drugs 2009; 9:135–142.
17 Pareek A, Chandurkar NB, Sharma R, Tiwari D, Gupta BS. Efficacy and tolerability of a fixed-dose combination of metoprolol extended release/amlodipine in patients with mild-to-moderate hypertension: a randomized, parallel-group, multicentre comparison with losartan plus amlodipine. Clin Drug Investig 2010; 30:123–131.
18 De la Sierra A, Roca-Cusachs A, Redon J, et al. Effectiveness and tolerability of fixed-dose combination enalapril plus nitrendipine in hypertensive patients: results of the 3-month observational, postmarketing, multicentre, prospective CENIT study. Clin Drug Investig 2009; 29:459–469.
19 Arif AF, Kadam GG, Joshi C. Treatment of hypertension: postmarketing surveillance study results of telmisartan monotherapy, fixed dose combination of telmisartan þ hydrochlorothiazide/amlodipine. J Indian Med Assoc 2009; 107:730–733.
20 Bramlage P, Wolf WP, Stuhr T, et al. Effectiveness and tolerability of a fixeddose combination of olmesartan and amlodipine in clinical practice. Vasc Health Risk Manag 2010; 6:803–811.
21 Probstfield JL, O’Brien KD. Progression of cardiovascular damage: the role of renin–angiotensin system blockade. Am J Cardiol 2010; 105:10A–20A.
22 Ferrari R, Fox K. Insight into the mode of action of ACE inhibition in coronary artery disease: the ultimate ‘EUROPA’ story. Drugs 2009; 69:265–277.
23 Nilsson PM, Boutouyrie P, Cunha P, et al. Early vascular ageing in translation: from laboratory investigations to clinical applications in cardiovascular prevention. J Hypertens 2013; 31:1517–1526.
24 Safar ME, Struijker-Boudier HA. Cross-talk between macro- and microcirculation. Acta Physiol (Oxf) 2010; 198:417–430.
25 Safar ME, Blacher J, Jankowski P. Arterial stiffness, pulse pressure, and cardiovascular disease-is it possible to break the vicious circle? Atherosclerosis 2011; 218:263–271.
26 Redon J, Trenkwalder PR, Barrios V. Efficacy of combination therapy with angiotensin-converting enzyme inhibitor and calcium channel blocker in hypertension. Expert Opin Pharmacother 2013; 14:155–164.
27 Mason RP, Marche P, Hintze TH. Novel vascular biology of third-generation L-type calcium channel antagonists: ancillary actions of amlodipine. Arterioscler Thromb Vasc Biol 2003; 23:2155–2163.
28 Yusuf S, Sleight P, Pogue J, Bosch J, Davies R, Dagenais G. Effects of an angiotensin-converting-enzyme inhibitor, ramipril, on cardiovascular events in high-risk patients. The Heart Outcomes Prevention Evaluation Study Investigators. N Engl J Med 2000; 342:145–153.
29 Fox KM. Efficacy of perindopril in reduction of cardiovascular events among patients with stable coronary artery disease: randomised, double-blind, placebo-controlled, multicentre trial (the EUROPA study). Lancet 2003; 362:782–788. 30 Jamerson K, Weber MA, Bakris GL, et al. Benazepril plus amlodipine or hydrochlorothiazide for hypertension in high-risk patients. N Engl J Med 2008; 359:2417–2428.
31 Braunwald E, Domanski MJ, Fowler SE, et al. Angiotensin-convertingenzyme inhibition in stable coronary artery disease. N Engl J Med 2004; 351:2058–2068.
32 Yusuf S, Diener HC, Sacco RL, et al. Telmisartan to prevent recurrent stroke and cardiovascular events. N Engl J Med 2008; 359:1225–1237.
33 Yusuf S, Healey JS, Pogue J, et al. Irbesartan in patients with atrial fibrillation. N Engl J Med 2011; 364:928–938.
34 Yusuf S, Teo K, Anderson C, et al. Effects of the angiotensin-receptor blocker telmisartan on cardiovascular events in high-risk patients intolerant to angiotensin-converting enzyme inhibitors: a randomised controlled trial. Lancet 2008; 372:1174–1183.
35 Yusuf S, Teo KK, Pogue J, et al. Telmisartan, ramipril, or both in patients at high risk for vascular events. N Engl J Med 2008; 358:1547–1559.
36 Haller H, Ito S, Izzo JL Jr, et al. Olmesartan for the delay or prevention of microalbuminuria in type 2 diabetes. N Engl J Med 2011; 364:907–917.
37 Imai E, Chan JC, Ito S, et al. Effects of olmesartan on renal and cardiovascular outcomes in type 2 diabetes with overt nephropathy: a multicentre, randomised, placebo-controlled study. Diabetologia 2011; 54:2978–2986.
38 Parving HH, Brenner BM, McMurray JJ, et al. Cardiorenal end points in a trial of aliskiren for type 2 diabetes. N Engl J Med 2012; 367:2204–2213.
39 Van Vark LC, Bertrand M, Akkerhuis KM, et al. Angiotensin-converting enzyme inhibitors reduce mortality in hypertension – a meta-analysis of randomized clinical trials of renin–angiotensin–aldosterone-system inhibitors involving 158,998 patients. Eur Heart J 2012; 33:2088–2097.
40 Gonzalez-Juanatey JR, Cordero A. Benefits of delapril in hypertensive patients along the cardiovascular continuum. Expert Rev Cardiovasc Ther 2013; 11:271–281.
41 Ferrari R, Rosano GM. Not just numbers, but years of science: putting the ACE inhibitor–ARB meta-analyses into context. Int J Cardiol 2013; 166:286–288.
42 Strauss MH, Hall AS. Angiotensin receptor blockers may increase risk of myocardial infarction: unraveling the ARB-MI paradox. Circulation 2006; 114:838–854.
43 Ruilope LM. Telmisartan for the management of patients at high cardiovascular risk. Curr Med Res Opin 2011; 27:1673–1682.
44 Nicholls SJ, Bakris GL, Kastelein JJ, et al. Effect of aliskiren on progression of coronary disease in patients with prehypertension: the AQUARIUS randomized clinical trial. JAMA 2013; 310:1135–1144.
45 Nissen SE, Tuzcu EM, Libby P, et al. Effect of antihypertensive agents on cardiovascular events in patients with coronary disease and normal blood pressure: the CAMELOT study: a randomized controlled trial. JAMA 2004; 292:2217–2225.
46 Verdecchia P, Reboldi G, Angeli F, et al. Angiotensin-converting enzyme inhibitors and calcium channel blockers for coronary heart disease and stroke prevention. Hypertension 2005; 46:386–392.
47 Turnbull F. Effects of different blood-pressure-lowering regimens on major cardiovascular events: results of prospectively-designed overviews of randomised trials. Lancet 2003; 362:1527–1535.
48 Ferrari R. Optimizing the treatment of hypertension and stable coronary artery disease: clinical evidence for fixed-combination perindopril/ amlodipine. Curr Med Res Opin 2008; 24:3543–3557.
49 Ferrari R, Bertrand ME, Remme WJ, Simoons ML, Deckers JW, Fox KM. Insight into ACE inhibition in the prevention of cardiac events in stable coronary artery disease: the EUROPA trial. Expert Rev Cardiovasc Ther 2007; 5:1037–1046.
50 Williams B, Lacy PS, Thom SM, et al. Differential impact of blood pressurelowering drugs on central aortic pressure and clinical outcomes: principal results of the Conduit Artery Function Evaluation (CAFE) study. Circulation 2006; 113:1213–1225.
51 Schwartzkopff B, Brehm M, Mundhenke M, Strauer BE. Repair of coronary arterioles after treatment with perindopril in hypertensive heart disease. Hypertension 2000; 36:220–225. Extended cardiovascular continuum Borghi et al. 9
52 Schulte KL, Meyer-Sabellek W, Liederwald K, van Gemmeren D, Lenz T, Gotzen R. Relation of regression of left ventricular hypertrophy to changes in ambulatory blood pressure after long-term therapy with perindopril versus nifedipine. Am J Cardiol 1992; 70:468–473.
53 Morishita T, Tsutsui M, Shimokawa H, et al. Long-term treatment with perindopril ameliorates dobutamine-induced myocardial ischemia in patients with coronary artery disease. Jpn J Pharmacol 2002; 88:100–107.
54 Ferrari R. Effects of angiotensin-converting enzyme inhibition with perindopril on left ventricular remodeling and clinical outcome: results of the randomized Perindopril and Remodeling in Elderly with Acute Myocardial Infarction (PREAMI) Study. Arch Intern Med 2006; 166:659–666.
55 Bounhoure JP, Bottineau G, Lechat P, Garnham J, Lapeyre G. Value of perindopril in the treatment of chronic congestive heart failure. Clin Exp Hypertens 1989; A11:575–586.
56 Levine CB, Fahrbach KR, Frame D, et al. Effect of amlodipine on systolic blood pressure. Clin Ther 2003; 25:35–57.
57 Perondi R, Saino A, Zanchetti A, Mancia G. Coronary vascular reactivity and calcium antagonist therapy in patients with angina. J Cardiovasc Pharmacol 1994; 24 (Suppl. A):S30–S36.
58 Islim IF, Watson RD, Ihenacho HN, Ebanks M, Singh SP. Amlodipine: effective for treatment of mild to moderate essential hypertension and left ventricular hypertrophy. Cardiology 2001; 96 (Suppl. 1):10–18.
59 Deanfield JE, Detry JM, Lichtlen PR, Magnani B, Sellier P, Thaulow E. Amlodipine reduces transient myocardial ischemia in patients with coronary artery disease: double-blind Circadian Anti-Ischemia Program in Europe (CAPE Trial). J Am Coll Cardiol 1994; 24:1460–1467.
60 Ahmed M. Efficacy and safety of a perindopril/amlodipine-based titration regimen on blood pressure goal achievement in hypertensive untreated patients or uncontrolled on monotherapy. 2012. In: 22nd European Meeting on Hypertension and Cardiovascular Protection; London, UK; 26–29 April 2012; abstract no. 1839.
61 Makani H, Bangalore S, Romero J, Wever-Pinzon O, Messerli FH. Effect of renin–angiotensin system blockade on calcium channel blockerassociated peripheral edema. Am J Med 2011; 124:128–135.
62 Hatala R, Pella D, Hatalova K, Sidlo R. Optimization of blood pressure treatment with fixed-combination perindopril/amlodipine in patients with arterial hypertension. Clin Drug Investig 2012; 32:603–612.
63 Karpov Y. Efficacy and tolerability of perindopril/amlodipine combination in patients with uncontrolled hypertension. 2012. In: 22nd European Meeting on Hypertension and Cardiovascular Protection; London, UK; 26–29 April 2012; abstract No. 947.
64 Nagy VL. Twenty-four-hour ambulatory blood pressure reduction with a perindopril/amlodipine fixed-dose combination. Clin Drug Investig 2013; 33:469–476.
65 Bertrand ME, Ferrari R, Remme WJ, Simoons ML, Deckers JW, Fox KM. Clinical synergy of perindopril and calcium-channel blocker in the prevention of cardiac events and mortality in patients with coronary artery disease. Post hoc analysis of the EUROPA study. Am Heart J 2010; 159:795–802.
66 Egan BM, Bandyopadhyay D, Shaftman SR, Wagner CS, Zhao Y, Yu-Isenberg KS. Initial monotherapy and combination therapy and hypertension control the first year. Hypertension 2012; 59:1124–1131.
67 Guo W, Turlapaty P, Shen Y, et al. Clinical experience with perindopril in patients nonresponsive to previous antihypertensive therapy: a large US community trial. Am J Ther 2004; 11:199–205.
68 Julius S, Cohn JN, Neutel J, et al. Antihypertensive utility of perindopril in a large, general practice-based clinical trial. J Clin Hypertens (Greenwich) 2004; 6:10–17.
69 Dinicolantonio JJ, Lavie CJ, O’Keefe JH. Not all angiotensin-converting enzyme inhibitors are equal: focus on ramipril and perindopril. Postgrad Med 2013; 125:154–168.
70 Tsoukas G, Anand S, Yang K. Dose-dependent antihypertensive efficacy and tolerability of perindopril in a large, observational, 12-week, general practice-based study. Am J Cardiovasc Drugs 2011; 11:45–55.
71 Makani H, Bangalore S, Supariwala A, Romero J, Argulian E, Messerli FH. Antihypertensive efficacy of angiotensin receptor blockers as monotherapy as evaluated by ambulatory blood pressure monitoring: a meta-analysis. Eur Heart J 2014; 35:1732–1742.
72 Walters MR, Bolster A, Dyker AG, Lees KR. Effect of perindopril on cerebral and renal perfusion in stroke patients with carotid disease. Stroke 2001; 32:473–478.
73 Ceconi C, Francolini G, Olivares A, Comini L, Bachetti T, Ferrari R. Angiotensin-converting enzyme (ACE) inhibitors have different selectivity for bradykinin binding sites of human somatic ACE. Eur J Pharmacol 2007; 577:1–6.
74 Valcarcel Y, Jimenez R, Hernandez V, Aristegui R, Gil A. Efficacy and safety of amlodipine: a comparative study of hypertensive patients treated at primaryand specialised-care centres. Clin Drug Investig 2006; 26:125–133.
75 Mourad JJ. Which patients benefit the most from the perindopril/amlodipine combination? J Hypertens 2011; 29 (Suppl. 1):S23–S28.
76 Ferrari R, Ceconi C. The combination of perindopril/amlodipine for the management of hypertension with or without coronary artery disease. Med Prog 2011; 8:286–296.
77 Manisty CH, Zambanini A, Parker KH, et al. Differences in the magnitude of wave reflection account for differential effects of amlodipine- versus atenololbased regimens on central blood pressure: an Anglo-Scandinavian Cardiac Outcome Trial substudy. Hypertension 2009; 54:724–730.
78 Dolan E, Stanton AV, Thom S, et al. Ambulatory blood pressure monitoring predicts cardiovascular events in treated hypertensive patients – an AngloScandinavian cardiac outcomes trial substudy. J Hypertens 2009; 27:876–885.
79 Mancia G, Parati G, Bilo G, et al. Ambulatory blood pressure values in the Ongoing Telmisartan Alone and in Combination with Ramipril Global Endpoint Trial (ONTARGET). Hypertension 2012; 60:1400–1406.
80 Bruining N, de Winter S, Roelandt JR, et al. Coronary calcium significantly affects quantitative analysis of coronary ultrasound: importance for atherosclerosis progression/regression studies. Coron Artery Dis 2009; 20:409–414.
81 Pitt B, Byington RP, Furberg CD, et al. Effect of amlodipine on the progression of atherosclerosis and the occurrence of clinical events. PREVENT Investigators. Circulation 2000; 102:1503–1510.
82 Brener SJ, Ivanc TB, Poliszczuk R, et al. Antihypertensive therapy and regression of coronary artery disease: insights from the Comparison of Amlodipine versus Enalapril to Limit Occurrences of Thrombosis (CAMELOT) and Norvasc for Regression of Manifest Atherosclerotic Lesions by Intravascular Sonographic Evaluation (NORMALISE) trials. Am Heart J 2006; 152:1059–1063.







