TÓM LƯỢC
TỔNG QUAN Thử nghiệm PEGASUS-TIMI 54 – Phòng ngừa biến cố tim mạch bằng Ticagrelor so với giả dược trên bệnh nhân có tiền sử nhồi máu cơ tim (NMCT) đang sử dụng Aspirin ngừa huyết khối – nghiên cứu hai liều Ticagrelor, 90mg hai lần mỗi ngày và 60mg hai lần mỗi ngày, với mục đích phòng ngừa lâu dài biến cố thiếu máu cục bộ trên bệnh nhân có tiền sử NMCT.
(Storey RF, Angiolillo DJ, Bonaca MP, Thomas MR, Judge HM, Rollini F, Franchi F, Ahsan AJ, Bhatt DL, Kuder JF, Steg PG, Cohen M,
Muthusamy R, Braunwald E, Sabatine MS. Platelet Inhibition With Ticagrelor 60 mg Versus 90 mg Twice Daily in the PEGASUS-TIMI 54 Trial.
J Am Coll Cardiol. 2016 Mar 15;67(10):1145-54.)
Lược dịch:ThS. BS. Hồ Minh Tuấn
Cả hai liều đều làm giảm tỉ lệ biến cố thiếu máu cục bộ so với giả dược. Dược động học (PK) và dược lực học (PD) liều Ticagrelor 60mg chưa từng được nghiên cứu.
MỤC TIÊU Trong nghiên cứu này, các tác giả nghiên cứu dược động học và dược lực học của ticagrelor, so sánh giữa 2 liều – 60mg hai lần mỗi ngày và 90 mg hai lần mỗi ngày.
PHƯƠNG PHÁP Tổng cộng 180 bệnh nhân nhận hơn 4 tuần thuốc nghiên cứu được lấy mẫu máu vào buổi sáng và lập lại sau 2 giờ. Tất cả bệnh nhân đều dùng Aspirin. Nồng độ ticagrelor và chất chuyển hóa có hoạt tính AR-C124910XX đã được xác định. Chất ức chế P2Y12 được đánh giả bởi xét nghiệm VerifyNow (Accumetrics, Inc., San Diego, California) (Đơn vị phản ứng tiểu cầu P2Y12 [PRU]), đo ngưng tập quang học(adenosine diphosphate 5 và 20 mmol/l và axit arachidonic) và xét nghiệm phosphoryl hoá của phosphoprotein do hoạt hoá dãn mạch (VASP). Xét nghiệm VerifyNow Aspirin và đo nồng độ B2 thromboxane huyết thanh đã được thực hiện.
KẾT QUẢ Nồng độ trung bình Ticagrelor huyết tương trước và sau liều thấp hơn 35% và 38% tương ứng với liều 60mg và 90mg. Cả hai liều đều đạt được mức độ ức chế tiểu cầu cao trước và sau liều, có sự biến đổi nhẹ về số lượng lớn hơn với liều 60mg,giá trị trung bình PRU trước liều 60 mg ticagrelor là 59 +/-63 trong khi giá trị trung bình PRU trước liều 90 mg là 47+/- 43 tương ứng (p = 0.34). Phản ứng tiểu cầu cao, được xác định bởi PRU > 208, rất hiếm với trước liều 60mg và không xảy ra sau liều. Phản ứng tiểu cầu trước và sau liều chỉ thấp hơn về trị số (không có ý nghĩa thống kê) ở liều 90mg so với liều 60mg khi được đo bằng ngưng tập quang học hoặc xét nghiệm phosphoryl hoá của phosphoprotein do hoạt hoá dãn mạch. Phản ứng Aspirin không bị ảnh hưởng bởi một trong hai liều.
KẾT LUẬN Liều Ticagrelor 60mg hai lần mỗi ngày đạt được mứcức chế tiểu cầu cao ở nồng độ đáy và đỉnh trong huyết thanhở tất cả các bệnh nhân tương đương với liều Ticagrelor 90 mg hai lần mỗi ngày, giúp cho việc lý giải tính hiệu quả của liều Ticagrelor thấp hơn trong thực nghiệm PEGASUS-TIMI 54
Ticagrelor là một chất đối kháng thụ thể P2Y12 mạnh, gắn kết có hồi phục, hoạt động trực tiếp mà không cần sự chuyển hoá, mặc dù chất chuyển hóa có hoạt tính của nó AR-C124910XX có hiệu lực tương tự tại P2Y12 (1). Do đó, mức độ ức chế thụ thể P2Y12 lại làm cong đường nồng độ huyết tương của ticagrelor và AR-C124910XX, vì ức chế tiểu cầu phục hồi như các mức giảm (2). Ticagrelor với liều duy trì 90 mg hai lần mỗi ngày cho thấy sự ức chế thụ thể P2Y12 tiểu cầu lớn hơn và ưu việt hơn so với clopidogrel trên bệnh nhân có bệnh mạch vành ổn định và hội chứng vành cấp. Nghiên cứu PLATO (Platelet Inhibition and Patient Outcomes) đã chứng minh tính hiệu quả vượt trội của ticagrelor so với clopidogrel, với liều duy trì 90 mg hai lần mỗi ngày lên đến 1 năm trên bệnh nhân mắc hội chứng vành cấp (5). Do đó, phác đồ điều trị Ticagrelor đã được khuyến cáo trong hướng dẫn quốc tế như một điều trị đầu tay lên đến 1 năm đối với bệnh nhân hội chứng vành cấp – không hoặc có ST chênh lên (6,7) – có can thiệp mạch vành (8,9).
Thử nghiệm PEGASUS-TIMI 54 (Phòng ngừa biến cố tim mạch bằng Ticagrelor so với giả dược trên bệnh nhân có tiền sử NMCT đang sử dụng Aspirin) đã xác định lợi ích của việc điều trị lâu dài với ticagrelor kết hợp Aspirin so với giả dược. Bệnh nhân nghiên cứu phải có tiền căn NMCT trong vòng 1-3 năm trước, được chọn ngẫu nhiên và phải có yếu tố nguy cơ cao về biến cố bệnh lý do xơ vữa (NCT01225562) (10,11). Ticagrelor được nghiên cứu ở hai liều: liều 90 mg hai lần mỗi ngày, như những nghiên cứu trước đó và đã được chấp thuận điều trị trên hội chứng vành cấp, hoặc liều 60 mg hai lần mỗi ngày, liều chưa được nghiên cứu trước đây. Trên cơ sở mô hình thực nghiệm, nó chỉ ra rằng sự ức chế tiểu cầu ở liều 60 mg hai lần mỗi ngày sẽ thấp hơn liều 90 mg hai lần mỗi ngày, tuy nhiên nó lại ức chế tốt hơn và với biến đổi ít hơn liều clopidogrel 75 mg mỗi ngày (10). Tuy nhiên, chúng ta không có dữ liệu thực về dược động học và dược lực học.
Trong nghiên cứu, cả hai liều Ticagrelor đều có tính hiệu quả và độ an toàn so với giả dược: tỉ số nguy cơ của tiêu chí nghiên cứu chính về tính hiệu quả (tổng hợp các ca tư vong tim mạch, NMCT và đột quỵ) là 0.85 (95% khoảng tin cậy[CI]: 0.75 to 0.96) và 0.84 (95% CI: 0.74 to 0.95) và tiêu chí nghiên cứu chính về độ an toàn (xuất huyết nặng/Tiêu sợi huyết trong NMCT) là 2.69 (95% CI: 1.96 to 3.70) và 2.32 (95% CI: 1.68 to 3.21) tương ứng liều 90 mg và 60 mg hai lần một ngày (11). Chúng tôi thực hiện nghiên cứu phụ ở các bệnh nhân đã tham gia PEGASUS-TIMI 54 để nghiên cứu so sánh về tác dụng PK và PD của Ticagrelor trong liều 60 mg hai lần một ngày với liều 90 mg hai lần một ngày.
PHƯƠNG PHÁP
THIẾT KẾ NGHIÊN CỨU Tổng cộng có 180 bệnh nhân đã tham gia PEGASUS-TIMI cung cấp sự đồng ý bổ sung để tham gia vào nghiên cứu phân nhóm này, được thực hiện tại 4 trung tâm: 3 tại Vương quốc Anh (Sheffield, Rotherham, và Nottingham) và 1 ở Hoa Kỳ (Jacksonville, Florida). Các nghiên cứu phân nhóm được tiến hành theo một giao thức đã được chấp thuận bởi của ủy ban đạo đức có liên quan và hội đồng xét duyệt. Bệnh nhân được phân nhóm ngẫu nhiên tỉ lệ 1: 1: 1 (nhóm giả dược, nhóm ticagrelor 60mg, và nhóm ticagrelor 90mg) sau khi họ dung thuóc nghiên cứu ít nhất trong 4 tuần. Bệnh nhân tham dự nghiên cứu vào buổi sáng sau khi đã dùng liều cuối thuốc nghiên cứu dự kiến cho buổi tối trước đó.
Mẫu máu tĩnh mạch được xét nghiệm vào buổi sáng sau đó bệnh nhân được uống thuốc nghiên cứu và thực hiện lại xét nghiệm máu sau 2h. Sự phân tích PK và PD được mô tả trong các phần sau.
NGHIÊN CỨU DƯỢC ĐỘNG HỌC (PK) mẫu máu tĩnh mạch được cho vào ống nghiệm có chứa heparin và được ngâm trong đá trước khi ly tâm ở 1500g trong vòng 30 phút. Huyết tương được chuyển vào ống nghiệm làm từ nhựa polypropylene và ngay lập tức làm đông lạnh ở 20 C trước khi được vận chuyển đến Trung tâm Covance (Indianapolis, Indiana) để phân tích nồng độ ticagrelor và nồng độ AR-C124910XX (12). Giới hạn dưới ngưỡng phát hiện của xét nghiệm là 1 ng / ml cho ticagrelor và 2,5 ng / ml cho AR-C124910XX.
XÉT NGHIỆM VERIFYNOW P2Y12 và ASPIRIN mẫu máu tĩnh mạch chứa trong ống citrate 2ml và phân tích bằng các xét nghiệm VerifyNow P2Y12, xét nghiệm Aspirin (Accumetrics, Inc., San Diego, California) theo hướng dẫn của nhà sản xuất (4). Đối với các xét nghiệm P2Y12, đơn vị phản ứng tiểu cầu P2Y12 (PRU) và tỷ lệ phần trăm ức chế (suy ra từmô phỏng của một phản ứngtối thiểugây ra bởi peptit có chức năng kích hoạt thụ thể thrombin) đã được ghi lại. Các xét nghiệm thuốc aspirin đã được thực hiện trong một phân nhóm các bệnh nhân và các đơn vị phản ứng thuốc aspirin đã được ghi lại.
ĐO NGƯNG TẬP QUANG HỌC (LTA) được thực hiện bằng máy đo ngưng tập Chrono-log (havertown, Pennsylvania) sử dụng adenosine diphosphate (ADP) (5 và 20 mmol/l) và acid arachidonic (1 mmol/l; thực hiện sau liều trong một phân nhóm bệnh nhân ) như là chất đồng vận (3). Tỷ lệ phần trăm tối đa phản ứng ngưng tập quang hoc đã được ghi lại.
XN PHOSPHORYL HOÁ CỦA PHOSPHOPROTEIN HOẠT HOÁ DÃN MẠCH (VASP) máu được phân thành những mẫu nhỏ và được xử lý bằng 1 kit xét nghiệm phosphoryl hoá của phosphoprotein do hoạt hoá dãn mạch, và chỉ số phản ứng tiểu cầu (PRI) đã được xác định theo hướng dẫn của nhà sản xuất. (BioCytex, Marseille, France)(4).
THROMBOXANE B2 HUYẾT THANH mẫumáu tĩnh mạch được thêm vào ống tách huyết thanh (Becton Dickinson, Oxford, Vương quốc Anh) và ủ ở 37 độ C trong 30 phút, tiếp theo ly tâm ở 1000 g trong 15 phút. Huyết thanh nổi sau đó đã được chuyển vào ống lưu mẫu và được bảo quản ở -80 độ C trước khi phân tích. Nồng độ B2 thromboxane được đo bởi một kit ELISA (Cayman Chemicals, Ann Arbor, Michigan).
CỠ MẪU VÀ PHÂN TÍCH THỐNG KÊ Dựa vào giá trị trung bình dự kiến của pre dose PRUtrong nhóm ticagrelor 90 mg là 79 PRU và độ lệch chuẩn là 78 PRU ( 4 ) , 57 bệnh nhân được yêu cầu trong mỗi nhóm ticagrelor để cung cấp 80 % khả năng phát hiện giá trị trung bình PRU trong nhóm Ticagrelor 60mg và cao hơn 50 PRU trong nhóm 90 mg với chỉ số alpha = 0.01 . Tổng cộng có 180 bệnh nhân được cho phép cho sự mất cân đối trong dự kiến số lượng cuối cùng trong mỗi 3 nhóm .
Dữ liệu được phân tích bằng phần mềm SAS phiên bản 9.3 ( SAS Institute, Cary , North Carolina ) và trình bày theo giá trị trung bình và độ lệch chuẩn hoặc trung vị và phương sai. Biến liên tục cho các nhóm giả dược và ticagrelor được so sánh bằng cách sử dụng phép kiểm Kruskal- Wallis. Các kiểu biến số được so sánh bằng phép kiểm Fisher. Có ý nghĩa thống kê khi giá trị p < 0.01 cho phép so sánh nhiều nhóm.
Tỷ lệ bệnh nhân trong mỗi nhóm điều trị (là những người có phản ứng lớn hơn các giá trị ngưỡng trước đây liên quan đến nguy cơ thiếu máu gia tăng cao (hoạt tính tiểu cầu cao)) được xác định như sau: kết quả xét nghiệm Verify- Now P2Y12 >208 PRU (14,15); giá trị cực đại của ngưng kết tiểu cầu quang hoc (LTA)so vớiADP 20 mmol/l >59% (16–18); giá trị cực đại của ngưng kết tiểu cầu quang hoc so vớiADP 5 mmol/l >46% (17,18); PRI >50% (18,19); các đơn vị phản ứng aspirin VerifyNow >550 (20,21); vàgiá trị cực đại của ngưng kết tiểu cầu quang hoc so vớiarachidonic acid >=20% (22,23).
KẾT QUẢ
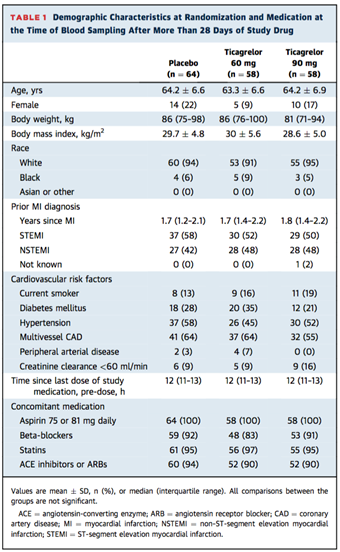
DÂN SỐ NGHIÊN CỨU Tổng cộng có 180 bệnh nhân được nghiên cứu sau ít nhất 4 tuần điều trị duy trì với giả dược (n = 64), ticagrelor 60 mg hai lần mỗi ngày (n = 58), hoặc ticagrelor 90 mg hai lần mỗi ngày (n = 58), đặc điểm nhân khẩu học và thuốc sử dụng kèm theo nhìn chung phù hợp trong 3 nhóm điều trị (Bảng 1). Tất cả các bệnh nhân được nhận liều thấp aspirin. Các đặc điểm cơ bản của bệnh nhân nghiên cứu phân nhóm so với toàn bộ nhóm thử nghiệm được thể hiện trong Bảng 1.
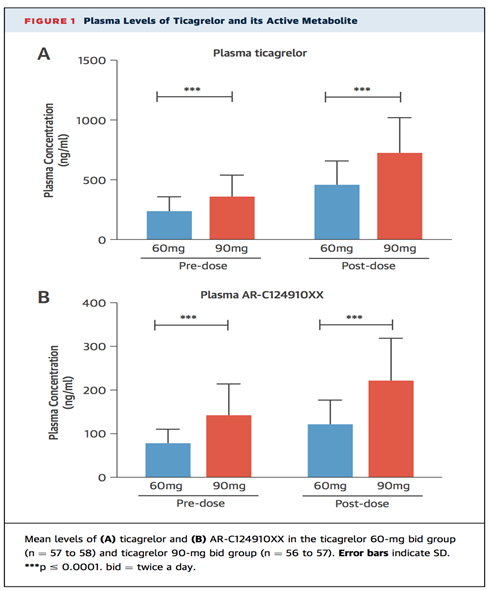
KẾT QUẢ DƯỢC ĐỘNG HỌC nồng độ trung bình ticagrelor trong huyết tương trước và sau sử dụng là 65% ở nhóm liều 60-mg và tương ứng là 62% ở nhóm liều 90-mg, và nồng độ trung bình AR-C124910XX huyết tương sau liều của nhóm liều 60mg đều bằng 54% của những BN nhóm liều 90mg
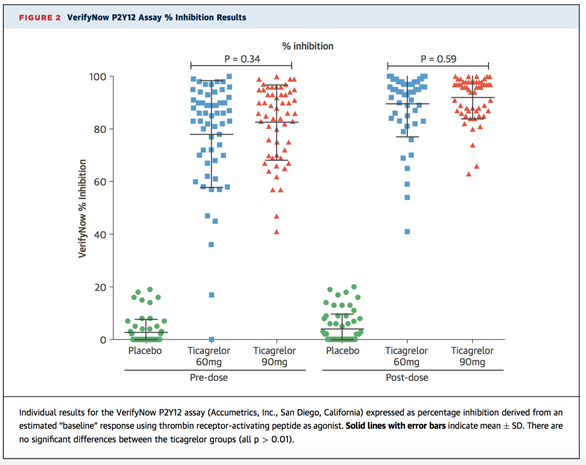
ĐO ĐỘ ỨC CHẾ THỤ THỂ P2Y12 TIỂU CẦU Tất cả các tính toán phản ứng tiểu cầu qua trung gian thụ thể P2Y12 được thể hiện bằng số (nhưng không có ý nghĩa thống kê) ức chế tiểu cầu lớn hơn ở liều ticagrelor 90 mg hai lần mỗi ngày khi so sánh với liều 60 mg hai lần mỗi ngày, kể cả trước và sau liều (Central Illustration, Figures 2 to 4, Online Table 2). Kết quả xét nghiệm VerifyNow P2Y12 mức độ ức chế tiểu cầu trung bình đạt mức cao ở cả hai nhóm liều ticagrelor, nhưng mức độ trung bình lớn hơn nhẹ ở phác đồ 60-mg (Central Illustration, Figure 2, Online Table 2): giá trị trung bình trước liều của PRU là 59 +/- 63 PRU (nhóm liều 60-mg) so với 47 +/- 43 PRU (nhóm liều 90-mg), và giá trị sau liều là 29 +/- 39 PRU so với 20 +/- 19 PRU, tương ứng ở hai nhóm liều.
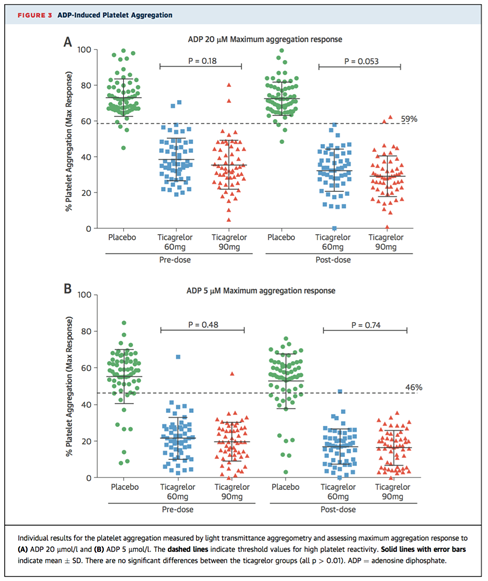
Tương tự, phản ứng LTA với ADP trung bình (Figure 3) và mức độ PRI trung bình (Figure 4) đều thấp ở cả hai liều ticagrelor khi so sánh với giả dược, trước và sau liều. Các đánh giá VerifyNow P2Y12 ước lượng tỉ lệ ức chế cho thấy sự khác biệt lớn về giá trị giữa nhóm giả dược và nhóm ticagrelor (Figure 2).
PHẢN ỨNG TIỂU CẦU CAO QUA TRUNG GIAN P2Y12 Nhìn chung, phản ứng tiểu cầu cao với các biện pháp ức chế P2Y12 là hiếm gặp (Central Illustration, Figures 3 and 4, Table 2). Với xét nghiệm VerifyNow P2Y12, chỉ hai bệnh nhân ở nhóm ticagrelor liều 60-mg có giá trị PRU >208 trước liều (3.5%), và không có trường hợp khác của phản ứng tiểu cầu cao (Central Illustration). Một trong số bệnh nhân này cũng có phản ứng tiểu cầu cao đối với ADP xác định bởi phương pháp LTA, và tất cả đều có phản ứng tiểu cầu cao được xác định bởi VSAP. Bệnh nhân – với giá trị PRU trước liều 369 (ức chế 0%) có mức độ dược động học (PK) ở cả ticagrelor và AR-C124910XX là dưới ngưỡng phát hiện, cho thấy sự kém tuân thủ điều trị, và giá trị PRU trước liều của các bệnh nhân này là 122 (ức chế 69%). Một bệnh nhân khác có giá trị PRU trước liều 211 (17% ức chế) cũng có nồng độ PK thấp đối với ticagrelor (40 ng/ml) và AR-C124910XX (18 ng/ml) và có giá trị PRU sau liều là 39 PRU (ức chế 86%).
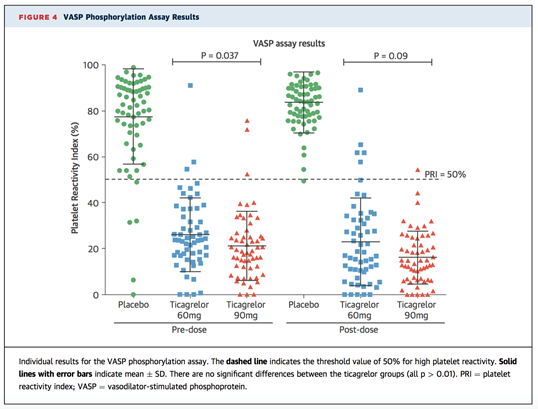
Vài trường hợp có phản ứng tiểu cầu cao trong cả hai nhóm ticagrelor theo một trong hai phản ứng LTA cho ADP hoặc mức độ PRI (Hình 3 và 4, Bảng 2).
ĐO PHẢN ỨNG ASPIRIN Xét nghiệm phản ứng Aspirin VerifyNow, LTA với arachidonic acid như một chất đồng vận, và nồng độ thromboxane B2 huyết thanh – tất cả cho thấy sự ức chế cyclooxygenase-1 ở mức độ cao bởi Aspirin ở hầu hết các bệnh nhân, với một vài bệnh nhân có phản ứng tiểu cầu cao với arachidonic acid trong mỗi nhóm điều trị trước và sau liều (Online Figure 1, Online Table 3). Giữa hai nhóm ticagrelor và giả dược không có sự khác biệt có ý nghĩa.
BÀN LUẬN
PEGASUS-TIMI 54 là nghiên cứu phân nhóm đầu tiên đánh về sự tác dụng của PK và PD trong phác đồ ticagrelor 60 mg. Như những nghiên cứu trước đây dựa vào cơ sở dữ liệu PK dự kiến, kết quả cho thấy nồng độ PK trong ticagrelor liều 60 mg xấp xỉ hai phần ba so với nồng độ PK trong ticagrelor liều 90 mg. Điều quan tâm nhất chính là sự ức chế trung bình thụ thể P2Y12 tiểu cầu đạt được gần như nhau trong hai liều ticagrelor 60-90 mg. Đây là điều bất ngờ, vì nó đã được dự đoán đạt nồng độ ức chế tiểu cầu thấp hơn với phác đồ 60 mg (10), nhưng theo quan sát sự ức chế tiểu cầu tương tự giữa 2 nhóm ticagrelor là hoàn toàn phù hợp với các kết quả trong thử nghiệm chính gần như giống hệt với tác dụng của phác đồ ticagrelor 60và 90 mg so với giả dược (11). Theo xét nghiệm VerifyNow P2Y12, chỉ có 2 bệnh nhân trong nhóm ticagrelor 60 mg có phản ứng tiểu cầu cao trước liều, và tất cả họ đều có được sự ức chế tiểu cầu mạnh mẽ sau liều. Hơn nữa, đã có bằng chứng cho thấy sự kém tuân thủ điều trị với thuốc nghiên cứu ở một trong số những bênh nhân trên. Khả năng dung nạp ở phác đồ 60 mg tương đối tốt hơn so với phác đồ 90 mg: tần suất tác dụng phụ khó thở liên quan đến ticagrelor ở mức độ vừa phải khi kết hợp với liều và nồng độ PK (24-27), tỷ lệ khó thở là một con số thấp hơn ở liều ticagrelor 60 mg so với liều ticagrelor 90 mg trong thực nghiệm PEGASUS-TIMI 54 (11). Thêm vào đó, tỷ lệ chảy máu, truyền máu, và bệnh gout ở liều ticagrelor 60-mg chiếm số lượng thấp hơn so với liều ticagrelor 90 mg. Do đó, kết quả của chúng tôi bảo vệ việc ưu tiên sử dụng liều ticagrelor 60 mg thay vì liều 90 mg ở những bệnh nhân – tiền sử NMCT hơn 1 năm – có tuân thủ tốt với điều trị.Cách tiếp cận này đã được xác nhận bởi Cục Quản lý dược và thực phẩm Hoa Kì gần đây phê duyệt việc sử dụng lâu dài ticagrelor 60 mg liều hai lần mỗi ngày cho bệnh nhân sau NMCT (28). Hơn nữa, một điều trị thử nghiệm liều 60 mg- ticagrelor được xem xét trên bệnh nhân sau NMCT, những người không thể dung nạp được liều 90 mg do khó thở hay chảy máu nhẹ.
Chúng tôi quan sát thấy không có ảnh hưởng của ticagrelor trên các phép đo của phản ứng aspirin, cụ thể ít nhất trong những bệnh nhân được điều trị bằng aspirin, ức chế thụ thể P2Y12 không làm ảnh hưởng đáng kể việc phóng thích chất đồng vận tiểu cầu của tiểu cầu thromboxane A2 (vì các biện pháp PD phản ứng thuốc aspirin phản ánh chuyển arachidonic axit thành thromboxane A2). Điều này đặt ra một lưu ý thận trọng về việc bỏ thuốc aspirin khi điều trị và chỉ dùng ticagrelor nếu có nguy cơ huyết khối cao và nhấn mạnh tầm quan trọng của việc chờ đợi kết quả đủ mạnh về nghiên cứu hiệu quả lâm sàng của ticagrelor đơn trị so với kháng kết tập tiểu cầu kép.
GIỚI HAN NGHIÊN CỨU Nghiên cứu phân nhóm PK / PD không đủ lớn để cho phép đánh giá các mối quan hệ giữa kết quả chức năng tiểu cầu và kết quả lâm sàng. Chúng tôi không đánh giá hiệu quả của 2 phác đồ ticagrelor về sự tái hấp thu adenosine, và không thể loại trừ một sự khác biệt có ý nghĩa giữa 2 phác đồ ticagrelor trên nồng độ adenosine huyết tương, việc này cũng có thể đóng góp vào sự ức chế tiểu cầu trong cơ thể (29,30); điều này đang được đánh giá trong một nghiên cứu trên các bệnh nhân không bắt buộc trải qua can thiệp mạch vành qua da (NCT02327624). Chúng tôi cũng không đánh giá phản ứng tiểu cầu trước khi khởi đầu thuốc nghiên cứu; chúng tôi dựa trên xét nghiệm VerifyNow ước tính sự ức chế, sử dụng thụ thể thrombin kích hoạt gây ra phản ứng peptide để cung cấp phản ứng dự đoán ban đầu, hơn là việc bắt nguồn dữ liệu ức chế từ phản ứng tiểu cầu trước khi điều trị. Nghiên cứu phân nhóm này không bao gồm các bệnh nhân châu Á và đa số bệnh nhân có trọng lượng cơ thể thấp giới hạn (<60 kg), các nghiên cứu PK / PD nên tiếp tục được yêu cầu đánh giá ở các nhóm này.
KẾT LUẬN
Chúng tôi đã chỉ ra rằng liều ticagrelor 60 mg hai lần mỗi ngày đạt được nồng độ đỉnh và đáy cao của sự ức chế tiểu cầu với bệnh nhân có tiền sử NMCT, tương tự với sự ức chế tiểu cầu ở liều 90 mg hai lần mỗi ngày. Những kết quả này giúp giải thích cho sự so sánh tính hiệu quả của liều ticagrelor thấp hơn trong nghiên cứu.
ĐỀ XUẤT
KHẢ NĂNG ĐIỀU TRỊ BỆNH NHÂN những bệnh nhân tiền sử NMCT đang điều trị kháng kết tập tiểu càu kép, liều Ticagrelor 60 mg hai lần mỗi ngày mang đến một mức độ ức chế tiểu cầu tương đương với liều 90 mg đạt được. Điều này lý giải tính hiệu quả gần như tương đương ở các liều trong việc phòng ngừa sự tái phát những biến cố thiếu máu cục bộ.
THÔNG ĐIỆP Những quan sát này kêu gọi nghiên cứu thêm về tính hiệu quả và độ an toàn của liều ticagrelor 60 mg hai lần mỗi ngày tại các cơ sở y tế liên quan đến bệnh lý mạch máu do xơ vữa.
TÀI LIỆU THAM KHẢO
1. F. Franchi, D.J. Angiolillo. Novel antiplatelet agents in acute coronary syndrome. Nat Rev ardiol, (2015), pp. 30–47
2. P.A. Gurbel, K.P. Bliden, K. Butler,et al. Randomized double-blind assessment of the ONSET and OFFSet of the antiplatelet effects of ticagrelor versus clopidogrel in patients with stable oronary artery disease: the ONSET/OFFSET study. Circulation, 120 (2009), pp. 2577–2585
3. R.F. Storey, S. Husted, R.A. Harrington,et al. Inhibition of platelet aggregation by AZD6140, a reversible oral P2Y12 receptor antagonist, compared with clopidogrel in patients with acute coronary syndromes. JAm Coll Cardiol, 50 (2007), pp. 1852–1856
4. R.F. Storey, D. Angiolillo, S. Patil,et al. Inhibitory effects of ticagrelor compared to clopidogrel on platelet function in patients with acute coronary syndromes: the PLATO (PLATelet Inhibition and patient Outcomes) PLATELET Substudy. JAm Coll Cardiol, 56 (2010), pp. 1456–1462
5. L. Wallentin, R.C. Becker, A. Budaj, for the PLATO Investigators,et al. Ticagrelor versus clopidogrel in patients with acute coronary syndromes. NEngl J Med, 361 (2009), pp. 1045–1057
6. E.A. Amsterdam, N.K. Wenger, R.G. Brindis,et al. 2014 AHA/ACC guideline for the management of patients with non–ST-elevation acute coronary syndromes: a report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines. JAm Coll Cardiol, 64 (2014), pp. e139–e228
7. M. Roffi, C. Patrono, J.-P. Collet,et al. 2015 ESC guidelines for the management of acute coronary syndromes in patients presenting without persistent ST-segment elevation. Eur Heart J, 37 (2016), pp. 267–315
8. P.T. O’Gara, F.G. Kushner, D.D. Ascheim,et al. 2013ACCF/AHA guideline for the management of ST-elevation myocardial infarction: a report of theAmerican College of Cardiology Foundation/American Heart Association Task Force on Practice Guidelines. JAm Coll Cardiol, 61 (2013), pp. e78–e140
9. P.G. Steg, S.K. James, D. Atar,et al. ESC guidelinesfor the management of acute myocardial infarction in patients presenting with ST-segment elevation. Eur Heart J, 33 (2012), pp. 2569–2619
10. M.P. Bonaca, D.L. Bhatt, E. Braunwald,et al. Design and rationale for the Prevention of Cardiovascular Events in Patients With Prior Heart Attack Using Ticagrelor Compared to Placebo on a Background of Aspirin–Thrombolysis In Myocardial Infarction 54 (PEGASUS-TIMI 54) trial. Am Heart J, 167 (2014), pp. 437–444.e5
11. M.P. Bonaca, D.L. Bhatt, M. Cohen, for thePEGASUS-TIMI 54 Steering Committee and Investigators,et al. Long-term use of ticagrelor in patients with prior myocardial infarction. NEngl J Med, 372 (2015), pp. 1791–1800
12. F. Franchi, F. Rollini, J.R. Cho,et al. Impact of escalating loading dose regimens of ticagrelor in patients with ST-segment elevation myocardial infarction undergoing primary percutaneous coronary intervention: results of a prospective randomized pharmacokinetic and pharmacodynamic investigation. JAm Coll Cardiol Intv, 8 (2015), pp. 1457–1469
13. U.S. Tantry, L. Bonello, D. Aradi, for theWorking Group on On-Treatment Platelet Reactivity,et al. Consensus and update on the definition of on-treatment platelet reactivity to adenosine diphosphate associated with ischemia and bleeding. JAm Coll Cardiol, 62 (2013), pp. 2261–2273
14. M.J. Price, S. Endemann, R.R. Gollapudi,et al. Prognostic significance of post-clopidogrel platelet reactivity assessed by a point-of-care assay on thrombotic events after drug-eluting stent implantation. Eur Heart J, 29 (2008), pp. 992–1000
15. G.W. Stone, B. Witzenbichler, G. Weisz, forthe ADAPT-DES Investigators,et al. Platelet reactivity and clinical outcomes after coronary artery implantation of drug-eluting stents (ADAPT-DES): a prospective multicentre registry study. Lancet, 382 (2013), pp. 614–623
16. D.J. Angiolillo, S.B. Shoemaker, B. Desai,et al. Randomized comparison of a high clopidogrel maintenance dose in patients with diabetes mellitus and coronary artery disease. Results of the Optimizing Antiplatelet Therapy in Diabetes Mellitus (OPTIMUS) Study. Circulation, 115 (2007), pp. 708–716
17. P.A. Gurbel, M.J. Antonino, K.P. Bliden,et al. Platelet reactivity to adenosine diphosphate and long-term ischemic event occurrence following percutaneous coronary intervention: a potential antiplatelet therapeutic target. Platelets, 19 (2008), pp. 595–604
18. L. Bonello, U.S. Tantry, R. Marcucci, for the Working Group on High On-Treatment Platelet Reactivity,et al. Consensus and future directions on the definition of high on-treatment platelet reactivity to adenosine diphosphate. JAm Coll Cardiol, 56 (2010), pp. 919–933
19. L. Bonello, F. Paganelli, M. Arpin-Bornet,et al. Vasodilator-stimulated phosphoprotein phosphorylation analysis prior to percutaneous coronary intervention for exclusion of postprocedural major adverse cardiovascular events. JThromb Haemost, 5 (2007), pp. 1630–1636
20. H.L. Nielsen, S.D. Kristensen, S.S. Thygesen,et al. Aspirin response evaluated by the VerifyNow Aspirin System and light transmission aggregometry. Thromb Res, 123 (2008), pp. 267–273
21. N. Blais, C. Pharand, M. Lordkipanidzé,et al. Response to aspirin in healthy individuals—cross-comparison of light transmission aggregometry, VerifyNow system, platelet count drop, thromboelastography (TEG) and urinary 11-dehydrothromboxane B2. Thromb Haemost, 102 (2009), pp. 404–411
22. P.A. Gum, K. Kottke-Marchant, P.A. Welsh,et al. Aprospective, blinded determination of the natural history of aspirin resistance among stable patients with cardiovascular disease. JAm Coll Cardiol, 41 (2003), pp. 961–965
23. J. DiChiara, K.P. Bliden, U.S. Tantry,et al. The effect of aspirin dosing on platelet function in diabetic and nondiabetic patients: an analysis from the Aspirin-Induced Platelet Effect (ASPECT) Study. Diabetes, 56 (2007), pp. 3014–3019
24. S. Husted, H. Emanuelsson, S. Heptinstall,et al. Pharmacodynamics, pharmacokinetics, and safety of the oral reversible P2Y12 antagonist AZD6140 with aspirin in patients with atherosclerosis: adouble-blind comparison to clopidogrel with aspirin. Eur Heart J, 27 (2006), pp. 1038–1047
25. C.P. Cannon, S. Husted, R.A. Harrington, for the DISPERSE-2 Investigators,et al. Safety, tolerability, and initial efficacy of AZD6140, the first reversible oral adenosine diphosphate receptor antagonist, compared with clopidogrel, in patients with non-ST-segment elevation acute coronary syndrome: primary results of the DISPERSE-2 trial. JAm Coll Cardiol, 50 (2007), pp. 1844–1851
26. R.F. Storey, K. Bliden, S.B. Patil, for the ONSET/OFFSET Investigators,et al. Incidence of dyspnea and assessment of cardiac and pulmonary function in patients with stable coronary artery disease receiving ticagrelor, clopidogrel or placebo in the ONSET/OFFSET Study. JAm Coll Cardiol, 56 (2010), pp. 185–193
27. R.F. Storey, R.C. Becker, R.A. Harrington,et al. Characterization of dyspnoea in PLATO study patients treated with ticagrelor or clopidogrel and its association with clinical outcomes. Eur Heart J, 32 (2011), pp. 2945–2953
28. American College of Cardiology. FDA Expands Approval for Heart Attack Drug. 2015. Available at:http://www.acc.org/latest-in-cardiology/articles/2015/09/04/11/55/fda-expands-approval-for-heart-attack-drug?w_nav=LC. Accessed January 4,2016.
29. S. Nylander, E.A. Femia, M. Scavone,et al. Ticagrelor inhibits human platelet aggregation via adenosine in addition to P2Y12 antagonism. JThromb Haemost, 11 (2013), pp. 1867–1876
30. L. Bonello, M. Laine, N. Kipson,et al. Ticagrelor increases adenosine plasma concentration in patients with an acute coronary syndrome. JAm Coll Cardiol, 63 (2014), pp. 872–877







