 Vai trò của tần số (Ts) tim đã được xác định trong quá trình tiến triển của thiếu máu cục bộ (TMCB) cơ tim. Ở bệnh nhân (BN) có bệnh mạch vành (BMV), hầu hết các đợt TMCB là do tăng Ts tim (do gắng sức, xúc cảm…)
Vai trò của tần số (Ts) tim đã được xác định trong quá trình tiến triển của thiếu máu cục bộ (TMCB) cơ tim. Ở bệnh nhân (BN) có bệnh mạch vành (BMV), hầu hết các đợt TMCB là do tăng Ts tim (do gắng sức, xúc cảm…)
Bệnh viện Nhân dân 115
Mở đầu:
Vai trò của tần số (Ts) tim đã được xác định trong quá trình tiến triển của thiếu máu cục bộ (TMCB) cơ tim. Ở bệnh nhân (BN) có bệnh mạch vành (BMV), hầu hết các đợt TMCB là do tăng Ts tim (do gắng sức, xúc cảm…) dẫn tới mất cân bằng cung cầu O2. Vì thế giảm Ts tim là một nguyên tắc điều trị quan trọng để ngăn chặn TMCB cơ tim do làm giảm nhu cầu O2 và kéo dài thời gian tâm trương. Cho đến nay, chẹn β vẫn là thuốc hàng đầu trong điều trị BMV mạn ổn định cùng với các thuốc Nitrate & chẹn kênh Calcium. Tuy nhiên cả ba thuốc này đều có ảnh hưởng trên huyết động nên dùng đơn liệu hay phối hợp trong điều trị thực sự có khó khăn (do tác dụng phụ , chống chỉ định, không dung nạp…). Ngoài ra việc phối hợp cả ba thuốc chưa chắc đã đem lại hiệu quả tốt hơn so với đơn trị liệu hay phối hợp 2 thuốc (1,2,3,4).
Ivabradine, thuốc ức chế kênh If là thuốc có tác dụng giảm TMCB đơn thuần chỉ dựa trên làm giảm tần số tim, không ảnh hưởng lên huyết động và có thể dùng được cho cả bệnh nhân bị tình trạng co thắt phế quản (hen phế quản, COPD nặng), vốn là một tình trạng mà có thể gặp tới 16% ở BN BMV, và khoảng 30% bệnh nhân tim mạch (5,6). Ivabradine hiện đã và đang được sử dụng rộng rãi ở Châu Âu & bắt đầu sử dụng ở Việt Nam hơn 2 năm qua. Vai trò của thuốc Ivabradine trong kiểm soát nguy cơ tim mạch cũng như chỉ định và chiến lược dùng thuốc hiện nay sẽ được đề cập trong bài viết này.
I. Vai trò của nhịp tim trong bệnh tim mạch
1. Nhịp tim: yếu tố nguy cơ (YTNC) độc lập trong bệnh tim mạch
1.1. Ở người bình thường và người tăng huyết áp (THA)
Số liệu dịch tễ khi theo dõi lâu dài trên những người khỏe mạnh cho thấy có sự kết hợp độc lập giữa tăng Ts tim với tỉ lệ tử vong và thương tật do bệnh tim mạch. Nghiên cứu trên 180.000 người khỏe & THA cho thấy tỉ lệ tử vong tim mạch tăng có ý nghĩa khi Ts tim tăng. Trong nghiên cứu Framingham với 30 năm theo dõi ở nam và nữ khỏe mạnh, kết hợp tăng Ts tim với tử vong (TV) gặp cả ở nam và nữ, cũng như ở người trẻ và người lớn tuổi (Bảng 1) (4)
|
Bảng 1 : Liên quan TV với tần số tim ở nam và nữ trong nghiên cứu Framingham |
||||
|
Tần số tim khi nghỉ |
Tỷ lệ hằng năm điều chỉnh theo tuổi |
|||
|
Nam |
Nữ |
|||
|
36 – 64 |
65 – 94 |
36 – 64 |
65 – 94 |
|
|
30 – 67 |
6 |
35 |
3 |
22 |
|
68 – 75 |
8 |
43 |
4 |
28 |
|
76 – 83 |
11 |
46 |
6 |
25 |
|
84 – 91 |
13 |
61 |
8 |
30 |
|
92 – 220 |
14 |
64 |
9 |
35 |
1.2. Bệnh mạch vành:
Ở bệnh nhân BMV, cả cấp và mạn, tăng Ts tim là YTNC độc lập cho các biến cố mạch vành (MV) chính, tử vong tim mạch & đột tử theo cơ chế giống như ở người khỏe & THA (h1 &
; h2) (7,8).
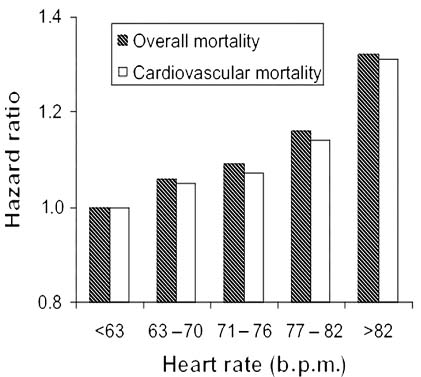
Hình1: Liên quan TV TM với Ts tim trong nghiên cứu CASS ( Coronary Artery Surgery Study ) trên 24.913 bệnh nhân theo dõi 14,7 năm (7).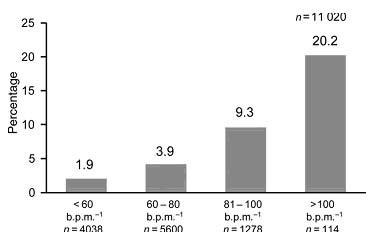
Hình 2: Liên quan tần số tim với TV trong 6 tháng trong nghiên cứu GISSI- 3 trên 11.020 bệnh nhân NMCT cấp (8).
Cơ chế là do tăng Ts tim làm tăng nhu cầu O2 cơ tim. Trong điều kiện tuần hoàn vành nguyên vẹn, dãn mạch do chuyển hóa (metabolic vasodilation) giúp tăng lưu lượng máu vành để đáp ứng với tăng nhu cầu O2 đủ để bù lại lưu lượng vành hạn chế do giảm thời gian tâm trương. Tuy nhiên, trong trường hợp hẹp mạch vành nặng, khi khả năng điều hòa của tuần hoàn vành đã quá mức để duy trì lưu lượng vành bình thường lúc nghỉ, việc tăng thêm tần số tim (làm giảm thêm thời gian tâm trương) sẽ làm giảm lưu lượng vành (hình 3) (9).
1.3 Bệnh nhân suy tim :
Các thử nghiệm trên bệnh nhân suy tim sung huyết cũng chứng minh rằng tần số tim ban đầu là yếu tố (YT) tiên đoán độc lập của TV mọi nguyên nhân, TV tim mạch & nhập viện vì suy tim (hình 4). Những bệnh nhân suy tim với nhịp nhanh thường có nhiều YTNC hơn, độ NYHA nặng hơn. Nếu điều trị làm giảm nhịp tim, sẽ cải thiện được tiên lượng tử vong cho bệnh nhân(4,10).
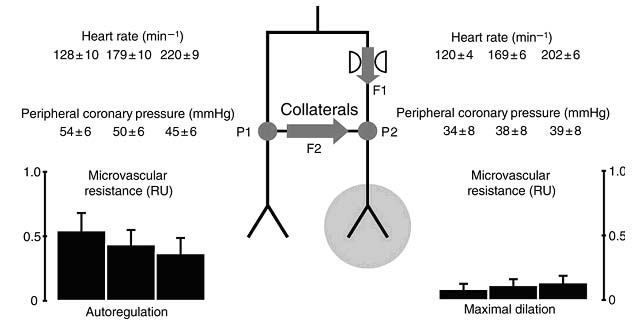
Hình 3. Hiện tượng cướp máu tuần hoàn bàng hệ & xuyên thành. P1 là áp lực ở vùng tuần hoàn bàng hệ. P2 là áp lực ở vùng tuần hoàn bàng hệ đổ vào gường mạch máu tận cùng bị TMCB (sau chỗ hẹp), F1 là lưu lượng qua chỗ hẹp, F2 là lưu lượng tuần hoàn bàng hệ. Giãn giường mao mạch tận cùng ở vùng không TMCB sẽ làm giảm P1, do đó làm giảm P2 & F2. Tăng tần số tim làm giảm kháng lực vi tuần hoàn & áp lực ở vùng không TMCB (trái), nhưng làm tăng kháng lực vi tuần hoàn và áp lực ở vùng sau chỗ hẹp (phải), hậu quả là lưu lượng tuần hoàn bàng hệ F2 (P1 – P2) giảm khoảng 2/3 (9).
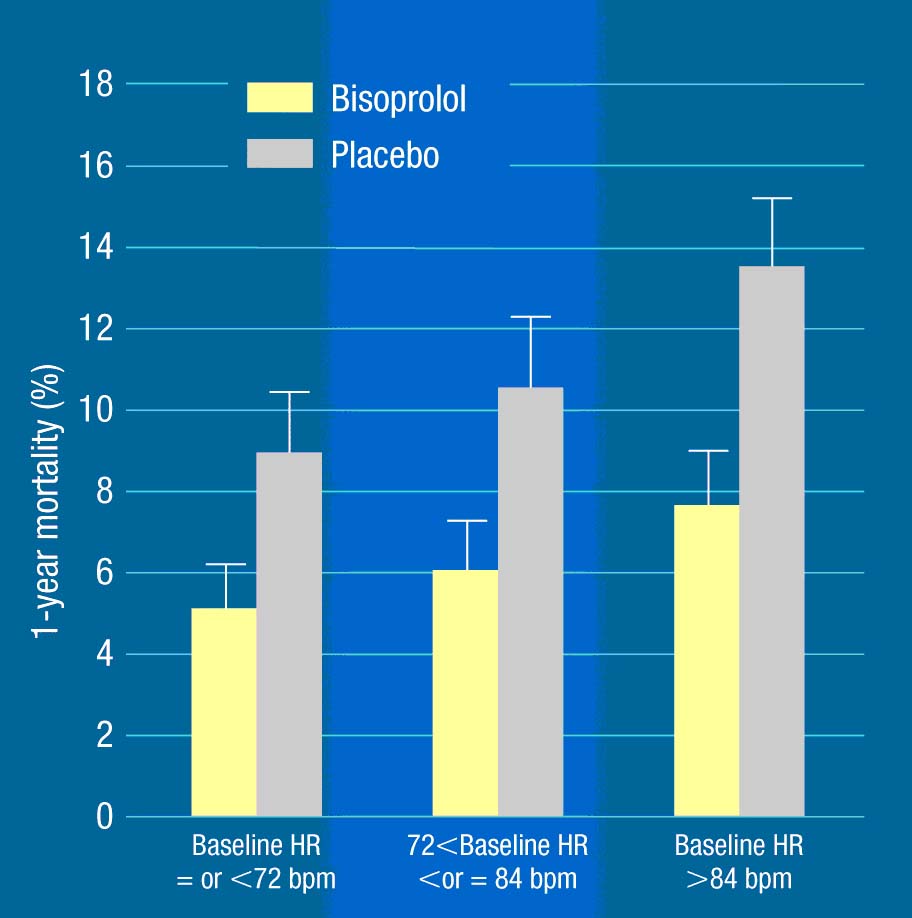
Hình 4: liên quan giữa Ts tim và TV ở BN suy tim trong nghiên cứu CIBIS – 2 (10).
2. Lợi ích của giảm nhịp tim:
Năm 1981, 3 thử nghiệm lâm sàng lớn trên bệnh nhân NMCT cấp đã chứng minh rằng chẹn β như Timolol, Metoprolol và Propranalol làm giảm TV do mọi nguyên nhân, TV tim mạch & đột tử. Trong các nghiên cứu này, điều đáng ghi nhận là những bệnh nhân với tần số tim ban đầu cao có tỷ lệ tử vong cao hơn trong thời gian theo dõi và hiệu quả của chẹn là rõ nhất ở những bệnh nhân có tần số tim cao nhất lúc ban đầu. Trong thử nghiệm Goteborg Metoprolol, người ta nhận thấy rằng Metoprolol có hiệu quả tốt nhất ở bệnh nhân tần số tim lúc đầu nhanh (>70 l/phút). Hiệu quả này bao gồm tỉ lệ TV do mọi nguyên nhân, đột tử, rung thất, NMCT sau 3-24 tháng (hình 5). Khi phân tích tất cả các thử nghiệm ở bệnh nhân NMCT có dùng chẹn b so với chứng Kjekshus và Gullestad cũng nhận thấy mối liên quan có ý nghĩa giữa giảm Ts tim khi nghỉ & giảm TV do mọi nguyên nhân. Phân tích gộp gần đây từ các thử nghiệm ngẫu nhiên điều trị β dài hạn có đối chứng ở bệnh nhân sau NMCT cấp cho thấy giảm có ý nghĩa tỉ lệ TV tim mạnh (P = 0,02), đột tử (P<0,01), và tái NMCT (P < 0,01) (4).
Kjekshus và Gullestad cũng nhận thấy mối liên quan có ý nghĩa giữa giảm Ts tim khi nghỉ & giảm TV do mọi nguyên nhân. Phân tích gộp gần đây từ các thử nghiệm ngẫu nhiên điều trị chẹn β dài hạn có đối chứng ở bệnh nhân sau NMCT cấp cho thấy giảm có ý nghĩa tỉ lệ TV tim mạnh (P = 0,02), đột tử (P<0,01), và tái NMCT (P < 0,01) (4).
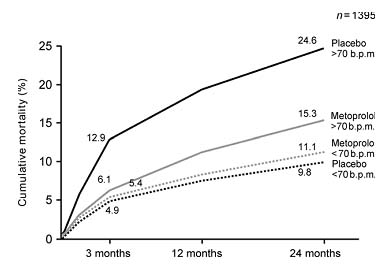
Hình 5. Liên quan TV và Ts tim lúc ban đầu ( trên và dưới 70) ở BN nghi ngờ NMCT cấp lúc nhập phòng cấp cứu trong nghiên cứu Goteborg Metoprolol (4).
Ở bệnh nhân suy tim, cũng có mối liên quan tương tự giữa thay đổi Ts tim & tỉ lệ TV mọi nguyên nhân, không chỉ khi sử dụng chẹn β, mà cả khi dùng ức chế men chuyển. Trong 2 thử nghiệm lớn ở bệnh nhân suy tim mạn CIBIS – II và MERIT-HF, bệnh nhân với Ts tim nhanh hơn ban đầu có tỉ lệ TV cao nhất và trong số những bệnh nhân này, hiệu quả của thuốc chẹn β là nhiều nhất (4,10).
Thuốc làm giảm Ts tim cũng làm giảm đau ngực ở bệnh nhân BMV mạn. Trong nghiên cứu mù đôi so sánh hiệu quả liều thấp & cao của 3 loại chẹn kênh Calcium khác nhau ở 335 bệnh nhân ĐTNOĐ, cải thiện thời gian tới lúc TMCB trong Test GS xe đạp liên quan trực tiếp tới giảm TS tim. Phân tích hồi quy cho thấy hiệu quả chống TMCB của thuốc phụ thuộc nhiều vào giảm tần số tim ( hình 6) (11,12).
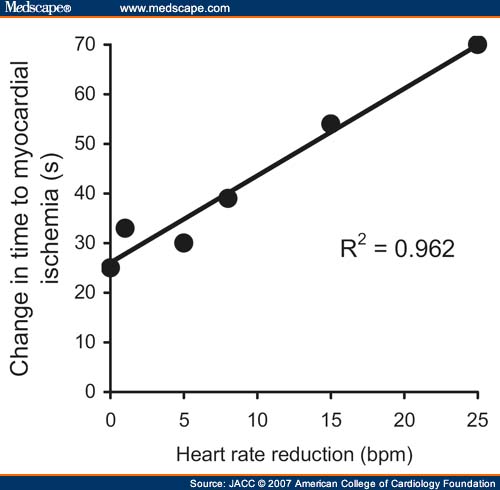
Hình 6. Giảm Ts tim và TMCB cơ tim. Liên quan giữa giảm Ts tim và cải thiện thời gian tới TMCB trên GS bằng xe đạp ở BN ĐTN ổn định sử dụng 2 liều trong 3 loại ức chế kênh calcium khác nhau (amlodipine, diltiazem, và mibefradil ) (12).
II. Thuốc ức chế kênh If:
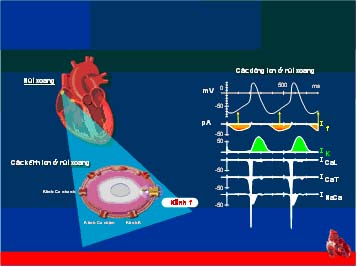
Nút xoang là chủ nhịp của tim. Tại nút xoang có nhiều kênh ion khác nhau như kênh Ca, kênh K & kênh f (hình 7) (13).

Hình 7. Các kênh ion của nút xoang, mỗi kênh cho 1 dòng ion đi qua và ảnh hưởng đến hình dạng điện thế hoạt động tại những giai đoạn khác nhau (13).
Kênh f có nguồn gốc từ chữ “funny”, có n
ghĩa là “lạ lùng” & chỉ mới được phát hiện vào năm 1979 bởi Brown và cộng sự. Kênh này phân bố chủ yếu ở nút xoang & ít hơn ở nút nhĩ thất. Trong điều kiện nút xoang hoạt động bình thường, kênh f ở nút nhĩ thất ở trạng thái ngủ yên, không hoạt động. Kênh này được mở ra khi có tăng phân cực của điện thế màng hoặc khi gắn trực tiếp vào AMP vòng. Nhìn vào hình 7 ta thấy, mỗi kênh cho một dòng ion đi qua và ảnh hưởng đến hình dạng điện thế hoạt động ở những giai đoạn khác nhau. Trong thời kỳ tâm trương, chỉ có kênh f hoạt động cho phép dòng Ion đi qua & tạo ra độ dốc khử cực thì tâm trương của điện thế hoạt động. Vì thế, kênh f ở nút xoang chính là yếu tố quyết định nhịp tim (13). Trong thời kỳ tâm thu điện thế màng tăng cao (hình 8) kênh f đóng. Ngược lại, trong thời kỳ tâm trương, điện thế màng trở về mức ngày càng âm, nghĩa là có sự tăng phân cực & đây chính là điều kiện kích hoạt kênh f mở ra cho phép dòng Na đi vào nội bào và một ít K đi ra ngoại bào, tạo ra độ dốc khử cực thì tâm trương (hình 8) (14,15).
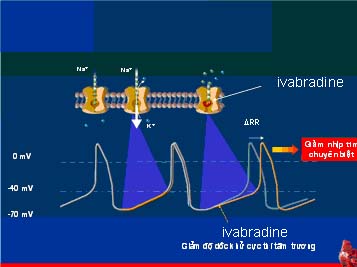
Hình 8. Cơ chế hoạt động kênh f và thuốc Ivabradine (14)
Ivabradine đi vào tế bào khi kênh f mở ra, sau đó gắn chuyên biệt vào kênh f và ức chế dòng ion đi vào nội bào. Sự ức chế chọn lọc dòng ion qua kênh f làm giảm độ dốc khử cực tâm trương và dẫn tới kéo dài thời gian cần để tạo ra một điện thế hoạt động mới, từ đó làm giảm nhịp tim một cách chuyên biệt (hình 8) (14,15).
Gọi là tác động chuyên biệt vì Ivabradine chỉ ức chế dòng ion qua kênh f, kênh ion chịu trách nhiệm chính cho tính tự động của nút xoang và không gây bất kỳ một ảnh hưởng nào đến các kênh ion khác có ở nút xoang. Thuốc cũng duy trì đặc tính dãn mạch vành khi GS, điều này đặc biệt có lợi cho bệnh nhân ĐTNÔĐ khi TMCB cơ tim thường xảy ra sau GS. Bên cạnh đó thuốc cũng không có tác động ức chế co bóp cơ tim. Đó là lý do vì sao với cùng một mức giảm nhịp tim, nhưng chỉ có Ivabradine cải thiện được cung lượng tim một cách có ý nghĩa khi so với chẹn β. Như vậy giữa Ivabradine & chẹn β có nhiều sự khác biệt (bảng 2) (16,17,18).
Bảng 2: Sự khác biệt giữa chẹn β và Ivabradine
|
Hiệu quả TM |
Chẹn |
Ivabradine |
|
Tính dẫn truyền |
Ưc chế |
Ưc chế |
|
Sức co bóp |
Ưc chế |
Không |
|
Tính thư giãn |
Ưc chế |
Không |
|
Dẫn truyền trong tim |
Ưc chế |
Không |
|
Kích thích cơ tim |
Ưc chế |
Không |
III. Các nghiên cứu chứng minh hiệu quả lâm sàng của Ivabradine:
1. Nghiên cứu so sánh Ivabradine với chẹn β và ức chế kênh Calcium
Lợi ích của Ivabradine trong CĐTNÔĐ đã được so sánh với Atenolol và Amlodipine. Thử nghiệm INITIATIVE (IN ternatIonal TrIAl on Treatment of angina with IVabradinE versus atenolol) đánh giá hiệu quả của Ivabradine so với Atenolol. Kết quả cho thấy, sau 4 tháng điều trị, hiệu quả của Ivabradine tương đương với Atenolol trên các thông số tổng thời gian GS, thời gian tới lúc ĐTN trên TNGS giới hạn triệu chứng và thời gian xuất hiện ST chênh xuống 1mm. Khi phân tích ở nhóm bệnh nhân trên 65 tuổi, hiệu quả này càng rõ rệt hơn. Điều này chứng tỏ thuốc có hiệu quả trên cả người lớn tuổi và rất có ý nghĩa lâm sàng vì hơn ¾ BN ĐTN ÔĐ > 65 tuổi (19).
Hiệu quả lâm sàng của Ivabradine so với Amlodipine cũng được đánh giá trong một thử nghiệm ngẫu nhiên mù đôi, đa trung tâm. Kết quả cho thấy thuốc có hiệu quả tương đương Amlodipine trong dự phòng ĐTN (20).
2. Trên bệnh nhân BMV ổn định và rối loạn chức năng thất trái – Nghiên cứu BEAUTIFUL morBidity-mortality EvAlUaTion of the If inhibitor ivabradine in patients with coronary artery disease and left ventricULar dysfuncsion):
Là nghiên cứu ngẫu nhiên mù đôi nhằm đánh giá Ivabradine so với chứng khi bổ xung vào điều trị chuẩn ở bệnh nhân BMVÔĐ, nhịp xoang, có rối loạn chức năng thất trái (RLCNTT) trên tiêu chí gộp bao gồm TV TM, NMCT cấp, suy tim mới khởi phát hay xấu đi phải nhập viện. Nghiên cứu gồm khoảng 11.000 bệnh nhân co bằng chứng bệnh MV mạn, nhịp xoang ≥ 60 l/phút và EF ≤ 39%.
BN được dùng 5mg Ivabradine 2 lần/ngày, tăng dần 7,5mg 2 lần/ngày sau 2 tuần, hoặc dùng Placebo để đạt mục tiêu nhịp tim < 60 l/phút.
Kết quả chung cho thấy Ivabradine khi bổ sung vào điều trị chuẩn ở bệnh nhân BMVÔĐ và RLCNTT không làm giảm các tiêu chí tiên phát. Tuy nhiên, khi phân tích ở phân nhóm bệnh nhân có nhịp tim lúc đầu ≥ 70 l/phút thì lợi ích thể hiện rất rõ. Thêm Ivabradine giúp làm giảm 30% các trường hợp cần phải tái thông mạch, 30% NMCT TV và không TV ở nhóm có nhịp tim > 70 lần/phút (hình 9,10). T
ương tự, ở phân nhóm bệnh nhân có ĐTNOĐ, thêm Ivabradine giúp làm giảm 24% TV do tim mạch, nhập viện vì suy tim và NMCT (hình 11). Kết quả này chứng tỏ Ivabradine có lợi để làm giảm biến cố tim mạch chính ở bệnh nhân BMV ổn định và RLCNTT có nhịp tim ≥ 70 l/phút hoặc có cơn ĐTNOĐ (21,22).
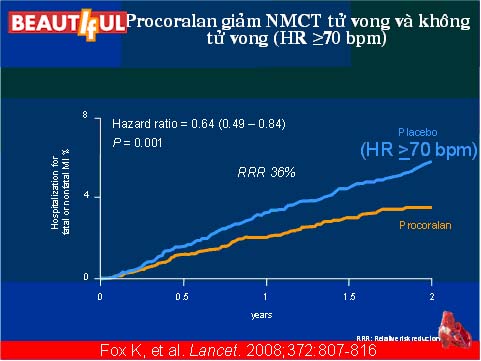
Hình 9. Hiệu quả của Ivabradine trên NMCT tử vong và không TV ở BN nhip tim > 70 lần /phút (21)
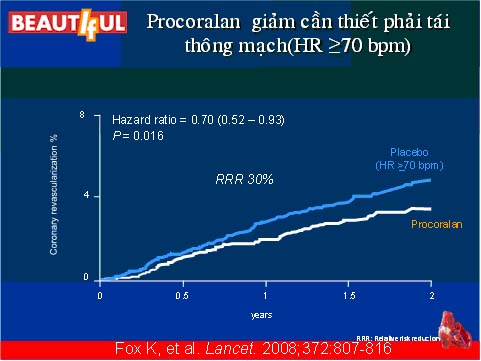
Hình 10. Hiệu quả của Ivabradine trên tái thông mạch ở BN nhip tim > 70 lần /phút (21)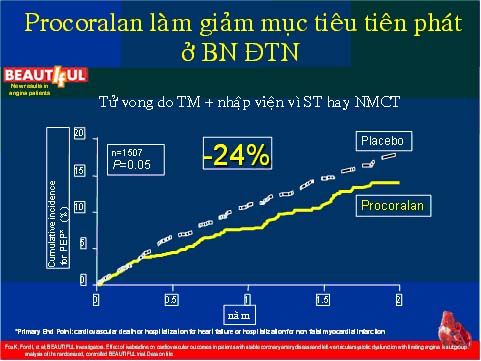
Hình 11. Hiệu quả của Ivabradine trên TV do tim mạch, nhập viện vì suy tim và NMCT ở phân nhóm BN có cơn ĐTN (22).
3. Nghiên cứu phối hợp Ivabradine với chẹn β (23):
Hiệu quả chống ĐTN và chống TMCB của Ivabradine ở Bn ĐTNÔĐ đang điều trị bằng chẹn β được đánh giá qua nghiên cứu ASSIOCIATE (evaluation of the Anti-anginal efficacy and Safety of the aSsocIation Of the if Current Inhibitor ivabrAdine wiTh beta-blockEr). Đây là nghiên cứu ngẫu nhiên mù đôi nhóm song song gồm 889 bn BMVÔĐ. Tiêu chuẩn chọn bệnh:
+ Tuổi ≥ 18 tuổi và ≤ 75 tuổi
+ Tiền sử đau thắt ngực mạn tính liên quan gắng sức ≥ 3 tháng trước khi vào nghiên cứu.
+ Có bằng chứng BMV (1 trong các tiêu chuẩn sau):
- NMCT ≥ 3 tháng
- PCI mạch vành ≥ 6 tháng hay CABG ≥ 3 tháng
- Hẹp ≥ 50% 1 hoặc 2 nhánh mạch vành chính trên chụp MV
- TNGS hình ảnh dương tính
+ Nhịp xoang ≥ 60 l/phút
+ Đang điều trị bằng Atenolol 50mg/ngày hay các β khác liều tương đương.
Nghiên cứu gồm 6 đến 8 tuần khởi động, sau đó theo dõi trong 4 tháng. Trong giai đoạn khởi động, tất cả bn điều dùng 50mg Atenolol và trải qua 3 lần TNGS. BN được chọn nếu tất cả 3 lần TNGS này điều dương tính và phân ngẫu nhiên dùng Ivabradine hay chứng. TNGS sẽ thực hiện tiếp vào tháng thứ 2 và tháng thứ 4.
Mục tiêu chính của nghiên cứu là thay đổi tổng thời gian GS toàn bộ.
Kết quả cho thấy tổng thời gian GS vào tháng thứ 4 tăng 24,3 ± 64,30 ở nhóm Ivabradine so với 7,7 ± 63,8 ở nhóm chứng (P < 0,001). Nhóm dùng Ivabradine cũng tốt hơn nhóm chứng trên mọi chỉ tiêu GS ở tháng thứ 2 và tháng thứ 4 (P < 0,001) (hình 12). Phối hợp này cũng an toàn với chỉ 1,1% bn ngưng thuốc do nhịp chậm ở nhóm Ivabradine. Điều đặc biệt trong nghiên cứu này là liều Atenolol chỉ dùng 50mg/ngày vì trong thực hành, hầu hết bn điều sử dụng liều điều trị này vì đa số các bác sĩ không tăng liều chẹn vì ngại tác dụng phụ xảy ra với bn.
Như vậy, nghiên cứu này chứng tỏ phối hợp Ivabradine (5-7,5mg x 2 lần/ngày) với Atenolol ở liều thông thường có hiệu quả bổ sung và an toàn, dung nạp tốt ở bn BMVÔĐ. Nó cho thấy khả năng của một phương thức phối hợp thuốc mới trong điều trị BMVÔĐ vì không phải lúc nào chúng ta cũng có thể tăng liều chẹn hoặc phối hợp β với Nitrate hay ức chế Calcium.
IV. Chỉ định và thực hành lâm sàng:
Qua các nghiên cứu về đặc điểm dược học của thuốc, cũng như qua các thử nghiệm lâm sàng lớn, chúng ta thấy rằng Ivabradine là thuốc có hiệu quả chống TMCB, cải thiện khả năng GS cho bn BMV, cải thiện chất lượng cuộc sống. Thuốc duy trì hiệu quả lâu dài, ngay cả khi dùng chung với các thuốc tim mạch khác, kể cả β, do đó là một giải pháp hiệu quả cho bn MV hiện nay cũng như trong tương lai. Hướng dẫn điều trị ĐTNÔĐ của Hội tim mạch Châu Au, Mỹ, các sách tim mạch, cũng như Hiệp hội thuốc Châu Âu gần đây đã thống nhất chỉ định dùng Ivabradine như sau (2,3,24,25):
1. Điều trị triệu chứng ĐTNÔĐ ở bn nhịp xoang bình thường:
i. Có chống chỉ định hay không dung nạp với β.
ii. Hoặc phối hợp với β ở bn chưa kiểm soát tốt bằng chẹn và tần số tim > 60l/phút.
2. Điều trị nhịp xoang nhanh không thích hợp hay kháng trị
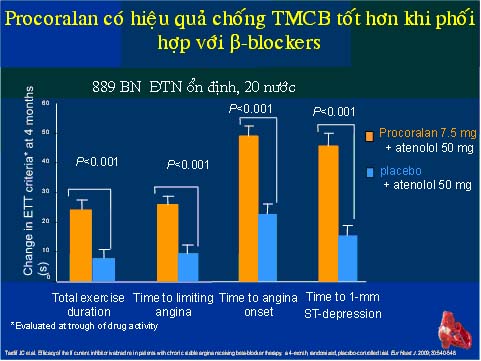
Hình 12. Hiệu quả chống TMCB của Ivabradineở BN đã dùng chẹn beta (23).
Qua kinh nghiệm gần 2 năm sử dụng cùng với các tài liệu thu thập được, chúng tôi nhận thấy một số điểm lưu ý sau đây khi dùng Ivabradine :
(1). Nên khởi đầu với liềù 2,5mg x 2 lần/ngày trong 2 tuần. Nếu không đạt hiệu quả mới tăng liều lên 5mg x 2 lần/ngày. Sau 2 tuần, nếu không đạt mục tiêu điều trị mới tăng lên 7,5mg x 2 lần/ngày. Cũng cần biết khi dùng với liều điều trị tối thiểu (5mg x 2 lần/ngày) nhịp tim giảm ít nhất là 10 –> 12 nhịp/ phút. Chúng ta có thể căn cứ vào mức này để tiên đoán khả năng đạt hiệu quả điều trị của BN, qua đó chỉnh liều cho phù hợp. Ở người lớn tuổi (> 75 tuổi) chỉ nên bắt đầu bằng liều 2,5mg/ngày. Mục tiêu nhịp tim cần đạt là khoảng 60 –> 65 lần/phút. Ở bn kèm COPD hay các bệnh phổi mạn tính khác, nhịp tim đích có thể cao hơn (khoảng 70 lần/phút), tuy nhiên cũng còn phụ thuộc từng người bệnh.
(2). Thuốc có thể dùng chung với các thuốc TM khác: kháng tiểu cầu, statin, ức chế men chuyển hay thụ thể, chẹn kênh Calcium Dihydropyridine, Fibrate, Nitrate, Warfarin, Digoxin. Không nên phối hợp với các thuốc chẹn trên Calcium nhóm Non Dihydropyridine, các thuốc chống loạn nhịp khác, cũng như các thuốc chủ yếu chuyển hóa qua men CYP3A4 ở gan, kháng sinh nhóm Macrolid, thuốc ức chế men protein HIV,…
(3). Hiện nay thuốc đã được cho phép dùng chung với β. Tuy nhiên, chỉ được phối hợp với liều β thông thường (50mg Atenolol hoặc tương đương) và khi nhịp tim > 70 lần/phút. Trong thời gian đầu sử dụng nên theo dõi sát nhịp tim và ECG của BN (đo ECG mỗi tuần). Rối loạn dẫn truyền trong thất không phải là chống chỉ định dùng Ivabradine.
4. Minh họa 2 trường hợp lâm sàng: H13A & B.
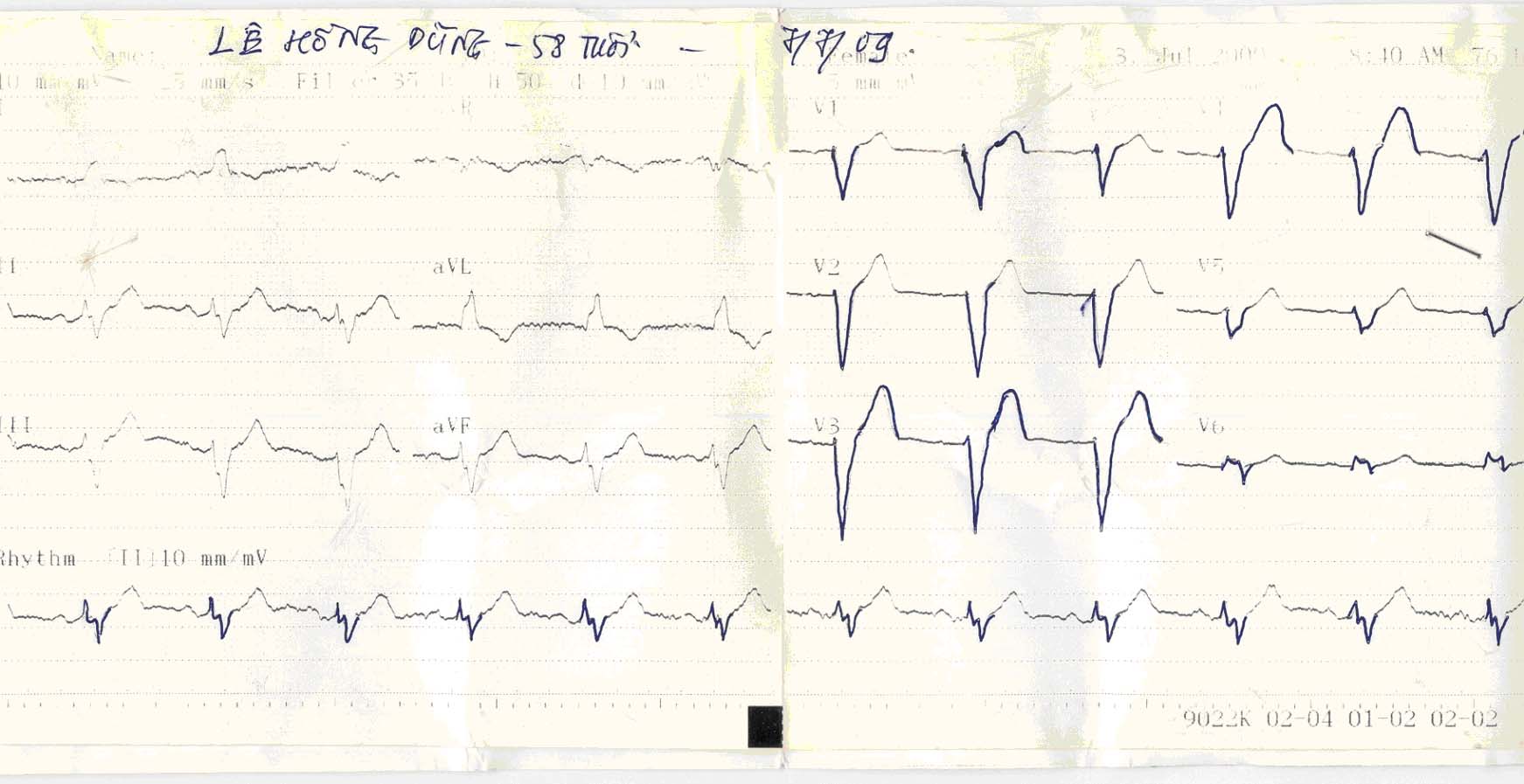
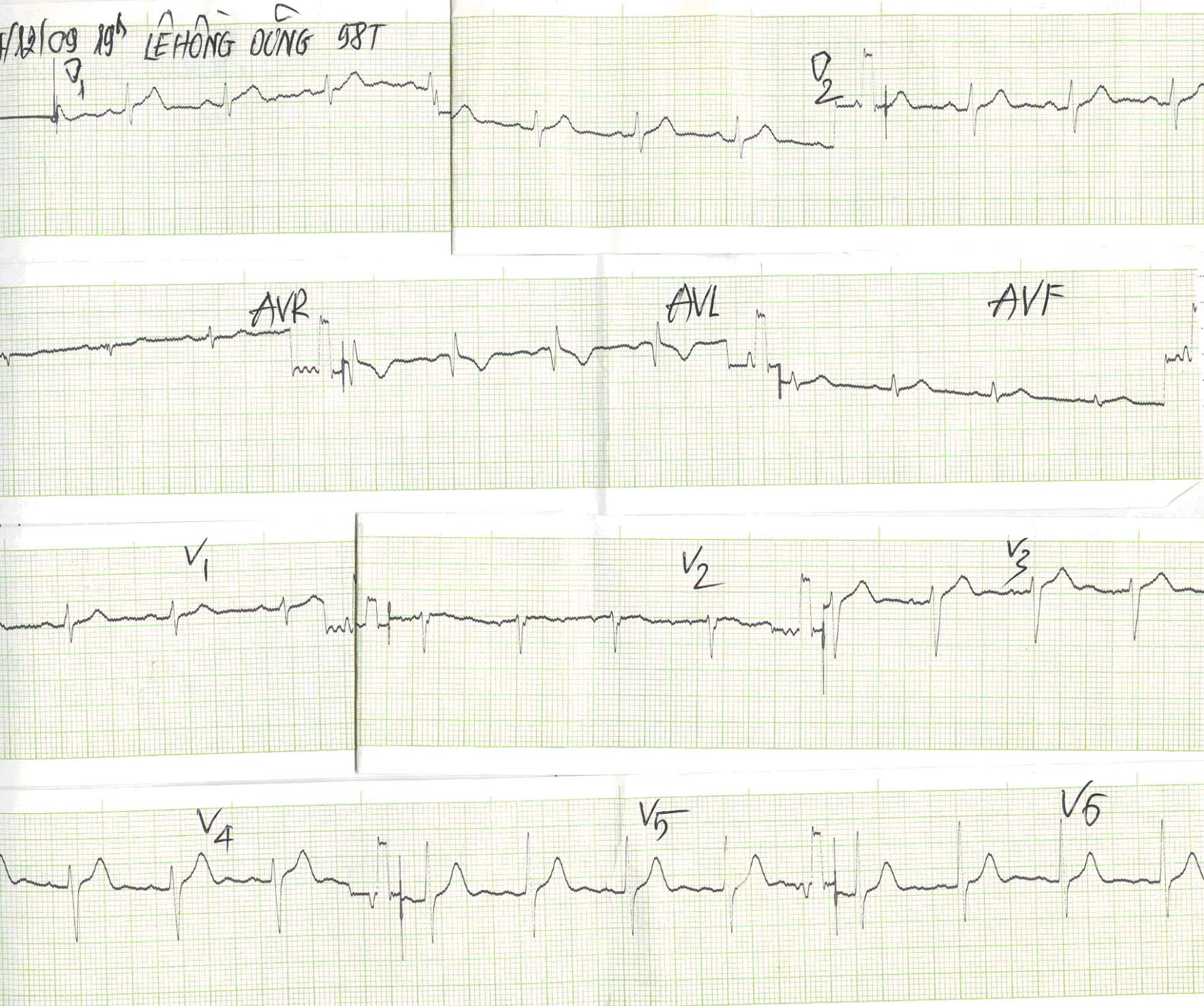
Hình 13A
Hình 13B
BN nam 58 tuổi bị CĐTNOĐ, CCS II-III với tiền căn lao phổi, COPD, THA, đái tháo đường type 2 được điều trị bằng ACEIs, Nitrate, statin, aspirine, và thuốc chống đái tháo đường (BN không dùng được βeta).
(A) là trước khi dùng procorolan. BN vẫn còn đau ngực và ECG biểu hiện nhịp xoang, tần số khoảng 88 lần/ph kèm block nhánh trái. (B) là sau khi dùng procorolan 2,5mg/lần x 2 lần/ngày. BN hết đau ngực, nhịp tim còn khoảng 75 lần phút và hết block nhánh.
H14 a & b.
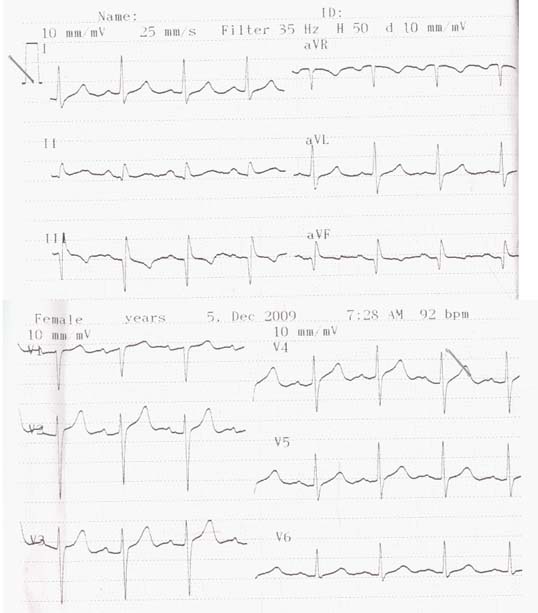
Hình 14A
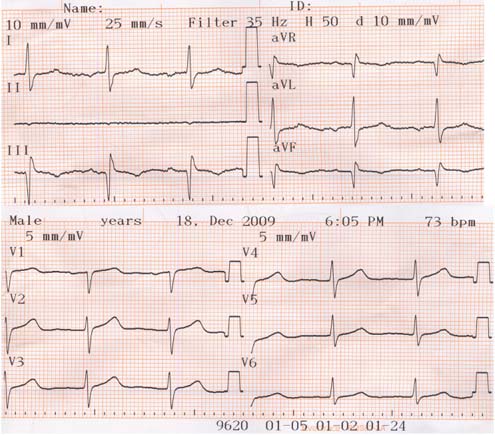
Hình 14B
BN nữ, 76 tuổi bệnh 2 nhánh mạch vành đã đặt stent. Sau đặt BN vẫn còn có cơn đau ngực dù đã dùng βeta (atenolol 50mg/ngày) và nitrate. Hình A là trước khi phối hợp với procorolan, nhịp tim khoảng 85 lần/ph, BN vẫn còn có cơn đau ngực. Hình B là sau dùng procorolan, 2,5mg/tuần. Nhịp tim còn 72 lần/ph, không còn cơn đau ngực.
Tài liệu tham khảo
1. Opie.H.L et cs: Controversies in stable coronary artery disease. Lancet 2006; 367: 69-78.
2. Opie.HL : Drugs for the Heart. 7th 2009., p: 48-54.
3. ESC guideline on the management of stable angina pectoris. 2006.
4. Hajalmarson.A : Heart rate- an independent risk factor of cardiovascular disease. Eur Heart J 2007. 9 (Supplement F) : F3-F7
5. Curkendall.S.M et al: Cardiovascular disease in patients with chronic obstructive pulmonary disease. Ann epidemiol 2006; 16: 63- 70.
6. Falk.JA et al: Cardiovascular disease in COPD. Proc Am Thorac Soc 2008; vol 5; p:543 – 548.
7. Diaz.A et al: Long-term prognostic value of resting heart rate in patients with suspected or proven coronary artery disease. Eur Heart J 2005;26:967-974.
8. Zuanetti.G et al: Relevalence of heart rate as a prognostic factor in patients with acute myocardial infaction: the GISSI experience. 1999; ( suppl. H ); H52-57.
9. Heurch.G & Schulz.R : the role of heart rate and the benefist of heart rate reduction in acute myocardial ischaemia. Eur Heart J 2007. 9 (Supplement F) : F 8-14.
10. Lechat.P et al : The CIBIS II. Circulation 2001 ;103 : 1428-1433.
11. Shattock.M, Camma AJ : pure heart rate reduction : the If channel from discovery to the therapeutic target. Br J Cardiol 2006 ;13( 1) : 27-35.
12. Fox.K et al : Resting heart rate in cardiovascular disease. JACC 2007 ;50 (9) : 823-30.
13. Robinson RB, DiFrancesco D. Fundamental and Clinical Cardiology; NY; Marcel Decker; 2001:151-170.
14. Thollon C et al: Electrophysiological effects of S 16257, a novel sinoatrial node modulator, on rabbit and guinea-pig cardiac preparation: comparision with UL-FS 49 . Br J Pharmacol. 1994;112:37-42.
15. DiFrancesco A, et al: Heart rate lowering by specific and selective If current inhibition with ivabradine. Drugs. 2004;64:1757-1765.
16. Bois P et a : Mode of action of bradycardic agent, S 16257, on ionic current of rabbit sinoatrial node cells. Br J Pharmacol. 1996;118:1051-1057.
17. Simon L et al : Coronary and hemodynamic effects of S 16257, a new bradicardic agent, in resting and exercising. J Pharmacol Exp Ther. 1995;275:659-666.
18. Valataine.JP : The discovery of the selective If current inhibitor ivabradine. A new therapeutic approach to ischemic heart disease. Pharmacological Research 2006 ; 53 : 424-434.
19. Tardif JC, et al: Efficacy of Ivabradine, a new selective If inhibitor, compared with atenolol in patients with chronic stable angina. Eur Heart J. 2005;26:2529-2536.
20. Ruzyllo W., Ford IF., Tendera MT, Fox KF.
Antianginal and anti-ischemic effects of the If current inhibitor ivabradine compared to amlodipine as monotherapies in patients with chronic stable angina. Randomised, controlled, double-blind trial.
ESC congress 2004;abstract 878.
21. Fox K, Ford I, et al; BEAUTIFUL Investigators. Effect of ivabradine on cardiovascular outcomes in patients with stable coronary artery diseaseand left-ventricular systolic dysfunction with limiting angina: a subgroup analysis of the randomized, controlled BEAUTIFUL trial. Data on file.
22. Fox K, et al: BEAUTIFUL trial. Lancet. 2008;372:807-816
23. Tardif JC et al. Efficacy of the If current inhibitor ivabradine in patients with chronic stable angina receiving beta-blocker therapy: a 4-month, randomized, placebo-controlled trial. Eur Heart J. 2009;30:540-548.
24. Libby. P et al: Braunwald’s Heart Disease. 8th. 2008; p: 867 & 1377.
25. EMEA/CHMP 2009.