BS. NGUYỄN THANH HIỀN
BS. NGUYỄN TRẦN THU THỦY
I. Mở đầu
Các phương pháp quản lý suy tim phân suất tống máu giảm (HFrEF) hiện nay đã cải thiện đáng kể tỷ lệ sống sót, giảm tỷ lệ nhập viện và nâng cao chất lượng cuộc sống cho bệnh nhân. Các thử nghiệm lâm sàng chứng minh rằng việc bắt đầu điều trị kịp thời mang lại lợi ích sớm và các liệu pháp toàn diện mang lại lợi ích lớn theo thời gian. Mặc dù có các khuyến cáo rõ ràng, việc thực thi điều trị theo hướng dẫn (GDMT) trong thực tế vẫn còn hạn chế ở các khâu: bắt đầu dùng thuốc, tăng liều (up-titration) và duy trì lâu dài. Các rào cản chính bao gồm yếu tố từ phía bệnh nhân (bệnh nặng, HA thấp, suy thận…)/người chăm sóc, bác sĩ và dịch vụ y tế, chẳng hạn như bệnh đồng mắc, tuổi cao, tình trạng dùng quá nhiều loại thuốc (polypharmacy) và nhận thức hạn chế về bệnh.
Huyết áp (HA) thấp là một trong những rào cản phổ biến nhất khiến bác sĩ e ngại khi bắt đầu hoặc tăng liều thuốc, vì nhiều loại thuốc điều trị suy tim có tác dụng hạ HA. Một khảo sát quốc tế của Hiệp hội Suy tim (HFA) cho thấy 66% bác sĩ coi hạ HA là mối lo ngại chính. Tuy nhiên, chúng ta cần thay đổi quan điểm về HA thấp vì huyết áp thấp không triệu chứng hoặc có triệu chứng tối thiểu không nên là rào cản đối với việc triển khai GDMT. Mặc dù HA thấp ở bệnh nhân HFrEF thường liên quan đến tiên lượng xấu, nhưng việc duy trì GDMT thực tế lại giúp làm giảm bớt mối liên quan tiêu cực này, mang lại lợi ích ngay cả ở những người có HA thấp. Do tính phức tạp trong quản lý, các tài liệu đề xuất phương pháp tiếp cận cá nhân hóa, dựa trên đặc điểm lâm sàng của từng bệnh nhân (như HA, nhịp tim, bệnh đồng mắc) để hướng dẫn việc tối ưu hóa việc bắt đầu tăng dần liều lượng thuốc (1-5).
Mục tiêu của bài viết này nhằm tổng hợp các bằng chứng mới nhất và đề xuất các chiến lược cụ thể để tối ưu hóa GDMT cho bệnh nhân HFrEF có HA thấp trong thực hành lâm sàng (hình trung tâm) (6).
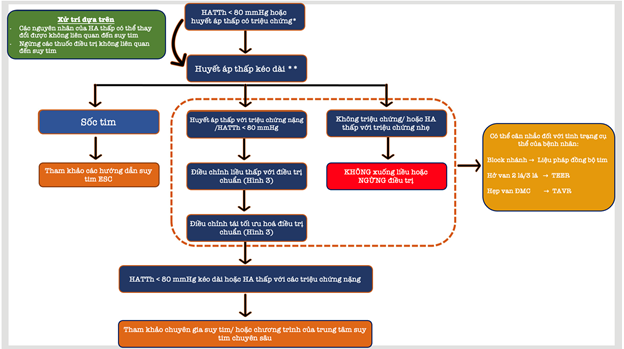
Hình trung tâm: TÓM TẮT THÔNG ĐIỆP
Ghi chú: ESC: Hiệp hội tim mạch Châu Âu, TAVR: thay van động mạch chủ qua catheter; TEER: sửa chữa cạnh-cạnh qua catheter; TR, hở van ba lá. * thấp có triệu chứng nhẹ hoặc nặng. **Huyết áp tâm thu <80 mmHg hoặc huyết áp thấp có triệu chứng hoặc huyết áp thấp không triệu chứng (6).
II. Tỷ lệ HA thấp trong quần thể bệnh nhân HFrEF
II.1. Định nghĩa phức tạp và mang tính quy ước
Việc xác định thế nào là “HA thấp” trong HFrEF thường không đồng nhất và mang tính quy ước tùy theo từng nghiên cứu lâm sàng. Các định nghĩa phổ biến bao gồm:
- Chỉ số tuyệt đối: HA tâm thu (SBP) < 90 mmHg hoặc HA động mạch trung bình (MAP) < 65 mmHg khi nghỉ ngơi.
- Hạ HA tư thế: SBP giảm > 20 mmHg hoặc HA tâm trương (DBP) giảm > 10 mmHg khi đứng.
- Hạ HA có triệu chứng: Mức SBP khoảng 90–100 mmHg đi kèm các triệu chứng như chóng mặt, ngất, đau đầu, rối loạn thị giác hoặc mệt mỏi.
Các tài liệu cũng lưu ý cần phân biệt rõ giữa “HA thấp” (chỉ số sinh tồn) và “hạ HA” (thường bị dùng sai để chỉ tình trạng có triệu chứng) vì sự xuất hiện của triệu chứng có ý nghĩa quan trọng trong quản lý lâm sàng (4,7,8).
II.2. Tỷ lệ hiện mắc trong thực tế (Bệnh nhân ngoại trú)
Dữ liệu từ các sổ bộ thế giới thực cho thấy tỷ lệ HA thấp ở bệnh nhân HFrEF ngoại trú dao động khoảng 3–4% (với ngưỡng SBP < 90 hoặc 95 mmHg). Tuy nhiên, một nghiên cứu tại Anh trên hơn 18.000 bệnh nhân cho thấy tỷ lệ này có thể lên tới 14% trong thời gian theo dõi trung bình 3,3 năm. Đáng chú ý, phụ nữ trẻ (18–39 tuổi) là nhóm có nguy cơ cao nhất với tỷ lệ 17,72 trường hợp trên 100 bệnh nhân-năm (9,10).
II.3. HA thấp trong suy tim cấp (Bệnh nhân nội trú)
Tỷ lệ HA thấp tăng tỉ lệ thuận với mức độ nặng của suy tim và cao hơn đáng kể ở môi trường bệnh viện:
- Trong các sổ bộ suy tim cấp, tỷ lệ này dao động từ 9% (ngưỡng SBP < 90 mmHg) đến 25% (ngưỡng HA tâm thu-SBP < 120 mmHg).
- Tình trạng này liên quan mật thiết đến mức độ nghiêm trọng của bệnh lý và các liệu pháp điều trị đang được áp dụng tại thời điểm nhập viện (11,12).
II.4. Các yếu tố ảnh hưởng
Tỷ lệ HA thấp không cố định mà phụ thuộc vào nhiều yếu tố như: mức độ nặng của suy tim, các bệnh đồng mắc, tuổi tác, giới tính và biểu hiện lâm sàng của từng bệnh nhân. Trong các thử nghiệm lâm sàng, ngưỡng HA thấp thường được cố định (thường gần 90 mmHg) để đảm bảo sức mạnh thống kê và tránh việc bệnh nhân bỏ trị giữa chừng (6).
III. Tiên lượng dự hậu của HA thấp
Huyết áp không chỉ là một rào cản điều trị mà còn là một chỉ số tiên lượng quan trọng đối với HFrEF. Vai trò của nó được thể hiện qua các khía cạnh sau:
- Dấu hiệu dự báo nguy cơ: HA thấp là thành phần chính trong nhiều mô hình đánh giá rủi ro nổi tiếng như PROMPT-HF, LIFE-HF và Seattle Heart Failure Model.
- Mối liên quan giữa chỉ số HA và rủi ro: Theo dữ liệu từ Sổ bộ Suy tim Thụy Điển, nguy cơ gộp (bao gồm tử vong tim mạch hoặc nhập viện do suy tim) tăng lên tỉ lệ nghịch với mức SBP. Cụ thể, so với mức SBP 120 mmHg, nguy cơ này tăng gấp 1,5 lần khi SBP < 100 mmHg và tăng gấp 2,5 lần khi SBP < 80 mmHg.
- Vai trò của điều trị nội khoa tối ưu (GDMT): Một điểm đáng chú ý là tác động tiêu cực của SBP thấp đối với tiên lượng sẽ giảm đi đáng kể khi bệnh nhân được điều trị theo GDMT. Điều này gợi ý rằng tỷ lệ tử vong cao ở nhóm HA thấp có thể một phần do bệnh nhân không được dùng đủ liều thuốc khuyến cáo, thay vì chỉ do mức độ nặng của bệnh.
- Sự kết hợp giữa nhịp tim và HA: Dữ liệu từ sổ bộ quốc tế QUALIFY chỉ ra rằng những bệnh nhân có đồng thời nhịp tim nghỉ ngơi cao và SBP thấp là nhóm có nguy cơ gặp biến cố tim mạch cao nhất.
- Tác động trong suy tim cấp (nội trú): Trong môi trường bệnh viện, SBP thấp ngay lúc nhập viện là một yếu tố dự báo độc lập về tăng tỷ lệ bệnh tật và tử vong. Tương tự, tình trạng SBP thấp trong suốt quá trình nằm viện cũng được xác định là yếu tố dự báo độc lập cho các biến cố lâm sàng bất lợi như những bệnh nhân HFrEF được thu nhận vào thử nghiệm EVEREST (Hiệu quả của thuốc đối kháng Vasopressin trong suy tim: Nghiên cứu kết quả với Tolvaptan).
Tóm lại, mặc dù HA thấp cảnh báo tiên lượng xấu, nhưng việc duy trì và tối ưu hóa các liệu pháp GDMT giúp cải thiện đáng kể kết cục lâm sàng cho nhóm bệnh nhân này (4, 13-15).
IV. Ảnh hưởng của các phương pháp điều trị suy tim lên HA
Nhiều liệu pháp điều trị suy tim có thể làm giảm HA, trong đó mức giảm rõ nhất thường gặp với thuốc ức chế thụ thể angiotensin–neprilysin (ARNi). Tuy nhiên, các liệu pháp nền theo GDMT đã được chứng minh là hiệu quả và an toàn trên toàn bộ phổ SBP ban đầu, và tác động hạ HA của thuốc suy tim có xu hướng giảm dần khi SBP nền càng thấp (15).
Trong các thử nghiệm với thuốc ức chế SGLT2, tỷ lệ hạ HA nhìn chung thấp và tương đương giả dược (SOLOIST-WHF: 6% vs 4,6%; EMPEROR-Reduced: 5,7% vs 5,5%; DAPA-HF: 0,3% vs 0,5%). Đáng chú ý, ở nhóm SBP nền thấp, mức giảm HA trung bình rất nhỏ hoặc thậm chí có xu hướng tăng huyết áp theo thời gian (quan sát trong DAPA-HF, EMPEROR-Reduced và COPERNICUS), có thể phản ánh sự cải thiện chức năng tim. Tương tự, trong EMPHASIS-HF, eplerenone làm tăng nhẹ SBP ở nhóm có SBP nền thấp (6, 16).
Trong PARADIGM-HF, hạ HA là nguyên nhân quan trọng khiến bệnh nhân không hoàn tất giai đoạn run-in, nhưng hiệu quả và độ an toàn của sacubitril/valsartan vẫn được duy trì bất chấp sự xuất hiện của hạ HA hay không và nhất quán trên mọi mức SBP nền. Đáng chú ý, ở bệnh nhân HFrEF thuộc nhóm có SBP nền thấp nhất (95–110 mmHg), HA có xu hướng tăng nhẹ trong suốt thời gian theo dõi ở cả hai nhánh điều trị, mặc dù mức tăng rõ rệt hơn ở nhóm dùng enalapril. Điều này củng cố quan điểm rằng HA thấp không nên là rào cản cho tối ưu hóa GDMT (17).
Các biến cố hạ HA xảy ra thường xuyên hơn trong bối cảnh suy tim cấp. Trong ASCEND-HF, 22% bệnh nhân có ít nhất một đợt hạ HA nội viện. Trong PIONEER-HF, dù đã áp dụng các biện pháp phòng ngừa, hạ HA triệu chứng vẫn xảy ra ở khoảng 15% bệnh nhân dùng sacubitril/valsartan. STRONG-HF ghi nhận hạ HA ở 5% nhóm tối ưu hóa nhanh so với 1% chăm sóc thường quy (7,12,18).
Với các liệu pháp mới hơn, vericiguat trong VICTORIA gây giảm SBP sớm chủ yếu ở bệnh nhân có SBP nền cao hơn, trong khi bệnh nhân SBP thấp có xu hướng tăng HA theo thời gian. Đáng chú ý, omecamtiv mecarbil trong GALACTIC-HF cải thiện biến cố suy tim ở bệnh nhân SBP thấp (≤100 mmHg) mà không ảnh hưởng đáng kể đến HA (19,20).
Tóm lại, mặc dù GDMT có thể làm giảm HA, nguy cơ hạ HA có triệu chứng nhìn chung thấp và lợi ích điều trị được duy trì trên toàn bộ phổ SBP. Do đó, HA thấp đơn thuần không nên ngăn cản việc khởi trị hoặc tối ưu hóa điều trị nền ở bệnh nhân HFrEF.
V. HA thấp trong bối cảnh lâm sàng
Trong thực hành lâm sàng, tình trạng HA thấp ở bệnh nhân suy tim là một thách thức phổ biến, có thể xuất hiện kèm theo triệu chứng hoặc hoàn toàn im lặng. Tình trạng này xảy ra ở cả bệnh nhân nội trú và ngoại trú, mặc dù tần suất ghi nhận thường cao hơn trong các đợt nhập viện vì suy tim cấp. Đáng chú ý, hạ HA không chỉ xuất hiện ở những người mới bắt đầu điều trị mà còn có thể xảy ra ngay cả trên những bệnh nhân đang được quản lý nội khoa tối ưu.
Để có hướng xử trí đúng đắn, việc xác định chính xác hoàn cảnh và thời điểm xảy ra các đợt HA thấp là vô cùng thiết yếu, đặc biệt là mối liên hệ với các loại thuốc điều trị suy tim đang sử dụng. Các chuyên gia nhấn mạnh việc phân loại nguyên nhân thành hai nhóm chính:
(1). Yếu tố thuận nghịch (có thể đảo ngược): Bao gồm việc sử dụng quá liều thuốc lợi tiểu dẫn đến mất nước, hoặc tác động hiệp đồng từ các loại thuốc điều trị bệnh đồng mắc khác. Việc nhận diện sớm các yếu tố này là cực kỳ quan trọng, vì khi được can thiệp kịp thời, bệnh nhân có thể tiếp tục duy trì và tối ưu hóa GDMT – nền tảng giúp cải thiện tiên lượng sống.
(2). Yếu tố không thuận nghịch: Liên quan trực tiếp đến tiến trình tự nhiên của bệnh như giai đoạn suy tim tiến triển hoặc do tuổi tác của bệnh nhân.
HA thấp có thể bắt nguồn từ các vấn đề tim mạch (như suy giảm cung lượng tim) hoặc các vấn đề ngoài tim mạch (như bệnh lý nội tiết, nhiễm trùng). Việc đánh giá toàn diện xác định nhanh chóng nguyên nhân gốc rễ là yêu cầu cấp thiết, đặc biệt trong bối cảnh cấp cứu, nhằm đưa ra quyết định lâm sàng chính xác: liệu nên điều chỉnh các yếu tố thúc đẩy hay phải bắt buộc giảm liều thuốc điều trị suy tim. . Các yếu tố góp phần gây hạ HA ở bệnh nhân suy tim có thể được phân loại thành hai nhóm riêng biệt (Bảng 1):
a. Các yếu tố liên quan đến tim mạch: bao gồm các yếu tố liên quan đến mức độ nghiêm trọng của bệnh và các liệu pháp điều trị, bao gồm phân loại NYHA tiến triển, bệnh van tim từ trung bình đến nặng, thuốc tim mạch (ví dụ: thuốc hạ HA, nitrat, thuốc lợi tiểu) và các tình trạng như viêm cơ tim và thiếu máu cục bộ cấp tính làm trầm trọng thêm tình trạng suy tim mất bù do giảm thể tích nhát bóp và/hoặc tăng áp lực đổ đầy. Đáng chú ý, trong trường hợp cấp tính, ý nghĩa lâm sàng của hạ HA thường chỉ ra tình trạng giảm cung lượng tim và thể tích nhát bóp, mặc dù hoạt hóa giao cảm tăng cao, điều này thường làm tăng sức cản ngoại vi và tăng sức co bóp cơ tim.
b. Các yếu tố không liên quan đến tim mạch: bao gồm một số bệnh đi kèm, chẳng hạn như nhiễm trùng và bệnh Parkinson, hoặc các phương pháp điều trị y tế không liên quan đến tim mạch, như thuốc chẹn alpha trong điều trị phì đại tuyến tiền liệt, thuốc ức chế phosphodiesterase-5 trong điều trị rối loạn cương dương, thuốc ức chế tái hấp thu serotonin và norepinephrine và thuốc chống trầm cảm ba vòng/bốn vòng trong điều trị trầm cảm, levodopa trong điều trị bệnh Parkinson. Đáng chú ý là các yếu tố này có thể chồng chéo và gây ra tác động hiệp đồng làm HA thấp trong các trạng thái bệnh lý khác nhau, đôi khi dẫn đến việc hiểu sai là dấu hiệu của suy tim nặng hơn. Ví dụ, một đánh giá ngắn gọn có thể bỏ qua những phức tạp ở bệnh nhân tiểu đường bị suy tim, trong đó HA thấp có thể bị nhầm lẫn là do suy tim nặng hơn thay vì rối loạn chức năng tự chủ do tình trạng bệnh kéo dài (6,11,21-24).
Bảng 1: Các nguyên nhân tim mạch và không tim mạch có khả năng gây ra HA thấp
| Nguyên nhân liên quan đến tim mạch | Nguyên nhân không liên quan đến tim mạch |
| · Suy tim tiến triển (tình trạng cung lượng tim thấp – NYHA IIIb – IV; hạ natri máu)
· Giảm thể tích máu (chảy máu gần đây, chấn thương …) · Bệnh van tim (hở van hai lá, hở van ba lá và hẹp van hai lá đáng kể) · Nhịp tim chậm (block nhĩ thất …) · Mất nước (tiểu nhiều; sốt cao, tiêu chảy) · Tăng liều thuốc lợi tiểu trong một tuần trước · Nghỉ ngơi tại giường kéo dài (hạ huyết áp tư thế) · Mang thai 24 tuần đầu · Thuốc hạ huyết áp: Chẹn kênh canxi; thuốc chẹn alpha, tác dụng lên trung ương; thuốc lợi tiểu (thiazide …); thuốc ức chế men chuyển; thuốc chẹn thụ thể angiotensin; thuốc chẹn beta · Thuốc điều trị đau thắt ngực: chẹn beta; chẹn kênh canxi; nitrat · Thuốc điều trị suy tim không phải nhóm I: hydralazine/nitrat · Ngất do trung gian thần kinh · Thay đổi phản ứng mạch máu liên quan đến các bệnh lý đồng mắc (đái tháo đường) Các tình trạng cấp tính – tiến triển nhanh • Bệnh cơ tim chu sinh • Viêm cơ tim • Tăng áp lực ổ bụng (cổ trướng) • Các dấu hiệu sung huyết dai dẳng cần dùng thuốc lợi tiểu liều cao hoặc thuốc giãn mạch |
· Người cao tuổi (nhóm tuổi rất cao )
· Bệnh thận mạn tính · Các vấn đề về nội tiết: suy giáp; suy thượng thận (bệnh Addison); hạ đường huyết; tiểu đường · Nhiễm trùng (khi nặng): Nhiễm trùng đường tiết niệu, sốc nhiễm trùng · Phản ứng dị ứng (sốc phản vệ) · Thiếu hụt chất dinh dưỡng: vitamin B12 và folate gây thiếu máu · Thiếu sắt · Bệnh gan: xơ gan · Bệnh phổi tắc nghẽn mạn tính (COPD) · Bệnh Dementia · Bệnh Parkinson · Trầm cảm · Thuốc: – Thuốc chống trầm cảm – Thuốc chống loạn thần (thế hệ thứ 2) – Thuốc đối kháng Dopamine – Thuốc ức chế PDE5 (rối loạn cương dương) – Thuốc chẹn alpha (BPH) – Thuốc bổ sung và thay thế – Thuốc gây nghiện và rượu – Thuốc chẹn beta nội nhãn (trong glaucoma) |
VI. Ảnh hưởng của các thiết bị, thủ thuật can thiệp và thuốc điều trị không thuộc nhóm I đến việc tối ưu hóa điều trị suy tim
Các thiết bị và thủ thuật can thiệp liên quan đến suy tim có thể được xem xét sớm hơn trong một số trường hợp nhất định, khi việc tối ưu hóa điều trị y tế cho bệnh nhân HFrEF gặp khó khăn do HA thấp. Những can thiệp này có khả năng cải thiện kết quả, giảm triệu chứng, nâng cao chất lượng cuộc sống và cuối cùng là giúp tăng HA, do đó tạo điều kiện thuận lợi cho việc điều trị bằng các liệu pháp nội khoa dựa trên bằng chứng. Mặc dù dữ liệu hiện tại vẫn chưa đủ để xác nhận liệu việc tối ưu hóa điều trị tiêu chuẩn sau các can thiệp như vậy có dẫn đến kết quả tốt hơn hay không, nhưng việc xem xét lại khả năng tối ưu hóa điều trị sau các thủ thuật này là rất đáng giá (6).
VI.1. Các thiết bị và thủ thuật can thiệp
1. Liệu pháp tái đồng bộ tim
Thiết bị tái đồng bộ tim (CRT) đã được chứng minh là rất hiệu quả trong việc cải thiện chất lượng cuộc sống và giảm tỷ lệ nhập viện cũng như tử vong do suy tim ở một số bệnh nhân được chọn lọc mắc HFrEF và rối loạn không đồng bộ điện học thất trái. Việc cấy ghép thiết bị tái đồng bộ tim trong bối cảnh lâm sàng này thường dẫn đến tăng 5% HA trung bình, chủ yếu là do tăng cường đồng bộ cơ tim và cải thiện phân suất tống máu thất trái do đảo ngược tình trạng tái cấu trúc. Ngoài ra, liệu pháp này có thể cho phép tăng liều thuốc chẹn beta ở những bệnh nhân bị nhịp tim chậm có triệu chứng (1).
2. Can thiệp van qua catheter và các thủ thuật khác
Các bệnh van tim, chẳng hạn như hẹp van động mạch chủ (ĐMC) hoặc hở van hai lá hoặc ba lá, trong bối cảnh HFrEF có thể gây ra hoặc làm nặng thêm tình trạng hạ HA, chủ yếu làm giảm thể tích nhát bóp và cung lượng tim. Việc giảm tình trạng hẹp van ĐMC đã được chứng minh là làm tăng đáng kể HA sau thủ thuật. Thật vậy, trong thử nghiệm PARTNER I (Thay van ĐMC qua catheter), tập trung vào những bệnh nhân bị hẹp van ĐMC nặng, có triệu chứng, có nguy cơ phẫu thuật cao hoặc hạn chế phẫu thuật, được tiến hành thay van ĐMC qua catheter (TAVR), 55% người tham gia đã ghi nhận sự gia tăng HA tâm thu 30 ngày sau thủ thuật. Hơn 6 tháng sau thủ thuật, SBP tăng vừa phải <10 mmHg và HA tâm trương giảm nhẹ <5 mmHg. Một nghiên cứu khác trên 105 bệnh nhân bị hẹp van ĐMC nặng đã báo cáo sự gia tăng SBP ngay sau thủ thuật thay van (trung bình 15 ± 31 mmHg), kéo dài hơn 5 ngày ở 51% bệnh nhân. Mặc dù không có dữ liệu cụ thể nào cho các nghiên cứu có thực hiện thủ thuật này trên đối tượng bn HFrEF, nhưng về mặt sinh học, có thể quan sát thấy những lợi ích tương tự trong việc cải thiện HA ở những bệnh nhân này (25,26).
Tương tự, việc sửa chữa mép van qua ống thông (TEER) đối với van nhĩ thất có thể làm giảm dòng phụt ngược trong tuần hoàn phổi hoặc tuần hoàn hệ thống, do đó làm giảm tắc nghẽn và tăng cường lưu lượng tim và tưới máu. Sự cải thiện này có thể mang lại những tác động có lợi cho HA và chức năng thận, và tạo điều kiện thuận lợi cho việc tối ưu hóa các điều trị tiêu chuẩn. Một nghiên cứu đáng chú ý gần đây thu thập dữ liệu từ sổ đăng ký EuroSMR (Sổ đăng ký sửa chữa van qua catheter cho hở hai lá thứ phát tại Châu Âu), bao gồm một nhóm bệnh nhân đoàn hệ lớn, không được chọn lọc, bị hở hai lá nặng và HFrEF, cho thấy yếu tố dự báo độc lập quan trọng nhất về việc tăng cường điều trị nội khoa sau thủ thuật sửa hai lá là mức độ giảm tối đa của tình trạng hở hai lá (27,28).
Rung nhĩ có thể ảnh hưởng xấu đến tình trạng suy tim. Việc không có nhịp nhĩ, kiểm soát nhịp tim kém, khả năng thích ứng kém của nhịp tim với nhu cầu chuyển hóa và nhịp tim không đều có thể góp phần gây suy tim mất bù và hạ HA. Các quan sát trước đây đã chỉ ra rằng một chuỗi khoảng RR không đều có thể làm giảm cung lượng tim khoảng 0,8 L/phút, không phụ thuộc vào nhịp tim. Ở những bệnh nhân HFrEF, khi RN được cho là có góp phần đáng kể vào tình trạng HA thấp, khôi phục nhịp xoang có thể là một phương pháp hợp lý (29).
VI.2. Các thuốc khác:
(1) Ivabradine
Thuốc ức chế kênh If xoang nhĩ Ivabradine làm giảm hiệu quả nhịp tim nhanh ở những bệnh nhân có nhịp xoang mà không ảnh hưởng xấu đến huyết áp, thay vào đó có thể cho thấy sự gia tăng nhẹ HA. Ivabradine có thể đặc biệt có lợi ở những bệnh nhân HFrEF khi HA thấp hạn chế việc tối ưu hóa điều trị hoặc tăng liều thuốc chẹn beta, có khả năng cho phép quản lý thuốc chẹn beta hiệu quả hơn theo thời gian, cả trong các trường hợp suy tim mạn tính và cấp tính. Đáng chú ý, một phân tích thứ cấp của nghiên cứu SHIFT (Thử nghiệm Điều trị Suy tim Tâm thu bằng Thuốc ức chế If Ivabradine) đã chứng minh rằng việc giảm nhịp tim lúc nghỉ bằng Ivabradine có hiệu quả trong việc cải thiện kết quả lâm sàng cho bệnh nhân HFrEF với SBP thấp (30,31).
(2) Digoxin
Digoxin, một glycoside tim có đặc tính tăng co bóp cơ tim và tác dụng điều hòa thần kinh-hormone bằng cách thiết lập lại độ nhạy của thụ thể baroreceptor với các tác dụng giống phó giao cảm và kháng adrenergic kéo dài, dẫn đến tăng cung lượng tim, giảm hậu tải và giảm áp lực mao mạch phổi ở bệnh nhân HFrEF. Các hướng dẫn hiện hành khuyến cáo sử dụng digoxin ở nhóm bệnh nhân này như một phương pháp điều trị bậc hai để kiểm soát tần số rung nhĩ, kết hợp với thuốc chẹn beta. Do digoxin không làm giảm (hoặc thậm chí làm tăng) huyết áp, nên có thể cân nhắc sử dụng cho bệnh nhân HFrEF, rung nhĩ và nhịp tim tăng cao, khi việc tối ưu hóa điều trị tiêu chuẩn bị hạn chế bởi HA thấp, nhằm giúp tăng cường tối ưu hóa các phương pháp điều trị được khuyến cáo khác. Một thử nghiệm ngẫu nhiên hiện đang được tiến hành để đánh giá tác động của việc bổ sung digoxin liều thấp vào chế độ chăm sóc tiêu chuẩn nhằm giảm tỷ lệ tử vong và các biến cố suy tim ở bệnh nhân HFrEF hoặc giảm nhẹ, dù ở nhịp xoang hay rung nhĩ (nghiên cứu DECISION [Đánh giá Digoxin trong suy tim mạn tính: Nghiên cứu điều tra trên bệnh nhân ngoại trú tại Hà Lan]. DECISION là thử nghiệm ngẫu nhiên, mù đôi, đối chứng giả dược, tuyển bệnh nhân suy tim mạn có LVEF <50%, bao gồm cả bệnh nhân nhịp xoang và rung nhĩ. Liều khởi đầu thường 0,2 mg/ngày, giảm còn 0,1 mg/ngày nếu tuổi ≥75, eGFR ≤60 mL/phút/1,73 m² hoặc có thuốc tương tác. Người bệnh được phân ngẫu nhiên theo tỷ lệ 1:1 vào nhóm digoxin liều thấp hoặc giả dược. Liều digoxin được điều chỉnh trong quá trình theo dõi nhằm duy trì nồng độ huyết thanh mục tiêu 0,5–0,9 ng/mL. Tiêu chí đánh giá chính là tiêu chí gộp gồm tử vong tim mạch, tổng số lần nhập viện do suy tim, hoặc tổng số lần đến viện khẩn cấp vì suy tim nặng lên. Cỡ mẫu dự kiến là 982 bệnh nhân, nhưng nghiên cứu đã hoàn tất tuyển bệnh với 1002 bệnh nhân vào tháng 12/2023. Thử nghiệm DECISION được kỳ vọng sẽ cung cấp thêm bằng chứng về vai trò của digoxin liều thấp khi bổ sung vào điều trị nền hiện đại ở bệnh nhân suy tim có LVEF giảm hoặc giảm nhẹ. Ngoài ra, một thử nghiệm đối chứng ngẫu nhiên khác nhằm đánh giá hiệu quả và tính an toàn của Digitoxin như một liệu pháp bổ trợ cho điều trị ST hiện đại ở bệnh nhân HFrEF tiến triển (nc DIGIT-HF) cũng mới công bố năm ngoái cho thấy digitoxin làm giảm có ý nghĩa tiêu chí gộp gồm tử vong do mọi nguyên nhân hoặc nhập viện đầu tiên vì suy tim nặng lên ở bệnh nhân HFrEF đang được điều trị nội khoa chuẩn. Tuy nhiên, lợi ích này không rõ ràng trên từng thành phần riêng lẻ của tiêu chí chính, và tỷ lệ biến cố bất lợi nghiêm trọng cao hơn ở nhóm digitoxin (32,33,34).
VII. Các tiếp cận thực hành với HA thấp
Do HA có giá trị hạn chế trong việc chỉ thị trực tiếp chức năng tim và tình trạng tưới máu cơ quan, các quyết định lâm sàng không nên bị ảnh hưởng quá mức bởi các chỉ số HA thấp, trừ khi chúng ở mức thấp nghiêm trọng (ví dụ: SBP < 80 mmHg), cho thấy tình trạng suy giảm huyết động đáng kể. Thay vào đó, việc đánh giá bệnh nhân nên tập trung vào kiểm tra các triệu chứng và/hoặc sự tưới máu cơ quan, vì HA thấp không phải lúc nào cũng tương quan với tình trạng giảm tưới máu (6, 35).
Ngưỡng SBP < 80 mmHg hoặc tình trạng hạ HA gây ra các triệu chứng nghiêm trọng ở bệnh nhân HFrEF mạn tính, bất kể trong bối cảnh nào, là một ngưỡng tới hạn cần được chú ý đặc biệt. Tình trạng này có thể đòi hỏi phải đánh giá lại quá trình điều trị nội khoa, bao gồm cả việc cân nhắc điều chỉnh liệu pháp GDMT. Ngược lại, hạ HA chỉ đi kèm với các triệu chứng nhẹ không phải là lý do để trì hoãn hoặc giảm liều GDMT điều trị suy tim.
Các tác giả đề xuất thực hiện đánh giá bệnh nhân một cách toàn diện thay vì chỉ dựa vào các chỉ số HA đơn thuần. Điều này nhằm đảm bảo việc quản lý HA thấp được cá thể hóa dựa trên biểu hiện lâm sàng của từng bệnh nhân và các yêu cầu cụ thể của bối cảnh cấp tính hoặc mạn tính (6)
VII.1. HA thấp ở bệnh nhân suy tim mạn tính
Sau khi xác nhận tưới máu cơ quan vẫn đầy đủ (nghĩa là không có tình trạng giảm tưới máu/sốc tim), bước đầu tiên cần làm là xác minh lại các chỉ số HA. Nếu bệnh nhân có các triệu chứng nghiêm trọng, cần đánh giá xem liệu các triệu chứng đó có tương xứng với các giá trị HA thấp đo được hay không (bảng 2). Tình trạng giảm tưới máu cơ quan kém kéo dài (có thể đi kèm với chức năng thận suy giảm nghiêm trọng) là dấu hiệu cần phải đánh giá toàn diện và có thể đòi hỏi bệnh nhân phải nhập viện hoặc chuyển tuyến nhanh đến các chương trình quản lý suy tim tiến triển (hình 1) (6).
a. Các bước ban đầu trong quản lý HA thấp
Do các triệu chứng chỉ thị tình trạng hạ HA (như chóng mặt và mệt mỏi) thường không đặc hiệu, việc thiết lập mối liên hệ giữa sự xuất hiện của chúng (đặc biệt là khi đứng hoặc ở tư thế thẳng đứng) với tình trạng HA thấp là vô cùng thiết yếu.
Quy trình này bao gồm việc đo huyết áp ở cả hai tư thế: nằm ngửa và đứng. Nếu SBP giảm 20 mmHg và/hoặc HA tâm trương giảm 10 mmHg trong vòng 3 phút đầu tiên khi đứng, điều đó gợi ý nguyên nhân gây ra triệu chứng là do HA.
Trong trường hợp hạ HA tư thế không được xác nhận qua đo tại phòng khám, có thể sử dụng theo dõi huyết áp lưu động (ABPM) để xác định các đợt hạ HA có tương quan với các triệu chứng mà bệnh nhân báo cáo; phương pháp này cũng cung cấp các thông tin tiên lượng quan trọng. Nếu mức SBP vẫn không khớp với các triệu chứng hạ HA tư thế, nên đánh giá lại bệnh nhân trong thời gian ngắn bằng ABPM và các bài kiểm tra HA tư thế đứng.
Bước tiếp theo là xác định các yếu tố gây hạ HA không liên quan đến HFrEF, chẳng hạn như:
- Các tình trạng bệnh lý tạm thời dẫn đến mất nước (như tiêu chảy, sốt, hoặc điều trị quá liều thuốc lợi tiểu).
- Việc sử dụng các loại thuốc tim mạch không được khuyến cáo cho HFrEF (như thuốc chẹn kênh calci, thuốc hạ HA tác dụng trung ương, hoặc thuốc chẹn alpha cho bệnh tuyến tiền liệt); những loại thuốc này nên được giảm liều hoặc ngừng sử dụng.
Các bước xử trí kế tiếp sẽ khác nhau tùy thuộc vào việc bệnh nhân mới bắt đầu điều trị hay đã đang sử dụng liệu pháp GDMT (6,26,37)
Bảng 2: Cách xác định khi HA có ý nghĩa lâm sàng hay không
| 1. Đo HA tại phòng khám
• Đo HA ở tư thế nằm ngửa/ngồi và đứng (trong 3 phút) để xác định bệnh nhân có bị hạ HA tư thế đứng (giảm 20 mmHg SBP và/hoặc 10 mmHg huyết áp tâm trương) hay không. • Nếu có triệu chứng trong khi xác định hạ HA tư thế đứng => Hạ HA có triệu chứng 2. Đo HA liên tục ABPM • Xem xét đo huyết áp liên tục nếu không xác định được hạ HA tư thế đứng khi đo HA tại phòng khám • So sánh các triệu chứng với đợt hạ HA trên HA liên tục, nếu so sánh được => Hạ HA có triệu chứng 3. Đánh giá lại • Nếu HA ban đầu tại phòng khám (+/− thiết bị đo HA liên tục) không xác định được hạ HA có triệu chứng, hãy cân nhắc đánh giá lại trong quá trình theo dõi 4. Trong mọi trường hợp (ngay cả khi không có triệu chứng liên quan đến hạ HA), hãy giải quyết các yếu tố gây hạ HA không liên quan đến HFrEF: a. các tình trạng bệnh lý thoáng qua (ví dụ: tiêu chảy hoặc sốt) b. Sử dụng các phương pháp điều trị tim mạch không được khuyến cáo cho HFrEF |
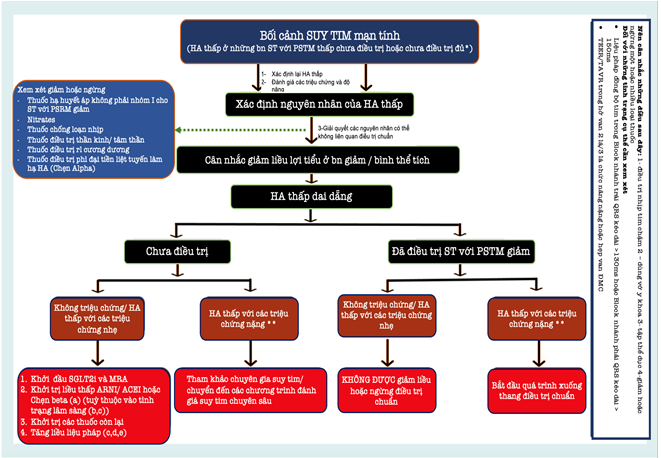
Hình 1: Mô hình đề xuất để tối ưu hóa điều trị ở bệnh nhân HFrEF và HA thấp, cả những bệnh nhân chưa từng điều trị và đã điều trị.
Ghi chú: ACEI, thuốc ức chế men chuyển angiotensin; ARNI, thuốc ức chế thụ thể angiotensin-neprilysin, BB, thuốc chẹn beta; BP, huyết áp; BPH, phì đại tuyến tiền liệt lành tính; CRT, liệu pháp đồng bộ tim; GDMT, liệu pháp điều trị nội khoa theo hướng dẫn; HF, suy tim; HFrEF, suy tim có phân suất tống máu giảm; MRA, thuốc đối kháng thụ thể mineralocorticoid; SGLT2i, chất ức chế đồng vận chuyển natri-glucose 2; TAVR, thay van động mạch chủ qua catheter; TEER, sửa chữa cạnh-cạnh qua catheter.
*Nếu bệnh nhân ổn định với điều trị tối ưu thì không có khả năng liên quan đến liệu pháp điều trị cho HFrEF và hãy tìm kiếm các nguyên nhân khác; trong khi nếu điều trị mới được bắt đầu hoặc tăng liều thì rất có thể liên quan đến một trong các loại thuốc điều trị chuẩn.
**Huyết áp tâm thu <80mmHg; hạ huyết áp tư thế đứng đáng kể, mệt mỏi, uể oải, chóng mặt, v.v.
(a) Bắt đầu với liều thấp nhất và tăng liều từ từ với mức tăng nhỏ cho dù là đối với hệ thống renin – angiotensin – aldosterone hay BB.
(b) Vì huyết áp thấp, có thể dung nạp sacubitril/valsartan liều thấp nếu không bắt đầu ACEI liều thấp/và thử tăng liều (sau một thời gian có thể chuyển sang sacubitril/valsartan).
(c) Bắt đầu SGLT2i và MRA trong bước đầu tiên vì chúng không làm giảm BP, sau đó xem xét dùng BB liều thấp nếu nhịp tim >70 nhịp/phút hoặc ARNI/ACEI/ARB ở liều thấp rồi tăng liều hàng tuần với mức tăng nhỏ cho đến khi đạt liều mục tiêu hoặc liều dung nạp cao nhất. Đôi khi huyết áp cải thiện và có thể tăng liều thuốc dễ dàng hơn (tăng cung lượng tim). Nếu bệnh nhân đạt được liều ACEI hoặc ARB phù hợp (dung nạp được việc tăng liều), có thể chuyển sang sacubitril/valsartan liều thấp.
(d) Nếu không dung nạp được ngay cả liều thấp của ức chế beta và nhịp xoang vẫn còn, có thể sử dụng ivabradine và sau đó có thể bắt đầu hoặc tăng liều ức chế beta. Trong trường hợp rung nhĩ và nhịp tim không kiểm soát, có thể sử dụng digoxin.
(e) Tăng liều từng bước nhỏ mỗi 1-2 tuần, mỗi lần một loại thuốc và theo dõi chặt chẽ.
b. HA thấp ở bệnh nhân suy tim ngoại trú chưa từng điều trị
Quản lý HA thấp ở bệnh nhân HFrEF chưa từng điều trị (naïve) là một thách thức lớn trong lâm sàng, đòi hỏi sự thận trọng nhưng không nên vì thế mà trì hoãn các liệu pháp cứu sống bệnh nhân. Dưới đây là phân tích chi tiết dựa trên các nguồn tài liệu về lộ trình tiếp cận đối tượng bệnh nhân này:
(1). Ý nghĩa của huyết áp thấp ở bệnh nhân mới (Naïve)
- Dấu hiệu tiên lượng: Tình trạng SBP thấp dai dẳng ở bệnh nhân chưa điều trị có thể phản ánh giai đoạn suy tim tiến triển.
- Tiêu chuẩn chẩn đoán: Tuy nhiên, cần lưu ý rằng chỉ riêng chỉ số HA thấp không phải là tiêu chuẩn chính để chẩn đoán suy tim giai đoạn D (giai đoạn cuối) theo tiêu chuẩn của ACC/AHA.
- Hành động ban đầu: Bước đầu tiên luôn là xác định và xử lý các yếu tố thuận nghịch, chẳng hạn như ngừng các thuốc hạ áp không thiết yếu cho suy tim. Nếu HA bình thường hóa sau đó, cần bắt đầu liệu pháp GDMT ngay lập tức.
(2). Chiến lược khởi trị tuần tự (Low-dose Sequencing)
Đối với những bệnh nhân có HA thấp dai dẳng nhưng không có triệu chứng hoặc triệu chứng nhẹ và tưới máu cơ quan vẫn tốt, các tác giả đề xuất lộ trình khởi trị như sau:
- Nhóm ưu tiên 1 (Ít ảnh hưởng đến HA): Nên bắt đầu với thuốc ức chế SGLT2 (SGLT2i) và thuốc kháng thụ thể mineralocorticoid (MRA). Hai nhóm này có tác dụng hạ HA rất ít nhưng mang lại lợi ích lâm sàng nhanh chóng, thậm chí trong một số trường hợp còn giúp cải thiện chức năng tim và làm tăng nhẹ HA.
- Nhóm ưu tiên 2 (Cân nhắc theo đặc điểm lâm sàng):
- Thuốc chẹn beta (BB): Cân nhắc bắt đầu liều thấp nếu nhịp tim (HR) > 70 nhịp/phút. Các nguồn tài liệu ưu tiên các thuốc chẹn beta chọn lọc (như bisoprolol, metoprolol) hơn các thuốc có đặc tính giãn mạch (như carvedilol) vì chúng ít gây hạ huyết áp hơn.
- ARNI (Sacubitril/Valsartan): Có thể khởi đầu với liều thấp (50 mg ngày 2 lần) hoặc liều rất thấp (25 mg ngày 2 lần). Nếu bệnh nhân không dung nạp được ARNI, có thể thay thế bằng thuốc ức chế men chuyển (ACEi) liều thấp.
- Giải pháp hỗ trợ (Ivabradine): Nếu bệnh nhân không dung nạp được thuốc chẹn beta về mặt huyết động, ivabradine là một lựa chọn thay thế khả thi (đối với nhịp xoang) giúp kiểm soát nhịp tim mà không làm giảm thêm huyết áp, từ đó tạo điều kiện để tăng liều thuốc chẹn beta sau này.
(3). Nguyên tắc thực hiện và theo dõi
- Tăng liều từng bước: Chiến lược quan trọng nhất là khởi đầu liều thấp nhất, tăng liều dần dần (từng thuốc một) với các khoảng tăng nhỏ cho đến khi đạt được liều tối đa mà bệnh nhân có thể dung nạp được.
- Quản lý dịch thể: Thuốc lợi tiểu cần được điều chỉnh sát sao theo tình trạng thể tích của bệnh nhân. Cần tránh tình trạng lợi tiểu quá mức (overdiuresis) vì đây là nguyên nhân thường gặp gây hạ HA thuận nghịch.
- Theo dõi sát: Việc giám sát chặt chẽ các triệu chứng và chức năng thận là bắt buộc trong suốt quá trình tối ưu hóa thuốc.
Tóm lại: Mục tiêu cao nhất là không để con số HA thấp (trừ khi SBP < 80 mmHg hoặc có sốc tim) trở thành rào cản ngăn bệnh nhân tiếp cận với GDMT (1,6,31,37,38,39)
c. HA thấp ở bệnh nhân suy tim ngoại trú đang điều trị
Dựa trên các tài liệu gần đây, việc quản lý HA thấp ở bệnh nhân HFrEF ngoại trú đang điều trị bằng liệu pháp GDMT đòi hỏi một cách tiếp cận đa chiều, ưu tiên việc duy trì các thuốc cứu sống bệnh nhân.
Dưới đây là những phân tích chi tiết về quy trình và nguyên tắc xử trí trong bối cảnh lâm sàng này:
(1). Nhận thức đúng về tình trạng hạ HA triệu chứng
- Tần suất và sự dung nạp: HA thấp rất thường gặp ở bệnh nhân HFrEF ngoại trú và không phải lúc nào cũng đồng nghĩa với việc bệnh nhân không dung nạp được thuốc điều trị suy tim.
- Vai trò của giáo dục bệnh nhân: Các triệu chứng nhẹ như chóng mặt thoáng qua khi đứng dậy thường có thể quản lý được thông qua việc tư vấn và giáo dục mà không cần giảm liều thuốc. Khi bệnh nhân hiểu rằng đây là tác dụng phụ của các loại thuốc giúp kéo dài sự sống, giảm nhập viện và cải thiện chất lượng sống (QoL), họ sẽ cảm thấy an tâm và tuân thủ điều trị tốt hơn.
(2). Quy tắc đánh giá cho bệnh nhân ổn định
- Tìm kiếm nguyên nhân ngoài GDMT: Đối với những bệnh nhân đang ổn định lâm sàng nhưng có HA thấp, nguyên nhân thường không trực tiếp do các thuốc GDMT. Bác sĩ cần nhanh chóng đánh giá các yếu tố khác bao gồm:
- Nguyên nhân tim mạch: Bệnh lý van tim hoặc thiếu máu cục bộ cơ tim.
- Nguyên nhân ngoài tim mạch: Bắt đầu sử dụng các thuốc mới như thuốc chẹn alpha để điều trị phì đại tuyến tiền liệt lành tính.
- Tránh ngừng thuốc không cần thiết: Việc xác định các yếu tố này giúp tránh việc gián đoạn hoặc ngừng sử dụng các liệu pháp HFrEF nền tảng một cách không cần thiết.
(3). Quy trình xử trí ưu tiên: Thuốc lợi tiểu là bước đầu tiên
- Đánh giá tình trạng sung huyết: Bước đầu tiên trong việc xử lý HA thấp là đánh giá xem bệnh nhân có còn tình trạng sung huyết hay không thông qua khám lâm sàng, xét nghiệm sinh học hoặc siêu âm phổi/tim.
- Điều chỉnh lợi tiểu: Nếu không có dấu hiệu sung huyết, bác sĩ có thể thận trọng giảm liều thuốc lợi tiểu. Các thử nghiệm lâm sàng gần đây cho thấy việc giảm hoặc ngừng thuốc lợi tiểu là khả thi ở những bệnh nhân ổn định.
- Theo dõi sát: Việc theo dõi nồng độ peptide lợi niệu (natriuretic peptide) một cách định kỳ là rất hữu ích trong quá trình chỉnh liều lợi tiểu để đảm bảo tình trạng sung huyết không trở nên tồi tệ hơn.
- Chiến lược ưu tiên và trình tự thuốc (Sequencing)
- Phân loại tác động của thuốc lên huyết áp: Các bác sĩ cần nhận biết rằng các thuốc như ức chế SGLT2 (SGLT2i) và thuốc kháng thụ thể mineralocorticoid (MRA) rất hiếm khi gây hạ HA. Ngược lại, sacubitril/valsartan (ARNI) có khả năng gây hạ HA triệu chứng cao hơn.
- Cân nhắc liều lượng: Nếu việc điều chỉnh lợi tiểu không thành công và tình trạng hạ HA triệu chứng nghiêm trọng vẫn kéo dài, lúc này mới cần xem xét lại liều lượng hoặc loại thuốc GDMT khác. Điều này đặc biệt quan trọng đối với những bệnh nhân đang trong giai đoạn tối ưu hóa hoặc tăng liều thuốc, vì đây là thời điểm HA thấp dễ xảy ra nhất do tác động của thuốc điều trị suy tim.
Tóm lại, thông điệp cốt lõi từ các nguồn tài liệu là HA thấp không triệu chứng hoặc triệu chứng nhẹ không nên là lý do để ngừng GDMT. Việc quản lý cần tập trung vào loại bỏ các yếu tố gây nhiễu và tối ưu hóa tình trạng dịch thể trước khi can thiệp vào các loại thuốc giúp cải thiện tiên lượng sống của bệnh nhân (1,2,4,9,40,41) .
VII.2. Huyết áp thấp ở bệnh nhân suy tim cấp
Trong bối cảnh suy tim cấp, các giá trị HA nên được diễn giải trong bối cảnh biểu hiện lâm sàng và diễn biến bệnh của bệnh nhân. Trong một nghiên cứu gần đây về suy tim cấp, bệnh nhân có SBP thấp và không có dấu hiệu giảm tưới máu có tiên lượng tương tự như bệnh nhân có SBP bình thường. Thật vậy, việc đánh giá lâm sàng dựa trên tình trạng sung huyết và tưới máu là rất quan trọng vì chỉ riêng HA là không đủ để định hướng điều trị và dự đoán tiên lượng.
- Phân loại kiểu hình: Việc lập hồ sơ lâm sàng dựa trên tình trạng sung huyết (congestion) và tưới máu (perfusion) là cực kỳ quan trọng. Đa số bệnh nhân cấp tính thuộc kiểu hình “wet and warm” (sung huyết nhưng tưới máu tốt), trường hợp này không có chống chỉ định duy trì hoặc khởi trị liệu pháp GDMT sau khi đã ổn định lâm sàng.
- Loại trừ sốc tim: Cần phân biệt hạ HA đơn thuần với sốc tim (được định nghĩa là SBP < 90 mmHg kèm theo dấu hiệu giảm tưới máu cơ quan). Đáng lưu ý, tình trạng giảm tưới máu có thể xảy ra mà không có hạ HA trong giai đoạn đầu của sốc tim do cơ chế co mạch bù trừ.
(1). Chiến lược quản lý theo dòng thời gian (Timeline)
- Trong 48 giờ đầu nhập viện: Mục tiêu chính là ổn định huyết động, điều trị quá tải thể tích/sung huyết và đảm bảo oxy hóa mô. Ở giai đoạn này, đối với các kiểu hình “cold” (lạnh – giảm tưới máu), có thể cần tạm dừng hoặc giảm liều GDMT, đặc biệt là thuốc chẹn beta và thuốc ức chế hệ renin–angiotensin.
- Sau 48 giờ: Khi bệnh nhân đã ổn định, có thể bắt đầu hoặc tái khởi động GDMT. Việc bắt đầu lại hoặc tăng liều dựa trên diễn biến lâm sàng và các đặc điểm cụ thể của bệnh nhân (ví dụ: điều trị tối ưu hoặc chưa tối ưu, suy tim cấp tính mới mắc, v.v.)
- Thứ tự ưu tiên: Nên bắt đầu với các thuốc ít ảnh hưởng đến HA nhất như thuốc ức chế SGLT2 (SGLT2i) hoặc thuốc kháng thụ thể mineralocorticoid (MRA) liều thấp.
- Tăng liều dần dần: Quá trình tăng liều có thể kéo dài từ 4–6 tuần, thực hiện tuần tự từng loại thuốc với các bước điều chỉnh nhỏ và theo dõi sát sao. Cần nỗ lực hết sức để bắt đầu bất kỳ liệu pháp nền tảng nào còn thiếu, trừ khi có chống chỉ định (Hình 2) (1,6,42,43,44).
(2). Bài học từ nghiên cứu STRONG-HF và tính cá thể hóa
Chiến lược tối ưu hóa điều trị sớm này được hỗ trợ bởi kết quả của thử nghiệm STRONG-HF, cho thấy rằng một chiến lược điều trị tích cực, bao gồm tăng liều các thuốc điều trị nền theo GDMT lên 100% liều khuyến cáo trong vòng 2 tuần sau xuất viện và theo dõi chặt chẽ sau nhập viện vì suy tim cấp, đã giảm đáng kể triệu chứng, cải thiện chất lượng cuộc sống (QoL), đồng thời giảm tử vong do mọi nguyên nhân hoặc tái nhập viện vì suy tim trong 180 ngày so với chiến lược điều trị thông thường.
Mặc dù các bệnh đồng mắc ngoài tim mạch hoặc tuổi cao không hạn chế việc tăng liều nhanh, cường độ cao các liệu pháp suy tim, cũng như không làm giảm lợi ích trên tiêu chí chính, nhưng HA nền thấp lại làm tăng khả năng xuất hiện các tiêu chí an toàn được sử dụng để hướng dẫn tăng liều (ví dụ: eGFR <30 mL/phút/1,73 m², kali máu >5,0 mmol/L, huyết áp tâm thu <95 mmHg, nhịp tim <55 bpm, và nồng độ NT-proBNP tăng >10% so với trước xuất viện). Điều này dẫn đến việc sử dụng liều GDMT thấp hơn, tỷ lệ đạt liều tối ưu trung bình thấp hơn, và mức cải thiện chất lượng cuộc sống kém hơn; tuy nhiên, lợi ích của chiến lược điều trị tích cực trong việc giảm bệnh suất và tử vong vẫn được duy trì bất kể với SBP ban đầu. Do đó, những bệnh nhân hồi phục sau nhập viện vì suy tim cấp có HA thấp có thể cần một chiến lược tăng liều từ từ hơn và theo dõi chặt chẽ hơn sau xuất viện nhằm đảm bảo tối ưu hóa điều trị suy tim (45,46).
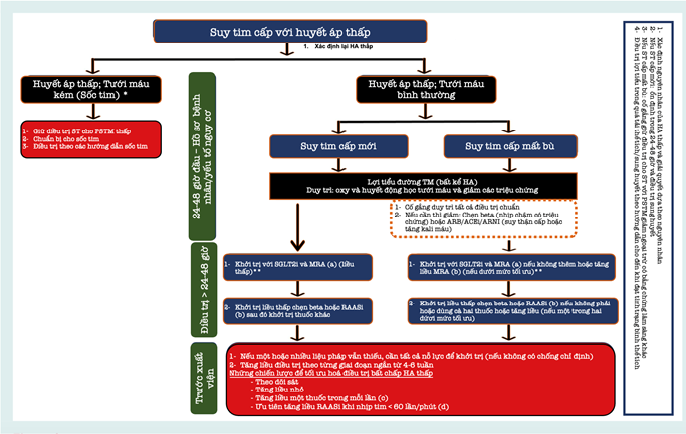
Hình 2: Mô hình đề xuất để tối ưu hóa điều trị ở bệnh nhân HFrEF và HA thấp trong bối cảnh suy tim cấp.
Ghi chú: ACEi, thuốc ức chế men chuyển angiotensin; ARB, thuốc chẹn thụ thể angiotensin; ARNI, thuốc ức chế thụ thể angiotensin-neprilysin;HA, huyết áp; HFrEF, suy tim có phân suất tống máu giảm; NT, nhịp tim; TM, tiêm tĩnh mạch; MRA, thuốc đối kháng thụ thể mineralocorticoid; RAASi, thuốc ức chế hệ renin-angiotensin-aldosterone; SGLT2i, chất ức chế đồng vận chuyển natri-glucose 2.
*Đặc điểm lâm sàng: ướt/lạnh hoặc khô/lạnh.
**Tốc độ lọc cầu thận ước tính >30ml/phút/1,73m2 đối với MRA hoặc >20 ml/phút/1,73 m2 đối với SGLT2i.
- Nếu kali <5,0.
- Tốt nhất nên bắt đầu dùng ARNI liều thấp nếu không dung nạp, chuyển sang ACEi/ARB.
- Nếu nhịp tim không kiểm soát được, không dung nạp BB và nhịp xoang, có thể cân nhắc dùng ivabradine và rung nhĩ, cân nhắc dùng digoxin.
- Bắt đầu dùng ARNI liều rất thấp (25 mg x 2 lần/ngày) và tăng liều, nếu không dung nạp, chuyển sang ACEi/ARB liều thấp.
VII.3. Các tình trạng lâm sàng cụ thể
Ở những bệnh nhân HFrEF và HA thấp, điều quan trọng là phải nhận ra rằng khi một số tình trạng lâm sàng nhất định cùng tồn tại, chỉ có HA thấp đơn thuần, hạ HA triệu chứng hoặc bằng chứng giảm tưới máu có thể đặc biệt bất lợi và có thể ảnh hưởng xấu đến kết cục. Những tình trạng này bao gồm bệnh mạch máu ngoại vi nặng, đặc biệt là với các vết loét và vết thương không lành, hẹp động mạch cảnh hai bên nặng chưa được điều trị, tai biến mạch máu não gần đây (cơn thiếu máu não thoáng qua hoặc đột quỵ), thiếu máu cục bộ ruột hoặc đau thắt ngực bụng, bệnh thận giai đoạn cuối đang chạy thận nhân tạo và tình trạng rối loạn chức năng thần kinh tự chủ. Điều trị hiệu quả trong những tình huống này đòi hỏi một phương pháp tiếp cận đa chuyên khoa để cải thiện kết quả điều trị cho bệnh nhân.
VII.4. Cách sắp xếp trình tự ngừng thuốc trong các tình huống khác nhau
Khi tất cả các chiến lược kiểm soát HA thấp ở bệnh nhân HFrEF đã được thực hiện (ngừng, giảm hoặc thay đổi các phương pháp điều trị không được chỉ định trong hướng dẫn điều trị suy tim năm 2021, liệu pháp điều trị bệnh đi kèm và các thuốc có lợi khác chưa được chứng minh) và các triệu chứng chính hoặc HA thấp nghiêm trọng (<80 mmHg) vẫn tiếp diễn, việc giảm hoặc ngừng một hoặc nhiều loại thuốc điều trị tiêu chuẩn có thể là cần thiết. Điều quan trọng là phải nhận thức rằng kết quả kém liên quan đến tác dụng phụ của thuốc điều trị suy tim có thể xuất phát từ việc ngừng thuốc chứ không phải do bản thân tác dụng phụ. Trong bối cảnh suy tim ngoại trú thực tế, nghiên cứu Rossignol đã phân tích dữ liệu từ sổ đăng ký Suy tim Dài hạn của Chương trình Nghiên cứu Quan sát Châu Âu (EORP) của ESC HFA để tìm hiểu mối quan hệ giữa tăng kali máu, việc ngừng thuốc ức chế hệ renin-angiotensin-aldosterone (RAASi) và các kết quả liên quan. Trong khi tăng kali máu đặt ra một thách thức đáng kể đối với việc bắt đầu và tiếp tục liệu pháp RAASi, nó cũng có thể đóng vai trò là một dấu hiệu nguy cơ góp phần vào việc ngừng điều trị và sử dụng thuốc không tối ưu, cuối cùng dẫn đến tỷ lệ tử vong cao hơn (1,47).
Trong một phân tích của TOPCAT-Americas, những bệnh nhân được phân ngẫu nhiên vào nhóm spironolactone có nhiều khả năng nhận được liều thấp hơn và ngừng thuốc nghiên cứu với tỷ lệ lên tới 30% trong năm đầu tiên trong số những người bị tăng kali máu và tốc độ lọc cầu thận giảm. Đáng chú ý, việc ngừng spironolactone có liên quan đến nguy cơ cao gấp hai đến bốn lần gặp các tác dụng phụ sau đó. Trong một phân tích của Nghiên cứu quan sát từ dự án Stockholm CRE-Atinine Measurements (SCREAM), việc ngừng MRA sau một đợt tăng kali máu có liên quan đến việc giảm nguy cơ tăng kali máu tái phát, nhưng nguy cơ tử vong hoặc các biến cố tim mạch cao hơn. Trong các trường hợp cần ngừng thuốc theo trình tự, việc hiểu rõ các đặc điểm lâm sàng hoặc kiểu hình của bệnh nhân là rất quan trọng để đưa ra quyết định sáng suốt (Hình 4). Trong quá trình này, mọi nỗ lực nên tập trung vào việc tiếp tục điều trị bằng thuốc ức chế SGLT2 và có thể là MRA (nếu không chống chỉ định), vì những thuốc này ít ảnh hưởng nhất đến HA (6,48,49). Đồng thời, để làm giảm các triệu chứng của HA thấp và duy trì tỷ lệ điều trị cao hơn, nên áp dụng các biện pháp can thiệp không dùng thuốc. Các biện pháp này bao gồm giãn cách thời gian dùng thuốc để giảm tác dụng hạ HA hiệp đồng của thuốc điều trị suy tim, tham gia các bài tập thể dục và rèn luyện thể chất đã được chứng minh là cải thiện cả hạ HA tư thế đứng và HA thấp, và sử dụng vớ y khoa để giúp giảm thiểu tình trạng tụt HA tư thế đứng do thay đổi tư thế (50-52). Vì bằng chứng thực tế cho thấy việc ngừng hoặc không bắt đầu lại liệu pháp điều trị suy tim có thể làm tăng đáng kể tỷ lệ tử vong, nên việc bắt đầu lại điều trị càng sớm càng tốt là điều cần thiết. Một số mẹo thực tế có thể giúp tạo điều kiện thuận lợi cho việc bắt đầu hoặc bắt đầu lại điều trị tiêu chuẩn (Hình 3):
- Luôn dùng lại thuốc ở liều thấp nhất có thể và tăng liều cẩn thận kèm theo theo dõi chặt chẽ, tránh bắt đầu lại đồng thời hai loại thuốc.
- Bắt đầu điều trị với liều ARNi thấp hoặc rất thấp. Nếu không dung nạp, chuyển sang liều thấp thuốc ức chế men chuyển hoặc thuốc chẹn thụ thể angiotensin II (ARB), những thuốc này ít ảnh hưởng rõ rệt đến HA.
- Cân nhắc chuyển từ carvedilol hoặc nebivolol sang thuốc chẹn beta chọn lọc không có đặc tính giãn mạch, chẳng hạn như metoprolol hoặc bisoprolol.
- Nếu không đạt được nhịp tim mục tiêu (<70 nhịp/phút) và việc tăng liều thuốc chẹn beta không khả thi, hãy cân nhắc thêm ivabradine cho bệnh nhân có nhịp xoang hoặc digoxin cho bệnh nhân rung nhĩ.
- Đối với tất cả bệnh nhân HFrEF, HA thấp và eGFR >20ml/phút/1,73m2, hãy bắt đầu điều trị bằng thuốc ức chế SGLT2. Nếu bệnh nhân đã dùng thuốc ức chế SGLT2, hãy cân nhắc tăng liều MRA nếu eGFR >25 –30ml /phút/1,73m2, hoặc ưu tiên thuốc chẹn beta nếu eGFR <2 5–30ml/phút/1,73m2.
- Nếu việc tái điều trị dẫn đến HA thấp dai dẳng có triệu chứng và/hoặc giảm tưới máu, hãy chuyển bệnh nhân đến một nhóm chuyên gia suy tim chuyên sâu để được theo dõi và điều trị thêm.
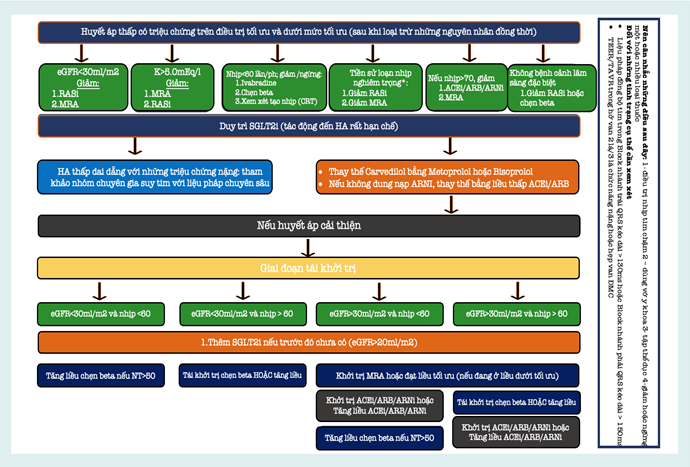
Hình 3: Mô hình đề xuất để giảm liều và tối ưu hóa việc tái điều trị suy tim ở những bệnh nhân HFrEF và HA thấp.
Ghi chú: ACEi, thuốc ức chế men chuyển angiotensin, ARB, thuốc đối kháng thụ thể angiotensin; ARNI, thuốc ức chế thụ thể angiotensin-neprilysin; BB, thuốc chẹn beta; CRT, liệu pháp tái đồng bộ tim; eGFR, ước tính tốc độ lọc cầu thận;ST, suy tim; HFrEF, suy tim có phân suất tống máu giảm; NT, nhịp tim; TM, tĩnh mạch; LBBB, block nhánh trái; MRA, thuốc đối kháng thụ thể mineralocorticoid; RASi, thuốc ức chế hệ renin-angiotensin; RBBB, block nhánh phải; SGLT2i, thuốc ức chế đồng vận chuyển natri-glucose 2; TEER, sửa chữa cạnh-cạnh qua ống thông; TAVR, thay van động mạch chủ qua catheter.
*Chẹn beta quan trọng trong việc kiểm soát loạn nhịp tim
VIII. Kết luận
Để cải thiện việc thực hiện các khuyến cáo trong hướng dẫn điều trị suy tim, điều quan trọng là phải giải quyết các yếu tố lâm sàng hạn chế việc bắt đầu, tối ưu hóa và tiếp tục điều trị tiêu chuẩn, nhằm cải thiện việc chăm sóc và kết quả của bệnh nhân suy tim phân suất tống máu thấp (Bảng 3). Các tác giả nhấn mạnh tầm quan trọng của GDMT ở bệnh nhân HFrEF và HA thấp, định nghĩa hạ HA có liên quan đến lâm sàng, đề xuất một lộ trình để xác định nguyên nhân và các chiến lược quản lý điều trị suy tim trong các tình huống khác nhau. Các tác giả cũng nhấn mạnh vai trò của các can thiệp không dùng thuốc có thể giúp tăng huyết áp và tối ưu hóa điều trị. Mục tiêu chính của tài liệu này là hỗ trợ các nhà cung cấp dịch vụ chăm sóc sức khỏe điều trị bệnh nhân suy tim (bác sĩ tim mạch, bác sĩ hồi sức tích cực và bác sĩ đa khoa) khắc phục tình trạng trì trệ lâm sàng bằng cách cải thiện việc khởi đầu và tối ưu hóa điều trị, đồng thời giảm tỷ lệ ngừng điều trị suy tim. Hơn nữa, tài liệu nhấn mạnh sự cần thiết của việc các bác sĩ ở các chuyên khoa khác tham khảo ý kiến của nhóm điều trị suy tim trước khi giảm hoặc ngừng thuốc điều trị suy tim do nhận thức về chỉ số “HA thấp”. Cuối cùng, các tài liệu đưa ra lời kêu gọi hành động để giải quyết những thiếu sót đáng kể về kiến thức trong lĩnh vực này.
Bảng 3: Những thông điệp chính
| Những thông điệp chính |
| · HA thấp không triệu chứng hoặc có triệu chứng nhẹ không nên là lý do để giảm hoặc ngừng GDMT
· Khuyến cáo nên giảm hoặc ngừng một hoặc nhiều điều trị chuẩn trong trường hợp SBP <80 mmHg hoặc HA thấp kèm theo các triệu chứng liên quan · Trong suy tim mạn tính, luôn đánh giá các triệu chứng hạ HA/hạ HA tư thế · Trong suy tim cấp, luôn đánh giá tưới máu cơ quan (sốc hoặc tiền sốc). · Ngưỡng HA, như một tiêu chí loại trừ trong các thử nghiệm lâm sàng, chủ yếu được thiết lập để ngăn ngừa tình trạng bỏ cuộc và duy trì sức mạnh thống kê của thử nghiệm. · SGLT2 và MRA có tác dụng ít nhất lên HA và ở nhóm HA thấp, chúng có thể làm tăng HA. · Trong một số trường hợp cụ thể, các loại thuốc hoặc thiết bị khác có thể phù hợp để tối ưu hóa điều trị (ivabradine, CRT, TEER, digoxin, …). · Trong trường hợp HA thấp, bước đầu tiên là ngừng các thuốc tim mạch không cần thiết và sau đó tìm kiếm các nguyên nhân thoáng qua và có thể hồi phục. · Phối hợp chăm sóc đa chuyên khoa để lựa chọn các phương pháp thay thế phù hợp có tác dụng hạ HA ít hơn đối với các thuốc không liên quan đến tim mạch (ví dụ: thuốc điều trị phì đại tuyến tiền liệt, thuốc chống trầm cảm). · Khi cần ngừng hoặc giảm liều điều trị: bắt đầu với thuốc ít dung nạp hơn. · Trong trường hợp hạ HA dai dẳng không thể bắt đầu hoặc điều chỉnh điều trị tiêu chuẩn, hãy chuyển sớm đến các chuyên gia về suy tim hoặc các chương trình điều trị nâng cao. · Khi HA cải thiện, luôn cân nhắc bắt đầu lại hoặc thử lại thuốc dựa trên mức độ dung nạp tốt hơn trước. · Cố gắng đạt được liệu pháp tối ưu bằng cách: 1. Chia liều thuốc thành nhiều lần trong ngày. 2. Cho BB chọn lọc hoặc cân nhắc ivabradine. 3. Nếu không dung nạp ARNI, hãy thử dùng và tối ưu hóa ACEi/ARB. |
Tài liệu tham khảo
- McDonagh TA et al. 2021 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure: Developed by the Task Force for the diagnosis and treatment of acute and chronic heart failure of the European Society of Cardiology (ESC). With the special contribution of the Heart Failure Association (HFA) of the ESC. Eur J Heart Fail 2022; 24:4–131.
- Vaduganathan M et al. Estimating lifetime benefits of comprehensive disease-modifying pharmacological therapies in patients with heart failure with reduced ejection fraction: A comparative analysis of three randomised controlled trials. Lancet 2020; 396:121–128
- D’Amario D et al. Association between dosing and combination use of medications and outcomes in heart failure with reduced ejection fraction: Data from the Swedish Heart Failure Registry. Eur J Heart Fail 2022; 24:871–884
- N et al. Hypotension in heart failure is less harmful if associated with high or increasing doses of heart failure medication: Insights from the Swedish Heart Failure Registry. Eur J Heart Fail 2024; 26:359–369
- Rosano GMC et al. Patient profiling in heart failure for tailoring medical therapy. A consensus document of the Heart Failure Association of the European Society of Cardiology. Eur J Heart Fail 2021;23: 872–881
- H et al. Clinical management and therapeutic optimization of patients with heart failure with reduced ejection fraction and low blood pressure. A clinical consensus statement of the Heart Failure Association (HFA) of the ESC. European Journal of Heart Failure (2025). doi:10.1002/ejhf.3618
- A et al. Safety, tolerability and efficacy of up-titration of guideline-directed medical therapies for acute heart failure (STRONG-HF): A multinational, open-label, randomised, trial. Lancet 2022; 400:1938–1952
- JF, Brunner-La Rocca HP, Linssen GCM et al; CHECK-HF Investigators. Treatment differences in chronic heart failure patients with reduced ejection fraction according to blood pressure. Circ Heart Fail 2020; 13:e006667. https://doi.org/10.1161/CIRCHEARTFAILURE.119
- Melendo-Viu. M et al. Hypotension at heart failure discharge: Should it be a limiting factor for drug titration? Int J Cardiol 2023; 386:59–64
- O, Feldman L, Cohen N. Heart failure and orthostatic hypotension. Heart Fail Rev 2016; 21:529–538
- Martin-Perez. M, et al. Development of hypotension in patients newly diagnosed with heart failure in UK general practice: Retrospective cohort and nested case-control analyses. BMJ Open 2019;9: e028750. https://doi.org/10.1136/bmjopen-2018-028750
- PA et al. Hypotension during hospitalization for acute heart failure is independently associated with 30-day mortality: Findings from ASCEND-HF. Circ Heart Fail 2014; 7: 918–925
- Abdin A. et al. Associations between baseline heart rate and blood pressure and time to events in heart failure with reduced ejection fraction patients: Data from the QUALIFY international registry. Eur J Heart Fail 2023; 25:1985–1993.
- AP, et al. Clinical profile and prognostic value of low systolic blood pressure in patients hospitalized for heart failure with reduced ejection fraction: Insights from the Efficacy of Vasopressin Antagonism in Heart Failure: Outcome Study with Tolvaptan (EVEREST) trial. Am Heart J 2013; 165:216–225.
- O, et al. Incidence, predictors, and outcomes associated with hypotensive episodes among heart failure patients receiving Sacubitril/valsartan or Enalapril: The PARADIGM-HF trial (Prospective Comparison of Angiotensin Receptor Neprilysin Inhibitor with Angiotensin-Converting Enzyme Inhibitor to Determine Impact on Global Mortality and Morbidity in Heart Failure). Circ Heart Fail 2018; 11: e004745. https://doi.org/10.1161/CIRCHEARTFAILURE.117.004745
- M, et al. Mineralocorticoid receptor antagonists, blood pressure, and outcomes in heart failure with reduced ejection fraction. JACC Heart Fail 2020; 8:188–198 Desai. AS, Solomon S, Claggett B, McMurray JJV, Rouleau J, Swedberg K, et al. Factors associated with noncompletion during the run-in period before randomization and influence on the estimated benefit of LCZ696 in the PARADIGM-HF trial. Circ Heart Fail 2016; 9: e002735. https://doi.org/10.1161/CIRCHEARTFAILURE.115.002735
- EJ, et al.; PIONEER-HF Investigators. Angiotensin-neprilysin inhibition in acute decompensated heart failure. N Engl J Med 2019; 380:539–548.
- CSP, et al. VICTORIA Study Group. Blood pressure and safety events with vericiguat in the VICTORIA trial. J Am Heart Assoc 2021; 10: e021094. https://doi.org/10.1161/JAHA.121.021094
- M, et al. Effects of omecamtiv mecarbil in heart failure with reduced ejection fraction according to blood pressure: The GALACTIC-HF trial. Eur Heart J 2022; 43:5006–5016
- Jain S, Goldstein DS. Cardiovascular dysautonomia in Parkinson disease: From pathophysiology to pathogenesis. Neurobiol Dis 2012; 46:572–580.
- Hotchkiss RS, et al. Sepsis and septic shock. Nat Rev Dis Primers 2016; 2:16045. https://doi.org/10.1038/nrdp.2016.45
- Raj SR, Stein CM, Saavedra PJ, Roden DM. Cardiovascular effects of noncardiovascular drugs. Circulation 2009; 120:1123–1132.
- Pop-Busui R. Cardiac autonomic neuropathy in diabetes: A clinical perspective. Diabetes Care 2010; 33:434–441.
- Lindman BR, et al.Blood pressure and arterial load after transcatheter aortic valve replacement for aortic stenosis. Circ Cardiovasc Imaging 2017; 10: e006308. https://doi.org/101161/CIRCIMAGING.116.006308
- Perlman GY, et al. Post-procedural hypertension following transcatheter aortic valve implantation: Incidence and clinical significance. JACC Cardiovasc Interv 2013; 6:472–478.
- (84). Siegel RJ, et al. The acute hemodynamic effects of MitraClip therapy. J Am Coll Cardiol 2011; 57:1658–1665.
- Adamo M, et al. Impact of transcatheter edge-to-edge mitral valve repair on guideline-directed medical therapy uptitration. JACC Cardiovasc Interv 2023; 16:896–905
- Clark DM, et al. Hemodynamic effects of an irregular sequence of ventricular cycle lengths during atrial fibrillation. J Am Coll Cardiol 1997; 30:1039–1045
- Swedberg K, et al. SHIFT Investigators. Ivabradine and outcomes in chronic heart failure (SHIFT): A randomised placebo-controlled study. Lancet 2010; 376:875–885. https://doi.org/10.1016/S0140-6736(10)61198-1
- Bagriy AE, Schukina EV, Samoilova OV, Pricolota OA, Malovichko SI, Pricolota AV, et al. Addition of ivabradine to beta-blocker improves exercise capacity in systolic heart failure patients in a prospective, open-label study. Adv Ther 2015; 32:108–119
- Kirch C, Grossmann M, Fischer S, Neumeister V, Kirch W. Effect of digoxin on circadian blood pressure values in patients with congestive heart failure. Eur J Clin Invest 2000; 30:285–289.
- Van Veldhuisen DJ, et al.; DECISION Investigators and Committees. Efficacy and safety of low-dose digoxin in patients with heart failure. Rationale and design of the DECISION trial. Eur J Heart Fail 2024; 26:2223–2230
- U et al. Digitoxin in Patients with Heart Failure and Reduced Ejection Fraction. DIGIT-HF Study. This article was published on August 29, 2025, at NEJM.org. DOI: 10.1056/NEJMoa2415471
- Meng L. Heterogeneous impact of hypotension on organ perfusion and outcomes: A narrative review. Br J Anaesth 2021; 127:845–861
- Cautela J, Tartiere JM, Cohen-Solal A, Bellemain-Appaix A, Theron A, Tibi T, et al. Management of low blood pressure in ambulatory heart failure with reduced ejection fraction patients. Eur J Heart Fail 2020; 22:1357–1
- McEvoy JW, McCarthy CP, Bruno RM, Brouwers S, Canavan MD, Ceconi C, et al. 2024 ESC Guidelines for the management of elevated blood pressure and hypertension. Eur Heart J 2024; 45:3912–4018.
- Crespo-Leiro MG, Metra M, Lund LH, Milicic D, Costanzo MR, Filippatos G, et al. Advanced heart failure: A position statement of the Heart Failure Association of the European Society of Cardiology. Eur J Heart Fail 2018; 20:1505–1535.
- Kim H, Oh J, Lee S, Ha J, Yoon M, Chun KH, et al. Clinical evidence of initiating a very low dose of sacubitril/ valsartan: A prospective observational analysis. Sci Rep 2021; 11:16335. https://doi.org/10.1038/s41598-021-95787-w
- Izumi K, Kohno T, Goda A, Takeuchi S, Shiraishi Y, Saji M, et al. Low blood pressure and guideline-directed medical therapy in patients with heart failure with reduced ejection fraction. Int J Cardiol 2023; 370:255–262
- Mueller C, McDonald K, de Boer RA, Maisel A, Cleland JGF, Kozhuharov N, et al.; Heart Failure Association of the European Society of Cardiology. Heart Failure Association of the European Society of Cardiology practical guidance on the use of natriuretic peptide concentrations. Eur J Heart Fail 2019; 21:715–731
- Mebazaa A, Yilmaz MB, Levy P, Ponikowski P, Peacock WF, Laribi S, et al. Recommendations on pre-hospital & early hospital management of acute heart failure: A consensus paper from the Heart Failure Association of the European Society of Cardiology, the European Society of Emergency Medicine and the Society of Academic Emergency Medicine. Eur J Heart Fail 2015; 17:544–558
- Bhagat AA, Greene SJ, Vaduganathan M, Fonarow GC, Butler J. Initiation, continuation, switching, and withdrawal of heart failure medical therapies during JACC Heart Fail 2019; 7:1–12
- SS et el. 2025 Concise Clinical Guidance: An ACC Expert Consensus Statement on the Evaluation and Management of Cardiogenic Shock. J Am Coll Cardiol. 2025; 85(16):1618–1641 Chioncel O, Davison B, Adamo M, Antohi LE, Arrigo M, Barros M, et al. Non-cardiac comorbidities and intensive up-titration of oral treatment in patients recently hospitalized for heart failure: Insights from the STRONG-HF trial. Eur J Heart Fail 2023; 25:1994–2006. https://doi.org/10.1002/ejhf.3039
- Pagnesi M, Vilamajo OAG, Meirino A, Dumont CA, Mebazaa A, Davison B, et al. Blood pressure and intensive treatment up-titration after acute heart failure hospitalization: Insights from the STRONG-HF trial. Eur J Heart Fail 2024; 26:638–651
- Rossignol P, Lainscak M, Crespo-Leiro MG, Laroche C, Piepoli MF, Filippatos G, et al.; Heart Failure Long-Term Registry Investigators Group. Unravelling the interplay between hyperkalaemia, renin-angiotensin-aldosterone inhibitor use and clinical outcomes. Data from 9222 chronic heart failure patients of the ESC-HFA-EORP Heart Failure Long-Term Registry. Eur J Heart Fail 2020; 22:1378–1389
- Ferreira JP, Rossello X, Pocock SJ, Rossignol P, Claggett BL, Rouleau JL, et al. Spironolactone dose in heart failure with preserved ejection fraction: Findings from TOPCAT. Eur J Heart Fail 2020; 22:1615–1624. Trevisan M, Fu EL, Xu Y, Savarese G, Dekker FW, Lund LH, et al. Stopping mineralocorticoid receptor antagonists after hyperkalaemia: Trial emulation in data from routine care. Eur J Heart Fail 2021; 23:1698–1707.
- Gorelik O, Almoznino-Sarafian D, Litvinov V, Alon I, Shteinshnaider M, Dotan E, et al. Seating-induced postural hypotension is common in older patients with decompensated heart failure and may be prevented by lower limb compression Gerontology 2009; 55:138–144.
- Gorelik O, Fishlev G, Almoznino-Sarafian D, Alon I, Weissgarten J, Shteinshnaider M, et al. Lower limb compression bandaging is effective in preventing signs and symptoms of seating-induced postural hypotension. 2004 ;102:177–183.
- Shibao C, Lipsitz LA, Biaggioni I; American Society of Hypertension Writing Evaluation and treatment of orthostatic hypotension. J Am Soc Hypertens 2013; 7:317–324







