PGS.TS. BS. HỒ ANH BÌNH*, TS.BS. HOÀNG VĂN**
TS.BS. ĐẶNG DUY PHƯƠNG***, ThS.BS. TRẦN QUỐC BẢO****
(*) Giám đốc Trung tâm Tim mạch, BV Trung ương Huế
(**) Phó Giám đốc Bệnh viện Tim Hà Nội
(***) Viện Tim TP Hồ Chí Minh
(****) Trung tâm Tim mạch, BV Trung ương Huế
TÓM TẮT
Bệnh nhân cao tuổi mắc nhồi máu cơ tim ST chênh lên (STEMI) kèm bệnh thận mạn là nhóm có nguy cơ cao đồng thời về huyết khối và xuất huyết khi điều trị chống huyết khối. Chúng tôi báo cáo trường hợp bệnh nhân nam 86 tuổi, bệnh thận mạn giai đoạn IV (eGFR 22 mL/phút/1,73 m²), nhập viện vì STEMI trước rộng. Sau khi đánh giá nguy cơ xuất huyết cao theo thang điểm PRECISE-DAPT, bệnh nhân được lựa chọn kháng kết tập tiểu cầu kép bằng aspirin và clopidogrel. Liệu pháp chống đông bằng enoxaparin được hiệu chỉnh liều 1 mg/kg mỗi 24 giờ và không sử dụng bolus tĩnh mạch do tuổi ≥75 và suy giảm chức năng thận. Can thiệp mạch vành qua da được thực hiện thành công, không ghi nhận biến cố xuất huyết nặng hoặc thiếu máu cục bộ tái phát trong thời gian nằm viện. Trường hợp này nhấn mạnh vai trò của cá thể hóa điều trị chống đông ở bệnh nhân rất cao tuổi kèm suy thận mạn nhằm tối ưu hóa cân bằng giữa hiệu quả chống huyết khối và an toàn xuất huyết.
Từ khóa: Nhồi máu cơ tim ST chênh lên; bệnh thận mạn; Heparin trọng lượng phân tử thấp; enoxaparin; cá thể hóa điều trị.
ĐẶT VẤN ĐỀ
Nhồi máu cơ tim là một cấp cứu nội khoa cần được đặt ra chẩn đoán và điều trị sớm, đây là một trong những nguyên nhân phổ biến gây tử vong ngay cả khi được sử dụng liệu pháp điều trị tối ưu và tái thông mạch. Về cơ chế bệnh sinh, nhồi máu cơ tim khởi phát từ tình trạng viêm mạch, rối loạn chức năng nội mô và sự vỡ hoặc ăn mòn mảng xơ vữa, dẫn đến hoạt hóa tiểu cầu và hệ thống đông máu. Huyết khối hình thành trên nền mảng xơ vữa tổn thương ban đầu chủ yếu gồm tiểu cầu, sau đó các con đường đông máu được kích hoạt mạnh mẽ thông qua yếu tố mô biểu hiện tại vùng tổn thương. Yếu tố mô gắn với yếu tố VIIa, hoạt hóa các yếu tố IX và X, hình thành phức hợp Xa-Va thúc đẩy chuyển prothrombin thành thrombin; thrombin tiếp tục khuếch đại dòng thác đông máu và chuyển fibrinogen thành fibrin, tạo nên huyết khối nội mạch. Trong những trường hợp nặng, quá trình này dẫn đến tắc nghẽn hoàn toàn động mạch vành và nhồi máu cơ tim ST chênh lên (STEMI). Chính vì cơ chế bệnh sinh này,bên cạnh các thuốc chống ngưng tập tiểu cầu, thuốc chống đông đóng vai trò nền tảng trong điều trị NMCT nhằm hạn chế sự lan rộng huyết khối và phòng ngừa biến cố thiếu máu cục bộ tái phát. Trong một nghiên cứu gồm 21.009 bệnh nhân NMCT, khoảng 20,9% có bệnh thận mạn (CKD), và nhóm này có tuổi trung bình cao hơn đáng kể so với nhóm không CKD với độ tuổi trung bình là 82 so với 70 tuổi(1). Đây là những đối tượng khi sử dụng thuốc chống đông sẽ làm tăng các biến cố xuất huyết có nguy cơ đe doạ tính mạng như xuất huyết tiêu hoá, xuất huyết não,…đặc biệt khi kết hợp chống đông với các thuốc kháng kết tập tiểu cầu kép(1). Do đó, việc lựa chọn và điều chỉnh liệu pháp chống đông ở bệnh nhân cao tuổi kèm suy thận trong NMCT luôn là một thách thức lớn, đòi hỏi chiến lược cá thể hóa nhằm cân bằng giữa hiệu quả chống huyết khối và an toàn xuất huyết. Chính vì vậy, bài viết này nhằm phân tích vai trò và lựa chọn thuốc và liều lượng chống đông dựa trên các bằng chứng nhằm cân bằng giữa lợi ích tim mạch lẫn nguy cơ xuất huyết.
GIỚI THIỆU CA BỆNH
Bệnh nhân nam 86 tuổi, tiền sử tăng huyết áp nhiều năm và bệnh thận mạn giai đoạn IV. Bệnh nhân nhập viện vì đau ngực dữ dội kéo dài 10 giờ. Khám ban đầu ghi nhận huyết áp 105/65 mmHg, mạch 92 lần/phút, ran ẩm nhẹ đáy phổi hai bên, xếp Killip II.
Điện tâm đồ cho thấy ST chênh lên rõ tại V1–V6 (hình 1). Troponin tăng. Creatinine 2,8 mg/dL. Hemoglobin 11,8 g/dL. Tiểu cầu 210 G/L, eGFR 22 ml/phút/1,73 m². Siêu âm tim ghi nhận EF 30%, giảm động nặng vùng trước – mỏm, không có huyết khối thất trái.
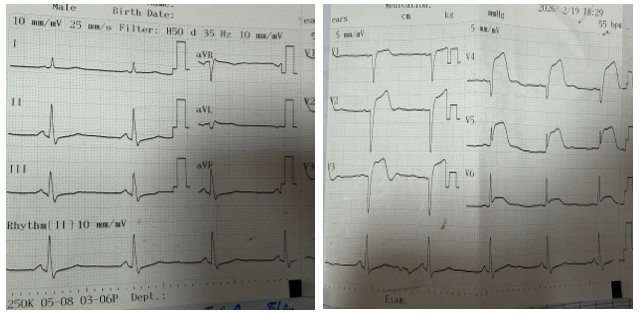
Hình 1. Điện tâm đồ lúc nhập viện: Nhịp xoang, tần số 55 lần/phút, ST chênh lên V1-V6 kèm sóng Q hoại tự từ V1-V4
Bệnh nhân được chẩn đoán STEMI trước rộng trên nền CKD giai đoạn IV và được chỉ định can thiệp mạch vành cấp cứu. Trước can thiệp, bệnh nhân được sử dụng aspirin 324 mg, clopidogrel 300 mg và Enoxaparin 1 mg/kg tiêm dưới da mỗi 24 giờ. Do bệnh nhân ≥75 tuổi, không sử dụng bolus tĩnh mạch. Với eGFR <30 ml/phút, liều được điều chỉnh còn 1 mg/kg mỗi 24 giờ theo khuyến cáo.
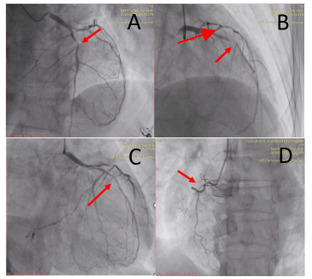
Hình 2. Kết quả chụp động mạch vành: hẹp 50–60% đoạn xa thân chung, hẹp khít 99% động mạch liên thất trước đoạn gần (LAD) (mũi tên hình A và B), hẹp 70–80% động mạch mũ (LCx) và tắc mạn tính động mạch vành phải (RCA) (mũi tên hình D).
Với kết quả trên, bệnh nhân có chỉ định can thiệp cấp cứu LAD, can thiệp trì hoãn RCA.
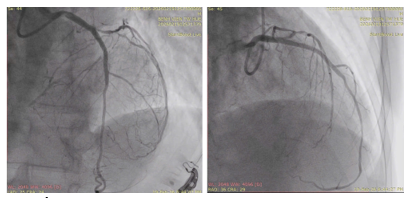
Hình 3: Kết quả sau can thiệp LAD với Stent tại vị trí đoạn thân chung và LAD đoạn đầu.
Sau khi can thiệp cấp cứu LAD, bệnh nhân được tiến hành can thiệp trì hoãn tiếp theo nhánh RCA dưới sự hướng dẫn của siêu âm nội mạch (IVUS) (hình 4 và hình 5). Bệnh nhân sau đó ổn định và ra viện sau một tuần điều trị.
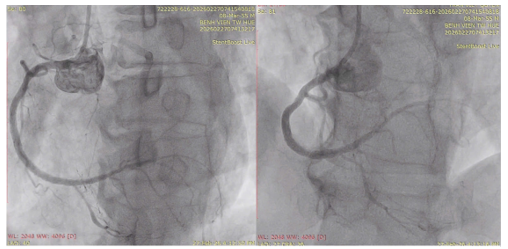
Hình 4. Kết quả sau can thiệp RCA với stent từ DI đến đoạn DIII.
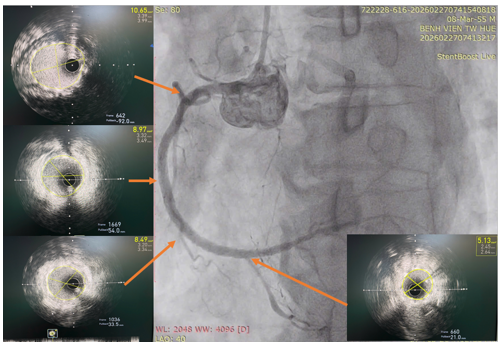
Hình 5. Hình ảnh IVUS sau can thiệp với kết quả Stent nở tốt, áp sát thành mạch với diện tích lòng mạch lần lượt là 5,13 mm2, 8,49mm2; 8.97 mm2; 10,65 mm2 từ đoạn xa đến đoạn gần.
BÀN LUẬN
Trong nhồi máu cơ tim ST chênh lên, huyết khối giàu fibrin trên nền mảng xơ vữa vỡ là cơ chế trung tâm gây tắc động mạch vành cấp. Vì vậy, chiến lược chống huyết khối toàn diện – kết hợp ức chế tiểu cầu và ức chế dòng thác đông máu – cần được triển khai sớm. Theo khuyến cáo hiện nay, liệu pháp kháng kết tập tiểu cầu kép với aspirin và một thuốc ức chế P2Y12 phải được dùng ngay khi chẩn đoán xác lập, với liều nạp tiêu chuẩn và không cần chỉnh liều theo chức năng thận. Tuy nhiên, lựa chọn thuốc P2Y12 cần cá thể hóa dựa trên cân bằng giữa nguy cơ thiếu máu cục bộ và xuất huyết. Ở bệnh nhân 86 tuổi của chúng tôi, với điểm PRECISE-DAPT 34 (nguy cơ xuất huyết cao), clopidogrel được ưu tiên thay vì các thuốc thế hệ mới nhằm tối ưu độ an toàn trong bối cảnh đa bệnh lý. Bên cạnh đó, chống đông sớm trong giai đoạn cấp, đặc biệt khi can thiệp mạch vành qua da (PCI), có vai trò quan trọng trong ức chế hình thành và lan rộng huyết khối giàu fibrin, giảm tắc vi tuần hoàn và góp phần bảo tồn tối đa vùng cơ tim còn khả năng cứu vãn (2).
Khác với kháng kết tập tiểu cầu, thuốc chống đông đòi hỏi cân nhắc chức năng thận và tuổi do liên quan trực tiếp đến dược động học. Cả heparin không phân đoạn (UFH) và heparin trọng lượng phân tử thấp (LMWH) đều hoạt động thông qua cơ chế gắn với antithrombin III, tăng cường khả năng bất hoạt yếu tố Xa và thrombin (IIa). So với UFH, LMWH có sinh khả dụng cao hơn, ít bị trung hòa bởi tiểu cầu hoạt hóa, có tỷ lệ hoạt tính anti-Xa/anti-IIa cao hơn và dược động học ổn định hơn, do đó có thể sử dụng liều cố định theo cân nặng mà không cần theo dõi aPTT thường quy(3).
Tuy nhiên, do enoxaparin được thải trừ chủ yếu qua thận, ở bệnh nhân có độ thanh thải creatinine giảm- bao gồm suy thận mạn và/hoặc người cao tuổi – hoạt tính anti-Xa có thể tích lũy nếu dùng liều chuẩn. Sau 2–3 ngày điều trị, nồng độ anti-Xa có thể vượt ngưỡng điều trị an toàn, làm gia tăng đáng kể nguy cơ xuất huyết nghiêm trọng(3). Vì vậy, trong nhóm bệnh nhân này, cần giảm liều theo mức lọc cầu thận hoặc cân nhắc UFH khi cần khả năng kiểm soát và đảo ngược nhanh, nhằm tối ưu hóa hiệu quả điều trị trong khi vẫn đảm bảo an toàn.
Nghiên cứu của Sanderink cho thấy dược động học anti-Xa không thay đổi đáng kể ở suy thận nhẹ–trung bình, nhưng ở suy thận nặng (ClCr <30 mL/phút), độ thanh thải anti-Xa giảm khoảng 39%, dẫn đến tích lũy thuốc theo thời gian. Sau nhiều liều lặp lại, AUC anti-Xa có thể tăng khoảng 65% vào ngày thứ 4, làm tăng nguy cơ chống đông quá mức và xuất huyết nặng nếu dùng liều chuẩn (4). Ở người cao tuổi, sự suy giảm mức lọc cầu thận sinh lý, giảm khối cơ và thay đổi dược động học càng làm giảm thanh thải enoxaparin. Nghiên cứu PROPHRE.75 (≥75 tuổi) ghi nhận hoạt tính anti-Xa tương quan nghịch với ClCr và cân nặng, cho thấy nguy cơ tích lũy chủ yếu liên quan đến suy giảm chức năng thận hơn là tuổi đơn thuần (5). Điều này cho thấy nguy cơ tích lũy thuốc ở người già không chỉ do tuổi đơn thuần mà chủ yếu do suy giảm chức năng thận đi kèm. Dữ liệu lâm sàng từ ExTRACT-TIMI 25 trên bệnh nhân STEMI điều trị tiêu sợi huyết cho thấy enoxaparin giảm tử vong hoặc tái nhồi máu so với UFH (9,9% so với 12,0%), nhưng làm tăng nhẹ xuất huyết nặng, đặc biệt xuất huyết nội sọ ở người cao tuổi nếu không chỉnh liều. Phân tích dưới nhóm cho thấy ở bệnh nhân ≥75 tuổi, chiến lược không dùng bolus tĩnh mạch và giảm liều còn 0,75 mg/kg mỗi 12 giờ giúp duy trì lợi ích chống huyết khối đồng thời hạn chế biến cố xuất huyết. Những dữ liệu này khẳng định enoxaparin vẫn hiệu quả ở người cao tuổi, nhưng bắt buộc phải hiệu chỉnh liều theo chức năng thận để tối ưu cân bằng lợi ích–nguy cơ (6).
Bệnh nhân trong ca này thuộc nhóm nguy cơ rất cao của STEMI: 86 tuổi, CKD giai đoạn IV, EF 30% và tổn thương thân chung – đa nhánh phức tạp. CKD tạo nên “nghịch lý” sinh lý bệnh khi vừa làm tăng trạng thái tiền huyết khối, vừa làm gia tăng nguy cơ xuất huyết. Do đó, lựa chọn chống đông cần cá thể hóa trên cơ sở cân bằng lợi ích – nguy cơ.
UFH có ưu điểm không tích lũy và đảo ngược nhanh, nhưng dược động học khó dự đoán và phụ thuộc aPTT, dễ dao động mức chống đông. Trong bối cảnh nguy cơ huyết khối rất cao, sự ổn định và tính dự đoán của chống đông là yếu tố then chốt.
Chúng tôi lựa chọn enoxaparin 1 mg/kg mỗi 24 giờ, phối hợp aspirin và clopidogrel, không dùng bolus tĩnh mạch để giảm nguy cơ xuất huyết. Quyết định này dựa trên sinh khả dụng cao, hoạt tính anti-Xa ưu thế và dược động học ổn định của enoxaparin, nhằm tối ưu hiệu quả chống huyết khối trong khi vẫn kiểm soát an toàn.
Bên cạnh lựa chọn phân tử thuốc, tính tương đương của enoxaparin biosimilar có ý nghĩa thực tiễn rõ rệt. Các thử nghiệm ngẫu nhiên, mù đôi, chéo trên người khỏe mạnh (liều 100 mg tiêm dưới da) cho thấy diện tích dưới đường cong và nồng độ đỉnh của hoạt tính kháng yếu tố Xa và kháng yếu tố IIa giữa biosimilar và biệt dược gốc hoàn toàn tương đương, đáp ứng tiêu chuẩn tương đương sinh học của Cơ quan Dược phẩm Châu Âu. Nghiên cứu lâm sàng so sánh trực tiếp cũng không ghi nhận khác biệt về biến cố huyết khối hoặc xuất huyết.
Do đó, khi đạt tiêu chuẩn nghiêm ngặt, biosimilar có hiệu quả và độ an toàn tương đương thuốc gốc, đồng thời giúp giảm chi phí và tăng khả năng tiếp cận điều trị. Tuy nhiên, việc hiệu chỉnh liều theo tuổi và chức năng thận vẫn là yếu tố then chốt để bảo đảm an toàn, bất kể sử dụng chế phẩm nào (7), (8).
KẾT LUẬN
Ở bệnh nhân nhồi máu cơ tim cao tuổi kèm suy thận mạn, chống đông vẫn là trụ cột điều trị nhưng phải cá thể hóa do nguy cơ xuất huyết tăng từ tích lũy hoạt tính kháng yếu tố Xa. Enoxaparin có thể sử dụng an toàn khi hiệu chỉnh theo tuổi và mức lọc cầu thận: tránh bolus tĩnh mạch ở bệnh nhân ≥75 tuổi, giảm liều hoặc kéo dài khoảng cách tiêm khi độ thanh thải creatinine <30 mL/phút, đồng thời theo dõi chặt chẽ cân bằng lợi ích – nguy cơ.
Các chế phẩm enoxaparin sinh học tương tự, khi đạt tiêu chuẩn tương đương sinh học, có thể thay thế biệt dược gốc, bảo đảm hiệu quả và an toàn, đồng thời giúp tối ưu chi phí điều trị trong thực hành tại Việt Nam.
TÀI LIỆU THAM KHẢO
- Freese Ballegaard EL, Lerkevang Grove E, Kamper AL, Feldt-Rasmussen B, Gislason G, Torp-Pedersen C, et al. Acute Myocardial Infarction and Chronic Kidney Disease: A Nationwide Cohort Study on Management and Outcomes from 2010 to 2022. Clin J Am Soc Nephrol. 2024;19(10):1263-74.
- Byrne RA, Rossello X, Coughlan JJ, Barbato E, Berry C, Chieffo A, et al. 2023 ESC Guidelines for the management of acute coronary syndromes. Eur Heart J. 2023;44(38):3720-826.
- Hirsh J, Warkentin TE, Raschke R, Granger C, Ohman EM, Dalen JE. Heparin and low-molecular-weight heparin: mechanisms of action, pharmacokinetics, dosing considerations, monitoring, efficacy, and safety. Chest. 1998;114(5 Suppl):489S-510S.
- Sanderink GJ, Guimart CG, Ozoux ML, Jariwala NU, Shukla UA, Boutouyrie BX. Pharmacokinetics and pharmacodynamics of the prophylactic dose of enoxaparin once daily over 4 days in patients with renal impairment. Thromb Res. 2002;105(3):225-31.
- Berges A, Laporte S, Epinat M, Zufferey P, Alamartine E, Tranchand B, et al. Anti-factor Xa activity of enoxaparin administered at prophylactic dosage to patients over 75 years old. Br J Clin Pharmacol. 2007;64(4):428-38.
- Fox KA, Dabbous OH, Goldberg RJ, Pieper KS, Eagle KA, Van de Werf F, et al. Prediction of risk of death and myocardial infarction in the six months after presentation with acute coronary syndrome: prospective multinational observational study (GRACE). BMJ. 2006;333(7578):1091.
- Martinez Gonzalez J, Monreal M, Ayani Almagia I, Llaudo Garin J, Ochoa Diaz de Monasterioguren L, Gutierro Aduriz I. Bioequivalence of a biosimilar enoxaparin sodium to Clexane((R)) after single 100 mg subcutaneous dose: results of a randomized, double-blind, crossover study in healthy volunteers. Drug Des Devel Ther. 2018;12:575-82.
- Dziri C, Ben Hmida W, Dougaz W, Khalfallah M, Samaali I, Jerraya H, et al. Biosimilar versus branded enoxaparin to prevent postoperative venous thromboembolism after surgery for digestive tract cancer: Randomized trial. PLoS One. 2023;18(11):e0293269.







