TS. PHẠM HỮU VĂN
(…)
Chương 3:
CÁC BỆNH ĐỒNG MẮC
Cần lưu ý các trường hợp trong phần này đề cập đến các thiết bị ICD được cấy để phòng ngừa tiên phát.
Các giả định và xem xét
■ Giả định rằng thiết bị “tốt nhất” cho từng bệnh nhân cụ thể sẽ được lựa chọn, trừ khi có chỉ định khác, ví dụ: thiết bị một buồng, hai buồng, CRT, hoặc đặt qua tĩnh mạch so với đặt toàn bộ dưới da.
Việc cấy ICD phòng ngừa tiên phát ở những bệnh nhân suy tim với EF giảm kèm theo các bệnh lý đi kèm nhìn chung cho thấy lợi ích giảm tỷ lệ tử vong do ICD giảm dần theo tuổi tác, [63,74] bệnh tiểu đường,[75,76] bệnh thận mãn tính (CKD) (bao gồm cả lọc máu), [77,78] các bệnh lý đi kèm, [62,79] phân loại chức năng NYHA cao hơn, [80] khoảng cách đi bộ 6 phút (6MWT) thấp hơn, [81] tình trạng suy nhược,[82] và tỷ lệ tử vong hàng năm do mọi nguyên nhân tăng lên.[83-86] Một khái niệm thống nhất cho thấy lợi ích của ICD giảm dần khi nguy cơ tử vong không phải đột tử tăng lên.[28,29,85,87-89]
Trong thử nghiệm SCD-HeFT, những bệnh nhân có tỷ lệ tử vong ước tính theo Mô hình Suy tim Seattle >20%/năm không nhận được lợi ích từ ICD. [90] Những phát hiện tương tự đã được chứng minh trong thử nghiệm MADIT II, với lợi ích giảm dần khi tỷ lệ tử vong do mọi nguyên nhân tăng lên theo ước tính của Mô hình Nguy cơ MADIT II. [84,91]
Một phân tích tổng hợp của 5 thử nghiệm ICD phòng ngừa tiên phát đã chứng minh lợi ích của ICD giảm ở những bệnh nhân có Chỉ số bệnh lý kèm theo Charlson ≥ 2 (HR: 0,59 so với 0,71). [62] Bệnh thận mạn tính và đái tháo đường nghiêm trọng dường như làm giảm lợi ích của ICD. Trong thử nghiệm MADIT II, những bệnh nhân có nitơ urê máu >50 mg/dL hoặc creatinine ≥ 2,5 mg/dL có nguy cơ rất cao và không có lợi ích từ ICD. [84] Tốc độ lọc cầu thận ước tính < 60 mL/min/1,73 m2 có liên quan đến việc giảm đáng kể lợi ích của ICD trong việc phòng ngừa đột tử (HR: 0,68 so với 0,22) và tử vong do mọi nguyên nhân (HR: 0,80 so với 0,49). [78] Bệnh nhân đang chạy thận nhân tạo có nguy cơ đột tử cao hơn. Thử nghiệm ICD2 (Cấy Máy khử rung tim ở bệnh nhân chạy thận nhân tạo) đã đánh giá ICD ở bệnh nhân (EF >35%) đang chạy thận nhân tạo. [92] Thử nghiệm không cho thấy sự giảm thiểu đột tử hoặc tử vong do mọi nguyên nhân khi sử dụng ICD.
Bệnh nhân tiểu đường được báo cáo có nguy cơ đột tử cao hơn. Mặc dù bệnh nhân tiểu đường có tỷ lệ tử vong cao hơn, nhưng tỷ lệ điều trị ICD thích hợp lại thấp hơn, cho thấy đột tử liên quan đến bệnh tiểu đường có thể không phải do rối loạn nhịp tim nhanh.[75] Trong một phân tích tổng hợp, không có lợi ích nào của ICD ở bệnh nhân mắc bệnh tiểu đường so với bệnh nhân không mắc bệnh tiểu đường (HR: 0,88 so với 0,56).[93] Rất có thể các bệnh đồng mắc khác làm tăng nguy cơ tử vong không đột tử, chẳng hạn như xơ gan, sa sút trí tuệ, ung thư và bệnh phổi, cũng có thể liên quan đến việc giảm lợi ích từ ICD phòng ngừa tiên phát.[94,95]
Tuổi tác ngày càng cao có liên quan đến sự gia tăng tử vong không đột tử nhiều hơn so với tử vong do đột tử, dẫn đến giảm tỷ lệ tử vong do đột tử. [96] ICD phòng ngừa tiên phát có liên quan đến lợi ích ICD giảm trong một phân tích tổng hợp, mặc dù bệnh nhân trên 75 tuổi vẫn được hưởng lợi.[74] Trong thử nghiệm DANISH, bệnh nhân trên 70 tuổi bị CM không do thiếu máu cục bộ không được hưởng lợi từ ICD. [63]
Một số mô hình nguy cơ đã được sử dụng để cố gắng xác định những bệnh nhân sẽ được hưởng lợi nhiều hơn từ ICD. Mô hình MADIT II đã xác định 5 biến số: tuổi >70, phân loại chức năng NYHA > II, nitơ urê máu >26 mg/dL, rung nhĩ và QRS >120 ms. [84] Các nhà nghiên cứu đã tìm thấy mối quan hệ hình chữ U, không có lợi ích với 0 biến số hoặc bệnh nhân có nguy cơ rất cao với nitơ urê máu > 50 mg/dL hoặc creatinine >2,5 mg/dL; Tuy nhiên, trong quá trình theo dõi 8 năm của thử nghiệm MADIT II, lợi ích tối đa đạt được ở những người có 0 biến số rủi ro và sự tương tác giữa các biến số rủi ro với lợi ích của ICD không đáng kể. [91]
Mô hình Suy tim Seattle được xây dựng để dự đoán tỷ lệ tử vong do mọi nguyên nhân chủ yếu ở những bệnh nhân suy tim với EF giảm. Bệnh nhân có nguy cơ thấp hơn có tỷ lệ tử vong do đột tử cao hơn, trong khi bệnh nhân có nguy cơ cao hơn có tỷ lệ tử vong do suy tim cao hơn. [97] Mô hình này đã được thử nghiệm trong thử nghiệm SCD-HeFT. [90] Lợi ích của ICD trong việc ngăn ngừa tử vong đột ngột và tử vong do mọi nguyên nhân bị suy giảm, vì ước tính tỷ lệ tử vong tăng lên mà không có lợi ích nào khi tỷ lệ tử vong hàng năm lớn hơn khoảng 20%.
Một phương pháp thay thế về nguy cơ cạnh tranh đã được sử dụng với Mô hình Nguy cơ Tỷ lệ Seattle, dự đoán tỷ lệ tử vong đột tử so với tử vong không đột tử. [88] Mười biến số được tìm thấy có liên quan độc lập với tỷ lệ tử vong đột tử tăng lên: tuổi trẻ hơn, phân loại chức năng NYHA thấp hơn, phân suất tống máu thấp hơn, chỉ số khối cơ thể cao hơn, giới tính nam, huyết áp tâm thu gần 140 mm Hg, không mắc bệnh tiểu đường, sử dụng digoxin và nồng độ natri và creatinine huyết thanh trong phạm vi bình thường. Các biến số mạnh nhất trong mô hình là tuổi, nồng độ creatinine, chỉ số khối cơ thể, bệnh tiểu đường và giới tính. Việc áp dụng mô hình này trong các thử nghiệm ICD quan sát và ngẫu nhiên đã chứng minh những bệnh nhân có tỷ lệ tử vong đột tử được dự đoán cao hơn sẽ nhận được lợi ích ICD lớn hơn trong việc ngăn ngừa tử vong đột tử và tử vong do mọi nguyên nhân. [28,29,85,87]
Các phương pháp khác đã cố gắng dự đoán sốc/điều trị ICD và/hoặc tử vong do mọi nguyên nhân. Các mô hình này không nhằm mục đích ước tính lợi ích của ICD mà chỉ so sánh tỷ lệ sốc ICD và tử vong do mọi nguyên nhân. [94,95,98]
Bảng 3.1 và Hình 15 mô tả các tình huống gồm các điều kiện hoặc bệnh lý đi kèm cụ thể có thể ảnh hưởng đến quyết định cấy ICD cho mục đích phòng ngừa tiên phát.
Bảng 3.1 Các tình trạng đặc biệt/Bệnh lý Đồng mắc ở bệnh nhân để phòng ngừa tiên phát (Đáp ứng chỉ định cấy ICD liên quan đến chẩn đoán Suy tim với LVEF ≤ 30% khi điều trị nội khoa theo hướng dẫn > 3 tháng)
| Chỉ định | Điểm sử dụng phù hợp (1-9) | |||
| Tuổi thọ | ||||
| 140 | ■ Tuổi thọ <1 năm do bệnh tim hoặc bệnh không liên quan đến tim R | R (1) | ||
| 141 | ■ Bệnh không liên quan đến tim với tuổi thọ 1-2 năm | M (4) | ||
| Người già | ||||
| Class NYHA chức năng | I | II | III | |
| 142 | ■ 80-84 tuổi | M (5) | M (6) | M (6) |
| 143 | ■ 85-89 tuổi | M (4) | M (5) | M (5) |
| 144 | ■ 90 tuổi | R (3) | M (4) | R (3) |
| Suy giảm nhận thức | Điểm sử dụng phù hợp (1-9) | |||
| 145 | ■ Không thể hiểu hoặc đưa ra sự đồng ý có hiểu biết
■ Người đại diện chăm sóc sức khỏe đồng ý với ICD |
M (4) |
||
| 146 | ■ Không thể hiểu hoặc đưa ra sự đồng ý có hiểu biết
■ Không thể xác định được người đại diện chăm sóc sức khỏe |
R (2) |
||
| Suy giảm tâm thần nghiêm trọng | ||||
| 147 | n Các bệnh tâm thần nghiêm trọng có thể trở nên trầm trọng hơn do cấy ghép thiết bị hoặc có thể cản trở việc theo dõi thường xuyên | R (1) | ||
| Bệnh thận mạn | ||||
| Class NYHA chức năng | I | II | III | |
| 148 | ■ Bệnh thận mạn đang chạy thận nhân tạo
■ Không có chỉ định đặt máy tạo nhịp hoặc CRT ■ Cấy ICD qua đường tĩnh mạch |
M (5) | M (5) | M (4) |
| 149 | ■ Bệnh thận mạn với CrCl <30 mL/min chưa chạy thận nhân tạo nhưng đủ điều kiện để chạy thận nhân tạo
■ Không có chỉ định đặt máy tạo nhịp hoặc CRT ■ Cấy ICD qua đường tĩnh mạch |
M (5) | M (5) | M (5) |
| Các bệnh lý đi kèm khác hoặc các trường hợp bệnh nhân đặc biệt | ||||
| Các nguy cơ đặc biệt về nhiễm trùng | Điểm sử dụng phù hợp | |||
| 150 | ■ Rối loạn sử dụng chất gây nghiện đường tĩnh mạch (đang diễn ra)
■ Cấy ICD qua đường tĩnh mạch |
R (2) | ||
| 151 | ■ Nhiễm trùng chưa được giải quyết liên quan đến nguy cơ gieo mầm theo đường máu
■ Cấy ICD qua đường tĩnh mạch |
R (2) | ||
| Tuân thu điều trị | Điểm sử dụng phù hợp | |||
| 152 | ■ Không tuân thủ liệu pháp điều trị và theo dõi | R (3) | ||
| HF class IV | Điểm sử dụng phù hợp | |||
| 153 | 153. n Đang trong danh sách chờ ghép tim (tình trạng ngoại trú) | A (7) | ||
| 154 | ■ Không đủ điều kiện để ghép tim, CRT hoặc VAD
■ Triệu chứng kháng thuốc khi điều trị bằng thuốc uống |
R (2) | ||
| 155 | ■ Bệnh nhân ngoại trú có LVAD | M (4) | ||
| 156 | ■ Không đủ điều kiện để ghép tim hoặc VAD
■ Không đáp ứng tiêu chí CRT ■ Dự kiến điều trị tăng co bóp cơ tim liên tục qua đường tĩnh mạch ngoại trú để giảm nhẹ triệu chứng |
R (2) | ||
A = Phù hợp; CrCl = độ thanh thải creatinine; CRT = liệu pháp tái đồng bộ tim; HF = suy tim; ICD = máy khử rung tim có thể cấy; IV = tiêm tĩnh mạch; LVAD = thiết bị hỗ trợ tâm thất trái; LVEF = phân suất tống máu tâm thất trái; M = Có thể phù hợp; NYHA = Hiệp hội Tim mạch New York; R = Hiếm khi phù hợp; RV = tâm thất phải; VAD = thiết bị hỗ trợ tâm thất.
Kết quả và Bàn luận
Lợi ích và nguy cơ của liệu pháp ICD có thể bị ảnh hưởng do các bệnh lý đồng mắc cụ thể, ngay cả khi có các chỉ định phòng ngừa tiên phát khác cho việc cấy ghép ICD. Các bệnh lý đồng mắc có thể làm giảm tuổi thọ hoặc tăng nguy cơ thủ thuật. Các nguy cơ và lợi ích tiềm tàng cần được đánh giá trên cơ sở từng cá nhân, và các lựa chọn nên được thảo luận giữa nhà cung cấp dịch vụ chăm sóc sức khỏe và bệnh nhân thông qua việc ra quyết định chung. Nhóm biên soạn đã tạo ra các kịch bản với các bệnh lý đồng mắc cụ thể có thể làm thay đổi quyết định liên quan đến việc cấy ghép ICD để phòng ngừa tiên phát khi ICD đáp ứng các tiêu chí cấy khác.
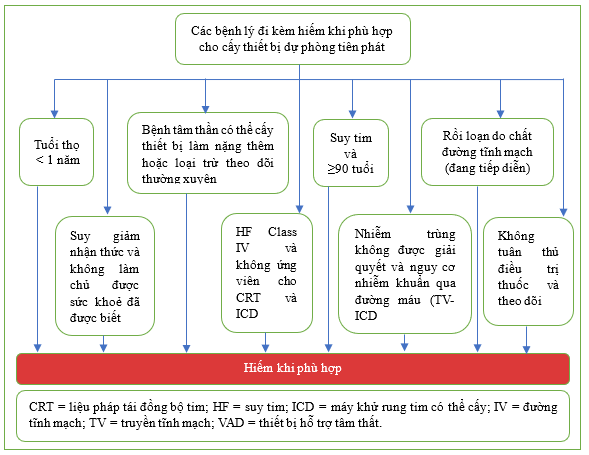
Hình 15. Tóm tắt Bảng 3.1, Các bệnh đồng mắc cần phòng ngừa tiên phát: Các chỉ định hiếm khi phù hợp
Các bệnh lý đi kèm được cho là khiến việc cấy ICD hiếm khi phù hợp gồm: tuổi thọ dự kiến <1 năm, tuổi > 90 tuổi với các triệu chứng thuộc phân loại chức năng NYHA I đến III, không có khả năng hiểu hoặc đưa ra sự đồng ý có hiểu biết khi không có người đại diện chăm sóc sức khỏe, bệnh tâm thần nghiêm trọng có thể trầm trọng hơn do cấy ghép thiết bị hoặc có thể cản trở việc theo dõi thường xuyên, lạm dụng ma túy đường tĩnh mạch đang diễn ra, nhiễm trùng chưa được giải quyết liên quan đến nguy cơ mầm bệnh theo đường máu với cấy máy khử rung tim qua đường tĩnh mạch (TV-ICD) đã được lên kế hoạch, không tuân thủ điều trị y tế và theo dõi, hoặc một số bệnh nhân thuộc phân loại chức năng NYHA IV, chẳng hạn như những người không đủ điều kiện cho các liệu pháp nâng cao (ví dụ: ghép tim, CRT hoặc thiết bị hỗ trợ tâm thất) (Bảng 3.1, Hình 15). Có nhiều mức độ và lý do không tuân thủ điều trị y tế và theo dõi, một số trong đó có thể được cải thiện thông qua giáo dục tốt hơn và tăng cường khả năng tiếp cận chăm sóc. Do đó, tình trạng của từng bệnh nhân cần được xem xét rõ ràng trước khi xác định điều kiện đủ điều kiện để điều trị bằng ICD.
Trong số các bệnh đồng mắc được xem xét, cấy ICD được coi là Có thể Phù hợp cho những bệnh nhân mắc bệnh không liên quan đến tim có tuổi thọ từ 1 đến 2 năm hoặc những người từ 80 đến 90 tuổi. Mặc dù SCD tăng theo tuổi, nhưng bệnh nhân cao tuổi lại ít được đại diện trong các thử nghiệm lâm sàng, và các bệnh đồng mắc ở người cao tuổi có thể làm giảm lợi ích của liệu pháp ICD. Có bằng chứng cho thấy bệnh nhân lớn tuổi được cấy ghép ICD có tỷ lệ sống sót thấp hơn so với bệnh nhân trẻ tuổi vì tỷ lệ tử vong liên quan đến các bệnh đồng mắc ở bệnh nhân cao tuổi cao hơn tỷ lệ tử vong liên quan đến rối loạn nhịp thất. [74] Ngoài ra, đặc điểm của bệnh nhân được cấy ghép ICD trong thực hành lâm sàng có thể khác với những bệnh nhân tham gia các thử nghiệm lâm sàng ngẫu nhiên. Ví dụ, trong các thử nghiệm ICD phòng ngừa tiên phát, tuổi trung bình chỉ từ 60 đến 67 tuổi. [50,54,55,99] Ngược lại, dữ liệu thực tế cho thấy một tỷ lệ đáng kể bệnh nhân lớn tuổi hơn được điều trị bằng ICD. Trong Sổ đăng ký về những tiến bộ trong liệu pháp ICD, gồm 4.566 bệnh nhân đã trải qua thủ thuật cấy ICD lần đầu tiên, 12% bệnh nhân từ 80 tuổi trở lên (75% trong số đó được cấy ghép thiết bị để phòng ngừa tiên phát), tương tự như NCDR (Đăng ký Dữ liệu Tim mạch Quốc gia: National Cardiovascular Data Registry) (N = 74.476 bệnh nhân) vào thời điểm đó, trong đó 12,4% bệnh nhân được cấy ghép ICD từ 80 tuổi trở lên.[100] Như dự đoán, nguyên nhân tử vong có nhiều khả năng không liên quan đến tim mạch ở bệnh nhân lớn tuổi hơn so với bệnh nhân trẻ tuổi. Trong một báo cáo tiếp theo về dữ liệu NCDR, 16,8% bệnh nhân được cấy ghép ICD từ 80 tuổi trở lên và 75% số ICD được cấy ở tất cả bệnh nhân là để phòng ngừa tiên phát. [101]
Các nghiên cứu trước đây đã đặt câu hỏi về lợi ích của việc cấy ICD ở bệnh nhân mắc bệnh thận mạn tính (CKD), đặc biệt là ở những bệnh nhân đang chạy thận nhân tạo. [92,102,103] Việc cấy ICD để phòng ngừa tiên phát được coi là Có thể Phù hợp cho bệnh nhân CKD đang chạy thận nhân tạo hoặc CKD có độ thanh thải creatinine < 30 mL/min và chưa chạy thận nhân tạo (nhưng là ứng cử viên cho chạy thận nhân tạo). CKD và các bệnh đồng mắc liên quan làm giảm khả năng sống sót lâu dài của bệnh nhân và hạn chế tác động có lợi của liệu pháp ICD. Bệnh nhân CKD đang chạy thận nhân tạo cũng có nguy cơ biến chứng cao hơn liên quan đến việc cấy ICD, gồm tăng nguy cơ chảy máu và nhiễm trùng. [104,105] Do nguy cơ nhiễm trùng nội mạch tăng cao ở bệnh nhân chạy thận nhân tạo mãn tính, ICD dưới da hiện nay thường được coi là một lựa chọn thay thế cho hệ thống TVICD (ICD qua đường tĩnh mạch). [106]
Cấy ICD có thể đóng vai trò như một cầu nối đến việc ghép tạng bằng cách ngăn ngừa SCD trong môi trường ngoại trú. Đối với bệnh nhân suy tim độ IV theo phân loại NYHA đang trong danh sách chờ ghép tim (ngoại trú), cấy ghép ICD được coi là Phù hợp, trong khi cấy ICD cho bệnh nhân ngoại trú độ IV theo phân loại NYHA có thiết bị hỗ trợ tâm thất trái (LVAD) được coi là Có thể Phù hợp (Bảng 3.1, Hình 15). Trong trường hợp suy tim độ IV theo phân loại NYHA, nếu bệnh nhân không được coi là ứng cử viên cho ghép tim, liệu pháp tái đồng bộ tim (CRT) hoặc thiết bị hỗ trợ tâm thất, liệu pháp ICD được đánh giá là Hiếm khi Phù hợp khi có các triệu chứng kháng thuốc khi điều trị bằng thuốc uống hoặc khi có kế hoạch điều trị tăng co bóp cơ tim liên tục ngoại trú để giảm nhẹ triệu chứng (Bảng 3.1, Hình 15). Điều này phù hợp với tỷ lệ sống sót thấp dự kiến trong 1 năm đối với bệnh nhân suy tim độ IV theo phân loại NYHA kháng thuốc, không phải là ứng cử viên cho ghép tim hoặc CRT.
Lợi ích về tỷ lệ sống sót và các biến chứng liên quan đến cấy ICD phòng ngừa tiên phát bị ảnh hưởng do tuổi tác, phân loại suy tim, khả năng tham gia các can thiệp khác và các bệnh lý đồng mắc từ trước như bệnh thận mãn tính. Do đó, cần thảo luận cởi mở với những người có ý định cấy ghép ICD về những ảnh hưởng bất lợi tiềm tàng của các bệnh lý đi kèm trước khi cấy ghép thiết bị để tăng cường quá trình ra quyết định sáng suốt.
Chương 4:
ICD THAY THẾ MÁY THEO CHỈ SỐ THAY THẾ TỰ NGUYỆN
(ELECTIVE REPLACEMENT INDICATOR )
Các giả định và xem xét
■ Giả định rằng việc ra quyết định chung đã diễn ra, đặc biệt nếu không có rối loạn nhịp thất nào có ý nghĩa lâm sàng kể từ khi cấy, hiện tại với tiên lượng sống sót dưới 1 năm.
Có rất ít dữ liệu về việc quản lý bệnh nhân đến khám để thay máy tạo nhịp tự chọn trong trường hợp các thiết bị ICD hoặc CRT đã được cấy trước đó đang sắp hết hạn sử dụng. Trong suốt cuộc đời của bệnh nhân, tình trạng lâm sàng sẽ thay đổi và các tình trạng bệnh lý trước đây cần cấy ghép ICD hoặc CRT có thể thay đổi. Tình trạng lâm sàng và các bệnh kèm theo của từng bệnh nhân có thể thay đổi, do đó cần xem xét không chỉ việc thay thế máy tạo nhịp mà còn có thể thay đổi loại thiết bị (ví dụ: từ ICD sang PM). Hơn nữa, bằng chứng lâm sàng về việc đặt CIED có thể thay đổi theo thời gian, với các nghiên cứu đang diễn ra và sự sẵn có của dữ liệu thử nghiệm mới. Sau khi bệnh nhân đã được điều trị ICD thích hợp cho rối loạn nhịp thất, họ sau đó được coi là “phòng ngừa thứ phát” tại thời điểm thay thế máy tạo nhịp trong NCDR. Hiện tại, có rất ít dữ liệu liên quan đến việc thay máy ở những bệnh nhân đã được cấy ICD để phòng ngừa tiên phát nhưng chưa gặp phải các rối loạn nhịp tim có ý nghĩa lâm sàng kể từ khi cấy ghép ban đầu, và việc thay thế máy thường vẫn được thực hiện bất kể LVEF khi theo dõi; tuy nhiên, quyết định thực hiện thay thế máy hoặc xem xét “nâng cấp” thiết bị không phải là không có rủi ro. Như đã lưu ý trước đó, tỷ lệ biến chứng cao là 15,3% được quan sát thấy trong Sổ đăng ký REPLACE ở những bệnh nhân trải qua việc bổ sung dây dẫn qua tĩnh mạch theo kế hoạch để thay thế hoặc nâng cấp lên thiết bị có khả năng thực hiện các liệu pháp bổ sung. [57] Do đó, các chỉ định nhằm mục đích đánh giá sự phù hợp cho nhiều tình huống lâm sàng khác nhau liên quan đến việc “thay thế thiết bị CIED hiện có” hoặc “hạ cấp” ICD hoặc CRT-ICD xuống PM.
Các kịch bản xem xét chỉ định ban đầu cho thiết bị, tuổi thọ, rối loạn nhịp thất tạm thời hoặc sự phục hồi LVEF được mô tả trong Bảng 4.1 đến 4.4. Việc thay CRT-ICD bằng CRT PM khi LVEF đã được cải thiện kể từ khi cấy ghép thiết bị ban đầu cho các chỉ định phòng ngừa tiên phát là một kịch bản thường gặp. Dữ liệu hạn chế cho thấy nguy cơ rối loạn nhịp tim giảm ở những bệnh nhân có LVEF được cải thiện, mặc dù trong thử nghiệm MADIT-CRT (Thử nghiệm cấy ghép máy khử rung tim tự động đa trung tâm – Liệu pháp tái đồng bộ tim), nguy cơ rối loạn nhịp nhanh thất đáng kể vẫn còn ngay cả ở những bệnh nhân có chức năng LV được cải thiện hoặc phân loại chức năng NYHA vượt quá khuyến nghị hướng dẫn cấy ICD phòng ngừa tiên phát, khiến các tác giả kết luận việc bảo vệ bằng máy khử rung tim vẫn có thể biện minh được. [107] Một mức độ nguy cơ rối loạn nhịp tim nhất định cũng vẫn còn ở nhóm bệnh nhân đáp ứng CRT siêu tốt. [108]
Bảng 4.1. Phòng ngừa tiên phát bằng ICD khi cấy khởi đầu
| Chỉ định | Điểm sử dụng phù hợp (1-9) | ||
| Không có rối loạn nhịp thất nào có ý nghĩa lâm sàng được ghi nhận trên máy ICD kể từ khi cấy. | |||
| 157 | ■ Bệnh nhân được ICD điều trị dự phòng tiên phát khi LVEF là ≤35%
■ LVEF hiện không thay đổi |
A (8) | |
| 158 | n Bệnh nhân được ICD điều trị dự phòng tiên phát khi LVEF là ≤35%
■ LVEF hiện tại là 36%-49% |
M (6) | |
| 159 | ■ Bệnh nhân được ICD điều trị dự phòng tiên phát khi LVEF là ≤ 35%
■ LVEF hiện tại là ≥ 50% (đã bình thường hóa) |
M (4) | |
| Không có rối loạn nhịp thất có ý nghĩa lâm sàng trên ICD kể từ khi cấy (Hiện tại có Tiên lượng <1 năm) | Thay ICD | Thay PM* | |
| 160 | ■ Bệnh nhân được điều trị ICD dự phòng tiên phát
■ Phụ thuộc vào máy tạo nhịp tim |
M (4) | A (8) |
| 161 | ■ Bệnh nhân được điều trị ICD dự phòng tiên phát
■ Không có chỉ định tạo nhịp tim |
R (2) | R (2) |
| Loạn nhịp thất có ý nghĩa lâm sàng trên ICD kể từ khi cấy ghép | Điểm sử dụng phù hợp | ||
| 162 | ■ Bệnh nhân được điều trị ICD dự phòng tiên phát khi LVEF là ≤35%
■ LVEF hiện không thay đổi |
A (9) | |
| 163 | ■ Bệnh nhân được điều trị ICD dự phòng tiên phát khi LVEF là ≤35%
■ LVEF hiện ở mức 36%-49% |
A (8) | |
| 164 | ■ Bệnh nhân được điều trị ICD dự phòng tiên phát khi LVEF là ≤35%
■ LVEF hiện ở mức ≥ 50% (bình thường hóa) |
A (7) | |
| 165 | ■ Bệnh nhân được điều trị ICD dự phòng tiên phát
■ Hiện có tiên lượng <1 năm |
M (5) | |
Bảng 4.2. Phòng ngừa thứ phát bằng ICD khi cấy khởi đầu
| Chỉ định
|
Điểm sử dụng phù hợp (1-9) | |
| 166 | ■ Bệnh nhân được cấy ICD phòng ngừa thứ phát
■ Không có rối loạn nhịp thất kể từ lần cấy ghép ban đầu |
A (8) |
| 167 | ■ Bệnh nhân được cấy ICD phòng ngừa thứ phát
■ Có rối loạn nhịp nhanh thất trong vùng theo dõi kéo dài >30 giây, nhưng không có rối loạn nhịp thất được điều trị kể từ lần cấy ban đầu |
A (8) |
| 169 | ■ Bệnh nhân được cấy ICD phòng ngừa thứ phát
■ Có rối loạn nhịp thất được điều trị bằng ICD kể từ khi cấy ghép |
A (9) |
A = Phù hợp; ICD = máy khử rung tim có thể cấy.
Bảng 4.3. Phòng ngừa tiên phát khi cấy khởi đầu: Thay thế CRT-ICD do ERI
| Chỉ định | Điểm sử dụng phù hợp (1-9) | ||
| Thay thế bằng
CRT-ICD |
Thay thế bằng Máy tạo nhịp – CRT | ||
| 169 | ■ Bệnh nhân được cấy CRT-ICD khi LVEF là ≤35%
■ LVEF hiện không thay đổi (mặc dù tình trạng lâm sàng được cải thiện) |
A(9) |
R(3) |
| 170 | ■ Bệnh nhân được cấy CRT-ICD khi LVEF là ≤35%
■ LVEF hiện ở mức 36%-49% |
A(8) |
M(6) |
| 171 | ■ Bệnh nhân được cấy CRT-ICD khi LVEF là ≤35%
■ LVEF hiện ở mức ≥ 50% (bình thường) |
A(7) |
M(8) |
A = Phù hợp; CRT = liệu pháp tái đồng bộ tim; ERI (elective replacement indicator) = chỉ số thay thế tự chọn; ICD = máy khử rung tim có thể cấy; LVEF = phân suất tống máu thất trái; M = Có thể phù hợp; R = Hiếm khi phù hợp.
(Vui lòng xem tiếp trong kỳ sau)
TÀI LIỆU THAM KHẢO
- Elming MB, Nielsen JC, Haarbo J, et al. Age and outcomes of primary prevention implantable cardioverter-defibrillators in patients with nonischemic systolic heart failure. Circulation. 2017;136:1772–1780.
- Køber L, Thune JJ, Nielsen JC, et al. Defibrillator implantation in patients with nonischemic systolic heart failure. N Engl J Med. 2016;375:1221–1230.
- McMurray JJ, Packer M, Desai AS, et al. Angiotensin-neprilysin inhibition versus enalapril in heart failure. N Engl J Med. 2014;371:993–1004.
- Halliday BP, Gulati A, Ali A, et al. Association between midwall late gadolinium enhancement and sudden cardiac death in patients with dilated cardiomyopathy and mild and moderate left ventricular systolic dysfunction. Circulation. 2017;135:2106–2115.
- Maceira AM, Mohiaddin RH. Cardiovascular magnetic resonance in systemic hypertension. J Cardiovasc Magn Reson. 2012;14:28.
- Kuruvilla S, Adenaw N, Katwal AB, et al. Late gadolinium enhancement on cardiac magnetic resonance predicts adverse cardiovascular outcomes in nonischemic cardiomyopathy: a systematic review and meta-analysis. Circ Cardiovasc Imaging. 2014;7:250– 258.
- Elming MB, Hammer-Hansen S, Voges I, et al. Myocardial fibrosis and the effect of primary prophylactic defibrillator implantation in patients with nonischemic systolic heart failure—DANISH-MRI. Am Heart J. 2020;221:165–176.
- Bänsch D, Steffgen F, Grönefeld G, et al. The 1þ1 trial: a prospective trial of a dual- versus a singlechamber implantable defibrillator in patients with slow ventricular tachycardias. Circulation. 2004;110: 1022–1029.
- Kadish A, Dyer A, Daubert JP, et al. Prophylactic defibrillator implantation in patients with nonischemic dilated cardiomyopathy. N Engl J Med. 2004;350:2151– 2158.
- Caforio AL, Pankuweit S, Arbustini E, et al. Current state of knowledge on aetiology, diagnosis, management, and therapy of myocarditis: a position statement of the European Society of Cardiology Working Group on Myocardial and Pericardial Diseases. Eur Heart J. 2013;34:2636–2648, 2648a-2648d.
- Towbin JA, McKenna WJ, Abrams DJ, et al. 2019 HRS expert consensus statement on evaluation, risk stratification, and management of arrhythmogenic cardiomyopathy. Heart Rhythm. 2019;16:e301–e372.
- Hess PL, Al-Khatib SM, Han JY, et al. Survival benefit of the primary prevention implantable cardioverter-defibrillator among older patients: does age matter? An analysis of pooled data from 5 clinical trials. Circ Cardiovasc Qual Outcomes. 2015;8:179–186.
- Junttila MJ, Pelli A, Kenttä TV, et al. Appropriate shocks and mortality in patients with versus without JACC VOL. – , NO. – , 2025 Russo et al – , 2025: – – – AUC for ICD, CRT, and Pacing
- Sharma A, Al-Khatib SM, Ezekowitz JA, et al. Implantable cardioverter-defibrillators in heart failure patients with reduced ejection fraction and diabetes. Eur J Heart Fail. 2018;20:1031–1038.
- Bansal N, Szpiro A, Reynolds K, et al. Long-term outcomes associated with implantable cardioverter defibrillator in adults with chronic kidney disease. JAMA Intern Med. 2018;178:390–398.
- Pun PH, Al-Khatib SM, Han JY, et al. Implantable cardioverter-defibrillators for primary prevention of sudden cardiac death in CKD: a meta-analysis of patient-level data from 3 randomized trials. Am J Kidney Dis. 2014;64:32–39.
- Lee DS, Tu JV, Austin PC, et al. Effect of cardiac and noncardiac conditions on survival after defibrillator implantation. J Am Coll Cardiol. 2007;49:2408–2415.
- Barra S, Providencia R, Agarwal S. Do we need further clinical-effectiveness estimates to support the use of primary prevention implantable cardioverterdefibrillators in New York Heart Association class III patients? Int J Cardiol. 2016;203:184–186.
- Fishbein DP, Hellkamp AS, Mark DB, et al. Use of the 6-min walk distance to identify variations in treatment benefits from implantable cardioverterdefibrillator and amiodarone: results from the SCDHeFT (sudden cardiac death in heart failure trial). J Am Coll Cardiol. 2014;63:2560–2568.
- Bibas L, Levi M, Touchette J, et al. Implications of frailty in elderly patients with electrophysiological conditions. JACC Clin Electrophysiol. 2016;2:288–294.
- Goldenberg I, Gillespie J, Moss AJ, et al. Long-term benefit of primary prevention with an implantable cardioverter-defibrillator: an extended 8-year followup study of the multicenter automatic defibrillator implantation trial II. Circulation. 2010;122:1265–1271.
- Goldenberg I, Vyas AK, Hall WJ, et al. Risk stratification for primary implantation of a cardioverterdefibrillator in patients with ischemic left ventricular dysfunction. J Am Coll Cardiol. 2008;51:288–296.
- Levy WC, Hellkamp AS, Mark DB, et al. Improving the use of primary prevention implantable cardioverter-defibrillators therapy with validated patient-centric risk estimates. JACC Clin Electrophysiol. 2018;4:1089–1102.
- Zabel M, Willems R, Lubinski A, et al. Clinical effectiveness of primary prevention implantable cardioverter-defibrillators: results of the EU-CERT-ICD controlled multicentre cohort study. Eur Heart Jl. 2020;41:3437–3447.
- Levy WC, Li Y, Reed SD, et al. Does the implantable cardioverter-defibrillator benefit vary with the estimated proportional risk of sudden death in heart failure patients? JACC Clin Electrophysiol. 2017;3:291–298.
- Shadman R, Poole JE, Dardas TF, et al. A novel method to predict the proportional risk of sudden cardiac death in heart failure: Derivation of the Seattle proportional risk model. Heart Rhythm. 2015;12:2069– 2077.
- Levy WC, Poole JE, Hellkamp AS, et al. Benefits of ICD therapy: connecting treatment decisions to individualized SCD risk estimates within SCD-HeFT—Seattle Proportional Risk Model (abstract). J Inter Card Electrophysiology. 2015;42:208.
- Levy WC, Lee KL, Hellkamp AS, et al. Maximizing survival benefit with primary prevention implantable cardioverter-defibrillator therapy in a heart failure population. Circulation. 2009;120:835–842.
- Barsheshet A, Moss AJ, Huang DT, et al. Applicability of a risk score for prediction of the long-term (8- year) benefit of the implantable cardioverter-defibrillator. J Am Coll Cardiol. 2012;59:2075–2079.
- Jukema JW, Timal RJ, Rotmans JI, et al. Prophylactic use of implantable cardioverter-defibrillators in the prevention of sudden cardiac death in dialysis patients. Circulation. 2019;139:2628–2638.
- Gutman SJ, Costello BT, Papapostolou S, et al. Reduction in mortality from implantable cardioverterdefibrillators in non-ischaemic cardiomyopathy patients is dependent on the presence of left ventricular scar. Eur Heart J. 2019;40:542–550.
- Bilchick KC, Stukenborg GJ, Kamath S, et al. Prediction of mortality in clinical practice for medicare patients undergoing defibrillator implantation for primary prevention of sudden cardiac death. J Am Coll Cardiol. 2012;60:1647–1655.
- Lee DS, Hardy J, Yee R, et al. Clinical risk stratification for primary prevention implantable cardioverter defibrillators. Circ Heart Fail. 2015;8:927–937.
- Krahn AD, Connolly SJ, Roberts RS, et al. Diminishing proportional risk of sudden death with advancing age: implications for prevention of sudden death. Am Heart J. 2004;147:837–840.
- Mozaffarian D, Anker SD, Anand I, et al. Prediction of mode of death in heart failure: the Seattle heart failure model. Circulation. 2007;116:392–398.
- Alba AC, Walter SD, Guyatt GH, et al. Predicting survival in patients with heart failure with an implantable cardioverter defibrillator: The Heart Failure Meta-Score. J Card Fail. 2018;24:735–745.
- Moss AJ, Hall WJ, Cannom DS, et al. Improved survival with an implanted defibrillator in patients with coronary disease at high risk for ventricular arrhythmia. Multicenter Automatic Defibrillator Implantation Trial Investigators. N Engl J Med. 1996;335:1933–1940.
- Epstein AE, Kay GN, Plumb VJ, et al. Implantable cardioverter-defibrillator prescription in the elderly. Heart Rhythm. 2009;6:1136–1143.
- American College of Cardiology Foundation. NCDR ICD Registry Institutional Outcomes Report 2020Q4. 2020.
- Cuculich PS, Sánchez JM, Kerzner R, et al. Poor prognosis for patients with chronic kidney disease despite ICD therapy for the primary prevention of sudden death. Pacing Clin Electrophysiol. 2007;30: 207–213.
- Hager CS, Jain S, Blackwell J, et al. Effect of renal function on survival after implantable cardioverter defibrillator placement. Am J Cardiol. 2010;106:1297– 1300.
- Ayoub K, Fry E, Marji M, et al. Implantable cardioverter-defibrillators with end stage renal disease: nationwide inpatient sample database results. Pacing Clin Electrophysiol. 2022;45:124–131.
- Tompkins C, McLean R, Cheng A, et al. End-stage renal disease predicts complications in pacemaker and ICD implants. J Cardiovasc Electrophysiol. 2011;22: 1099–1104.
- El-Chami MF, Burke MC, Herre JM, et al. Outcomes of subcutaneous implantable cardioverterdefibrillator in dialysis patients: results from the SICD post-approval study. Heart Rhythm. 2020;17: 1566–1574.
- Sherazi S, Shah F, Kutyifa V, et al. Risk of ventricular tachyarrhythmic events in patients who improved beyond guidelines for a defibrillator in MADIT-CRT. JACC Clin Electrophysiol. 2019;5:1172– 1181.
- Manne M, Rickard J, Varma N, et al. Normalization of left ventricular ejection fraction after cardiac resynchronization therapy also normalizes survival. Pacing Clin Electrophysiol. 2013;36:970–977.
- Pillarisetti J, Gopinathannair R, Haney MJ, et al. Risk of ventricular tachyarrhythmias following improvement of left ventricular ejection fraction in patients with implantable cardiac defibrillators implanted for primary prevention of sudden cardiac death. J Interv Card Electrophysiol. 2017;48:283–289.
- Schliamser JE, Kadish AH, Subacius H, et al. Significance of follow-up left ventricular ejection fraction measurements in the defibrillators in non-ischemic cardiomyopathy treatment evaluation trial (DEFINITE). Heart Rhythm. 2013;10:838–846.
- Defaye P, Boveda S, Klug D, et al. Dual- vs. singlechamber defibrillators for primary prevention of sudden cardiac death: long-term follow-up of the défibrillateur automatique implantable-prévention primaire registry. Europace. 2017;19:1478–1484.
- Deisenhofer I, Kolb C, Ndrepepa G, et al. Do current dual chamber cardioverter defibrillators have advantages over conventional single chamber cardioverter defibrillators in reducing inappropriate therapies? A randomized, prospective study. J Cardiovasc Electrophysiol. 2001;12:134–142.
- Kühlkamp V, Dörnberger V, Mewis C, et al. Clinical experience with the new detection algorithms for atrial fibrillation of a defibrillator with dual chamber sensing and pacing. J Cardiovasc Electrophysiol. 1999;10:905– 915. 114. Lawrence D, Von Bergen N, Law IH, et al. Inappropriate ICD discharges in single-chamber versus dual-chamber devices in the pediatric and young adult population. J Cardiovasc Electrophysiol. 2009;20:287– 290.
- Theuns DA, Klootwijk A, Goedhart DM, et al. Prevention of inappropriate therapy in implantable cardioverter-defibrillators: results of a prospective, randomized study of tachyarrhythmia detection algorithms. J Am Coll of Cardiol. 2004;44(12):2362–2367.
- Ruwald AC, Sood N, Ruwald MH, et al. Frequency of inappropriate therapy in patients implanted with dual- versus single-chamber ICD devices in the ICD arm of MADIT-CRT. J Cardiovasc Electrophysiol. 2013;24: 672–679.
- Briongos-Figuero S, Sánchez A, Pérez ML, et al. Single-brand dual-chamber discriminators to prevent inappropriate shocks in patients implanted with prophylactic implantable cardioverter defibrillators: a propensity-weighted comparison of single- and dualchamber devices. J Interv Card Electrophysiol. 2019;54:267–275.
- Friedman PA, McClelland RL, Bamlet WR, et al. Dual-chamber versus single-chamber detection enhancements for implantable defibrillator rhythm Russo et al JACC VOL., NO., 2025 AUC for ICD, CRT, and Pacing – , 2025: 62 diagnosis: the detect supraventricular tachycardia study. Circulation. 2006;113:2871–2879
- Matlock DD, Peterson PN, Wang Y, et al. Variation in use of dual-chamber implantable cardioverterdefibrillators: results from the national cardiovascular data registry. Arch Intern Med. 2012;172:634–641. discussion 641.
- Borne RT, Varosy P, Lan Z, et al. Trends in use of single- vs dual-chamber implantable cardioverterdefibrillators among patients without a pacing indication, 2010-2018. JAMA Network Open. 2022;5. e223429-e223429.







