PGS.TS. Châu Ngọc Hoa*
* Giảng viên Đại hoc Y Dược TP.HCM
Tần suất thiếu máu ở bệnh nhân suy tim mạn (STM) khá cao và là một mục tiêu điều trị mới của dân số này. Bài tổng quan này tóm tắt những hiểu biết hiện nay về tần suất, nguyên nhân, các tương quan sinh lý bệnh của thiếu máu trong STM và những yếu tố nguy cơ cũng như lợi ích của việc điều trị thiếu máu bằng các thưốc erythropoietin trong STM.
Tần suất thiếu máu trong STM
Tần suất của thiếu máu ở bệnh nhân STM có phân suất tống máu thấp thay đổi khá rộng từ 4-61% (trung bình 18%).1-15 Sự biến thiên này một phần do việc sử dụng không đồng nhất các định nghĩa về thiếu máu của các báo cáo. Định nghĩa thiếu máu của Tổ chức Y tế thế giới tính đến sự khác biệt về giới trong sự phân bổ các giá trị hemoglobin (nồng độ hemoglobin < 13 g/dL ở nam và < 12 g/dL ở nữ),16 trái lại Hiệp hội Thận Quốc gia định nghĩa thiếu máu khi hemoglobin £ 12 g/dL ở nam và nữ mãn kinh.17 Những định nghĩa chuẩn về thiếu máu này không dựa trên những quy phạm về sinh lý hay dân số đã được biết. Mặc dù không thống nhất về định nghĩa, nhưng các nghiên cứu đều cho thấy tần suất của thiếu máu tăng ở những bệnh nhân STM có bệnh thận đi kèm, tuổi cao, và có nhiều triệu chứng nặng hơn khi so sánh với những người ít triệu chứng hơn. Một số báo cáo ghi nhận tần suất thiếu máu cũng khá cao ở những bệnh nhân có phân suất tống máu bảo tồn.18-20
Nguyên nhân thiếu máu trong STM
Thiếu máu xảy ra khi có sự thiếu hụt lượng hồng cầu mới được tạo ra tương đối so với lượng hồng cầu già bị chết đi. Erythropoietin, một yếu tố tăng trưởng glycoprotein 30,4-kDa tạo ra từ thận, là thành phần chính điều hòa khối lượng hồng cầu và cung cấp oxygen cho mô.21-24 Erythropoietin ngăn ngừa sự chết theo chương trình của các tế bào gốc dòng hồng cầu và do đó kích thích sự tăng sinh, trưởng thành, và biệt hóa.23 Bất kỳ yếu tố nào làm thận giảm bài tiết erythropoietin hoặc làm tủy xương giảm đáp ứng với erythropoietin đều có thể gây thiếu máu.
Thiếu máu thiếu sắt hiện diện ở < 30% những bệnh nhân STM, nghĩa là đa số bệnh nhân là thiếu máu đẳng bào, thường được xem là thiếu máu của bệnh lý mạn tính. Các đặc tính lâm sàng kết hợp với tăng nguy cơ thiếu máu ở dân số STM được liệt kê trong Bảng 1. Các yếu tố nguy cơ góp phần vào thiếu máu ở bệnh nhân STM. Một số nguyên nhân quan trọng được tóm tắt trong Hình 1.
Suy thận mạn thường đi kèm với STM và là yếu tố dự báo độc lập của thiếu máu. Bệnh thận mạn mức độ trung bình đến nặng (GFR < 60 ml/phút) không có suy tim, sự giảm sản xuất erythropoietin và hemoglobin có liên quan với giảm độ lọc cầu thận. Khoảng 20-40% dân số này có thiếu máu.4,9,26,27
Bảng 1. Các đặc tính lâm sàng kết hợp với tăng nguy cơ thiếu máu
Tuổi cao
Giới nữ
Bệnh thận mạn (tăng creatinine huyết thanh hoặc giảm GFR)
Giảm chỉ số khối cơ thể
Dùng thuốc ức chế men chuyển
Phù chân
Một số nghiên cứu cũng cho thấy thiếu máu thường đi kèm với giảm chỉ số khối cơ thể, gợi ý những bệnh nhân suy kiệt (cachexia) có nguy cơ bị thiếu máu nhiều hơn. Nồng độ của các cytokines tiền viêm trong huyết thanh tăng cao ở những bệnh nhận STM có suy kiệt góp phần gây thiếu máu. Các cytokines tiền viêm bao gồm yếu tố hoại tử mô a (TNF-a), interleukin-1, và interleukin-6 làm phá vỡ nhiều khâu trong quá trình tạo hồng cầu, như giảm bài tiết erythropoietin từ thận, ức chế hoạt động của erythropoietin, và giảm sinh khả dụng của dự trữ sắt cho quá trình tổng hợp hemoglobin.28-31 Các cytokines tiền viêm cũng làm tăng nồng độ hepcidin, hormone peptide có nguồn gốc từ gan.32-33 Hepcidin tương tác với ferroportin và các protein vận chuyển sắt khác ở tế bào ruột để ức chế hấp thu sắt qua đường ruột qua đó làm giảm cung cấp sắt cho sự tổng hợp hemoglobin.32-33 Trên chuột bị suy tim do nhồi máu cơ tim, thiếu máu liên kết với sự hoạt hóa của con đường tín hiệu TNF-a/Fas.34 Số lượng tế bào gốc tủy xương và khả năng tăng sinh của các tế bào này giảm 40-50% ở chuột bị suy tim so với nhóm chứng. Quá trình chết tế bào theo chương trình tăng 3 lần ở các tế bào gốc của chuột suy tim có tương quan chặt với sự tăng hoạt động của TNF-a/Fas ở tế bào T và các tế bào tiêu diệt tự nhiên ở tủy xương.34 Trên bệnh nhân STM, nồng độ các cytokines tiền viêm gia tăng (TNF-a và các thụ thể TNF tan trong nước) và các chất đánh dấu viêm khác trong máu (C-reactive protein) tỷ lệ nghịch với nồng độ hemoglobin.35
Hệ renin-angiotensin đóng một vai trò không thể thiếu trong việc điều hòa thể tích huyết tương và hồng cầu. Tăng tín hiệu angiotensin II ở thận sẽ làm thay đổi áp lực oxygen quanh ống thận (peritubular oxygen tension), một yếu tố điều hòa then chốt cho sự bài tiết erythropoietin.21,24 Giảm áp lực oxygen ở các nguyên bào sợi quanh ống (peritubular fibroblasts) của vỏ thận kết hợp với tăng tăng nồng độ các dạng oxygen phản ứng trong tế bào dẫn đến tăng hoạt hóa HIF-1 (hypoxia inducible factor-1) và sự biểu hiện gene erythropoietin.36
Angiotensin II làm tăng bài tiết erythropoietin do làm giảm lưu lượng máu thận và tăng tái hấp thu ở ống thận gần.21 Angiotensin II cũng kích thích trực tiếp lên các tế bào gốc của hồng cầu ở tủy xương.37 Nồng độ erythropoietin tăng vừa phải ở bệnh nhân STM tương ứng với mức độ hoạt hóa của hệ renin-angiotensin.38 Ức chế hệ renin-angiotensin bằng ức chế men chuyển hoặc ức chế thụ thể angiotensin làm giảm sản xuất erythropoietin và giảm nồng
độ hemoglobin.12,39,40 Ức chế men chuyển cũng làm xúc tác cho quá trình phá vỡ của Ac-SDKP, chất ức chế quá trình sinh hồng cầu. Ở những bệnh nhân STM có thiếu máu được điều trị bằng ức chế men chuyển có hoạt động của men chuyển trong huyết thanh thấp, nồng độ Ac-SDKP tăng so với những người STM không thiếu máu.41 Huyết thanh lấy từ những bệnh nhân thiếu máu STM có nồng độ Ac-SDKP cao gây ức chế sự hình thành các nguyên hồng cầu khi cấy so với huyết thanh của những người STM không thiếu máu hay nhóm chứng khỏe mạnh. Tác động của ức chế men chuyển lên hematocrit thì phức tạp khi ức chế men chuyển có thể làm giảm sản xuất hồng cầu và cũng làm giảm thể tích huyết tương (xem phần thảo luận về pha loãng máu ở dưới). Trong các thử nghiệm lâm sàng, khi ức chế he renin-angiotensin thường kết hợp với giảm nhẹ hemoglobin có ý nghĩa thống kê.12,40,42
Thiếu máu thường đi kèm với các triệu chứng cơ năng và thực thể của sung huyết, gợi ý tăng thể tích huyết tương có thể góp phần vào thiếu máu trong STM do quá trình pha loãng máu. Trong số 37 bệnh nhân STM thiếu máu không phù, một kỹ thuật đánh dấu albumin bằng đồng vị phóng xạ để đo trực tiếp thể tích huyết tương cho thấy 46% bệnh nhân hematocrit thấp có thể tích hồng cầu bình thường, như vậy có thể quy cho thiếu máu làm tăng thể tích huyết tương và hậu quả là pha loãng máu.3 Bệnh nhân bị pha loãng máu có lâm sàng tương tự như những người có thể tích hồng cầu giảm nhưng có nguy cơ tử vong cao hơn trong quá trình theo dõi. Việc sử dụng erythropoietin nhằm làm tăng khối lượng hồng cầu ở bệnh nhân pha loãng máu có thể làm tăng nhiều hơn thể tích máu toàn bộ cùng với những hậu quả lâm sàng xấu hơn. Điều trị tích cực bằng lợi tiểu có thể làm giảm thể tích huyết tương và điều chỉnh hiệu quả hơn thiếu máu ở những bệnh nhân có pha loãng máu.
Các hậu quả sinh lý bệnh của thiếu máu
Khi không có bệnh tim thực thể, nồng độ hemoglobin giảm nặng (4-5 g/dL) kết hợp với giữ muối nước, giảm lưu lượng máu thận và độ lọc cầu thận, và bằng chứng của hoạt hóa thần kinh thể dịch.43 Những đáp ứng tim-thận này có thể do ảnh hưởng của thiếu máu nặng trên độ nhớt máu, áp lực oxygen ở giường mao mạch, và hiệu lực của nitric oxide.44,45
Mức độ thiếu máu nhẹ hơn có thể góp phần vào sự hoạt hóa thần kinh thể dịch và tiến triển của bệnh trong STM.46 Ở những bệnh nhân có hội chứng b-thalassemia, suy tim là một biến chứng thường gặp qua trung gian của các tác động huyết động học và thần kinh thể dịch của thiếu máu mạn nặng và quá tải sắt thứ phát sau truyền sắt lâu ngày.47 Điều trị sắt tích cực làm giảm đáng kể nhưng không loại bỏ được nguy cơ suy tim ở những bệnh nhân này.
Nồng độ hemoglobin trong máu là một yếu tố quyết định quan trọng sự cung cấp oxygen cho co xương vận động. Bệnh nhân STM thiếu dự trữ sinh lý để bù trừ sự giảm hemoglobin và có biểu hiện giảm khả năng hoạt động gắng sức.48 Một số nhà nghiên cứu đã báo cáo sự kết hợp giữa giảm hemoglobin với giảm chức năng nhiều theo phân loại NYHA.3,15,49 Kalra và cộng sự50 đã chứng minh mối quan hệ tuyến tính giữa giảm hemoglobin với mức tiêu thụ oxygen đỉnh ở những bệnh nhân thiếu máu STM có hemoglobin < 13 g/dL.
Khối cơ tim tăng 25% ở chuột bị thiếu máu mạn.51 Một tỷ lệ nghịch giữa giá trị hemoglobin hay hematocrit với phì đại thất trái cũng được mô tả trong các nghiên cứu lâm sàng ở những bệnh nhân phải lọc thận định kỳ hoặc bệnh thận mạn trước giai đoạn lọc thận.52 Trong một phân nhóm bệnh nhân STM trong thử nghiệm RENAISSANCE (the Randomized Etanercept North American Strategy to Study Antagonism of Cytokines) với dữ liệu MRI tim, tăng 1 g/dL hemoglobin kết hợp với giảm 4,1 g/m2 khối cơ thất trái sau 24 tuần.49 Kết quả này độc lập với nghiên cứu điều trị thuốc và không cung cấp bằng chứng quan hệ nhân quả giữa những thay đổi của hemoglobin với những thay đổi về khối cơ thất trái. Trong hai thử nghiệm ngẫu nhiên trên những bệnh nhân bệnh thận mạn, hemoglobin gia tăng với điểu trị erythropoietin nhưng không kết hợp với giảm phì đại thất trái.53-54
Thiếu máu và dự hậu lâm sàng
Giảm hemoglobin trong STM được chứng minh làm tăng nguy cơ nhập viện và tử vong do mọi nguyên nhân.2-6,8,9,11-13,15,19,42,49 Các kết quả này gợi ý một sự liên quan tuyến tính giữa giảm hemoglobin và tăng nguy cơ tử vong. Trong các nghiên cứu phân tích hemoglobin như là một biến liên tục, giảm 1 g/dL hemoglobin kết hợp độc lập với tăng có ý nghĩa nguy cơ tử vong (Hình 2). Những cơ chế tiềm tàng liên kết thiếu máu với tăng nguy cơ tử vong trong STM chưa được mô tả nhưng có thể liên quan đến những biến đổi về tình trạng chịu tải của thất và cấu trúc tim, sự hoạt hóa thần kinh thể dịch, hay giảm khả năng dọn dẹp các gốc tự do. Thiếu máu cũng có thể là một dấu chứng của bệnh cơ tim căn bản nặng hơn.
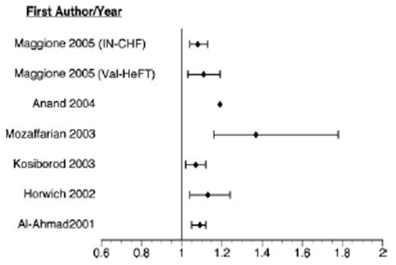
Hình 2. Ước lượng tỉ số rủi ro (KTC 95%) cho tử vong do mọi nguyên nhân kết hợp với giảm 1 g/dL hemoglobin. Ước lượng theo mô hình rủi ro tỉ lệ Cox có điều chỉnh các biến không đồng nhất. Các nghiên cứu của Al-Ahmad, Kosiborod và Mozaffarian ước lượng tỉ số rủi ro từ dữ liệu được công bố cho rằng giảm 1 g/dL hemoglobin tương đương với giảm 3% hematocrit. Phân tích của Mozaffarian bao gồm những bệnh nhân có hematocrit ≤ 37,5%. Anand và cộng sự không báo cáo khoảng tin cậy cho ước lượng nguy cơ. Maggione và cộng sự ước lượng nguy cơ từ 2 dân số nghiên cứu trong đăng bộ IN-CHF và thử nghiệm lâm sàng Val-HeFT.
Các tiếp cận điều trị
Truyền máu cho những bệnh nhân bệnh tim mạch có thiếu máu còn tranh cãi. Theo hướng dẫn của Hội Thầy thuốc Hoa Kỳ (American College of Physicians) và Hội Gây mê Hoa Kỳ (American Society of Anesthesiology), “ngưỡng truyền máu” cho những bệnh nhân không có yếu tố nguy cơ tim mạch là hemoglobin từ 6-8 g/dL.55 Trong 78 974 bệnh nhân lớn tuổi nhập viện vì nhồi máu cơ tim cấp, truyền máu kết hợp với tỉ lệ tử vong 30 ngày thấp hơn có ý nghĩa ở những người có hematocrit ≤ 30% lúc nhập viện.56 Trong 838 bệnh nhân nặng (26% bệnh tim mạch), duy trì hemoglobin 10-12 g/dL không mang lại thêm lợi ích nào trên tử vong 30 ngày so với duy trì hemoglobin 7-9 g/dL.57 Truyền máu có thể đi kèm với những tai biến phụ khác bao gồm ức chế miễn dịch làm tăng ngu
y cơ nhiễm trùng, dễ nhạy cảm với kháng nguyên HLA, và quá tải sắt.58,59 Với những dữ liệu về nguy cơ và lợi ích này, truyền máu được xem xét như là điều trị cấp cho thiếu máu nặng tùy từng trường hợp nhưng có lẽ không phải là một chiến lược điều trị sống còn trong điều trị dài hạn thiếu máu mạn ở bệnh nhân STM.
Mặc dù nồng độ erythropoietin tăng vừa phải trong STM, nhưng mức tăng này thấp hơn so với các dân số thiếu máu khác.27,38,60 Theo đó, thiếu máu trong STM có thể đáp ứng với bổ sung erythropoietin ngoại sinh. Cơ chế chính trong đó erythropoietin kích thích tạo hồng cầu là ức chế quá trình chết theo chương trình của các tế bào gốc hồng cầu tại tủy xương.23 Thụ thể erythropoietin là một thành viên của dòng họ thụ thể cytokine nhóm I.61 Sự gắn kết của erythropoietin với thụ thể sẽ hoạt hóa các đường truyền tín hiệu chống chết tế bào theo chương trình.23,62 Các tế bào gốc hồng cầu ở tủy xương thoát khỏi quá trình chết theo chương trình sẽ tăng sinh dẫn đến sự trưởng thành và phát triển của các tiền nguyên hồng cầu và nguyên hồng cầu. Tiếp đến, sự tăng sinh tế bào lưới xảy ra và nồng độ hemoglobin gia tăng.
Có 3 thuốc erythropoietin được dùng trong điều trị thiếu máu: epoetin-a, epoetin-b (cả hai đều là erythropoietin người tái tổ hợp [rHuEpo]), và darbepoetin-a.31 rHuEpo được tổng hợp đầu tiên vào năm 1985, 2 năm sau gene erythropoietin được nhân bản, và được Cục Quản lý Thuốc và Thực phẩm Hoa Kỳ (FDA) cấp phép sử dụng trên lâm sàng trong điều trị thiếu máu ở bệnh thận mạn giai đoạn cuối vào năm 1998.63 Các nghiên cứu trước đó trên những bệnh nhân bệnh thận mạn lọc thận định kỳ cho thấy tiêm tĩnh mạch hoặc tiêm dưới da 150-200 UI/kg mỗi tuần (trong 1 hoặc chia làm 3 liều)làm tăng nồng độ hemoglobin lên 10-12 g/dL trong 83-90% bệnh nhân thiếu máu có bệnh thận mạn.64 Thời gian bán hủy trong huyết tương của rHuEpo sau khi tiêm tĩnh mạch từ 6-8 giờ. Khoảng 25% liều dùng được hấp thu sau khi tiêm dưới da, nhưng thời gian bán hủy huyết tương lên đến > 24 giờ.65 Số lượng rHuEpo tiêm dưới da cần để đạt hemoglobin mục tiêu ở những bệnh nhân bệnh thận mạn ít hơn 25% liều cần dùng khi tiêm tĩnh mạch.65 Darbepoetin-a là một đồng phân liên kết N, tác dụng kéo dài của erythropoietin người được FDA chấp thuận cho điều trị thiếu máu ở bệnh thận mạn năm 2001.30 So với hai erythropoietin tự nhiên và tái tổ hợp, nó có ái lực mạnh hơn với thụ thể erythropoietin và thời gian bán hủy huyết tương gần 48 giờ, do đó khoảng cách liều điều trị duy trì sẽ dài hơn từ 1-2 tuần.66,67
Hiệu quả điều trị của rHuEpo trên bệnh nhân thiếu máu STM được báo cáo đầu tiên bởi Silverberg và cộng sự.1 Trong một thiết kế nghiên cứu mở, 26 bệnh nhân STM thiếu máu (NYHA III-IV và hemoglobin < 12 g/dL) được tiêm dưới da rHuEpo (liều trung bình 5277 UI/tuần) và sucrose sắt tiêm tĩnh mạch (liều trung bình 185 mg/tháng) và theo dõi trong thời gian 4-15 tháng (trung bình 7 tháng). Điều trị rHuEpo làm tăng hemoglobin trung bình từ 10,2-12,1 g/dL và đi cùng với cải thiện phân độ chức năng NYHA (3,7±0,5 ở thời điểm ban đầu xuống 2,7±0,7, P < 0,05), tăng phân suất tống máu thất trái (28±5% ở thời điểm ban đầu lên 35±8%, P < 0,001), và giảm nhu cầu dùng furosemide uống cũng như tiêm tĩnh mạch.1 Các tác giả này sau đó tiếp tục báo cáo một thử nghiệm mở ngẫu nhiên trong thời gian theo dõi trung bình 8 tháng so sánh hiệu quả của điều chỉnh một phần thiếu máu bằng rHuEpo tiêm dưới da và sucrose tiêm tĩnh mạch với điều trị thông thường trên 32 bệnh nhân STM nặng có thiếu máu (NYHA III-IV và hemoglobin < 11,5 g/dL).68 Kết quả điều trị bằng rHuEpo (tiêm dưới da 4000 UI 1-3 lần/tuần cộng với tiêm tĩnh mạch sucrose sắt 200 mg mỗi 2 tuần) làm tăng đáng kể nồng độ hemoglobin (10,3-12,9 g/dL so với 10,9-10,8 g/dL, P < 0,0001), cải thiện phân độ NYHA (rHuEpo 3,8±0,4 g 2,2±0,7 so với điều trị thông thường 3,5±0,7 g 3,9±0,3, P < 0,0001), và số ngày nằm viện (rHuEpo 13,8±7,2 g 2,9±6,6 ngày so với điều trị thông thường 9,9±4,8 15,5±9,8 ngày, P < 0,0001).68 Mancini và cộng sự70 tiến hành một thử nghiệm mù đơn, ngẫu nhiên, so sánh với giả dược của điều trị rHuEpo trên 26 bệnhnhân STM tiến triển có thiếu máu (hematocrit < 35%). Bệnh nhân được tiêm dưới da 5000 UI rHuEpo 3 lần/tuần và được điều chỉnh để nâng hematocrit lên > 45% sau 3 tháng hoặc tiêm dưới da 1 mũi nước muối sinh lý. Sắt và folate cũng được bổ sung bằng đường uống ở những bệnh nhân dùng rHuEpo. So sánh với nhóm giả dược, nhóm điều trị rHuEpo làm tăng có ý nghĩa hemoglobin (11,0±0,5 g 14,3±1,0 g/dL, P < 0,05), đỉnh hấp thu oxygen (11,0±1,8 g 12,7±2,8 mL/phút/kg, P < 0,05), thời gian gắng sức bằng thảm lăn (590±107 g 657119 giây, P < 0,004). Sự tăng nồng độ hemoglobin liên quan tuyết tính với tăng đỉnh hấp thu oxygen (r = 0,53; P < 0,02).70 Những bệnh nhân có thiếu máu do pha loãng lẫn thiếu máu thực sự với thể tích hồng cầu giảm dường như đều cải thiện khả năng gắng sức khi điều trị với rHuEpo. Trong phân nhóm pha loãng máu với tăng thể tích huyết tương, hematocrit tăng đáp ứng với rHuEpo là do giảm thể tích huyết tương. Khi mà liều lợi tiểu không thay đổi trong suốt nghiên cứu, các kết quả này gợi ý erythropoietin có tác dụng trực tiếp hoặc gián tiếp lên sự điều hòa thể tích huyết tương của thận.
Những tính chất về dược lực và dược động học của darbepoetin-a được so sánh trên 33 bệnh nhân STM có thiếu máu (hemoglobin ≤ 12,5 g/dL) so với 30 người khỏe mạnh.71 Darbepoetin-a được dùng mỗi tháng 1 lần với liều 20 mg/kg hay cao hơn làm tăng kéo dài nồng độ hemoglobin ở bệnh nhân STM thiếu máu mà không gây tác dụng phụ nặng nề nào.71 Hiệu quả của điều trị bằng darbepoetin-a (0,7 mg/kg tiếm dưới da mỗi 2 tuần trong 26 tuần) trên khả năng dung nạp với gắng sức được đánh giá trong một thử nghiệm ngẫu nhiên có so sánh với giả dược trên 41 bệnh nhân STM thiếu máu (hemoglobin 9-12 g/dL).72 Kết quả cho thấy tác dụng có lợi của darbepoetin-a trên thời gian gắng sức và chất lượng cuộc sống khi so sánh với giả dược.72 Một thử nghiệm khác lớn hơn STAMINA HeFT (Studies of Anemia in Heart Failure Trial) thực hiện trên 300 bệnh nhân STM thiếu máu nhằm xác định có cải thiện khả năng gắng sức và chất lượng cuộc sống hay không đã hoàn tất quá trình lấy mẫu nhưng kết quả chưa được công bố.73
Những nguy cơ tiềm tàng khi điều trị bằng erythropoietin
Điều trị bằng erythropoietin làm tăng nguy cơ tạo huyết khối. Nguy cơ này một phần do tác dụng từ sự tăng nồng độ hemoglobin, tăng độ
nhớt máu hay sự tương tác tiểu cầu-hồng cầu hoặc do tác động trực tiếp của erythropoietin lên tiểu cầu hay các tế bào nội mạc.74-76 Các nghiên cứu về tỉ lệ huyết khối do điều trị bằng rHuEpo ở bệnh nhân bệnh thận giai đoạn cuối có thiếu máu lọc thận định kỳ cho những kết quả khác nhau.77-79 Trong thử nghiệm lâm sàng ngẫu nhiên lớn nhất tính đến thời điểm hiện tại, Besarab và cộng sự77 so sánh hiệu quả của rHuEpo trên mục tiêu hematocrit thấp 30% với mục tiêu hemoglobin bình thường 42% trên 1233 bệnh nhân bệnh thận giai đoạn cuối phải lọc thận có bệnh tim mạch đi kèm. Nghiên cứu này đã phải kết thúc sớm do xu hướng tăng nguy cơ tử vong hoặc nhồi máu cơ tim không tử vong ở nhóm mục tiêu hematocrit 30% (RR = 1,3; 95% CI; 0,9-1,9). Cơ chế chưa rõ, trong mỗi nhóm điều trị giá trị hemoglobin cao hơn thì nguy cơ thấp hơn.
Trong một nghiên cứu hồi cứu trên những bệnh nhân thiếu máu bị ung thư cổ tử cung, điều trị rHuEpo mạn kết hợp với tăng nguy cơ huyết khối tĩnh mạch sâu độc lập với hematocrit.80
Điều trị rHuEpo cũng kết hợp với tăng nguy cơ tử vong do mọi nguyên nhân trong hai thử nghiệm ngẫu nhiên có so sánh với giả dược ở những bệnh nhân ung thư vú và ung thư vùng đầu cổ.81,82 Các tai biến huyết khối không phải là nguyên nhân gây tử vong thường gặp trong các nghiên cứu này. Mặc dù các kết quả trên bệnh thận mạn và dân số bị ung thư có thể không đúng trực tiếp cho những bệnh nhân STM nhưng nó gợi ý cần có những thử nghiệm khác để xác định hiệu quả và độ an toàn dài hạn của các thuốc erythropoietin trên dân số STM.
Trong thử nghiệm lâm sàng nhỏ trên bệnh nhân thiếu máu STM được tóm tắt ở trên, không có tai biến huyết khối hay tác dụng phụ khác nào của erythropoietin trên gần 300 bệnh nhân.1,68-70,72 Việc dùng các thuốc chống kết tập tiểu cầu và kháng đông ở bệnh nhân STM có thể làm nhẹ đi tác dụng tiền đông của các thuốc erythropoietin.
Dùng rHuEpo dài ngày thường kết hợp với tăng huyết áp.83,84 Các cơ chế có thể bao gồm tăng khối lượng hồng cầu làm tăng độ nhớt máu, thay đổi môi trường thần kinh thể dịch, và tác dụng trực tiếp trên cấu trúc và chức năng vi mạch.84,85 Ở những bệnh nhân bệnh thận mạn, các yếu tố nguy cơ của tăng huyết áp gồm tăng nhanh hematocrit trong quá trình điều trị, hematocrit ban đầu thấp, dùng rHuEpo tiêm mạch liều cao và yếu tố di truyền liên quan đến tăng huyết áp.85
Các tác dụng phụ đáng kể khác của rHuEpo được báo cáo gồm co giật và ngừng tạo hồng cầu do hình thành kháng thể chống lại erythropoietin.
Vai trò của bổ sung sắt
Mặc dù thiếu sắt chỉ rõ ràng trong thiểu số bệnh nhân STM, thiếu sắt chức năng, đặc trưng bởi giảm khả năng dự trữ sắt của ở mô để cung cấp cho quá trình tạo hồng cầu, có thể là vấn đề thường gặp trong STM.86 Một số nghiên cứu nhỏ có giá trị trên bệnh nhân thiếu máu STM cho thấy hemoglobin tăng đáng kể với điều trị bằng rHuEpo tiêm tĩnh mạch và bổ sung sắt đường uống.69,70 Hướng dẫn hiện tại của Hiệp hội Thận Quốc gia khuyến cáo dùng sắt đường tĩnh mạch để duy trì nồng độ ferritin huyết thanh từ 100-800 ng/mL và độ bão hòa transferrin 20-50% nhằm tối ưu hóa đáp ứng lâm sàng với các thuốc erythropoietin.17 Mặc dù dạng trình bày sucrose sắt và gluconate sắt tĩnh mạch không gây phản ứng phản vệ và thường được dung nạp tốt ở dân số bệnh thận mạn, vẫn cần lưu ý về sự quá tải sắt kết hợp với tăng nguy cơ nhiễm trùng và tai biến tim mạch.17,87,88 Cần xác định thêm về hiệu quả và độ an toàn của bổ sung sắt bằng đường tĩnh mạch trên những bệnh nhân thiếu máu STM có thiếu sắt chức năng.
Khuyến cáo cho thực hành hiện nay
Những hướng dẫn lâm sàng về STM gần đây ít thảo luận về việc đánh giá và chọn lựa điều trị thiếu máu.89,90 Với cơ sở dữ liệu đã có, cần khuyến cáo đo nồng độ hemoglobin đối với những bệnh nhân STM mỗi sáu tháng một lần nhằm phát hiện thiếu máu vì những lợi ích có thể có nếu được đánh giá và điều trị đúng mức. Việc đánh giá bao gồm đo lường sắt, các chất dinh dưỡng khác và tính độ lọc cầu thận. Đối với những người có thiếu máu trung bình – nặng (hemoglobin < 11 g/dL) và bệnh thận mạn trung bình – nặng đi kèm (GFR ≤ 60 mL/phút), hướng dẫn hiện nay của Hiệp hội Thận Quốc gia khuyến cáo điều trị bằng erythropoietin và bổ sung sắt để đạt hemoglobin mục tiêu 12 g/dL.17,27 Mục tiêu tiên phát của điều trị là cải thiện chất lượng cuộc sống. Do thiếu những bằng chứng và dữ liệu về dự hậu dài hạn và sự lo lắng về tỉ lệ tử vong tăng ở những dân số thiếu máu khác, không khuyến cáo dùng erythropoietin cho những bệnh nhân STM thiếu máu nhẹ và có chức năng thận bảo tồn.91
Tài liệu tham khảo
1. Silverberg DS, Wexler D, Blum M, Keren G, Sheps D, Leibovitch E, Brosh D, Laniado S, Schwartz D, Yachnin T, Shapira I, Gavish D, Baruch R, Koifman B, Kaplan C, Steinbruch S, Iaina A. The use of subcutaneous erythropoietin and intravenous iron for the treatment of the anemia of severe, resistant congestive heart failure improves cardiac and renal function and functional cardiac class, and markedly reduces hospitalizations. J Am Coll Cardiol. 2000; 35: 1737-1744.
2. Al-Ahmad A, Rand WM, Manjunath G, Konstam MA, Levey AS, Sarnak MJ. Reduced kidney function and anemia as risk factors for mortality in patients with left ventricular dysfunction. J Am Coll Cardiol. 2001; 38: 955-962.
3. Androne AS, Katz SD, Lund L, LaManca J, Hudaihed A, Hryniewicz K, Mancini DM. Hemodilution is common in patients with advanced heart failure. Circulation. 2003; 107: 226-229.
4. Ezekowitz JA, McAlister FA, Armstrong PW. Anemia is common in heart failure and is associated with poor outcomes: insights from a cohort of 12 065 patients with new-onset heart failure. Circulation. 2003; 107: 223-225.
5. Mozaffarian D, Nye R, Levy WC. Anemia predicts mortality in severe heart failure: the prospective randomized amlodipine survival evaluation (PRAISE). J Am Coll Cardiol. 2003; 41: 1933-1939.
6. Horwich TB, Fonarow GC, Hamilton MA, MacLellan WR, Borenstein J. Anemia is associated with worse symptoms, greater impairment in functional capacity and a significant increase in mortality in patients with advanced heart failure. J Am Coll Cardiol. 2002; 39: 1780-1786.
7. Cromie N, Lee C, Struthers AD. Anaemia in chronic heart failure: what is its frequency in the UK and its underlying causes? Heart. 2002; 87: 377-378.
8. Kosiborod M, Smith GL, Radford MJ, Foody JM, Krumholz HM. The prognostic importance of anemia in patients with heart failure. Am J Med. 2003; 114: 112-119.
9. McClellan WM, Flanders WD, Langston RD, Jurkovitz C, Presley R. Anemia and renal insufficiency are independent risk factors for death among patients with co
ngestive heart failure admitted to community hospitals: a population-based study. J Am Soc Nephrol. 2002; 13: 1928-1936.
10. Tanner H, Moschovitis G, Kuster GM, Hullin R, Pfiiffner D, Hess OM, Mohacsi P. The prevalence of anemia in chronic heart failure. Int J Cardiol. 2002; 86: 115-121.
11. Felker GM, Gattis WA, Leimberger JD, Adams KF, Gheorghiade M, O’Connor CM. Usefulness of anemia as a predictor of death and rehospitalization in patients with decompensated heart failure. Am J Cardiol. 2003; 92: 625-628.
12. Anand IS, Kuskowski MA, Rector TS, Florea VG, Glazer RD, Hester A, Chiang YT, Aknay N, Maggioni AP, Opasich C, Latini R, Cohn JN. Anemia and change in hemoglobin over time related to mortality and morbidity in patients with chronic heart failure: results from Val-HeFT. Circulation. 2005; 112: 1121-1127.
13. Szachniewicz J, Petruk-Kowalczyk J, Majda J, Kaczmarek A, Reczuch K, Kalra PR, Piepoli MF, Anker SD, Banasiak W, Ponikowski P. Anaemia is an independent predictor of poor outcome in patients with chronic heart failure. Int J Cardiol. 2003; 90: 303-308.
14. Wexler D, Silverberg D, Sheps D, Blum M, Keren G, Iaina A, Schwartz D. Prevalence of anemia in patients admitted to hospital with a primary diagnosis of congestive heart failure. Int J Cardiol. 2004; 96: 79-87.
15. Maggioni AP, Opasich C, Anand I, Barlera S, Carbonieri E, Gonzini L, Tavazzi L, Latini R, Cohn J. Anemia in patients with heart failure: prevalence and prognostic role in a controlled trial and in clinical practice. J Card Fail. 2005; 11: 91-98.
16. McCullough PA, Lepor NE Anemia: a modifiable risk factor for heart disease. Introduction. Rev Cardiovasc Med. 2005; 6 (Suppl 3): S1-S3.
17. IV. NKF-K/DOQI Clinical Practice Guidelines for Anemia of Chronic Kidney Disease: update 2000. Am J Kidney Dis. 2001; 37: S182-S238.
18. Berry C, Hogg K, Norrie J, Stevenson K, Brett M, McMurray J. Heart failure with preserved left ventricular systolic function: a hospital cohort study. Heart. 2005; 91: 907-913.
19. Brucks S, Little WC, Chao T, Rideman RL, Upadhya B, Wesley-Farrington D, Sane DC. Relation of anemia to diastolic heart failure and the effect on outcome. Am J Cardiol. 2004; 93: 1055-1057.
20. Klapholz M, Maurer M, Lowe AM, Messineo F, Meisner JS, Mitchell J, Kalman J, Phillips RA, Steingart R, Brown EJ Jr, Berkowitz R, Moskowitz R, Soni A, Mancini D, Bijou R, Sehhat K, Varshneya N, Kukin M, Katz SD, Sleeper LA, Le Jemtel TH. Hospitalization for heart failure in the presence of a normal left ventricular ejection fraction: results of the New York Heart Failure Registry. J Am Coll Cardiol. 2004; 43: 1432-1438.
21. Katz SD. Mechanisms and treatment of anemia in chronic heart failure. Congest Heart Fail. 2004; 10: 243-247. 22. Bauer C, Kurtz A. Oxygen sensing in the kidney and its relation to erythropoietin production. Annu Rev Physiol. 1989; 51: 845-856.
23. Jelkmann W. Molecular biology of erythropoietin. Intern Med. 2004; 43: 649-659.
24. Donnelly S. Why is erythropoietin made in the kidney? The kidney functions as a critmeter. Am J Kidney Dis. 2001; 38: 415-425.
65. Fisher JW. Erythropoietin: physiology and pharmacology update. Exp Biol Med (Maywood). 2003; 228: 1-14.
66. Locatelli F, Canaud B, Giacardy F, Martin-Malo A, Baker N, Wilson J. Treatment of anaemia in dialysis patients with unit dosing of darbepoetin alfa at a reduced dose frequency relative to recombinant human erythropoietin (rHuEpo). Nephrol Dial Transplant. 2003; 18: 362-369.
67. Macdougall IC, Matcham J, Gray SJ. Correction of anaemia with darbepoetin alfa in patients with chronic kidney disease receiving dialysis. Nephrol Dial Transplant. 2003; 18: 576-581.
68. Silverberg DS, Wexler D, Sheps D, Blum M, Keren G, Baruch R, Schwartz D, Yachnin T, Steinbruch S, Shapira I, Laniado S, Iaina A. The effect of correction of mild anemia in severe, resistant congestive heart failure using subcutaneous erythropoietin and intravenous iron: a randomized controlled study. J Am Coll Cardiol. 2001; 37: 1775-1780.
69. Silverberg DS, Wexler D, Blum M, Tchebiner JZ, Sheps D, Keren G, Schwartz D, Baruch R, Yachnin T, Shaked M, Schwartz I, Steinbruch S, Iaina A. The effect of correction of anaemia in diabetics and non-diabetics with severe resistant congestive heart failure and chronic renal failure by subcutaneous erythropoietin and intravenous iron. Nephrol Dial Transplant. 2003; 18: 141-146.
70. Mancini DM, Katz SD, Lang CC, LaManca J, Hudaihed A, Androne AS. Effect of erythropoietin on exercise capacity in patients with moderate to severe chronic heart failure. Circulation. 2003; 107: 294-299.
71. Cleland JG, Sullivan JT, Ball S, Horowitz JD, Agoram B, Rosser D, Yates W, Tin L, Fuentealba P, Burton PB. Once-monthly administration of darbepoetin alfa for the treatment of patients with chronic heart failure and anemia: a pharmacokinetic and pharmacodynamic investigation. J Cardiovasc Pharmacol. 2005; 46: 155-161.
72. Cleland JG, Coletta AP, Clark AL, Velavan P, Ingle L. Clinical trials update from the European Society of Cardiology Heart Failure meeting and the Am College of Cardiology: darbepoetin alfa study, ECHOS, and ASCOT-BPLA. Eur J Heart Fail. 2005; 7: 937-939.
73. Mitka M. Researchers probe anemia-heart failure link. JAMA. 2003; 290: 1835-1838.
74. Valles J, Santos MT, Aznar J, Martinez M, Moscardo A, Pinon M, Broekman MJ, Marcus AJ. Platelet-erythrocyte interactions enhance alpha(IIb)beta(3) integrin receptor activation and P-selectin expression during platelet recruitment: down-regulation by aspirin ex vivo. Blood. 2002; 99: 3978-3984.
75. Diaz-Ricart M, Etebanell E, Cases A, Lopez-Pedret J, Castillo R, Ordinas A, Escolar G. Erythropoietin improves signaling through tyrosine phosphorylation in platelets from uremic patients. Thromb Haemost. 1999; 82: 1312-1317. 76. Fuste B, Serradell M, Escolar G, Cases A, Mazzara R, Castillo R, Ordinas A, Diaz-Ricart M. Erythropoietin triggers a signaling pathway in endothelial cells and increases the thrombogenicity of their extracellular matrices in vitro. Thromb Haemost. 2002; 88: 678-685.
77. Besarab A, Bolton WK, Browne JK, Egrie JC, Nissenson AR, Okamoto DM, Schwab SJ, Goodkin DA. The effects of normal as compared with low hematocrit values in patients with cardiac disease who are receiving hemodialysis and epoetin. N Engl J Med. 1998; 339: 584-590.
78. Foley RN, Parfrey PS, Morgan J, Barre PE, Campbell P, Cartier P, Coyle D, Fine A, Handa P, Kingma I, Lau CY, Levin A, Mendelssohn D, Muirhead N, Murphy B, Plante RK, Posen G, Wells GA. Effect of hemoglobin levels in hemodialysis patients with asymptomatic cardiomyopathy. Kidney Int. 2000; 58: 1325-1335.
79. Churchill DN, Muirhead N, Goldstein M, Posen G, Fay W, Beecroft ML, Gorman J, Taylor DW. Probability of thrombosis of vascular access among hemodialysis patients treated with recombinant human erythropoietin. J Am Soc Nephrol. 1994; 4: 1809-1813.
80. Wun T, Law L, Harvey D, Sieracki B, Scudder SA, Ryu JK. Increased incidence of symptomatic venous thrombosis in patients with cervical carcinoma treated with concurrent chemotherapy, radiation, and erythropoietin. Cancer. 2003; 98: 1514-1520.
81. Henke M, Laszig R, Rube C, Schafer U, Haase KD, Schilcher B, Mose S, Beer KT, Burger U, Dougherty C, Frommhold H. Erythropoietin to treat head and neck cancer patients with anaemia undergoing radiotherapy: randomised, double-blind, placebo-controlled trial. Lancet. 2003; 362: 1255-1260.
82. Leyland-Jones B, Semiglazov V, Pawlicki M, Pienkowski T, Tjulandin S, Manikhas G, Makhson A, Roth A, Dodwell D, Baselga J, Biakhov M, Valuckas K, Voznyi E, Liu X, Vercammen E. Maintaining normal hemoglobin levels with epoetin a
lfa in mainly nonanemic patients with metastatic breast cancer receiving first-line chemotherapy: a survival study. J Clin Oncol. 2005; 23: 5960-5972.
83. Mann JF. Hypertension and cardiovascular effects-long-term safety and potential long-term benefits of r-HuEPO. Nephrol Dial Transplant. 1995; 10 (Suppl 2): 80-84.
84. Vaziri ND. Mechanism of erythropoietin-induced hypertension. Am J Kidney Dis. 1999; 33: 821-828.
85. Maschio G. Erythropoietin and systemic hypertension. Nephrol Dial Transplant. 1995; 10 (Suppl 2): 74-79.
86. Cavill I. Intravenous iron as adjuvant therapy: a two-edged sword? Nephrol Dial Transplant. 2003; 18 (Suppl 8): viii24-viii28.
87. Day SM, Duquaine D, Mundada LV, Menon RG, Khan BV, Rajagopalan S, Fay WP. Chronic iron administration increases vascular oxidative stress and accelerates arterial thrombosis. Circulation. 2003; 107: 2601-2606.
88. Sullivan JL. Iron therapy and cardiovascular disease. Kidney Int Suppl. 1999; 69: S135-S137.
89. Swedberg K, Cleland J, Dargie H, Drexler H, Follath F, Komajda M, Tavazzi L, Smiseth OA, Gavazzi A, Haverich A, Hoes A, Jaarsma T, Korewicki J, Levy S, Linde C, Nieminen MS, Pierard L, Remme WJ. Guidelines for the diagnosis and treatment of chronic heart failure: executive summary (update 2005): The Task Force for the Diagnosis and Treatment of Chronic Heart Failure of the European Society of Cardiology. Eur Heart J. 2005; 26: 1115-1140.
90. Hunt SA, Abraham WT, Chin MH, Feldman AM, Francis GS, Ganiats TG, Jessup M, Konstam MA, Mancini DM, Michl K, Oates JA, Rahko PS, Silver MA, Stevenson LW, Yancy CW, Antman EM, Smith SC Jr, Adams CD, Anderson JL, Faxon DP, Fuster V, Halperin JL, Hiratzka LF, Hunt SA, Jacobs AK, Nishimura R, Ornato JP, Page RL, Riegel B. ACC/AHA 2005 Guideline Update for the Diagnosis and Management of Chronic Heart Failure in the Adult-Summary Article: A Report of the Am College of Cardiology/Am Heart Association Task Force on Practice Guidelines (Writing Committee to Update the 2001 Guidelines for the Evaluation and Management of Heart Failure): Developed in Collaboration With the Am College of Chest Physicians and the International Society for Heart and Lung Transplantation: Endorsed by the Heart Rhythm Society. Circulation. 2005; 112: 1825-1852.
91. Pfeffer MA, Solomon SD, Singh AK, Ivanovich P, McMurray JJ. Uncertainty in the treatment of anemia in chronic kidney disease. Rev Cardiovasc Med. 2005; 6 Suppl 3: S35-41.








