Phân tích tổng hợp
Đái tháo đường (ĐTĐ) đang gia tăng, phổ biến rộng khắp thế giới và tác động đến khoảng 6,6% dân số người trưởng thành toàn cầu, hoặc tương đương 285 triệu người. Đến năm 2030, ước tính 350 triệu người trên toàn thế giới sẽ chung sống với bệnh ĐTĐ.
Jun Cheng, MD; Wen Zhang, MMed; Xiaohui Zhang, MMed; Fei Han, MD; Xiayu Li, MD;
Xuelin He, MD; Qun Li, MMed; Jianghua Chen, MMed
Dịch:
BS. CKI. Văn Thị Bích Thủy
Bệnh viện ĐHYD Tp. HCM
Là một yếu tố nguy cơ độc lập cao đối với bệnh tim mạch (CV), ĐTĐ liên quan đến nhiều biến chứng mạch máu lớn. ĐTĐ là nguyên nhân hàng đầu gây tử vong sớm, và ước tính 6,8% người trưởng thành tử vong trên toàn thế giới do bệnh tim hoặc đột quỵ được cho là do ĐTĐ. Tỷ lệ tử vong do bệnh tim mạch ở các bệnh nhân ĐTĐ cao hơn từ 2-4 lần so với các bệnh nhân không ĐTĐ.
Hiệp hội ĐTĐ Hoa kỳ (ADA)16 khuyến cáo rằng các bệnh nhân ĐTĐ và THA nên được điều trị với phác đồ điều trị dùng thuốc bao gồm một ức chế men chuyển (ƯCMC) hoặc ức chế thụ thể (ƯCTT). Cả 2 loại thuốc đều hạn chế tác động của angiotensin II, nhưng cơ chế tác động không giống nhau.17 Vậy nên, theo lý thuyết, có thể có sự khác biệt tương quan giữa các nhóm thuốc. Phân tích tổng hợp gần đây của Van Vark và cộng sự cho thấy ƯCMC hoặc ƯCTT có tác động khác nhau lên tỷ lệ tử vong do mọi nguyên nhân ở các bệnh nhân THA. Sự khác biệt này cũng có thể tồn tại trong điều trị ĐTĐ. Tuy nhiên, khó đánh giá các tác động liên quan của ƯCMC và ƯCTT do thiếu các thử nghiệm so sánh đối đầu. Xem xét những điều trên, chúng tôi đã làm phân tích tổng hợp hiện tại nhằm vượt qua hạn chế này bằng cách đánh giá tác động của ƯCMC và ƯCTT một cách riêng lẻ so với giả dược hoặc các thuốc khác trên tỷ lệ tử vong do mọi nguyên nhân, tử vong do bệnh tim mạch, và các biến cố tim mạch ở các bệnh nhân ĐTĐ.
Phương pháp
Tiêu chuẩn Thu nhận và Loại trừ
Nghiên cứu được đưa vào nếu đó là một thử nghiệm lâm sàng có đối chứng ngẫu nhiên (RCT), bao gồm phân tích hậu kiểm và các phân tích dưới nhóm trên những bệnh nhân ĐTĐ, với thời gian theo dõi trung vị hoặc trung bình ít nhất 12 tháng. Nghiên cứu được đưa vào nếu có so sánh ƯCMC và ƯCTT (bất kể loại và liều dùng) với giả dược, không điều trị, hoặc các thuốc hạ áp khác (bao gồm ƯCMC so với ƯCTT). Nghiên cứu bị loại nếu thử nghiệm lâm sàng có đối chứng ngẫu nhiên (RCT) không đánh giá tác động của các ƯCMC và ƯCTT trên ĐTĐ dựa trên tỉ lệ tử vong do bệnh tim mạch hoặc tử vong do mọi nguyên nhân. Cuối cùng, các nghiên cứu bị loại nếu là các thử nghiệm bắt chéo.
Chiến lược tìm kiếm
Chúng tôi thực hiện tổng quan hệ thống các y văn phù hợp với phương pháp tiếp cận theo khuyến cáo của PRISMA để thực hiện các phân tích tổng hợp của những nghiên cứu can thiệp.19 Các tìm kiếm điện tử được thực hiện bằng cách sử dụng MEDLINE (01/01/1966 đến 31/12/2012) và EMBASE (01/01/1988 đến 31/12/2012). Trung tâm đăng ký Cochrane về các thử nghiệm có đối chứng cũng được tìm kiếm. Các thuật ngữ tiêu đề y khoa và các từ trong nội dung sau được sử dụng: ĐTĐ type 2, ĐTĐ type 1 hoặc ĐTĐ, các biến cố hoặc tử vong tim mạch, nhồi máu cơ tim, đột quỵ, suy tim, các ức chế men chuyển, thụ thể Angiotensin II, các ức chế thụ thể, chẹn thụ thể Angiotensin II, thụ thể Angiotensin, tử vong do bệnh tim mạch, thử nghiệm có đối chứng ngẫu nhiên, và thử nghiệm lâm sàng. Danh sách các tài liệu tham khảo từ các bài báo được trích dẫn cũng được tìm kiếm. Các thử nghiệm lâm sàng ngẫu nhiên được đăng ký là đã hoàn tất nhưng chưa công bố cũng được tìm trên trang clinicaltrials.gov. Các phần tóm tắt đã trình bày tại các phiên họp của Hiệp hội ĐTĐ Hoa Kỳ từ 2005 đến 2012 cũng được tìm kiếm để có thêm những dữ liệu chưa được công bố.
Tựa đề và phần tóm tắt của các bài báo từ những tìm kiếm trên được phân tích độc lập bởi hai tác giả (J. Cheng và W. Z.) để xác định tính đồng nhất của tiêu chuẩn thu nhận. Nội dung đầy đủ của một bài báo được xem xét kỹ nếu kết quả sàng lọc tựa đề và phần tóm tắt không rõ để thu nhận.
Đánh giá chất lượng nghiên cứu
Chúng tôi đánh giá chất lượng của các nghiên cứu được đưa vào dựa trên phương pháp che giấu phân nhóm và phân tích theo ý định điều trị; sự làm mù của nghiên cứu viên, người tham gia, và người đánh giá kết cục; và sự hoàn tất theo dõi. Ngoài ra, chúng tôi dùng thang Jadad để xác định chất lượng của các thử nghiệm.20
Kết cục
Các kết cục chính là tử vong do mọi nguyên nhân và tử vong do các nguyên nhân tim mạch. Các kết cục phụ là các tác động của ƯCMC và ƯCTT lên tần suất của các biến cố tim mạch chính, được định nghĩa là sự tổng hợp của tử vong do bệnh tim mạch, nhồi máu cơ tim (NMCT) không tử vong và đột quỵ, suy tim xung huyết, và phẫu thuật bắc cầu động mạch vành hoặc can thiệp mạch vành qua da, ở các bệnh nhân ĐTĐ, cũng như tác động của ƯCMC và ƯCTT lên NMCT, đột quỵ, và suy tim xung huyết ở các bệnh nhân ĐTĐ. Những định nghĩa kết cục được tham khảo từ các bài báo gốc đã được xuất bản. Các kết cục được dựa trên thời gian theo dõi dài nhất có trong mỗi nghiên cứu.
Phân tích thống kê
Dữ liệu từng bệnh nhân không có sẵn cho các nghiên cứu trong phân tích này; vậy nên, dữ liệu bảng được dùng. Dùng giá trị tỷ số nguy cơ (RR) và khoảng tin cậy (KTC) 95% để phân tích dữ liệu kết cục nhị phân từ các thử nghiệm riêng lẻ.
Để xác định sự chắc chắn của các tác động gộp, chúng tôi so sánh phân tích sơ khởi của chúng tôi với các mô hình tác động ngẫu nhiên.21 Các kết quả được xác định bởi mô hình ảnh hưởng cố định Mantel-Haenszel để tránh các nghiên cứu nhỏ được định lượng quá mức. Các biểu đồ phễu và thử nghiệm Begg được dùng để thăm dò sai lệch trong công bố. Độ không đồng nhất giữa các nghiên cứu cũng được đánh giá, sử dụng thống kê I2, phân các giá trị nhỏ hơn 25% là thiểu số, 25% đến 49% là trung bình, và 50% hoặc nhiều hơn là trọng yếu.
Kết quả
Quá trình thử nghiệm và các đặc điểm của nghiên cứu
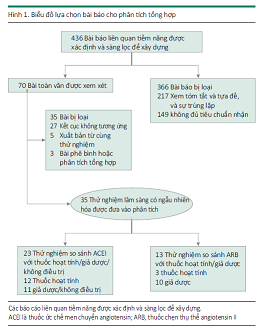
Tìm kiếm kết hợp MEDLINE, EMBASE, và Cochrane bao gồm một vài tìm kiếm thủ công ở các tạp chí thận học thích hợp, tìm được 436 trích dẫn. Sau khi loại bỏ một số bài trùng lặp, thu được bằng cách tìm kiếm riêng lẻ và xem xét tất cả tựa đề và phần tóm lược, nhiều nghiên cứu được loại ra vì không phải là RCT, không nghiên cứu những kết cục mà nghiên cứu quan tâm, hoặc những nghiên cứu cơ bản hoặc trên động vật. Nhìn chung, 35 thử nghiệm (35 với 1 nghiên cứu dùng cả ƯCMC và ƯCTT) thu nhận tổng cộng 56.444 bệnh nhân được chọn vào phân tích này (Hình 1).
Hai mươi ba nghiên cứu (n=32.827) so sánh ƯCMC với liệu pháp đối chứng, và 13 nghiên cứu (n=23.867) so sánh ƯCTT với liệu pháp đối chứng. 23 nhóm chất so sánh gồm 11 nhóm so sánh ƯCMC với giả dược và 12 nhóm được so sánh với điều trị chủ động.
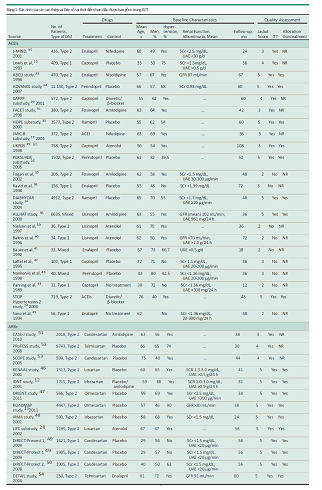
Các chi tiết của thử nghiệm can thiệp, các đặc điểm ban đầu của các nhóm dân số, thời gian nghiên cứu, thuốc dùng kèm, và theo dõi trong các RCT được chọn vào phân tích của chúng tôi được tóm tắt ở Bảng 1.
Đánh giá chất lượng
Chất lượng của các nghiên cứu được chọn được đánh giá độc lập bởi 2 trong số các tác giả (W. Z và J. Cheng) sử dụng thang Jadad, có thang từ 0-5 điểm. Chất lượng nghiên cứu nhìn chung tốt. Hai mươi mốt nghiên cứu (60,0%) có thang Jadad lớn hơn 3 (Bảng 1). Người tham gia và nghiên cứu viên được làm mù trong 27 thử nghiệm. Mười tám nghiên cứu (51,4%) đạt các tiêu chuẩn của phương pháp che giấu phân nhóm, và 26 nghiên cứu (74,3%) đạt tiêu chuẩn phân tích theo ý định điều trị.
Kết cục chính
Tác động của ƯCMC lên tỷ lệ tử vong do mọi nguyên nhân và tử vong do bệnh tim mạch
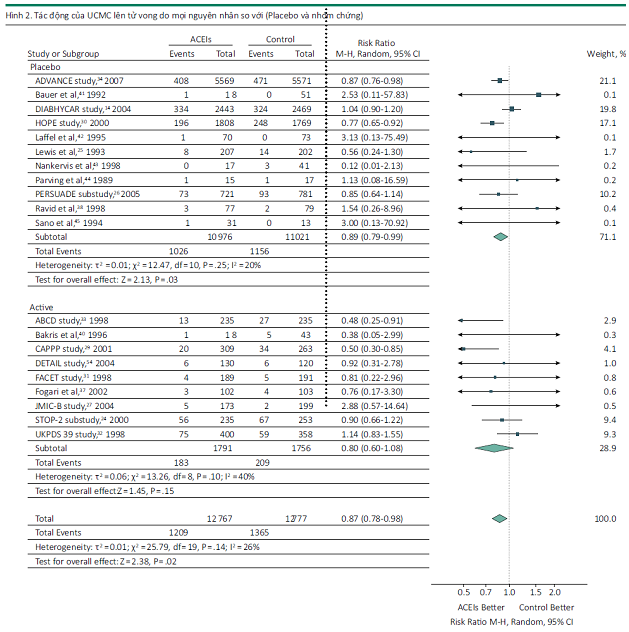
Tổng cộng 20 nghiên cứu trong số 23 RCT được phân tích để khảo sát tiền cứu hiệu quả của ƯCMC cho tử vong do mọi nguyên nhân ở tổng cộng 25544 bệnh nhân ĐTĐ. Trong 20 thử nghiệm được kết hợp, ƯCMC liên quan đến mức giảm có ý nghĩa thống kê là 13% tử vong do mọi nguyên nhân so với đối chứng (RR, 0,87; KTC 95%, 0,78-0,98; P=.02) (Hình 2). Các kết quả cũng tương tự khi so sánh ƯCMC với giả dược hoặc điều trị chủ động (P=.49). Có sự không đồng nhất ở mức độ thấp đến trung bình (I2 = 26%; P=.14) và không có bằng chứng có sai lệch trong công bố (P=.69) (Hình 1).
Mười ba trong số 23 RCT đã đánh giá tác động của ƯCMC đến sự xuất hiện tử vong do tim mạch trên 24334 bệnh nhân ĐTĐ. Theo phân tích tổng hợp của chúng tôi, nơi mà những nghiên cứu riêng lẻ được chú ý lượng giá, ƯCMC làm giảm 17% tử vong do tim mạch so với đối chứng (RR, 0.83; KTC 95% 0.70-0.99; P= .04). Hơn nữa, các kết quả tương tự khi ƯCMC được so sánh với giả dược hoặc điều trị chủ động (P= .96). Về kết cục của tử vong do tim mạch, có sự không đồng nhất ở mức trung bình (I2 = 40%; P= .07), nhưng không có bằng chứng về sai lệch công bố (P= .51) (Hình 2).
Tác động của ƯCTT lên tử vong do mọi nguyên nhân và tử vong do tim mạch
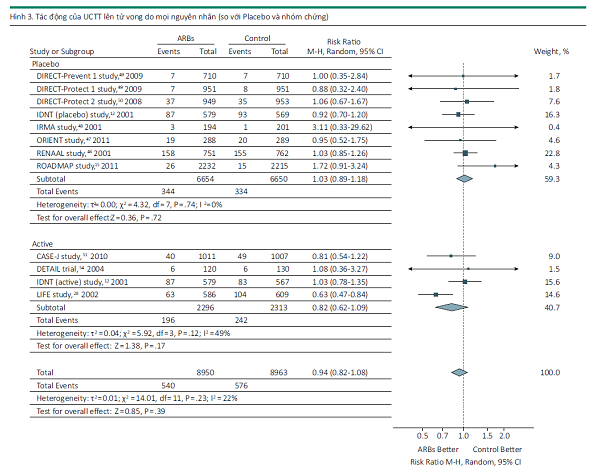
11 nghiên cứu bao gồm 17334 bệnh nhân đã được công bố về tác động của ƯCTT lên tử vong do mọi nguyên nhân ở những bệnh nhân ĐTĐ. ƯCTT không làm giảm có ý nghĩa nguy cơ tổng tử vong so với liệu pháp đối chứng ở những bệnh nhân ĐTĐ (RR, 0.94; KTC 95% 0.82-1.08; P= .39) (Hình 3). Các kết quả tương tự khi ƯCTT được so sánh với giả dược hoặc điều trị chủ động (P = .16).
Bảy nghiên cứu đã đánh giá tác động của ƯCTT lên sự xuất hiện tử vong do bệnh tim mạch ở 10.801 bệnh nhân ĐTĐ. Theo phân tích tổng hợp của chúng tôi, trong đó những nghiên cứu riêng lẻ được chú ý lượng giá, điều trị ƯCTT không làm giảm đáng kể nguy cơ tử vong do bệnh tim mạch so với điều trị đối chứng (RR, 1.21; KTC 95%, 0,81-1,80; P = .35). Hơn nữa, kết quả tương tự khi so sánh ƯCTT với giả dược hoặc điều trị chủ động (P = .12). Tuy nhiên, độ không đồng nhất của tác động điều trị giữa tất cả các thử nghiệm là có ý nghĩa (P = .01; I2 = 61%). Nghiên cứu ROADMAP15 và Thử nghiệm Olmesartan làm giảm tỷ lệ mới mắc bệnh thận giai đoạn cuối ở bệnh thận do ĐTĐ (ORIENT)47 sử dụng olmesartan làm thuốc điều trị. Sau khi loại bỏ 2 thử nghiệm có dùng olmesartan, sự không đồng nhất giữa các thử nghiệm đã không còn khác biệt đáng kể (I2 = 41%; RR, 0,98). Khi điều trị bằng olmesartan được so sánh với giả dược, có sự gia tăng đáng kể nguy cơ tử vong do bệnh tim mạch (2 thử nghiệm, 5024 bệnh nhân; RR, 4,10; KTC 95%, 1,68-9,98; P = .002). Khi ƯCTT được so sánh với liệu pháp đối chứng ở những bệnh nhân ĐTĐ, không có bằng chứng về sai lệch trong công bố về kết cục của tử vong do mọi nguyên nhân (P = .50) (Hình 3) và tử vong do bệnh tim mạch (P = .23).
Kết cục phụ
Tác động của ƯCMC lên các biến cố tim mạch chính và các kết cục tim mạch đặc trưng theo nguyên nhân
Mười bốn nghiên cứu đánh giá tác động của ƯCMC lên tần suất các biến cố tim mạchchính ở 34.352 bệnh nhân. Các thuốc trong nhóm này làm giảm đáng kể nguy cơ của các biến cố tim mạch chính đến 14% (RR, 0,86; KTC 95%, 0,77-0,95) so với điều trị đối chứng. Sự không đồng nhất giữa các thử nghiệm là có ý nghĩa đối với tất cả các biến cố tim mạch (P = .003; I2 = 59%). Phân tích phân nhóm cho thấy sự không đồng nhất chủ yếu xuất phát từ nhóm đối chứng chủ động (I2 = 65%); các kết quả tương tự khi ƯCMC được so sánh với giả dược hoặc điều trị chủ động (P = .31).
Nhồi máu cơ tim được báo cáo ở 11 thử nghiệm gồm 22.741 người tham gia, trong đó có 1.944 biến cố được quan sát. ƯCMC làm giảm nguy cơ nhồi máu cơ tim 21% (RR, 0,79; KTC 95%, 0,65-0,95; P = .01). Mười một thử nghiệm (33.508 người tham gia) đã báo cáo 1.775 biến cố đột quỵ, và 8 thử nghiệm (12.651 người tham gia) đã báo cáo 782 lần xuất hiện suy tim. ƯCMC có liên quan đến việc giảm 19% nguy cơ suy tim (RR, 0,81; KTC 95%, 0,71-0,93; P = .002), nhưng không có lợi ích rõ rệt đối với đột quỵ (0,95; 0,86-1,04; P = .28).
Tác động của ƯCTT lên các biến cố tim mạch chính và các kếtcục tim mạch đặc trưng theo nguyên nhân
Dữ liệu về tác động của ƯCTT lên các biến cố tim mạch chính có sẵn từ 9 thử nghiệm bao gồm 18.743 người tham gia và đã báo cáo 2.992 biến cố tim mạch. Gộp tất cả các thử nghiệm lại, không có sự giảm có ý nghĩa nguy cơ các biến cố tim mạch chính (RR, 0,94; KTC 0,85-1,01; P = .07). Không có sự không đồng nhất đáng kể giữacác thử nghiệm cho các tiêu chí kết cục này (P = .32; I2 = 13%). Các kết quả này tương tự khi so sánh ƯCTT với giả dược hoặc điều trị chủ động (P = .33).
Sáu thử nghiệm (11.454 người tham gia) đã báo cáo 415 biến cố nhồi máu cơ tim, và 8 thử nghiệm (17.796 người tham gia) đã báo cáo 1.064 lần đột quỵ. Không có lợi ích rõ rệt đối với nhồi máu cơ tim (RR, 0,89; KTC 95%, 0,74-1,07; P = .22; I2 = 0%) và đột quỵ (1,00; 0,89-1,12; P = .94; I2 = 0%).
Suy tim được báo cáo trong 4 thử nghiệm gồm 4.989 người tham gia, trong đó có 571 biến cố được quan sát. Liệu pháp ƯCTT làm giảm nguy cơ suy tim 30% (RR, 0.70; KTC, 0,59-0,82: P < .01; I2 = 0%). Không có sự không đồng nhất có ý nghĩa giữa các thử nghiệm cho những tiêu chí kết cục này.
Bàn luận
Phân tích tổng hợp này gồm dữ liệu từ 35 RCT cho thấy ƯCMC và ƯCTT có tác động khác nhau lên tử vong do mọi nguyên nhân, tử vong do tim mạch, và các biến cố tim mạch đối với bệnh nhân ĐTĐ. Theo phân tích tổng hợp này, ƯCMC làm giảm có ý nghĩa nguy cơ tử vong do mọi nguyên nhân khoảng 13% và tử vong do tim mạch khoảng 17%. Ngược lại, ƯCTT không có tác động có ý nghĩa lên tỷ lệ tử vong do mọi nguyên nhân và tử vong do tim mạch. Các thuốc ƯCMC làm giảm có ý nghĩa 14% nguy cơ các biến cố tim mạch chính, bao gồm 21%nhồi máu cơ tim và 19% suy tim. ƯCTT không làm giảm có ý nghĩa nguy cơ các biến cố tim mạch chính và nhồi máu cơ tim so với liệu pháp đối chứng ở các bệnh nhân ĐTĐ. Tuy nhiên, ƯCTT liên quan đến việc giảm 30% nguy cơ suy tim. Cả ƯCMC và ƯCTT đều không liên quan đến giảm nguy cơ đột quỵ ở các bệnh nhân ĐTĐ. Các kết quả tương tự khi so sánh ƯCMC và ƯCTT với giả dược và các điều trị chủ động đối với kết cục tử vong do mọi nguyên nhân và tử vong do tim mạch (P > .05 cho tất cả các so sánh).
Phân tích tổng hợp trước đó thực hiện bởi Nakao và cộng sự cho thấy điều trị ức chế hệ thống renin-angiotensin thông thường có thể được xem xét dùng thường quy cho bệnh nhân ĐTĐ để làm giảm các biến cố tim mạch chính. Một phân tích tổng hợp khác kết luận rằng sự ức chế hệ renin-angiotensin, chẹn kênh canxi, và thuốc lợi tiểu không cho thấy sự khác biệt trong việc bảo vệ tim mạch ở những bệnh nhân với các tình trạng bệnh lý cụ thể. Đối với bệnh nhân ĐTĐ và bệnh thận giai đoạn toàn phát, những bình luận này lấy từ các nghiên cứu có sử dụng phối hợp các thuốc ức chế hệ renin-angiotensin, ƯCMC và ƯCTT. Vài bình luận tập trung vào sự không đồng nhất giữa ƯCMC và ƯCTT với bệnh thận do ĐTĐ mới khởi phát60 và THA.18 Một số ít bình luận tập trung vào sự không đồng nhất giữa ƯCMC và ƯCTT đối với kết cục tử vong do mọi nguyên nhân và tử vong do tim mạch ở các bệnh nhân ĐTĐ. Tầm quan trọng trên lâm sàng của những khác biệt này đối với sự bảo vệ tim mạch được khẳng định trong nghiên cứu của chúng tôi; không giống như ƯCTT, ƯCMC làm giảm có ý nghĩa tỷ lệ tử vong do mọi nguyên nhân, tử vong do tim mạch, và các biến cố tim mạch, bao gồm nhồi máu cơ tim, so với nhóm chứng.
Phân tích hồi quy tổng hợp là một phương pháp hợp lý để tìm hiểu liệu các chất điều hòa tác động tiềm năng có thể giải thích sự không đồng nhất của tác động điều trị nào giữa các nghiên cứu không. Nhìn chung không nên dùng phân tích hồi quy tổng hợp khi có ít hơn 10 nghiên cứu trong phân tích. Vậy nên, phân tích dưới nhóm và hồi quy tổng hợp của chúng tôi chỉ có khả năng trong các thử nghiệm so sánh ƯCMC với nhóm đối chứng, vì lợi ích của nhóm thuốc này đối với tử vong do mọi nguyên nhân và tử vong do tim mạch. Thuốc ƯCMC có thể có những lợi ích riêng biệt đối với các tình trạng sinh lý bệnh của ĐTĐ. Cơ sở sinh học hợp lý cho những lợi ích của ƯCMC, chứ không phải ƯCTT, đối với tác động bảo vệ tim dường như liên quan đến sự đối kháng angiotensin (1-7) và bradykinin.8,17 Hai yếu tố này xảy ra với ƯCMC, chứ không phải ƯCTT, và tính chọn lọc của ƯCTT có thể không cần thiết là một lợi thế. Trong nghiên cứu hiện tại xem xét điều trị ƯCTT, có sự không đồng nhất có ý nghĩa đối với tử vong do tim mạch trên các bệnh nhân ĐTĐ (I2 = 61%). Theo nghiên cứu của chúng tôi, ƯCTT có liên quan đến khuynh hướng có nhiều biến cố tim mạch gây tử vong hơn so với giả dược (RR, 1.90). Sự không đồng nhất này chủ yếu là do nghiên cứu phụ LIFE28 và 2 thử nghiệm sử dụng olmesartan.15,47 Nghiên cứu phụ LIFE cho thấy losartan hiệu quả hơn atenolol trong việc làm giảm bệnh tật và tử vong do tim mạch cũng như tử vong do mọi nguyên nhân ở các bệnh nhân ĐTĐ. Sự không đồng nhất quy từ nghiên cứu phụ LIFE có thể liên hệ chặt chẽ với thiết kế nghiên cứu và những quan sát hậu kiểm. Mặt khác, điều trị olmesartan trong nghiên cứu ORIENT47 và ROADMAP15 cho thấy tăng có ý nghĩa nguy cơ tử vong do tim mạch (RR, 4.22) ở những bệnh nhân ĐTĐ. Các kết quả tiết lộ rằng sự không đồng nhất có thể có giữa các ƯCTT khác nhau.
Do tỷ lệ tử vong cao đối với các bệnh nhân ĐTĐ, ƯCMC nên được dùng như điều trị đầu tiên ở nhóm dân số này. DETAIL54 là thử nghiệm duy nhất so sánh các kết cục tim mạch ở những người tham gia bị ĐTĐ được phân nhóm ngẫu nhiên với một ƯCMC hoặc một ƯCTT. Có 21 biến cố tim mạch chính gây tử vong hoặc không tử vong trong số 130 người tham gia dùng enalapril (16.2%) so với 27 biến cố trong số 120 bệnh nhân dùng telmisartan (22.5%). Không có thống kê cho thấy liệu sự khác biệt có ý nghĩa thống kê hay không. Tuy nhiên, các kết quả của thử nghiệm phù hợp với các kết quả của phân tích tổng hợp hiện tại.
Có nhiều hạn chế trong phân tích của chúng tôi. Đầu tiên, hạn chế chính là không so sánh trực tiếp giữa ƯCMC và ƯCTT. Thứ hai, có nhiều khác biệt giữa các dân số được nghiên cứu. Ví dụ, các thử nghiệm dùng các ƯCMC hoặc ƯCTT khác nhau, mục tiêu hemoglobin A1C và huyết áp khác nhau, liều thuốc đối chứng và thuốc chủ động khác nhau, và thời gian theo dõi và liệu pháp nền khác nhau. Cuối cùng, những thử nghiệm ƯCMC và ƯCTT không tương đương nhau. Nhóm ƯCMC gồm nhiều nghiên cứu hơn (23 so với 13) và dân số nhiều hơn (32.827 so với 23.867). Hơn nữa, đặc điểm dân số đã tuyển vào các thử nghiệm ƯCMC và ƯCTT khác nhau. Nhiều bệnh nhân ĐTĐ kèm bệnh mạch vành hoặc xơ vữa động mạch được đưa vào các thử nghiệm ƯCMC nhiều hơn các thử nghiệm ƯCTT. Phân tầng bằng chứng hiện tại có khuynh hướng đặt mạng lưới phân tích tổng hợp bên dưới chứng cứ trực tiếp bởi vì những so sánh không trực tiếp có thể có những sai lệch tương tự như trong các nghiên cứu quan sát.62 Cơ quan Dược phẩm và Công nghệ về sức khỏe Canada63 chỉ cho phép mạng lưới phân tích tổng hợp như một phân tích hỗ trợ hoặc nhạy để bổ sung cho các bằng chứng trực tiếp.
Kết luận
Phân tích tổng hợp của chúng tôi cho thấy rằng ƯCMC làm giảm tử vong do mọi nguyên nhân, tử vong do tim mạch, và các biến cố tim mạch chính ở các bệnh nhân ĐTĐ, trong khi ƯCTT không có tác động có lợi trên những kết cục này. Vậy nên, ƯCMC nên được xem xét như liệu pháp đầu tiên để làm hạn chế mức độ tử vong và bệnh tật trong dân số này.
Nguồn:http://archinte.jamanetwork.com/article.aspx?articleid=1847572&resultClick=3
Tài liệu tham khảo:
1. Mokdad AH, Ford ES, Bowman BA, et al.
Diabetes trends in the US: 1990-1998. Diabetes
Care. 2000;23(9):1278-1283.
2. Wild S, Roglic G, Green A, Sicree R, King H. Global
prevalence of diabetes: estimates for the year
2000 and projections for 2030. Diabetes Care.
2004;27(5):1047-1053.
3. International Diabetes Federation. The Diabetes
Atlas. 4th ed. Brussels: International Diabetes
Federation; 2009.
4. Lloyd-Jones D, Adams RJ, Brown TM, et al;
Writing Group Members; American Heart
Association Statistics Committee and Stroke
Statistics Subcommittee. Heart disease and stroke
statistics—2010 update: a report from the American
Heart Association. Circulation. 2010;121(7):e46-
e215. doi:10.1161/CIRCULATIONAHA.109.192667.
5. Schroll M, Larsen S. A ten-year prospective
study, 1964-1974, of cardiovascular risk factors in
men and women from the Glostrup population born
in 1914: multivariate analyses. Dan Med Bull.
1981;28(6):236-251.
6. Sarnak MJ, Levey AS, Schoolwerth AC, et al;
American Heart Association Councils on Kidney in
Cardiovascular Disease, High Blood Pressure
Research, Clinical Cardiology, and Epidemiology
and Prevention. Kidney disease as a risk factor for
development of cardiovascular disease:
a statement from the American Heart Association
Councils on Kidney in Cardiovascular Disease, High
Blood Pressure Research, Clinical Cardiology, and
Epidemiology and Prevention. Circulation.
2003;108(17):2154-2169.
7. Ferrario CM, Strawn WB. Role of the
renin-angiotensin-aldosterone system and
proinflammatory mediators in cardiovascular
disease. Am J Cardiol. 2006;98(1):121-128.
8. Rüster C,Wolf G. Renin-angiotensin-aldosterone
system and progression of renal disease. J Am Soc
Nephrol. 2006;17(11):2985-2991.
9. Strippoli GF, Craig M, Deeks JJ, Schena FP, Craig
JC. Effects of angiotensin converting enzyme
inhibitors and angiotensin II receptor antagonists
on mortality and renal outcomes in diabetic
nephropathy: systematic review. BMJ.
2004;329(7470):828. doi:10.1136
/bmj.38237.585000.7C.
10. Ruggenenti P, Perna A, Remuzzi G; Gruppo
Italiano di Studi Epidemiologici in Nefrologia. ACE
inhibitors to prevent end-stage renal disease: when
to start and why possibly never to stop: a post hoc
analysis of the REIN trial results: Ramipril Efficacy in
Nephropathy. J Am Soc Nephrol. 2001;12(12):2832-
2837.
11. Matchar DB, McCrory DC, Orlando LA, et al.
Systematic review: comparative effectiveness of
angiotensin-converting enzyme inhibitors and
angiotensin II receptor blockers for treating
essential hypertension. Ann Intern Med.
2008;148(1):16-29.
12. Lewis EJ, Hunsicker LG, ClarkeWR, et al;
Collaborative Study Group. Renoprotective effect
of the angiotensin-receptor antagonist irbesartan in
patients with nephropathy due to type 2 diabetes.
N Engl J Med. 2001;345(12):851-860.
13. Remuzzi G, MaciaM, Ruggenenti P. Prevention
and treatment of diabetic renal disease in type 2
diabetes: the BENEDICT study. J Am Soc Nephrol.
2006;17(4)(suppl 2):S90-S97.
14. Marre M, Lievre M, Chatellier G, Mann JF, Passa
P, Ménard J; DIABHYCAR Study Investigators.
Effects of low dose ramipril on cardiovascular and
renal outcomes in patients with type 2 diabetes and
raised excretion of urinary albumin: randomised,
double blind, placebo controlled trial (the
DIABHYCAR study). BMJ. 2004;328(7438):
495-502.
15. Haller H, Ito S, Izzo JL Jr, et al; ROADMAP Trial
Investigators. Olmesartan for the delay or
prevention ofmicroalbuminuria in type 2 diabetes.
N Engl J Med. 2011;364(10):907-917.
16. American Diabetes Association. Executive
summary: standards of medical care in
diabetes—2012. Diabetes Care. 2012;35
(suppl 1):S4-S10.
17. Kon V, Fogo A, Ichikawa I. Bradykinin causes
selective efferent arteriolar dilation during
angiotensin I converting enzyme inhibition. Kidney
Int. 1993;44(3):545-550.
18. van Vark LC, Bertrand M, Akkerhuis KM, et al.
Angiotensin-converting enzyme inhibitors reduce
mortality in hypertension: a meta-analysis of
randomized clinical trials of renin-angiotensinaldosterone
system inhibitors involving 158,998
patients. Eur Heart J. 2012;33(16):2088-2097.
19. Liberati A, Altman DG, Tetzlaff J, et al. The
PRISMA statement for reporting systematic reviews
and meta-analyses of studies that evaluate health
care interventions: explanation and elaboration.
Ann Intern Med. 2009;151(4):W65-W94.
20. Juni P, Altman DG, Egger M. Systematic
reviews in health care: assessing the quality of
controlled clinical trials. BMJ. 2001;323:42-46.
21. DerSimonian R, Kacker R. Random-effects
model formeta-analysis of clinical trials: an update.
Contemp Clin Trials. 2007;28(2):105-114.
22. Altman DG, Bland JM. Interaction revisited: the
difference between two estimates. BMJ.
2003;326(7382):219.
23. Cochrane Handbook for Systematic Reviews of
Interventions, Version 5.10. http://handbook
.cochrane.org/. Accessed February 25, 2014.
24. Lindholm LH, Hansson L, Ekbom T, et al; STOP
Hypertension–2 Study Group. Comparison of
antihypertensive treatments in preventing
cardiovascular events in elderly diabetic patients:
results from the Swedish Trial in Old PatientsWith
Hypertension–2. J Hypertens. 2000;18(11):1671-
1675.
25. Lewis EJ, Hunsicker LG, Bain RP, Rohde RD;
Collaborative Study Group. The effect of
angiotensin-converting-enzyme inhibition on
diabetic nephropathy. N Engl J Med.
1993;329(20):1456-1462.
26. Daly CA, Fox KM, RemmeWJ, Bertrand ME,
Ferrari R, Simoons ML; EUROPA Investigators. The
effect of perindopril on cardiovascular morbidity
and mortality in patients with diabetes in the
EUROPA study: results from the PERSUADE
substudy. Eur Heart J. 2005;26(14):1369-1378.
27. Yui Y, Sumiyoshi T, Kodama K, et al. Nifedipine
retard was as effective as angiotensin converting
enzyme inhibitors in preventing cardiac events in
high-risk hypertensive patients with diabetes and
coronary artery disease: the Japan Multicenter
Investigation for Cardiovascular Diseases–B
(JMIC-B) subgroup analysis. Hypertens Res.
2004;27(7):449-456.
28. Lindholm LH, Ibsen H, Dahlöf B, et al; LIFE
Study Group. Cardiovascular morbidity and
mortality in patients with diabetes in the Losartan
Intervention for Endpoint Reduction in
Hypertension Study (LIFE): a randomised trial
against atenolol. Lancet. 2002;359(9311):1004-
1010.
29. Niskanen L, Hedner T, Hansson L, Lanke J,
Niklason A; CAPPP Study Group. Reduced
cardiovascular morbidity and mortality in
hypertensive diabetic patients on first-line therapy
with an ACE inhibitor compared with a
diuretic/_-blocker–based treatment regimen:
a subanalysis of the Captopril Prevention Project.
Diabetes Care. 2001;24(12):2091-2096.
30. Lonn E, Yusuf S, Hoogwerf B, et al; Heart
Outcomes Prevention Evaluation Study
Investigators. Effects of ramipril on cardiovascular
and microvascular outcomes in people with
diabetes mellitus: results of the HOPE study and
MICRO-HOPE substudy. Lancet. 2000;355(9200):
253-259.
31. Tatti P, Pahor M, Byington RP, et al. Outcome
results of the Fosinopril Versus Amlodipine
Cardiovascular Events Randomized Trial (FACET) in
patients with hypertension and NIDDM. Diabetes
Care. 1998;21(4):597-603.
32. UK Prospective Diabetes Study Group. Efficacy
of atenolol and captopril in reducing risk of
macrovascular and microvascular complications in
type 2 diabetes: UKPDS 39. BMJ. 1998;317(7160):
713-720.
33. Estacio RO, Jeffers BW, Hiatt WR, Biggerstaff
SL, Gifford N, Schrier RW. The effect of nisoldipine
as compared with enalapril on cardiovascular
outcomes in patients with non–insulin-dependent
diabetes and hypertension. N Engl J Med.
1998;338(10):645-652.
34. Patel A, MacMahon S, Chalmers J, et al;
ADVANCE Collaborative Group. Effects of a fixed
combination of perindopril and indapamide on
macrovascular and microvascular outcomes in
patients with type 2 diabetes mellitus (the
ADVANCE trial): a randomised controlled trial.
Lancet. 2007;370(9590):829-840.
35. Baba S; J-MIND Study Group. Nifedipine and
enalapril equally reduce the progression of
nephropathy in hypertensive type 2 diabetics.
Diabetes Res Clin Pract. 2001;54(3):191-201.
36. Chan JC, Ko GT, Leung DH, et al. Long-term
effects of angiotensin-converting enzyme inhibition
and metabolic control in hypertensive type 2
diabetic patients. Kidney Int. 2000;57(2):590-600.
37. Fogari R, Preti P, Zoppi A, et al. Effects of
amlodipine fosinopril combination on
microalbuminuria in hypertensive type 2 diabetic
patients. Am J Hypertens. 2002;15(12):1042-1049.
38. Ravid M, Brosh D, Levi Z, Bar-Dayan Y, Ravid D,
Rachmani R. Use of enalapril to attenuate decline in
renal function in normotensive, normoalbuminuric
patients with type 2 diabetes mellitus:
a randomized, controlled trial. Ann Intern Med.
1998;128(12, pt 1):982-988.
39. Nielsen FS, Rossing P, GallMA, Skøtt P, Smidt
UM, Parving HH. Long-term effect of lisinopril and
atenolol on kidney function in hypertensive NIDDM
subjects with diabetic nephropathy. Diabetes.
1997;46(7):1182-1188.
40. Bakris GL, Copley JB, Vicknair N, Sadler R,
Leurgans S. Calcium channel blockers versus other
antihypertensive therapies on progression of
NIDDM associated nephropathy. Kidney Int.
1996;50(5):1641-1650.
41. Bauer JH, Reams GP, Hewett J, et al.
A randomized, double-blind, placebo-controlled
trial to evaluate the effect of enalapril in patients
with clinical diabetic nephropathy. Am J Kidney Dis.
1992;20(5):443-457.
42. Laffel LM, McGill JB, Gans DJ; North American
Microalbuminuria Study Group. The beneficial
effect of angiotensin-converting enzyme inhibition
with captopril on diabetic nephropathy in
normotensive IDDM patients with
microalbuminuria. Am J Med. 1995;99(5):497-504.
43. Nankervis A, Nicholls K, Kilmartin G, Allen P,
Ratnaike S, Martin FI. Effects of perindopril on renal
histomorphometry in diabetic subjects with
microalbuminuria: a 3-year placebo-controlled
biopsy study. Metabolism. 1998;47(12)
(suppl 1):12-15.
44. Parving HH, Hommel E, Damkjaer Nielsen M,
Giese J. Effect of captopril on blood pressure and
kidney function in normotensive insulin dependent
diabetics with nephropathy. BMJ.
1989;299(6698):533-536.
45. Sano T, Kawamura T, Matsumae H, et al. Effects
of long-term enalapril treatment on persistent
micro-albuminuria in well-controlled hypertensive
and normotensive NIDDM patients. Diabetes Care.
1994;17(5):420-424.
46. Brenner BM, Cooper ME, de Zeeuw D, et al;
RENAAL Study Investigators. Effects of losartan on
renal and cardiovascular outcomes in patients with
type 2 diabetes and nephropathy. N Engl J Med.
2001;345(12):861-869.
47. Imai E, Chan JC, Ito S, et al; ORIENT Study
Investigators. Effects of olmesartan on renal and
cardiovascular outcomes in type 2 diabetes with
overt nephropathy: a multicentre, randomised,
placebo-controlled study. Diabetologia.
2011;54(12):2978-2986.
48. Parving HH, Lehnert H, Bröchner-Mortensen J,
Gomis R, Andersen S, Arner P; Irbesartan in Patients
with Type 2 Diabetes and Microalbuminuria Study
Group. The effect of irbesartan on the development
of diabetic nephropathy in patients with type 2
diabetes. N Engl J Med. 2001;345(12):870-878.
49. Bilous R, Chaturvedi N, Sjølie AK, et al. Effect of
candesartan onmicroalbuminuria and albumin
excretion rate in diabetes: three randomized trials.
Ann Intern Med. 2009;151(1):11-20, W3-W4.
50. Sjølie AK, Klein R, Porta M, et al; DIRECT
Programme Study Group. Effect of candesartan on
progression and regression of retinopathy in type 2
diabetes (DIRECT-Protect 2): a randomised
placebo-controlled trial. Lancet. 2008;372(9647):
1385-1393.
51. Nakao K, Hirata M, Oba K, et al; CASE-J Trial
Group. Role of diabetes and obesity in outcomes of
the Candesartan Antihypertensive Survival
Evaluation in Japan (CASE-J) trial. Hypertens Res.
2010;33(6):600-606.
52. Yusuf S, Diener HC, Sacco RL, et al; PRoFESS
Study Group. Telmisartan to prevent recurrent
stroke and cardiovascular events. N Engl J Med.
2008;359(12):1225-1237.
53. Trenkwalder P, Elmfeldt D, Hofman A, et al;
Study on Cognition and Prognosis in the Elderly
(SCOPE). The Study on Cognition and Prognosis in
the Elderly (SCOPE)—major CV events and stroke in
subgroups of patients. Blood Press.
2005;14(1):31-37.
54. Barnett AH, Bain SC, Bouter P, et al; Diabetics
Exposed to Telmisartan and Enalapril Study Group.
Angiotensin-receptor blockade versus
converting-enzyme inhibition in type 2 diabetes
and nephropathy. N Engl J Med. 2004;351(19):1952-
1961.
55. Vejakama P, Thakkinstian A, Lertrattananon D,
Ingsathit A, Ngarmukos C, Attia J. Reno-protective
effects of renin-angiotensin system blockade in
type 2 diabetic patients: a systematic review and
networkmeta-analysis. Diabetologia.
2012;55(3):566-578.
56. Sarafidis PA, Stafylas PC, Kanaki AI, Lasaridis
AN. Effects of renin-angiotensin system blockers on
renal outcomes and all-cause mortality in patients
with diabetic nephropathy: an updated
meta-analysis. Am J Hypertens. 2008;21(8):
922-929.
57. Hirst JA, Taylor KS, Stevens RJ, et al. The
impact of renin-angiotensin-aldosterone system
inhibitors on type 1 and type 2 diabetic patients
with and without early diabetic nephropathy.
Kidney Int. 2012;81(7):674-683.
58. Nakao YM, Teramukai S, Tanaka S, et al. Effects
of renin-angiotensin system blockades on
cardiovascular outcomes in patients with diabetes
mellitus: a systematic review and meta-analysis.
Diabetes Res Clin Pract. 2012;96(1):68-75.
59. Law MR, Morris JK,Wald NJ. Use of blood
pressure lowering drugs in the prevention of
cardiovascular disease: meta-analysis of 147
randomised trials in the context of expectations
from prospective epidemiological studies. BMJ.
2009;338:b1665.
60. Lv J, Perkovic V, Foote CV, Craig ME, Craig JC,
Strippoli GF. Antihypertensive agents for
preventing diabetic kidney disease. Cochrane
Database Syst Rev. 2012;12:CD004136.
61. Salanti G. Indirect and mixed-treatment
comparison, network, or multiple-treatments
meta-analysis: many names, many benefits, many
concerns for the next generation evidence
synthesis tool. Res SynthesisMethods.
2012;3(2):80-97. doi:10.1002/jrsm.1037.
62. Cipriani A, Higgins JP, Geddes JR, Salanti G.
Conceptual and technical challenges in network
meta-analysis. Ann Intern Med. 2013;159(2):130-137.
63. Wells GA, Sultan SA, Chen L, Khan M, Goyle D.
Indirect Evidence: Indirect Treatment Comparisons
in Meta-analysis. Ottawa, ON: Canadian Agency for
Drugs and Technologies in Health; 2009.







