Tóm tắt: Sốc điện đảo nhịp là một phương pháp đảo nhịp được áp dụng từ lâu để điều trị rung nhĩ mạn tính không do bệnh van tim và bệnh tim bẩm sinh. Một số nghiên cứu lớn như nghiên cứu AFFIRM hay AF-CHF đã chứng minh hiệu quả của đảo nhịp trong rung nhĩ.
Đỗ Văn Chiến
Vũ Điện Biên
Viện Tim mạch, Bệnh viện TƯQĐ 108
Tóm tắt: Sốc điện đảo nhịp là một phương pháp đảo nhịp được áp dụng từ lâu để điều trị rung nhĩ mạn tính không do bệnh van tim và bệnh tim bẩm sinh. Một số nghiên cứu lớn như nghiên cứu AFFIRM hay AF-CHF đã chứng minh hiệu quả của đảo nhịp trong rung nhĩ. Tuy nhiên tỉ lệ tái phát rung nhĩ sau điều trị bằng sốc điện còn cao. Tỉ lệ thành công của đảo nhịp bằng sốc điện phụ thuộc vào việc lựa chọn đối tượng bệnh nhân. Một số yếu tố đã được chứng minh là có giá trị tiên lượng thành công như tuổi, thời gian mắc rung nhĩ hay kích thước nhĩ trái. Ngày nay người ta còn quan tâm nhiều đến các yếu tố khác như CRP, Homocystein, proBNP hoặc một số chỉ số siêu âm sức căng, vận tốc căng, siêu âm đánh dấu mô nhĩ trái và siêu âm qua thực quản đánh giá kích thước và chức năng tiểu nhĩ trái giúp lựa chọn bệnh nhân để sốc điện với tỉ lệ thành công cao hơn.
1. Lịch sử sốc điện đảo nhịp
Sử dụng nguồn điện một pha để chuyển những rối loạn nhịp tim về nhịp xoang đã được biết đến từ rất lâu. Năm 1775 Abildgard lần đầu tiên thực hiện thí nghiệm thành công trên động vật. Ông dùng dòng điện làm ngừng tim gà thực nghiệm và cũng dùng chính dòng điện đó đánh sốc để cứu sống nó.[17] Năm 1947 Beck là tác giả đầu tiên sử dụng sốc điện trên người cứu sống một trường hợp bệnh nhân 14 tuổi có rung thất trong khi phẫu thuật trên tim. Năm 1961 Lown là người đầu tiên sử dụng sốc điện đồng bộ để chuyển rung nhĩ và rung thất về nhịp xoang. Sốc điện đảo nhịp bằng nguồn điện một pha hoặc hai pha để đưa rung nhĩ về nhịp xoang khác biệt với sốc điện trong rung thất và đảo nhịp bằng thuốc. Ưu điểm của sốc điện đảo nhịp là tránh được tác dụng phụ của các thuốc chống loạn nhịp. Tuy nhiên nhược điểm của sốc điện là có thể gây rung thất. Các máy sốc đảo nhịp dựa trên sự di chuyển của nguồn điện với mức năng lượng nhất định giữa hai bản điện cực và đồng bộ với sóng R hoặc S trên điện tim để tránh gây rung thất. Đỉnh của sóng T là sự kết thúc của quá trình trơ tuyệt đối và các sợi cơ tim trong giai đoạn này đang chuyển sang trạng thái tái cực nên rất dễ bị tổn thương và gây rung thất. Sốc điện thường gây đau và tác động đến tâm lý nên bệnh nhân phải được gây mê khi thực hiện kỹ thuật. Bản cực điện được đặt ở vị trí nền tim và mỏm tim hoặc ở trước tim và sau tim. Các nghiên cứu cho thấy việc đặt điện cực ở vị trí trước và sau sẽ giảm được cường độ dòng điện. Hiện nay người ta sử dụng chủ yếu các máy sốc hai pha nên sốc điện một pha không còn nhiều ứng dụng. Bardy và cs [5] chỉ ra rằng năng lượng 130J của dòng điện 2 pha tương đương 200J của dòng điện 1 pha và có hiệu quả như nhau (86% về nhịp xoang). Câu hỏi đặt ra là mức năng lượng bao nhiêu thì đủ để đảo nhịp? Ricard và cs [6] nghiên cứu trên 200 bệnh nhân có rung nhĩ mạn tính và các tác giả đã chỉ ra có đến 50% bệnh nhân thành công với mức dưới 100J và 75% thành công ở mức 200J và họ khuyến cáo dùng mức năng lượng thấp nhất là 50J. Joglar và cộng sự [7] lại sự dụng phương pháp nghiên cứu khác. Các tác giả chia ngẫu nhiên các bệnh nhân với mực năng lượng 100J, 200J và 360J và nhận thấy ở mức năng lượng 100J và 200J tỉ lệ thành công thấp hơn so với 360J vì vậy các tác giả khuyến cáo nên bắt đầu với mức 360J. Tuy nhiên phần lớn các trung tâm tim mạch trên thế giới đều áp dụng phương pháp nâng mức năng lượng từ từ cho đến khi đạt được hiệu quả cần thiết.
Sốc đảo nhịp đồng bộ là một phương pháp điều trị khá dễ dàng và hiệu quả. Phương pháp này được thực hiện trong một số trường hợp sau (Khuyến cáo về điều trị rung nhĩ mạn tính của Hội Tim Châu Âu năm 2010):
1. Sốc điện đảo nhịp cấp cứu được chỉ định bệnh nhân rung nhĩ có đáp ứng thất nhanh không đáp ứng với điều trị bằng thuốc và có triệu chứng thiếu máu tiếp diễn, tụt huyết áp, đau tức ngực hoặc có suy tim.(I,C)
2. Sốc điện đảo nhịp cấp cứu ở bệnh nhân rung nhĩ có hội chứng WPW khi nhịp thất nhanh và có huyết động không ổn định.(I,B)
3. Sốc điện đảo nhịp được chọn lọc như một biện pháp điều trị ban đầu trong chiến lược kiểm soát nhịp thất ở bệnh nhân rung nhĩ mạn tính.(IIa,B)
4. Có thể điều trị bằng amiodarone, flecainide, ibutilide, sotalol trước khi sốc điện nhằm nâng cao tỉ lệ thành công của sốc điện (IIa,B)
5. Chưa đủ bằng chứng về sử dụng thuốc ức chế thụ thể bêta, ức chế kênh canxi để nâng cao hiệu quả của sốc điện, các thuốc này được sử dụng chủ yếu với mục đích kiểm soát nhịp thất.(IIb,C)
2. Các bằng chứng lâm sàng qua các nghiên cứu điều trị rung nhĩ mạn tính
Trên các diễn đàn về điều trị rung nhĩ, đến nay vẫn có tranh luận hết sức sôi nổi diễn ra. Một số tác giả cho rằng kiểm soát nhịp thất có hiệu quả không kém gì so với chuyển về nhịp xoang. Một số khác lại ủng hộ việc đảo nhịp. Hai nghiên cứu đa trung tâm lớn là nghiên cứu AFFIRM và AF-CHF đã được thiết kế nhằm trả lời câu hỏi: chiến lược nào tốt hơn trong rung nhĩ mạn tính, đảo nhịp hay kiểm soát nhịp thất?
Nghiên cứu AFFIRM
The Atrial Fibrilation Follow-up Investigation of Rhythm Management (AFFIRM) là một thử nghiệm ngẫu nhiên, đa trung tâm với số lượng bệnh nhân lớn (4060 bệnh nhân), tuổi trung bình 70, với mục đích so sánh giữa chiến lược điều trị kiểm soát nhịp thất hoặc đảo nhịp ở bệnh nhân rung nhĩ [6].
Thiết kế nghiên cứu: bệnh nhân trên 65 tuổi có rung nhĩ dai dẳng, nguy cơ cao đột quị hoặc tử vong, không có chống chỉ định với các thuốc chống đông. Tất cả các bệnh nhân được phân ngẫu nhiên để điều trị đảo nhịp hoặc kiểm soát nhịp thất. Nhóm điều trị đảo nhịp có thể sử dụng phương pháp sốc điện hoặc các thuốc chống loạn nhịp. Các thuốc sử dụng để đảo nhịp có thể một trong số thuốc như amiodarone, disopyramide, flecainide, moricizine, procainamide, propafenone, quinidine, sotalol hoặc phối hợp các thuốc nói trên. Nhóm điều trị kiểm soát nhịp thất được sử dụng một trong số các thuốc như ức chế beta, ức chế canxi, digoxin hoặc phối hợp các thuốc trên với mục đích đạt được nhịp thất < 80 ck/phút khi nghỉ hoặc > 110 ck/phút trong nghiệm pháp đi bộ 6 phút. Tất cả bệnh nhân trong nghiên cứu đều được sử dụng thuốc Wafarin với mục tiêu INR=2-3. Riêng ở nhóm đảo nhịp, khi nhịp xoang được duy trì có thể dừng chống đông sau 4 tuần -12 tuần và những tuần tiếp theo với thuốc chống loạn nhịp. Nhóm điều trị kiểm soát tần số vẫn tiếp tục dùng thuốc chống đông theo khuyến cáo.
Kết quả: Trong số 4060 bệnh nhân được đưa vào hai nhóm nghiên cứu không có sự khác biệt có ý nghĩa về tuổi, giới và các chỉ số cận lâm sàng. Thời gian theo dõi bệnh nhân trung bình 3,5 năm. Dựa trên tiêu chí chính là tử vong do mọi nguyên nhân, nghiên cứu cho thấy việc chuyển về nhịp xoang không có lợi thế hơn so với kiểm soát nhịp thất. Tỷ lệ rủi ro (HR) của nhóm điều trị đảo nhịp cao hơn so với nhóm kiểm soát tần số sau khi đã hiệu chỉnh với tuổi, bệnh ĐMV, suy tim, chức năng tống máu thất trái (EF) và THA, mặc dù chưa có ý nghĩa thống kê (p=0,07). Tuy nhiên các tác giả khẳng định chuyển về nhịp xoang có lợi thế hơn kiểm soát tần số là ít xảy ra nguy cơ do các tác dụng bất lợi của các thuốc chống loạn nhịp. Thuốc chống đông phải được tiếp tục sử dụng ở các bệnh nhân có nguy cơ đột quị hoặc tử vong cao.
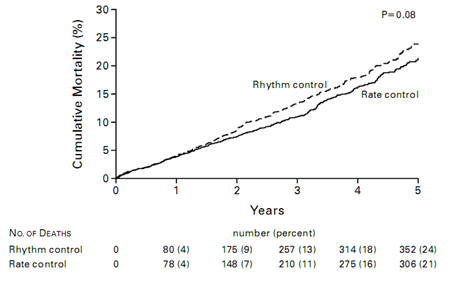
So sánh tỉ lệ tử vong do mọi nguyên nhân giữa hai nhóm nghiên cứu
Nghiên cứu AF-CHF
AF-CHF là một thử nghiệm ngẫu nhiên, đa trung tâm trên 1376 bệnh nhân rung nhĩ có suy tim với EF< 35%.[4] Nghiên cứu được thực hiện tại các trung tâm Tim mạch ở Mỹ, Canada và một số nước Châu Âu do Viện Tim Montreal tài trợ với mục đích so sánh chiến lược đảo nhịp và kiểm soát nhịp thất ở bệnh nhân rung nhĩ có suy tim.
Thiết kế nghiên cứu: Bệnh nhân rung nhĩ có chức năng thất trái EF< 35% được đo bằng siêu âm tim hoặc chụp xạ cơ tim < 6 tháng trước khi tham gia nghiên cứu. Các bệnh nhân được phân ngẫu nhiên vào nhóm đảo nhịp hoặc nhóm kiểm soát nhịp thất. Ở nhóm đảo nhịp phương pháp chính để đảo nhịp là sốc điện và các thuốc được dùng để duy trì nhịp xoang sau sốc điện là amiodarone, sotalol hoặc dofetilide. Kiểm soát nhịp thất được thực hiện bằng thuốc ức chế beta, ức chế chẹn canxi hoặc digoxin với tiêu chí nhịp tim lúc nghỉ <80ck/phút hoặc<110 ck/phút trong nghiệm pháp đi bộ 6 phút.
Kết quả: Tổng số 1376 bệnh nhân được đưa vào nghiên cứu với 682 bệnh nhân được đưa về nhịp xoang và 694 bệnh nhân được kiểm soát nhịp thất. Thời gian theo dõi trung bình 36 tháng.
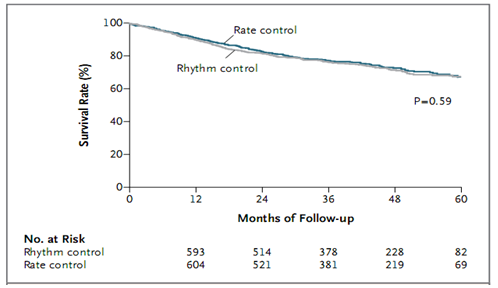
Đường Kaplan-Mayer đánh giá tử vong do nguyên nhân tim mạch.
Dựa trên các tiêu chí tử vong do mọi nguyên nhân các tác giả đưa ra kết luận rằng việc đảo nhịp ở bệnh nhân rung nhĩ có suy tim không cải thiện tử vong hơn so với kiểm soát nhịp thất.
Hai nghiên cứu AFFIRM và AF-CHF được thực hiện ở hai đối tượng bệnh nhân khác nhau và có các tiêu chí lựa chọn khác nhau nhưng đều có chung một kết luận rằng không có sự khác biệt trong cải thiện tỷ lệ sống còn giữa điều trị đảo nhịp và kiểm soát nhịp thất cho bệnh nhân rung nhĩ mạn tính. Tuy nhiên xét về một số khía cạnh khác đảo nhịp cho bệnh nhân rung nhĩ vẫn mang lại một số lợi ích mà trong hai nghiên cứu tiêu biểu cho thấy:
1. Giảm triệu chứng do rung nhĩ gây ra đặc biệt là khi rung nhĩ nhịp nhanh không kiểm soát được bằng thuốc.
2. Cải thiện huyết động nhờ việc kéo dài thời kỳ tâm trương của thất trái.
3. Không phải sử dụng các thuốc chống loạn nhịp lâu dài và tránh được các phản ứng bất lợi do chính các thuốc chống loạn nhịp gây ra (proarrhythmic).
4. Có thể ngừng được các thuốc kháng vitamin K sau khi tái lập được nhịp xoang và tránh được nguy cơ xuất huyết do các thuốc chống đông khi sử dụng lâu dài trong điều trị rung nhĩ mạn tính.
3. Các yếu tố dự báo hiệu quả của sốc điện đảo nhịp
Hiện nay trên thế giới có nhiều tác giả đang tập trung nghiên cứu các yếu tố dự báo sốc điện thành công ở bệnh nhân rung nhĩ. Malouf J.F và cs [8] đã nghiên cứu trên 67 bệnh nhân được sốc điện và nhận thấy C-reactive protein (CRP) là yếu tố độc lập dự báo sốc điện thành công (OR 2.19; 95% CI 1.05-4.55; p=0.036). Naji F và cs [9] nhận xét 83 trường hợp sốc điện đảo nhịp và nhận thấy nồng độ Homocystein máu ≤ 14.4 µmol/l (OR 0.39, 95% CI0.21-0.73; p=0,001) trước sốc điện có giá trị dự báo sốc điện thành công.
Tuy nhiên trong thực hành lâm sàng, các trung tâm tim mạch lớn chủ yếu dựa vào các chỉ số siêu âm tim để đánh giá khả năng thành công của sốc điện và tái phát rung nhĩ sau sốc điện. Trong số các chỉ số siêu âm tim, kích thước và chức năng nhĩ trái được coi là có ý nghĩa nhất. Giãn nhĩ trái từ lâu đã được biết đến như một dấu hiệu của suy chức năng tâm trương. Nghiên cứu của Hussein và cs [13] cho thấy diện tích nhĩ trái, chức năng tâm thu thất trái (EF) và nồng độ pro-BNP trước thủ thuật được xem là những yếu tố dự báo tái phát rung nhĩ sau đốt rung nhĩ bằng sóng cao tần. Chúng ta đều biết rằng nồng độ BNP có liên quan chặt với kích thước nhĩ trái và thất trái. Ở những bệnh nhân rung nhĩ tái phát có nhĩ trái lớn hơn, vận tốc sóng E lớn và tỉ lệ E/e’ tăng hơn so với nhóm duy trì được nhịp xoang. Tuy nhiên ngoài kích thước nhĩ trái cần phải đánh giá chức năng nhĩ trái tỉ mỉ hơn. Marchese và cs [14] theo dõi 411 bệnh nhân sốc điện thành công trên chỉ số thể tích nhĩ trái (iLAV). Trong số 250 bệnh nhân (60,8%) có tái phát rung nhĩ sau 6 tháng chỉ số iLAV cao hơn hẳn so với nhóm giữ được nhịp xoang. Trong phân tích của mình tác giả cho rằng cứ tăng 1ml/m2 iLAV làm tăng 21% tỉ lệ tái phát rung nhĩ. Các tác giả cho rằng iLAV=33.5ml/m2 có giá trị dự báo tái phát rung nhĩ với độ nhạy 83% và độ đặc hiệu 76%. Chỉ số Doppler mô E/e’ (vận tốc Doppler mô trung bình tại thành bên và vách liên thất) là một chỉ số quan trọng đánh giá mức độ suy tim tâm trương. Vai trò của E/e’ trong dự báo sốc điện thành công được Caputo M [15] nghiên cứu và cho thấy E/e’ có giá trị dự báo rung nhĩ tái phát sớm và muộn. Giá trị E/e’ tăng (5,6; 8,1 và 10,5) sẽ tăng nguy cơ tái phát rung nhĩ (lần lượt 25%, 50% và 75%).
Phương pháp đánh giá sức căng và tốc độ căng nhĩ trái cũng đang được nghiên cứu nhằm tìm ra giá trị dự báo tốt nhất để duy trì nhịp xoang. Tian Wang và cs [16] nghiên cứu trên 67 bệnh nhân cho thấy tốc độ căng đầu tâm trương (Esr) và đường kính ngang của nhĩ trái (LADtr) là những chỉ số độc lập dự báo rung nhĩ tái phát (theo thứ tự HR= 0,36; 95% CI: 0,14-0,88 và HR= 2,85; 95% CI: 1,33-6,10).
Gần đây một phương pháp siêu âm mới ra đời dựa trên cơ sở phân tích hiệu chỉnh các điểm màu đại diện cho các tổ chức được đánh dấu qua từng khung hình của chu chuyển tim trên 2-D và 3-D được gọi là “speckle tracking” (tạm dịch là siêu âm đánh dấu mô cơ tim) để đánh giá chức năng toàn bộ và chức năng vùng của thất trái, thất phải và nhĩ trái. Đây là một phương pháp đầy hứa hẹn trong tương lai để đánh giá chức năng nhĩ trái và qua đó tìm hiểu yếu tố tái cấu trúc nhĩ trái giúp người thầy thuốc lựa chọn bệnh nhân thích hợp để đảo nhịp và duy trì nhịp xoang.
Hiện nay siêu âm qua thực quản vẫn là một phương pháp đánh giá bệnh nhân rung nhĩ mạn tính dự kiến điều trị sốc điện đảo nhịp. Một trong số các nguy cơ trước, trong và sau sốc đảo nhịp điều trị rung nhĩ mạn tính là đột quị não và hoặc biến chứng tắc mạch ngoại vi. Theo khuyến cáo trước đây tất cả các bệnh nhân trước khi sốc điện đều phải được điều trị chống đông 3 tuần với INR=2-3. Hiện nay các khuyến cáo mới đều thống nhất rằng sử dụng thuốc chống đông trong sốc điện đảo nhịp dựa trên kết quả siêu âm tim qua thực quản tốt hơn là điều trị chống đông thường qui.[10] Siêu âm qua thực quản giúp chúng ta đánh giá được hình thái và chức năng của tiểu nhĩ trái (LAA) qua đó giúp chúng ta loại trừ được huyết khối, khả năng hình thành cục máu đông và dự báo đảo nhịp thành công. Vận tốc các sóng trong tiểu nhĩ trái cho phép chúng ta dự báo được sự hình thành huyết khối ở tiểu nhĩ trái. Huyết khối tiểu nhĩ trái được tìm thấy nhiều hơn ở bệnh nhân có vận tốc sóng tiểu nhĩ (< 20cm/s) so với nhóm có vận tốc lớn hơn( 17% so với 5%).[11] Hiện tượng “đờ” (stunning) cơ nhĩ và tiểu nhĩ trái sau sốc điện rất thường gặp. Mặc dù đã đưa được về nhịp xoang nhưng khi siêu âm qua thực quản chúng ta có thể thấy là vận tốc sóng tiểu nhĩ trái giảm hơn so với trước sốc điện. Điều này làm tăng nguy cơ hình thành các cục máu đông sau sốc điện đảo nhịp. Các nghiên cứu gần đây cho thấy siêu âm tim qua thực quản đánh giá nhĩ trái giúp chúng ta dự báo thành công sốc điện đảo nhịp điều trị rung nhĩ. Sóng tiểu nhĩ cũng có thể dự báo sốc điện thành công trong ngắn hạn và duy trì khả năng thành công dài hạn. Vận tốc sóng tiểu nhĩ lớn hơn 20cm/s được xem là yếu tố dự báo sốc điện thành công. Điều này có thể là do vận tốc sóng tiểu nhĩ có liên quan chặt chẽ đến kích thước nhĩ trái, tiểu nhĩ trái và áp lực đổ đầy nhĩ trái.[12]
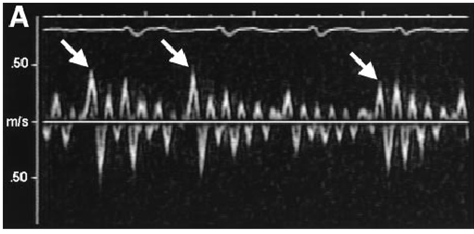
Sóng tiểu nhĩ ở bệnh nhân rung nhĩ
Kết luận: Việc đưa rung nhĩ trở về nhịp xoang và duy trì nhịp xoang vẫn đang là vấn đề có nhiều ý kiến trái ngược. Sốc điện đảo nhịp được xem là phương pháp đảo nhịp phổ biến và hiệu quả trong điều trị rung nhĩ mạn tính không do bệnh van tim. Tuy nhiên việc lựa chọn bệnh nhân rung nhĩ mạn tính để sốc điện đảo nhịp cần thực hiện đúng qui trình để tránh thất bại và tái phát. Có rất nhiều tiêu chí lâm sàng và cận lâm sàng trong đó các chỉ số như BNP, Homocystein, C-reactive protein và các chỉ số siêu âm tim qua thành ngực và thực quản có ý nghĩa quan trọng trong dự báo thành công của đảo nhịp.
Tài liệu tham khảo.
1. ACC/AHA/ESC 2006 Guidelines for management of patients with atrial fibrilation. Circulation 2006; 114; 700-752.
2. Brian Olshansky et al The atrial fibrilation follow-up investigation of rhythm management (AFFIRM) study. J Am Col Cardio 2004;7;3
3. Khuyến cáo của hội tim mạch Việt Nam về các bệnh lý tim mạch 2010.
4. Dennis Roy et al. Rhythm control versus rate control for atrial fibrilation and heart failure. N Engl J Med 2008; 358:2667-2677;
5. Bardy G.H et al. Multicenter comparison of truncated biphasic shocks and standard damped sine wave monophasic shocks for transthoracic ventricular defibrilation. Circulation 1996;94(10):2507-14
6. Ricard P et al. Prospective assessment of the minimum energy needed for external electrical cardioversion of atrial fibrilation. Am J Cardio 1997;79(6)815-6.
7. Jogler et al. Initial energy for elective external cardioversion of persistent atrial fibrilation. Am J Cardio 200;86(3):348-50.
8. Joseph F Malouf et al. High sensitivity C-reative protein: a novel predictor for reccurence of atrial fibrilation after successful cardioversion. J Am Col Cardio 2005;46(7)
9. Franjo Naji et al. High homocystein levels predict the reccurence of atrial fibrilation after successful cardioversion. In Heart J 201; 51:30-33
10. Klein A.L et al. Efficacy of transesophageal echocardiography-guided cardioversion of patients with atrial fibrilation at 6 month: a randomized controlled trial. Am Heart J 2006;151; 380-9.







