MỞ ĐẦU
Tắc stent do huyết khối là một biến chứng nghiêm trọng sau đặt stent động mạch vành (ĐMV), mặc dù tỉ lệ tắc stent do huyết khối thấp vào khoảng 0.5 – 1% trong 1 năm [1], [2],[3], [4],[7].
ThS Trần Hòa
PGS Châu Ngọc Hoa
Huyết khối tắc stent có thể cấp tính (trong vòng 24 giờ), bán cấp (trong vòng 1 – 30 ngày), trễ (trong vòng 1 tháng – 1 năm) hoặc rất trễ (sau 1 năm) sau khi đặt stent [6]. Trong một nghiên cứu với 437 trong tổng số 21009 bệnh nhân (chiếm 2.1%) chắc chắn bị huyết khối tắc stent trong thời gian theo dõi trung bình 31 tháng, với tắc stent cấp chiếm 32%, bán cấp 41%, trễ 13% và rất trễ 14% [6]. Phân tích gộp các thử nghiệm lâm sàng ngẫu nhiên ghi nhận tỉ lệ huyết tắc stent phóng thích thuốc ở thời điểm 30 ngày là 0.58% [28] và 1 năm là 0.7% [9]. Trong một phân tích gộp 28 thử nghiệm lâm sàng ngẫu nhiên (n=10727), tỉ lệ huyết tắc stent rất trễ (sau 1 năm) ở nhóm DES (0.7%) cao hơn nhóm stent thường (0.1%), với RR = 4.57, p = 0.006) [10]. Như vậy, stent phóng thích thuốc có tỉ lệ huyết tắc stent trong vòng 1 năm tương tự stent thường nhưng nguy cơ huyết tắc stent rất trễ (sau 1 năm) nhiều hơn [8].
Biểu hiện thường gặp nhất của huyết khối tắc stent là nhồi máu cơ tim cấp [3]. Điều trị huyết khối tắc stent hầu như luôn luôn cần phải tái thông lập lại, mặc dù kết quả tái thông tối ưu chỉ đạt được ở hai phần ba bệnh nhân. Tỉ lệ tử vong trong 30 ngày liên quan đến huyết khối tắc stent từ 10 – 25%. Hơn nữa, khoảng 20% số bệnh nhân bị huyết khối tắc stent lần đầu có thể sẽ bị tái phát trong vòng 2 năm [3]. Các định nghĩa và các yếu tố nguy cơ về huyết khối tắc stentđược trình bày trong các Bảng 1 và 2.
Bảng 1. Các định nghĩa về huyết khối tắc stent [5]
|
Thuật ngữ |
Định nghĩa |
|
Chắc chắn tắc stent do huyết khối |
Bằng chứng tắc stent do huyết khối trên hình chụp mạch hoặc tử thiết |
|
Khả năng có tắc stent do huyết khối |
Tử vong không tiên đoán được trong vòng 30 ngày sau đặt stent, hoặc nhồi máu cơ tim ở vùng chi phối bởi đoạn mạch được đặt stent bất kể thời gian nào |
|
Có thể có tắc stent do huyết khối |
Tử vong không rõ nguyên nhân sau 30 ngày cho đến lúc kết thúc theo dõi |
Sinh bệnh học của huyết khối tắc stent khá phức tạp, cho đến nay, người ta cũng chưa biết thật rõ. Có nhiều yếu tố được xem có liên quan đến biến cố này, gồm: cơ địa bệnh nhân, quá trình thủ thuật (gồm việc chọn lựa loại stent) và các yếu tố sau thủ thuật (bao gồm loại thuốc và thời gian sử dụng thuốc kháng tiểu cầu) [4].
Bảng 2. Các yếu tố nguy cơ liên quan đến huyết khối tắc stent [4]
|
Liên quan với stent |
Dị ứng với thuốc hoặc polymer Nội mạc hóa không hoàn toàn Thiết kế stent Stent phủ thuốc |
|
Liên quan với bệnh nhân |
Hội chứng mạch vành cấp Đái tháo đường Suy thận Suy chức năng thất trái Ngưng sớm liệu pháp hai thuốc kháng tiểu cầu Kháng aspirin Kháng clopidogrel Tiền sử chiếu xạ Bệnh ác tính |
|
Liên quan với tổn thương |
Tỉ lệ chiều dài tổn thương/stent Tỉ lệ đường kính mạch/stent Tổn thương phức tạp (phân đôi, tắc mạn tính) Hẹp cầu nối tĩnh mạch |
|
Liên quan với thủ thuật |
Stent không bung hoàn toàn Stent không áp sát vào thành mạch Bóc tách tồn lưu đầu stent |
CHIẾN LƯỢC GIẢM TỈ LỆ TẮC STENT DO HUYẾT KHỐI
Có nhiều chiến lược đã được sử dụng nhằm giảm thiểu tỉ lệ tắc stent do huyết khối [3].
Chọn lựa bệnh nhân
· Đánh giá sự tuân thủ với chế độ điều trị (gồm cả khả năng tuân thủ điều trị kháng tiểu cầu kép)
· Sàng lọc cẩn thận nguy cơ chảy máu (hoặc khả năng dung nạp điều trị kháng tiểu cầu kép)
· Khẳng định là bệnh nhân không có kế hoạch phẩu thuật chương trình trong thời gian gần đây (6 tuần với stent thường (BMS), 6 -12 tháng đối với stent tẩm thuốc (DES))
Chọn loại stent và kỹ thuật bung stent
· Xem xét việcsử dụng các stentđã được chứng minhtỷ lệ huyết khối stent thấpnhất
· Chọn stent với kích thước phù hợp
· Bung stent (deployment) áp lực cao và dùng bóng nong sau
· Bảo đảm không có bóc tách rìa stent
· Bảo đảm dòng chảy thích hợp sau đặt stent
· Tránh sử dụng 2 stent ở sang thương ngã ba (bifurcation lesions) (nếu có thể)
Chăm sóc bệnh nhân chu phẩu và sau thủ thuật
· Sử dụngphác đồ kháng tiểu cầu đường uống mạnh hơn (ví dụ, Prasugrel, Ticagrelor)ở những tình huống lâm sàngthích hợpnhưhội chứng mạch vành cấp tínhvới nguy cơ chảy máuchấp nhận được
· Giáo dục bệnh nhânvà luôn luônnhấn mạnhtầm quan trọng của việc tuân thủ chế độđiều trịkháng tiểu cầu kép
· Nếu cần tiến hành thủ thuật nội soi, nha khoa hay phẩu thuật, nên tiếp tục điều trịkháng tiểu cầu képmà không cần ngưng thuốc, (có tính khả thi đối với hầu hết các phẫu thuật ngoại trừ thủ thuật thần kinh-mạch máu)
VAI TRÒ THUỐC KHÁNG TIỂU CẦU TRONG VIỆC GIẢM TẮC STENT DO HUYẾT KHỐI
Điều trị kháng tiểu cầu là hòn đá tảng trong điều trị bệnh ĐMV nói chung và trong can thiệp ĐMV nói riêng (bệnh ĐMV mạn cũng như Hội chứng mạch vành cấp). Song song với sự phát triển không ngừng của can thiệp ĐMV (từ nong bóng đơn thuần đến can thiệp đặt stent, nhất là stent tẩm thuốc), trị liệu kháng tiểu cầu cũng tiến triển không ngừng trong 20 năm qua với nhiều loại thuốc mới và những thử nghiêm lâm sàng mới: từ đơn trị liệu (aspirin) đến bộ đôi trị liệu (aspirin kết hợp với thienopyridin hoặc kết hợp với non-thienopyridine) và bộ ba trị liệu (aspirin + thienopyridin + kháng thụ thể GP IIb/IIIa) [2].
Việc chọn lựa thuốc kháng tiểu cầu cần thiết phải xét đến sự cân bằng giữa tính hiệu quả và tính an toàn của thuốc. Thuốc kháng tiểu cầu làm giảm các nguy cơ thiếu máu cục bộ (NMCT tái phát, tắc stent) nhưng cũng có thể làm tăng nguy cơ chảy máu. Sự kết hợp aspirin và clopidogrel đã trở thành trị liệu nòng cốt trước, trong và sau can thiệp ĐMV và có lúc, người ta cho rằng đây là một công thức chuẩn lý tưởng không thể thay thế được. Tuy nhiên, sự ra đời của hàng loạt thuốc kháng tiểu cầu mới cùng với nhiều nghiên cứu mới đã công bố cho thấy clopidogrel có một số hạn chế đáng kể liên quan trực tiếp đến đặc tính dược lý học, dược động học và di truyền hay gen [2], [13], [16].
Một số hạn chế của clopidogrel:
1. Clopidogrel có phổ đáp ứng rộng tùy thuộc từng cá nhân.
Ước tính từ nhiều nghiên cứu có khoảng 15 – 48% bệnh nhân có đáp ứng kém hay tình trạng đề kháng với clopidogrel. Năm 2003, nghiên cứu trên 190 bệnh nhân can thiệp ĐMV chọn lọc có đặt stent và đo sự biến thiên của nồng độ kết tập tiểu cầu trước và sau uống 300mg clopidogrel 24 giờ; Gurbel và cộng sự đã nhận thấy có khoảng 31% bệnh nhân có độ biến thiên nồng độ kết tập tiểu cầu < 10%, được gọi là nhóm “đề kháng clopidogrel” [11]. Tính chất biến thiên của đáp ứng clopidogrel phụ thuộc vào nhiều yếu tố: liều nạp cũng như liều duy trì của clopidogrel, thời gian điều trị trước can thiệp, phương pháp đo độ kết tập tiểu cầu, sự tương tác thuốc, tình trạng hấp thu thuốc tại ruột và đặc biệt là tình trạng biến đổi di truyền liên quan đến cytochrome P – 450, một thành phần quan trọng trong chuyển hóa clopidogrel.
2. Hạn chế của clopidogrel liên quan đến di truyền:
Clopidogrel là một tiền chất đòi hỏi phải được chuyển dạng sinh học thành chất chuyển hóa hoạt động nhờ hệ thống men cytochrome P-450 (CYP). CYP2C19, đặc biệt là CYP2C19*2 đóng vai trò quan trọng trong chuyển hóa clopidogrel, đây cũng được xem là allene giảm chức năng “CYP2C19 reduced-function allele” [22]. Người mang kiểu gen này kèm theo giảm thấp mức độ hoạt động chuyển hóa của clopidogrel, giảmchức năng ức chế tiểu cầu dẫn đến làm tăng các biến cố tim mạch do thiếu máu cục bộ liên quan đến sự tạo lập huyết khối sau can thiệp.
Theo một nghiên cứu cho thấy có khoảng 30% người da trắng, 40% người da đen và có đến hơn 55% người đông Á có mang ít nhất một allene của kiểu gen giảm chức năng CYP2C19. Phân tích mẫu DNA của 1477 bệnh nhân trong nghiên cứu TRITON-TIMI 38 (71% HCMVC không ST chênh lên và 29% NMCT cấp ST chênh lên), có 27% số bệnh nhân có mang allene CYP2C19 [13].
Kết quả theo dõi sau 15 tháng điều trị:
Người mang allene CYP2C19 kèm theo tăng nguy cơ biến cố tim mạch chính (tử vong do tim mạch, NMCT cấp hoặc đột quỵ) so với nhóm người không mang allene này có ý nghĩa (12,1 % so với 8% với p = 0,01) (biểu đồ 1).
Đặc biệt, nguy cơ tắc stent do huyết khối ở nhóm mang allene CYP2C19 tăng gấp 3 lần so với nhóm không mang allene này (2,6% so với 0,8% với p = 0,02)[13].
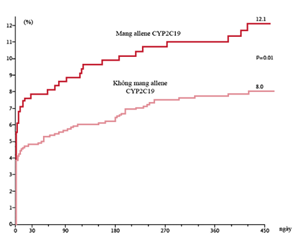
Biểu đồ 1. Người mang kiểu gen CYP2C19 kèm tiên lượng xấu hơn (các biến cố tim mạch chính) người không mang gen này
3. Nguy cơ chảy máu:Với tác dụng ức chế tiểu cầu không hồi phục, clopidogrel có thể làm tăng nguy cơ chảy máu sau mổ bắc cầu ĐMV nếu không được ngưng trước 5 – 7 ngày.
Một số giải pháp khắc phục hạn chế của clopidogrel trong can thiệp ĐMV
Tăng liều nạp cũng như liều duy trì của clopidogrel:
Năm 2005, Gurbel và cộng sự đã thực hiện NC so sánh sự đáp ứng giữa liều nạp 300 mg và 600 mg. Biểu đồ 7 cho thấy có khoảng 28% BN đề kháng hay đáp ứng kém với liều nạp clopidogrel 300 mg, trong khi có khoảng 8% BN đề kháng hay đáp ứng kém với liều nạp 600mg (Biểu đồ 2) [12]. Tăng liều nạp là một trong những phương cách giúp cải thiện tình trạng kém đáp ứng của clopidogrel. Tuy nhiên với liều cao clopidogrel 600 mg vẫn còn một số BN không đáp ứng với thuốc.
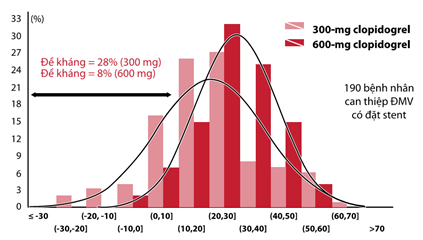
Biểu đồ 2. Tăng liều nạp (600 mg so với 300 mg) làm giảm tỉ lệ đề khángclopidogrel ở bệnh nhân được can thiệp đặt stent [12].
Clopidogrel liều cao (liều nạp và duy trì) trong HCMVC
– Nghiên cứu CURRENT-OASIS 7, so sánh tiên lượng cũng như tính an toàn giữa hai phác đồ clopidogrel trong điều trị Hội chứng mạch vành cấp. Đây là 1 nghiên cứu tiền cứu, mù đôi, thực hiện tại 597 trung tâm ở 39 nước. 25086 bệnh nhân (17232 BN chiếm gần 70% được can thiệp ĐMV và 7855 BN điều trị nội khoa) được phân chia ngẫu nhiên thành 2 nhóm : nhóm điều trị với phác đồ chuẩn với clopidogrel (liều nạp 300mg sau đó 75 mg mỗi ngày) và nhóm dùng clopidogrel liều cao (liều nạp 600 mg ngày thứ 1, sau đó 150 mg từ ngày thứ 2 đến thứ 7, sau đó là 75mg/ngày). Nhóm can thiệp ĐMV (n= 17232), liều gấp đôi clopidogrel (so với liều chuẩn) cải thiện tiên lượng trong 30 ngày theo dõi, với giảm các biến cố tim mạch chính, giảm tỉ lệ NMCT cấp và đặc biệt là giảm thấp nguy cơ tắc stent, đều có ý nghĩa thống kê. Trong khi đó, ở nhóm không can thiệp ĐMV (70% có bệnh ĐMV không có ý nghĩa khi chụp ĐMV hoặc ngưng sớm clopidogrel để mổ bắc cầu ĐMV), việc dùng liều cao clopidogrel không góp phần cải thiện tiên lượng so với nhóm điều trị liều chuẩn. So với nhóm điều trị phác đồ chuẩn, dùng liều gấp đôi clopidogrel làm tăng nguy cơ chảy máu nghiêm trọng (1,9% so với 1,6% với p = 0,04) và tăng nguy cơ phải truyền máu (≥ 2 đơn vị hồng cầu) (2,2% so với 1,7% với p = 0,01). Tuy nhiên, không có sự khác biệt có ý nghĩa về tỉ lệ tai biến chảy máu nội sọ hay chảy máu nguy hiểm đến tính mạng [15].
Với NC CURRENT – OASIS 7, việc dùng liều gấp đôi clopidogrel (liều nạp cũng như liều duy trì) trong HCMVC cần suy xét vì nó không mang lại lợi ích trên đối tượng chỉ điều trị nội khoa đơn thuần và làm tăng nguy cơ chảy máu. Phác đồ này chỉ có lợi trên đối tượng can thiệp ĐMV (giảm nguy cơ tắc stent, NMCT cấp cũng như biến cố gộp).
– Nghiên cứu GRAVITAS cho thấy không có lợi ích về mặt tiên lượng cũng như tắc stent với liều gấp đôi clopidogrel ở bệnh nhân được đặt stent tẩm thuốc (DES) nhưng mức hoạt động tiểu cầu tồn lưu cao (hay còn gọi là đối tượng có tình trạng đề kháng clopidogrel). 5429 BN đang uống clopidogrel 75mg/ngày được đánh giá chức năng tiểu cầu với phân tích VerifyNow từ 12 – 24 giờ sau can thiệp ĐMV, dân số nghiên cứu có nguy cơ tương đối thấp với 60% bệnh ĐMV mạn. Mức hoạt động tiểu cầu tồn lưu cao (khi đơn vị hoạt động tiểu cầu, PRU: platelet reactivity unit > 230) gặp ở 2214 BN chiếm 41% được chia ngẫu nhiên thành 2 nhóm : nhóm 1 tiếp tục điều trị phác đồ chuẩn với 75mg clopidogrel/ngày và nhóm 2 được uống 1 liều nạp 600mg ngày thứ 1 sau đó mỗi ngày 150 mg clopidogrel liên tục trong 6 tháng. Sau 6 tháng theo dõi, biến cố gộp gồm tử vong do tim mạch/NMCT cấp/thuyên tắc stent tương đương giữa hai nhóm, đều 2,3% và cũng không có sự khác biệt về nguy cơ chảy máu [14].
Từ NC CURRENT-OASIS 7 và GRAVITAS, rút ra những kết luận:
– Bệnh nhân HCMVC nhưng chỉ điều trị nội khoa: clopidogrel vẫn tiếp tục liều chuẩn (300 mg liều nạp và 75 mg liều duy trì).
– Bệnh nhân HCMVC can thiệp ĐMV có đặt stent: để dự phòng tắc stent có thể dùng clopidogrel liều gấp đôi: 600 mg liều nạp và 150 mg liều duy trì ít nhất trong 1 tuần sau can thiệp ĐMV.
– BN đề kháng với clopidogrel, liều gấp đôi clopidogrel không cải thiện tiên lượng cũng như nguy cơ tắc stent.
MỘT PHÁC ĐỒ THAY THẾ CLOPIDOGREL, VAI TRÒ CỦA TICAGRELOR ?
Ở nhóm bệnh nhân được can thiệp ĐMV nhưng có tình trạng đề kháng clopidogrel, việc sử dụng gấp đôi liều cũng không cải thiện được tiên lượng. Việc tìm kiếm một phác đồ điều trị thay thế là cần thiết.
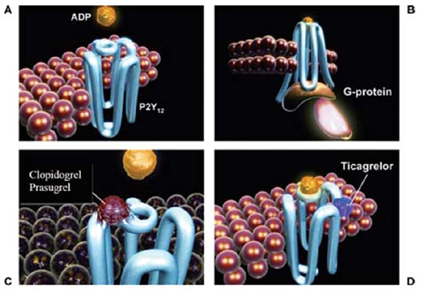
Ticagrelor là một thuốc ức chế thụ thể P2Y12non–thienopyridine. Ticagrelor có cấu trúc tương tự ADP là nguyên nhân làm ức chế có hồi phục thụ thể P2Y12. Thuốc này trực tiếp đối kháng ADP gắn kết vào thụ thể P2Y12 mà không cần bất kỳ hoạt động chuyển hóa nào (Xem biểu đồ 3). Ticagrelor được hấp thu nhanh chóng và bị thoái biến men ngay sau uống để thành dạng hoạt động. Nồng độ của ticagrelor trong huyết tương tăng phụ thuộc liều, không kể tuổi hay giới tính. Nồng độ huyết tương tối đa và ức chế tiểu cầu tối đa đạt được từ 1 – 3 giờ sau điều trị. Thời gian bán hủy 6–13 giờ thích hợp với liều điều trị 2 lần/ngày [16], [17], [18].
|
|
Biểu đồ 3. Avà B: Bình thường, ADP kết hợp với thụ thể P2Y12 làm thay đổi hình dạng và hoạt hóa G-protein. C: Thienopyridine đã hoạt hóa gắn kết với thụ thể P2Y12 gây ức chế không hồi phục, làm cho thụ thể không hoạt động suốt đời sống tiểu cầu.D: Ticagrelor ức chế có hồi phục thụ thể P2Y12 ở một vị trí khác biệt với vị trí gắn kết của ADP và ức chế tín hiệu ADP làm thay đổi hình dạng của thụ thể bằng cách “khóa” thụ thể trong một trạng thái bất hoạt. Thụ thể này sẽ hoạt động trở lại khi có sự phân ly của các phân tử ticagrelor [15]. |
Ticagrelor trong Hội chứng mạch vành cấp (HCMVC)
Nghiên cứu PLATO( PLATelet inhibition and patient Outcomes): là một NC đa trung tâm, ngẫu nhiên, mù đôi, trên 18.000 bệnh nhân HCMVC (ST chênh lên và không ST chênh lên). Ticagrelor được cho với liều nạp 180 mg và liều duy trì 90 mg 2 lần/ngày so sánh với nhóm dùng clopidogrel 300mg/75 mg. Tất cả bệnh nhân được điều trị với aspirin 75 – 100 mg/ngày [19].
– Tiêu chí chính đánh giá hiệu quả của NC (biến cố gộp của tử vong do tim mạch, NMCT hoặc đột quỵ) giảm thấp ở nhóm dùng ticagrelor so với nhóm dùng clopidogrel có ý nghĩa sau theo dõi 12 tháng (9,8% so với 11,7% p < 0,001) (Biểu đồ 17A). Đặc biệt, ở phân nhóm được can thiệp ĐMV và đặt stent, ticagrelor cũng làm giảm có ý nghĩa biến cố gộp so với clopidogrel (8.9% so với10.6% với p = 0,003).
Đặc biệt, trong số những bệnh nhân đặt stent, tỉ lệ tắc stent do huyết khối cũng giảm thấp ở nhóm điều trị ticagrelor so với clopidogrel có ý nghĩa (1,3% so với 1,9%, p = 0,009).
– Tiêu chí chính đánh giá sự an toàn của thuốc là nguy cơ chảy máu nghiêm trọng trong dân số chung cho thấy sự khác biệt giữa hai nhóm thuốc không có ý nghĩa (11.6% và 11.2% với p = 0,43) (Biểu đồ 4). Tuy nhiên, tỉ lệ chảy máu nghiêm trọng không liên quan đến CABG cao hơn ở nhóm dùng ticagrelor so với nhóm dùng clopidogrel (4,5% so với 3,8% với p = 0,03) và chảy máu theo tiêu chuẩn TIMI (2,8% so với 2,2% với p = 0,03). Nguy cơ chảy máu nội sọ tăng hơn ở nhóm điều trị với ticagrelor (0,3% so với 0,2% với p = 0,06), gồm chảy máu nội sọ trầm trọng (0,1% so với 0,01% với p =0,02). Ticagrelor có độ dung nạp tương đối cao, tuy nhiên, so với clopidogrel, tỉ lệ ngưng điều trị do tác dụng không mong muốn cao hơn so với clopidogrel (7,4% so với 6% với p < 0,001). Một số tác dụng phụ ghi nhận khi điều trị với ticagrelor gồm: khó thở 13,3% nhưng chỉ có 0,9% số bệnh nhân khó thở phải ngưng điều trị, tăng nhẹ nồng độ acid uric và creatinine trong huyết tương [19].
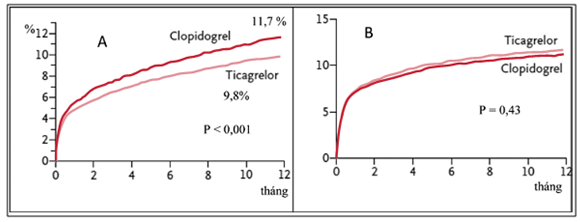
Biểu đồ 4:Nghiên cứu PLATO, so sánh ticagrelor và clopidogrel trong điều trị HCMVC
A. Tiêu chí chính về hiệu quả
B. Tiêu chí chính về tính an toàn (nguy cơ chảy máu nghiêm trọng)
KẾT LUẬN
Tắc stent do huyết khối sau đặt stent ĐMV là một thảm họa thật sự trong chuyên nghành tim mạch can thiệp. Việc chon lựa bệnh nhân và chú ý các nguy cơ sẽ giúp phòng tránh. Chọn lựa kháng tiểu cầu phù hợp sau đặt stent góp phần quan trọng trong việc giảm tối thiểu biến cố này. Bệnh nhân HCMVC can thiệp ĐMV có đặt stent: để dự phòng tắc stent có thể dùng clopidogrel liều gấp đôi: 600 mg liều nạp và 150 mg liều duy trì ít nhất trong 1 tuần sau can thiệp ĐMV. BN đề kháng với clopidogrel, liều gấp đôi clopidogrel không cải thiện tiên lượng cũng như nguy cơ tắc stent. Ticagrelor là một thuốc kháng tiểu cầu mới, thuộc nhóm non-thienopyridine, ức chế trực tiếp và có hồi phục thụ thể P2Y12, là một thuốc được khuyến cáo nhằm làm giảm thiểu nguy cơ tắc stent do huyết khối cũng như cải thiện tiên lượng bệnh.
TÀI LIỆU THAM KHẢO
1. Nguyễn Hữu Khoa Nguyên và Châu Ngọc Hoa. Các biến chứng của can thiệp động mạch vành. Trong sách: Can thiệp động mạch vành trong thực hành lâm sàng. Chủ biên: Đặng Vạn Phước, Châu Ngọc Hoa, Trương Quang Bình. Nhà xuất bản Y học – 2011, trang 31-52.
2. Trần Hòa và Châu Ngọc Hoa. Thuốc kháng tiểu cầu trong can thiệp động mạch vành. Trong sách: Can thiệp động mạch vành trong thực hành lâm sàng. Chủ biên: Đặng Vạn Phước, Châu Ngọc Hoa, Trương Quang Bình. Nhà xuất bản Y học – 2011, trang 77-118.
3. Ajay J. Kirtane, Gregg W. Stone. How to Minimize Stent Thrombosis. 2011;124:1283-1287 Circulation.
4. Holmes DR, Kereiakes DJ. Stent Thrombosis. J. Am. Coll. Cardiol. 2010;56;1357-1365.
5. Cutlip DE, Windecker S, Mehran R, et al. Clinical end points in coronary stent trials: a case for standardized definitions. Circulation 2007;115:2344 –51.
6. van Werkum JW, Heestermans AA. Predictors of coronary stent thrombosis: the Dutch Stent Thrombosis Registry. J Am Coll Cardiol. 2009;53(16):1399.
7. Leon MB, Baim DS. A clinical trial comparing three antithrombotic-drug regimens after coronary-artery stenting. Stent Anticoagulation Restenosis Study Investigators. N Engl J Med. 1998;339(23):1665.
8. Moreno R, Fernández C. Drug-eluting stent thrombosis: results from a pooled analysis including 10 randomized studies. J Am Coll Cardiol. 2005;45(6):954.
9. Roiron C, Sanchez P. Drug eluting stents: an updated meta-analysis of randomised con-trolled trials. Heart. 2006;92(5):641.
10. Roukoz H, Bavry AA, Sarkees ML, et al. Comprehensive metaanalysis on drug-eluting stents versus bare-metal stents during extended follow-up. Am J Med 2009;122:581.e1–10.
11. Gurbel PA, Bliden KP, Hiatt BL et al. Clopidogrel for coronary stenting: Response variability, drug resistance, and the effect of pretreatment platelet reactivity. Circulation 107:2908-2913
12. Gurbel PA, Bliden KP, Hayes KM et al.The relation of dosing to clopidogrel responsiveness and the incidence of high post-treatment platelet aggregation in patients undergoing coronary stenting. J Am Coll Cardiol 2005;45:1392–6.
13. Mega JL, Close SL, Wiviott SD, et al. Cytochrome p-450 polymorphisms and response to clopidogrel. N Engl J Med 2009;360:354–62.
14. Matthew J. Price. Standard Versus High-Dose Clopidogrel According to Platelet Function Testing After PCI: Results of the GRAVITAS Trial. AHA -2010-Chicago.
15. Mehta SR. A randomized comparison of a clopidogrel high loading and maintenance dose regimen versus standard dose, and high versus low dose aspirin in 25000 patients with acute coronary syndromes: results of the CURRENT-OASIS 7 trial. ESC 2009 Congress; 2009; Barcelona,Spain.
16. van Giezen JJJ. Optimizing platelet inhibition. Eur Heart J Suppl 2008;10(Suppl D):D23–D29.
17. Steen Husted1 & J.J.J. van Giezen. Ticagrelor: The First Reversibly Binding Oral P2Y12 receptor Antagonist Cardiovascular Therapeutics 27 (2009) 259–274
18. Paul A. Gurbel, Kevin P. Bliden et al. Randomized Double-Blind Assessment of the ONSET and OFFSET of the Antiplatelet Effects of Ticagrelor Versus Clopidogrel in Patients With Stable Coronary Artery Disease: The ONSET/OFFSET Study. Circulation 2009;120;2577-2585
19. Lars Wallentin, Robert A. Harrington et al. (PLATO Investigator). Ticagrelor versus Clopidogrel in Patients with Acute Coronary Syndromes. N Engl J Med 2009;361:1045-57.