TÓM TẮT
Giới thiệu: Giảm nhịp tim là một một phần không thể thiếu trong điều trị đau thắt ngực, nhưng nhiều bệnh nhân không đạt được mục tiêu dưới 60 nhịp/phút theo khuyến cáo mặc dù sử dụng thuốc chẹn bêta liều cao.
Maria Glezer, Yuri Vasyuk, Yuri Karpov
Biên dịch: ThS. BS. Bùi Cao Mỹ Ái – Đại học Y Dược TPHCM
Hiệu đính: PGS. TS. BS. Nguyễn Văn Trí – Chủ tịch Hội Lão khoa TPHCM
Thất bại trong việc tăng liều ức chế Beta có thể là một lý do. Để tìm ra những lựa chọn khác cho việc giảm nhịp tim và tăng cường kiểm soát cơn đau thắt ngực, nghiên cứu CONTROL-2 được tiến hành ở bệnh nhân đau thắt ngực ổn định nhằm so sánh hiệu quả và khả năng dung nạp của sự kết hợp ức chế Bêta với Ivabradine so với tăng liều ức chế Beta đến mức tối đa được dung nạp.
Phương pháp nghiên cứu: Đây là nghiên cứu mở, ngẫu nhiên, đa trung tâm bao gồm 1104 bệnh nhân đau thắt ngực ổn định CCS II và III (CCS (Canadian Cardiovascular Society): hội Tim Mạch Canada), nhịp xoang và trên nền điều trị ổn định với liều ức chế Beta không tối đa theo khuyến cáo. Bệnh nhân được phân bổ theo nhóm Ivabradine + BB hoặc tăng liều ức chế Beta theo tỷ lệ 4: 1.
Kết quả: Vào cuối nghiên cứu (tuần 16), bổ sung ivabradine vào điều trị ức chế Beta và sự tăng liều ức chế Beta dẫn đến giảm nhịp tim (61 ± 6 so với 63 ± 8 nhịp/phút; p = 0,001). Vào tuần thứ 16, có nhiều bệnh nhân đã về mức CCSI khi sử dụng ivabradine + ức chế Beta hơn so với tăng liều ức chế Beta (37,1% so với 28%; p = 0,017) và nhiều bệnh nhân không bị đau thắt ngực hơn (50,6% so với 34,2%; p <0,001). Tình trạng sức khỏe bệnh nhân dựa trên thang điểm VAS (visual analogue scale) cũng tốt hơn trong nhóm Ivabradine + ức chế Beta. Các biến cố bất lợi nhiều hơn đáng kể khi tăng liều ức chế Beta so với kết hợp Ivabradine với ức chế Beta (18,4% so với 9,4%, p <0,001).
Kết luận: Ở những bệnh nhân bị đau thắt ngực ổn định, liệu pháp phối hợp Ivabradine với ức chế Beta cho thấy khả năng dung nạp tốt, an toàn và cải thiện lâm sàng rõ rệt hơn, so với tăng liều ức chế Beta.
GIỚI THIỆU
Năm 2015, bệnh động mạch vành (BĐMV) là nguyên nhân gây tử vong hàng đầu trên toàn thế giới [1] và, mặc dù nhiều bệnh nhân hiện đang sống sót sau nhồi máu cơ tim cấp (AMI), vẫn còn một tỷ lệ đáng kể có đau thắt ngực [2]. Thật vậy, đau thắt ngực do BĐMV ảnh hưởng đến khoảng 112 triệu người trên toàn thế giới [3]. Mặc dù tỷ lệ tử vong hàng năm do đau thắt ngực là tương đối thấp [4, 5], triệu chứng thường gây giảm năng lực và ảnh hưởng bất lợi đến chất lượng cuộc sống của bệnh nhân. Trong một nghiên cứu toàn cầu, tỷ lệ giảm năng lực do BĐMV (CAD disability) cao nhất được thấy ở Đông Âu và Trung Á, và đau thắt ngực ổn định chiếm tỉ lệ lớn nhất cho giảm năng lực do BĐMV, tỉ lệ nhỏ hơn là do suy tim do bệnh cơ tim thiếu máu cục bộ và nhồi máu cơ tim không tử vong [6]. Đau thắt ngực cũng có tác động đáng kể lên chi phí chăm sóc sức khỏe và nó đã được chứng minh rằng, sau hội chứng mạch vành cấp, bệnh nhân đau thắt ngực sử dụng chi phí y tế gấp đôi bệnh nhân không triệu chứng [7].
Điều trị bệnh nhân bị đau thắt ngực ổn định tập trung chủ yếu vào việc giảm các triệu chứng, cải thiện chất lượng cuộc sống và phòng ngừa các biến cố tim mạch [8]. Giảm nhịp tim là một phần không thể thiếu trong điều trị đau thắt ngực; nhịp tim mục tiêu là dưới 60 nhịp/phút [8, 9] và thuốc ức chế Beta, thuốc chẹn kênh canxi và ivabradine được khuyến cáo để giảm nhịp tim và triệu chứng [8].Dữ liệu từ nghiên cứu CLARIFY, một nghiên cứu sổ bộ quốc tế lớn, đã chứng minh rằng mặc dù sử dụng ức chế Beta liều cao, bệnh nhân bị đau thắt ngực ổn định thường có nhịp tim lúc nghỉ lớn hơn 70 nhịp/phút, và điều này có liên quan đến đau thắt ngực và thiếu máu cục bộ thường xuyên hơn [10]. Đây có thể liên quan một phần với thất bại khi tăng liều ức chế Beta và ngưng điều trị [11], và có một nhu cầu rõ ràng trong việc giảm nhịp tim hơn nữa ở nhiều bệnh nhân đau thắt ngực ổn định.
Ivabradine là chất ức chế chọn lọc trên kênh If đầu tiên, nó kiểm soát sự khử cực tâm trương tự phát trong nút xoang và giảm nhịp tim [12]. Thuốc được chỉ định để điều trị triệu chứng đau thắt ngực ổn định mạn tính ở người lớn có BĐMV có nhịp xoang bình thường và nhịp tim tối thiểu là 70 nhịp/ phút cũng như điều trị bệnh nhân suy tim mạn.
Ivabradine cải thiện lưu lượng máu mạch vành thông qua các cơ chế khác nhau so với ức chế beta và điều này làm tăng cơ hội kết hợp điều trị ở những bệnh nhân vẫn còn triệu chứng khi đơn trị liệu ức chế beta. Trong một nghiên cứu nhỏ ở bệnh nhân đau thắt ngực ổn định, kết hợp điều trị bằng Ivabradine và Bisoprolol giảm các triệu chứng đau thắt ngực và cải thiện khả năng gắng sức so với tăng liều bisoprolol [13]. Trong nghiên cứu ASSOCIATE, nghiên cứulớn hơn với nhóm chứng giả dược,bổ sung ivabradine với điều trị atenolol dẫn đến cải thiện đáng kể khả năng gắng sức ở bệnh nhân bị đau thắt ngực ổn định [14].
Để làm rõ tiềm năng rộng hơn trong điều trị kết hợp ivabradine với ức chế beta, chúng tôi đã bắt đầu Nghiên cứu CONTROL-2 với dân số lớn bệnh nhân ở Nga có đau thắt ngực ổn định trên ở liều ức chế beta chưa phải là tối đa. Nghiên cứu so sánh tác dụng của việc thêm ivabradine vào ức chế beta so với tăng liều ức chế beta về nhịp tim, đau thắt ngực, việc sử dụng nitroglycerin và tình trạng sức khỏe của bệnh nhân. Nghiên cứu đã được xuất bản bằng tiếng Nga trước đó [15].
PHƯƠNG PHÁP
Nghiên cứu CONTROL-2 là một nghiên cứu tiền cứu, mở, ngẫu nhiên, đa trung tâm,với bệnh nhân được lựa chọn liên tiếp. Tổng cộng 389 bác sĩ từ 72 thành phố của Liên bang Nga tham gia vào nghiên cứu, bao gồm cả chuyên gia tim mạch (232; 60,6%), bác sĩ tổng quát (121; 31,6%) và bác sĩ nội trú nội khoa (30; 7,8%).
Những người tham gia nghiên cứu là bệnh nhân người lớn (≥18 tuổi) có đau thắt ngực khi gắng sức, CCS II-III, đã ổn định ít nhất 3 tháng, với ít nhất ba cơn mỗi tuần. Bệnh nhân có nhịp xoang với tần số tim tối thiểu 60 lần/ phút và đang trải qua điều trị đau thắt ngực ổn định đều đặn với một thuốc ức chế beta ở một liều dưới mức tối đa để điều trị đau thắt ngực. Tiêu chí loại trừ bao gồm suy tim mạn NYHA III-IV, không phải nhịp xoang, huyết áp lúc nghỉ lớn hơn 180/100 mmHg và đang được điều trị bằng verapamil hoặc diltiazem.
Thiết kế nghiên cứu được phác thảo trong hình 1. Bệnh nhân được phân bổ vào nhóm điều trị chuẩn với thuốc chẹn beta tăng liều đến liều dung nạp tối đa hoặc thêm ivabradine vào liều ức chế beta hiện tại, với tỷ lệ bệnh nhân là 1: 4. Tỷ lệ phân bổ điều trị này được sử dụng để tăng cơ hội phát hiện bất kỳ vấn đề dung nạp nào liên quan đến sự kết hợp của Ivabradine với ức chế beta. Việc tăng liều ức chế beta được thực hiện theo nhịp tim lúc nghỉ đạt được và khả năng dung nạp, ngược lại trong suy tim, không có khuyến cáo liều mục tiêu hoặc phân tử ức chế beta được khuyến cáo trong điều trị đau thắt ngực ổn định, và do đó một loạt các thuốc và liều phổ biến được sử dụng: atenolol 25–100 mg / ngày [16], bisoprolol 2,5–10 mg / ngày[16, 17], betaxolol 5–20 mg / ngày [16], carvedilol 6,25–100 mg / ngày [16], nebivolol 2,5–5 mg/ ngày [16, 17], metoprolol 50–200 mg / ngày [16, 17] và propranolol 40–320 mg / ngày [16].
Năm lần khám bệnh được thực hiện: lần cơ bản (lần khám 0), vào lúc 2 tuần (lần khám 1), lúc 4 tuần (lần khám 2), lúc 8 tuần (lần khám 3) và cuối cùng là 16 tuần (lần khám 4).
Kết cục lâm sàng là sự thay đổi nhịp tim trong thời gian thời gian điều trị 16 tuần, sự thay đổi độ CCS, số lượng các cơn đau thắt ngực với liệu pháp chuẩn so với ivabradine, tỷ lệ bệnh nhân không bị đau thắt ngực giữa những lần thăm khám và tình trạng sức khỏe tự báo cáo của bệnh nhân (thang điểm VAS). Định lượng các tham số được trình bày dưới dạng số trung bình và độ lệch chuẩn, nếu các giá trị được phân phối bình thường, hoặc là số trung vị với phần trăm thứ 25 và 75, nếu các giá trị phân phối không bình thường. Sự khác biệt trong các biến số định lượng giữa các nhóm được phân tích bằng cách sử dụng phép kiểm t đối với mẫu độc lập với sự phân phối tham số các giá trị hoặc phép kiểm Mann – Whitney đối với mẫu phi tham số. Thay đổi trong các biến định lượng trong quá trình điều trị được phân tích bằng cách sử dụng phép kiểm t cho các mẫu được cặp đôi hoặc phép kiểm Wilcoxon cho thông số phi tham số. Sự khác biệt trong biến phân loại giữa các nhóm được phân tích bằng phép thử Chi bình phương của Pearson với điều chỉnh Yates. Thay đổi trong các biến số phân loại trong quá trình điều trị được phân tích bằng cách sử dụng phép kiểm McNemar. Sự khác biệt được xem xét có ý nghĩa thống kê ở p <0,05.
Tuân thủ Nguyên tắc đạo đức
Tất cả các thủ tục tuân thủ các tiêu chuẩn đạo đức của ủy ban chịu trách nhiệm về thử nghiệm ở người (thể chế và quốc gia), Tuyên bố năm 1964 của Helsinki, được sửa đổi năm 2013 và Ủy ban đạo đức độc lập Châu Âu. Nghiên cứu CONTROL-2 là được phê duyệt bởi Ủy ban đánh giá đạo đức của Đại học Y Nha Moscow (số 18/2 22/09/2009; Mátxcơva). Tất cả các cá nhân những người tham gia nghiên cứu đều điền vào mẫu đồng ý. Nghiên cứu đã được đăng ký tại sổ bộ ISRCTN với tên nghiên cứu ISRCTN30654443.
|
|
Bệnh nhân đau thắt ngực ổ định CCS II – III được điều trị bằng ức chế beta |
|
|
Lần khám 0 |
Đánh giá bệnh nhân đủ tiêu chuẩn chọn Phân bố nhật ký bệnh nhân |
|
|
Lần khám 1 (ngẫu nhiên, tuần 2) |
Thêm Ivabradin 5mg/ ngày (chia 2 lần) |
Điều trị chuẩn: tăng liều ức chế beta. |
|
Lần khám 2 (tuần 4) |
Chỉnh liều Ivabradin lên 7.5 mg/ngày (chia 2 lần) |
Tăng liều ức chế beta |
|
Lần khám 3 (tuần 8) |
Đánh giá hiệu quả điều trị và sự dung nạp |
|
|
Lần khám 4 (tuần 16) |
Đánh giá hiệu quả điều trị và sự dung nạp |
|
Hình 1. Thiết kế nghiên cứu CONTROL – 2
KẾT QUẢ
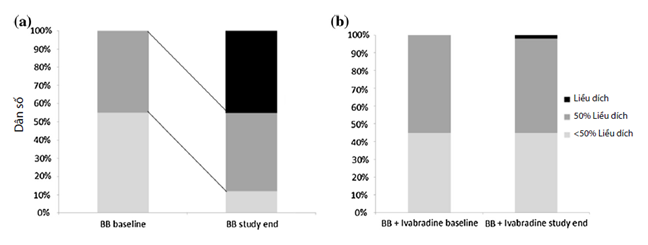
Trong khoảng thời gian từ tháng 11 năm 2009 đến tháng 4 năm 2010, 1104 bệnh nhân được nhận vào nghiên cứu (nhóm tăng liều ức chế beta: 228 bệnh nhân, 20,7%; nhóm ivabradine + ức chế beta: 876 bệnh nhân, 79,3%). Các đặc điểm cơ bản không khác biệt đáng kể giữa hai nhóm, ngoại trừ nhịp tim cao hơn đáng kể trong nhóm Ivabradine + ức chế beta (Bảng 1). Các ức chế beta được sử dụng thường xuyên nhất là bisoprolol và metoprolol (Hình 2). Cả hai nhóm, đều được điều trị đủ liều chuẩn bằng thuốc ức chế men chuyển angiotensin (UCMC) hoặc thuốc chẹn thụ thể angiotensin II (UCTT) (>80%), statin (75%), và kháng kết tập tiểu cầu (>90%) (Bảng 2). Vào lúc ban đầu, không có bệnh nhân nào đạt liều ức chế beta tối đa, mặc dù tỷ lệ bệnh nhân nhóm ivabradine + ức chế beta được cho ức chế beta ở liều ≥50% mức tối đa được khuyến cáo nhiều hơn so với tỉ lệ bệnh nhân nhóm ức chế beta (55% so với 45%) (Hình 3 và Bảng 3). Vào cuối nghiên cứu (tuần 16), điều trị bằng ức chế beta là 227 (99,6%) bệnh nhân ở nhóm tăng liều ức chế beta và 863 (98,5%) bệnh nhân ở nhóm ivabradine + ức chế beta (p = 0,323). 45% bệnh nhân đã đạt được mức tối đa liều ức chế beta trong nhóm tăng liều ức chế beta nhưng, như dự kiến, có rất ít thay đổi liều ức chế beta ở bệnh nhân dùng ivabradine + ức chế beta (Hình 3). Tỷ lệ điều trị ức chế beta riêng lẻ vào cuối nghiên cứu tương tự ở cả hai nhóm, nhưng liều lượng khác nhau đáng kể. Đến cuối nghiên cứu, liều hàng ngày của Ivabradine là 5 mg (2 lần/ngày) trong 220 (25,2%) bệnh nhân và 7,5 mg (2 lần/ ngày) trong 654 (74,8%) bệnh nhân.
Bảng 1. Đặc điểm cơ bản bệnh nhân trong nghiên cứu CONTROL – 2 (n = 1075)
|
Thông số |
Nhóm điều trị chuẩn (n = 228) |
Nhóm ivabradin (n = 876) |
p |
|
Thông số dịch tễ Tuổi, năm ≥65 tuổi, n (%) Nữ, n (%) BMI, kg/m2 BMI ≥30 kg/m2, n (%) Tiền căn Tăng huyết áp, n (%) NMCT cũ, n (%) Có mổ bắc cầu, n (%) Có can thiệp mạch vành, n (%) Suy tim NYHA I/II, n (%) Đái tháo đường Bệnh ĐM ngoại biên, n (%) Đột quỵ hoặc cơn thoáng thiếu máu não, n (%) Hen, n (%) COPD, n (%) Rối loạn lo âu, n (%) Rối loạn cương, n (%) Khám lâm sàng Số cơn ĐTN/ tuần Số viên nitroglycerin/tuần Đau thắt ngực CCS III, n (%) HATT, mmHg HATTr, mmHg Nhịp tim, nhịp/phút Phân suất tống máu, % Chụp mạch vành, n (%) Siêu âm gắng sức (+), n(%) NPGS (+), n (%)
|
61.2 ± 9.3 70 (31.5) 105 (46.1) 28.9 ± 4.4 76 (33.3)
202 (88.6) 91 (39.9) 18 (7.9) 15 (6.6) 56 (24.6)/ 107 (46.9) 34 (14.9) 28 (12.3) 16 (7.0)
2 (0.9) 19 (8.3) 17 (7.5) 24 (19.5)
7 (4; 12) 7 (4; 11) 67 (29.5) 144.9 ± 15.6 86.8 ± 8.6 83.2 ± 10.9 55.3 ± 7.7 48 (21.1) 10 (4.4) 123 (53.9)
|
60.0 ± 9.6 248 (29.6) 437 (49.9) 28.7 ± 5.1 275 (31.4)
754 (85.0) 320 (36.5) 41 (4.7) 38 (4.3) 163 (18.6)/ 412 (47.0) 130 (14.8) 107 (12.2) 37 (4.2)
17 (1.9) 89 (10.2) 80 (9.1) 87 (19.8)
7 (4;10) 7 (4; 10) 279 (31.9) 143.0 ± 17.5 86.5 ± 8.9 85.1 ± 10.4 56.0 ± 8.4 139 (15.9) 48 (5.5) 480 (54.8) |
0.097 0.633 0.339 0.603 0.638
0.207 0.387 0.079 0.216 0.078 1.000 1.000 0.113
0.394 0.483 0.506 1.000
0.818 0.846 0.538 0.115 0.409 0.015 0.588 0.078 0.622 0.877 |
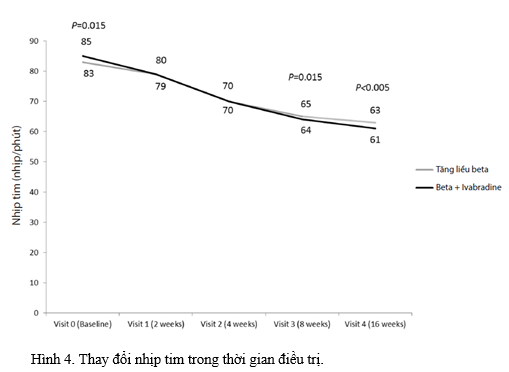
Nhịp tim giảm đáng kể ở cả hai nhóm từ 83,2 ± 10,9 đến 63 ± 8 bpm trong nhóm tăng liều ức chế beta và từ 85,1 ± 10,4 đến 61 ± 6 bmp trong nhóm Ivabradine + ức chế beta (hình 4). Trong cả hai nhóm, nhịp tim mục tiêu (55–60 nhịp/ phút) đã đạt được ở khoảng một nửa số bệnh nhân bị đau thắt ngực ổn định.
Sự giảm huyết áp có thể so sánh được thấy ở hai nhóm, từ 145/87 đến 125/78 mmHg trong nhóm tăng liều ức chế beta và 143/87 đến 126/78 mmHg trong nhóm Ivabradine + ức chế beta.
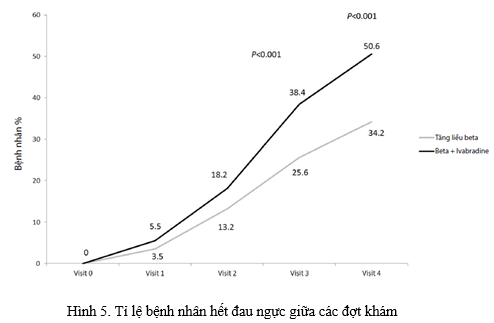
Việc tối ưu hóa điều trị dẫn đến hiệu quả giảm đau thắt ngực đáng kể ở cả hai nhóm. Tuy nhiên, vào cuối 16 tuần điều trị, tỷ lệ bệnh nhân bị đau thắt ngực CCS I cao hơn đáng kể trong nhóm Ivabradine + ức chế beta so với nhóm tăng liều ức chế beta (lần lượt là 37,1% và 28%; p = 0,017), trong khi ở đầu nghiên cứu không có bệnh nhân đau thắt ngực CCS I ở cả hai nhóm. Tỷ lệ bệnh nhân không bị đau thắt ngực sau tuần thứ 8 và tuần 16 của nghiên cứu lớn hơn đáng kể khi điều trị bằng ivabradine + ức chế beta so với tăng liều ức chế beta (Hình 5).
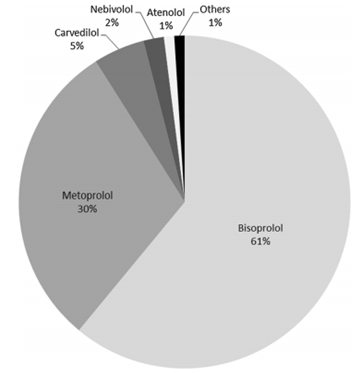
Hình 2. Các thuốc ức chế beta điều trị lúc đầu
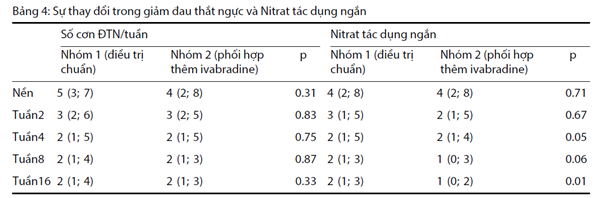
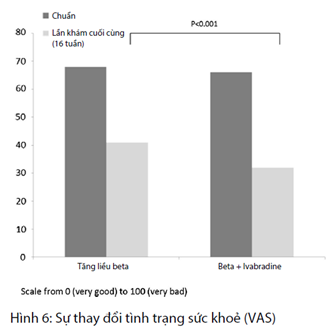
Phân tích sổ nhật ký bệnh nhân cho thấy có sự giảm tần suất cơn đau thắt ngực và sử dụng nitroglycerin ở cả hai nhóm (Bảng 4). Tuy nhiên, vào cuối nghiên cứu, nhu cầu nitroglycerin trong nhóm ức chế beta + ivabradine thấp hơn đáng kể: 1 (0; 2) so với 2 (1; 3), p = 0,015. Tình trạng sức khỏe bệnh nhân, dựa trên kết quả của thang điểm VAS, được cải thiện ở cả hai nhóm, từ 67 (51; 78) đến 41 (29; 65) trong nhóm tăng liều ức chế beta và từ 65 (48; 78) đến 32 (18; 47) trong nhóm ivabradine + ức chế beta. Sự cải thiện này là cao hơn trong nhóm Ivabradine + ức chế beta so với nhóm tăng liều ức chế beta (p = 0,001) (Hình 6).
|
Điều trị |
Tần suất kê toa, n (%) |
P |
|
|
Nhóm điều trị chuẩn, n = 228 |
Nhóm Ivabradin, n = 876 |
||
|
Aspirin hoặc KKTTC khác Nitrat tác dụng dài Thuốc giảm lipid máu Ức chế canxi ƯCMC ƯCTT Lợi tiểu Thiazide Trimetazidine |
210 (92.1)
110 (48.2) 169 (74.1) 39 (17.1) 161 (70.6) 26 (11.4) 45 (19.7) 36 (15.8) |
811 (92.6)
443 (50.6) 655 (74.8) 149 (17.0) 639 (72.9) 84 (9.6) 130 (14.8) 123 (14.0) |
0.919
0.582 0.908 1.000 0.536 0.490 0.089 0.573 |
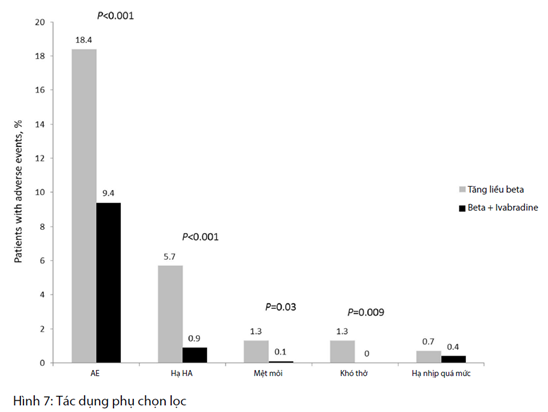
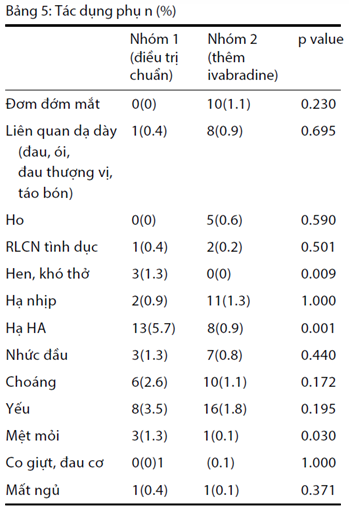
Những biến cố bất lợi
Những biến cố bất lợi phổ biến hơn đáng kể trong nhóm tăng liều ức chế beta so với nhóm Ivabradine + ức chế beta (18,4% so với 9,4%, p <0,001) (Hình 7). Tỷ lệ hen, khó thở, hạ huyết áp và mệt mỏi tất cả đều cao hơn đáng kể trong nhóm tăng liều ức chế beta (Bảng 5). Nhập viện (vì bất kỳ lý do nào) đã được báo cáo thường xuyên hơn trong nhóm điều trị chuẩn [6 trường hợp (2,6%) so với 8 trường hợp (0,9%), p = 0,083]. Tử vong, nhồi máu cơ tim không tử vong, hoặc đột quỵ không tử vong đã được báo cáo trong lần lượt 3 ca (1,3%) và 2 ca (0,2%) (p = 0,063). Nhịp tim ít hơn 50 nhịp/ phút được ghi nhận trên ít nhất một lần khám (1–4) ở 7 bệnh nhân: 1 (0,4%) ở nhóm tăng liều ức chế beta và 6 (0,7%) ở nhóm Ivabradine + ức chế beta (p = 1.000).
BÀN LUẬN
Trong thử nghiệm CONTROL-2, chúng tôi thấy rằng việc kết hợp điều trị Ivabradine với ức chế beta cho hiệu quả giảm đau thắt ngực rõ rệt hơn so với tăng liều ức chế beta, với tỷ lệ bệnh nhân hết đau thắt ngực cao hơn: một nửa số bệnh nhân điều trị phối hợp với Ivabradine và ức chế beta đã hết đau thắt ngực, so với khoảng một phần ba số bệnh nhân nhóm tăng liều chuẩn ức chế beta.
Việc bổ sung ivabradine vào liệu pháp ức chế beta cũng được dung nạp tốt hơn so với việc tăng liều ức chế beta, và sự cải thiện hiệu quả và khả năng dung nạp phản ánh sự cải thiện tình trạng sức khỏe lớn hơn ở bệnh nhân nhóm Ivabradine kết hợp ức chế beta.
Các yếu tố có thể góp phần vào ưu thế của điều trị kết hợp ivabradine với ức chế beta hơn là sự tăng liều ức chế beta bao gồm sự thất bại của hơn một nửa số bệnh nhân trong nhóm tăng liều để đạt được liều điều trị ức chế beta tối đa, và tác dụng bổ sung của ivabradine trên lưu lượng mạch vành. Các thuốc ức chế beta tác động trực tiếp lên tim để giảm nhịp tim, đồng thời ảnh hưởng đến co bóp cơ tim và dẫn truyền nhĩ thất [8]. Chúng làm tăng tưới máu vùng cơ tim thiếu máu cục bộ bằng cách kéo dài thời gian tâm trương và tăng kháng mạch máu ở những vùng không thiếu máu cục bộ [8] nhưng cũng làm giảm thư giãn thất đồng thể tích và do đó bù đắp 1 phần lợi điểm trên tích phân của huyết áp tâm trương theo thời gian [18]. Không giống ức chế beta, Ivabradine không có tác dụng co bóp âm (inotropic) và thư giãn cơ tim (lusitropic) khi giảm nhịp tim tương đương, dẫn đến kéo dài thời gian tâm trương hơn so với ức chế beta [19]. Thêm vào đó, Ivabradine không gây co mạch liên quan thụ thể alpha-adrenergic và, không giống như ức chế beta, do đó duy trì sự giãn mạch vành khi gắng sức [19]. So với ức chế beta, Ivabradine cũng tăng lưu lượng dự trữ mạch vành và sự tưới máu bàng hệ, thúc đẩy sự phát triển của mạch vành bàng hệ [19]. Cũng có bằng chứng từ thực nghiệm và các nghiên cứu lâm sàng rằng ivabradine có thể giảm thiếu máu cơ tim cục bộ và hiệu quả của nó không chỉ thông qua giảm nhịp tim mà cũng thông qua cơ chế tác dụng đa phương diện (pleiotropic) bổ sung có thể bao gồm sự giảm sự hình thành các thể hoạt hóa oxy trong ty thể tế bào cơ tim [20–22]. Một số dữ liệu từ các nghiên cứu lâm sàng cũng cho thấy một số lợi ích không liên quan với nhịp tim của ivabradine. Ví dụ: cải thiện vận tốc lưu lượng dự trữ mạch vành được đã được báo cáo với Ivabradine ở bệnh nhân BĐMV ổn định khi sự giảm nhịp tim bị hủy bởi nhịp nhĩ [23]. Trong một nghiên cứu khác trong bệnh nhân có BĐMV ổn định, ivabradine cải thiện lưu lượng dự trữ mạch vành mức độ lớn hơn đáng kể so với bisoprolol ở cùng nhịp tim bị giảm [24]. Những tính chất cộng thêm này của Ivabradine có thể giúp giải thích tác dụng chống đau thắt ngực có lợi của sự kết hợp điều trị với ức chế beta so với sự tăng liều ức chế beta.
Hình 3. Thay đổi liều ức chế beta trong nghiên cứu ở nhóm tăng liều ức chế beta (a) và nhóm ức chế beta + ivabradin (b)
Bảng 3. Thay đổi liều ức chế beta trong nghiên cứu
|
Khoảng liều ức chế beta |
Lúc đầu, n (%) |
P |
Cuối nghiên cứu, n (%) |
p |
||
|
|
Nhóm điều trị chuẩn, n = 228 |
Nhóm ivabradin, n = 876 |
Nhóm điều trị chuẩn, n = 228 |
Nhóm ivabradin, n = 876 |
|
|
|
≥50% liều tối đa (nhưng thấp hơn liều tối đa) |
102 (44.7)
|
481 (54.9) |
0.008 |
95 (41.6) |
453 (526) |
0.001 |
|
Liều tối đa |
– |
– |
|
103 (45.1) |
24 (2.8) |
0.005 |
|
<50% liều tối đa |
126 (55.3) |
395 (45.1) |
0.028 |
30 (13.1) |
385 (44.6) |
0.001 |
Những lợi thế của điều trị kết hợp Ivabradine với ức chế beta ở bệnh nhân đau thắt ngực ổn định mà chúng ta thấy trong nghiên cứu CONTROL-2 được hỗ trợ bởi dữ liệu từ nghiên cứu ngẫu nhiên trước đó [13, 14]. Trong một nghiên cứu trên 24 bệnh nhân đau thắt ngực ổn định, sự giảm tương đương nhịp tim lúc nghỉ trung bình được ghi nhận sau 2 tháng sử dụng Ivabradine kết hợp với bisoprolol 5 mg so với tăng bisoprolol từ 5 đến 10 mg. Khi điều trị kết hợp, có giảm đáng kể số lượng các cơn đau thắt ngực hàng tuần cần ngậm nitrat dưới lưỡi (p = 0,041) [13]. Trong nghiên cứu ASSOCIATE, bổ sung ivabradine (5–7,5 mg 2 lần/ngày) vào atenolol 50 mg 1 lần/ngày cải thiện đáng kể khả năng gắng sức sau 4 tháng, tương đương với giả dược, ở bệnh nhân đau thắt ngực ổn định điều trị bằng ức chế beta[25].
Trong nghiên cứu REDUCTION được thực hiện trong thực hành lâm sàng hàng ngày, sự giảm đáng kể nhịp tim (p <0,0001) và các cơn đau thắt ngực (p <0,0001) được ghi nhận trong 4 tháng theo dõi trong một nhóm gồm 344 bệnh nhân được điều trị bằng cả ivabradine và BBs [26]. Hiệu quả và sự dung nạp được xếp loại là ‘rất tốt / tốt’ ’với 96% và 99% bệnh nhân được điều trị [26]. Hỗ trợ thêm cho việc điều trị phối hợp Ivabradine với ức chế beta trong đau thắt ngực ổn định xuất phát từ dữ liệu gộp từ ba nghiên cứu quan sát lớn với tổng số 8555 bệnh nhân trong đó điều trị bằng Ivabradine 4 tháng liên quan đến sự giảm đáng kể tần suất các cơn đau thắt ngực (p <0,0001) và sự sử dụng nitrat tác dụng ngắn (p <0,0001), không phân biệt tuổi tác, bệnh đồng mắc, và việc sử dụng ức chế beta [27]. Nhịp tim giảm 16% khi điều trị bằng Ivabradine và 85% bệnh nhân đạt được nhịp tim dưới 70 nhịp/ phút hoặc giảm ít nhất 10 nhịp/phút. Tình trạng lâm sàng và chất lượng cuộc sống cũng đã được cải thiện [27].
Ý nghĩa lâm sàng
Với tiềm năng hiệu ứng hiệp đồng giữa ức chế beta và ivabradine, kết quả của CONTROL-2 cho thấy, ở những bệnh nhân vẫn còn triệu chứng khi dùng ức chế beta, kết hợp ivabradine và ức chế beta cho hiệu quả tốt hơn tăng liều ức chế beta.
Dữ liệu về hiệu quả tốt hơn của sự kết hợp Ivabradine và ức chế beta cung cấp lý do cho sự kết hợp liều cố định của Ivabradine và metoprolol hiện có sẵn để sử dụng trong thực hành lâm sàng và có thể có lợi về mặt tuân thủ điều trị, có thể tiếp tục cải thiện hiệu quả của sự kết hợp trị liệu này.
Hạn chế
Ngưỡng nhịp tim để tham gia vào CONTROL-2 (≥ 60 bpm) thấp hơn ngưỡng nhịp tim tối thiểu là 70 nhịp/ phút hiện đang được khuyến cáo cho điều trị bằng ivabradine. Tuy nhiên, đặc điểm dân số tại thời điểm ban đầu được biểu hiện rõ (Bảng 1), tất cả bệnh nhân trong nghiên cứu đều có nhịp tim lớn hơn 70 bpm. Thật vậy, bệnh nhân trong ivabradine + ức chế beta có nhịp tim cao hơn đáng kể so với nhóm tăng liều ức chế beta ở thời điểm bắt đầu, do thiết kế mở của nghiên cứu. Mặc dù sự ngẫu nhiên khi chọn bệnh của CONTROL-2 không tạo bởi máy tính, việc lựa chọn bệnh nhân ngẫu nhiên liên tục với tỉ lệ 4:1cho Ivabradine + ức chế beta so với tăng liều ức chế beta đã loại bỏ tiềm năng sai lệch do người khảo sát, dẫn đến việc bệnh nhân được phân vào nhánh điều trị dựa theo cảm nhận độ nặng của bệnh.
Tỷ lệ bệnh nhân đã trải qua phẫu thuật/thủ thuật cho chứng đau thắt ngực ổn định (mổ bắc cầu mạch vành và can thiệp mạch vành qua da) thấp hơn dự kiến ở dân số châu Âu và Mỹ. Trong CONTROL-2, dưới 8% bệnh nhân trong nhóm tăng liều ức chế beta và ít hơn 5% số người dùng Ivabradine + ức chế beta có mổ bắc cầu mạch vành, và tương đương vậy, có dưới 7% và dưới 5% có can thiệp mạch vành qua da. Điều này so với 22% và 59% trong nghiên cứu REDUCTION ở Đức [26]. Tuy nhiên, những phát hiện trong CONTROL – 2 là điển hình trong thực hành ở Nga, nơi mà việc tiếp cận các can thiệp như vậy bị giới hạn.
CONTROL-2 nhấn mạnh thách thức của giảm nhịp tim và cải thiện các triệu chứng đau thắt ngực với đơn trị liệu ức chế beta, và khó khăn của việc tăng liều ức chế beta là do các vấn đề về khả năng dung nạp. Trước dữ liệu từ nghiên cứu CLARIFY ở BĐMV mạn ổn định cho thấy 41% bệnh nhân dung ức chế beta có nhịp tim ít nhất 70 bpm và chỉ có 22% trong số đó có các triệu chứng đau thắt ngực có nhịp tim từ 60 nhịp/ phút trở xuống [9]. Trong một nghiên cứu ở Anh trên 500 bệnh nhân có can thiệp mạch vành vì đau thắt ngực ổn định mạn tính, 78% được dung ức chế beta, với liều tương đương trung bình với bisoprolol là 3,1 mg [28] – ở ngưỡng dưới của liều khuyến cáo [16, 17]. Trong nghiên cứu CONTROL ở những bệnh nhân đau thắt ngực ổn định, được thực hiện trước đó, liều ức chế beta trung bình cũng thấp (bisoprolol 5 mg, metoprolol 50 mg, nebivolol 5 mg) [29].
KẾT LUẬN
Ở những bệnh nhân đau thắt ngực ổn định, kết hợp điều trị bằng Ivabradine với ức chế beta đã chứng minh sự cải thiện lâm sàng rõ rệt hơn về tình trạng sức khỏe của bệnh nhân so với tăng liều ức chế beta. Điều trị được dung nạp tốt và hiệu quả, giải quyết sự thất bại hiện tại trong việc tối ưu hóa điều trị đau thắt ngực và kiểm soát nhịp tim với ức chế beta đơn trị liệu, ít nhất một phần, đối với những bệnh nhân không có khả năng đạt được liều thỏa đáng.
THÔNG TIN LIÊN QUAN:
Cảm ơn các nhà nghiên cứu: Các tác giả cảm ơn tất cả các điều tra viên tham gia cùng những đóng góp của họ cho nghiên cứu này.
Tuân thủ Nguyên tắc đạo đức:Nghiên cứu cùng các thủ tục liên quan đều tuân thủ các Tiêu chuẩn đạo đức của Ủy ban chịu trách nhiệm về thử nghiệm trên người (thể chế và quốc gia), Tuyên bố Helsinki năm 1964 (được sửa đổi năm 2013) và Ủy ban Đạo đức độc lập châu Âu. Đề cương nghiên cứu CONTROL-2 được phê duyệt bởi Ủy ban đánh giá đạo đức của Đại học Y Nha Moscow (số 18/2 ngày 22/09/2009; Moscow). Tất cả các cá nhân tham gia vào nghiên cứu đều ký vào văn bản đồng ý Tuân thủ Nguyên tắc đạo đức.
Truy cập mở: Bài viết này được xuất bản Creative Commons Attribution – NonCommercial 4.0 International License (http://creativecommons.org/licenses/by-nc/4.0/), cho phép bất kỳ việc sử dụng phi thương mại nào, phân phối và sản xuất bằng bất kỳ phương tiện nào, miễn là người sử dụng ghi tác giả bài gốc và nguồn, cung cấp liên kết tới Creative Commons, và cho biết có chỉnh sửa nội dung không.
TÀI LIỆU THAM KHẢO
1. GBD 2015 Mortality and Causes of Death Collaborators. Global, regional, and national life expectancy, all-cause mortality, and cause-specific mortality for 249 causes of death, 1980–2015: a systematic analysis for the Global Burden of Disease Study 2015. Lancet. 2016;388:1459–544.
2. Maddox TM, Reid KJ, Spertus JA, et al. Angina at 1 year after myocardial infarction: prevalence and associated findings. Arch Intern Med. 2008;168(12):1310–6.
3. Vos T, Flaxman AD, Naghavi M, et al. Years lived with disability (YLDs) for 1160 sequelae of 289 diseases and injuries 1990–2010: a systematic analysis for the Global Burden of Disease Study 2010. Lancet. 2012;380(9859):2163–96.
4. Dargie HJ, Ford I, Fox KM. Total Ischemic Burden European Trial (TIBET). Effects of ischaemia and treatment with atenolol, nifedipine SR and their combination on outcome in patients with chronic stable angina. The TIBET Study Group. Eur Heart J. 1996;17:104–12.
5. Pepine CJ, Handberg EM, Cooper-DeHoff RM, et al. A calcium antagonist vs a non-calcium antagonist hypertension treatment strategy for patients with coronary artery disease. The International Verapamil-Trandolapril Study (INVEST): a randomized controlled trial. JAMA. 2003;290:2805–16.
6. Moran AE, Forouzanfar MH, Roth GA, et al. The global burden of ischemic heart disease in 1990 and 2010: the Global Burden of Disease 2010 study. Circulation. 2014;129(14):1493–501. 7. Arnold SV, Morrow DA, Lei Y, et al. Economic impact of angina after an acute coronary syndrome: insights from the MERLIN-TIMI 36 trial. Circ Cardiovasc Qual Outcomes. 2009;2(4):344–53.
8. Montalescot G, Sechtem U, Achenbach S, et al. 2013 ESC guidelines on the management of stable coronary artery disease: the Task Force on the management of stable coronary artery disease of the European Society of Cardiology. Eur Heart J. 2013;34(38):2949–3003.
9. Tendera M, Fox K, Ferrari R, et al. Inadequate heart rate control despite widespread use of beta-blockers in outpatients with stable CAD: findings from the international prospective CLARIFY registry. Int J Cardiol. 2014;176(1):119–24.
10. Steg PG, Ferrari R, Ford I, et al. Heart rate and use of beta-blockers in stable outpatients with coronary artery disease. PLoS One. 2012;7(5):e36284.
11. Kalra PR, Morley C, Barnes S, et al. Discontinuation of beta-blockers in cardiovascular disease: UK primary care cohort study. Int J Cardiol. 2013;167(6):2695–9.
12. DiFrancesco D. Funny channels in the control of cardiac rhythm and mode of action of selective blockers. Pharmacol Res. 2006;53(5):399–406.
13. Amosova E, Andrejev E, Zaderey I, Rudenko U, Ceconi C, Ferrari R. Efficacy of ivabradine in combination with beta-blocker versus uptitration of beta-blocker in patients with stable angina. Cardiovasc Drugs Ther. 2011;25(6):531–7.
14. Tardif JC, Ponikowski P, Kahan T, et al. Effects of ivabradine in patients with stable angina receiving b-blockers according to baseline heart rate: an analysis of the ASSOCIATE study. Int J Cardiol. 2013;168(2):789–94.
15. Karpov YuA, Glezer MG, Vasyuk YuA, Saygitov RT, Shkolnik EL. Antianginal effectiveness and tolerability of ivabradine in patients with stable angina: CONTROL-2 study results. Cardiovasc Ther Prev. 2011;10(8):83–9 (in Russian).
16. Lopez-Sendon J, Swedberg K, McMurray J, et al. Expert consensus document on beta-adrenergic receptor blockers. Eur Heart J. 2004;25:1341–62.
17. Ponikowski P, Voors AA, Anker SD, et al. 2016 ESC guidelines for the diagnosis and treatment of acute and chronic heart failure: The Task Force for the diagnosis and treatment of acute and chronic heart failure of the European Society of Cardiology (ESC). Developed with the special contribution of the Heart Failure Association (HFA) of the ESC. Eur J Heart Fail. 2016;18:891–975.
18. Heusch G. Heart rate in the pathophysiology of coronary blood flow and myocardial ischaemia: benefit from selective bradycardic agents. Br J Pharmacol. 2008;153(8):1589–601.
19. Camici PG, Gloekler S, Levy BI, et al. Ivabradine in chronic stable angina: effects by and beyond heart rate reduction. Int J Cardiol. 2016;15(215):1–6.
20. Heusch G, Skyschally A, Schulz R. Cardioprotection by ivabradine through heart rate reduction and beyond. J Cardiovasc Pharmacol Ther. 2011;16(3–4):281–4.
21. Heusch G, Skyschally A, Gres P, Van Caster P, Schilawa D, Schulz R. Improvement of regional myocardial blood flow and function and reduction of infarct size with ivabradine: protection beyond heart rate reduction. Eur Heart J. 2008;29:2265–75.
22. Kleinbongard P, Gedik N, Witting P, Freedman B, Klocker N, Heusch G. Pleiotropic, heart rate-independent cardioprotection by ivabradine. Br J Pharmacol. 2015;172:4380–90.
23. Skalidis EI, Hamilos MI, Chlouverakis G, Zacharis EA, Vardas PE. Ivabradine improves coronary flow reserve in patients with stable coronary artery disease. Atherosclerosis. 2011;215:160–5.
24. Tagliamonte E, Cirillo T, Rigo F, et al. Ivabradine and bisoprolol on doppler-derived coronary flow velocity reserve in patients with stable coronary artery disease: beyond the heart rate. Adv Ther. 2015;32:757–67.
25. Tardif JC, Ponikowski P, Kahan T, ASSOCIATE Study Investigators. Efficacy of the I(f) current inhibitor ivabradine in patients with chronic stable angina receiving beta-blocker therapy: a 4-month, randomized, placebo-controlled trial. Eur Heart J. 2009;30(5):540–8.
26. Koester R, Kaehler J, Ebelt H, Soeffker G, Werdan K, Meinertz T. Ivabradine in combination with betablocker therapy for the treatment of stable angina pectoris in every day clinical practice. Clin Res Cardiol. 2010;99(10):665–72.
27. Werdan K, Perings S, Ko¨ster R, et al. Effectiveness of ivabradine treatment in different subpopulations with stable angina in clinical practice: a pooled analysis of observational studies. Cardiology. 2016;135(3):141–50.
28. Elder DH, Pauriah M, Lang CC, et al. Is there a Failure to Optimize theRapy in anGina pEcToris (FORGET) study? QJM. 2010;103(5):305–10.
29. Glezer MG, Saygitov RT. Antianginal efficacy and tolerability of ivabradine in the treatment of patients with stable angina: results of CONTROL study. Kardiologia. 2010;11:65–75. Adv Ther







