FERRI, A. CORSINI, R. PONTREMOLI
Lược dịch và hiệu đính: ThS.BS. NGUYỄN TRƯỜNG DUY*
BSNT. NGUYỄN NHẬT TÀI*
* Bộ môn Nội – Đại Học Y Dược Thành phố Hồ Chí Minh
Bảo vệ thận với Lercanidipine: Các nghiên cứu thí nghiệm
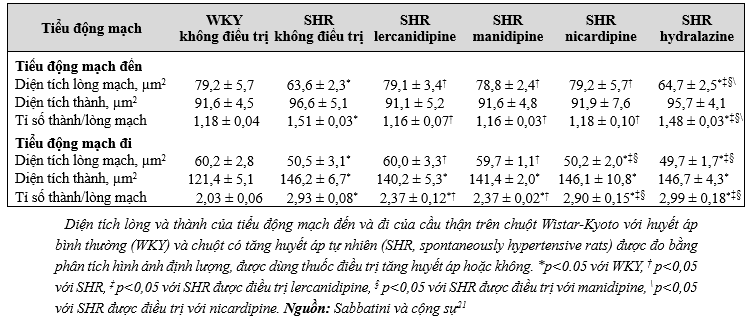
Lercanidipine gây giãn mạch ở cả tiểu động mạch đến và tiểu động mạch đi tại các vi mạch máu của thận trong một mô hình tiền lâm sàng trên chuột có tăng huyết áp (Bảng III)21. Việc sử dụng lercanidipine đã ngăn chặn sự dày của thành mạch và hẹp lòng mạch máu trong các động mạch kích thước nhỏ và các tiểu động mạch cầu thận của chuột Cohen-Rosenthal mắc bệnh đái tháo đường và tăng huyết áp (Hình 3)30. Mặc dù vậy, thông qua sự so sánh gián tiếp, những kết quả này có thể có các tác động đáng kể trên lâm sàng. Các thuốc chẹn kênh canxi nhóm DHP trước đây, gồm amlodipine, tác động chủ yếu lên kênh canxi loại L. Đáp ứng giãn mạch với các thuốc chẹn kênh canxi loại L chỉ được quan sát thấy ở các mạch máu nhỏ tiền vi cầu thận mà không ảnh hưởng đến các tiểu động mạch đi trong giường mạch máu thận. Điều này dẫn đến tăng áp lực mao mạch cầu thận và trong cầu thận, tăng tiểu protein và tăng tổn thương thận.
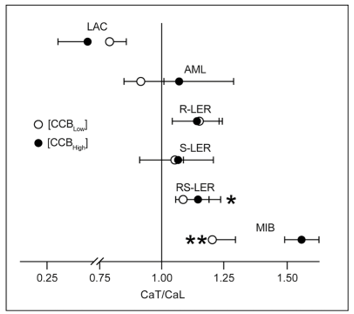
Hình 3. Hình ảnh phân tích các tiểu động mạch cầu thận của chuột Cohen-Rosenthal mắc bệnh đái tháo đường và tăng huyết áp (CRDH, Cohen-Rosenthal diabetic-hypertensive) được sử dụng hoặc không sử dụng lercanidipine. CCB: chẹn kênh canxi; LAC, lacidipine; AML, amlodipine; MIB, mibefradil; LER, lercanidipine; *p < 0,05; **p < 0,01 so với LAC (nồng độ thấp)
Ngược lại, lercanidipine, bằng cách giãn mạch cả tiểu động mạch đến và tiểu động mạch đi của các vi mạch máu thận, có thể điều chỉnh tình trạng tăng huyết áp tại cầu thận và có thể có tác dụng bảo vệ trong quá trình tiến triển tổn thương thận. Ở chuột bị cắt bỏ thận có chủ ý và bị tăng huyết áp sau đó, lercanidipine đã cho thấy làm giảm huyết áp, ngăn chặn sự tiến triển tổn thương thận và cải thiện các thay đổi mô bệnh học và nồng độ creatinin huyết thanh với protein niệu giảm đáng kể24. Tác dụng bảo vệ thận tương tự của lercanidipine đã được quan sát trên mô hình chuột được chuyển gen kép với tăng cường biểu hiện các gen renin và angiotensinogen của người31. Điều trị với lercanidipine đã ngăn ngừa tổn thương thận và tỉ lệ tử vong do angiotensin II gây ra. So với chuột không được điều trị, protein niệu giảm và nồng độ creatinin huyết thanh được duy trì trong khoảng bình thường. Ngoài ra, hiệu ứng kháng viêm và chống xơ hóa ở các mạch máu thận đã được quan sát với sự giảm thâm nhập của đơn bào, giảm hình thành chất nền ngoại bào và xơ hóa, kèm theo cải thiện độ sinh khả dụng của nitric oxit (NO, nitric oxide).
Thật vậy, lercanidipine đã cho thấy có khả năng ức chế protein kinase C và làm giảm nồng độ asymmetric dimethylarginine (ADMA) trong huyết tương, một chất ức chế tổng hợp NO, ở chuột được tăng biểu hiện các gen renin và angiotensinogen của người, với tăng nồng độ NO nội bào cao hơn. Các tác động trong tế bào này có vẻ liên quan đến giảm nồng độ canxi trong nội bào22.
Thuốc chẹn kênh canxi thế hệ thứ ba làm giảm áp lực cầu thận, phân suất lọc (FF, Filtration fraction) và protein niệu, với tác dụng bảo vệ thận tương tự như các chất ức chế hệ RAS16. Việc kết hợp các thuốc này có thể cung cấp các tác động bổ sung cho nhau vì thuốc chẹn kênh canxi và thuốc ức chế hệ RAS không có cùng cơ chế hoạt động như chất ức chế hệ RAS.
Thực tế, hai nghiên cứu18,32 đã ghi nhận lợi ích bổ sung khi lercanidipine được kết hợp với các thuốc ức chế hệ RAS15. Do đó, phối hợp liều cố định giữa lercanidipine với enalapril rất phù hợp để kiểm soát huyết áp và tổn thương thận liên quan đến tăng huyết áp. Các thuốc CKCa là những chất gây giãn mạch mạnh từ đó kích hoạt phản xạ của hệ thần kinh giao cảm và hệ RAS. Do đó, các thuốc ƯCMC có thể bù trừ được cho sự kích hoạt quá mức này. Ngoài ra, thuốc CKCa thúc đẩy cân bằng natri âm và tăng nồng độ angiotensin II, và vì lý do này, ƯCMC có thể tăng cường tác dụng hạ huyết áp. Trong khi đó, việc đồng thời sử dụng cả hai loại thuốc trên có thể giảm các biến cố bất lợi, đặc biệt là phù ngoại biên – do tăng áp lực trong mao mạch thứ phát sau giảm trương lực chọn lọc chỉ ở các tiểu động mạch trước mao mạch trong khi ngăn chặn dòng canxi nhập bào . Các ƯCMC giảm phù chi dưới gây ra bởi CKCa do khả năng giãn cả giường mạch máu động mạch và khả năng chứa của máu của tĩnh mạch32. Tóm lại, có bằng chứng mạnh để kết hợp lercanidipine với enalapril.
Bảng III. Các thông số của tiểu động mạch đến và đi trên chuột Wistar-Kyoto với huyết áp bình thường và chuột có tăng huyết áp tự nhiên theo các điều trị khác nhau.
Bảo vệ thận với Lercanidipine và phối hợp Lercanidipine/Enalapril: Các nghiên cứu lâm sàng
Một số nghiên cứu lâm sàng đã đánh giá hiệu quả bảo vệ thận của lercanidipine hoặc lercanidipine/ enalapril (Bảng IV). Trong nghiên cứu DIAL (Diabete Ipertensione Albuminuria Lercanidipina), 277 bệnh nhân có đái tháo đường típ 2 có tăng huyết áp nhẹ đến trung bình và tiểu albumin vi lượng dai dẳng được tuyển chọn, và trong số đó có 180 người được ngẫu nhiên điều trị với lercanidipine (10 – 20 mg/ngày) hoặc ramipril (5 – 10 mg/ngày). Sau thời gian theo dõi 9 – 12 tháng, lercanidipine giảm tỉ lệ bài tiết albumin trong nước tiểu tương tự ramipril (-17,4 ± 65 µg/phút, p < 0,05 và -19,7±52,5 µg/phút,
p < 0,05) tương ứng trong nhóm lercanidipine và ramipril33. Một vài nghiên cứu khác đã đánh giá hiệu quả của lercanidipine khi dùng đơn trị hoặc khi phối hợp với các thuốc ức chế hệ RAS trên bệnh nhân có bệnh thận mạn và/hoặc có albumin niệu34-36. Robles và cộng sự34 đã nghiên cứu tác dụng bảo vệ trên chức năng thận khi bổ sung lercanidipine (10 mg/ngày) ở bệnh nhân mắc bệnh thận mạn và huyết áp không được kiểm soát dù đã được điều trị với thuốc ƯCMC hoặc CTTA. Tổng cộng có 203 bệnh nhân mắc bệnh thận mạn và huyết áp cao hơn mức khuyến cáo được tuyển chọn (63% dùng thuốc ƯCMC và 37% dùng CTTA), và có 175 bệnh nhân được đánh giá. Trong khoảng thời gian theo dõi 6 tháng, lercanidipine đã chứng minh là hiệu quả và an toàn, giảm huyết áp hơn nữa (huyết áp tâm thu từ 162 xuống 132 mmHg, huyết áp tâm trương từ 93 xuống 78 mmHg) đồng thời còn giảm protein trong nước tiểu (từ 3,5 xuống 2,8 g/ngày). Nồng độ creatinin huyết tương không thay đổi, nhưng độ thanh thải creatinin tăng lên (41,8 ± 16 tại thời điểm ban đầu và 45,8 ± 18 mL/phút sau 6 tháng, p = 0,019)34. Nhóm nghiên cứu này cũng báo cáo một nghiên cứu tương tự trên 68 bệnh nhân tăng huyết áp kèm suy thận mạn trong một nghiên cứu nhãn mở 35. Bệnh nhân đã được dùng một thuốc CTTA hoặc một thuốc ƯCMC nhưng không đạt được mức huyết áp mục tiêu sẽ tiếp tục được điều trị thêm lercanidipine (20 mg/ngày) và theo dõi trong 6 tháng. Điều thú vị là: mặc dù huyết áp tâm thu và tâm trương giảm (từ 152/86 mmHg ở thởi điểm ban đầu xuống còn 135/77 mmHg sau 6 tháng, với mức huyết áp giảm trung bình lần lượt là -16,8/-9,3 mmHg) thấp hơn so với nghiên cứu ZAFRA, lercanidipine giảm lượng protein niệu gấp 2 lần trong nghiên cứu này với hiệu quả tuyến tính theo liều, điều này có vẻ độc lập với sự thay đổi huyết áp, ít nhất là một phần36. Tác dụng bảo vệ thận, ngăn tình trạng tiểu albumin có thể do tác động của lercanidipine trên huyết động học tại cầu thận và một số tác động khác như ức chế sự tăng sinh tế bào gian mao mạch và các tác dụng thông qua trung gian của endothelin, các tác dụng chống oxy hóa liên quan đến tăng hoạt động tổng hợp nitric oxide. Lượng protein niệu ban đầu trong nghiên cứu là 1,63 ±1,34 g/ngày và giảm đi 23% trong tháng đầu tiên, 37% sau 3 tháng và 33% sau 6 tháng (p <0,001 ở tất cả các mốc thời gian) (Hình 4)35.
Cuối cùng, trong nghiên cứu RED LEVEL (REnal Disease: LErcanidipine Valuable Effect on urine protein Losses), hiệu quả của các điều trị phối hợp lercanidipine/enalapril và amlodipine/enalapril được so sánh trực tiếp trong một nghiên cứu tiến cứu, nhãn mở, ngẫu nhiên, mù đôi, đa trung tâm kéo dài 12 tháng trên bệnh nhân tăng huyết áp kèm tiểu albumin 36,37. Theo thời gian, so với giá trị ban đầu albumin niệu giảm đáng kể chỉ ghi nhận trong nhóm được điều trị bằng lercanidipine/enalapril [thay đổi so với giá trị ban đầu : -162,5 mg/24 h (p = 0,04), -425,8 mg/24 h (p = 0,001), -329,0 mg/24 h (p = 0,001) tương ứng tại tháng 3, 6 và 12]. Tuy nhiên, albumin niệu lại không thay đổi đáng kể ở bệnh nhân được điều trị bằng kết hợp amlodipine/enalapril. Thay đổi trị số huyết áp đáng kể ở cả hai nhóm điều trị, tuy không có sự khác biệt có ý nghĩa36.
Ý kiến chuyên gia
Trong khi giảm huyết áp hiệu quả là yếu tố then chốt để bảo vệ thành công tim mạch và thận, các nhóm thuốc điều trị tăng huyết áp khác nhau có các đặc tính bảo vệ cơ quan đích khác nhau ngoài việc giảm trị số huyết áp. Các thuốc CKCa trước đây được xem là những thuốc hạ áp mạnh nhưng không hiệu quả bằng các thuốc ức chế hệ RAS trong việc bảo tồn chức năng thận kéo dài.
Lercanidipine là một thuốc CKCa thế hệ thứ ba với vai trò trong điều trị tăng huyết áp đã được xác định. Lercanidipine có đặc điểm dược lực học đặc biệt, khác với các loại thuốc chẹn kênh canxi thế hệ đầu tiên và thứ hai, vì nó làm giãn cả tiểu động mạch đến và tiểu động mạch đi của cầu thận đồng thời bảo tồn áp lực trong cầu thận. Tác động này dẫn đến những thay đổi thuận lợi về huyết động học tại thận và mang lại lợi ích lâm sàng so với đặc tính nhóm. Trong khi các loại thuốc CKCa khác sẽ bảo vệ thận nếu được sử dụng kết hợp với ƯCMC hoặc CTTA thì lercanidipine bảo vệ chức năng thận ngay khi dùng đơn trị. Khi sử dụng đơn trị hoặc phối hợp với ƯCMC, lercanidipine đã được chứng minh mang lại hiệu quả bảo vệ mạch máu thận trong thí nghiệm và giảm protein niệu trong các nghiên cứu lâm sàng35,36.
Bảng IV. Các thử nghiệm lâm sàng về tác động bảo vệ thận của lercainidipine trong đơn trị hoặc kết hợp với ƯCMC/CTTA
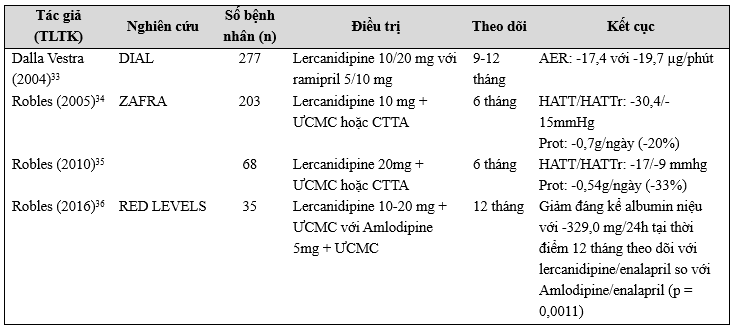
Prot: thay đổi protein niệu (g/24h); AER: thay đổi tỉ lệ bài tiết albumin (albumin excretion rate) (µg/phút). ƯCMC = thuốc ức chế men chuyển; CTTA = thuốc chẹn thụ thể Angiotensin II; HATT = huyết áp tâm thu; HATTr = huyết áp tâm trương (mmHg)
Tác động bảo vệ thận và ngăn tình trạng tiểu albumin của lercanidipine có thể do tác động đặc hiệu của thuốc lên huyết động học tại cầu thận và những tác động khác như ức chế tăng sinh các tế bào gian mao mạch, ức chế các tác động do endothelin gây ra trên thận và tăng hoạt động tổng hợp nitric oxit (NO), điều này đã được chứng minh có tác dụng chống oxy hóa35,36. Việc giảm tình trạng stress oxy hóa khi sử dụng lercanidipine đi kèm với các lợi ích tích cực trên lâm sàng, như ức chế sự tăng sinh tế bào nội mạc mới và tế bào cơ trơn của mạch máu và và tích tụ cholesterol38-40.
Tác động của lercanidipine trong giảm đạm niệu có lẽ phụ thuộc vào liều lượng và không liên quan với hoạt tính hạ huyết áp32,33. Bảo vệ thận với sự giảm đáng kể tiểu albumin vi lượng và cải thiện độ thanh thải creatinin đã được ghi nhận trên bệnh nhân đái tháo đường và suy thận, đây là một nhóm bệnh nhân có nguy cơ cao của tổn thương cơ quan đích.
Do lercanidipine được dung nạp tốt và đi kèm nguy cơ phù mắt cá chân thấp, thuốc có thể được xem là một công cụ trị liệu dễ sử dụng cho việc kiểm soát tăng huyết áp trên nhóm bệnh nhân có nguy cơ cao tổn thương thận.
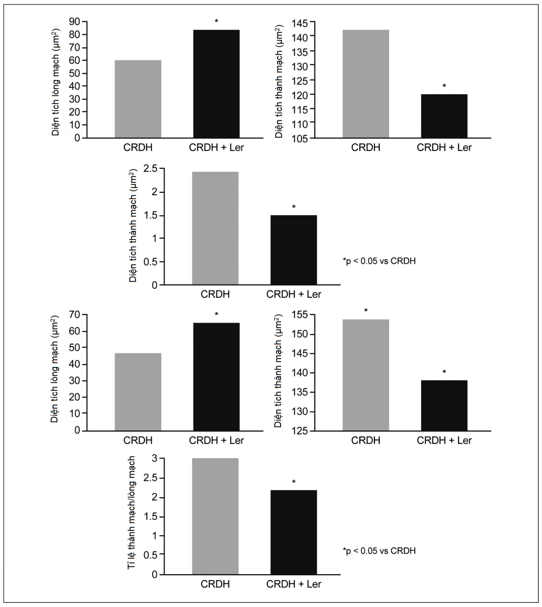
Hình 4. Phần trăm giảm protein niệu sau 1, 3 và 6 tháng điều trị với lercanidipine 20mg/ngày. Kết hợp với ƯCMC hoặc CTTA, trên những bệnh nhân tăng huyết khó kiếm soát có bệnh thận mạn. Dữ liệu từ Rovles và cộng sự35.
Kết luận
Lercanidipine là thuốc điều trị tăng huyết áp hiệu quả và an toàn, có thể được sử dụng cho những bệnh nhân có nguy cơ tổn thương thận. Các nghiên cứu trên bệnh nhân tăng huyết áp kèm đái tháo đường hoặc bệnh thận mạn đã chứng minh lercanidipine có tác dụng bảo vệ thận vì lercanidipine giãn tiểu động mạch đến và tiểu động mạch đi của cầu thận, bảo tồn áp lực mao mạch trong cầu thận. Đáng chú ý, lercanidipine đã được chứng minh làm giảm đạm niệu, tác dụng đặc biệt trong nhóm thuốc chẹn kênh canxi và đây được công nhận là một yếu tố nguy cơ cho các biến cố tim mạch ở bệnh nhân tăng huyết áp. Điểm đặc biệt này đã được xác nhận thông qua một thử nghiệm so sánh trực tiếp, trong đó protein niệu đã giảm sau khi sử dụng phối hợp lercanidipine/enalapril, nhưng không giảm khi sử dụng phối hợp amlodipine/enalapril36. Tuy nhiên, RED LEVEL là nghiên cứu so sánh trực tiếp duy nhất giữa các thuốc CKCa khác nhau về mặt bảo vệ thận. Do đó, cần thận trọng khi rút ra kết luận về độ an toàn dài hạn trên thận đối với các loại thuốc chẹn kênh canxi khác nhau. Tuy nhiên, dựa trên dữ liệu được thảo luận trong bài báo này, lercanidipine với cơ chế tác động đặc biệt tại thận, cũng như khả năng làm giảm albumin niệu đã được chứng minh, có thể là loại CKCa lý tưởng để sử dụng cho bệnh nhân tăng huyết áp có nguy cơ tổn thương thận.
Tài liệu tham khảo:
- NCD Risk Factor Collaboration (NCD-RisC). Worldwide trends in hypertension prevalence and progress in treatment and control from 1990 to 2019: a pooled analysis of 1201 population-representative studies with 104 million participants. Lancet 2021; 398: 957-980.
- Williams B, Mancia G, Spiering W, Agabiti Rosei E, Azizi M, Burnier M, Clement DL, Coca A, de Simone G, Dominiczak A, Kahan T, Mahfoud F, Redon J, Ruilope L, Zanchetti A, Kerins M, Kjeldsen SE, Kreutz R, Laurent S, Lip GYH, McManus R, Narkiewicz K, Ruschitzka F, Schmieder RE, Shlyakhto E, Tsioufis C, Aboyans V, De sormais I; ESC Scientific Document Group. 2018 ESC/ESH Guidelines for the management of arterial hypertension. Eur Heart J 2018; 39: 3021-3104.
- Tocci G, Muiesan ML, Parati G, Agabiti Rosei E, Ferri C, Virdis A, Pontremoli R, Mancia G, Borghi C, Volpe M; Working Group of the Italian Society of Hypertension (SIIA) and SIIA Foundation. Trends in Prevalence, awareness, treatment, and control of blood pressure recorded from 2004 to 2014 during world hypertension day in Italy. J Clin Hypertens (Greenwich) 2016; 18: 551-556.
- Rea F, Savaré L, Franchi M, Corrao G, Mancia G. Adherence to treatment by initial antihypertensive mono and combination therapies. Am J Hypertens 2021; 34: 1083-1091.
- Rea F, Corrao G, Merlino L, Mancia G. Initial antihypertensive treatment strategies and therapeutic inertia. Hypertension 2018; 72: 846-853.
- Leoncini G, Viazzi F, Pontremoli R. Chronic kidney disease and albuminuria in arterial hypertension. Curr Hypertens Rep 2010; 12: 335-341.
- Pontremoli R, Leoncini G, Ravera M, Viazzi F, Vettoretti S, Ratto E, Parodi D, Tomolillo C, Deferrari G. Microalbuminuria, cardiovascular, and renal risk in primary hypertension. J Am Soc Nephrol 2002; 13: S169-S172.
- Carlström M, Wilcox CS, Arendshorst WJ. Renal autoregulation in health and disease. Physiol Rev. 2015; 2: 405-511.
- Mennuni S, Rubattu S, Pierelli G, Tocci G, Fofi C, Volpe M. Hypertension and kidneys: unraveling complex molecular mechanisms underlying hypertensive renal damage. J Hum Hypertens. 2014; 28: 74-79.
- Neuringer JR, Brenner BM. Hemodynamic theory of progressive renal disease: a 10-year update in brief review. Am J Kidney Dis 1993; 22: 98-104.
- Viazzi F, Leoncini G, Grassi G, Pontremoli R. Antihypertensive treatment and renal protection: Is there a J-curve relationship? J Clin Hypertens (Greenwich) 2018; 20: 1560-1574.
- Bakris G. Are there effects of renin-angiotensin system antagonists beyond blood pressure control? Am J Cardiol 2010; 105: 21A-29A.
- Jamerson K, Weber MA, Bakris GL, Dahlöf B, Pitt B, Shi V, Hester A, Gupte J, Gatlin M, Velazquez EJ; ACCOMPLISH Trial Investigators. Benazepril plus amlodipine or hydrochlorothiazide for hypertension in high-risk patients. N Engl J Med 2008; 359: 2417-2428.
- Barrios V, Escobar C, Echarri R. Fixed combinations in the management of hypertension: perspectives on lercanidipine-enalapril. Vasc Health Risk Manage 2008; 4: 847-853.
- Burnier M. Renal protection with calcium antagonists: the role of lercanidipine. Curr Med Res Opin 2013; 29: 1727-1735.
- Sabbatini M, Leonardi A, Testa R, Tomassoni D, Vitaioli L, Amenta F. Effects of dihydropyridine-type Ca2+ antagonists on the renal arterial tree in spontaneously hypertensive rats. J Cardiovasc Pharmacol 2002; 39: 39-48.
- Tocci G, Palano F, Pagannone E, Chin D, Ferrucci A, Volpe M. Fixed-combination therapies in hypertension management: focus on enalapril/lercanidipine. Expert Rev Cardiovasc Ther. 2009; 7:115-123.
- Borghi C, Cicero AF. Rationale for the use of a fixed-dose combination in the management of hypertension: efficacy and tolerability of lercanidipine/enalapril. Clin Drug Investig 2010; 30: 843-854.
- Gasser R, Klein W, Köppel H. Lercanidipine, a new third generation Ca-antagonist in the treatment of hypertension. J Clin Basic Cardiol 1999; 2: 169-174.
- Brixius K, Gross T, Tossios P, Geissler HJ, Mehlhorn U, Schwinger RH, Hekmat K. Increased vascular selectivity and prolonged pharmacological efficacy of the L-type Ca2+ channel antagonist lercanidipine in human cardiovascular tissue. Clin Exp Pharmacol Physiol 2005; 32: 708-713.
- Sabbatini M, Leonardi A, Testa R, Vitaioli L, Amenta F. Effect of calcium antagonists on glomerular arterioles in spontaneously hypertensive rats. Hypertension 2000; 35: 775-779.
- Grassi G, Robles NR, Seravalle G, Fici F. Lercanidipine in the management of hypertension: an update. J Pharmacol Pharmacother 2017; 8: 155-165.
- Hayashi K, Homma K, Wakino S, Tokuyama H, Sugano N, Saruta T, Itoh H. T-type Ca channel blockade as a determinant of kidney protection. Keio J Med 2010; 59: 84-95.
- Hayashi K, Ozawa Y, Fujiwara K, Wakino S, Kumagai H, Saruta T. Role of actions of calcium antagonists on efferent arterioles–with special references to glomerular hypertension. Am J Nephrol 2003; 23: 229-244.
- Cerbai E, Mugelli A. Lercanidipine and T-type calcium current. Eur Rev Med Pharmacol Sci 2018; 22: 4025-4031.
- Barchielli M. Lercanidipine pharmacokinetics. J Cardiovasc Pharmacol 1997; 29: S1-S15.
- Lercanidipine Smpc. Available at: https://www.medicines.org.uk/emc/product/5802/smpc#gref .
- Hanauer Schaab E, Lanchote VL, Balthazar Nardotto GH, Marques Pereira MP, Dantas M, Paiva CE, Barbosa Coelho E. Effect of lercanidipine on the pharmacokinetics-pharmacodynamics of carvedilol enantiomers in patients with chronic kidney disease. J Clin Pharmacol 2020; 60: 75-85.
- Dinnendahl V, Fricke U. Arzneistoff-Profile (in German). Eschborn, Germany: Govi Pharmazeutischer Verlag. Arzneistoff-Profile (in German), 2015.
- Rosenthal T, Rosenmann E, Tomassoni D, Amenta F. Effect of lercanidipine on kidney microanatomy in Cohen-Rosenthal diabetic hypertensive rats. J Cardiovasc Pharmacol Ther 2007; 12: 145- 152.
- Menne J, Park JK, Agrawal R, Lindschau C, Kielstein JT, Kirsch T, Marx A, Muller D, Bahlmann FH, Meier M, Bode-Böger SM, Haller H, Fliser D. Cellular and molecular mechanisms of tissue protection by lipophilic calcium channel blockers. FASEB J 2006; 20: 994-996.
- Borghi C, Santi F. Fixed combination of lercanidipine and enalapril in the management of hypertension: focus on patient preference and adherence. Patient Prefer Adherence 2012; 6: 449- 455.
- Dalla Vestra M, Pozza G, Mosca A, Grazioli V, Lapolla A, Fioretto P, Crepaldi G. Effect of lercanidipine compared with ramipril on albumin excretion rate in hypertensive type 2 diabetic patients with microalbuminuria: DIAL study (diabete, ipertensione, albuminuria, lercanidipina). Diabetes Nutr Metab 2004; 17: 259-266.
- Robles NR, Ocon J, Gomez CF, Manjon M, Pastor L, Herrera J, Villatoro J, Calls J, Torrijos J, Rodríguez VI, Rodriguez MM, Mendez ML, Morey A, Martinez FI, Marco J, Liebana A, Rincon B, Tornero F. Lercanidipine in patients with chronic renal failure: the ZAFRA study. Ren Fail 2005; 27: 73-80.
- Robles NR, Romero B, de Vinuesa EG, Sánchez-Casado E, Cubero JJ. Treatment of proteinuria with lercanidipine associated with renin–angiotensin axis-blocking drugs. Ren Fail 2010; 32: 192-197.
- Robles NR, Calvo C, Sobrino J, Espinel E, Esteban R, Mateos L, Macias JF. Lercanidipine valuable effect on urine protein losses: the RED LEVEL study. Curr Med Res Opin 2016; 32: 29-34.
- Hansson L, Hedner T, Dahlöf B. Prospective randomized open blinded end-point (PROBE) study. A novel design for intervention trials. Prospective Randomized Open Blinded End-Point. Blood Press 1992; 1: 113-119.
- Wu JR, Liou SF, Lin SW, Chai CY, Dai ZK, Liang JC, Chen IJ, Yeh JL. Lercanidipine inhibits vascular smooth muscle cell proliferation and neointimal formation via reducing intracellular reactive oxygen species and inactivating Ras-ERK1/2 signaling. Pharmacol Res 2009; 59: 48-56.
- ALOGPS Available at: http://www.vcclab.org/lab/alogps.
- Lercanidipine S Available at: https://pubchem.ncbi.nlm.nih.gov/compound/S_ Lercanidipine#- section=2D-Structure.







