BS. HUỲNH ANH KIỆT*
BS. NGUYỄN THANH HIỀN
*Khoa nội TM, BV Đại Học Y Dược, Tp. Hồ Chí Minh
I. MỞ ĐẦU
Thay thế một van tim bị bệnh bằng một van tim nhân tạo sẽ đánh đổi bệnh lý diễn tiến tự nhiên với các biến chứng liên quan đến van tim nhân tạo. Các biến chứng bao gồm tắc nghẽn van nhân tạo(huyết khối và pannus), sự không phù hợp giữa bệnh nhân và thiết bị nhân tạo, biến cố tắc mạch, chảy máu, hở van tim nhân tạo (trong van và cạnh van), viêm nội tâm mạc nhiễm trùng và tán huyết liên quan đến van nhân tạo1,2.
Van tim nhân tạo cơ học, mặc dù bền hơn so với van nhân tạo sinh học, nhưng dễ gây huyết khối hơn và cần dùng thuốc kháng đông suốt đời. Rối loạn chức năng van cơ học có thể do 4 hiện tượng chính: 1) huyết khối; 2) pannus xơ hoá tiến triển vào bên trong; 3) thoái hóa; và 4) viêm nội tâm mạc.Những hiện tượng này có thể xảy ra đồng thời, vì vậy việc xác định nguyên nhân chính của rối loạn chức năng van cơ học là rất quan trọng để có cách xử trí thích hợp.3 Bài viết này tập trung vào chiến lược chẩn đoán và điều trị huyết khối gây tắc nghẽn van nhân tạo cơ học.
II. TỶ LỆ VÀ NGUYÊN NHÂN
Tỷ lệ huyết khối van nhân tạo hàng năm ước tính dao động từ 0,1% đến 5,7%, tỷ lệ caotrong vòng 3 tháng kể từ khi phẫu thuật, tỉ lệ xảy ra cao hơn đối với van hai lá hoặc van ba lá so với van động mạch chủ.
Về mặt lịch sử, van cơ học có thể được nhóm thành 3 thiết kế chính: van bi, đĩa nghiêng và van hai lá. Trong khi các thiết kế hai lá van đã trở thành tiêu chuẩn cho các loại van hiện đại, van đĩa nghiêng cũ hơn và van bi vẫn có thể gặp ở những bệnh nhân lớn tuổi và khả năng bị huyết khối cao hơn. Van đĩa nghiêng thường liên quan đến huyết khối van nhân tạonặng nề hơn, ngượcvới van bi và van hai lá,do tại van có rối loạn dòng chảy và máu bị ứ đọng thúc đẩy sự hình thành huyết khối, mô phát triển quá mức và vôi hóa.
Dòng chảy tạo ra lực xé cao có thể dẫn đến tổn thương tế bào máu và kích hoạt tiểu cầu.Ngoài ra, trong khi lớp nội mô lành mạnh chống lại sự hình thành huyết khối, bề mặt van nhân tạo cơ họcthúc đẩy quá trình đông máu thông qua các quá trình phức tạp bao gồm hấp phụ protein; kết dính tiểu cầu, bạch cầu và hồng cầu; tạo thrombin; và kích hoạt bổ thể4.
III. LÂM SÀNG VÀ CHẨN ĐOÁN
III.1. BIỂU HIỆN LÂM SÀNG
Biểu hiện của huyết khối van nhân tạo có một loạt các triệu chứng lâm sàng phụ thuộc phần lớn vào mức độ nghiêm trọng và mức độ tắc nghẽn van tim và/hoặc hở. Huyết khối van nhân tạo tắc nghẽn thường có các dấu hiệu và triệu chứng từ suy tim mất bù đến sốc tim, đặc biệt nếu chẩn đoán bị trì hoãn. Tuân thủ kém, điều trị gián đoạn, hoặc INR dưới mức mục tiêukhi dùng kháng đông là phổ biến5.
Thời gian từ khi thay van timđến khi có rối loạn chức năng cũng có thể giúp xác định nguyên nhân. Rối loạn chức năng van sớm (ví dụ, rò rỉ cạnh van, bệnh nhân-van nhân tạo không phù hợp, hở van tim, viêm nội tâm mạc) thường liên quan đến những sự cốkỹ thuật trong quá trình phẫu thuật hoặc nhiễm trùng. Rối loạn chức năng van muộn (ví dụ pannus, huyết khối và thuyên tắc huyết khối) thay đổi nhiều hơn tùy theo loại van nhân tạo và khả năng sinh huyết khối, cũng như các yếu tố liên quan đến bệnh nhân (ví dụ, tình trạng tăng đông, điều trị khángđông không liên tục).
Khi khám thực thể, có thể không có tiếng lách tách liên quan đến đóng mở van, âm thổi mới, dấu hiệu phù phổi và suy tim, di chứng của thuyên tắcphổi do huyết khối hoặc thuyên tắc hệ thống.Đột quỵ thiếu máu cục bộ cấp tính là biểu hiện thường gặp nhất của thuyên tắc vantim nhân tạo bên trái6.
Chẩn đoán phụ thuộc nhiều vào khả năng nghi ngờ trên lâm sàng caovà hình ảnh học được thực hiện nhanh chóng, với mỗi phương thức hỗ trợchẩn đoán đều có những lợi ích và hạn chế riêng.
III.2. HÌNH ẢNH HỌC ĐA PHƯƠNG THỨC
Có nhiều phương thức hình ảnh họcđược sử dụng để xác định nguyên nhân, vị trí, mức độ nặngvà những thay đổi huyết động liên quan đến huyết khối van nhân tạo. Độ chênh áp qua van tăng lên, giảm khả năng vận động lá van, hở van tim và nhìn thấy huyết khối là những phát hiện đặc biệt liên quan huyết khối van nhân tạo.
2.1. SIÊU ÂM TIM
Đánh giá ban đầu huyết khối van tim nhân tạo bằng siêu âm tim 2 chiều (2D) hoặc 3D tập trung vào hình thái, tính di động của lá van và sự hiện diện của huyết khối. Van tim cơ học xuất hiện dưới dạng cấu trúc phản âm với các mức độ tạo bóng xảo ảnh khác nhau, tùy thuộc vào vị trí van và mặt phẳng hình ảnh. Ở các van hoạt động bình thường, có thể dễ dàng đánh giá được chuyển động của lá van. Siêu âm tim M-mode có thể được sử dụng để tăng độ phân giải thời gian nhằm xác định tốt hơn chuyển động đặc trưng của lá van. Việc xác định huyết khối phụ thuộc vào kích thước và vị trí, với bóng mờ củaxảo ảnh là hạn chế chính, che khuất các khu vực phía xa van. Mỗi van tim cơ học có một góc đóng và mở dự kiến do nhà sản xuất xác định trước và có thể quan sát thấy sai lệch. Góc mở/đóng của van hai lá cơ học có thể được xác định chính xác bằng siêu âm tim qua thành ngực ở 85% và bằng siêu âm tim quathực quản ở 100% bệnh nhân, bất kể vị trí van6.
Siêu âm tim Doppler màu
Tắc nghẽn van có thể được đánh giá bằng cách sử dụng Doppler màu, biểu hiện là tốc độ dòngmáu tăng cao và gia tốc dòng chảy từ vị trí tắc nghẽn tương ứng với mức độ nghiêm trọng. Hình ảnh dòng máu qua van bị hạn chế, một dấu hiệu cho thấy sự hạn chế vận động của lá van và có thể do huyết khối7.Khi van đóng không hoàn toàn, có thể xuất hiện hiện tượng hở van bất thường, có thể là hởtrongvan hoặc hởcạnh van, nguyên nhân đầu tiên là do chuyển động của các đĩa van bị giảm do sùi, pannus hoặc huyết khối cản trởlá vanđónghoàn toàn.Mặt khác, rò cạnh van xảy ra do đứtđường chỉ khâudo lỗi phẫu thuật, khâu hỏng, đứt vòng vanhoặc viêm nội tâm mạc. Việc phân biệt giữa 2 loại này là rất quan trọng, vì nó giúp xác định nguyên nhân rối loạn chức năng van vàchọn phương pháp điều trị phù hợp. Siêu âm tim qua thực quản có thể tốt hơn trong việc xác định nguyên nhân và vị trí hở van, đặc biệt trong các trường hợp có bóng lưng, Doppler màu 3D đóngvai trò quan trọng trong việc xác định vị trí và mức độ nặng8.
Doppler quang phổ
Độ chênh áp qua van nhân tạo được xác định bởi diện tích lỗ hiệu quả (EOA, the effective orifice area), thể tích máu và khoảng thời gian mà dòngmáu di chuyển. Như vậy, tắc nghẽn nặng, thể tích trào ngược, cung lượng tim và nhịp tim đều ảnh hưởng đến mứcđộ chênh áp qua van. Tất cả các van cơ học vốn có độ chênh áp qua van cao hơn so với van tự nhiên bình thường và độ dốc dự kiến tuỳ thuộc từng loại và kích cỡ van. Tắc nghẽn van nhân tạo thường được định nghĩa là độ chênh áp trung bình qua van tăng >50% (hoặc tăng >10 mmHg qua van động mạch chủ nhân tạo) so với giá trị ban đầu sau phẫu thuật8. Lưu ý rằng độ chênh áp tăng cao cũng có thể có ở bệnh nhâncópannus, thoái hóa van, lưu lượng dòng chảy cao hoặc bệnh nhân với thiết bị nhân tạo không phù hợp.
2.2. SOI HUỲNH QUANG
Soi dưới màng huỳnh quanglà một phương pháp không xâm lấn để đánh giá chuyển động của lá van cơ học, đặc biệt ở những bệnh nhân có hình ảnh van tim trên siêu âm tim qua thành ngựcdưới mức tối ưu hoặc cóbất thường nhưng không thể kết luận. Đối với van hai lá cơ học, các đĩa có thể được hiển thị trực tiếp, các góc mở và đóng được đo trong chế độ xem trực diện, sau đó được so sánh với các góc “bình thường” do mỗi nhà sản xuất van báo cáo9.Nội soi huỳnh quang cũng có thể được sử dụng để theo dõi chức năng van sau can thiệp. Trong một nghiên cứu liên tiếp ở 82 bệnh nhân nghi ngờ huyết khối van nhân tạo cơ học được đánh giá bằng phương pháp soi huỳnh quang, độ nhạy và độ đặc hiệu để chẩn đoán tắc van nhân tạo ở van hai lá hoặc van động mạch chủ lần lượt là 87% và 78%. Tương tự như vậy, các giá trị tiên đoán dương tính và âm tính lần lượt là 80% và 91%10.
3.3.CT TIM VÀ CỘNG HƯỞNG TỪ
Ở những bệnh nhân mà siêu âm tim hoặc soi huỳnh quang không thể kết luận được, CT đa đầu dò có thể hữu ích,vì nó có thể đánh giá mức độ hạn chế của lá van khi soi tia huỳnh quang bị giới hạn bởi các hình có thể đạt được của C-arm trong phòngthông tim.
Các nghiên cứu đã cho thấy không có vai trò tương đương giữa 2 phương thức hình ảnh này 11.Tương tự như vậy, CT có thể cung cấp thêm thông tin để xác định nguyên nhân gây tắc nghẽn van nhân tạo khi siêu âm tim chưa xác định được chẩn đoán . Nguyên nhân của rối loạn chức năng van có thể được phân biệt bằng cách sử dụng các mức độ giảm đậm độ để giúp phân biệt huyết khối với pannus.
Trong khi không có chống chỉ định đối với cộng hưởng từ tim để đánh giá huyết khối van nhân tạo, các xảo ảnh thường cản trở đáng kể việc đánh giá chính xác cấu trúc và chức năng. Hiện tại, cộng hưởng từ tim không được khuyến cáotrong bất kỳ hướng dẫn nào.
IV. ĐIỀU TRỊ
1. Những yếu tố chính cần cân nhắc trước khi khởi trị và một số biện pháp chung
- Điều trị tắc nghẽnvan nhân tạo cơ học dựa trên biểu hiện lâm sàng (ví dụ: các triệu chứng và dấu hiệu của suy tim) và nguyên nhân gây tắc nghẽn. Huyết khối hình thành trên van nhân tạo cơ học có thể gây tắc nghẽn hoặc không và có thể gây ra các biến cố thuyên tắc huyết khối3.
- Tắc van nhân tạo cơ học có thể do huyết khối hoặc pannus. Việc đánh giá tắc nghẽn van nhân tạo cơ học tập trung vào việc phân biệt hai nguyên nhân này vì huyết khối có thể được điều trị bằng thuốc chống đông, tiêu sợi huyết hoặc phẫu thuật van (lấy huyết khối hoặc thay van tim), trong khi pannus chỉ có thể được điều trị bằng phẫu thuật.
- Viêm nội tâm mạc nhiễm trùng hiếm khi gây tắc nghẽn van tim nhưng vẫn cần được xem xét trong quá trình đánh giá chẩn đoán và điều trị.
Điều trị ban đầu: Hỗ trợ hô hấp khi cần thiết, điều trị tình trạng quá tải thể tích bằng thuốc lợi tiểu thận trọng. Nếu INR thấp hơn ngưỡng điều trị, xem xét dùng kháng đông heparin không phân đoạn (UFH). Bệnh nhân bị tắc nghẽn van nhân tạo có triệu chứng, các phương pháp điều trị nội khoa như thuốc lợi tiểu và thuốc hạ huyết áp có nguy cơ gây huyết động không ổn định.
Đánh giá cá thể hóa bệnh nhân để chọn phương pháp điều trị — Đối với bệnh nhân bị tắc nghẽn van nhân tạo có chỉ định phẫu thuật van hoặc tiêu sợi huyết, các tác giả khuyên nên chuyển bệnh nhân đến nhóm chuyên gia về bệnh van tim để đánh giá đầy đủcác nguy cơ và lợi ích của phẫu thuật và tiêu sợi huyết8.
♦ Các yếu tố sau có lợi cho điều trị tiêu sợi huyết:
- Đặc điểm lâm sàng – Nguy cơ của phẫu thuật cao, phân độ chức năng từ I đến III theo Hiệp hội Tim mạch New York (NYHA), không có chống chỉ định tiêu sợi huyết, lần đầu tiên có huyết khối van.
- Chỉ định đồng thời – Không cần phẫu thuật tim khác như phẫu thuật bắc cầu động mạch vành (CABG) hoặc bệnh van tim hoặc động mạch chủ khác.
- Hình ảnh học – Ghi nhận khối phù hợp với huyết khối, cục máu đông nhỏ (≤0,8 cm2), không có huyết khối nhĩ trái.
- Nguồn lực – Không đủ khả năng chuyên môn về phẫu thuật.
♦ Các yếu tố sau có lợi cho phẫu thuật:
- Đặc điểm lâm sàng – Nguy cơ của phẫu thuật thấp, phân loại chức năng NYHA IV, chống chỉ định tiêu sợi huyết, huyết khối van tái phát.
- Đặc điểm hình ảnh – Có thể hoặc nghi ngờ có pannus, cục máu đông lớn (>0,8 cm2) hoặc huyết khốinhĩ trái.
- Chỉ định đồng thời – Bệnh động mạch vành cần phẫu thuật CABG, bệnh van tim đồng thời hoặc bệnh động mạch chủ cần phẫu thuật.
- Nguồn lực – Chuyên môn phẫu thuật sẵn có.
- Đối với những bệnh nhân có chỉ định phẫu thuật nhưng đăc điểm lâm sàng, chất lượng cuộc sống không cải thiện sau phẫu thuật hoặc ky vọng sống < 1 năm, nên giản thích thân nhân, bệnh nhân thực hiện chăm sóc giảm nhẹ.
2. Đối với huyết khối van tim gây tắc nghẽn
Đối với bệnh nhân bị huyết khối gây tắc nghẽn van nhân tạo có phân độ chức năng suy tim NYHA I đến III, điều trị nhằm mục đích kiểm soát kịp thời các triệu chứng lâm sàng và xử trí nguyên nhân tắc nghẽn. Bệnh nhân có huyết khối van nhân tạo cơ học tắc nghẽn, kế hoạch điều trị nên được cá thể hóa theo tình huống lâm sàng. Các lựa chọn điều trị bao gồm: 1) tối ưu hóa kháng đông; 2) tiêu sợi huyết; 3) can thiệp bằng ống thông; và 4) phẫu thuật. Hiện tại, các hướng dẫn của Hiệp hội Tim mạch Châu Âu khuyến cáo Loại I đối với phẫu thuật để điều trị huyết khối van nhân tạo cơ học tắc nghẽn ở những bệnh nhân nguy kịch nhưng không có bệnh kèm theo nghiêm trọng. Tiêu sợi huyết nên được xem xét với van cơ học bên phải hoặc khi phẫu thuật quá rủi ro hoặc không sẳn có1.
- Đối với bệnh nhân huyết khối van cơ học bên trái gây tắc nghẽn có NYHA từ I đến III và có huyết khối nhỏ (không di động và <0,8 cm2 hoặc di động và đường kính ≤0,3 cm), các tác giả đề nghị dùng kháng đông đường tĩnh mạch heparin không phân đoạn (UFH) trong vài ngày (ví dụ: 5 đến 7) ngày với aPTT mục tiêu gấp 2 đến 2,5 lần; tiếp tục kết hợp dùng aspirin 75 đến 100 mg mỗi ngày.
Siêu âm tim qua thực quản được thực hiện để đánh giá mức độ ly giải hoặc tiến triển của huyết khối và đánh giá chức năng van.Nếu huyết khối vẫn tồn tại, các tác giả đề nghịđề nghị điều trị tiêu sợi huyết.
- Đối với những bệnh nhân huyết khối gây tắc nghẽn van cơ học bên trái với phân độ NYHA II dai dẳng (hoặc các triệu chứng nặng hơn) mặc dù đã dùng tiêu sợi huyết hoặc có chống chỉ định tuyệt đối với tiêu sợi huyết, các tác giả đề nghịđề nghị phẫu thuậtlại van tim.
- Đối với bệnh nhân bị huyết khối gây tắc nghẽn van nhân tạo cơ học bên phải, các tác giả đề nghị khuyên dùng liệu pháp tiêu sợi huyết. Tiếp tục dùng aspirin 75 đến 100 mg mỗi ngày và vẫn tiếp tục thuốc kháng vitamin K (VKA)14,15,18.
3. Đối với huyết khối van tim không gây tắc nghẽn: việc điều trị nhằm mục đích xử trí huyết khối.
Đối với bệnh nhân huyết khối van nhân tạo cơ học bên trái hoặc bên phải có huyết khối nhỏ (không di động và <0,8 cm2 hoặc di động và đường kính <0,3 cm) không có triệu chứng tắc nghẽn, các tác giả đề nghịkhuyên dùng thuốc chống đông (bắc cầu IV UFH đến VKA tối ưu) kết hợp với aspirin (75 đến 100 mg/ngày), và theo dõi chặt chẽ bằng siêu âm tim để đánh giá hiệu quả điều trị hoặc tiến triển của huyết khối.
4. Các biện pháp điều trị huyết khối van
4.1. Thuốc chống đông
Thuốc chống đông cho van cơ học vẫn chỉ giới hạn ở thuốc chống đông đường uống với warfarin và thuốc heparine đường tiêm. Kháng đông dưới mức điều trị là yếu tố quan trọng nhất liên quan đến cơ chế bệnh sinh của huyết khối van nhân tạo6.Điều trị bằng heparin không phân đoạn (UFH) kết hợp với warfarin đã thành công, ít nhất là một phần huyết khốiđược xử trí ở những bệnh nhân có huyết khối van cơ học bên trái, nhỏ (<10 mm) không có triệu chứng.
Thuốc chống đông đường uống trực tiếp dễ sử dụng mà không cần thay đổi chế độ ăn uống, lấy máu thường xuyên và điều chỉnh liều lượng, nhưng hiện tại thuốc này chống chỉ định sử dụng khi có van cơ học.
Dabigatran là thuốc chống đông máu đường uống trực tiếp được nghiên cứu nhiều nhất ở bệnh nhân van cơ học, và mặc dù các nghiên cứu trên mô hình động vật và in vitro ban đầu rất hứa hẹn, một thử nghiệm ngẫu nhiên có đối chứng đa trung tâm giai đoạn II đánh giá việc sử dụng dapigatranở bệnh nhânvan cơ học đã bị dừng sớm do tỷ lệ biến cố huyết khối và chảy máu cao hơn ở nhóm bệnh nhân dùng dabigatran12.
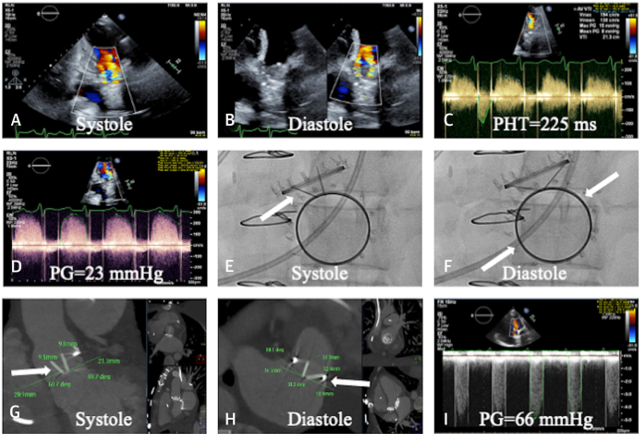
Hình 1. Huyết khối van cơ học động mạch chủ và van hai lá được điều trị bằng tPA liều thấp
Soria Jiménez CE, et al. J Am Coll Cardiol. 2023;81(21):2115–2127.
Một phụ nữ thay van hai lá cơ học St Jude 25 mm và van động mạch chủ cơ học 21 mm bị suy tim mất bù. Siêu âm tim qua thành ngực cho thấy dòng chảy rối và aliasing Doppler màu van động mạch chủ (A) và van hai lá (B), vận tốc qua động mạch chủ tối đa là 4,9 m/s, chỉ số không thứ nguyên (dimensionless index) là 0,11và hở van động mạch chủ với thời gian nửa áp lực (PHT) là 225 mili giây (C). Độ chênh áp qua van hai lá tăng cao (D), với sự hạn chế của lá van được xác định trên soi huỳnh quang (E, F) (mũi tên chỉ ra các lá van bị hạn chế). Bắt đầu truyền chất kích hoạt plasminogen mô (tPA) liều thấp, cực chậm. Hình ảnh chụp cắt lớp vi tính sau đó cho thấy chuyển động của lá van được cải thiện (G, H) (mũi tên chỉ tờ rơi). Độ chênh áp qua van động mạch chủ (I) và van hai lá (J) được cải thiện trước khi BN xuất viện về nhà. Soi huỳnh quang bệnh nhân ngoại trú ghi nhận các lá van di động (K, L) (mũi tên chỉ các lá van)13.
4.2. Tiêu sợi huyết
Phác đồ — Đối với bệnh nhân mắc huyết khối van nhân tạo có chỉ định tiêu sợi huyết (còn được gọi là tiêu huyết khối), các tác giả đề nghị đề xuất phác đồ liều thấp truyền cực chậm dựa trên các nghiên cứu quan sát được mô tả bên dưới 14. Hình ảnh học giúp đánh giá hiệu quả của tiêu sợi huyết, siêu âm tim qua thành ngực (TTE) thường được sử dụng để xác định ảnh hưởng đến độ chênh lệch qua van nhân tạo trong các trường hợp tắc nghẽn và siêu âm tim qua thực quản (TEE) thường được sử dụng để xác định kích thước huyết khối và hình dạng của van nhân tạo (Hình 1).
- Đánh giá các chống chỉ định của liệu pháp tiêu sợi huyết (tương tự như trong trường hợp nhồi máu cơ tim).
- Nếu chống chỉ định dùng thuốc tiêu sợi huyết thì có thể tiến hành phẫu thuật thay van (lấy huyết khối hoặc thay van lại).
- Nếu không có chống chỉ định tiêu sợi huyết, ngưng thuốc kháng đông trong quá trình điều trị tiêu sợi huyết và đợi cho đến khi INR<2,5 (hoặc aPTT <50 giây nếu bệnh nhân đang dùng UFH) trước khi bắt đầu điều trị tiêu sợi huyết. Có nhiều phác đồ sử dụng thốc tiêu sợi huyết để điều trị. Hiện nay hay dùng hai phác đồ truyền chậm (slow, 25mg alteplase /6h, thường cho bệnh nhân NYHA III-IV, xem hình 5 phần kết luận) và phác đồ siêu chậm (ultra slow)
- Truyền tĩnh mạch 25 mg alteplase trong 25 giờ (ultra slow) mà không cần dùng liều tải. Tiếp theo là truyền UFH trong sáu giờ (70 đơn vị/kg bolus và 16 đơn vị/kg/giờ [tối đa 1000 đơn vị/giờ] với aPTT mục tiêu từ 1,5 đến 2,0 lần giá trị kiểm soát).
- Đối với bệnh nhân bị tắc nghẽn van nhân tạo, thực hiện siêu âm tim qua thành ngực để đánh giá độ chênh áp qua van nhân tạo.
- Nếu độ chênh áp giảm, hãy thực hiện siêu âm tim qua thực quản (TEE):
- Nếu TEE cho thấy huyết khối đã ly giải một phần (giảm kích thước <75 phần trăm), lặp lại truyền 25 mg alteplase trong 25 giờ, sau đó truyền UFH trong 6 giờ, sau đó lặp lại TEE.
- Nếu TEE cho thấy huyết khối đã ly giải (kích thước giảm ≥75 phần trăm), dừng alteplase và bắt đầu UFH và VKA.
- Nếu độ chênh áp không được cải thiện, lặp lại truyền 25 mg alteplase trong 25 giờ sau đó truyền UFH trong 6 giờ, sau đó lặp lại TTE.
- Đối với bệnh nhân huyết khối không tắc nghẽn, lặp lại TEE.
- Nếu huyết khối được xử lý (kích thước giảm ≥75 phần trăm), dừng alteplase và bắt đầu UFH và VKA.
- Nếu huyết khối không thay đổi hoặc chỉ được xử lý một phần (giảm kích thước <75 phần trăm), lặp lại truyền 25 mg alteplase trong 25 giờ, sau đó truyền UFH trong 6 giờ, sau đó lặp lại TEE.
- Đối với những bệnh nhân bị huyết khối dai dẳng khi thực hiện TEE lặp lại, có thể lặp lại việc truyền 25 mg alteplase trong 25 giờ (tiếp theo là truyền UFH trong 6 giờ) nếu cần (có đánh giá TEE sau mỗi liều) cho đến liều tích lũy tối đa là 200 mg alteplase. Hầu hết bệnh nhân chỉ cần truyền ít hơn ba lần14,15,18.
Khi tiêu sợi huyết thành công đã được xác nhận, liệu pháp UFH và VKA được bắt đầu . UFH được tiếp tục cho đến khi VKA đạt được mục tiêu INR trong hai ngày liên tiếp 8.
Bằng chứng — Có bằng chứng hạn chế để hướng dẫn sử dụng thuốc tiêu sợi huyết ở bệnh nhân mắc huyết khối van nhân tạo. Chỉ có dữ liệu quan sát về hiệu quả và độ an toàn của phác đồ điều trị tiêu sợi huyết đối với huyết khối van nhân tạo. Dữ liệu so sánh trực tiếp giữa các chế độ tiêu sợi huyết khác nhau còn thiếu, đa số các nghiên cứu chỉ giới hạn ở kinh nghiệm đơn trung tâm. Hầu hết các bằng chứng được công bố về quá trình tiêu sợi huyết đối với huyết khối van nhân tạo đều liên quan đến alteplase, chỉ có các báo cáo ca về tenecteplase và reteplase.
Hầu hết các nghiên cứu về liệu pháp tiêu sợi huyết cho huyết khối van nhân tạo chủ yếu tập trung vào huyết khối van nhân tạo bên trái. Các nghiên cứu sử dụng phương pháp truyền chậm hoặc siêu chậm dưới sự hướng dẫn của siêu âm tim, phác đồ tiêu sợi huyết liều thấp đã chứng minh tỷ lệ hiệu quả cao (85 đến 90 phần trăm hoặc cao hơn 15,16) với tỷ lệ biến chứng tương đối thấp (ví dụ: 10,5 phần trăm bao gồm cả không tử vong khi truyền trong 6 giờ; 6,7% [bao gồm tỷ lệ tử vong 0,8%] với truyền trong 25 giờ ). Kết quả với các chế độ điều trị chậm hoặc siêu chậm liều thấp này thuận lợi hơn so với kết quả quan sát được trong các nghiên cứu tiêu sợi huyết trước đó (trước năm 2013) với tốc độ truyền nhanh và liều cao hơn (tỷ lệ thành công huyết động là 75%, tỷ lệ tử vong trong 30 ngày là 7%, thuyên tắc huyết khối tỷ lệ 13%, và tỷ lệ chảy máu nặng là 6%) 8.
Các biến chứng sau điều trị tiêu sợi huyết bao gồm chảy máu nặng, tắc mạch hệ thống, huyết khối van nhân tạo tái phát và tử vong 17,18. Các yếu tố nguy cơ biến chứng ở bệnh nhân được điều trị bằng thuốc tiêu sợi huyết truyền chậm (hoặc siêu chậm) bao gồm NYHA độ III hoặc IV và kích thước huyết khối lớn (ví dụ: diện tích trên TEE ≥1,0 cm2 15).
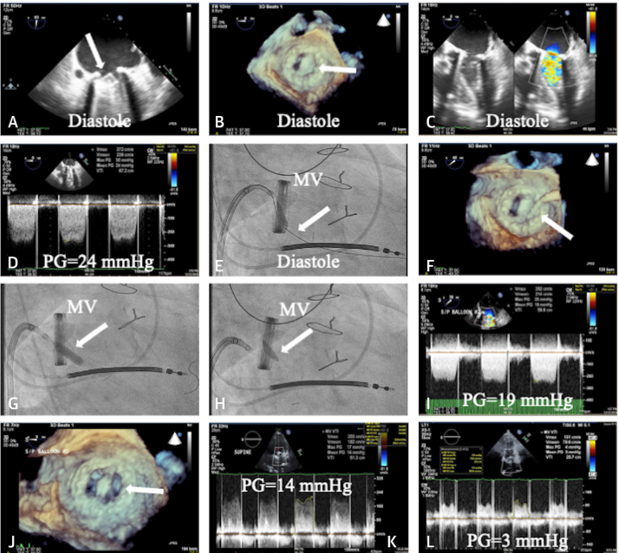
Hình 2. Huyết khối van hai lá cơ học được điều trị thành công bằng can thiệp qua ống thông
Soria Jiménez CE, et al. J Am Coll Cardiol. 2023;81(21):2115–2127.
Một phụ nữ thay van hai lá nhân tạo 29 mm Carbomedics (Corcym) nhập viện với tình trạng sốc tim. Siêu âm tim qua thực quản ba chiều ghi nhận một lá van bị hạn chế vận động (A, B) (mũi tên chỉ lá van), dòng chảy rối (turbulent flows) (C), chênh áp cao (PG) (D) và vận tốc qua van tối đa là 2,7 m/s. Với nguy cơ phẫu thuật cao của cô ấy và INR cao hơn ngưỡng điều trị nhiều, can thiệp van bị tắc nghẽn bằng ống thông đã được thực hiện. Sử dụng phương pháp soi huỳnh quang, dùng dây dẫn 0,014 inch đi ngang qua van bằng phương pháp xuyên vách (E, F) (mũi tên chỉ ống thông đi ngang qua van hai lá). Dùng bóng nong mạch vành áp lực cao nong (G) (mũi tên chỉ bóng được bơm căng), tái thông van tắc nghẽn (H) (mũi tên chỉ lá van di động), giảm chênh áp qua van hai lá (I) và lá van cải thiện sự di động (J). Chênh áp qua van hai lá (K, L) cải thiện trước xuất viện. MV= van hai lá13.
4.3. Can thiệp bằng ống thông
Can thiệp bằng ống thông qua da các lá van cơ học bị tắc nghẽn như một lựa chọn khả thi ở những bệnh nhân thất bại sau khi dùng tiêu sợi huyết, sốc tim hoặc nguy cơ khi phẫu thuật quá cao. Can thiệp qua ống thông có thể không phải là phương pháp điều trị dứt điểm nhưng nó có thể là cầu nối để phẫu thuật lại ở những bệnh nhân quá nặng. Chỉ có một vài trường hợp can thiệp qua da ở bệnh nhân huyết khối van cơ học được báo cáo. Mặc dù phương pháp tiếp cận qua da không phải là một phần của hướng dẫn xử trí huyết khối van cơ học tắc nghẽn, quy trình này đã được chứng minh là an toàn và hiệu quả ở một số ít bệnh nhân và nên được xem xét cho những người thất bại hoặc có chống chỉ định với tiêu sợi huyết, từ chối phẫu thuật lại, nguy cơ của phẫu thuật cao và là cầu nối để phẫu thuật lại qua giai đoạn cấp tính của sốc tim (Hình 2) 13.
4.4. Phẫu thuật lại (REDO SURGERY)
Một số thử nghiệm khảo sát kết quả phẫu thuật huyết khối van cơ học. Phân độ suy tim nặng hơn sẽ có nguy cơ của phẫu thuật cao hơn, một nghiên cứu chứng minh rằng bệnh nhân suy tim độ IV theo Hiệp hội Tim mạch New York có nguy cơ tử vong chu phẫu là 17,5% so với 4,7% ở bệnh nhân suy tim độ I đến độ III19. Phẫu thuật điều trị tắc nghẽn hoặc huyết khối van nhân tạo (thay van hoặc lấy huyết khối) có liên quan đến tỷ lệ tử vong phẫu thuật cao (tỷ lệ tử vong chung trong 30 ngày từ 10 đến 15% 8) phần lớn liên quan đến phân loại chức năng NYHA (ví dụ: 17,5% ở bệnh nhân có các triệu chứng NYHA IV (bảng 1) so với 4,7% ở nhóm phân loại chức năng NYHA I đến III khi khảo sát 106 bệnh nhân ). Tỷ lệ tử vong cao tới 35% đã được mô tả ở những bệnh nhân bị bệnh nặng20. Ưu điểm của phẫu thuật là nó cho phép thay các van tim cũ dễ sinh huyết khối bằng van tim có thiết kế mới hơn, phẫu thuật còn cho phép chẩn đoán và điều trị dứt điểm các trường hợp không rõ nguyên nhân (Hình 3) 13, 17.
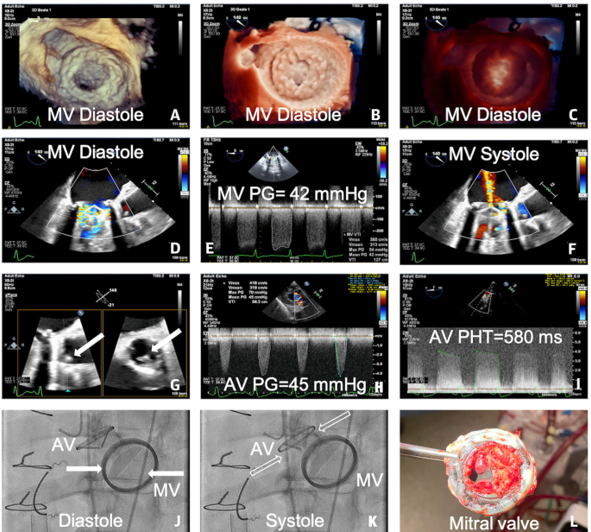
Hình 3. Phẫu thuật lại ở bệnh nhân huyết khối van cơ học kép sau khi dùng thuốc tiêu sợi huyết thất bại
Soria Jiménez CE, et al. J Am Coll Cardiol. 2023;81(21):2115–2127.
Một phụ nữ có van hai lá cơ học Carbomedics 31 mm (Corcym) và van động mạch chủ cơ học St Jude 21 mm (Abbott Laboratories) nhập viện trong tình trạng sốc tim. Siêu âm tim cho thấy các lá van hai lá bất động (A đến C), dòng chảy rối (flow turbulence), tăng chênh áp qua van (D, E) và hở van (F). Có huyết khối ở lá vành phải (G) (mũi tên chỉ huyết khối), chênh áp qua động mạch chủ (H) tăng cao (chỉ số không thứ nguyên (dimensionless index): 0,19; thời gian tăng tốc [AT]: 80 mili giây; thời gian tống máu [ET]: 170 mili giây; AT/ET : 0,47), và trào ngược (I). Soi huỳnh quang xác nhận có van hạn chế vận động (J, K) (mũi tên liền và nét đứt tương ứng biểu thị các lá van hai lá và động mạch chủ bất động). Bệnh nhân đã thay (L cho thấy van hai lá nhân tạo) van động mạch chủ nhân tạo sinh học Inspiris 19 mm (Edwards Lifescatics) và van hai lá nhân tạo sinh học Epic (Abbott) 27 mm13.
5. Điều trị tiếp theo sau điều trị huyết khối van nhân tạo
Bệnh nhân bị huyết khối van nhân tạo được điều trị bằng liệu pháp chống huyết khối và/hoặc liệu pháp tiêu sợi huyết có nguy cơ bị huyết khối van nhân tạo tái phát (#6% trong thời gian theo dõi trung bình 10 tháng sau khi điều trị bằng thuốc tiêu sợi huyết siêu chậm). Vì vậy, những bệnh nhân này cần được theo dõi cẩn thận bao gồm chế độ điều trị chống huyết khối tối ưu.
Khi huyết khối van nhân tạo xảy ra mặc dù đã điều trị bằng thuốc chống huyết khối, bước đầu tiên quan trọng là xác định thuốc chống huyết khối nào (ví dụ: warfarin và/hoặc aspirin) mà bệnh nhân đang dùng và mức độ đầy đủ của thuốc chống đông(bao gồm cả thời gian gần đây trong phạm vi điều trị). Nguy cơ biến chứng chảy máu khi tăng cường chống đông cũng nên được đánh giá. Liệu pháp chuẩn chống huyết khốicho van cơ học bao gồm aspirin liều thấp (75 đến 100 mg/ngày) kết hợp với thuốc kháng đông (thuốc kháng vitamin K [VKA] hoặc heparin). Thuốc kháng đông đường uống trực tiếp (thuốc ức chế thrombin trực tiếp đường uống và thuốc ức chế yếu tố Xa) không được khuyến cáo sử dụng cho bệnh nhân có van nhân tạo cơ học.
Nếu liệu pháp chống huyết khối không đủ trước khi xảy ra huyết khối van hoặc thuyên tắc huyết khối, cần tiến hành liệu pháp thích hợp, bao gồm tối ưu hóa thời gian INR đạt mục tiêu (ví dụ: giáo dục bệnh nhân, theo dõi thường xuyên hơn, quản lý bởi phòng khám chuyên vềkháng đông do dược sĩ hướng dẫn hoặc bệnh nhân tự giám sát), nên là bước điều trị đầu tiên 1,8.
Cách tiếp cận sau đây được đề xuất cho những bệnh nhân có van cơ học đã được điều trị huyết khối van, mặc dù còn thiếu dữ liệu về hiệu quả của các phác đồ này:
- Đối với bệnh nhân thuyên tắc huyết khối đã được điều trị đầy đủ bằng kháng đông VKA (ví dụ warfarin) nhưng không dùng aspirin, có thể thêm aspirin (75 đến 100 mg/ngày).
- Đối với bệnh nhân thuyên tắc huyết khối hoặc huyết khối van trong khi điều trị kháng đông đạt mục tiêu INR là 2,5 (ví dụ: bệnh nhân thay van động mạch chủ cơ học mà không có thêm các yếu tố nguy cơ) và đang dùng aspirin thì tăng mục tiêu INR lên 3,0.
- Đối với bệnh nhân thuyên tắc huyết khối hoặc huyết khối van khi điều trị kháng đông đạt mục tiêu INR là 3,0 kết hợp với aspirin, mục tiêu INR có thể cần tăng lên 4,0.
Cách tiếp cận này nhằm điều chỉnh liệu pháp chống huyết khối phù hợp với hướng dẫn về bệnh van tim của Đại học Tim mạch Hoa Kỳ/Hiệp hội Tim mạch Hoa Kỳ năm 20208.
KẾT LUẬN
Huyết khối van nhân tạo có biểu hiện lâm sàngkhác nhau, nênbác sĩ cần nghi ngờ huyết khối van cơ học ở bệnh nhân thay van nhân tạo cơ học có triệu chứng và dấu hiệu của suy tim hoặc sốc tim. Hình ảnh họcđa phương thức gồm siêu âm tim, soi huỳnh quang và CT đóng vai trò quan trọng để chẩn đoán kịp thời và hướng dẫn điều trị phù hợp. Chiến lược điều trị tối ưu gồm kháng đông, tiêu sợi huyết, can thiệp qua ống thông, hoặc phẫu thuật lại, phụ thuộc vào mức độ tắc nghẽn, tình trạng huyết động và bệnh kèm theo của bệnh nhân khi nhập viện (hình 4,5).
Hình 4. Sơ đồ chỉ dẫn tiếp cận chẩn đoán và điều trị huyết khối van nhân tạo cơ học. Biểu hiện lâm sàng của huyết khối van cơ học có thể khác nhau. Hình ảnh đa phương thức đóng vai trò rất quan trọng trong việc xác định chẩn đoán, với chiến lược điều trị tối ưu chủ yếu phụ thuộc vào mức độ tắc nghẽn và tình trạng huyết động.
AC = anticoagulation13.
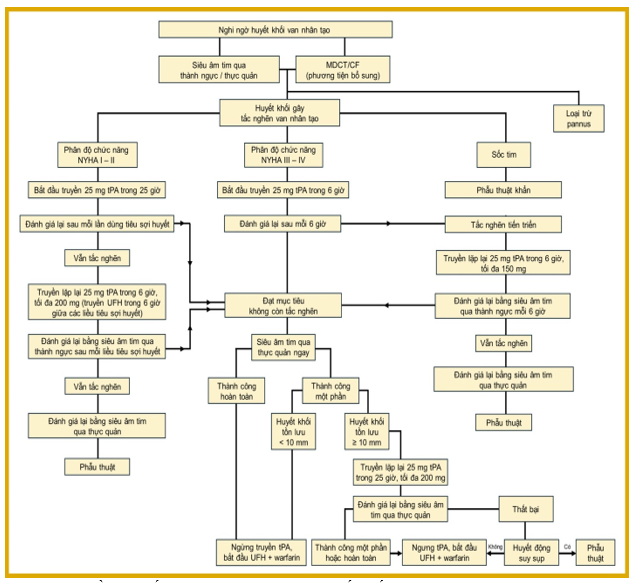
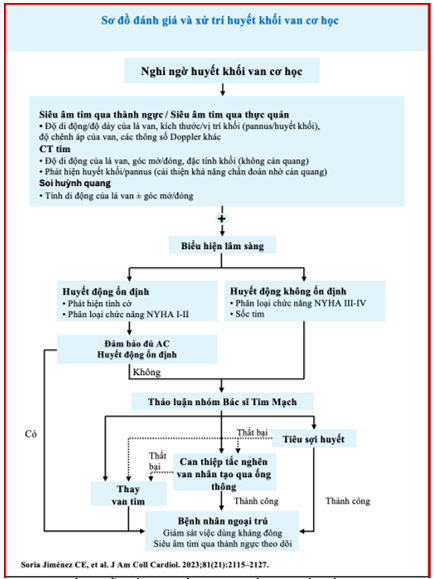
Hình 5. Lưu đồ xử trí tắc nghẽn van nhân tạo do huyết khối.
CF= nội soi huỳnh quang; MDCT= chụp cắt lớp vi tính đa đầu dò; NYHA= Hiệp hội Tim mạch New York; PVT = huyết khối van nhân tạo; TEE = siêu âm tim qua thực quản; t-PA = chất kích hoạt plasminogen mô; TT = điều trị bằng tiêu sợi huyết; TTE = siêu âm tim qua thành ngực; UFH = heparin không phân đoạn21.
TÀI LIỆU THAM KHẢO
- Vahanian A, Beyersdorf F, Praz F, et al. 2021 ESC/EACTS Guidelines for the management of valvular heart disease. Eur Heart J. Feb 12 2022;43(7):561-632. doi:10.1093/eurheartj/ehab395
- Whitlock RP, Sun JC, Fremes SE, Rubens FD, Teoh KH. Antithrombotic and thrombolytic therapy for valvular disease: Antithrombotic Therapy and Prevention of Thrombosis, 9th ed: American College of Chest Physicians Evidence-Based Clinical Practice Guidelines. Chest. Feb 2012;141(2 Suppl):e576S-e600S. doi:10.1378/chest.11-2305
- Roudaut R, Serri K, Lafitte S. Thrombosis of prosthetic heart valves: diagnosis and therapeutic considerations. Heart. 2007;93(1):137-142. doi:10.1136/hrt.2005.071183
- Jaffer IH, Fredenburgh JC, Hirsh J, Weitz JI. Medical device‐induced thrombosis: what causes it and how can we prevent it? Journal of Thrombosis and Haemostasis. 2015/06/01/ 2015;13:S72-S81. doi:https://doi.org/10.1111/jth.12961
- Deviri E, Sareli P, Wisenbaugh T, Cronje SL. Obstruction of mechanical heart valve prostheses: Clinical aspects and surgical management. Journal of the American College of Cardiology. 1991/03/01/ 1991;17(3):646-650. doi:https://doi.org/10.1016/S0735-1097(10)80178-0
- Dürrleman N, Pellerin M, Bouchard D, et al. Prosthetic valve thrombosis: twenty-year experience at the montreal heart institute. The Journal of Thoracic and Cardiovascular Surgery. 2004/05/01/ 2004;127(5):1388-1392. doi:https://doi.org/10.1016/j.jtcvs.2003.12.013
- Marcoff L, Koulogiannis KP, Aldaia L, et al. Color Paucity as a Marker of Transcatheter Valve Thrombosis. JACC Cardiovasc Imaging. Jan 2017;10(1):78-81. doi:10.1016/j.jcmg.2016.08.016
- Otto CM, Nishimura RA, Bonow RO, et al. 2020 ACC/AHA Guideline for the Management of Patients With Valvular Heart Disease: Executive Summary: A Report of the American College of Cardiology/American Heart Association Joint Committee on Clinical Practice Guidelines. Circulation. Feb 2 2021;143(5):e35-e71. doi:10.1161/cir.0000000000000932
- Suh YJ, Kim YJ, Hong YJ, et al. Measurement of Opening and Closing Angles of Aortic Valve Prostheses In Vivo Using Dual-Source Computed Tomography: Comparison with Those of Manufacturers’ in 10 Different Types. Korean J Radiol. Sep-Oct 2015;16(5):1012-23. doi:10.3348/kjr.2015.16.5.1012
- Montorsi P, De Bernardi F, Muratori M, Cavoretto D, Pepi M. Role of cine-fluoroscopy, transthoracic, and transesophageal echocardiography in patients with suspected prosthetic heart valve thrombosis. Am J Cardiol. Jan 1 2000;85(1):58-64. doi:10.1016/s0002-9149(99)00607-4
- Suchá D, Symersky P, Vonken EJ, Provoost E, Chamuleau SA, Budde RP. Multidetector-row computed tomography allows accurate measurement of mechanical prosthetic heart valve leaflet closing angles compared with fluoroscopy. J Comput Assist Tomogr. May-Jun 2014;38(3):451-6. doi:10.1097/RCT.0b013e3182ab5f15
- Eikelboom JW, Connolly SJ, Brueckmann M, et al. Dabigatran versus Warfarin in Patients with Mechanical Heart Valves. New England Journal of Medicine. 2013;369(13):1206-1214. doi:10.1056/NEJMoa1300615
- Soria Jiménez CE, Papolos AI, Kenigsberg BB, et al. Management of Mechanical Prosthetic Heart Valve Thrombosis: JACC Review Topic of the Week. J Am Coll Cardiol. May 30 2023;81(21):2115-2127. doi:10.1016/j.jacc.2023.03.412
- Özkan M, Gündüz S, Gürsoy OM, et al. Ultraslow thrombolytic therapy: A novel strategy in the management of PROsthetic MEchanical valve Thrombosis and the prEdictors of outcomE: The Ultra-slow PROMETEE trial. Am Heart J. Aug 2015;170(2):409-18. doi:10.1016/j.ahj.2015.04.025
- Gündüz S, Özkan M, Yesin M, et al. Prolonged Infusions of Low-Dose Thrombolytics in Elderly Patients With Prosthetic Heart Valve Thrombosis. Clin Appl Thromb Hemost. Apr 2017;23(3):241-247. doi:10.1177/1076029615609698
- Özkan M, Gündüz S, Biteker M, et al. Comparison of different TEE-guided thrombolytic regimens for prosthetic valve thrombosis: the TROIA trial. JACC Cardiovasc Imaging. Feb 2013;6(2):206-16. doi:10.1016/j.jcmg.2012.10.016
- Özkan M, Gündüz S, Güner A, et al. Thrombolysis or Surgery in Patients With Obstructive Mechanical Valve Thrombosis. Journal of the American College of Cardiology. 2022/03/15 2022;79(10):977-989. doi:10.1016/j.jacc.2021.12.027
- Pislaru.S et Connolly.HM: Management of mechanical prosthetic valve thrombosis and obstruction. Uptodate 2023.







