Trong nghiên cứu ngẫu nhiên, mù đôi, có đối chứng giả dược ATLANTIC (Administration of Ticagrelor in the cath Lab or in the Ambulance for New ST elevation myocardial infarction to open the Coronary artery),
BS CKI. Thái Minh Thiện
(Lược dịch theo “Effect of Pre-Hospital Ticagrelor During the First 24 Hours After
Primary PCI in Patients With ST-Segment Elevation Myocardial Infarction – The ATLANTIC-H24 Analysis”)
sử dụng thuốc kháng thụ thể P2Y12 Ticagrelor trên xe cấp cứu trong khoảng thời gian ngắn trước khi can thiệp mạch vành qua da (PCI) đã không cải thiện tình trạng tái tưới máu trước PCI của động mạch thủ phạm so với khi sử dụng trong phòng thông tim can thiệp, được tính bằng sự hiện diện của dòng chảy TIMI cấp 3 trên kết quả chụp mạch vành và khả năng cải thiện ≥70% độ chênh ST trên điện tâm đồ (1). Thời gian trung vị từ lúc phân ngẫu nhiên đến khi chụp mạch vành và thời gian giữa liều tải ticagrelor của 2 nhóm (trước bệnh viện so với trong bệnh viện) tương ứng chỉ có 48 phút và 31 phút. Các khoảng chênh lệch thời gian ngắn như vậy có thể lý giải cho việc vẫn chưa ghi nhận được lợi ích khi sử dụng ticagrelor trên xe cứu thương đối với khả năng tái tưới máu mạch vành trước PCI (2). Tuy nhiên sử dụng ticagrelor trước nhập viện làm giảm nguy cơ huyết khối trong stent trong 30 ngày tiếp theo. Tác giả đưa ra giả thuyết rằng hiệu quả của việc sử dụng sớm ticagrelor đã không được biểu hiện mãi cho đến sau PCI do khoảng thời gian ngắn từ lúc dùng thuốc đến khi chuyển vào phòng thông tim can thiệp. Do đó nhóm nghiên cứu đã tiến hành một phân tích thăm dò (phân tích ATLANTIC-H24) để kiểm tra chặt chẽ hơn tất cả các dữ liệu có sẵn trong 24 giờ đầu tiên sau khi PCI tiên phát, bao gồm phân tích chức năng tiểu cầu, tái tưới máu mạch vành, tiêu chí biến cố thiếu máu cục bộ, và tính an toàn.
PHƯƠNG PHÁP NGHIÊN CỨU
Thiết kế và quy trình nghiên cứu
ATLANTIC là nghiên cứu ngẫu nhiên với quy mô toàn cầu trong đó bệnh nhân nhồi máu cơ tim ST chênh lên (STEMI) được điều trị mù đôi với một liều nạp 180 mg ticagrelor, tại thời điểm hoặc là trước nhập viện (trên xe cứu thương) hoặc là trong bệnh viện (tại phòng thông tim can thiệp), trên nền aspirin và chăm sóc chuẩn (3). Trung tâm điều phối là ACTION Study Group tại Bệnh viện Pitié-Salpêtrière ở Paris.
Thiết kế nghiên cứu và các kết quả chính đã được báo cáo (1). Tóm tắt lại, bệnh nhân đủ điều kiện được xác định bởi các nhân viên cấp cứu để đưa vào nghiên cứu sau khi có kết quả chẩn đoán là STEMI trong khoảng từ > 30 phút đến < 6 h và thời gian dự kiến từ lúc có kết quả điện tâm đồ đến thời điểm nong bóng đầu tiên phải < 120 phút. Bệnh nhân được phân ngẫu nhiên và sử dụng liều nạp của ticagrelor hoặc giả dược tương ứng ngay lập tức sau khi có kết quả chẩn đoán STEMI được khẳng định bởi điện tim đồ. Sau đó bệnh nhân được chuyển vào phòng thông tim can thiệp để chụp mạch vành và PCI, tại đây bệnh nhân được sử dụng liều nạp thứ hai. Tất cả bệnh nhân sau đó được điều trị duy trì bằng ticagrelor 90 mg hai lần mỗi ngày trong ít nhất 30 ngày và tối đa là 12 tháng.
Việc sử dụng các chất ức chế glycoprotein IIb/IIIa không được khuyến khích trên xe cứu thương, tuy nhiên sẽ phụ thuộc vào cân nhắc của nhân viên y tế. Sau khi có kết quả chụp mạch vành, sử dụng ức chế glycoprotein IIb/IIIa trong phòng can thiệp phải được xác định như là chiến lược điều trị lựa chọn hoặc điều trị cấp cứu trong PCI. Lý do sử dụng thuốc ức chế glycoprotein IIb/IIIa tiêm tĩnh mạch trong phòng thông tim được các nghiên cứu viên ghi nhận lại.
Một phân tích dưới nhóm về dược động học đã được tiến hành tại 5 trung tâm tham gia nghiên cứu để đánh giá sự ức chế tiểu cầu trong 24 giờ đầu tiên sau khi bắt đầu liệu pháp điều trị bằng ticagrelor trước nhập viện hoặc trong bệnh viện. Đơn vị phản ứng tiểu cầu (PRUs) được đo bằng test VerifyNow P2Y12 ngay lập tức sau khi PCI và tại các thời điểm 1, 6, và 12 h sau PCI trước khi dùng liều duy trì đầu tiên của ticagrelor.
Tiêu chí nghiên cứu
Mặc dù mục tiêu chính của nghiên cứu ATLANTIC là đánh giá khả năng tái tưới máu mạch vành lúc từ lúc nhập viện đến khi vào phòng thông tim và kết cục lâm sàng sau 30 ngày sau khi sử dụng ticagrelor trước nhập viện so với trong bệnh viện, phân tích ATLANTIC-H24 chỉ tập trung đánh giá kết quả trong 24 giờ đầu sau khi PCI ở những bệnh nhân có PCI. Tất cả các tiêu chí của phân tích ATLANTIC-H24 này đánh giá hiệu quả phối hợp của chiến lược điều trị bằng ticagrelor với thủ thuật tái thông mạch máu. Như vậy, phân tích này tiến hành từ lúc bắt đầu thủ thuật PCI đến 24 giờ sau đó. Tiêu chí cải thiện tái tưới máu mạch vành bao gồm: 1) cải thiện độ chênh ST bằng cách tính tỷ lệ bệnh nhân giảm ≥ 70% đoạn ST chênh 1 h sau PCI và mức độ giảm trung bình đoạn ST chênh 1 giờ sau khi PCI (trung vị %); và 2) cải thiện dòng chảy TIMI tính bằng tỷ lệ bệnh nhân đạt dòng chảy TIMI cấp 3 tại động mạch liên quan nhồi máu khi kết thúc PCI. Cải thiện độ chênh ST được tính toán bằng cách so sánh 2 giá trị biến trên điện tâm đồ (đoạn ST chênh lên trên điện tâm đồ ở thời điểm bắt đầu và 1 giờ sau khi PCI). Kết cục lâm sàng đánh giá trong 24 giờ đầu sau khi PCI bao gồm các biến cố gộp đánh giá tỷ lệ tử vong và thiếu máu cục bộ cơ tim do nhồi máu cơ tim, huyết khối trong stent xác định, tái thông mạch máu khẩn cấp, hoặc sử dụng ức chế glycoprotein IIb/IIIa tiêm tĩnh mạch trong khi làm thủ thuật (sau khi bắt đầu PCI, không tính lần tiêm sau khi chụp động mạch vành nhưng trước khi PCI), và mỗi thông số riêng của biến cố gộp này. Tiêu chí an toàn bao gồm tỷ lệ chảy máu lớn, đe dọa tính mạng hoặc chảy máu nhỏ (không bao gồm chảy máu liên quan thủ thuật bắc cầu mạch vành) trong vòng 24 giờ đầu tiên theo định nghĩa xuất huyết của PLATO, TIMI, STEEPLE (Safety and Efficacy of Enoxaparin in Percutaneous Coronary Intervention Patients), GUSTO (Global Utilization of Streptokinase and Tissue Plasminogen Activator for Occluded Coronary Arteries), and BARC (Bleeding Academic Research Consortium).
Với mục đích so sánh, tất cả các tiêu chí đã được đánh giá trong toàn bộ dân số nghiên cứu bao gồm những bệnh nhân được PCI sau khi chụp mạch vành và những bệnh nhân có chụp mạch vành nhưng không làm PCI.
Kết quả chụp mạch vành và điện tâm đồ được làm mù tập trung bởi Cardialysis (Rotterdam, Hà Lan) và ERT (eResearch Technology Inc, Peterborough, Vương quốc Anh). Một ủy ban đánh giá độc lập tiến hành xem xét mù tất cả các kết cục lâm sàng (ngoại trừ trường hợp tử vong và biến cố xuất huyết tối thiểu) (1).
Phân tích thống kê
Phân tích ATLANTIC-H24 đánh giá dữ liệu thu được trong 24 giờ đầu tiên sau khi PCI là một phân tích hồi cứu không được xác định trước trong đề cương nghiên cứu. Nó chỉ được thực hiện như một phân tích thăm dò, và do đó các kết quả này không thể được xem như tuyệt đối.
Phân tích hiệu quả được thực hiện trên dân số dự định điều trị (intent-to-treat) đã có điều chỉnh, định nghĩa là tất cả các bệnh nhân được phân ngẫu nhiên có sử dụng ít nhất 1 liều thuốc nghiên cứu. Bệnh nhân thiếu kết quả đo đoạn chênh ST hoặc phân loại dòng chảy TIMI được loại khỏi phân tích các tiêu chí. Tính toán kết cục lâm sàng theo Kaplan-Meier được tiến hành trong khoảng thời gian từ 0 đến 24 h sau khi PCI và được so sánh bằng cách sử dụng tỷ lệ nguy cơ (Hazard ratio) thu được từ mô hình nguy cơ tương quan Cox. Bởi vì không có giả thuyết định trước, kiểm tra thống kê của tất cả các biến thứ cấp, bao gồm cả các kết cục lâm sàng, được coi như là khám phá ngẫu nhiên, và không có sự điều chỉnh thống kê đa so sánh. Tỷ lệ odds và giá trị p cho 2 nhóm sử dụng ticagrelor trước và trong bệnh viện đã được tính toán bằng cách sử dụng mô hình hồi quy logistic với nhóm điều trị nghiên cứu là biến giải thích duy nhất. Trường hợp khi so sánh mà không có biến cố nào trong 1 nhóm, giá trị p được tính bằng kiểm định chính xác Fisher.
Phân tích an toàn bao gồm tất cả các bệnh nhân đã nhận được ít nhất 1 liều thuốc nghiên cứu. Các biến cố chảy máu đã đánh giá được tổng hợp một cách riêng biệt theo định nghĩa đề cương nghiên cứu PLATO và các định nghĩa định trước khác (1). Các giá trị p cho khác biệt giữa hai nhóm theo phân loại xuất huyết của PLATO được tính toán bằng cách sử dụng kiểm định chi bình phương.
KẾT QUẢ
Dân số nghiên cứu
Tổng cộng có 1862 bệnh nhân đồng ý tham gia được phân ngẫu nhiên để dùng ticagrelor hoặc trước hoặc trong bệnh viện. Trong số này, 1629 bệnh nhân có làm PCI tiên phát được điều trị theo nghiên cứu, 799 ở nhóm trước bệnh viện và 830 ở nhóm trong bệnh viện, với số liệu đánh giá trong 24 giờ đầu tiên sau khi PCI được đưa vào phân tích (Bảng 1, Hình 1). Bên cạnh đó, 197 bệnh nhân có chụp mạch vành nhưng không có PCI (Bảng 1).
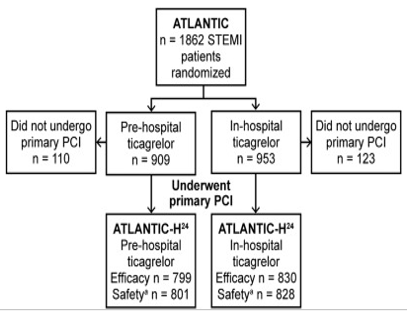
Hình 1.
Phân nhóm bệnh nhân nghiên cứu
Trong số 1862 bệnh nhân được phân ngẫu nhiên của nghiên cứu ATLANTIC, 1629 bệnh nhân được làm PCI tiên phát với dữ liệu có thể đánh giá được trong 24 giờ đầu tiên sau khi PCI. Để đánh giá hiệu quả, có 799 bệnh nhân được phân vào nhóm trước bệnh viện và 830 ở nhóm trong bệnh viện. Để đánh giá an toàn, đã có 891 bệnh nhân trong nhóm trước bệnh viện và 828 ở nhóm trong bệnh viện.
|
Bảng 1. Dữ liệu ban đầu về nhân khẩu học, đặc điểm lâm sàng và liệu pháp điều trị của các bệnh nhân được đưa vào phân tích ATLANTIC-H24 |
||||||
|
|
PCI Population
|
Angiography-Only Population
|
||||
|
Pre-Hospital Ticagrelor (n = 799) |
In-Hospital Ticagrelor (n = 830) |
p Value |
Pre-Hospital Ticagrelor (n = 90) |
In-Hospital Ticagrelor (n = 107) |
p Value |
|
|
Age, yrs |
60.9 ± 12.1 |
60.9 ± 12.0 |
0.901 |
57.5 ± 13.8 |
61.9 ± 15.5 |
0.040 |
|
Female |
150 (18.8) |
159 (19.20) |
0.844 |
20 (22.2) |
34 (31.8) |
0.134 |
|
BMI, kg/m2 |
27.1 ± 4.7 |
26.9 ± 4.4 |
0.509 |
26.9 ± 4.4 |
25.6 ± 4.3 |
0.045 |
|
Diabetes mellitus |
98 (12.3) |
116 (14.0) |
0.307 |
15 (16.7) |
19 (17.8) |
0.840 |
|
TIMI risk score |
|
|
|
|
|
|
|
0–2 |
489 (61.2) |
511 (61.6) |
0.883 |
52 (57.8) |
53 (49.5) |
0.232 |
|
3–6 |
296 (37.0) |
307 (37.0) |
|
33 (36.7) |
51 (47.7) |
|
|
>6 |
14 (1.8) |
12 (1.4) |
|
5 (5.6) |
3 (2.8) |
|
|
Killip class I |
722 (90.4) |
767 (92.4) |
0.141 |
83 (92.2) |
89 (83.2) |
0.058 |
|
First medical contact |
|
|
|
|
|
|
|
Ambulance |
612 (76.6) |
637 (76.7) |
0.874 |
61 (67.8) |
73 (68.2) |
0.651 |
|
Emergency/casualty department |
129 (16.1) |
135 (16.3) |
|
20 (22.2) |
23 (21.5) |
|
|
Specialty ward/floor |
4 (0.5) |
4 (0.5) |
|
0 |
0 |
|
|
Acute care/general hospital |
42 (5.3) |
37 (4.5) |
|
5 (5.0) |
9 (8.4) |
|
|
General medicine/medical floor |
12 (1.5) |
17 (2.0) |
|
|
|
|
|
MI location |
|
|
|
|
|
|
|
Anterior |
361 (45.2) |
417 (50.2) |
0.041 |
65 (72.2) |
69 (64.5) |
0.246 |
|
Inferior/unknown |
438 (54.8) |
413 (49.8) |
|
25 (27.8) |
38 (35.5) |
|
|
Time from onset of index event to PCI, min |
157 (59–6,345) |
161 (50–4,231) |
0.111 |
|
|
|
|
Procedure for index event |
|
|
|
|
|
|
|
Sheath insertion site |
|
|
|
|
|
|
|
Femoral |
247 (30.9) |
271 (32.7) |
0.452 |
32 (35.6) |
38 (35.5) |
0.995 |
|
Radial |
547 (68.5) |
556 (67.0) |
|
57 (63.3) |
69 (64.5) |
|
|
Unknown |
5 (0.6) |
3 (0.4) |
|
1 (1.1) |
0 |
|
|
Thromboaspiration |
470 (58.8) |
470 (56.6) |
0.370∗ |
N/A |
N/A |
|
|
PCI with stent |
759 (95.0) |
776 (93.5) |
0.194∗ |
N/A |
N/A |
|
|
Any drug-eluting stent |
466 (58.3) |
479 (57.7) |
0.802∗ |
N/A |
N/A |
|
|
Any bare-metal stent |
305 (38.2) |
312 (37.6) |
0.809∗ |
N/A |
N/A |
|
|
CV drug use in PCI patients |
|
|
|
|
|
|
|
Aspirin LD |
721 (90.2) |
737 (88.8) |
0.342 |
N/A |
N/A |
|
|
Started aspirin maintenance |
777 (97.2) |
811 (97.7) |
0.550 |
N/A |
N/A |
|
|
Glycoprotein IIb/IIIa inhibitor before start of PCI |
269 (33.7) |
255 (30.7) |
0.204 |
N/A |
N/A |
|
|
Abciximab |
148 (18.5) |
128 (15.4) |
0.095 |
N/A |
N/A |
|
|
Eptifibatide |
72 (9.0) |
61 (7.3) |
0.221 |
N/A |
N/A |
|
|
Tirofiban |
49 (6.1) |
66 (8.0) |
0.152 |
N/A |
N/A |
|
|
IV anticoagulant during hospitalization |
|
|
|
|
|
|
|
Heparin |
541 (67.7) |
579 (69.8) |
0.372 |
N/A |
N/A |
|
|
Enoxaparin |
224 (28.0) |
223 (26.9) |
0.598 |
N/A |
N/A |
|
|
Bivalirudin |
172 (21.5) |
184 (22.2) |
0.754 |
N/A |
N/A |
|
|
Fondaparinux |
45 (5.6) |
59 (7.1) |
0.223 |
N/A |
N/A |
|
|
Statin use post-qualifying ECG/pre-PCI |
78 (9.8) |
105 (12.7) |
0.065 |
N/A |
N/A |
|
Phân nhóm chức năng tiểu cầu
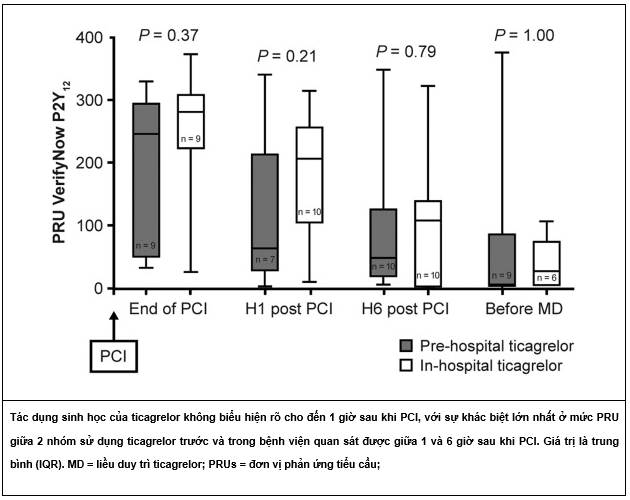
Phân tích phân nhóm chức năng tiểu cầu được thực hiện trên một nhóm dân số (n = 37) tuyển từ 5 trung tâm. Mức độ đơn vị phản ứng tiểu cầu (PRUs) cho thấy hiệu quả sinh học của ticagrelor đã không được biểu hiện rõ ràng cho đến thời điểm 1 giờ sau khi PCI (Hình 2). Sự khác biệt lớn nhất (nhưng không có ý nghĩa) trên mức độ PRU trung bình giữa 2 chiến lược điều trị (trước bệnh viện so với trong bệnh viện) đã được ghi nhận trong giai đoạn từ 1 – 6 giờ sau khi PCI
Hình 2. Ức chế tiểu cầu được đo bằng VerifyNow P2Y12 và thể hiện qua thông số PRUs
Sử dụng ức chế glycoprotein IIb/IIIa tiêm tĩnh mạch
Tỷ lệ sử dụng ức chế glycoprotein IIb/IIIa tiêm tĩnh mạch thấp hơn ở nhóm sử dụng ticagrelor trước bệnh viện so với nhóm sử dụng trong bệnh viện (9.4% so với 12.0%, OR: 0.76; KTC 95%: 0.55-1.04), chênh lệch tuyệt đối là 2.6% (không có ý nghĩa thống kê). Sự khác biệt chủ yếu là do giảm dòng chảy mạch vành, thiếu máu cục bộ, hoặc lựa chọn bác sĩ làm thủ thuật, tất cả các nguyên nhân này đều xảy ra thường xuyên hơn ở nhóm sử dụng ticagrelor trong bệnh viện (Bảng 2). Ngược lại, thuyên tắc mạch ngoại biên đã được xác định là lý do sử dụng ức chế glycoprotein IIb/IIIa tiêm tĩnh mạch thường xuyên hơn ở nhóm sử dụng ticagrelor trước bệnh viện.
|
Bảng 2. Sử dụng ức chế Glycoprotein IIb/IIIa tiêm tĩnh mạch trong quá trình PCI |
||||
|---|---|---|---|---|
|
Endpoint |
Pre-Hospital Ticagrelor |
In-Hospital Ticagrelor |
Odds Ratio |
p Value |
|
Patients with thrombotic bail-out with glycoprotein IIb/IIIa inhibitors |
75 (9.4) |
100 (12.0) |
0.756 (0.551–1.038) |
0.084 |
|
Reason |
|
|
|
|
|
Decrement in TIMI flow grade or abrupt closure |
8 (1.0) |
20 (2.4) |
|
|
|
No reflow |
8 (1.0) |
8 (1.0) |
|
|
|
Side-branch closure |
2 (0.3) |
1 (0.1) |
|
|
|
Dissection with decreased flow |
2 (0.3) |
3 (0.4) |
|
|
|
Distal embolization |
15 (1.9) |
9 (1.1) |
|
|
|
Clinical instability due to ischemia/prolonged ischemia during the procedure |
7 (0.9) |
11 (1.3) |
|
|
|
Other (physician’s decision) |
33 (4.1) |
48 (5.8) |
|
|
Tái tưới máu mạch vành sau can thiệp
Không có sự khác biệt có ý nghĩa thống kê giữa 2 nhóm dùng ticagrelor trước và trong bệnh viện sau PCI về tiêu chí đạt dòng chảy TIMI cấp 3 hoặc giảm ≥70% đoạn chênh ST tại thời điểm 1 h (Bảng 3). Tuy nhiên, cả hai tiêu chí đều cho thấy sự khác biệt về số học theo hướng có lợi của nhóm sử dụng ticagrelor trước bệnh viện. Cải thiện độ chênh ST ≥70% đo 1 giờ sau khi PCI xảy ra ở 57.5% bệnh nhân trong nhóm trước bệnh viện và ở 52.5% bệnh nhân trong nhóm trong bệnh viện (p = 0.055). Mức độ cải thiện đoạn ST chênh sau khi PCI là khác biệt có ý nghĩa giữa 2 nhóm (trung bình 75.0% trong nhóm trước nhập viện, so với 71.4% ở nhóm trong bệnh viện, p = 0.049).
|
Bảng 3. Tái tưới máu mạch vành sau PCI |
||||
|
Endpoint |
Pre-Hospital Ticagrelor |
In-Hospital Ticagrelor |
Odds Ratio (95% CI) |
p Value |
|
No. of subjects∗ |
760 |
784 |
|
|
|
TIMI flow grade 3 of MI culprit vessel post-PCI |
625 (82.2) |
630 (80.4) |
1.132 (0.876–1.462) |
0.344 |
|
No. of subjects∗ |
713 |
743 |
|
|
|
ST-segment elevation resolution ≥70% post-PCI |
410 (57.5) |
390 (52.5) |
1.225 (0.996–1.506) |
0.055 |
|
No. of subjects∗ |
713 |
743 |
|
0.049† |
|
Degree of ST-segment elevation resolution 1 h post-PCI, % |
66.7 ± 36.8, 75.0 |
63.9 ± 34.3, 71.4 |
|
|
Kết quả tương tự cũng được quan sát thấy trong dân số chung ở 2 nhóm sử dụng ticagrelor trước và trong bệnh viện ở tiêu chí đạt dòng chảy TIMI 3 sau PCI/chụp mạch vành (82.1% so với 80.4%; p = 0.389), tỷ lệ bệnh nhân cải thiện độ chênh ST ≥70% (54.5% so với 50.1%; p = 0.080), và mức độ cải thiện độ chênh ST (trung bình 73.3%, so với 70.0%; p = 0.045).
Kết cục lâm sàng trong 24 h
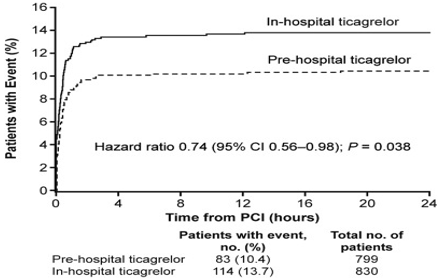
Tại thời điểm 24 giờ, tỷ lệ biến cố gộp thiếu máu cơ tim cục bộ gồm tử vong, nhồi máu cơ tim (MI), tái thông mạch máu khẩn cấp, huyết khối trong stent xác định, hoặc tiêm tĩnh mạch chất ức chế glycoprotein IIb/IIIa thấp hơn có ý nghĩa đến 27% giữa nhóm sử dụng ticagrelor trước bệnh viện so với nhóm trong bệnh viện (10.4 % so với 13.7%; p = 0.039) (bảng 4, hình 3).
|
Bảng 4. Kết cục lâm sàng trong vòng 24h |
||||
|
Endpoint |
Pre-Hospital Ticagrelor |
In-Hospital Ticagrelor |
Odds Ratio |
p Value |
|
Composite of death/new MI/urgent revascularization/definite stent thrombosis/bail-out glycoprotein IIb/IIIa inhibitor use |
83 (10.4) |
114 (13.7) |
0.728 (0.539–0.984) |
0.039 |
|
Composite of death/new MI/urgent revascularization/definite stent thrombosis |
10 (1.3) |
17 (2.0) |
0.606 (0.276–1.332) |
0.213 |
|
New MI or definite acute stent thrombosis |
0 (0.0) |
13 (1.6) |
0.027 (0.017–0.184)∗ |
<0.001∗ |
|
New MI |
0 (0.0) |
6 (0.7) |
0.058 (0.032–0.541)† |
0.031∗ |
|
Definite stent thrombosis |
0 (0.0) |
8 (1.0) |
0.044 (0.025–0.357)† |
0.008∗ |
|
Bail-out glycoprotein IIb/IIIa inhibitor use |
75 (9.4) |
100 (12.0) |
0.756 (0.551–1.038) |
0.084 |
|
Urgent revascularization |
1 (0.1) |
5 (0.6) |
0.207 (0.024–1.774) |
0.151 |
|
Stroke (ischemic) |
1 (0.1) |
0 (0) |
3.558 (0.303–9.545)† |
0.491∗ |
|
All-cause mortality |
9 (1.1) |
2 (0.2) |
4.716 (1.016–21.896) |
0.048 |
Khi loại trừ tiêu chí sử dụng ức chế glycoprotein IIb/IIIa tiêm tĩnh mạch từ tiêu chí biến cố gộp, sự khác biệt vẫn giữ theo hướng có lợi cho việc sử dụng ticagrelor trước bệnh viện nhưng không còn ý nghĩa thống kê (1.3% so với 2.0%; p = 0.212) (Hình 4). Tuy nhiên, 2 tiêu chí riêng biệt gồm tỷ lệ huyết khối trong stent xác định và tỷ lệ NMCT mới thấp hơn có ý nghĩa ở nhóm trước bệnh viện. Điều thú vị là tất cả các biến cố (ngoại trừ 1 biến cố NMCT) đều xảy ra ở những bệnh nhân không có biểu hiện huyết khối trong stent: đó là những biến cố mới không lên quan đến sang thương đã được đặt stent.
|
Hình 3. Biến cố gộp Tử vong/NMCT/Tái tưới máu khẩn/Huyết khối trong stent xác định/ Sử dụng ức chế glycoprotein IIb/IIIa tiêm tĩnh mạch trong vòng 24h sau PCI |
|
|
|
Tại thời điểm 24h, tỷ lệ biến cố gộp của nhóm sử dụng ticagrelor trước nhập viện thấp hơn có ý nghĩa so với nhóm sử dụng ticagrelor trong bệnh viện (10.4% vs. 13.7%; p = 0.04)
|
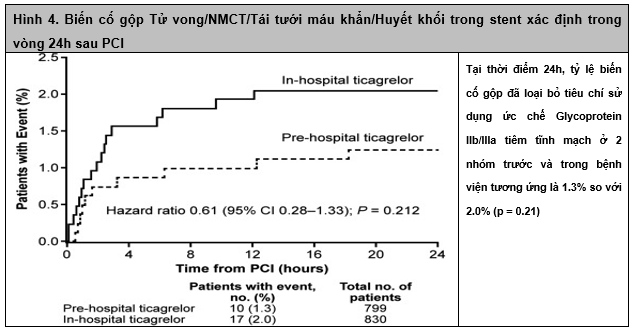
Tiêu chí kép của nhồi máu cơ tim mới hoặc huyết khối trong stent cũng thấp hơn có ý nghĩa ở nhóm dùng ticagrelor trước bệnh viện, và tất cả các biến cố đều xảy ra ở nhóm sử dụng ticagrelor trong bệnh viện trong vòng 24 giờ, hầu hết trong vòng 4 giờ đầu tiên (Hình 5).
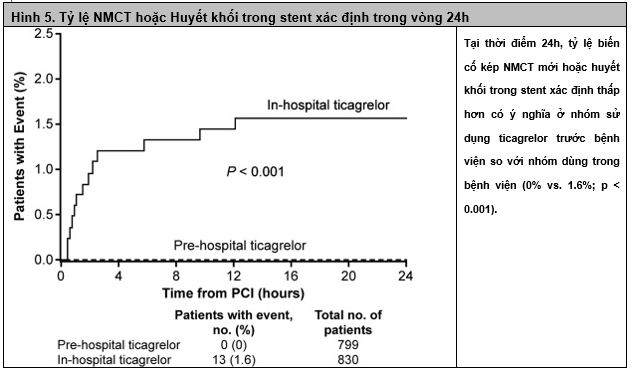
Kết cục lâm sàng tại thời điểm 24 h ở cả 2 nhóm dùng ticagrelor trước so với trong bệnh viện trên dân số chung (PCI và chụp mạch vành) có thể so sánh với kết quả của nhóm dân số có PCI trên các tiêu chí gộp tử vong, NMCT và tái thông mạch máu khẩn cấp (1.1% so với 1.3%; p = 0.761), NMCT đơn độc (0% so với 0.6%; p = 0.031). Tuy nhiên sự khác biệt ở tiêu chí tử vong do mọi nguyên nhân không còn ý nghĩa thống kê (9 bệnh nhân [1.0%] so với 3 bệnh nhân [0.3%]; p = 0.083).
Các nguyên nhân gây tử vong trong giai đoạn này bao gồm sốc tim (n = 4), ngừng tim (n = 3), các biến chứng cơ học (n = 3) và suy tim (n = 1). Ngoài ra còn có 5 bệnh nhân tử vong ngay sau khi phân ngẫu nhiên nhưng trước khi tiến hành thủ thuật (3 bệnh nhân ở nhóm trước nhập viện do ngừng tim, rung thất, và suy tim còn 2 bệnh nhân ở nhóm trong bệnh viện do ngừng tim và tràn máu màng phổi) không được đưa vào phân tích bắt đầu từ thời điểm PCI.
Tính an toàn
Trong bảng 5 là tỷ lệ chảy máu không liên quan đến mổ bắc cầu mạch vành trong vòng 24h sau PCI. Không có sự khác biệt có ý nghĩa thống kê giữa 2 nhóm điều trị về các biến chứng chảy máu lớn hay nhỏ. Các kết quả phù hợp với tất cả mọi định nghĩa và phân loại chảy máu điều chỉnh bởi Ủy ban biến cố lâm sàng.
|
Bảng 5. Tỷ lệ chảy máu không liên quan đến mổ bắc cầu mạch vành trong vòng 24h sau PCI |
|||
|---|---|---|---|
|
Definition and Bleeding Category |
With Bleeding Event∗
|
p Value |
|
|
Pre-Hospital Ticagrelor |
In-Hospital Ticagrelor |
||
|
PLATO |
|
|
|
|
Major |
13 (1.6) |
8 (1.0) |
0.240 |
|
Minor |
7 (0.9) |
9 (1.1) |
0.663 |
|
Composite of major and minor |
20 (2.5) |
17 (2.1) |
0.548 |
|
STEEPLE |
|
|
|
|
Major |
14 (1.7) |
7 (0.8) |
0.107 |
|
Minor |
5 (0.6) |
10 (1.2) |
0.218 |
|
Unknown |
2 (0.2) |
1 (0.1) |
0.544 |
|
TIMI |
|
|
|
|
Major |
7 (0.9) |
3 (0.4) |
0.186 |
|
Minor |
13 (1.6) |
11 (1.3) |
0.622 |
|
Minimal |
1 (0.1) |
4 (0.5) |
0.191 |
|
GUSTO |
|
|
|
|
Severe or life-threatening |
7 (0.9) |
3 (0.4) |
0.186 |
|
Moderate |
2 (0.2) |
2 (0.2) |
0.974 |
|
Mild |
12 (1.5) |
13 (1.6) |
0.906 |
|
BARC type |
|
|
|
|
0 |
0 |
0 |
|
|
1 |
1 (0.1) |
1 (0.1) |
0.981 |
|
2 |
8 (1.0) |
11 (1.3) |
0.535 |
|
3 |
11 (1.4) |
6 (0.7) |
0.198 |
|
3a |
4 (0.5) |
3 (0.4) |
0.672 |
|
3b |
6 (0.7) |
3 (0.4) |
0.292 |
|
3c |
1 (0.1) |
0 |
|
|
4 |
0 |
0 |
|
|
5 |
1 (0.1) |
0 |
|
|
5a |
0 |
0 |
|
|
5b |
0 |
0 |
|
|
Unknown |
0 |
0 |
|
BÀN LUẬN
Các kết quả chính của nghiên cứu ATLANTIC cho thấy không có sự khác biệt giữa hai nhóm điều trị bằng ticagrelor trước và trong bệnh viện về tái tưới máu mạch vành trước PCI, tính bằng mức độ đạt được cải thiện đoạn ST chênh và dòng chảy TIMI cấp 3 tại thời điểm nhập phòng thông tim can thiệp (1). Tuy nhiên, ở nhóm điều trị trước bệnh viện có ghi nhận thấy khả năng làm giảm sớm biến cố huyết khối trong stent. Các nhà nghiên cứu đưa ra giả thuyết rằng phát hiện này có thể không phải là ngẫu nhiên mà nhiều khả năng chính là hiệu quả khi sử dụng ticagrelor trước nhập viện, và có thể dẫn đến khả năng bảo vệ sớm hơn của động mạch liên quan nhồi máu và các vi mạch máu bị tắc sau khi PCI. Thật ra, nếu cân nhắc thời gian khởi phát tác động của ticagrelor, sự chênh lệch thời gian ngắn chỉ khoảng 31 phút giữa 2 chiến lược điều trị dường như là quá ngắn để mang đến lợi ích về tái tưới máu tiền PCI (4). Phân tích này đã khảo sát khoảng thời gian 24 giờ đầu tiên sau khi bắt đầu PCI tiên phát để xem liệu có bất kỳ tác động nào của chiến lược điều trị trước nhập viện trên các biến cố tắc nghẽn mạch vành sau PCI hay không. Các biến cố xảy ra sau đó cho đến sau 30 ngày theo dõi có thể ít liên quan đến chiến lược điều trị ban đầu, do đó làm giảm hiệu quả tích cực ban đầu
Phân tích này cho thấy sự khác biệt lớn nhất về tình trạng kết tập tiểu cầu giữa 2 chiến lược xảy ra ngay sau khi PCI (không thực hiện đo lường trong khi PCI), và sự khác biệt lớn nhất ở mức độ cải thiện độ chênh đoạn ST được quan sát thấy tại thời điểm 1 giờ sau khi PCI. Những phát hiện này là phù hợp với báo cáo trước đó về chỉ số phản ứng tiểu cầu đo bằng test phosphoryl hóa phosphoprotein kích thích bằng thuốc giãn mạch của các bệnh nhân điều trị bằng ticagrelor trước bệnh viện (trung bình khoảng 2.3 h để đạt được mức phản ứng tiểu cầu <50%) (5) và kết quả được báo cáo trong nghiên cứu ATLANTIC, trong đó bao gồm mức phản ứng trước PCI (1).
Trong suốt quá trình làm thủ thuật, tỷ lệ sử dụng thuốc ức chế glycoprotein IIb/IIIa tiêm tĩnh mạch bởi các nhà nghiên cứu đã được làm mù về chiến lược điều trị ticagrelor là một tiêu chí phản ánh những biến chứng hoặc quan ngại về huyết khối. Một số nhỏ bệnh nhân cần sử dụng các chất ức chế glycoprotein IIb/IIIa trong quá trình làm thủ thật ở nhóm điều trị trước bệnh viện. Tỷ lê biến cố gộp thiếu máu cơ tim cục bộ bao gồm tử vong, NMCT, tái thông mạch máu khẩn cấp, huyết khối trong stent xác định, và sử dụng chất ức chế glycoprotein IIb/IIIa tiêm tĩnh mạch là thấp hơn đáng kể tại thời điểm 24 h ở nhóm trước bệnh viện. Tiêu chí gộp trên phản ánh các biến chứng mạch vành của PCI dẫn đến huyết khối trong stent, sử dụng chất ức chế glycoprotein IIb/IIIa tiêm tĩnh mạch, hoặc tái thông mạch máu khẩn cấp sau khi PCI. Tỷ lệ huyết khối trong stent và NMCT cũng thấp hơn đáng kể ở nhóm dùng ticagrelor trước bệnh viện. Điều thú vị là ngoại trừ một tiêu chí, tất cả các biến cố NMCT khác đều không liên quan đến huyết khối trong stent, cho thấy nhóm điều trị trước bệnh viện đã được bảo vệ chống thuyên tắc mạch vành tốt hơn ở những đoạn mạch không phải động mạch thủ phạm nếu bệnh nhân tổn thương đa mạch (6). Khi biến cố huyết khối trong stent được kết hợp với biến cố NMCT tái phát, tất cả đều xảy ra trong 24 giờ sau khi PCI ở nhóm điều trị bằng ticagrelor trong bệnh viện (Hình 4), điều đó cho thấy khả năng bảo vệ trong thời gian sau thủ thuật khi điều trị bằng ticagrelor sớm hơn. Các kết quả hiện này phù hợp với kết quả của nghiên cứu CLARITY-TIMI 28, trong đó cho thấy lợi ích rõ ràng của clopidogrel so với giả dược trên khả năng cải thiện tắc nghẽn mạch vành tổng thể và kết quả lâm sàng ở bệnh nhân STEMI bước đầu điều trị bằng tiêu sợi huyết cũng cho thấy rằng ít nhất một trong những lợi ích của các thuốc kháng thụ thể P2Y12 có thể quan sát thấy sau khi tái tưới máu (7, 8). Ngoài ra kết quả này cũng tương đồng với kết quả của nghiên cứu HORIZONS-AMI trong đó quan sát thấy nguy cơ huyết khối trong stent sớm có tỷ lệ cao hơn ở những bệnh nhân được điều trị với bivalirudin so với những người điều trị với heparin không phân đoạn cộng với một chất ức chế glycoprotein IIb/IIIa (9). Tất cả bệnh nhân cũng nhận được một liều nạp clopidogrel hay ticlopidine trước khi can thiệp, và các tác giả đánh giá rằng tỷ lệ huyết khối trong stent sớm cao hơn ở nhóm bivalirudin có khả năng liên quan đến kích hoạt tiểu cầu bởi adenosine diphosphate trước khi các thụ thể P2Y12 được bất hoạt tối đa hoặc hoạt động tồn dư của thrombin sau khi ngưng bivalirudin (khi kết thúc chụp động mạch hoặc PCI). Cuối cùng, lợi ích quan sát được ở nhóm sử dụng ticagrelor sớm trong nghiên cứu cũng tương tự với kết quả của cangrelor tác động nhanh ở những bệnh nhân PCI (10, 11).
An toàn trong 24 giờ đầu tiên đã được so sánh trong 2 nhóm nghiên cứu cho cả biến chứng chảy máu lớn và nhỏ, mặc dù việc sử dụng các thuốc ức chế glycoprotein IIb/IIIa tiêm tĩnh mạch nhiều hơn ở nhóm dùng ticagrelor trong bệnh viện. Những phát hiện này là nhất quán với nhiều định nghĩa khác nhau được sử dụng.
Xu hướng tử vong cao hơn quan sát được trong nghiên cứu ATLANTIC ở nhóm sử dụng ticagrelor trước bệnh viện đã được chứng minh rõ trong 24 giờ đầu tiên sau khi PCI. Phát hiện này trái ngược với tỷ lệ thấp hơn của các biến cố thiếu máu cục bộ không tử vong và tỷ lệ biến chứng xuất huyết ở nhóm điều trị sớm so với nhóm điều trị trong bệnh viện. Phân tích các nguyên nhân tử vong cụ thể cũng cho thấy rằng các trường hợp tử vong này không liên quan đến biến cố thiếu máu cục bộ hay chảy máu mà chủ yếu là do mức độ nghiêm trọng của biến cố NMCT dẫn đến biến chứng cơ học và sốc. Các bệnh nhân chết là thường già hơn rất nhiều so với những người sống sót, đa phần là phụ nữ, bệnh nhân bị bệnh tiểu đường, hoặc bệnh nhân có suy tim, điểm nguy cơ TIMI cao hơn, và các biến chứng cơ học hoặc sốc phát triển nhanh chóng sau khi PCI.
Tỷ lệ dùng stent phủ thuốc và can thiệp qua động mạch quay cũng ít hơn trong nhóm những bệnh nhân tử vong. Thời gian tử vong cũng cho thấy các trường hợp này không liên quan đến việc sử dụng ticagrelor trước hay trong bệnh viện vì một số trường hợp tử vong xảy ra rất sớm, trước khi ticagrelor có hiệu quả về mặt sinh học. Giả thuyết về nguy cơ gây tử vong ngay của ticagrelor vốn chỉ được quan sát ở nhóm trước bệnh viện bên cạnh sự khác biệt chỉ có 31 phút giữa 2 nhóm điều trị là không có giá trị xem xét. Nhiều khả năng là do ngẫu nhiên và sự mất cân bằng giữa 2 nhóm điều trị về mức độ nghiêm trọng của các biến cố, dẫn đến tỷ lệ sốc tim sớm, ngừng tim, hoặc vỡ tim cao hơn ở nhóm trước nhập viện. Tuy nhiên cần lưu ý rằng nghiên cứu này không đủ mạnh để so sánh giữa các nhóm bệnh nhân về tỷ lệ tử vong.
Nhìn chung, phân tích thăm dò này là phù hợp với các kết quả chính của nghiên cứu ATLANTIC và chứng minh thêm rằng những giờ đầu tiên sau khi PCI là khoảng thời gian dễ bị tổn thương, cũng như những lợi ích tiềm năng của việc sử dụng ticagrelor trước nhập viện ở bệnh nhân STEMI được PCI tiên phát. Kết quả cũng cho thấy tiềm năng của các thuốc kháng tiểu cầu truyền tĩnh mạch trong giai đoạn đầu khi các chất đối kháng thụ thể P2Y12 đường uống vẫn chưa thể hiện hết hiệu quả tối đa (10, 11, 12, 13, 14, 15 và 16). Ticagrelor dạng nghiền cũng có thể cho hiệu quả ức chế tiểu cầu sớm hơn so với dạng viên (17)
HẠN CHẾ CỦA NGHIÊN CỨU
Hạn chế của phân tích ATLANTIC-H24 nằm ở tính chất chỉ thăm dò của phân tích hậu kiểm này. Cũng như nghiên cứu ATLANTIC tổng thể, hạn chế liên quan đến kích cỡ mẫu, đặc biệt ở phân nhóm chức năng tiểu cầu. Những phát hiện này cần được diễn giải một cách thận trọng vì số liệu rất nhỏ và những khác biệt không có ý nghĩa thống kê đối với tất cả các tiêu chí. Tuy nhiên phân tích ATLANTIC-H24 đã nỗ lực để giải quyết hạn chế do khoảng thời gian chênh lệch ngắn giữa 2 chiến lược điều trị cũng như giữa chẩn đoán và PCI.
KẾT LUẬN
Hiệu quả của ticagrelor trước bệnh viện trở nên rõ ràng sau khi PCI, với sự khác biệt đáng quan tâm trong phản ứng tiểu cầu và tái tưới máu ngay lập tức sau PCI, kết hợp với giảm các biến cố thiếu máu cục bộ, bao gồm huyết khối trong stent, trong 24 giờ đầu tiên, trong khi chỉ làm tang nhẹ tỷ lệ tử vong.
TÀI LIỆU THAM KHẢO
1. Montalescot G, van t Hof AW, Lapostolle F, et al. Prehospital ticagrelor in ST-segment elevation myocardial infarction. N Engl J Med 2014; 371:1016–27.
2. Montalescot G, van t Hof AW. Prehospital ticagrelor in ST-segment elevation myocardial infarction (letter). N Engl J Med 2014; 371:2339.
3. Montalescot G, Lassen JF, Hamm CW, et al. Ambulance or in-catheterization laboratory administration of ticagrelor for primary percutaneous coronary intervention for ST-segment elevation myocardial infarction: rationale and design of the randomized, double-blind Administration of Ticagrelor in the cath Lab or in the Ambulance for New ST elevation myocardial Infarction to open the Coronary artery (ATLANTIC) study. Am Heart J 2013; 165:515–22.
4. Valgimigli M, Tebaldi M, Campo G, et al. Prasugrel versus tirofiban bolus with or without short post-bolus infusion with or without concomitant prasugrel administration in patients with myocardial infarction undergoing coronary stenting: the FABOLUS PRO (Facilitation through Aggrastat By drOpping or shortening Infusion Line in patients with ST-segment elevation myocardial infarction compared to or on top of PRasugrel given at loading dOse) trial. J Am Coll Cardiol Intv 2012; 5:268–77.
5. Koul S, Andell P, Martinsson A, et al. A pharmacodynamic comparison of 5 anti-platelet protocols in patients with ST-elevation myocardial infarction undergoing primary PCI. BMC Cardiovasc Disord 2014; 14:189.
6. Wald DS, Morris JK, Wald NJ. Preventive angioplasty in myocardial infarction. N Engl J Med 2014; 370:283.
7. Sabatine MS, Cannon CP, Gibson CM, et al. Addition of clopidogrel to aspirin and fibrinolytic therapy for myocardial infarction with ST-segment elevation. N Engl J Med 2005; 352:1179–89.
8. Scirica BM, Sabatine MS, Morrow DA, et al. The role of clopidogrel in early and sustained arterial patency after fibrinolysis for ST-segment elevation myocardial infarction: the ECG CLARITY-TIMI 28 Study. J Am Coll Cardiol 2006; 48:37–42.
9. Stone GW, Witzenbichler B, Guagliumi G, et al. Bivalirudin during primary PCI in acute myocardial infarction. N Engl J Med 2008; 358:2218–30.
10. Bhatt DL, Lincoff AM, Gibson CM, et al. Intravenous platelet blockade with cangrelor during PCI. N Engl J Med 2009; 361:2330–41.
11. Bhatt DL, Stone GW, Mahaffey KW, et al. Effect of platelet inhibition with cangrelor during PCI on ischemic events. N Engl J Med 2013; 368:1303–13.
12. Montalescot G, Barragan P, Wittenberg O, et al. Platelet glycoprotein IIb/IIIa inhibition with coronary stenting for acute myocardial infarction. N Engl J Med 2001;344: 1895–903.
13. De Luca G, Navarese E, Marino P. Risk profile and benefits from Gp IIb-IIIa inhibitors among patients with ST-segment elevation myocardial infarction treated with primary angioplasty: a meta-regression analysis of randomized trials. Eur Heart J 2009; 30:2705–13.
14. Huber K, Holmes DR, Jr., van t Hof AW, et al. Use of glycoprotein IIb/IIIa inhibitors in primary percutaneous coronary intervention: insights from the APEX-AMI trial. Eur Heart J 2010; 31:1708–16.
15. Stone GW, Grines CL, Cox DA, et al. Comparison of angioplasty with stenting, with or without abciximab, in acute myocardial infarction. N Engl J Med 2002; 346:957–66.
16. van t Hof AW, ten Berg JM, Heestermans T, et al. Prehospital initiation of tirofiban in patients with ST-elevation myocardial infarction undergoing primary angioplasty (On-TIME 2): a multicentre, double-blind, randomised controlled trial. Lancet 2008; 372:537–46.
17. Parodi G, Xanthopoulou I, Bellandi B, et al. Ticagrelor crushed tablets administration in STEMI patients: the MOJITO study. J Am Coll Cardiol 2015; 65:511–2.