ThS.BS. HOÀNG PHI ĐIỆP
Bệnh viện Đông Đô
Tóm tắt
Biến chứng tim mạch là một trong những vấn đề quan trọng sau ghép tế bào gốc tạo máu (HSCT) và ảnh hưởng đáng kể đến tiên lượng người bệnh. Chúng tôi báo cáo một trường hợp suy tim cấp xuất hiện sớm sau ghép tế bào gốc tạo máu đồng loài ở bệnh nhân nữ 39 tuổi mắc lơ-xê-mi cấp dòng tủy (AML-M2). Bệnh nhân được điều trị nhiều đợt hóa trị chứa anthracycline và cytarabine, đạt lui bệnh hoàn toàn trước khi ghép tế bào gốc từ người cho nửa hòa hợp là chị gái. Trước ghép, bệnh nhân không có bệnh tim mạch và chức năng tim bình thường với phân suất tống máu thất trái (EF) 62%. Giai đoạn sớm sau ghép, bệnh nhân sốt kéo dài và từ ngày D+3 xuất hiện khó thở, phù toàn thân và tăng cân nhanh, gợi ý quá tải dịch hoặc rối loạn chức năng tim cấp. Từ ngày D+13 đến D+17, tình trạng hô hấp xấu đi và được chẩn đoán xuất huyết phế nang lan tỏa, đồng thời xuất hiện suy tim cấp với phù phổi và NT-proBNP tăng rất cao. Bệnh nhân được điều trị tích cực bằng lợi tiểu liều cao, sacubitril/valsartan, corticosteroid và các biện pháp kiểm soát xuất huyết. Sau điều trị, triệu chứng cải thiện nhanh với giảm phù, giảm cân và NT-proBNP giảm dần, bệnh nhân cai oxy từ ngày D+22. Sau 11,5 tháng, chức năng tim hồi phục hoàn toàn với EF 69% và bệnh nhân dừng các thuốc điều trị suy tim. Tuy nhiên, theo dõi đến sau 3 năm, EF 68% và chỉ số strain cơ tim giảm còn -16.4%. Bệnh nhân được chỉ định dùng lại các thuốc tim mạch và đến nay tình trạng lâm sàng ổn định. Trường hợp này nhấn mạnh tầm quan trọng của việc nhận diện sớm biến chứng suy tim cấp sau HSCT và cho thấy chiến lược điều trị tích cực theo dõi lâu dài có thể giúp phục hồi chức năng tim và cải thiện tiên lượng lâu dài.
Từ khóa: Suy tim cấp; Ghép tủy / ghép tế bào gốc tạo máu; Bạch cầu cấp; Độc tính tim do hóa trị; Cyclophosphamide / anthracycline;
Tổng quan
Ghép tế bào gốc tạo máu (hematopoietic stem cell transplantation, HSCT) hiện là phương pháp điều trị có khả năng chữa khỏi cho nhiều bệnh lý huyết học ác tính, trong đó có bạch cầu cấp, đồng thời cũng được áp dụng cho một số bệnh không ác tính. Đến cuối năm 2019, khoảng 1,5 triệu người trên thế giới đã được thực hiện HSCT, với tần suất khoảng 84.000 ca mỗi năm [5]. Nhờ cải thiện lựa chọn người bệnh, người cho, phác đồ điều kiện hóa và điều trị hỗ trợ, kết quả sống còn sau ghép đã được cải thiện rõ rệt. Tuy nhiên, vẫn có một tỉ lệ đáng kể các bệnh nhân gặp các biến chứng nặng sau ghép, đặc biệt là biến chứng tim mạch. Biến chứng này có thể xuất hiện ở cả giai đoạn sớm và muộn, với các biểu hiện thường gặp như rối loạn nhịp, suy tim, nhồi máu cơ tim và tràn dịch màng tim. Phân tích gộp 37 nghiên cứu với 30.957 bệnh nhân cho thấy tỷ lệ biến cố tim mạch chung sau HSCT là 16,84%; trong đó suy tim sung huyết 3,66%, rối loạn nhịp 3,91%, tăng huyết áp 17.71%, đột quỵ 0,22% và tử vong 1,53% [2].
Ở giai đoạn sớm sau ghép, việc nhận diện biến cố tim mạch đặc biệt quan trọng vì biểu hiện lâm sàng dễ bị che lấp bởi nhiễm trùng, quá tải dịch, độc tính thuốc hoặc các biến chứng liên quan GVHD. Tỉ lệ biến cố tim mạch trong 100 ngày đầu là 4.5% [1] và trong 180 ngày đầu lên đến 8.4% [6]. Trong đó, tỉ lệ suy tim chiếm đến hơn 37.21% [6]. Nguy cơ này tăng đáng kể ở nhóm ghép đồng loài so với ghép tự thân, bệnh bạch cầu, dùng cyclophosphamide sau ghép (PTCY), xạ toàn thân và có bệnh tim từ trước [6].
Về cơ chế bệnh sinh, độc tính tim sau HSCT là kết quả của nhiều yếu tố phối hợp, bao gồm phơi nhiễm anthracycline hoặc xạ trị trước ghép, phác đồ điều kiện hóa chứa cyclophosphamide/TBI, PTCY, bệnh ghép chống chủ (GVHD) và các rối loạn chuyển hóa xuất hiện sau ghép. Zhao và cộng sự nhấn mạnh rằng đánh giá chức năng tim trước ghép và theo dõi sau ghép bằng siêu âm tim kết hợp biomarker tim như troponin và peptide lợi niệu là cần thiết để lựa chọn phác đồ điều kiện hóa phù hợp và phát hiện sớm tổn thương tim [9]. Ở nhóm sống sót lâu dài sau HSCT, mô hình tiên lượng của Armenian cho thấy các yếu tố tuổi, liều anthracycline >250 mg/m², tăng huyết áp, đái tháo đường, hút thuốc và xạ trị ngực giúp phân tầng nguy cơ tim mạch 10 năm; tỷ lệ bệnh tim mạch tích lũy là 3,7% ở nhóm nguy cơ thấp, 9,9% ở nhóm trung gian và 26,2% ở nhóm nguy cơ cao [10].
Xuất phát từ những dữ kiện trên, suy tim cấp sau ghép tủy ở bệnh nhân bạch cầu cấp là một biến chứng không thường gặp nhưng có thể đe dọa tính mạng, dễ chẩn đoán muộn và chịu ảnh hưởng đồng thời của điều trị trước ghép, phác đồ điều kiện hóa cũng như các biến cố trong giai đoạn sau ghép. Việc báo cáo ca bệnh này nhằm làm rõ đặc điểm lâm sàng, yếu tố nguy cơ, cách tiếp cận chẩn đoán và chiến lược xử trí trong bối cảnh phối hợp giữa huyết học và tim mạch.
Trình bày ca bệnh
Bệnh nhân nữ, 39 tuổi, tiền sử khỏe mạnh. Tháng 12/2021, bệnh nhân xuất hiện mệt nhiều kèm rong kinh, được phát hiện giảm hai dòng tế bào máu và chuyển đến Viện Huyết học. Tại đây, bệnh nhân được chẩn đoán lơ-xê-mi cấp dòng tủy thể LAM2, các xét nghiệm khác không ghi nhận bất thường đáng kể. Trong năm 2021–2022, bệnh nhân được điều trị nhiều đợt hóa chất gồm phác đồ 3+7 (Gồm 2 thuốc hóa trị chính: là Anthracycline dùng trong 3 ngày đầu và Cytarabine dùng 7 ngày liên tiếp), tiếp theo là IDAC (Intermediate-Dose Cytarabine là phác đồ dùng cytarabine liều trung bình) và HIDAC (High-Dose Cytarabine là phác đồ dùng cytarabine liều cao), đạt lui bệnh hoàn toàn trước ghép. Quá trình đánh giá trước ghép ghi nhận chức năng hô hấp bình thường, khám chuyên khoa tim mạch không phát hiện bất thường, phân suất tống máu thất trái (EF) 62%. Bệnh nhân được chỉ định ghép tế bào gốc tạo máu đồng loài nửa hòa hợp từ chị gái, nhập viện ghép ngày 31/10/2022; điều kiện hóa bằng phác đồ Bu-Cy-Cypent (Gồm Busulfan, Cyclophosphamide và Pentostatin), truyền tế bào gốc ngày 14/11/2022.
Sau ghép, bệnh nhân diễn biến phức tạp ngay từ giai đoạn sớm. Từ D+1, bệnh nhân sốt liên tục, procalcitonin tăng cao. Đến D+3, xuất hiện khó thở, phù toàn thân, tăng 9 kg, phải điều trị lợi tiểu tích cực. D+5 ghi nhận tiêu chảy nhiều lần, xét nghiệm Clostridioides difficile dương tính. Từ D+13 đến D+15, tình trạng khó thở tăng dần; chụp cắt lớp vi tính lồng ngực cho hình ảnh viêm phổi do xuất huyết và bệnh nhân được chẩn đoán xuất huyết phế nang lan tỏa (diffuse alveolar hemorrhage, DAH), điều trị methylprednisolone liều 2 mg/kg/ngày. D+16, bệnh nhân khó thở tăng, nhịp thở 40 lần/phút, SpO2 90% khi thở oxy mask 8 L/phút, phải tăng oxy lên 12 L/phút; lợi tiểu ban đầu đáp ứng kém.
Tại thời điểm D+17, bệnh nhân ho máu kéo dài, ran ẩm hai phổi, vẫn phụ thuộc oxy lưu lượng cao. Xét nghiệm ghi nhận Pro-BNP khoảng 16.000 pg/mL, kèm phù phổi và quá tải dịch, gợi ý suy tim cấp sớm sau ghép trên nền biến chứng hô hấp nặng. Bệnh nhân được tăng liều lợi tiểu lên 120 mg/ngày, đồng thời khởi trị sacubitril/valsartan và dapagliflozin, phối hợp corticoid liều trung bình và Novo-7 (thuốc chứa yếu tố đông máu VIIa tái tổ hợp) để kiểm soát xuất huyết phế nang. D+18 kết quả cấy máu dương tính với Enterobacter cloacae complex, đáp ứng với loại kháng sinh đang sử dụng. Sau điều trị, bệnh nhân giảm 3 kg chỉ sau 1 ngày, Pro-BNP giảm nhanh theo diễn tiến 16.069 → 10.388 → 5.477 → 1.615 pg/mL, tình trạng phù cải thiện rõ, cai oxy từ D+22, hô hấp hồi phục hoàn toàn. Trong quá trình điều trị sau ghép, bệnh nhân đã được truyền 8 khối hồng cầu và 9 khối tiểu cầu. Ngày D+83, bệnh nhân ra viện, đơn thuốc tim mạch gồm sacubitril/valsartan và dapagliflozin.
Tuy nhiên, ngay sau khi ra viện, từ D+83 đến D+105 bệnh nhân phải tạm ngừng thuốc tim mạch do chóng mặt và huyết áp thấp. Tại các lần tái khám sau, chức năng tim có giai đoạn giảm nhẹ với EF 57% và đánh giá sức căng cơ tim (GLS) -16,2% sau 3,5 tháng, bệnh nhân được chỉ định sacubitril/valsartan 100 mg/ngày, Bisoprolol 2.5 mg/ngày và Spironolacton 50 mg/ngày, Furosemide 20 mg/ngày; sau 7 tháng EF 55%, GLS -12,5%, huyết áp thấp, được điều chỉnh thuốc tim mạch Perindopril 5 mg/ngày và Metoprolol succinate 25 mg/ngày. Đến 11,5 tháng sau ghép, EF cải thiện lên 69% (không được đo GLS), bệnh nhân dừng các thuốc điều trị suy tim. Tuy nhiên, tại thời điểm 12/11/2025, sau khoảng 3 năm theo dõi, bệnh nhân có EF 68%, GLS -16,4%, lâm sàng ổn định, bệnh nhân được chỉ định điều trị Perindopril 5 mg/ngày và Metoprolol succinate 25 mg/ngày. Đến nay, tình trạng bệnh nhân ổn định.
Bảng 1. Tóm tắt diễn biến bệnh
| Thời điểm | Diễn biến chính |
| 12/2021 | Chẩn đoán lơ-xê-mi cấp dòng tủy (LAM2) sau khi vào viện vì mệt nhiều và rong kinh. |
| 2021–2022 | Điều trị hóa chất các phác đồ 3+7, IDAC, HIDAC; đạt lui bệnh hoàn toàn trước ghép. |
| 17/10/2022 | Đánh giá trước ghép: chức năng tim mạch bình thường, EF 62%. |
| 31/10/2022 | Nhập viện ghép tế bào gốc tạo máu đồng loài. |
| 14/11/2022 (D0) | Truyền tế bào gốc từ chị gái, ghép nửa hòa hợp. |
| D+3 | Xuất hiện khó thở, phù toàn thân, tăng 9 kg (Gợi ý quá tải dịch/biến cố tim mạch sớm sau ghép). |
| D+15 | Chẩn đoán xuất huyết phế nang lan tỏa (DAH), điều trị methylprednisolone. |
| D+17 | Tình trạng nặng nhất: khó thở tăng, ho máu, ran ẩm hai phổi, Pro-BNP ~16.000 pg/mL; chẩn đoán suy tim cấp, bắt đầu sacubitril/valsartan và tăng cường lợi tiểu. |
| D+22 | Đáp ứng điều trị tốt: cai oxy, phù giảm rõ, Pro-BNP giảm nhanh. |
| D+83 | Ra viện trong tình trạng ổn định. |
| D+84 – D+105 | Chóng mặt, huyết áp thấp. Dừng thuốc điều trị suy tim |
| Sau 3.5 tháng | EF 57%, GLS -16.2%. Duy trì thuốc điều trị suy tim |
| Sau 7 tháng | EF 55%, GLS 12.5%. Duy trì thuốc điều trị suy tim |
| Sau 11,5 tháng | Chức năng tim cải thiện, EF 69%. Dừng thuốc điều trị suy tim |
| Sau 3 năm | EF 68% GLS -16.4%. Tiếp tục các thuốc điều trị suy tim |
Chẩn đoán
Dựa trên diễn biến lâm sàng và cận lâm sàng, bệnh nhân được chẩn đoán suy tim cấp sớm sau ghép tế bào gốc tạo máu đồng loài, biểu hiện bằng khó thở tiến triển, quá tải dịch, phù phổi, ran ẩm hai phổi và Pro-BNP tăng rất cao khoảng 16.000 pg/mL. Chẩn đoán này được củng cố bởi đáp ứng rõ sau điều trị theo hướng suy tim, với giảm cân nhanh sau tăng cường lợi tiểu, giảm dần Pro-BNP và cải thiện hô hấp.
Bên cạnh đó, bệnh nhân được chẩn đoán xuất huyết phế nang lan tỏa (diffuse alveolar hemorrhage – DAH) từ D+15 dựa trên biểu hiện ho máu kéo dài, hình ảnh chụp cắt lớp lồng ngực gợi ý viêm phổi do xuất huyết và đáp ứng với methylprednisolone phối hợp Novo-7. Ngoài ra cần chẩn đoán phân biệt giữa DAH và hội chứng suy hô hấp quanh mọc mảnh ghép (PERDS), do bệnh nhân đáp ứng với methylprednisolone liều 2 mg/kg/ngày; ngoài ra, kết quả cấy đờm mọc Enterobacter cloacae complex cho thấy cần cân nhắc thêm nhiễm trùng hô hấp phối hợp.
Vì vậy, ở thời điểm cấp, chẩn đoán hợp lý nhất là: suy tim cấp sớm sau ghép trên nền ghép tế bào gốc tạo máu đồng loài, kèm xuất huyết phế nang lan tỏa; chưa loại trừ hoàn toàn PERDS và nhiễm trùng phổi phối hợp.
Về cơ chế gây bệnh, bệnh nhân đã được điều trị nhiều đợt hóa chất trước ghép, sau đó tiếp tục trải qua phác đồ điều kiện hóa Bu-Cy-Cypent, cũng như truyền một lượng lớn máu và dịch sau ghép. Theo tổng quan của Zhao và cộng sự, các yếu tố như anthracycline, phác đồ chứa cyclophosphamide, cùng các biến cố sau ghép là những nguyên nhân quan trọng góp phần vào biến chứng tim mạch sau HSCT; đánh giá bằng siêu âm tim và biomarker tim như peptide lợi niệu não có giá trị trong theo dõi thường quy [9]. Điều này củng cố thêm tính hợp lý của chẩn đoán suy tim cấp trong ca bệnh này.
Điều trị và theo dõi
Sau khi xác lập chẩn đoán suy tim cấp sớm sau ghép trên nền suy hô hấp tiến triển, bệnh nhân được điều trị theo hướng phối hợp đồng thời kiểm soát quá tải tuần hoàn, hỗ trợ tim mạch và xử trí tổn thương phổi xuất huyết. Sau khi được điều trị phối hợp, người bệnh đáp ứng lâm sàng và cận lâm sàng khá rõ. Tình trạng quá tải dịch và suy hô hấp cải thiện nhanh sau khi tăng cường lợi tiểu và bổ sung điều trị tim mạch, thể hiện qua giảm cân nhanh, giảm dần nhu cầu oxy và xu hướng giảm mạnh của Pro-BNP. Đồng thời, tổn thương phổi xuất huyết cũng cải thiện sau điều trị phối hợp corticoid và Novo-7, với biểu hiện lâm sàng ổn định hơn và không còn cần hỗ trợ oxy.
Ở giai đoạn sau, bệnh nhân tiếp tục được duy trì điều trị nội khoa tim mạch thêm một thời gian, sau đó phải điều chỉnh thuốc do tụt huyết áp và chóng mặt. Theo dõi định kỳ cho thấy chức năng tim có giai đoạn giảm nhẹ trong những tháng đầu sau ra viện, nhưng không diễn tiến xấu thêm và dần hồi phục theo thời gian. Đến 11,5 tháng sau ghép, chức năng tâm thu thất trái phục hồi tốt. Tuy nhiên, sau khoảng 3 năm theo dõi, mặc dù EF trong giới hạn bình thường nhưng GLS có dấu hiệu giảm nhẹ và bệnh nhân dùng lại các thuốc tim mạch.
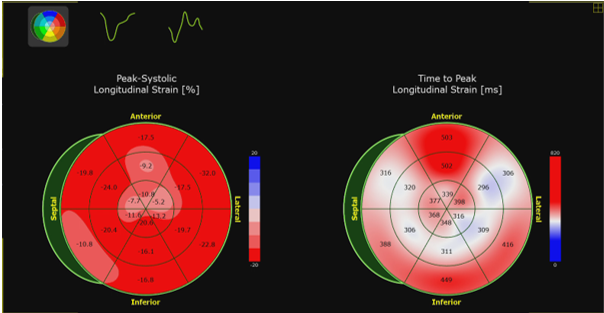
Hình 1. Kết quả đo GLS của bệnh nhân 3 năm sau HSCT. (GLS: -16.4%)
Nhìn chung, diễn biến của ca bệnh gợi ý suy tim cấp sau ghép có khả năng hồi phục nếu được nhận diện sớm, xử trí tích cực trong giai đoạn cấp. Đồng thời vẫn cần theo dõi tim mạch lâu dài sau ghép để dự phòng những tổn thương tồn dư.
Bàn luận
Ca bệnh của chúng tôi minh họa một biến chứng tim mạch cấp nặng nhưng dễ bị bỏ sót trong giai đoạn sớm sau ghép tế bào gốc tạo máu đồng loài ở bệnh nhân bạch cầu cấp. Trên thực tế, bệnh tim mạch sau HSCT đang ngày càng được quan tâm do số lượng bệnh nhân ghép tăng lên, tuổi ghép cao hơn và gánh nặng bệnh đồng mắc ngày càng lớn. Gent và cộng sự cho biết đến cuối năm 2019 đã có khoảng 1,5 triệu ca ghép tế bào gốc tạo máu trên toàn thế giới, với khoảng 84.000 ca mỗi năm; các biến chứng tim mạch thường gặp sau ghép gồm rối loạn nhịp nhĩ, suy tim, nhồi máu cơ tim và tràn dịch màng tim [5]. Trong phân tích gộp năm 2023 trên 30.957 bệnh nhân, tỷ lệ biến cố tim mạch chung sau HSCT là 16,84%, trong đó suy tim sung huyết chiếm 3,66% và rối loạn nhịp chiếm 3,91%; nguy cơ cao hơn ở ghép đồng loài so với ghép tự thân, và cao hơn ở nhóm bệnh bạch cầu [2]. Các dữ kiện này cho thấy biến chứng tim mạch sau ghép không phải là hiếm gặp, đặc biệt trong bối cảnh ghép đồng loài điều trị bệnh lý ác tính huyết học.
Điểm nổi bật của ca bệnh là suy tim cấp xuất hiện rất sớm sau ghép, đồng thời chồng lấp với các biến chứng hô hấp nặng như xuất huyết phế nang lan tỏa và có thể cả hội chứng suy hô hấp quanh mọc mảnh ghép. Theo tổng quan của Zhao và cộng sự, trong 100 ngày đầu sau HSCT, tỷ lệ rối loạn nhịp ở người lớn dao động từ 2–10%, suy tim sung huyết mới xuất hiện từ 0,4–2,2%, còn độc tính tim cấp nặng từ 0,9–8,9% [9] Nghiên cứu của Pérez-Valencia và cộng sự trên bệnh nhân ghép đồng loài ghi nhận tỷ lệ biến cố tim sớm trong 180 ngày đầu là 8,8%; trong đó các biến cố này làm tăng rõ tỉ lệ tử vong, với tỉ lệ rủi ro (Hazard Ratio – HR) 3,03 đối với giảm sống còn toàn bộ 2 năm và HR 4,68 đối với tử vong [6]. Ở nghiên cứu của Alblooshi và cộng sự, biến cố tim mạch trong 100 ngày đầu sau ghép đồng loài xảy ra ở 4,5% trường hợp; bệnh nhân có EF trước ghép <50% có nguy cơ cao hơn 5,3 lần so với nhóm EF >60% [1]. Trong ca bệnh này, EF trước ghép còn bảo tồn (62%), nhưng bệnh nhân lại có tiền sử điều trị nhiều đợt hóa chất trước ghép, sau đó tiếp tục được điều kiện hóa bằng phác đồ Bu-Cy-Cypent, rồi xuất hiện khó thở, phù toàn thân, Pro-BNP tăng tới 16.069 pg/mL và đáp ứng rõ với lợi tiểu cùng điều trị tim mạch, ủng hộ mạnh cho chẩn đoán suy tim cấp sớm sau ghép.
Về cơ chế bệnh sinh, suy tim cấp trong trường hợp này nhiều khả năng không phải do một yếu tố đơn độc mà là kết quả của độc tính tim tích lũy và các stress sinh lý đồng thời. Zhao và cộng sự nhấn mạnh rằng các yếu tố góp phần quan trọng vào biến chứng tim mạch sau HSCT bao gồm phơi nhiễm anthracycline trước ghép, xạ trị, phác đồ điều kiện hóa chứa cyclophosphamide, cùng các bệnh đồng mắc sau ghép như GvHD và nhiễm trùng [9]. Ca bệnh của chúng tôi có nhiều yếu tố thuận lợi như bạch cầu cấp dòng tủy, điều trị hóa chất cảm ứng và củng cố có anthracycline trước ghép, sau đó dùng phác đồ Bu-Cy-Cypent, kèm nhiễm trùng, quá tải dịch, tổn thương phổi xuất huyết và đáp ứng viêm toàn thân trong giai đoạn sớm sau ghép. Tổng quan của Gent và cộng sự cũng cho thấy cyclophosphamide liên quan với tỉ lệ suy tim/giảm chức năng thất trái, viêm màng ngoài tim, tràn dịch màng tim và rối loạn nhịp; trong khi cyclophosphamide sau ghép (PTCy) có thể đi kèm giảm chức năng thất trái đến 14,3–21,9%, suy tim có triệu chứng 5,1% và rối loạn nhịp 3,6% [3]. Tuy nhiên, mối liên quan giữa PTCy và độc tính tim không hoàn toàn đồng nhất giữa các nghiên cứu: Yeh và cộng sự ghi nhận 38/585 bệnh nhân (6,5%) có độc tính tim cấp trong 100 ngày đầu sau ghép, nhưng không thấy PTCy làm tăng nguy cơ so với nhóm không dùng PTCy, trong khi các yếu tố nguy cơ rõ hơn là tuổi >55, tăng huyết áp, đái tháo đường, tiền sử rối loạn nhịp và bệnh tim sẵn có [8]. Do đó, ở ca bệnh này, cyclophosphamide cần được xem là một mắt xích trong cơ chế đa yếu tố, hơn là nguyên nhân đơn độc.
Một điểm đáng chú ý khác là vai trò của biomarker tim, đặc biệt NT-proBNP/BNP, trong phát hiện sớm và tiên lượng độc tính tim sau ghép. Zhao và cộng sự khuyến nghị đánh giá chức năng tim bằng siêu âm tim kết hợp biomarker như troponin và peptide lợi niệu não như một phần theo dõi thường quy ở bệnh nhân HSCT [9]. Nghiên cứu mới của Polomski và cộng sự trên 807 bệnh nhân ghép đồng loài cho thấy NT-proBNP nền ≥125 ng/L liên quan với giảm sống còn 5 năm và tăng nguy cơ tử vong mọi nguyên nhân; trong phân tích đa biến, NT-proBNP ≥125 ng/L có HR hiệu chỉnh 1,29 còn NT-proBNP log-transform có HR 1,21 [7]. Mặc dù nghiên cứu này tập trung vào NT-proBNP nền trước ghép, kết quả của nó củng cố giá trị lâm sàng của peptide lợi niệu não như chỉ dấu nhận diện bệnh nhân nguy cơ cao. Trong ca bệnh hiện tại, Pro-BNP tăng rất cao đúng vào thời điểm bệnh cảnh lâm sàng nặng nhất, sau đó giảm nhanh song song với cải thiện phù, khó thở và nhu cầu oxy, cho thấy biomarker này có giá trị thực hành rõ rệt không chỉ trong chẩn đoán mà còn trong theo dõi đáp ứng điều trị. Tuy nhiên, hiện nay chưa khuyến cáo xét nghiệm các peptit lợi niệu thường quy khi bệnh nhân không có triệu chứng [4].
Ca bệnh này còn cho thấy thách thức chẩn đoán phân biệt trong thực hành. Khó thở và thâm nhiễm phổi sau ghép dễ quy cho viêm phổi, DAH, PERDS hoặc quá tải dịch đơn thuần; tuy nhiên, đáp ứng rất rõ với lợi tiểu, diễn tiến Pro-BNP, và hiệu quả của điều trị suy tim gợi ý rằng thành phần tim mạch có vai trò trung tâm trong bệnh cảnh này. Nói cách khác, suy tim cấp sau ghép có thể bị che lấp bởi các biến chứng hô hấp và nhiễm trùng đồng thời. Từ ca bệnh này, thông điệp thực hành là ở bệnh nhân bạch cầu cấp sau ghép đồng loài có tiền sử dùng anthracycline và phác đồ chứa cyclophosphamide, khi xuất hiện khó thở, tăng cân nhanh, phù và tăng nhu cầu oxy, cần chủ động nghĩ tới suy tim cấp, làm biomarker tim và siêu âm tim sớm thay vì chỉ tập trung vào nguyên nhân nhiễm trùng hoặc xuất huyết phổi [3, 7-9].
Diễn biến sau điều trị của bệnh nhân cũng mang nhiều ý nghĩa lâm sàng. Sau tăng cường lợi tiểu và khởi trị sacubitril/valsartan, bệnh nhân giảm cân nhanh, Pro-BNP giảm mạnh và cai oxy từ D+22. Chiến lược này phù hợp với khuyến cáo điều trị suy tim sau HSCT của Hội tim mạch Hoa Kì, trong đó nhấn mạnh việc kiểm soát dịch chặt chẽ [4]. Về dài hạn, EF giảm nhẹ thoáng qua trong vài tháng đầu rồi hồi phục dần, đạt 69% sau 11,5 tháng và ổn định 68% sau khoảng 3 năm. Điều này phù hợp với nhận định rằng một phần độc tính tim sau ghép có thể hồi phục nếu được nhận diện sớm và xử trí tích cực, nhất là khi yếu tố khởi phát cấp như quá tải dịch, viêm hệ thống hoặc độc tính thuốc được kiểm soát [3, 9]. Tuy nhiên, sự tồn tại của giai đoạn giảm EF/GLS kéo dài nhiều tháng sau ra viện cho thấy ngay cả khi lâm sàng cải thiện nhanh, bệnh nhân vẫn cần được theo dõi tim mạch lâu dài. Đây cũng là điểm thực hành quan trọng, bởi độc tính tim sau HSCT không chỉ là biến cố cấp tính mà còn có thể để lại hậu quả chức năng cơ tim kéo dài [3, 7, 9]. Về các thuốc điều trị, nhóm thuốc kháng thụ thể GLT2 (SGLT2i) đã có bằng chứng cải thiện tiên lượng ở bệnh nhân suy tim có phơi nhiễm với độc tính của các thuốc điều trị ung thư [11]. Tuy nhiên, cho đến nay vẫn khuyến cáo sử dụng các thuốc theo hướng dẫn điều trị suy tim chung mà không có nhóm thuốc ưu tiên cho bệnh nhân sau HSCT hay ung thư [4].
Cuối cùng, báo cáo này có một số hạn chế. Đây là một ca bệnh đơn lẻ nên chưa thể xác định chính xác vai trò tương đối của từng yếu tố như anthracycline, cyclophosphamide, DAH/PERDS, nhiễm trùng hay quá tải dịch trong cơ chế suy tim cấp. Bên cạnh đó, bệnh cảnh hô hấp phức tạp khiến việc tách biệt hoàn toàn tổn thương tim do thuốc với suy tim thứ phát do stress toàn thân là rất khó. Dù vậy, chính tính chất đa yếu tố và chồng lấp này lại là giá trị của ca bệnh, vì nó phản ánh đúng thách thức của thực hành lâm sàng ở bệnh nhân HSCT. Việc nhận diện sớm, điều trị tích cực và theo dõi tim mạch lâu dài có thể cải thiện kết cục và góp phần hạn chế tử suất không do tái phát ở nhóm người bệnh này [1, 6-9].
Kết luận
Ca bệnh cho thấy suy tim cấp sau ghép tủy là biến chứng đa yếu tố, dễ bị che lấp bởi các biến chứng hô hấp sau ghép nhưng có thể hồi phục nếu được nhận diện sớm và xử trí tích cực trong giai đoạn cấp. Đồng thời, về lâu dài, vẫn cần theo dõi tim mạch chủ động, đặc biệt bằng các dấu ấn sinh học khi có triệu chứng và EF/GLSS cả khi không có triệu chứng để dự phòng những tổn thương tồn dư, góp phần cải thiện tiên lượng người bệnh.
Tài liệu tham khảo
- Rehab Alblooshi, Solaf Kanfar, Bridgette Lord, et al. (2021), Clinical prevalence and outcome of cardiovascular events in the first 100 days postallogeneic hematopoietic stem cell transplant, European Journal of Haematology, số 106(1), tr. 32-39.
- Azin Alizadehasl, Nashmil Ghadimi, Hossein Hosseinifard, et al. (2023), Cardiovascular diseases in patients after hematopoietic stem cell transplantation: Systematic review and Meta-analysis, Current Research in Translational Medicine, số 71(1), tr. 103363.
- G. Gent David, Muhammad Saif, Rebecca Dobson, et al. (2024), Cardiovascular Disease After Hematopoietic Stem Cell Transplantation in Adults, JACC: CardioOncology, số 6(4), tr. 475-495.
- Salim S. Hayek, Vlad G. Zaha, Carmel Bogle, et al. (2024), Cardiovascular Management of Patients Undergoing Hematopoietic Stem Cell Transplantation: From Pretransplantation to Survivorship: A Scientific Statement From the American Heart Association, Circulation, số 149(16), tr. e1113-e1127.
- Dietger Niederwieser, Helen Baldomero, Nosa Bazuaye, et al. (2022), One and a half million hematopoietic stem cell transplants: continuous and differential improvement in worldwide access with the use of non-identical family donors, Haematologica, số 107(5), tr. 1045-1053.
- Amanda Isabel Pérez-Valencia, Enric Cascos, Sara Carbonell-Ordeig, et al. (2023), Incidence, risk factors, and impact of early cardiac toxicity after allogeneic hematopoietic cell transplant, Blood Advances, số 7(10), tr. 2018-2031.
- A. S. Polomski Elissa, A. von dem Borne Peter, Hendrik Veelken, et al. (2026), Prognostic Value of NT-proBNP in Patients Treated With Allogeneic Stem Cell Transplantation, JACC: Advances, số 5(1), tr. 102415.
- Jason Yeh, Laura Whited, Rima M. Saliba, et al. (2021), Cardiac toxicity after matched allogeneic hematopoietic cell transplant in the posttransplant cyclophosphamide era, Blood Advances, số 5(24), tr. 5599-5607.
- Ying Zhao, Rui He, Sandra Oerther, et al. (2022), Cardiovascular complications in hematopoietic stem cell transplanted patients, Journal of Personalized Medicine, số 12(11), tr. 1797.
- S. H. Armenian, D. Yang, J. B. Teh, et al. (2018), Prediction of cardiovascular disease among hematopoietic cell transplantation survivors, Blood Adv, số 2(14), tr. 1756-1764.
- V. Avula, G. Sharma, M. N. Kosiborod, et al. (2024), SGLT2 Inhibitor Use and Risk of Clinical Events in Patients With Cancer Therapy-Related Cardiac Dysfunction, JACC Heart Fail, số 12(1), tr. 67-78.







