Bệnh tim mạch (BTM) là nguyên nhân hàng đầu gây tử vong và tàn tật trên thế giới. Khoảng một triệu người tử vong hàng năm do BTM ở Hoa Kỳ[1]. Chi phí y tế cũng chiếm một khoảng không nhỏ, tiêu tốn cho chăm sóc trực tiếp
BS. Nguyễn Thanh Hiền
BS. Phạm Tú Quỳnh
BV nhân dân 115
Bệnh tim mạch (BTM) là nguyên nhân hàng đầu gây tử vong và tàn tật trên thế giới. Khoảng một triệu người tử vong hàng năm do BTM ở Hoa Kỳ[1]. Chi phí y tế cũng chiếm một khoảng không nhỏ, tiêu tốn cho chăm sóc trực tiếp và gián tiếp BTM ở liên minh châu Âu hàng năm ước khoảng 192 tỷ euro[2]. Nhiều nguyên nhân dẫn đến BTM. Trong đó, có những yếu tố nguy cơ (YTNC) không điều chỉnh được như tuổi, giới nam nhưng cũng có nhiều yếu tố có thể điều chỉnh được liên quan đến lối sống như hút thuốc lá, ít hoạt động thể lực, thói quen ăn uống hay liên quan đến các rối loạn khác như tăng huyết áp (THA), đái tháo đường (ĐTĐ), rối loạn lipid máu (RLLM). Việc điều trị sớm và tích cực các YTNC đóng vai trò quan trọng trong hạn chế tiến triển BTM. Nhiều nghiên cứu và thử nghiệm cho thấy vai trò quan trọng của điều trị RLLM trong dự phòng tiên phát và thứ phát BTM. Do đó, điều trị RLLM và cập nhật các hướng dẫn mới nhất về xử trí RLLM là phần không thể thiếu đối với bác sỹ chuyên khoa tim mạch nói riêng cũng như các bác sỹ tổng quát nói chung.
I. Phân tầng nguy cơ BTM
Đánh giá nguy cơ BTM là bước đầu tiên trong xử trí RLLM. Thái độ và mức độ xử trí RLLM tùy thuộc nhiều vào nguy cơ BTM của từng cá thể được đánh giá.
Hầu hết những hướng dẫn thực hành điều trị RLLM đều theo phân tầng nguy cơ dựa trên thang điểm SCORE hay Framingham. Thang điểm Framingham có dân số nghiên cứu ở vùng đông bắc Mỹ, còn thang điểm SCORE bắt nguồn từ dân số châu Âu. Thang điểm Framingham đánh giá nguy cơ bệnh động mạch vành (ĐMV) trong mười năm (không bao gồm tất cả các biến chứng của xơ vữa mạch máu như đột quỵ, thiếu máu não thoáng qua, khập khiễng cách hồi, và suy tim…). Trong khi đó, thang điểm SCORE đánh giá nguy cơ tử vong do biến cố xơ vữa mạch máu trong mười năm (chứ không chỉ là tử vong liên quan đến bệnh động mạch vành (ĐMV)); và ước lượng nguy cơ toàn bộ (tử vong và không tử vong) các biến cố nặng BTM. Nguy cơ toàn bộ biến cố nặng BTM được ước lượng bằng 3 lần nguy cơ tử vong do BTM. Do đó, thang điểm SCORE cho thấy được mức độ trầm trọng của BTM nhiều hơn thang điểm Framingham, cùng với thang điểm này đánh giá trên người châu Âu mà hội tim mạch châu Âu (European Society of Cardiology: ESC) và hội xơ vữa mạch máu châu Âu (European Atherosclerosis Society: EAS) đã đồng thuận chọn thang điểm SCORE là nền tảng cho hướng dẫn điều trị RLLM mới đây.
Hình 1. Bảng điểm SCORE: nguy cơ tử vong trong 10 năm do BTM
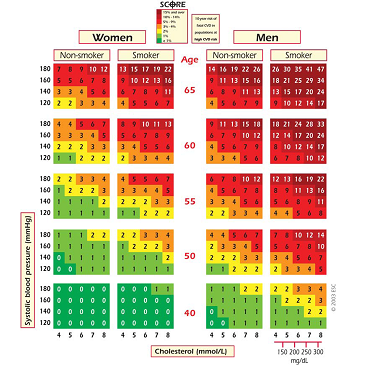
Nguy cơ toàn bộ (tử vong và không tử vong) các biến cố nặng BTM bằng 3 lần nguy cơ tử vong ở nam, bằng 4 lần với nữ. Thang điểm SCORE không dùng cho người BTM toàn phát, ĐTĐ, bệnh thận mãn, hay những YTNC nặng
Nguy cơ rất cao:
• Đã được chẩn đoán BTM
• ĐTĐ type 2, ĐTĐ type 1 có tổn thương cơ quan đích
• Bệnh thận mãn nặng (độ lọc cầu thận < 60mL/phút/1,73m2)
• Điểm SCORE ≥ 10% (tử vong 10 năm do BTM)
Nguy cơ cao:
• Những YTNC riêng lẻ nặng như RLLM gia đình và THA nặng
• Điểm SCORE ≥ 5% và <10% (tử vong 10 năm do BTM)
Nguy cơ trung bình
• Điểm SCORE ≥ 1% và <5% (tử vong 10 năm do BTM). Nguy cơ này cần được đánh giá thêm các yếu tố như tiền sử gia đình có BTM sớm, béo bụng, mức độ hoạt động thể lực, HDL-C, triglyceride, hs-CRP, Lp(a), fibrinogen, homocystein, apo B.
Nguy cơ thấp
• Điểm SCORE <1% (tử vong 10 năm do BTM)
II. Mục tiêu điều trị RLLM
RLLM có thể biểu hiện nhiều dạng. Tăng choleserol toàn phần và tăng LDL-C được quan tâm nhiều nhất do có nhiều bằng chứng mạnh và thuyết phục cho thấy giảm choleserol toàn phần và LDL-C có thể phòng ngừa BTM. Vì vậy, choleserol toàn phần và LDL-C tiếp tục là mục tiêu điều trị chính. Bên cạnh đó, do các bằng chứng thử nghiệm còn hạn chế về hiệu quả và độ an toàn can thiệp của các RLLM khác như tăng triglyceride, hạ HDL-C, tăng LDL nhỏ đậm đặc nên các RLLM này chỉ được xem như mục tiêu thứ cấp trong dự phòng BTM.
Mục tiêu điều trị RLLM tùy theo nguy cơ BTM của từng cá thể:
• Nguy cơ rất cao BTM, mục tiêu LDL-C<1,8 mmol/L (<70 mg/dL) và/hoặc giảm ≥ 50% LDL-C nếu không đạt được đích điều trị trên [ESC/EAS: IA]
• Nguy cơ BTM cao, mục tiêu LDL-C<2,5 mmol/L (<100 mg/dL) [ESC/EAS: IIa-A]
• Nguy cơ BTM trung bình, mục tiêu LDL-C<3 mmol/L (<115mg/dL) [ESC/EAS: IIa-A]
Những chú ý trong xét nghiệm LDL-C[3]
LDL-C thường được ước lượng từ công thức Friedewald:
• LDL-C = cholesterol toàn phần – VLDL-C – HDL-C
VLDL-C được ước lượng bằng 1/5 nồng độ triglyceride nên có thể có một số sai số liên quan đến tính LDL-C:
• Công thức chỉ có giá trị khi nồng độ triglyceride dưới 400mg/dL. Nếu triglyceride trên mức này, LDL-C cần được đo trực tiếp bằng phân tích siêu ly tâm hay kỹ thuật kết tủa miễn dịch.
• Ước lượng LDL-C bị ảnh hưởng bởi các sai số trong xét nghiệm cholesterol toàn phần, triglyceride và HDL-C. Vì cholesterol toàn phần, triglyceride bị ảnh hưởng đáng kể theo chế độ ăn nên theo quy ước chung hiện nay, các xét nghiệm lipid máu nên làm lúc đói (> 12 giờ không ăn).
• Ước tính VLDL-C bằng nồng độ triglyceride đã đánh giá thấp hơn thực tế lượng cholesterol cũng có khả năng sinh xơ vữa trong VLDL remnants hay còn gọi là IDL (intermediate density lipoprotein).
• LDL-C ước tính bao gồm cả các choleserol của các lipoprotein khác như lipoprotein(a) và lipoprotein-X. Lipoprotein(a) có thể liên quan đến nguy cơ BMV độc lập với LDL. Nhưng, lipoprotein-X là phần tử chứa cholesterol được tạo ra trong bệnh gan ứ mật, lại không liên quan đến BTM.
Số lượng phần tử LDL liên quan mạnh với BTM. Tuy nhiên, bằng kỹ thuật phân tích định lượng cholesterol trong LDL thì không thể xác định chính xác số các phần tử LDL. Các LDL kích thước nhỏ mang ít cholesterol hơn các LDL kích thước lớn. Cùng một lượng LDL-C, bệnh nhân có LDL nhỏ có nhiều hơn 70% số phần tử LDL so với người có kích thước LDL lớn.
Ở người có tình trạng đề kháng insulin (hội chứng chuyển hóa, ĐTĐ type 2) có sự không đồng bộ giữa LDL-C với nồng độ các phần tử LDL và apolipoprotein B. Đó là do đề kháng insulin gây ra tái cấu trúc LDL, các phần tử LDL bị tách bớt cholesterol và kích thước trở nên nhỏ hơn, dẫn đến tăng số lượng các phần tử LDL. Vì vậy, tăng đề kháng insulin hay tăng số lượng các YTNC chuyển hóa không làm tăng mức LDL-C đáng kể, nhưng làm tăng nhiều nồng độ phần tử LDL nhỏ và tăng tổng lượng phần tử LDL.
Gần 2/3 bệnh nhân ĐTĐ type 2 dù đang điều trị statin và có LDL-C dưới 100 mg/dL, vẫn còn có quá nhiều phần tử LDL. Tương tự, 41% bệnh nhân ĐTĐ type 2 dù đang điều trị statin và có LDL-C dưới 70 mg/dL cũng còn có quá nhiều phần tử LDL. Do đó, những trường hợp đề kháng insulin mà đã đạt mức LDL-C đích nên đo lường nồng độ các phần tử LDL hay thay thế bằng xét nghiệm apo B.
Những mục tiêu khác LDL-C
Apo B (Apolipoprotein B). Apo B là apolipoprotein chủ yếu của nhóm lipoprotein sinh xơ vữa (VLDL, IDL, LDL), nên nồng độ apoB là ước lượng chính xác các thành phần này trong máu, đặc biệt quan trọng khi số LDL nhỏ đậm đặc tăng cao. Đo lường apo B ít bị sai số hơn so với LDL-C, là xét nghiệm không cần phải nhịn đói và không bị ảnh hưởng khi triglyceride máu tăng cao. Điều bất lợi lớn của apo B là chưa được tính toán trong các bảng phân tầng nguy cơ, chưa được đặt làm tiêu chí chính trong các thử nghiệm lâm sàng, và cũng chưa làm được tại nhiều cơ sở y tế. Vì vậy, apo B vẫn còn được xem là mục tiêu điều trị thứ cấp. Mục tiêu điều trị apo B là < 80mg/dL với đối tượng nguy cơ rất cao, và <100 mg/dL với người nguy cơ cao.
non HDL-C: non HDL-C được dùng để đánh giá toàn bộ các phần tử sinh xơ vữa trong máu (VLDL, IDL, LDL) và liên quan tốt với mức apoB. Non HDL-C được tính bằng cholesterol trừ HDL-C. Mục tiêu non HDL-C nên cao hơn 0,8 mmol/L (30 mg/dL) với mức mục tiêu LDL-C tương ứng với từng cá thể.
HDL-C: mặc dù tăng HDL-C tiên đoán giảm mảng xơ vữa và hạ HDL-C có liên quan đến gia tăng biến cố và tử vong ở bệnh nhân bệnh ĐMV. Tuy nhiên, do còn thiếu các bằng chứng thuyết phục về hiệu quả can thiệp loại RLLM này trên nguy cơ BTM, nên HDL-C vẫn còn được xem là mục tiêu điều trị thứ cấp
Triglyceride. Tăng triglyceride máu thường liên quan đến hạ HDL-C và tăng LDL nhỏ đậm đặc. Vì vậy, ảnh hưởng của tăng triglyceride máu trên BTM có thể do tình trạng hạ HDL-C và tăng LDL nhỏ đậm đặc. Do còn thiếu các bằng chứng thuyết phục nên hiện nay, triglyceride chưa được xem là YTNC BTM.
Hs-CRP do còn thiếu bằng chứng nên hs-CRP vẫn còn được xem là mục tiêu điều trị thứ cấp
III. Các phương pháp điều chỉnh RLLM
Xử trí RLLM bao gồm điều trị thay đổi lối sống và dùng thuốc. Tùy theo mức độ RLLM và nguy cơ BTM mà chỉ sử dụng phương pháp thay đổi lối sống hoặc kết hợp cả thay đổi lối sống và dùng thuốc. Khi quyết định dùng thuốc, tương tự cũng tùy mức độ RLLM và nguy cơ BTM mà trì hoãn dùng thuốc hay sử dụng thuốc ngay lập tức.
Bảng 1. Can thiệp lipid máu dựa vào nguy cơ BTM toàn bộ và lượng LDL-C máu[2]
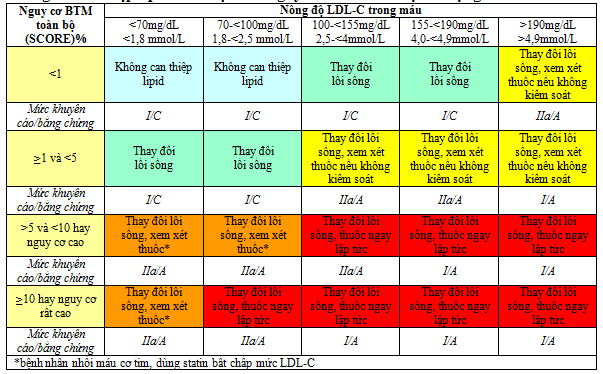
III.1. Thay đổi lối sống
Cân nặng và hoạt động thể lực
Quá cân khi BMI ≥25 kg/m2 và <30 kg/m2; béo phì khi BMI ≥30kg/m2. Béo bụng với người châu Á khi vòng eo ở nam ≥ 90 cm, ở nữ ≥ 80 cm. Quá cân, béo phì, béo bụng góp phần gây RLLM. Do đó, giảm cân làm cải thiện lipid máu, hơn nữa còn tác động có lợi lên các YTNC BTM khác thường đi kèm trên các bệnh nhân này. Cần khuyên bệnh nhân giảm thức ăn giàu năng lượng cũng như tăng tiêu thụ năng lượng bằng tăng vận động thể lực để tổng năng lượng mỗi ngày âm 300-500 kcal. Nên hoạt động thể lực đều đặn ít nhất 30 phút mỗi ngày.
Chế độ ăn
Lượng lipid ăn vào[2]
Tổng lượng lipid ăn vào nên khoảng 25-35% calo thu nhập. Khi lượng lipid >35% calo thu nhập thường liên quan đến tăng acid béo bão hòa và tăng calo thu nhập. Ngược lại, nếu lượng lipid quá thấp có nguy cơ làm giảm hấp thu vitamin E và các acid béo thiết yếu, góp phần làm thay đổi bất lợi trên HDL.
Cơ thể người hấp thu lipid chủ yếu dưới dạng các acid béo tự do, và một phần nhỏ hơn là cholesterol. Nhiều nghiên cứu cho thấy loại lipid ăn vào đóng vai trò quan trọng không kém tổng lượng lipid thu nhập (bảng 2).
• Lượng mỡ ăn vào nên chứa nhiều acid béo không bão hòa đơn và cả acid béo không bão hòa đa n-3, n-6 (omega-3, omega-6).
• Dầu cá và acid béo không bão hòa đa n-3 có nguồn gốc thực vật có thể giảm nguy cơ tử vong tim mạch và đột quỵ nhưng không ảnh hưởng đáng kể lên chuyển hóa lipoprotein máu.
• Lượng acid béo không bão hòa đa n-6 nên < 10% calo thu nhập.
• Lượng acid béo bão hòa nên < 10% calo thu nhập. Nếu có tăng cholesterol máu, lượng acid béo bão hòa tối ưu nên < 7% calo thu nhập.
• Lượng acid béo chuyển hóa <1% calo thu nhập.
• Lượng cholesterol trong chế độ ăn lý tưởng nên < 300mg/ngày.
Bảng 2. Loại lipid và ảnh hưởng lên chuyển hóa, tim mạch[4]
|
Loại lipid |
Ảnh hưởng lên chuyển hóa |
Ảnh hưởng lên tim mạch |
|
Acid béo bão hòa (SFA: saturated fatty acids) |
-Tăng HDL-C và LDL-C -Có thể thúc đẩy tạo huyết khối |
-Tăng tỷ lệ bệnh ĐMV -Có thể tăng nguy cơ ung thư tiền liệt tuyến, đại tràng |
|
Acid béo không bão hòa đơn (MUFA: monounsaturated fatty acids) |
-Giảm LDL-C nhẹ -Tăng HDL-C -Có thể cản trở quá trình oxy hóa |
-Có thể giảm thấp bệnh ĐMV |
|
Acid béo không bão hòa đa n-3 (PUFA: polyunsaturated fatty acids) |
-Có thể giảm tạo huyết khối -Quan trọng trong phát triển võng mạc và não |
-Tăng tỷ lệ n-3/n-6 có thể giảm tỷ lệ bệnh ĐMV -n-3 có thể tăng trọng lượng sinh -Có thể ngừa đột tử tim |
|
Acid béo không bão hòa đa n-6 (PUFA: polyunsaturated fatty acids) |
-Acid arachidonic, chất quan trọng trong viêm |
-Có thể giảm bệnh ĐMV -Lượng nhiều có thể sinh ung thư |
|
Acid béo chuyển hóa (trans fatty acids) , chủ yếu từ hydrogen hóa PUFA trong công nghiệp thực phẩm |
-Tăng LDL-C -Giảm HDL-C -Tăng Lp(a) -Cản trở chuyển hóa PUFA |
-Tăng tỷ lệ bệnh ĐMV |
Carbonhydrate trong chế độ ăn
Lượng carbonhydrate nên chiếm khoảng 45-55% calo thu nhập. Khuyến khích ăn nhiều rau, trái cây, hạt, và ngũ cốc nguyên hạt.
Lượng đường cần giảm < 10%. Hạn chế các loại nước ngọt. Cần tiết chế chặt chẽ hơn với bệnh nhân có tăng cân hay tăng triglyceride máu.
Rượu
Lượng rượu tối đa mỗi ngày mà không làm tăng triglyceride là 20-30g với nam, và 10-20g ở nữ. Đối với người tăng triglyceride, khuyến cáo bỏ rượu.
Thực phẩm chức năng
Phytosterol là một hoạt chất thuộc nhóm sterol có nguồn gốc thực vật, khác với cholesterol là sterol có nguồn gốc động vật. Phytosterol cạnh tranh hấp thu với cholesterol ở ruột non giúp làm giảm cholesterol máu (bảng 3). Phytosterol liều 2g/ngày giảm cholesterol toàn phần và LDL-C khoảng 7-10%. Chưa có bằng chứng rõ ràng về hiệu quả dự phòng BTM của loại thực phẩm chức năng này. Những thực phẩm được làm giàu phytospherols (1-2 g/ngày) có thể được xem xét ở những người tăng cholesterol và LDL-C máu nhưng chưa đến mức phải dùng thuốc hạ cholesterol máu[5].
Protein đậu nành làm giảm LDL-C vừa phải (3-5%). Nên dùng các thực phẩm đậu nành thay thế các thức ăn có nguồn gốc động vật vốn có nhiều acid béo bão hòa.
Chất xơ. Những thực phẩm nhiều chất xơ hòa tan thường được dung nạp tốt, có hiệu quả giảm LDL-C. Liều khuyến cáo 5-15 g chất xơ hòa tan mỗi ngày. Để điều trị tốt mỡ máu, chế độ ăn cần 25-40g chất xơ, tối thiểu 7-13 g chất xơ hòa tan.
Acid béo không bão hòa đa n-3 (omega 3). Dầu cá (nhiều acid béo n-3 chuỗi dài) với lượng 2-3 gram mỗi ngày có thể giảm triglyceride 25-30% ở người lipid máu bình thường cũng như người có RLLM.
Red yeast rice (gạo men đỏ). Red Yeast Rice là sản phẩm lên men màu đỏ của gạo nếp nấu chín. Thực phẩm này thường được dùng để tạo màu và hương vị cho món ăn của người Trung Quốc. Cơ chế có thể giống với statin (ức chế HMG-CoA reductase), giúp làm giảm cholesterol toàn phần và LDL-C.
Chế độ ăn góp phần ngăn ngừa BTM
Nên ăn nhiều và đa dạng loại trái cây, rau quả để có nhiều và đa dạng chất chống oxy hóa. Tối thiểu 2-3 bữa cá mỗi tuần để ngừa BTM, nên ăn những thực phẩm có nhiều acid béo không bão hòa đa n-3. Nên ăn < 5 g muối mỗi ngày.
Thuốc lá
Ngưng hút thuốc lá có lợi rõ ràng trên nguy cơ tử vong toàn bộ BTM, ảnh hưởng đặc biệt làm tăng HDL-C.
Bảng 3. Ảnh hưởng của thay đổi lối sống lên mức lipid[2]
|
|
Mức độ ảnh hưởng |
Mức độ bằng chứng |
|
Thay đổi lối sống làm giảm cholesterol và LDL-C |
||
|
Giảm acid béo bão hoà |
+++ |
A |
|
Giảm acid béo chuyển hóa |
+++ |
A |
|
Tăng chất xơ |
++ |
A |
|
Giảm lượng cholesterol |
++ |
B |
|
Thực phẩm chức năng giàu phytosterol |
+++ |
A |
|
Giảm quá cân |
+ |
B |
|
Sản phẩm từ đậu nành |
+ |
B |
|
Tăng thói quen vận động |
+ |
A |
|
Bổ sung red yeast rice |
+ |
B |
|
Thay đổi lối sống làm giảm triglyceride |
||
|
Giảm quá cân |
+++ |
A |
|
Giảm rượu |
+++ |
A |
|
Giảm mono và disaccharides |
+++ |
A |
|
Tăng thói quen vận động |
++ |
A |
|
Giảm carbonhydrate |
++ |
A |
|
Acid béo không bão hoà đa n-3 |
++ |
A |
|
Thay acid béo bão hoà bằng acid béo không bão hoà |
+ |
B |
|
Thay đổi lối sống làm tăng HDL-C |
||
|
Giảm acid béo chuyển hóa |
+++ |
A |
|
Tăng thói quen vận động |
+++ |
A |
|
Giảm quá cân |
++ |
A |
|
Giảm carbonhydrate và thay bằng acid béo không bão hoà |
++ |
A |
|
Rượu vừa phải |
++ |
B |
|
Thực phẩm chứa carbonhydrate với chỉ số đường thấp và nhiều chất xơ |
+ |
C |
|
Bỏ thuốc lá |
+ |
B |
|
Giảm mono và disaccharides |
+ |
C |
III.2. Thuốc hạ lipid máu
III.2.1. Statin
Cơ chế tác dụng[6]:
• Statin ức chế cạnh tranh với HMG-CoA reductase, ngăn chặn con đường tổng hợp cholesterol trong tế bào. Sự giảm sản xuất cholesterol trong tế bào dẫn đến hoạt hóa protein gắn yếu tố điều hòa sterol – một yếu tố sao chép, đặc biệt tại tế bào gan – làm tăng sản xuất thụ thể LDL và do đó tăng loại trừ LDL khỏi máu.
• Statin tác động làm giảm tiết apoB ở gan kèm với tăng receptor apoB/E ở gan, giảm hồi phục hoạt động của men HMG-CoA reductase nên làm giảm tổng hợp VLDL và triglyceride.
Tác dụng trên lipid máu[7]:
• Giảm LDL-C: 20-60%
• Giảm triglyceride: 10-33%.
• Tăng HDL-C: 5 – 10%.
Thử nghiệm lâm sàng:
Statin là thuốc được nghiên cứu nhiều nhất trong dự phòng BTM. Nhiều thử nghiệm lâm sàng chứng minh statin làm giảm tỷ lệ tử vong do BTM trong cả dự phòng tiên phát và thứ phát[8-10]. Statin cũng cho thấy làm chậm tiến triển, ngay cả thúc đẩy thoái triển mảng xơ vữa mạch vành[2].
Phân tích gộp
Trong phân tích gộp CTT (cholesterol treatment trialist’ collaboration) trên 170 000 người trong 26 thử nghiệm ngẫu nhiên statin, giảm 10% tử vong do mọi nguyên nhân và 20% tử vong do bệnh ĐMV mỗi 1 mmol/L (~ 40mg/dL) LDL-C được giảm[8]. Nguy cơ biến cố ĐMV giảm 23% và nguy cơ đột quỵ 17% mỗi 1 mmol/L (~40mg/dL) LDL-C được giảm. Tỷ lệ giảm biến cố BTM tương tự các nhóm khi phân tích dưới nhóm. Lợi ích đạt được quan trọng trong năm đầu tiên, nhưng còn lớn hơn trong những năm tiếp theo. Không có tăng nguy cơ tử vong do nguyên nhân khác ngoài tim(kể cả ung thư). Nguy cơ hủy cơ vân với statin nhỏ và không có ý nghĩa[8]. Đối với người nguy cơ BTM thấp, cân nhắc dùng statin để dự phòng tiên phát do hiệu quả-chi phí không có lợi và ảnh hưởng đến chất lượng cuộc sống[11].
Các loại statin khác nhau có mức tác động làm giảm LDL-C khác nhau (biểu đồ 1). Lợi ích lâm sàng từng loại statin chủ yếu dựa vào mức độ hạ LDL-C. Vì vậy, cần chọn loại statin và liều dùng statin để đạt mức LDL-C mục tiêu.







