Tóm tắt
Đây là nghiên cứu ngẫu nhiên, mù đôi, có kiểm soát trong 8 tuần so sánh hiệu quả và mức độ dung nạp của thuốc viên phối hợp (chỉ 1 viên duy nhất) Telmisartan/Amlodipin (T/A) so với cách thức đơn trị liệu một
Joel M. Neutel, MD;1 Giusepe Mancia, MD;2 Henry R. Black, MD;3 Bjorn Dahlo¨ f, MD;4 Holly Defeo
RN;5 Ludwin Ley, MD;6 Richard Vinisko, MS;5 and on behalf of the TEAMSTA Severe HTN Study Investigators*
Người dịch: Nguyễn Thị Phương Hồng
Khoa Phòng khám theo yêu cầu
Bệnh viện Nhân dân 115
Tóm tắt
Đây là nghiên cứu ngẫu nhiên, mù đôi, có kiểm soát trong 8 tuần so sánh hiệu quả và mức độ dung nạp của thuốc viên phối hợp (chỉ 1 viên duy nhất) Telmisartan/Amlodipin (T/A) so với cách thức đơn trị liệu một trong hai thuốc Telmisartan và Amlodipin ở 858 bệnh nhân bị tăng huyết áp nặng (huyết áp tâm thu/ huyết áp tâm trương >= 180/95 mmHg). Ở tuần thứ 8, T/A cho thấy hiệu quả hạ huyết áp tốt hơn có ý nghĩa thống kê khi so sánh với đơn trị liệu Telmisartan (P< 0.0001) hoặc Amlodipin (P< 0.0002) cho những bệnh nhân đo huyết áp ở tay trong tư thế ngồi với mức độ hạ huyết áp so với ban đầu là 47.5mm Hg huyết áp tâm thu và 18.7mm Hg huyết áp tâm trương. Khả năng hạ huyết áp tốt hơn này xuất hiện rõ ràng ngay cả ở tuần đầu tiên, tuần thứ 2, 4 và 6. Tỷ lệ đạt huyết áp mục tiêu và tỷ lệ đáp ứng điều trị của T/A cũng cao hơn 1 cách nhất quán khi so với đơn trị liệu Telmisartan hoặc Amlodipin. T/A cũng cho thấy mức độ dung nạp tốt với ít tác dụng phụ hơn khi so sánh với Amlodipin (12.6% ít hơn so với 16.4%) và số ca phù ngoại vi cũng như bỏ thuốc của T/A cũng thấp hơn.
Kết luận, điều trị bằng viên phối hợp T/A cho bệnh nhân bị tăng huyết áp mức độ nặng mang lại hiệu quả hạ huyết áp tốt hơn, đạt huyết áp mục tiêu nhiều hơn, tỷ lệ đáp ứng điều trị cao hơn cũng như dung nạp tốt hơn khi so sánh với đơn trị liệu hoặc Telmisartan hoặc Amlodipin.
Mở đầu
Dựa theo những bằng chứng của một số lượng lớn các nghiên cứu thử nghiệm về việc điều trị tăng huyết áp, hầu hết các Hướng dẫn (Guidelines) đều cho thấy để thành công trong việc đạt được huyết áp mục tiêu thì việc phối hợp thuốc điều trị tăng huyết áp là điều cần thiết ở phần lớn các bệnh nhân. Chỉ một số ít bệnh nhân đạt được huyết áp mục tiêu với một thuốc duy nhất. Hơn nữa, nghiên cứu ACCOMPLISH cho thấy rằng có 1 sự giảm có ý nghĩa thống kê các biến cố tim mạch và tỷ lệ tử vong khi dùng phối hợp thuốc Ức chế men chuyển và Chẹn kênh Canxi để điều trị bệnh nhân bị tăng huyết áp kèm nguy cơ tim mạch. Dù đã có nhiều Hướng dẫn dể hiểu và chi tiết, cũng như xu hướng phối hợp thuốc đã nhiều lên trong thực tế, tuy nhiên cũng có vài nghiên cứu cho thấy vẫn còn tồn tại một tỷ lệ những bệnh nhân không đạt được huyết áp mục tiêu. Kiểm soát huyết áp kém làm nặng nề thêm các yếu tố nguy cơ tim mạch hay gặp ở những bệnh nhân bị tăng huyết áp, ví dụ như tăng cholesteron máu, béo phì, đái tháo đường type 2, hút thuốc lá… Chính vì thế nhu cầu cấp thiết là cải thiện việc điều trị tăng huyết áp. Phối hợp 2 thuốc ở 2 nhóm khác nhau, có cơ chế tác động bổ sung lẫn nhau là 1 cách tiếp cận hợp lý. Việc phối hợp như vậy làm giảm huyết áp nhiều hơn, làm tăng tỷ lệ đạt được huyết áp mục tiêu so với đơn trị liệu. Hơn nữa, một số nghiên cứu còn cho chúng ta thấy thuốc viên phối hợp mang lại sự gia tăng tỉ lệ tuân thủ điều trị đồng thời làm giảm chi phí điều trị.
Phối hợp 2 thuốc Chẹn kênh Canxi và Ức thế thụ thể Angiotensin II là 1 phối hợp hợp lý, và ngày càng có nhiều bằng chứng cho thấy các phối hợp này có hiệu quả. Mục tiêu nghiên cứu hiện tại là so sánh tính hiệu quả và mức độ dung nạp của thuốc viên phối hợp gồm 80mg Telmisartan/10mg Amlodipin (T80/A10) so với đơn trị liệu hoặc Telmisartan 80mg hoặc Amlodipin 10mg cho những bệnh nhân bị tăng huyết áp mức độ nặng (HA >= 180/95 mm Hg)
PHƯƠNG PHÁP NGHIÊN CỨU
Thiết kế nghiên cứu
Đây là nghiên cứu ngẫu nhiên, mù đôi, có nhóm chứng, tiêu chuẩn chặt chẽ, đa trung tâm, đa quốc gia trong việc so sánh tính hiệu quả và mức độ dung nạp của thuốc viên phối hợp gồm 80mg Telmisartan/ 10mg Amlodipin (T80/A10) so với đơn trị liệu hoặc Telmisartan 80mg, hoặc Amlodipin 10mg cho những bệnh nhân bị tăng huyết áp mức độ nặng (HA >= 180/95 mmHg). Bệnh nhân được tuyển chọn từ 114 trung tâm ở 11 quốc gia (Bulgaria, cộng hòa Séc, Pháp, Hungary, Rumania, Nga, Slovakia, Hàn quốc, Tây Ban Nha, Ukraina, và Mỹ) trong khoảng thời gian từ tháng 3 năm 2009 đến tháng 12 năm 2009. Thử nghiệm này được kiểm soát/ quản lý phù hợp với Công ước Helsinki (1996) và Hướng dẫn cách hòa hợp 3 bên trong thực hành lâm sàng (ICH Harmonized Tripartite Guideline for Good Clinical Practice), nghiên cứu này cũng được Ban nghành có thẩm quyền Y tế hoặc Ủy ban về đạo đức trung lập của mỗi nước tham gia nghiên cứu chấp thuận.
Các bệnh nhân đều được cung cấp thông tin và ghi cam kết đồng ý trước khi tham gia nghiên cứu này (phù hợp với Hướng dẫn thực hành lâm sàng tốt và Pháp luật địa phương).
Sau khi tầm soát và cho uống thử giả dược trong 1-14 ngày theo cách thức mù đơn thì các bệnh nhân thích hợp được xếp ngẫu nhiên thành 3 nhóm tùy theo cách thức điều trị (tỷ lệ 2:1:1): dùng viên phối hợp T80/A10 hoặc đơn trị liệu T80, hoặc A10. Tất cả bệnh nhân trong nhóm T/A và A đều được nhận liều thấp 5mg Amlodipin trong 2 tuần đầu, sau đó các bệnh nhân này được dùng thuốc tăng liều lên đến liều mục tiêu Telmisartan 80mg/ Amlodipin 10mg hoặc Amlodipin 10mg trong vòng 6 tuần còn lại; nhóm bệnh nhân Telmisartan 80mg cũng bắt đầu và vẫn theo cách điều trị tương tự nhóm kia trong toàn bộ 8 tuần. Người bệnh uống thuốc thử nghiệm vào buổi sáng, giờ tương tự nhau, ngày 1 lần duy nhất. Trong nghiên cứu này, bệnh nhân không dùng các thuốc hạ áp khác hoặc các thuốc điều trị các bệnh đi kèm mà có ảnh hưởng đến huyết áp.
Người bệnh
Bệnh nhân nam hoặc nữ tuổi từ 18 trở lên có huyết áp đo ở tay trong tư thế ngồi từ 180 mmHg và 95 mmHg trở lên, những bệnh nhân này có thể ngưng thuốc hạ áp đang dùng mà không gây ra nguy cơ nào đáng kể (theo sự suy xét/ tiên lượng của người nghiên cứu) thì được chọn lựa 1 cách ngẫu nhiên.
Các bệnh nhân có 1 trong các tiêu chuẩn sau sẽ không được chọn vào nghiên cứu :
– Nghi ngờ hay đã biết các trường hợp tăng huyết áp mà HA tâm thu trung bình từ 200 mmHg trở lên và/ hoặc HA tâm trương trung bình từ 120 mmHg trở lên.
– Suy tim sung huyết (theo phân loại suy tim NYHA nhóm 3, 4)
– Rối loạn nhịp tim thấy rõ trên lâm sàng, như nhịp nhanh thất; rung nhĩ, nhịp flutter nhĩ
– Bệnh lý gan nặng, như suy gan, ứ mật hoặc tắc nghẽn đường mật mức độ vừa-nặng.
– Bệnh lý thận mức độ nặng, như Creatinin huyết thanh > 3mg% (> 265 uMol/L), độ thanh thải Creatinin < 30ml/phút, hoặc có dấu hiệu lâm sàng suy thận nặng.
– Bệnh Đái tháo đường không ổn định hoặc không kiểm soát tốt (HbA1c >= 10% trong vòng 3 tháng trước thời điểm nghiên cứu)
– Các nhóm bệnh nhân khác được cho là không an toàn cho phác đồ điều trị gồm : đang mang thai, đang cho con bú, người tiền mãn kinh, người chuẩn bị/ sắp mang thai nhưng không có được các biện pháp kiểm soát thai kỳ/ thai sản tốt.
– Tiền căn bị phù mạch khi dùng thuốc Ức chế men chuyển hay Ức chế thụ thể.
– Nhóm bệnh nhân có chống chỉ định dùng giả dược trong giai đoạn thử: đột quỵ trong vòng 6 tháng, nhồi máu cơ tim, đã phẫu thuật tim, đặt stent mạch vành qua da, đau thắt ngực không ổn định, hoặc phẫu thuật đặt mảnh ghép mạch vành trong vòng 3 tháng trước.
– Tiền sử nghiện ma túy, nghiện rượu trong vòng 6 tháng trước nghiên cứu này.
– Tiền căn đã có sự bỏ điều trị hoặc không thể hợp tác với phác đồ điều trị.
Đánh giá kết quả
Huyết áp được đo vào các thời điểm sau: ngay cuối giai đoạn dùng giả dược, tức là trước khi phân loại ngẫu nhiên (HA ban đầu để so sánh sau này); sau 1, 2, 4, 6, 8 tuần trong giai đoạn điều trị mù đôi (ở 24 giờ sau liều thuốc cuối cùng).
Công việc đo huyết áp được thực hiện giống nhau cho tất cả bệnh nhân, bao gồm:
– Đo huyết áp ở tay, tư thế ngồi
– Dụng cụ đo tiêu chuẩn, có 1 túi khí được bọc vải
– Cùng 1 mã hiệu và cùng do 1 công ty sản xuất (mã số UA-787EJ, công ty Y khoa A&D, Canton, GA)
– Đo huyết áp 3 lần liên tiếp, cách nhau 2 phút kèm bắt mạch liên tục trong 2 phút giữa lần đo huyết áp thứ 2 và 3.
Mục tiêu ban đầu là có sự thay đổi huyết áp tâm thu trung bình so với ban đầu sau 8 tuần điều trị. Mục tiêu thứ hai mấu chốt đó là thay đổi huyết áp tâm thu trung bình so với ban đầu sau 1, 2, 4 và 6 tuần dùng thuốc. Các mục tiêu thứ hai khác sau 1, 2, 4, 6, 8 tuần điều trị bao gồm:
– Huyết áp tâm thu dưới 140 mmHg, hoặc < 130 mmHg; hay huyết áp tâm trương < 90 mmHg hoặc < 80 mmHg;
– Đạt huyết áp mục tiêu, huyết áp tâm thu < 140 mmHg và huyết áp tâm trương < 90 mmHg
Các phần phụ khác: Phân nhóm nhỏ cho các bệnh nhân theo huyết áp tâm thu ban đầu theo mỗi 10 mmHg (nhóm từ 180 mmHg đến dưới 190 mmHg, và nhóm dưới 190 mmHg), phân nhóm nhỏ theo tuổi, có Đái tháo đường type 2, chỉ số khối cơ thể BMI, chủng tộc, bệnh chuyển hóa kèm theo (như Đái tháo đường type 2, BMI lớn hơn 30kg/m2)
Việc ghi nhận tất cả các phản ứng phụ của thuốc, qua việc bệnh nhân kể lại cũng như thăm khám đều được ghi lại trong suốt quá trình nghiên cứu (từ lúc bắt đầu tầm soát đến lúc kết thúc nghiên cứu). Những tác dụng phụ được phân loại theo sách Từ điển Y khoa cho các hoạt động thông thường (MedDRA) phiên bản 12.1. Khi bắt đầu nghiên cứu, người bệnh được thăm khám lâm sàng cẩn thận và ghi nhận các chỉ số sinh tồn. Các xét nghiệm lúc tầm soát, lúc phân loại ngẫu nhiên và lúc kết thúc nghiên cứu cũng được thực hiện cho bệnh nhân. Đo điện tâm đồ vào thời điểm tầm soát và khi kết thúc.
PHÂN TÍCH THỐNG KÊ
Việc đo đi đo lại huyết áp nhiều lần một cách cẩn thận ở mức độ tối đa có thể để tìm ra khác biệt so với huyết áp ban đầu tại thời điểm sau uống thuốc. Mô hình bao gồm đánh giá tính hiệu quả điều trị cụ thể, rõ ràng, việc thăm khám, yếu tố tương tác, các thay đổi liên tục về huyết áp cơ bản.
Có 2 cách tính:
– Sử dụng huyết áp đo ban đầu và tất cả số đo huyết áp có sẵn sau đó làm chuẩn tham chiếu so sánh với huyết áp tuần 4, 6, 8.
– Sử dụng huyết áp đo ban đầu và huyết áp đo ở tuần 1 và 2 sau uống thuốc làm tham chiếu.
Phân tích theo nhóm nhỏ cũng được thực hiện theo cách này, phân tích tương tác trong nhóm.
Tỷ lệ đáp ứng kiểm soát huyết áp tâm thu, tâm trương được đánh giá theo phương pháp Hồi quy logistic.
Dùng phép tính toán mức độ mạnh dựa theo độ lệch chuẩn 15 mmHg cho huyết áp tâm thu cho thấy rằng có kích cỡ mẫu phải đạt 720 bệnh nhân được đánh giá mới có sức mạnh 95% để có thể phát hiện ra sự khác biệt sai lệch 5mmHg giữa các nhóm trị liệu với mức ý nghĩa thống kê sai số 0.05.
Phân tích tính hiệu quả ban đầu và hiệu quả thứ hai dựa trên toàn bộ dữ liệu có sẵn, bao gồm tất cả bệnh nhân đã được phân loại ngẫu nhiên dùng bất cứ liều thuốc nào trong các thuốc thử nghiệm mù đôi có dữ liệu đo đạc huyết áp cơ bản lúc ban đầu và số liệu đo đạc sau khi uống thuốc.
Đánh giá mức độ an toàn cho toàn bộ bệnh nhân dùng thuốc trong giai đoạn phân loại ngẫu nhiên
KẾT QUẢ
Sự phân bố và các thông số cơ bản của bệnh nhân
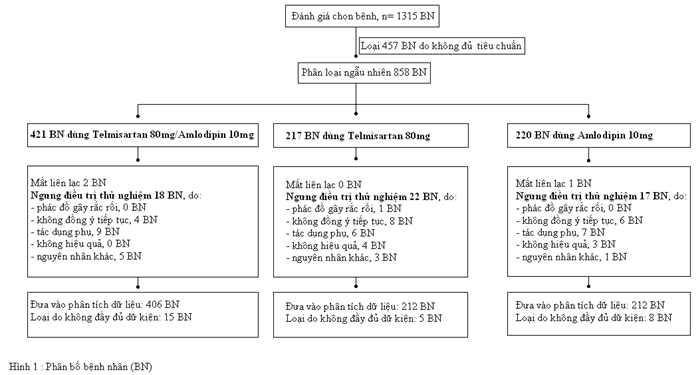
Mức độ giảm huyết áp
Sau 8 tuần, nhóm dùng viên phối hợp T80/A10 có mức giảm huyết áp rất tốt, giảm trung bình 47.5 mmHg +/- 13.4 mmHg (từ 185.4 +/- 4.6 mmHg xuống còn 137.9 mmHg +/- 12.8 mm Hg). Trong khi nhóm dùng Telmisartan 80mg chỉ giảm trung bình 36.9 mmHg +/- 13.1 mmHg (từ 185.6 +/- 4.5 mmHg xuống còn 149.6 +/- 18.1 mmHg) hoặc nhóm dùng Amlodipin 10mg chỉ giảm 43.2 +/- 9.1 mmHg (từ 185.1 +/- 4.5 mmHg xuống còn 141.9 +/- 12.9 mmHg) ( hình 2a và 2c). Như vậy, sau 8 tuần, nhóm dùng T80/A10 có huyết áp trung bình giảm hơn nhóm T80 là 10.6 mmHg. Mức giảm này có ý nghĩ về mặt thống kê với P < 0.0001, khoảng tin cậy 95%. Mức giảm huyết áp trung bình này là 4.4 mmHg có ý nghĩa về mặt thống kê (P=0.0002) tương tự khi so sánh nhóm T80/A10 với nhóm A10.
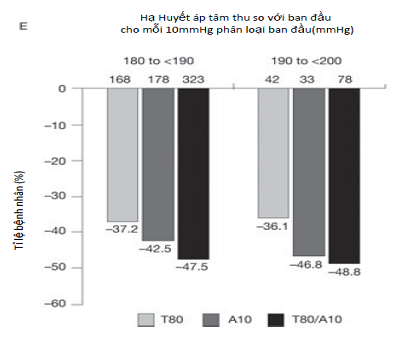
Nhóm dùng T80/A10 có mức giảm huyết áp duy trì liên tục mà không liên quan đến kiểu tăng huyết áp ban đầu là loại nào (hình 3). Trong đó, nhóm huyết áp 180 mmHg- <185 mmHg giảm 47 mmHg, nhóm 185- <190 mmHg giảm 48.3 mmHg, nhóm 190- < 195 mmHg giảm 48.7 mmHg, và nhóm 195- < 200mHg giảm 48.9 mmHg.
Ở tất cả các thời điểm đo huyết áp thì nhóm dùng T80/A10 đều có mức giảm huyết áp thấp hơn có ý nghĩa khi so sánh với các nhóm đơn trị liệu (P< 0.0001, khi so với nhóm T80; P <= 0.0077 khi so với nhóm A10)- hình 2a và 2c.. Sự giảm nhiều có ý nghĩa như vậy ở nhóm dùng viên phối hợp đã thấy rõ sau 1 tuần điều trị khi so với nhóm đơn trị liệu; mức giảm thêm này là 6.4 mmHg khi so với nhóm T80 với P< 0.0001; mức giảm thêm này là 3.3 mmHg khi so với nhóm A10 với P=0.0077. Sự giảm huyết áp ở nhóm dùng viên phối hợp nhiều hơn 2 nhóm kia vẫn tiếp tục duy trì trong suốt quá trình nghiên cứu.
Với nhóm dùng viên phối hợp, mức độ giảm trung bình của Huyết áp so với ban đầu ở tuần lễ 1, 2, 4 và 6 lần lượt là 31.9 mmHg, 38 mmHg, 44.6 mmHg, và 47 mmHg. Cũng ở nhóm này, mức độ giảm thêm huyết áp là 31.9, 37.9, 44.5, và 46.9 mmHg lần lượt tại các thời điểm tuần lễ 1, 2, 4 và 6. Hơn thế nữa, 80% mức giảm huyết áp tối đa (mức giảm 37.9 +/- 14.1 mmHg) đạt được chỉ sau 2 tuần điều trị. Mức giảm thêm huyết áp tâm thu là 7.8 mmHg khi so với nhóm Telmisartan 80mg với P<0.0001, mức giảm thêm này là 4.6 mmHg khi so với nhóm dùng Amlodipin 5mg, với P=0.0001.
Nhóm dùng thuốc viên phối hợp T80/A10 có mức giảm huyết áp trung bình nhiều hơn nhóm dùng T80 là hơn 10 mmHg. Mức giảm trung bình hơn 10.2, 10.6, và 10.6 mmHg lần lượt ở tuần thứ 4, 6 và 8, với P < 0.0001. Mức độ giảm huyết áp của nhóm thuốc viên phối hợp cũng nhiều hơn nhóm A10 gần 5 mmHg (giảm 4.8, 4.8 và 4.4 mmHg ở tuần 4, 6 và 8 với P=0.0001 và P=0.0002).
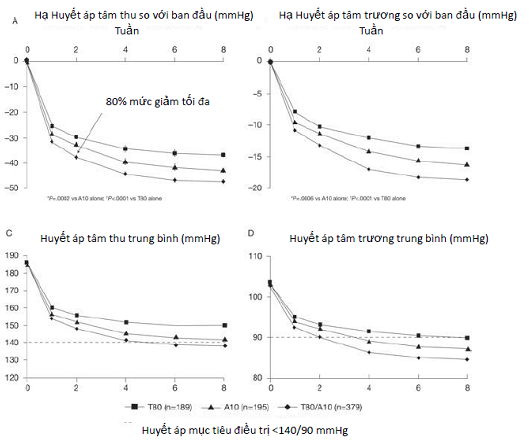
Hình 2 : Mức độ giảm huyết áp trung bình (+/- độ lệch chuẩn) so với ban đầu, huyết áp đo ở tay tư thế ngồi; bảng A, C: mức độ giảm huyết áp tâm thu; B,D: mức độ giảm huyết áp tâm trương; lưu ý một vài sai biệt lệch chuẩn quá nhỏ nên không thấy được. Nhóm T80/A10 dùng Telmisartan 80mg và Amlodipin 5mg trong 2 tuần đầu, sau đó Telmisartan 80mg và Amlodipin 10mg trong 6 tuần sau. Nhóm A10 dùng Amlodipin 5mg trong 2 tuần đầu, 10mg trong 6 tuần sau. Nhóm T80: dùng Telmisartan 80mg trong cả 8 tuần
Hình 3 : Mức độ giảm huyết áp tâm thu trung bình lúc kết thúc nghiên cứu, tức là sau 8 tuần điều trị. Mức độ giảm theo mỗi 10mmHg. Nhóm T80/A10 dùng Telmisartan 80mg và Amlodipin 5mg trong 2 tuần đầu, sau đó Telmisartan 80mg và Amlodipin 10mg trong 6 tuần sau. Nhóm A10 dùng Amlodipin 5mg trong 2 tuần đầu, 10mg trong 6 tuần sau. Nhóm T80 : dùng Telmisartan 80mg trong cả 8 tuần.
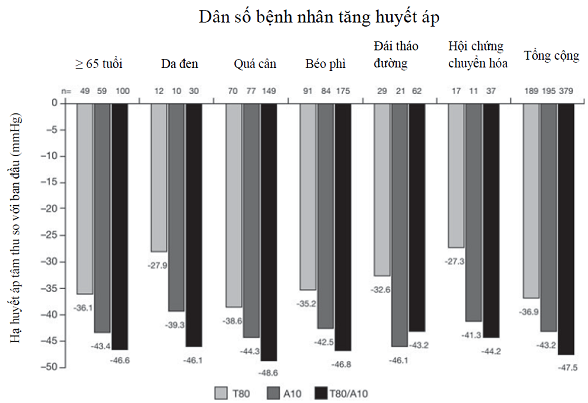
Hình 4: Mức độ giảm huyết áp so với ban đầu ở nhóm nhỏ trong nghiên cứu.
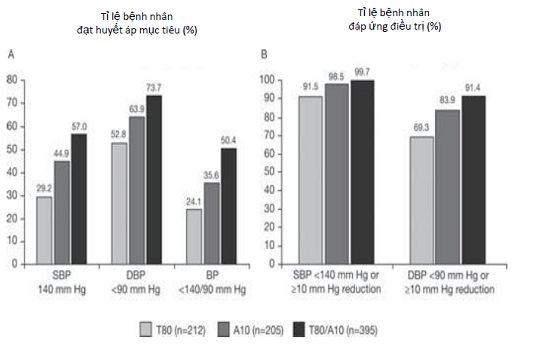
Hình 5: Tỷ lệ bệnh nhân đạt được huyết áp mục tiêu sau 8 tuần điều trị; SBP- huyết áp tâm thu, DBP- huyết áp tâm trương; BP- huyết áp.
Tỷ lệ đáp ứng và đạt huyết áp mục tiêu
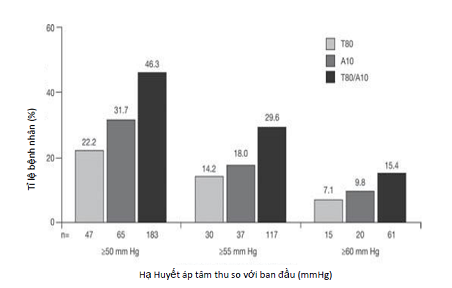
Tỷ lệ bệnh nhân đạt được huyết áp mục tiêu ở nhóm dùng thuốc viên phối hợp cao hơn một cách ổn định khi so với nhóm đơn trị liệu (hình 5). Nhóm dùng thuốc viên phối hợp cũng cho thấy có tỷ lệ đáp ứng cả huyết áp tâm thu lẫn tâm trương cũng cao hơn 2 nhóm kia. Nhìn chung, 99.7% nhóm T80/A10 có đáp ứng giảm huyết áp tâm thu (< 140mmHg, hoặc giảm hơn 10mmHg), so với tỷ lệ 91.5 của nhóm T80 và 98.5% của nhóm A10.
Nếu đặt tiêu chuẩn đáp ứng huyết áp tâm thu nghiêm ngặt hơn, tức là huyết áp < 140mmHg hoặc giảm hơn 15mmHg, thì tỷ lệ đáp ứng của nhóm T80/A10 sẽ là 99%. Trong khi tỷ lệ đáp ứng này là 88.7% và 98.5% lần lượt ở nhóm T80 và A10.
Tỷ lệ đáp ứng huyết áp tâm trương (huyết áp trung bình < 90mmHg hoặc giảm >= 10mmHg) của nhóm thuốc viên phối hợp T80/A10 đạt 91.4%. Hai nhóm kia chỉ đạt 69.3% cho nhóm T80 và 83.9% cho nhóm A10.
Mức độ an toàn
Viên phối hợp Telmisartan/ Amlodipin là an toàn và có độ dung nạp tốt. Tỷ lệ bệnh nhân bị tác dụng phụ của nhóm viên phối hợp này là tương tự như 2 nhóm kia, lần lượt là 32.8 cho T/A, 33.2% cho Telmisartan và 33.2% cho Amlodipin (Bảng II).
Những tác dụng phụ thường gặp nhất là:
– Phù ngoại biên 12.6%; 13.1% cho nhóm T80/A10, 3.7% cho nhóm T80 và 15% cho nhóm A10.
– Đau đầu 5.4%
– Chóng mặt 2.1%
– Rối loạn tiêu hóa 1.4%
Hầu hết các tác dụng phụ này (98.5%) có mức độ từ nhẹ đến trung bình.
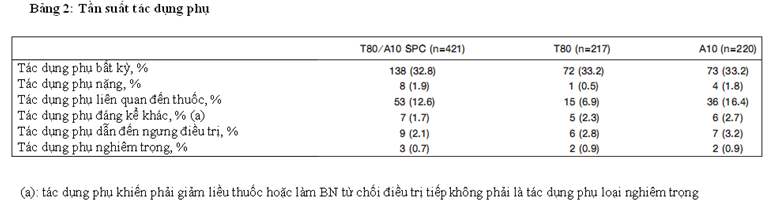
Những tác dụng phụ có liên quan đến điều trị chỉ gặp ở 12.6% nhóm dùng T80/A10, 6.9% nhóm T80 và 16.4% nhóm A10. Trong đó tỷ lệ phù ngoại biên lần lượt là 9.3, 2.3 và 13.2% cho các nhóm theo thứ tự trên. Vẫn thứ tự này, tỷ lệ đau đầu lần lượt là 1, 2.3 và 0.5%; tỷ lệ bị chóng mặt cũng theo thứ tự trên là 0.5, 0.5 và 0.9%.
Ngưng điều trị do tác dụng phụ gặp ở 2.1% cho nhóm T80/A10, 2.8% cho nhóm T80 và 3.2% cho nhóm A10. Tác dụng phụ nghiêm trọng chiếm tỷ lệ 0.7, 0.9 và 0.9% cho lần lượt cả 3 nhóm. Những tác dụng phụ nặng này được xem là chiếm tỷ thấp so với toàn bộ quá trình điều trị. Hầu hết tác dụng phụ nặng này là do nhập viện gây nên (6 bệnh nhân, chiếm 0.7%) và không có trường hợp tử vong. Tuy nhiên, có 3 trường hợp nghiêm trọng là: 1 bệnh nhân nhóm T80/A10 bị đột quỵ nhồi máu não, 1 người nhóm T80 bị thiếu máu não thoáng qua, 1 người trong nhóm A10 bị block nhĩ thất độ 2 (người này bị trong 2 tuần đầu tiên khi dùng Amlodipin 5mg).
BÀN LUẬN
Hơn 70% bệnh nhân tăng huyết áp không được kiểm soát huyết áp. Đại đa số bệnh nhân cần từ 2 viên thuốc hạ áp để đạt được huyết áp mục tiêu. Trong nghiên cứu này, nhóm người bệnh bị tăng huyết áp nặng (huyết áp >= 180/95 mmHg) dùng viên phối hợp Telmisartan 80mg/ Amlodipin 10mg có huyết áp giảm tốt hơn có ý nghĩa khi so với dùng đơn trị liệu 1 trong 2 thành phần trên cho dù trước đây có huyết áp có nặng thế nào. Cần lưu ý có hơn 60% bệnh nhân bị cao huyết áp hơn 5 năm và 31% người bệnh đã từng dùng 2 viên thuốc hạ áp. Với viên phối hợp thuốc này gồm Telmisartan 80mg/ Amlodipin 10mg thì thì hầu hết người bệnh (99.7%) có đáp ứng giảm huyết áp tâm thu, và quan trọng hơn là có hơn 50% người bệnh bị cao huyết áp nặng (>=180/95 mmHg) đạt được huyết áp mục tiêu < 140/90 mmHg chỉ sau 6 tuần điều trị. Bệnh nhân dùng thuốc phối hợp T/A đạt huyết áp tâm thu và hoặc tâm trương mục tiêu nhiều hơn khi so sánh với nhóm chỉ dùng 1 thành phần trong đó. Tỷ lệ đạt được huyết áp mục tiêu < 140/90 mmHg chỉ là 24% cho Telmisartan và 36% cho Amlodipin.
Người ta thấy phối hợp thuốc có hiệu quả tốt hơn so với đơn trị liệu làm giảm huyết áp tâm thu chỉ trong tuần đầu tiên, chính điều này rất quan trọng trong việc làm giảm nguy cơ tim mạch cho bệnh nhân bị cao huyết áp thật sự (> 180/95mmHg).
Khi so với đơn trị liệu, phối hợp thuốc làm giảm huyết áp có ý nghĩa trong suốt toàn bộ quá trình nghiên cứu, trong đó có đến 80% bệnh nhân đạt được hiệu quả tối đa chỉ sau 2 tuần dùng thuốc Telmisartan 80mg/ Amlodipin 5mg. Nghiên cứu VALUE cho thấy tầm quan trọng của việc hạ huyết áp nhanh chóng sẽ làm cải thiện kết quả bệnh tim mạch. Trong nghiên cứu này Amlodipin làm huyết áp hạ nhanh hơn trong thời gian đầu và Amlodipin tỏ ra tốt hơn ở tất cả các tiêu chí đánh giá trong 6 tháng đầu của nghiên cứu.
Tăng huyết áp có 1 tỷ lệ mắc khá cao, nhất là ở người lớn tuổi, béo phì, hoặc người da đen. Tăng huyết áp cũng làm gia tăng nguy cơ tim mạch cho người bệnh Đái tháo đường hoặc bệnh thận. Vì thế, nghiên cứu nhóm nhỏ cho các đối tượng này sẽ là rất thích hợp để có 1 cách điều trị toàn bộ. Việc dùng viên hạ áp phối hợp Telmisartan/ Amlodipin trong nghiên cứu này cho thấy có kết quả hạ áp tốt hơn so với điều trị chỉ 1 thuốc, nhưng sự khác biệt là không đủ nhiều để có ý nghĩa về mặt thống kê. Tuy nhiên, do nghiên cứu này không chú trọng vào phân tích các nhóm nhỏ và cũng không có kết luận rõ ràng nào về nhóm này. Người ta chỉ thấy không có tương tác qua lại trong khi điều trị các nhóm nhỏ có yếu tố nguy cơ này, ngoại trừ các bệnh nhân Đái tháo đường type 2, có lẽ là do số bệnh nhân Đái tháo đường quá ít trong nhóm nhỏ này. Kết quả này cho thấy viên phối hợp T/A có hiệu quả tương đương ngay cả đối với nhóm nguy cơ.
Những phát hiện của nghiên cứu này sẽ đồng hành cùng các nghiên cứu trước kia cũng về phối hợp Telmisartan/ Amlodipin trong nhóm dân số bị tăng huyết áp khác. Littlejohn cùng cộng sự đã phát hiện rằng việc dùng Telmisartan 40-80mg cùng với Amlodipin 5-10mg sẽ làm giảm huyết áp tâm thu/ tâm trương có ý nghĩa về mặt thống kê khi so sánh với đơn trị liệu dùng 1 trong 2 thành phần trên cho các bệnh nhân bị cao huyết áp độ 1 và 2. Hơn nữa, người ta thấy dùng phối hợp thuốc có tỷ lệ phù ngoại biên thấp hơn khi so với dùng Amlodipin đơn thuần. Hơn thế nữa, có tác giả còn thấy điều trị viên phối hợp T80/A10 giúp đạt huyết áp mục tiêu (<130/80 mmHg) nhiều hơn khi so với dùng A10, với tỷ lệ tương ứng là 82.7% so với 37.9%, P<0.0001.
Viên phối hợp Telmisartan/ Amlodipin cũng có hiệu quả giảm huyết áp tương đương với phối hợp 3 thứ thuốc cùng lúc với valsartan/ Amlodipin / hydrochlorothiazide (tài liệu tham khảo số 38). Viên phối hợp T/A làm hạ huyết áp mạnh và nhanh sẽ giúp người bệnh mau chóng đạt huyết áp mục tiêu và vì thế làm giảm nguy cơ bệnh và tử vong do tim mạch.
Mức độ an toàn của viên T80/A10 khi so sánh với từng thành phần T hoặc A thì tương đương với mức độ an toàn của các báo cáo trước kia [35,36]. Trong nghiên cứu này, viên T80/A10 đi kèm 9.3% phù ngoại biên, thấp hơn mức 13.2% do thuốc Amlodipin 10mg đơn trị liệu gây nên. Có 1% bệnh nhân bị nhức đầu do viên T80/A10 so với 2.3% do viên T80 đơn thuần. Mặc dù có 3 trường hợp có tác dụng không mong muốn mức độ nghiêm trọng (mỗi nhóm có 1 trường hợp nặng) có vẻ như là có liên quan đến điều trị, tuy nhiên những trường hợp nặng này cũng có thể do bệnh lý cao huyết áp cơ bản của bệnh nhân gây ra.
KẾT LUẬN
Nghiên cứu này cho thấy thuốc viên phối hợp Telmisartan/ Amlodipin có hiệu quả rất tốt, làm giảm huyết áp chỉ sau 1 tuần điều trị, hiệu quả này cũng duy trì liên tục trong suốt 8 tuần trị liệu khi so sánh với đơn trị liệu 1 trong hai thành phần Telmisartan hoặc Amlodipin .
Khi điều trị tăng huyết áp nặng với viên phối hợp T/A, huyết áp trung bình giảm 47.5mmHg, với 80% hiệu quả tối đa đạt được sau 2 tuần dùng thuốc. Nhìn chung, 99% bệnh nhân đáp ứng với phối hợp điều trị và quan trọng là hơn 50% người bệnh đạt được huyết áp mục tiêu (< 140/90 mmHg) sau điều trị 8 tuần với viên phối hợp T/A.
Khi dùng cho BN có huyết áp tâm thu cao mức độ nặng, tính an toàn và mức độ dung nạp của thuốc viên phối hợp T/A này cũng giống như mức độ an toàn và độ dung nạp của thuốc viên phối hợp T/A trong các nghiên cứu trước kia ở những nhóm bệnh nhân khác nhau. Như vậy, kết quả này cho thấy viên phối hợp T/A này là 1 thuốc hiệu quả và an toàn, nhất quán với hiệu quả và độ an toàn của từng thành phần thuốc riêng lẻ bên trong đó.
Tóm lại, phối hợp Telmisartan/ Amlodipin là 1 lựa chọn điều trị hiệu quả cho nhóm bệnh nhân tăng huyết áp khó trị, góp phần vào các nhóm thuốc dùng điều trị lâu dài cho bệnh tăng huyết áp cũng như góp phần phòng ngừa các biến cố và tử vong do bệnh tim mạch.
Tài liệu tham khảo:
1. Lewington S, Clarke R, Qizilbash N, et al. Age-specific relevance ofusual blood pressure to vascular mortality: a meta-analysis of individualdata for one million adults in 61 prospective studies. Lancet.2002;360:1903-1913.
2. INVEST. INVEST retrospective analyses. ACC2010. http://www.theheart.org/article/1055859.do.
3. ACCORD Study Group. Effects of intensive blood-pressure controlin type 2 diabetes mellitus. N Engl J Med. 2010;362:1575-1585.
4. Appel LJ, Wright JT Jr, Greene T, et al; AASK Collaborative Research Group. Intensive blood-pressure control in hypertensive chronic kidney disease. N Engl J Med. 2010;363:918-929.
5. Dickerson JE, Hingorani AD, Ashby MJ, et al. Optimization of antihypertensive treatment by crossover rotation of four major classes. Lancet. 1999;353:2008-2013.
6. Black H, Elliott J, Neaton J, et al. Baseline characteristics and early blood pressure control in the CONVINCE trial. Hypertension.
2001;37:12-18.
7. Cushman W, Ford C, Cutler J, et al. Success and predictors of blood pressure control in diverse North American settings: the Antihypertensive and Lipid Lowering treatment to prevent Heart Attack Trial (ALLHAT). J Clin Hypertens. 2002;4:393-404.
8. Bakris G. The importance of blood pressure control in the patient with diabetes. Am J Med. 2004;116(Suppl 5A):30S-38S.
9. Dahlo¨ f B, Sever PS, Poulter NR, et al; ASCOT Investigators Prevention of cardiovascular events with an antihypertensive regimen of amlodipine adding perindopril as required versus atenolol adding bendroflumethiazide as required, in the Anglo-Scandinavian Cardia Outcomes Trial-Blood Pressure Lowering Arm (ASCOT-BPLA): a multicentre randomized controlled trial. Lancet. 2005;366:895-906.
10. Chobanian AV, Bakris GL, Black HR, et al. The seventh report of the joint national committee on prevention, detection, evaluation, and treatment of high blood pressure. JAMA. 2003;289: 2560-2572.
11. Mancia G, De Backer G, Dominiczak A, et al. 2007 ESH-ESC practice guidelines for the Management of Arterial Hypertension: ESHESC Task Force on the Management of Arterial Hypertension. J Hypertens. 2007;25:1751-1762.
12. Ogihara T, Kikuchi K, Matsuoka H, et al. The Japanese Society of Hypertension Guidelines for the Management of Hypertension (JSH 2009). Hypertens Res. 2009;32:3-107.
13. Mancia G, Laurent S, Agabiti-Rosei E, et al. Reappraisal of European guidelines on hypertension management: a European Society of Hypertension Task Force document. European Society of Hypertension. J Hypertens. 2009;27:2121-2158.
14. National Collaborating Centre for Chronic Conditions. Hypertension: Management of Hypertension in Adults in Primary Care: Partial Update. London, UK: Royal College of Physicians; 2006 (http:// www.nice.org.uk/download.aspx?o=CG034fullguideline.pdf Accessed
February 2012).
15. Jamerson K, Weber MA, Bakris GL, et al; ACCOMPLISH Trial Investigators Benazepril plus amlodipine or hydrochlorothiazide for hypertension in high-risk patients. N Engl J Med. 2008;359:2417- 2428.
16. Ma J, Lee KV, Stafford RS. Changes in antihypertensive prescribing during US outpatient visits for uncomplicated hypertension between 1993 and 2004. Hypertension. 2006;48:846-852.
17. Egan BM, Zhao Y, Axon RN. US trends in prevalence, awareness, treatment, and control of hypertension 1988-2008. JAMA.
18. Volpe M, Tocci G, Trimarco B, et al. Blood pressure control in Italy: results of recent surveys on hypertension. J Hypertens. 2007;25:1491-1498.
19. Kearney PM, Whelton M, Reynolds K, et al. Worldwide prevalence of hypertension: a systematic review. J Hypertens. 2004;22:11-19.
20. Tedesco MA, Natale F, Calabro R. Effects of monotherapy and combination therapy on blood pressure control and target organ damage: a randomized prospective intervention study in a large population of hypertensive patients. J Clin Hypertens. 2006;8:634-641.
21. Khan NA, Hemmelgarn B, Padwal R, et al. Canadian Hypertension Education Program. The 2007 Canadian Hypertension Education Program recommendations for the management of hypertension: part 2 – therapy. Can J Cardiol. 2007;23:539-550.
22. Feldman RD, Zou GY, Vandervoort MK, et al. A simplified approach to the treatment of uncomplicated hypertension a cluster randomized, controlled trial. Hypertension. 2009;53:646-653.
23. Wald DS, Law M, Morris JK, et al. Combination therapy versus monotherapy in reducing blood pressure: meta-analysis on 11,000 participants from 42 trials. Am J Med. 2009;122:290-300.
24. Bangalore S, Kamalakkannan G, Parkar S, Messerli FH. Fixed-dose combinations improve medication compliance: a meta-analysis. Am J Med. 2007;120:713-719.
25. Gerbino PP, Shoheiber O. Adherence patterns among patients treated with fixed-dose combination versus separate antihypertensive agents. Am J Health Syst Pharm. 2007;64:1279-1283.
26. Dickson M, Plauschinat CA. Compliance with antihypertensive therapy
in the elderly. Am J Cardiovasc Drugs. 2008;8:45-50.
27. Gupta AK, Arshad S, Poulter NR. Compliance, safety, and effectiveness
of fixed-dose combinations of antihypertensive agents. A metaanalysis.
Hypertension. 2010;55:399-407.
28. Andreadis EA, Tsourous GI, Marakomichelakis GE, et al. High-dose
monotherapy vs low-dose combination therapy of calcium channel
blockers and angiotensin receptor blockers in mild to moderate
hypertension. J Hum Hypertens. 2005;19:491-496.
29. Kohlmann O, Oigman W, Mion D, et al. The ‘LOTHAR’ study:
evaluation of efficacy and tolerability of the fixed combination of
amlodipine and losartan in the treatment of essential hypertension.
Arq Bras Cardiol. 2006;86:39-51.
30. Julius S, Kjeldsen SE, Weber M, et al; VALUE Trial Group Outcomes
in hypertensive patients at high cardiovascular risk treated
with regimens based on valsartan or amlodipine: the VALUE randomised
trial. Lancet. 2004;363:2022-2031.
31. Weber MA, Julius S, Kjeldsen SE, et al. Blood pressure dependent
and independent effects of antihypertensive treatment on clinical
events in the VALUE Trial. Lancet. 2004;363:2049-2051.
32. Sekikawa A, Hayakawa T. Prevalence of hypertension, its awareness
and control in adult population in Japan. J Hum Hypertens.
2004;18:911-912.
33. Kearney PM, Whelton M, Reynolds K, et al. Global burden of
hypertension: analysis of worldwide data. Lancet. 2005;365:217-
223.
34. Brown MJ. Hypertension and ethnic group. BMJ. 2006;332:833-
836.
35. Littlejohn TW III, Majul CR, Olvera R, et al. Results of treatment
with telmisartan-amlodipine in hypertensive patients. J Clin Hypertens.
2009;11:1-7.
36. Littlejohn TW III, Majul CR, Olvera R, et al. Telmisartan plus amlodipine in patients with moderate or severe hypertension: results
from a subgroup analysis of a randomized, placebo-controlled, parallel-
group, 4 _ 4 factorial study. Postgrad Med. 2009;121:5-14.
37. White WB, Littlejohn TW, Majul CR, et al. Effects of telmisartan
and amlodipine in combination on ambulatory blood pressure in
stages 1-2 hypertension. Blood Press Monit. 2010;15:205-212.
38. Calhoun DA, Crikelair NA, Yen J, Glazer RD. Amlodipine ⁄ valsartan
⁄ hydrochlorothiazide triple combination therapy in moderate
⁄ severe hypertension: secondary analyses evaluating efficacy and
safety. Adv Ther. 2009;26:1012-1023.








