Bệnh thận mạn (BTM) là một vấn đề sức khỏe cộng đồng toàn cầu, hiện nay nó được xem là một yếu tố nguy cơ của bệnh tim mạch và tiến triển đến bệnh thận giai đoạn cuối mà cần phải điều trị thay thế [1,2,3].
PGS. TS. TRẦN VĂN HUY FACC FESC
Phó Chủ Tịch Phân Hội Tăng Huyết Áp Việt Nam,Chủ Tịch Hội Tim Mạch Khánh Hòa
Trưởng Khoa Tim Mạch Bệnh Viện Tỉnh Khánh Hòa
Bệnh thận mạn (BTM) là một vấn đề sức khỏe cộng đồng toàn cầu, hiện nay nó được xem là một yếu tố nguy cơ của bệnh tim mạch và tiến triển đến bệnh thận giai đoạn cuối mà cần phải điều trị thay thế [1,2,3]. Trong đó angiotensin II và các thành phần khác của hệ renin angiotensin aldosterone (RAAS) đóng một vai trò trung tâm trong bệnh sinh và tiến trình của chuổi bệnh lý tim mạch và thận.
Angiotensin II làm tăng áp lực các tiểu động mạch cầu thận đến và đi và các phản ứng mạch máu. Sự co mạch trong thận gây ra bởi angiotensin II làm tăng áp lực thẩm thấu cầu thận và gây rối loạn cấu trúc và chức năng trong thận gây tổn thương thận. Ngoài ra angiotensin còn điều chỉnh sự tăng sinh tế bào thận làm gia tăng thêm tổn thương cấu trúc thận. Tất cả đều nầy dẫn đến viêm mô kẻ xơ hóa cầu thận gây tiểu protein niệu và bệnh thận mạn tiến triển [3,4]
Hình 1. Vi đạm niệu làm tăng nguy cơ tử vong tim mạch và tử vong chung
Phát hiện sớm bệnh thận mạn qua sàng lọc tìm albumine niệu [mức bài xuất albumine nước tiểu 24 giờ, tỷ albumine ceatinine niệu (ACR)] và đo mức lọc cầu thận [5,6]. Trong hơn 2 thập kỷ qua, đã có nhiều nghiên cứu thực nghiệm, dịch tễ và lâm sàng chứng minh vai trò bảo vệ thận của các thuốc ức chế hệ RAAS với các ức chế men chuyển (ƯCMC) và chẹn thụ thễ angiotesin II (TT AII) [3-6].
Dự phòng khởi phát vi đạm niệu. Vai trò bảo vệ thận có thể can thiệp từ giai đoạn rất sớm là đừng để xuất hiện vi đạm niệu ở bệnh nhân đái tháo đường (ĐTĐ). Sự xuất hiện vi đam niệu ở bệnh nhân ĐTĐ là biểu hiệu giai đoạn sớm nhất của bệnh thận ĐTĐ và làm gia tăng nguy cơ tim mạch tử vong chung và tử vong tim mạch [3,6] (hình 1). Chính vì vậy vi đạm niệu được xem như một marker của bệnh tim mạch [2,3]. Trong thử nghiệm EUCLID (EURODIAB Controlled trial of Lisinopril in Insulin dependent Diabetes) ngẫu nhiên có đối chứng giữa ƯCMC lisinopril (10-20mg/ngày) và placebo ở 530 bệnh nhân ĐTĐ týp 1 có đạm niệu bình thường hoặc vi đạm niệu (15% vi đạm niệu, 85% đạm niệu bình thường), phân tích sau 2 năm ghi nhận tỷ lệ albumin creatinine niệu thấp hơn trong nhóm lisinopril so với placebo là 49.7% [7]. Trong thử nghiệm BENEDICT (Bergamo Nephrologic Diabetic Complications Trial) với 1.204 bệnh nhân tăng huyết áp ĐTĐ týp 2 và albumine niệu bình thường được ngẫu nhiên điều trị ƯCMC trandolapril (2mg/ngày), chẹn calci verapamil SR (240mg/ngày), phối hợp cả 2 và placebo, sau 3,6 năm cho thấy UCMC giảm có ý nghĩa 53% nguy cơ khởi phát microalbumine niệu HR 0.47 (0.26-0.83) P<0,01 [8] (hình 3). Đối với chẹn TT AII, các thử nghiệm DIRECT (Diabetic Retinopathy Candesartan Trial ) (2009) nghiên cứu trên 3326 bệnh nhân ĐTĐ týp 1 và 1905 bệnh nhân ĐTĐ týp 2 cho thấy chẹn TT AII (candesartan) không dự phòng khởi phát vi đạm niệu ở bệnh nhân ĐTĐ có huyết áp bình thường HR 0.95 [95% CI, 0.78 to 1.16]; P= 0.60) [27]. Nghiên cứu ROADMAP (randomised olmesartan and Diabetes microalbuminuria Prevention) (2010), 4447 bệnh nhân ĐTĐ týp 2 có ít nhất 1 yếu tố nguy cơ và albumine niệu bình thường, điều trị ngẫu nhiên chẹn TT AII hoặc placebo, sau 3,2 năm ghi nhận chẹn AII omesartan giảm khởi phát microalbumin 23% HR 0.77 (95% CI, 0.63-0.94) P=0.01. Mặc dầu tử vong chung không khác biệt nhưng tử vong tim mạch trong nhóm điều trị AII cao hơn có ý nghĩa so với placebo [15 (0,7%) vs 3(0,1) P <0,005) [9].
Dự phòng bệnh thận mạn có đạm niệu đại thể. Trong dự phòng ngăn ngừa từ vi đạm niệu tiến triển đến bệnh thận mạn có protein niệu >3g/24 giờ ngày. Có một bằng chứng lớn cho thấy bệnh nhân ĐTĐ có vi đạm niệu, ƯCMC và chẹn thụ thể AII đã làm giảm tiến triển thành bệnh thận mạn có đạm niệu đại thể và giảm nguy cơ tim mạch [10]. Một phân tích gộp gồm 12 nghiên với 689 bệnh nhân ĐTĐ týp 1, ghi nhận ƯCMC làm giảm đáng kể tiến triển đến bệnh thận ĐTĐ (odds ratio 0.38, 95% CI 0.25 to 0.57) [11]. Trong nghiên cứu HOPE (Heart Outcomes Prevention Evaluation ) với 9.000 đối tượng trong đó phân tích nhánh MICRO-HOPE (Microalbuminuria,Cardiovascular and Renal Outcomes) với 3.577 bệnh nhân ĐTĐ týp 2 có microalbumine niệu hoặc bình thường cho thấy ƯCMC ramipril giảm tỷ lệ bệnh thận mạn 24% (3-40, p=0·027) và giảm 25% tiêu chí chính bao gồm nhồi máu cơ tim, đột quỵ và tử vong tim mạch [12] (hình 2). Theo nghiên cứu BRILLIANT (Blood pressure, Renal effects, Insulin control, Lipids, Lisinopril And Nifedipine Trial) 335 bệnh nhân ĐTĐ týp 2 có tăng huyết áp và vi đạm niệu >20μg/phút, sau 12 tháng điều trị ƯCMC lisinopril làm thay đổi giảm bài xuất albumine hơn nifedipine có sự khác biệt 20μg/phút có ý nghĩa p<0,006. Lúc kết thúc 30% bệnh nhân trong nhóm lisinopril có albumine niệu trở về bình thường trong khi chỉ có 12% trong nhóm nifedipine [13]. Đối với chẹn TT AII, thử nghiệm IRMA 2 (irbesartan in patients with type 2 diabetes and microalbuminuria) ở bệnh nhân ĐTĐ có vi đạm niệu cho thấy nhóm chẹn thụ thể AII irbesartan 300mg có 5,2% (10/194 bệnh nhân) và nhóm irbesartan 150mg/n có 9,7% (19/195) so với nhóm chứng có 14,9% (30/201) phát triển bệnh thận mạn có đạm niệu đại thể (HR, 0.30 CI 95% 0.14-0.61; P<0.00) [14] (hình 3).
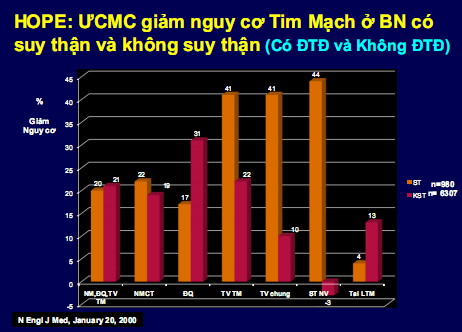
Hình 2: ƯCMC giảm nguy cơ bệnh tim mạch ở bệnh nhân có suy thận và không suy thận (NMCT: nhồi máu cơ tim,ĐQ: đột qụy, TVTM: tử vong tim mạch, STNV: suy tim nhập viện,LTM: lưu thông mạch)
Dự phòng bệnh thận mạn giai đoạn cuối và tử vong. Đối với ngăn ngừa tiến triển từ BTM có albumine đại thể đến bệnh thận giai đoạn cuối (BTGĐC) và tử vong, nhiều nghiên cứu cho thấy ƯCMC có hiệu qủa làm chậm tiến trình đến BTGĐC ở bệnh nhân đái tháo đường và không đái tháo đường có bệnh thận mạn. Ngay từ năm 1993 nghiên cứu Collaborative study trên 409 bệnh nhân ĐTĐ týp 1 có albumine >500mg/ngày và creatinine máu <221 μmol/l (<2.5 mg/dl), trong 3 năm điều trị captopril làm giảm 50% tỷ lệ BTGĐC và tăng gấp đôi creatinine máu HR 0.52 (0.16-0.67) P <0,007 [15]. Trong nghiên cứu REIN (Ramipril Efficacy In Nephropathy) ở bệnh nhân không ĐTĐ cho thấy ƯCMC giảm tỷ lệ độ lọc cầu thận 22%, 22%, và 35% và tỷ lệ BTGĐC 33% (P < 0.05), 37%, và 100% (P< 0.01) trong các mức lọc cầu thận thấp nhất, trung bình và cao nhất lần lượt [16]. Theo một nghiên cứu ngẫu nhiên đối chứng của Hou FF và cs cho thấy ƯCMC giảm 43% nguy cơ tăng gấp đôi creatinine máu, BTGĐC hoặc tử vong ở bệnh nhân không ĐTĐ với bệnh thận mạn đang tiến triển (creatinin 264-440mmol/l) [17]. Trong một phân tích gộp 11 thử nghiệm của Kshirsagar AV bao gồm cả ĐTĐ và không ĐTĐ có bệnh thận cho thấy ƯCMC đã làm giảm 40% nguy cơ BTGĐC hoặc tăng gấp đôi creatinine [18]. Đối với chẹn TT AII, thử nghiệm RENAAL (Reduction of Endpoints in NIDDM with the Angiotensin II Antagonist Losartan) ghi nhận chẹn TT AII losartan giảm 16% nguy cơ với các tiêu chí BTGĐC, tăng gấp creatinine và tử vong HR 0.84 (0.72-0.98) P <0,02[19]. Thử nghiệm INDT (Irbesartan in Diabetic Nephropathy Trial) với 1715 bệnh nhân tăng huyết áp có bệnh thận ĐTĐ điều trị với irbesartan (300mg ngày), amlodipine (10mg ngày), hoặc placebo.sau 2,6 năm
Hình 3: ƯCMC và chẹn TT AII ngăn ngừa khởi phát vi đạm niệu, tiến triển bệnh thận mạn, tiến triển BTGĐC và tử vong ở bệnh nhân ĐTĐ [21].
ghi nhận nhóm chẹn TT AII giảm các tiêu chí chính (BTGĐC, tăng gấp creatinine và tử vong) thấp hơn 20% so với placebo và thấp hơn 23% so với amlodipne độc lập với hạ áp (hình 3) [26]. Tuy nhiên trong nghiên cứu TRANCEND (Telmisartan Randomised Assessment Study in ACE Intolerant Subjects with Cardiovascular Disease 2009) với 5.927 bệnh nhân có bệnh tim mạch hoặc đái tháo đường với tổn thương cơ quan đích nhưng không có đạm niệu đại thể không dung nạp ƯCMC điều trị chẹn TT AII (telmisartan) phân tích theo tiêu chí về thận bao gồm thẩm phân máu, tăng gấp đôi creatinine, thay đổi mức lọc cầu thận và thay đổi albumine niệu đã cho thấy chẹn TT AII không có khác biệt với placebo HR 1.29 (CI 95% 0.87-1.89); P=0.2 [28]
Bệnh thận giai đoạn cuối . Đối với BTGĐC đang thẩm phân máu, ức chế RAAS là các thuốc hạ huyết áp ưu tiên hàng đầu, đặc biệt ở bệnh nhân ĐTĐ hoặc có tiền sử suy tim [5]. Theo nghiên cứu của Mois và cs phân tích 1842 bệnh nhân thẩm phân máu trong nghiên cứu USRDS Wave đã xác định ƯCMC là gắn liền với giảm 30% nguy cơ mất chức năng thận hiện còn lúc 1 năm. Theo Efrati và cs trong một phân tích hồi cứu 126 bệnh nhân xác định dùng ƯCMC là gắn liền với cải thiện tỷ lệ sống. Suzuki và cs nghiên cứu 366 bệnh nhân thẩm phân máu được ngẫu nhiên dùng các chẹn thụ thể TT AII và placebo, sau 36 tháng ghi nhận chẹn TT AII giảm các biến cố tim mạch không tử vong nhưng không khác biệt tử vong chung [22].
So sánh hiệu qủa giữa ƯCMC và chẹn AII. Một phân tích gộp của Strippoli G đánh giá ƯCMC và chẹn AII so với placebo đối với tử vong và các tiêu chí về thận (bao gồm BTGĐC, nhân đôi creatinine máu, ngăn ngừa tiến triển từ vi đạm niệu đến đạm niệu đại thể, làm giảm vi đạm niệu) điều trị ở những bệnh nhân có bệnh thận ĐTĐ đã cho thấy ƯCMC làm giảm tỷ lệ tử vong chung 21% có ý nghĩa so placebo RR 0,79 CI95% 0,63-0.99, nhưng chẹn TT AII thì không RR 0,99 CI95% 0.85-1,17. Các các tiêu chí về thận ghi nhận cả ƯCMC hoặc chẹn TT AII đều có hiệu qủa có ý nghĩa so với placebo [20]. So sánh trực tiếp giữa ƯCMC và chẹn AII, chỉ có một
Hình 4: Hiệu qủa ƯCMC và chẹn TT AII so với placebo trên tử vong chung ở bệnh nhân có bệnh thận mạn ĐTĐ, ƯCMC giảm tử vong chung 21% có ý nghĩa, chẹn TT AII không giảm [20]
nghiên cứu DETAIL ở bệnh nhân ĐTĐ có albumine, cho thấy không có sự khác biệt, tuy nhiên kết qủa sau 5 năm chẹn TT AII có các biến cố tim mạch xảy ra 22,5% so với ƯCMC chỉ có 16,2% [21]
Phối hợp ƯCMC và chẹn TT AII. Trong một số thử nghiệm nhỏ cho thấy có sự gia tăng giảm đạm niệu so với đơn trị, tuy nhiên cho đến nay chưa có những thử nghiệm lớn lâu dài so sánh giữa đơn trị với phối hợp về bảo vệ thận, mà cần phải đợi kết qủa VA NEPHRON-D trong việc giảm tiến triển BTGĐC và tử vong trong liệu trình phối hợp ƯCMC và chẹn AII so với đơn trị [21].
Về tính an toàn. Cả ƯCMC và chẹn thụ thể AII đều cho thấy có hiệu qủa bảo vệ thận và không chống chỉ định chỉ vì lý do creatinine tăng lúc bắt đầu điều trị, có một sự gia tăng creatinine ổn định đến 30-35% so với trị số ban đầu trong 2 tháng đầu điều trị nhưng không làm tăng kali thì vẫn có thể dung nạp được [23,29]. Vấn đế chú ý cẩn trọng là tình trạng tăng kali ở bệnh nhân suy thận mạn. ĐTĐ với bệnh thận là một nguy cơ gây tăng kali. Bệnh nhân đang dùng thuốc bổ sung kali, dùng lợi niệu giử kali hoặc các kháng viêm non steroid đều làm nguy cơ tăng kali. Nếu creatinine tăng >30% giảm liều ƯCMC 50% và dùng thêm các tác nhân hạ áp khác,
nếu creatinine vẫn tăng >30% và <50% trong tháng đầu tiên, các nguyên nhân thiếu dịch phải loại trừ, các thuốc kháng viêm non steroid phải ngừng. Nếu creatinine vẫn còn tăng trên > 30% sau 2 tháng có thể ngừng ƯCMC hoặc chẹn TT AII hoặc khi có tăng kali (mức kali máu tăng >5,6 mmol/L). Còn tăng creatinine nhanh >50% thì ngừng ngay và xem xét sàng lọc bệnh cảnh
Hình 4: Liên quan giữa giảm mức lọc cầu thận với thay đổi mức creatinine máu. Những người >65 tuổi hoặc gầy (49,5kg) có mức lọc cầu thận thấp hơn so với người bình thường. Vùng bôi nhạt cho thấy hiệu qủa của ƯCMC bảo vệ thận đã được chứng minh qua các thử nghiệm lâm sàng, vùng bôi đậm là cần thẩm phân máu [22]
hẹp động mạch thận 2 bên hay 1 bên ở bệnh nhân chỉ có một thận [23]. Theo dõi creatinine và điện giải đồ cần phải được tiến hành mỗi 1 đến 2 tuần. ƯCMC và chẹn AII thường gây tăng kali từ 0,3 đến 0,5 mEq/L [5,6,23]. Tuy nhiên chỉ có 1-2% bệnh nhân dùng RAAS ngừng điều trị do tăng kali ở bệnh nhân có bệnh thận không ĐTĐ [23]. Khi ƯCMC hoặc chẹn TT AII được dùng ở bệnh thận mạn nặng (hệ số thanh thải creatinine <30mL/phút), có hai vấn đề quan trọng: (a) nếu thuốc hoặc chuyển hóa của nó hoàn toàn (như lisinopril) hoặc một phần (như losartan) thải qua thận, liều thường dùng sẽ làm tích lũy và gia tăng nồng độ ở mô và huyết tương và (b) tăng các tác dụng phụ như tăng kali máu. Cho nên cần khuyến cáo theo dõi cẩn thận creatinine và điện giải đồ và cần phải xem xét kỷ về đường thải và các đặc điểm dược động học của thuốc để giảm liều và chia khoản cách giữa các liều trong ngày hoặc tuần (ví dụ cách ngày hay 3 lần /1 tuần) [22].
Các khuyến cáo hiện hành. Từ các chứng cứ trên, các khuyến cáo hiện nay như của Canada (CHEP) 2011 [24], Hội ĐTĐ Hoa kỳ (ADA 2011) [25], Hội Thận Hoa Kỳ (NKF 2007) [5], Hội Thận Vương Quốc Anh 2011 [6] đều khuyến cáo ƯCMC hoặc chẹn AII là thuốc ưu tiên
Bảng 1. Liều bắt đầu và tối đa, thời gian bán hủy của ƯCMC và chẹn TT AII ở bệnh thận giai đoạn cuối thẩm phân máu [22].

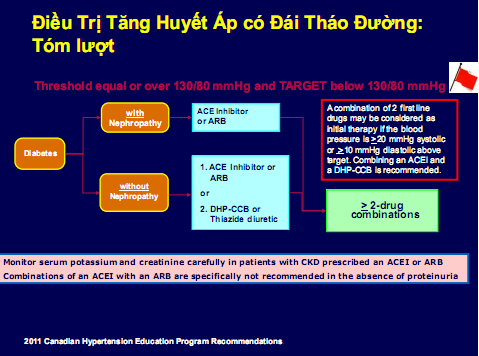
Hình 5 và 6: Điều trị tăng huyết áp có bệnh thận mạn và có đái tháo đường và không có đái tháo đường theo khuyến cáo canada 2011
hàng đầu trong THA có đái tháo đường hay không và có bệnh thận hay dự phòng khởi phát vi đạm niệu. Theo NKF và ADA ở bệnh nhân ĐTĐ có đạm niệu đại thể và huyết áp bình thường cũng cần chỉ định ƯCMC hoặc chẹn AII và xem xét ngay cả khi có đạm niệu vi thể. Khi có tăng huyết áp và bệnh thận ĐTĐ từ giai đoạn 1 đến 4 thì phải chỉ định ƯCMC hoặc chẹn TT AII (A) (NKF), và thường phối hợp với một chẹn calci (CHEP 2011). Theo khuyến cáo của Hội Thận Vương Quốc Anh 2011 ở bệnh nhân có bệnh thận mạn và protein niệu >0,5g/ngày, ƯCMC hoặc chẹn thụ thể AII phải được điều trị như một phần của liệu pháp hạ áp trừ phi có chống chỉ định (IA). Ở bệnh nhân ĐTĐ có vi đạm niệu phải được điều trị với ƯCMC hoặc chẹn thụ thể AII với tăng dần đến liều tối đa nếu dung nạp mà không xét huyết áp ban đầu, ngoại trừ chống chỉ định các thuốc nầy. Tình trạng hạ huyết áp cần phải tránh (IA) [6]. Theo NKF đối với BTGĐC thẩm phân máu, ƯCMC hoặc chẹn TT AII được ưu tiên chọn lựa hàng đầu đặc biệt ở bệnh nhân ĐTĐ hoặc có tiền sử suy tim [5
Tóm lượt. Điều chỉnh RAAS là nền tảng trong điều trị và ngăn ngừa chuổi bệnh lý tim mạch và thận. ƯCMC và chẹn TT AII đã được chứng minh có những hiệu qủa bảo vệ thận đặc hiệu ở bệnh nhân ĐTĐ và không ĐTĐ, hiệu qủa nầy có thể gia tăng khi chúng dùng kết hợp. ƯCMC chỉ định hàng đầu trong THA và chuổi bệnh lý tim mạch và thận có ĐTĐ hay không ĐTĐ, khi không dung nạp, chỉ định dùng chẹn TT A II. Bệnh nhân ĐTĐ có đạm niệu (đại thể, vi thể) và huyết áp bình thường cần chỉ định ƯCMC hoặc chẹn AII. Trong chỉ định cần ưu tiên những thuốc đã được chứng minh qua các chứng cứ lâm sàng về tính hiệu qủa, tính an toàn, giữa chi phí và hiệu qủa và tính dung nạp.
Tài liệu tham khảo:
1. Sarnak MJ, Levey AS, Schoolwerth AC, et al. Kidney disease as a risk factor for development of cardiovascular disease. A statement from the American Heart Association Councils on Kidney in Cardiovascular Disease, High Blood Pressure Research, Clinical Cardiology,and Epidemiology and Prevention. Circulation 2003;108: 2154-2169,
2.Levey AS, Atkins R, Coresh J, et al. Chronic kidney disease as aglobal public health problem: Approaches and initiatives












