BS.CKI. PHẠM NGUYỄN PHI KHANH (1)
BS.CKI. DƯƠNG NGỌC HUY HOÀNG (2)
CKI. NGUYỄN THANH HIỀN
(1) BV Nhân dân 115; (2) Đại học Y khoa Tân Tạo
- MỞ ĐẦU
Suy tim ảnh hưởng đến khoảng 50 triệu người trên toàn thế giới[8].Cách tiếp cận điều trị hiện nay trong suy tim là dùng các thuốc khác nhau nhắm vào các cơ chế khác nhau trong bệnh sinh suy tim, nhằm cải thiện chức năng tim mạch, giảm biến cố lâm sàng, kéo dài tuổi thọ và tăng chất lượng sống cho bệnh nhân. Dù vậy, các bệnh nhân này vẫn thường xuyên bị các đợt suy tim kịch phát, tỉ lệ tái nhập viện cao, chất lượng sống giảm, tử vong tăng, làm tăng gánh nặng cho bệnh nhân, gia đình và xã hội. Theo báo cáo từ nghiên cứu sổ bộ tại Hoa Kỳ, dù với các lựa chọn điều trị tối ưu theo khuyến cáo, tiên lượng ở bệnh nhân suy tim phân suất tống máu (PSTM) giảm vẫn xấu, với tử vong 5 năm lên đến 75% và tái nhập viện lên đến 82%[40]. Do đó, tình hình thực tế đặt ra vẫn cần nghiên cứu và phát triển thêm các loại thuốc mới nhằm giúp bệnh nhân suy tim có tiên lượng tốt hơn. Trong bài này, chúng tôi tập trung vào các tiến bộ mới về thuốc trong điều trị suy tim PSTM giảm trong thời gian vừa qua, đặc biệt trong giai đoạn năm 2019 – 2020.
Theo các khuyến cáo hiện nay của hội Tim mạch châu Âu cũng như Hội Tim mạch – Trường môn Tim mạch Hoa Kỳ, nền tảng điều trị suy tim PSTM giảm liên quan đến các thuốc ức chế hệ renin – angiotension – aldosterone (RAA) và hệ thần kinh giao cảm, cũng như tăng tác động có lợi của peptide lợi niệu trên hệ tim mạch và thận bằng cách ức chế men neprilysin – là một chất làm mất tác dụng có lợi của peptide lợi niệu. Ngoài ra, ivabradine – một chất ức chế nút xoang giúp làm chậm nhịp xoang – và thuốc dãn mạch hydralazine/ isosorbide dinitrate cũng có vai trò trong từng chỉ định cụ thể điều trị suy tim PSTM giảm[51].Gần đây, các bằng chứng về việc giảm hơn nữa biến cố và tử vong tim mạch ở bệnh nhân suy tim PSTM giảm đã điều trị suy tim chuẩn theo khuyến cáo được báo cáo qua các thử nghiệm lâm sàng của thuốc ức chế SGLT2 (dapagliflozin, empagliflozin), thuốc kích hoạt men guanylate cyclase (vericiguat), thuốc kích hoạt chọn lọc myosin cơ tim (omecamtiv mecarbil)[1],[5],[53].Với lợi ích đối với biến cố và tử vong tim mạch trên bệnh nhân suy tim PSTM giảm, có nhiều kì vọng rằng các thuốc này sẽ được các hiệp hội Tim mạch lớn trên thế giới xem xét và cập nhật trong các khuyến cáo điều trịtrong thời gian sắp tới.
- CON ĐƯỜNG THẦN KINH THỂ DỊCH
Kích hoạt hệ thần kinh thể dịch kéo dài là một cơ chế bệnh sinh quan trọng trong suy tim mạn, nhằm đáp ứng lại tình trạng giảm cung lượng tim và/ hoặc rối loạn đổ đầy của cơ tim. Từ lâu, nó được xem là cơ chế sinh tồn kinh điển đáp ứng với tổn thương cơ tim trải qua tiến hóa hàng ngàn năm để thích ứng với điều kiện môi trường và khí hậu khắc nghiệt[9],[46].Hệ thống này giúp ích cho sinh tồn bằng cách giữ muối nước và co mạch cho cơ thể (ví dụ trong trường hợp chảy máu). Bên cạnh đó, hệ thần kinh thể dịch còn cần thiết cho sự phát triển bình thường của phôi thai[10].
Các tác động lên huyết động của hệ thần kinh thể dịch giúp ích trong giai đoạn đầu suy tim, tuy nhiên khi tình trạng này kéo dài sẽ gây ra rối loạn điều hòa và kích hoạt các phản ứng có hại cho hệ thống tim mạch. Trong đó, hệ giao cảm và hệ RAA là hai hệ thống chính chịu trách nhiệm trong suy tim[24]. Do đó, trong vài thập kỷ vừa qua, các thử nghiệm lâm sàng tập trung vào các thuốc tác động lên hai hệ này, đã giúp các nhà nghiên cứu và thầy thuốc lâm sàng hiểu rõ thêm về ảnh hưởng chúng lên bệnh nhân suy tim (Bảng 2.1).
Ở bệnh nhân suy tim PSTM giảm, ức chế beta, ức chế men chuyển, chẹn thụ thể angiotensin II, lợi tiểu kháng aldosteron, và mới đây là thuốc ức chế thụ thể AGII – neprilysin(ARNI) giúp cải thiện tiên lượng tử vong[39].
Bảng 2.1: Các hệ thống chính trong hệ thần kinh thể dịch và các thuốc lên từng hệ thống trong suytim.
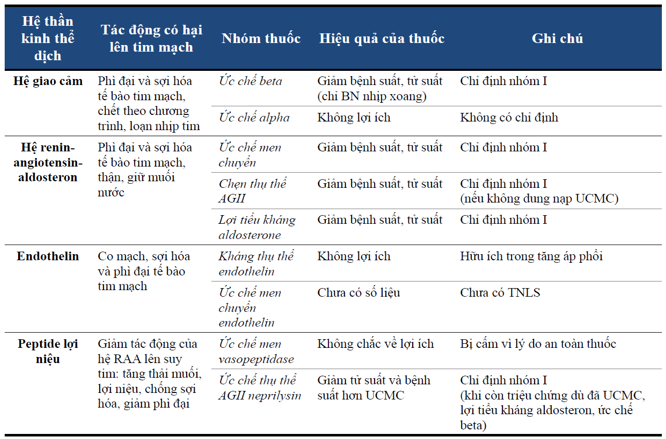
2.1. Hệ giao cảm và thuốc tác động trên hệ giao cảm
Kích hoạt hệ giao cảm giúp tăng thể tích nhát bóp, co mạch ngoại biên để duy trì áp lực tưới máu mô. Tương tác giữa sợi thần kinh giao cảm và hệ tim mạch hình thành thông qua thụ thể adrenergic. Trong suy tim, kích hoạt kéo dài hệ giao cảm do tăng nồng độ catecholamine máu dẫn đến giảm dần mật độ và chức năng của thụ thể beta-1 ở tim theo thời gian, làm cho bệnh tiến triển. Thuốc ức chế thụ thể beta là một thuốc điều trị quan trọng trong suy tim dựa trên các tác động có lợi về tử suất và bệnh suất được tìm thấy ở các thử nghiệm lâm sàng, dù ban đầu các nhà nghiên cứu nghĩ thuốc này chống chỉ định trong điều trị suy tim[22].Lợi ích của ức chế beta là do giảm nhịp tim và nhu cầu oxy cơ tim, giảm loạn nhịp tim và đột tử, và giảm tần suất thiếu máu cơ tim. Những cơ chế tác động vào bệnh học suy tim, giúp cân bằng hệ thần kinh tự động và thần kinh thể dịch dẫn đến những lợi ích rõ ràng cho nhóm bệnh nhân: suy tim PSTM giảm với nhịp xoang, ức chế beta làm giảm 24% tử vong do mọi nguyên nhân và tỉ lệ nhập viện[23]. Hiện nay, có 4 thuốc ức chế beta được chấp thuận đưa vào khuyến cáo điều trị suy tim đó là bisoprolol, metaprolo, carvedilol và nebivolol[39].
Gần đây các báo cáo mới thấy rằng lợi ích của ức chế beta trong suy tim PSTM giảm không thấy rõ ràng trên bệnh nhân có kèm theo rung nhĩ [20],[22]. Vai trò của hệ thần kinh tự động trong sinh bệnh học rung nhĩ rất phức tạp, liên quan đến điều hòa đáp ứng cả hệ giao cảm lẫn phó giao cảm. Khi bệnh nhân suy tim PSTM giảm xuất hiện rung nhĩ, hoạt tính giao cảm trung ương tăng lên, nhưng đáp ứng giao cảm với gắng sức lại giảm[16]. Những quan sát này dấy lên khả năng rằng ức chế beta không giúp giảm tử vong trong suy tim kèm rung nhĩ có lẽ liên quan đến sự khác biệt trong chức năng thần kinh tự chủ, và hệ quả là của hệ thần kinh thể dịch. Lập luận này được ủng hộ bởi có nghiên cứu quan sát thấy rằng nhịp tim có kết hợp với tử vong trong suy tim PSTM giảm có nhịp xoang, nhưng không liên quan nhau trong trường hợp suy tim kèm rung nhĩ[11].
2.2. Hệ renin- angiotensin- aldosterone và thuốc tác động trên hệ này
Hệ renin- angiotensin- aldosterone là một hệ thống thần kinh thể dịch phức tạp. Angiotensin II (AGII) và aldosterone là chất trung gian của các phản ứng bất lợi khi bị kích hoạt kéo dài, bao gồm giữ muối nước, co mạch ngoại biên dẫn đến tăng huyết áp, phì đại và sợi hóa cơ tim, thận và mạch máu. Thuốc ức chế hệ RAA đầu tiên được tìm ra cuối thập niên 80 của thế kỷ trước, đó là ức chế men chuyển (UCMC) với nhiều thử nghiệm lâm sàng chứng minh được lợi ích giảm tử vong của nó[13]. Thuốc chẹn thụ thể AGII được khuyến cáo sử dụng khi bệnh nhân không dung nạp UCMC.
Renin nằm trước men chuyển AGII trong con đường RAA, điều hòa các bước tạo ra AGII có hoạt tính sinh học. Thuốc ức chế bước đầu tiên trong con đường RAA từng được nghĩ là có tiềm năng có ích lợi cho bệnh nhân suy tim nhiều hơn UCMC. Tuy nhiên, nghiên cứu ATMOSPHERE (Aliskiren Trial to Minimize OutcomeS in Patients with HEart failuRE) thấy rằng thêm aliskiren vào enelapril lại làm tăng biến cố xấu mà không có lợi ích gì thêm[28]. Thiết kế nghiên cứu này không so sánh giữa đơn trị liệu aliskiren với enelapril. Một số nghiên cứu khác đã đi tìm liệu rằng có lợi ích không khi chặn con đường RAA ở nhiều cấp độ (không chỉ trong suy tim mà còn các bệnh lý tim mạch khác) đã thất bại trong việc thấy lợi ích của tác động kép trên hệ RAA[15],[34]. Do đó, dường như rằng chẹn con đường RAA với một thuốc (ví dụ liều tối đa UCMC) là đủ bảo đảm tác động chẹn tín hiệu AGII, cho dù phối hợp thêm aliskiren hay chẹn thụ thể AGII cũng không tăng lợi ích mà còn gây ra các tác dụng có hại.
Ngoài AGII, aldosterone gây sợi hóa và phì đại tim thận, và thường thoát khỏi chẹn đường RAA nếu chỉ ức chế men chuyển một mình[14]. Các nghiên cứu lâm sàng đã thấy rằng lợi tiểu kháng aldosterone có thể cải thiện tiên lượng sống còn khi thêm vào điều trị suy tim chuẩn với UCMC và ức chế beta[36]. Thuốc đối kháng aldosterone có khả năng chống lại sợi hóa ở tim, thận, mạch máu, phổi. Tuy nhiên, dù khuyến cáo mức I nhưng nó vẫn ít được dùng trên lâm sàng hàng ngày do lo ngại tác động xấu trên chức năng thận và kali máu của thuốc. Hiện nay, sau kết quả khả quan từ các nghiên cứu tiền lâm sàng, thuốc đối kháng aldosterone không steroid (Finerenone) đã được nghiên cứu trong thử nghiệm lâm sàng pha IIb ARTS-HF (the MinerAlocorticoid Receptor antagonist Tolerability Study – Heart Failure) so sánh finerenone với eplerenone. Thuốc này dung nạp tốt, giảm nguy cơ gây tăng kali máu cũng như suy thận ở bệnh nhân suy tim[12].
2.3. Thuốc tác động kép ức chế neprilysin và chẹn thụ thể AGII
Hệ peptide lợi niệu giúp thải muối và nước ra khỏi cơ thể, giúp hạ huyết áp. Trong suy tim, hệ này cũng tương tác với hệ giao cảm và RAA, do đó giảm mức độ phì đại và sợi hóa của tim mạch và thận, tình trạng viêm và tân sinh mạch máu [38]. Thủy phân các peptide lợi niệu bởi men metallopeptidase neprilysin là cơ chế thoái giáng của các peptide lợi niệu, vì vậy thuốc đánh vào neprilysin được đề nghị như là một phương án giúp phục hồi hay tăng hoạt tính có lợi của các peptide lợi niệu. Thuốc chỉ đơn thuần ức chế một mình neprilysin không cho thấy hiệu quả ở người[47]. Ngoài neprilysin gắn vào màng tế bào, còn có dạng tự do và có hoạt tính trong máu của bệnh nhân suy tim [6]. Việc hiểu thêm về cơ chế phân tử của suy tim giúp các nhà nghiên cứu nhận ra rằng để đạt được các lợi ích của việc ức chế neprilysin, hệ RAA cũng cần được ức chế đồng thời [27].
Omapatrilat – một thuốc ức chế vasopeptidase – đã được làm nhiều thử nghiệm lâm sàng đánh giá hiệu quả điều trị trong suy tim và tăng huyết áp. Omapatrilat cho thấy tác động hạ áp mạnh hơn so với enalapril trong nghiên cứu OCTAVE (n=25,302) [21]. Trong nghiên cứu pha IIb IMPRESS, omapatrilat giảm biến cố lâm sàng gộp (tử vong mọi nguyên nhân, nhập viện do suy tim) so với lisinopril[37].Tuy nhiên, nghiên cứu pha III OVERTURE sau đó lại không thấy được lợi ích giảm kết cục chính[33]. Quan trọng nữa là tỉ lệ bệnh nhân bị tác dụng phụ ngoại ý phù mạch trong các thử nghiệm trên lại cao đáng kể, do sự tích tụ bradykinin, dẫn đến việc các nghiên cứu tiếp sau về omapatrilat và các ức chế vasopeptidase khác đã bị dừng lại[29].
Một nỗ lực khác là nghiên cứu về kết hợp đồng thời giữa ức chế neprilysin và chẹn thụ thể AGII (the angiotensin receptor neprilysin inhibitors – ARNIs). Khi dùng chẹn thụ thể AGII thay vì UCMC, ARNI giúp tránh được vấn đề phù mạch do tích tụ bradykinin. Sacubitril/ valsartan, thuốc đầu tiên trong ARNI, đã được kiểm nghiệm trong điều trị suy tim và tăng huyết áp. Nghiên cứu PARADIGM-HF đánh giá sacubitril/valsartan so với enalapril trong điều trị suy tim PSTM giảm.Thử nghiệm này kết thúc sớm do lợi ích rõ rệt của thuốc mới. So với enelapril, sacubitril/valsartan giảm kết cục gộp chính gồm tử vong tim mạch và nhập viện do suy tim 20%. Ngoài ra, thuốc cũng giúp giảm các tiêu chí khác như thời gian đến lúc bị biến cố xấu hay tái nhập viện 30 ngày (bất kể tuổi, PSTM, rung nhĩ)[4]. Các nghiên cứu cơ bản cho thấy rằng sacubitril/valsartan giúp bảo vệ tổn thương tế bào cơ tim do AGII, phì đại và sợi hóa cơ tim hơn là chỉ ức chế hệ RAA đơn thuần[48].Tuy nhiên, đối với suy tim PSTM bảo tồn, nghiên cứu pha III PARAGON-HF lại thất bại trong chứng minh lợi ích của sacubitril/valsartan so với valsartan trong giảm tỉ lệ nhập viện do suy tim và tử vong tim mạch [41].
2.4. Các hệ thần kinh thể dịch khác có thể có tác động quan trọng trong suy tim
Endothelin-1, là 1 đồng phân chính của gia đình peptide endothelin trong hệ tim mạch, là 1 chất co mạch mạnh với tiềm năng gây phì đại, xơ hóa và khả năng gây phân bào đối với tế bào cơ tim và mạch máu. Kích hoạt endothelin trong suy tim gây rối loạn cân bằng nội môi của muối và nước, kích hoạt hệ RAA và giao cảm, gây co mạch, trực tiếp làm xấu đi diễn tiến bệnh tim và suy giảm chức năng thận[19]. Nồng độ endothelin-1 trong máu liên quan trực tiếp với tử suất và bệnh suất[25]. Cho đến thời điểm hiện tại, trừ các nghiên cứu trong tăng áp phổi, đa số các thử nghiệm lâm sàng lớn về thuốc đối kháng endothelin đều thất bại trong việc giảm biến cố lâm sàng[18].
Các hormon thần kinh thể dịch khác có vai trò trong sinh lý bệnh của suy tim là adrenomedullin, bradykinin, serotonin, and urotensin-II. Nhưng vai trò của chúng trong suy tim vẫn chưa được hiểu rõ, và cũng chưa có thuốc nào tác động lên chúng tiến được đến giai đoạn thử nghiệm lâm sàng.
- CON ĐƯỜNG ỨC CHẾ SGLT2
Nhóm thuốc ức chế SGLT2 được phát triển để điều trị tăng đường huyết ở bệnh nhân đái tháo đường típ 2 (ĐTĐ2), bằng cách ức chế tái hấp thu glucose tại ống lượn gần của thận. Nhiều thử nghiệm lâm sàng đã được tiến hành nhằm đánh giá hiệu quả và an toàn của nhóm thuốc này ở nhóm bệnh nhân ĐTĐ2 (có kèm bệnh tim mạch sẵn có, nhiều yếu tố nguy cơ tim mạch, hoặc suy thận) và nhóm bệnh nhân suy tim PSTM giảm (có hoặc không ĐTĐ2 kèm theo)[5],[30],[35],[49],[52],[53].
Kết quả từ nghiên cứu EMPA-REG OUTCOME (Empagliflozin Cardiovascular Outcomes Event Trial in Type 2 Diabetes Mellitus Patients—Removing Excess Glucose) cho thấy empagliflozin giúp bệnh nhân ĐTĐ2 kèm nguy cơ tim mạch cao giảm sớm nguy cơ bị biến cố chính về tim mạch và thận, bao gồm giảm đáng kể tử vong tim mạch và nhập viện do suy tim[53]. Những thử nghiệm lâm sàng lớn sau đó với các thuốc ức chế SGLT2 khác như canagliflozin (CANVAS và CREDENCE) và dapagloflozin (DECLARE-TIMI 58), cũng đã báo cáo các kết quả tích cực tương tự trong cả phòng ngừa tiên phát và thứ phát cho bệnh nhân ĐTĐ2. [30],[35],[49]
Trong khi các nghiên cứu đi trước đã cung cấp bằng chứng vững chắc ủng hộ nhóm ức chế SGLT2 có khả năng ngăn ngừa suy tim mới mắc ở bệnh nhân ĐTĐ2, vẫn còn 2 câu hỏi quan trọng chưa được trả lời. Thứ nhất, liệu rằng những trị liệu này có thể áp dụng cho trường hợp suy tim hiện mắc; và thứ hai, liệu rằng nhóm này có giúp ích cho nhóm bệnh nhân suy tim mà không kèm ĐTĐ2 không?
Bảng 3.1: Các thử nghiệm lâm sàng đánh giá khả năng bảo vệ tim mạch
của nhóm ức chế SGLT2 đối với các bệnh nhân ĐTĐ2 có nguy cơ tim mạch cao[52].
| Thử nghiệm | Năm công bố | Thuốc | N | Tiền căn suy tim (%) | Kết cục chính | Năm theo dõi | Số nhập viện
do suy tim mỗi 1000 BN-Năm |
Nhập viện do suy tim
HR (KTC 95%) |
|
| Ức chế SGLT2 | Giả dược | ||||||||
| EMPA-REG OUTCOME | 2015 | Empagliflozin | 7020 | 10.1 | Biến cố tim mạch chính | 3.1 | 9.4 | 14.5 | 0.65
(0.50-0.85) |
| CANVAS/
CANVAS-R |
2017 | Canagliflozin | 10,142 | 14.4 | Biến cố tim mạch chính | 2.4 | 5.5 | 8.7 | 0.67
(0.52-0.87) |
| DECLARE
-TIMI 58 |
2019 | Dapagliflozin | 17,160 | 10 | Biến cố tim mạch chính
Tử vong tim mạch hay nhập viện vì suy tim |
4.2 | 4.2 | 8.5 | 0.73
(0.61-0.88) |
| VERTIS-CV | Đang tiến hành | Ertugliflozin | 8238 | 23.1 | Biến cố tim mạch chính | Đang tiến hành | |||
CANVAS = Canagliflozin Cardiovascular Assessment Study; CANVAS-R = CANVAS-Renal; CI = confidence interval; CV = cardiovascular; CVOT = CV outcomes trial; DECLARE-TIMI 58 = Dapagliflozin Effect on Cardiovascular Events−Thrombolysis in Myocardial Infarction 58
Một phân tích gộp được thực hiện gần đây trên dữ liệu từ 3 thử nghiệm lâm sàng (EMPA-REG, CANVAS, DECLARE-TIMI 58) về hiệu quả bảo vệ tim mạch của nhóm ức chế SGLT2, bao gồm 34,322 bệnh nhân (60% có kèm bệnh tim mạch trước đó) (Hình 3.1). Trong suốt thời gian theo dõi, 3342 biến cố tim mạch chính và 2028 tử vong tim mạch hay nhập viện vì suy tim đã xảy ra. Đáng chú ý, mặc dù cả 3 thuốc ức chế SGLT2 giảm biến cố tim mạch chính 11% nhưng lợi ích này chỉ được thấy có ý nghĩa thống kê trong nhóm bệnh nhân có bệnh tim mạch biết trước. Ngược lại, nhóm thuốc này lại giảm nguy cơ gộp giữa tử vong tim mạch hay nhập viện vì suy tim đến 23%, bất kể có kèm bệnh lý tim mạch hay suy tim trước đó không. Điều trị với ức chế SGLT2 cho thấy lợi ích trên tiêu chí nhập viện do suy tim thể hiện rõ rệt nhất ở nhóm có bệnh thận mạn[52].
Hình 3.1: Phân tích gộp các thử nghiệm lâm sàng về tác động của nhóm thuốc ức chế SGLT2 lên tiêu chí nhập viện vì suy tim và tử vong tim mạch.[52]
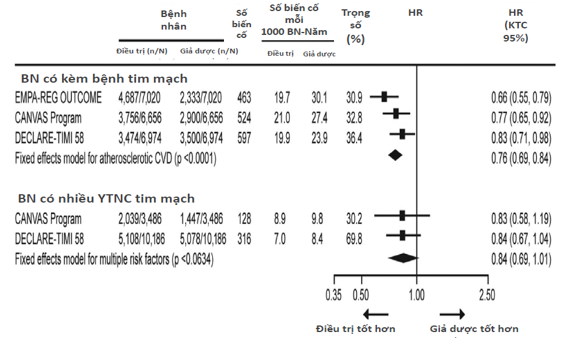
Như đã thấy trong bảng 3.1 tổng hợp 3 thử nghiệm lâm sàng EMPA-REG OUTCOME, CANVAS, DECLARE TIMI 58, tỉ lệ bệnh nhân có suy tim từ 10-14%, việc giảm số biến cố suy tim quan sát được trong các nghiên cứu chủ yếu thể hiện việc ngăn ngừa các trường hợp suy tim mới mắc ở bệnh nhân không có suy tim lúc ban đầu, hơn là việc giảm biến cố suy tim nặng lên ở những bệnh nhân đang bị suy tim. Đáng chú ý, nhóm ức chế SGLT2 không làm hạ đường huyết quá mức ở người không bị ĐTĐ2. Thêm vào đó, lợi ích đa tác động lên nhiều hệ cơ quan của nhóm thuốc này – bao gồm lợi niệu, hạ áp, tác động lên trục RAA, bảo tồn chức năng thận, tăng tạo erythropoetin, giảm viêm và stress oxy hóa, tăng chuyển hóa và năng lượng cơ tim – được mong đợi giúp ích cho bệnh nhân suy tim bất kể tình trạng đường huyết[26].
Điều này dẫn dến câu hỏi liệu rằng nhóm ức chế SGLT2 có được xem là một nhóm thuốc trong điều trị suy tim (bất kể tình trạng ĐTĐ2) hay không? Hiện nay có vài nghiên cứu lâm sàng đang được tiến hành nhằm trả lời câu hỏi quan trọng này, trong đó một số đã được công bố với dấu hiệu tích cực (Bảng 3.2). Bất kể thuốc nào được nghiên cứu, mỗi thử nghiệm của ức chế SGLT2 trong suy tim đều đánh giá cùng kết cục chính là tử vong tim mạch, suy tim (nhập viện hay phải đi khám sớm so với lịch hẹn). Chúng cũng lượng giá trên một phổ rộng bệnh nhân có chức năng thận dao động từ trên 20 mL/phút/1.73m2 da đến chức năng thận bình thường.
Bảng 3.2: Những thử nghiệm lâm sàng đánh giá hiệu quả bảo vệ tim mạch của nhóm ức chế SGLT2 ở nhóm bệnh nhân suy tim cấp hay mạn kèm hoặc không kèm ĐTĐ2.
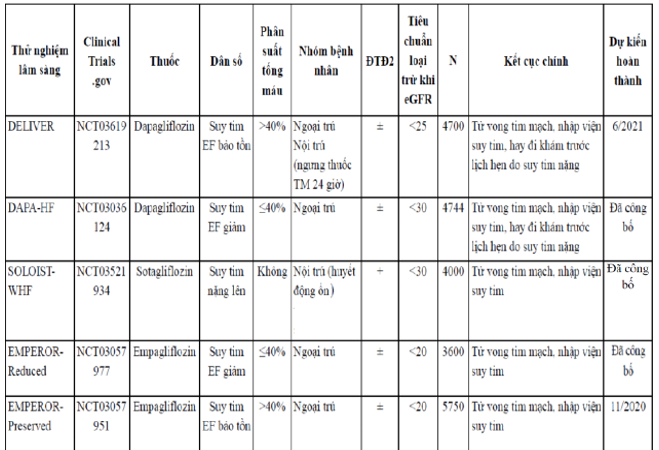
DAPA-HF = Dapagliflozin and Prevention of Adverse Outcomes in Heart Failure; DELIVER = Dapagliflozin Evaluation to Improve the Lives of Patients with Preserved Ejection Fraction Heart Failure; EF = ejection fraction; eGFR = estimated glomerular filtration rate; EMPEROR = Empagliflozin Outcome Trial in Patients with Chronic Heart Failure; SOLOIST-WHF =the Effect of Sotagliflozin on Cardiovascular Events in Patients with Type 2 Diabetes Post Worsening Heart Failure study
Nghiên cứu đầu tiên trong nhóm là DAPA-HF gần đây đã công bố kết quả vào tháng 11 năm 2019 trên The New England Journal of Medicine. Đây là một thử nghiệm lâm sàng ngẫu nhiên có đối chứng pha 3 trên 4744 bệnh nhân suy tim PSTM giảm (PSTM ≤40%) với phân độ NYHA II-IV. Bệnh nhân được dùng hoặc dapagliflozin 10mg hoặc giả dược trên nền điều trị chuẩn suy tim. Tiêu chí chính của nghiên cứu là tiêu chí gộp giữa suy tim nặng lên (nhập viện hoặc đi khám sớm do suy tim cần dùng lợi tiểu đường tĩnh mạch) hoặc tử vong tim mạch. Sau 18.2 tháng, kết cục chính xảy ra ở 16.3% nhóm dapagliflozin và 21.2% nhóm giả dược (HR 0.74; KTC95% [0.65 to 0.85];P<0.001). Suy tim nặng lên lần đầu ở 10% nhóm dapagliflozin so với 13.7% nhóm giả dược (HR 0.7; KTC95% [0.59-0.83]). Tử vong tim mạch xảy ra ở 9.6% trong nhóm dapagliflozin và 11.5% trong nhóm giả dược (HR 0.82; KTC95% [0.69-0.98]); 11.6% và 13.9% tương ứng đối với tiêu chí tử vong do mọi nguyên nhân (HR 0.83; KTC95% [0.71-0.97])(Hình 3.2)[5].
Hình 3.2: Kết cục tim mạch của bệnh nhân trong nghiên cứu DAPA-HF.[5]
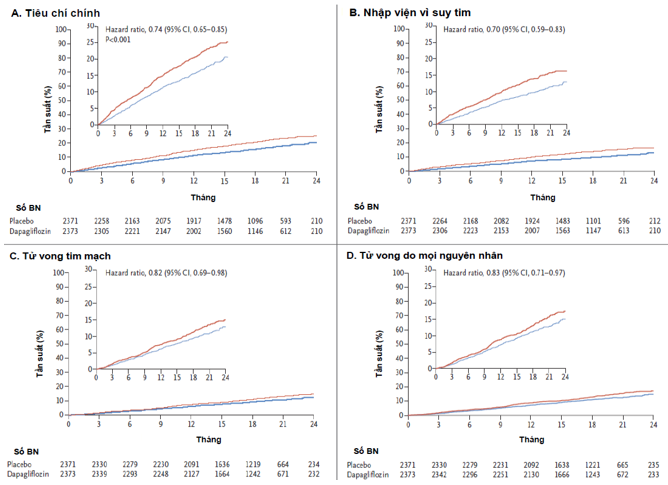
Kết quả từ nghiên cứu này cho thấy hiệu quả của dapagliflozin trong việc giúp giảm rõ rệt trong tiêu chí gộp chính (tử vong tim mạch hay nhập viện vì suy tim hay khám sớm vì suy tim) và tử vong do mọi nguyên nhân với dapagliflozin so với giả dược ở 4744 bệnh nhân suy tim PSTM giảm. Quan trọng là lợi ích điều trị rõ ràng trên mọi đối tượng bệnh nhân (độ tuổi, tổng trạng sức khỏe, và thuốc nội khoa nền tảng), và đặc biệt là bất kể bệnh nhân có tình trạng ĐTĐ2 hay không. Bên cạnh đó, tác dụng ngoại ý liên quan đến giảm thể tích tuần hoàn, rối loạn chức năng thận, hạ đường huyết không khác biệt giữa 2 nhóm điều trị[5].
Nghiên cứu EMPEROR-Reduced cũng vừa được công bố vào cuối tháng 8 năm 2020 trên The New England Journal of Medicine. Đây là một thử nghiệm ngẫu nhiên mù đôi, đối chứng giữa empagliflozin và giả dược (theo tỉ lệ 1:1) trên nền điều trị chuẩn suy tim ở bệnh nhân suy tim PSTM giảm (PSTM ≤40%), lâm sàng ổn định, có hoặc không kèm ĐTĐ2. Có 3730 bệnh nhân tham gia nghiên cứu và được theo dõi trong 16 tháng. Kết quả chính của nghiên cứu được trình bày trong Bảng 3.3[32].
Bảng 3.3: Kết cục lâm sàng giữa 2 nhóm trong nghiên cứu EMPEROR-Reduced
| Kết cục lâm sàng | Empagliflozin (n=1863) | Giả dược (n=1867) | HR
(KTC 95%); P |
||
| Số BN
(%) |
Số biến cố mỗi 100 Bệnh nhân-Năm | Số BN
(%) |
Số biến cố mỗi 100 Bệnh nhân-Năm | ||
| Tiêu chí chính (tử vong tim mạch hoặc nhập viện do suy tim) | 361
(19.4) |
15.8 | 462
(24.7) |
21.0 | 0.75
(0.65 – 0.86); <0.001 |
| Tử vong tim
mạch |
187
(10.0) |
7.6 | 202
(10.8) |
8.1 | 0.92
(0.75 – 1.12) |
| Nhập viện do
suy tim |
246
(13.2) |
10.7 | 342
(18.3) |
15.5 | 0.69
(0.59 – 0.81) |
| Tổng cộng số nhập viện do suy tim | 388 | – | 553 | – | 0.70
(0.58 – 0.85); <0.001 |
| Tử vong do bất kỳ nguyên nhân | 249
(13.4) |
10.1 | 266
(14.2) |
10.7 | 0.92
(0.77 – 1.1) |
| Thay đổi trong điểm chất lượng sống KCCQ tại tuần 52 | 5.8 ± 0.4 | – | 4.1±0.4 | – | 1.7
(0.5 – 3.0) |
| Kết cục gộp về thận (*) | 30 (1.6) | 1.6 | 58 (3.1) | 3.1 | 0.50
(0.32 – 0.77) |
| Biến đổi GFR/ năm | –0.55 ± 0.23 | – | –2.28 ± 0.23 | – | 1.73
(1.10 – 2.37) |
(*) Kết cục gộp về thận, bao gồm: chạy thận nhân tạo định kỳ; ghép thận; hoặc giảm ≥40% GFR kéo dài; hoặc GFR < 15 mL/phút/1.73m2 da kéo dài đối với người có chức năng thận nền tảng ≥30 mL/phút/1.73m2 da hay GFR < 10 mL/phút/1.73m2 da kéo dài đối với người có chức năng thận nền tảng <30 mL/phút/1.73m2 da
Qua kết quả của nghiên cứu này, thấy được rằng empagliflozin giúp cải thiện tiên lượng bệnh nhân suy tim PSTM giảm với lâm sàng ổn định trên nền tảng điều trị suy tim chuẩn theo khuyến cáo hiện hành, bất kể có kèm theo tình trạng tiểu đường hay không. Lợi ích đạt được chủ yếu là do thuốc giúp cải thiện rõ rệt nhập viện do suy tim. Bên cạnh đó, còn có lợi ích đạt được trên tiêu chí thận [32].
Cũng như nghiên cứu DAPA-HF đối với dapagliflozin, nghiên cứu EMPEROR-Reduced cũng có một nửa dân số là không mắc ĐTĐ2. Tuy nhiên, bệnh nhân trong nghiên cứu này có suy tim nặng hơn (PSTM 27% so với 31%, NT-proBNP 1907 so với 1437 của DAPA-HF), trên 70% bệnh nhân suy tim của EMPEROR-Reduced có PSTM ≤30%. Cũng như DAPA-HF, tiêu chí chính về tử vong tim mạch và suy tim cần nhập viện thấp hơn trong nhóm điều trị, và một lần nữa thấy rằng lợi ích này đạt được với thuốc ức chế SGLT2 bất kể bệnh nhân có tiểu đường kèm theo hay không. Tuy nhiên, khi phân tích từng tiêu chí thì có sự khác biệt trong 2 nghiên cứu, trong DAPA-HF HR cho tử vong tim mạch là 0.82 [0.69-0.98] có ý nghĩa thống kê; ngược lại trong EMPEROR-Reduced HR là 0.92 [0.75-1.12]. Liệu rằng có sự khác biệt trong tác dụng lên các tiêu chí tim mạch của 2 thuốc này? Có nhiều khả năng giải thích sự khác biệt này, tuy nhiên cần có một nghiên cứu đối đầu mới có thể trả lời rõ ràng cho câu hỏi này [17].
Khi một điều trị suy tim mới được tìm ra, điều quan trọng cần biết nữa là liệu rằng nó có cung cấp thêm lợi ích cho những điều trị nền tảng hiện có hay không. Câu hỏi này đặc biệt được quan tâm đối với sacubitril-valsartan, một thuốc đang được áp dụng chậm rãi trong thực hành lâm sàng dù FDA chấp thuận lưu hành năm 2015, khuyến cáo ở mức I năm 2016[50]. Ở DAPA-HF, chỉ 10.7% bệnh nhân dùng sacubitril-valsartan; đối với EMPAROR-Reduced là 19.5%. Trong cả 2 nghiên cứu, phân tích dưới nhóm cho thấy rằng lợi ích của ức chế SLGT2 là độc lập với việc có hay không sử dụng sacubitril-valsartan trước đó. Những kết quả từ EMPEROR-Reduced đã khẳng định lại những phát hiện từ nghiên cứu DAPA-HF và củng cố mạnh thêm lập luận dùng ức chế SGLT2 cho bệnh nhân suy tim PSTM giảm là có ích lợi.
Trong khi các nghiên cứu trước cho thấy các thuốc SGLT2 như dapagliflozin, empagliflozin giúp giảm suy tim ở bệnh nhân suy tim ổn định[5],[32], tuy nhiên hiệu quả và độ an toàn của nhóm thuốc này khi khởi động sớm ngay sau đợt suy tim mất bù cấp vẫn chưa rõ. Nghiên cứu SOLOIST-WHF (The Effect of Sotagliflozin on Cardiovascular Events in Patients with Type 2 Diabetes Post Worsening Heart Failure study) được tiến hành nhằm đánh giá hiệu quả của sotagliflozin – là loại thuốc uống ức chế cả SGLT1 và 2 – khi sử dụng sớm sau khi vừa ổn định tình trạng suy tim cấp (5/6 bệnh nhân là suy tim PSTM <50%). Đây là một thử nghiệm lâm sàng ngẫu nhiên, mù đôi, đa trung tâm trên các bệnh nhân đái tháo đường típ 2 nhập viện vì suy tim nặng lên. Suy tim cấp ổn định được định nghĩa là không cần thở oxy, huyết áp tâm thu ≥100 mmHg, cai vận mạch hay dãn mạch (trừ nitrate), và đã chuyển từ lợi tiểu chích sang đường uống. Bệnh nhân thỏa tiêu chuẩn được dùng sotagliflozin 200 – 400 mg hoặc giả dược trong vòng 3 ngày trước xuất viện. Kết cục chính là tử vong do nguyên nhân tim mạch và nhập viện do suy tim. Tuy nhiên, giai đoạn thu nhận bệnh nhân của nghiên cứu này kết thúc sớm do bị cắt nguồn tài trợ[7].
Hình 3.3: Đường Kaplan-Meier biểu diễn biến cố chính của sotagliflozin so với giả dược [7]
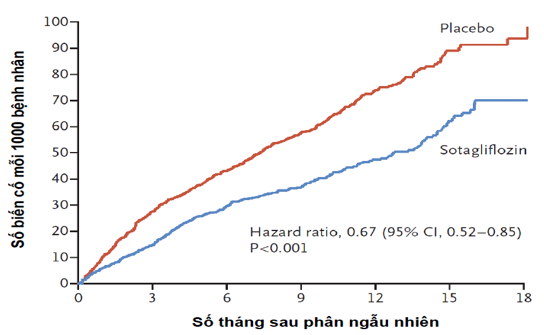
Qua nghiên cứu, thấy được ở bệnh nhân tiểu đường bị suy tim mất bù cấp, sử dụng sotagliflozin giúp giảm 33% kết cục xấu cho bệnh nhân là số tử vong tim mạch và nhập viện do suy tim (HR 0.67, KTC95% [0.52 – 0.85]). Khởi động sớm sotagliflozin sớm sau khi ổn định tình trạng suy tim giúp tăng cơ hội cải thiện tiên lượng cho người bệnh, thể hiện qua đường biểu diễn Kaplan-Meier tách ra sớm và rõ rệt từ tháng thứ 3 sau dùng thuốc[7]. Nghiên cứu SOLOIST-WHF ban đầu dự định đánh giá hiệu quả cả trên nhóm suy tim PSTM bảo tồn, nhưng do bị kết thúc sớm vì bị cắt tài trợ, cỡ mẫu trên nhóm bệnh nhân này tương đối nhỏ. Thế nên, khó có thể rút ra kết luận rõ ràng về hiệu quả của sotagliflozin trên suy tim PSTM bảo tồn. Các thử nghiệm lâm sàng song song khác là DELIVER (dapagliflozin) và EMPEROR-Preserved (empagliflozin) sẽ đánh giá tác động của ức chế SGLT2 trên tiêu chí lâm sàng khác như chất lượng cuộc sống và khoảng cách đi bộ 6 phút, tập trung lên nhóm suy tim mạn có PSTM bảo tồn kèm hay không kèm ĐTĐ2, dự kiến sẽ công bố trong thời gian sắp tới, sẽ giúp mở rộng thêm hiểu biết y khoa về điều trị trong suy tim PSTM bảo tồn.
Đến thời điểm hiện tại, Cục quản lý thực phẩm và dược phẩm Hoa Kỳ (FDA) đã chấp thuận công nhận thuốc dapagliflozin cho chỉ định điều trị suy tim PSTM giảm (bất kể tình trạng ĐTĐ2 kèm theo), đánh dấu 1 bước ngoặc trong điều trị suy tim, đây là lần đầu tiên một thuốc trị tiểu đường được cấp phép trong điều trị bệnh lý suy tim, thậm chí không có hiện diện của tình trạng tiểu đường. Tuy nhiên, sotagliflozin vẫn chưa được FDA phê duyệt trong điều trị ĐTĐ2.
Với bằng chứng vững chắc từ 2 nghiên cứu DAPA-HF và EMPEROR-Reduced, các khuyến cáo sẽ cần phải cập nhật những thay đổi quan trọng mới này. Hiện tại, Hội Tim mạch Canada và Hội suy tim Canada đã đưa khuyến cáo dùng thuốc ức chế SGLT2 cho bệnh nhân suy tim PSTM giảm (≤40%) có triệu chứng nhẹ – trung bình để cải thiện triệu chứng, nâng cao chất lượng sống, giảm nguy cơ nhập viện và tử vong tim mạch[31].
Vì có tính chất gây lợi niệu, do đó khuyến cáo hiện tại chỉnh liều lợi tiểu khi bệnh nhân dùng ức chế SGLT2 vẫn chưa rõ. Tương tự, với tác động trên huyết động dù ở mức độ nhẹ, nhưng việc sử dụng và vấn đề dung nạp của thuốc này đối với các bệnh nhân điều trị chuẩn suy tim vẫn cần được đánh giá kỹ lưỡng hơn trong các nghiên cứu tương lai.
- CON ĐƯỜNG KÍCH HOẠT MEN GUANYLATE CYCLASE
Vericiguat, được giới thiệu bởi công ty dược phẩm Bayer Healthcare and Merck, là 1 thuốc đường uống, có chức năng như 1 chất kích hoạt men guanylate cyclase hòa tan (soluble guanylate cyclase) ở bệnh nhân suy tim PSTM giảm. Thông qua việc kích hoạt men guanylate cyclase, vericiguat sẽ làm tăngGMP vòng (cGMP) nội bào và phục hồi độ nhạy cảm của nitric oxide, từ đó giúp dãn mạch, giảm độ co và độ cứng của thành động mạch.
4.1. Cơ chế tác động
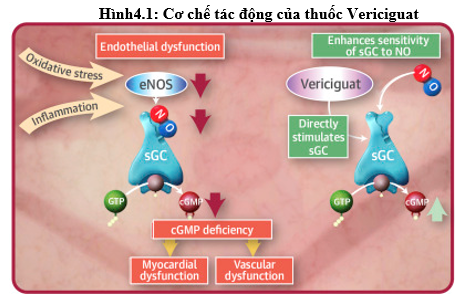 Bình thường, phân tử nitric oxide đi vào trong tế bào nội mạch mạch máu, gắn vào men guanlylate cyclase, làm men này chuyển GTP (guanosine triphosphate) thành GMP vòng (cyclic guanosine monophosphate). GMP vòng khi tạo thành sẽ tác động có lợi đến nhiều cơ quan trong cơ thể, mà cụ thể ở đây là hệ tim mạch. Nó gây dãn mạch nhằm cải thiện chức năng nội mạc, giảm sợi hóa và tái cấu trúc cơ tim.
Bình thường, phân tử nitric oxide đi vào trong tế bào nội mạch mạch máu, gắn vào men guanlylate cyclase, làm men này chuyển GTP (guanosine triphosphate) thành GMP vòng (cyclic guanosine monophosphate). GMP vòng khi tạo thành sẽ tác động có lợi đến nhiều cơ quan trong cơ thể, mà cụ thể ở đây là hệ tim mạch. Nó gây dãn mạch nhằm cải thiện chức năng nội mạc, giảm sợi hóa và tái cấu trúc cơ tim.
Tuy nhiên, suy tim là tình trạng trong đó có sự hiện diện của viêm mạn tính và stress oxide hóa, gây ra sự rối loạn chức năng nội mạc và giảm sự tạo thành nitric oxide. Khi có hiện diện của tình trạng stress oxide hóa trong suy tim sẽ làm giảm lượng cũng như độ nhạy cảm của nitric oxide, từ đó giảm hoạt tính của men guanylate cyclase dẫn đến mất tác dụng dãn mạch có lợi, cụ thể là làm tăng trương lực mạch máu hệ thống cũng như phổi, làm tăng gánh nặng thêm cho cơ tim của bệnh nhân suy tim[42].
Thuốc vericiguat tác động như một chất tác động kích thích trực tiếp men guanylate cyclase, độc lập với sự hiện diện của nitric oxide. Do đó, nó trực tiếp làm tăng lượng GMP vòng cũng như tăng tính nhạy cảm của nitric oxide, giúp duy trì các tác dụng có lợi trên hệ tim mạch sau đó.
4.2 Các thử nghiệm lâm sàng
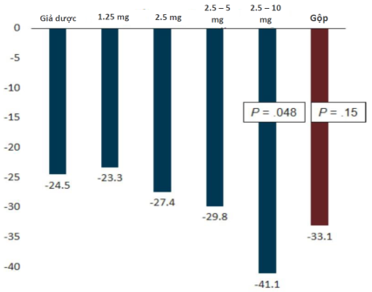
SOCRATES- REDUCED là 1 thử nghiệm lâm sàng ngẫu nhiên có đối chứng pha 2b trên 456 bệnh nhân suy tim PSTM< 45% và có đợt cấp suy tim mạn trong 4 tuần gần đây (định nghĩa là có triệu chứng suy tim sung huyết, khó thở cần nhập viện hoặc phải dùng lợi tiểu đường tĩnh mạch, và tăng peptide lợi niệu). Các bệnh nhân được phân nhóm ngẫu nhiên điều trị với giả dược (n=92) hoặc vericiguat liều 1,25, 2.5, 5 và 10mg (n=91 mỗi nhóm, trong đó nhóm 2.5, 5 và 10mg đều khởi đầu từ 1.25mg và tăng dần đến khi đạt liều đích) trên nền tảng thuốc nội khoa tối ưu theo khuyến cáo. Khi phân tích tiêu chí chính là cải thiện NT-proBNP sau 12 tuần điều trị thì thấy rằng không có sự khác biệt có ý nghĩa thống kê giữa thuốc vericiguat nói chung khi gộp chung các liều so với giả dược (P=0.15). Tuy nhiên, khi phân tích từng liều vericiguat so với placebo, liều 10mg kết hợp với mức độ cải thiện NTproBNP rõ rệt nhất, còn các liều còn lại thì không cho thấy sự khác biệt so với placebo (Hình 4.2). Trong khi đó, PSTM cải thiện nhiều hơn tại thời điểm tuần 12 trong nhóm vericiguat 10mg so với placebo (3.7% so với 1.5%). Nhập viện do suy tim tại thời điểm tuần 12 thấp hơn trong nhóm 5mg và 10mg (9.9%) so với placebo (17.4%), cũng như tiêu chí gộp tử vong tim mạch hay nhập viện vì suy tim (11%, 12.1% và 19.6% tương ứng). Tuy nhiên, nghiên cứu này không thiết kế để giúp đưa ra kết luận mạnh mẽ
về kết cục lâm sàng [3].
Hình 4.2: Biến đổi của nồng độ NTproBNP tại thời điểm tuần thứ 12
VICTORIA là thử nghiệm lâm sàng ngẫu nhiên, mù đôi pha 3 được tiến hành trên bệnh nhân suy tim PSTM giảm mạn có phân độ NYHA II-IV và tình trạng lâm sàng ổn định (định nghĩa là không dùng thuốc đường tĩnh mạch trong vòng 24 giờ) và có đợt mất bù cấp trong vòng 3 tháng gần đây (định nghĩa là suy tim nặng phải nhập viện, hoặc cần bổ sung lợi tiểu tĩnh mạch dù không phải nhập viện kèm theo tăng peptide lợi niệu) và PSTM< 45%. Tiêu chuẩn loại trừ là các bệnh nhân có dùng nitrate, ức chế PDE-5, riociguat, suy gan thận, bệnh nhân suy tim đang dùng dụng cụ trợ thất hoặc chờ ghép tim[1].
Nghiên cứu này lấy mẫu trên toàn thế giới nhưng tập trung đa số ở châu Âu, vùng châu Á Thái Bình Dương và châu Mỹ. Các bệnh nhân được phân nhóm ngẫu nhiên vericiguat (khởi đầu 2.5mg mỗi ngày, sau đó tăng dần lên 5mg rồi đến liều đích là 10mg) và placebo, dự kiến theo dõi trong 18 tháng. Tất cả các bệnh nhân đều được điều trị suy tim chuẩn theo khuyến cáo hiện hành. Lược đồ nghiên cứu được thiết kế như hình 4.3.
Hình 4.3: Protocol thiết kế của thử nghiệm lâm sàng VICTORIA.
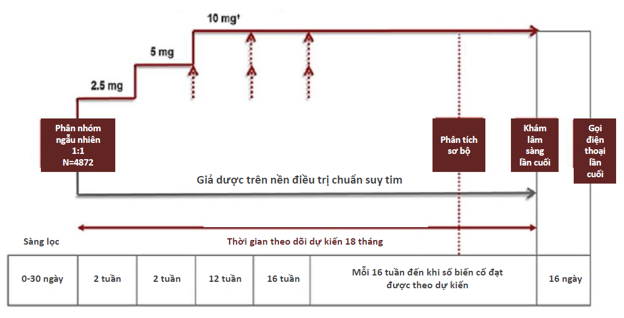
Có 5050 bệnh nhân tham gia nghiên cứu, chia đều cho 2 nhóm. Độ tuổi trung vị là 68 tuổi, nữ giới chiếm 24%. 85.7% dân số nghiên cứu có PSTM < 40%, PSTM trung bình là 29%. 41% bệnh nhân suy tim có phân loại NYHA III-IV. Thời gian từ lúc chẩn đoán suy tim đến thời điểm phân nhóm ngẫu nhiên là 5 năm. NTproBNP trung bình 2816 pg/dL. Cả 2 nhóm được điều trị suy tim chuẩn theo khuyến cáo: 60% được nhận 3 thuốc giức chế beta, đối kháng thụ thể aldosterone cùng với hoặc ức chế men chuyển hoặc chẹn thụ thể AGII hoặc ARNI.32% bệnh nhân có máy tạo nhịp 2 buồng thất và/ hoặc ICD. Tuân thủ điều trị đạt được 93% ở cả 2 nhóm. Tỉ lệ đạt liều đích vericiguat là 89%. Kết cục lâm sàng giữa 2 nhóm điều trị được tóm tắt trong Bảng 4.1.
Bảng 4.1: So sánh kết cục lâm sàng giữa Vericiguat so với giả dược[1].
| Kết cục lâm sàng | Vericiguat (n=2526) | Giả dược (n=2524) | HR (KTC 95%);
P |
||
| Số BN
(%) |
Số biến cố mỗi 100 Bệnh nhân-Năm | Số BN
(%) |
Số biến cố mỗi 100 Bệnh nhân-Năm | ||
| Tiêu chí chính (tử vong tim mạch hoặc nhập viện lần đầu do suy tim) | 897 (35.5) | 33.6 | 972 (38.5) | 37.8 | 0.90 (0.82 – 0.98);
0.02 |
| Tử vong tim
mạch |
414 (16.4) | 12.9 | 441 (17.5) | 13.9 | 0.93 (0.81 – 1.06);
0.269 |
| Nhập viện lần
đầu do suy tim |
691 (27.4) | 25.9 | 747 (29.6) | 29.1 | 0.90 (0.81- 1.00);
0.048 |
| Nhập viện tổng cộng do suy tim | 1223 | 38.3 | 1336 | 42.4 | 0.91 (0.84- 0.99);
0.02 |
| Tử vong do bất kỳ nguyên nhân | 512 (20.3) | 16.0 | 534 (21.2) | 16.9 | 0.95 (0.84- 1.07);
0.38 |
Nghiên cứu VICTORIA so sánh vericiguat với placebo ở bệnh nhân suy tim mạn PSTM giảm có đợt mất bù cấp gần đây đã cho thấy tiêu chí gộp tử vong tim mạch và nhập viện do suy tim thấp hơn ở nhóm vericiguat. Sự khác biệt này bắt đầu sau 3 tháng điều trị và duy trì trong suốt thời gian nghiên cứu. Việc giảm 10% nguy cơ tương đối do vericiguat trong 10.8 tháng theo dõi ở nhóm bệnh nhân nguy cơ cao này tương đương với giảm được 4.2 biến cố mỗi 100 bệnh nhân-năm, tính ra NNT (number needed to treat) là 24 tức cứ trung bình điều trị vericiguat cho 24 bệnh nhân trong 1 năm sẽ ngừa được 1 biến cố chính. Lợi ích này đạt được trên các bệnh nhân điều trị nội khoa chuẩn suy tim theo khuyến cáo hiện hành. Trong đó, khi phân tích vào từng thành phần trong tiêu chí chính, thấy rằng tỉ lệ nhập viện do suy tim thấp hơn khi dùng vericiguat, tỉ lệ tử vong tim mạch có xu hướng thấp hơn. Tử vong do mọi nguyên nhân không có sự khác biệt giữa 2 nhóm. Tuy nhiên, do nghiên cứu này thực hiện trên nhóm bệnh nhân suy tim nặng, nguy cơ cao, các biến cố chính xảy ra sớm hơn so với dự tính, vì vậy nghiên cứu được kết thúc sớm dẫn đến thời gian theo dõi trong nghiên cứu tương đối ngắn so với dự định (chỉ 10.8 tháng trong khi dự định theo dõi 18 tháng). Điều này có thể làm giới hạn khả năng phát hiện sự khác biệt có ý nghĩa thống kê giữa vericiguat và placebo đối với các tiêu chí phụ. Có thể khi nghiên cứu được kéo dài hơn sẽ thấy được lợi ích của vericiguat đối với các tiêu chí phụ như tử vong do mọi nguyên nhân.
Khi so sánh với 2 nghiên cứu gần đây cũng thực hiện trên bệnh nhân suy tim với PSTM giảm. Trong nghiên cứu PARADIGM-HF và DAPA-HF, tỉ lệ bệnh nhân suy tim NYHA III hay IV lần lượt là 25% và 32% so với 41% trong thử nghiệm VICTORIA. Tương tự, NTproBNP lần lượt là 1608 và 1437 pg/mL so với 2816 pg/mL trong VICTORIA.[4],[5] Điều này giải thích lý do vì sao tỉ lệ biến cố chính 12 tháng của VICTORIA lên đến 33.6%, nhiều hơn gấp 2 lần so với 2 nghiên cứu còn lại. Vì thế, mặc dù nghiên cứu PARADIGM-HF (HR 0.80 [0.73-0.87]) và DAPA-HF (HR 0.74 [0.65- 0.85]) cho thấy giảm nguy cơ tương đối của biến cố chính cao hơn so với VICTORIA (HR 0.90 [0.82-0.98]), thế nhưng khi tính ra độ giảm nguy cơ tuyệt đối về giảm số biến cố trên 100 người-năm thì lại tương đương nhau.[2]
Các tác dụng phụ như tụt huyết áp có triệu chứng và ngất thường gặp hơn trong nhóm vericiguat so với nhóm giả dược, ngoài ra vericiguat còn làm giảm hemoglobin nhiều hơn, tuy không có ý nghĩa thống kê. [1]Nhìn chung, tần suất gặp tác dụng phụ hầu như tương đương giữa 2 nhóm. Vericiguat không gây hại lên chức năng thận và điện giải đồ máu. Việc tuân thủ thuốc điều trị suy tim là điều tối quan trọng, tuy nhiên trong thực tế lâm sàng rất khó khăn do nhiều nguyên nhân, gây ra việc giảm tuân thủ của bệnh nhân sau 2-4 tháng xuất viện. Do đó, với tính chất an toàn khi dùng vericiguat, có thể sẽ giúp tỉ lệ tuân thủ điều trị ở nhóm bệnh nhân suy tim nặng nguy cơ cao tăng lên, góp phần cải thiện tiên lượng ngắn và dài hạn cho nhóm nguy cơ cao này. Trong nghiên cứu VICTORIA, có trên 89% bệnh nhân tuân thủ điều trị với liều đích 10mg sau 12 tháng theo dõi.
Với các kết quả tích cực đến từ VICTORIA, giữa tháng 1/2021, vericiguat đã được FDA chấp thuận cho chỉ định điều trị bệnh nhân suy tim PSTM giảm có triệu chứng, nguy cơ cao nhằm giảm nguy cơ biến cố tim mạch cho các bệnh nhân này.
- CON ĐƯỜNG KÍCH HOẠT CHỌN LỌC MYOSIN CƠ TIM
Suy tim PSTM giảm là bệnh lý do giảm hay mất chức năng của tế bào cơ tim. Việc giảm chức năng co bóp và tăng áp lực căng thành cơ tim kích hoạt các cơ chế bù trừ liên quan, như kích hoạt hệ thần kinh thể dịch và tái cấu trúc thất trái, làm tăng nhu cầu oxy cơ tim, giảm hiệu năng co bóp, hậu quả lại làm tăng thêm tổn thương và chết tế bào cơ tim. Hiện nay, có nhiều trị liệu tác động đến hệ thần kinh thể dịch trong suy tim PSTM giảm như ức chế hệ RAA, ức chế beta giao cảm. Tuy nhiên, các thuốc này không tác động đến cơ chế suy giảm chức năng tâm thu của tim. Các nhà nghiên cứu đặt giả thiết rằng khi cải thiện chức năng tâm thu sẽ ngăn ngừa hoặc làm giảm các phản ứng kích hoạt của hệ thần kinh thể dịch và tái cấu trúc thất trái, từ đó giúp cải thiện triệu chứng và giảm các biến cố lâm sàng của bệnh nhân suy tim.
Thật ra trước đây đã có nhiều thử nghiệm về thuốc tăng co bóp cơ tim trong suy tim mạn PSTM giảm, tuy nhiên tất cả đều thất bại trong việc giúp giảm tử vong ở nhóm bệnh nhân này. Những thuốc tăng co bóp cơ tim này có cùng cơ chế là tăng canxi nội bào, từ đó cải thiện chức năng cơ tim, tuy nhiên việc tăng dòng canxi nội bào này cũng tác động đến các chức năng điện sinh lý tim, có thể dẫn đến các rối loạn nhịp nguy hiểm như nhịp nhanh thất cho người bệnh. Do đó, các thuốc này được gọi là calcitropes, có thể kể đến như Ibopamine, Flosequinan, Milrinone, Enoximone. Qua các thử nghiệm lâm sàng cho thấy rằng nỗ lực cải thiện chức năng cơ tim với calcitropes đã thất bại do gây tăng tỉ lệ tử vong ở liều điều trị[44].
Omecamtiv Mecarbil (OM) được phát triển dựa trên ý tưởng kích hoat trực tiếp sarcomere có thể cải thiện khả năng co bóp của tim mà không gây ra các tác động có hại như các thuốc tăng co bóp truyền thống. OM là 1 chất kích hoạt chọn lọc trên myosin tim, tác động trực tiếp trên myofilament, giúp tăng sức co bóp, cải thiện hiệu năng của tim mà không làm tăng dòng canxi nội bào[44].
Nghiên cứu COSMIC-HF pha 2 về OM trên bệnh nhân suy tim mạn PSTM giảm cho thấy, khi dùng OM trong 20 tuần giúp tăng thời gian tâm thu và thể tích nhát bóp thất trái, giảm thể tích tâm thu và tâm trương thất trái (có thể có lợi về giảm tái cấu trúc thất trái), và giảm nhịp tim cũng như NTproBNP [45].
Nghiên cứu GALACTIC-HF là nghiên cứu pha 3, thử nghiệm lâm sàng ngẫu nhiên, mù đôi, có đối chứng về nhằm đánh giá liệu rằng điều trị omecamtiv mecarbil ở suy tim PSTM giảm có giúp giảm suy tim và tử vong tim mạch hay không? Hơn 8000 bệnh nhân suy tim mạn có triệu chứng NYHA II-IV có PSTM ≤ 35%, tăng peptide lợi niệu, hoặc đang điều trị nội trú do suy tim hoặc đang điều trị ngoại trú nhưng đã từng nhập viện do suy tim trong 1 năm gần đây, được dùng giả dược hoặc OM (liều 25, 37.5 hay 50mg uống 2 lần/ ngày, chọn liều theo hướng dẫn của dược động học). Tất cả các bệnh nhân đều được điều trị suy tim chuẩn theo khuyến cáo. Tiêu chí chính là cộng gộp biến cố suy tim hay tử vong tim mạch. Tiêu chí phụ là tử vong tim mạch, triệu chứng theo bộ câu hỏi Kansas, nhập viện lần đầu do suy tim, tử vong do mọi nguyên nhân. Sau thời gian theo dõi trung vị 21.8 tháng, kết cục lâm sàng được trình bày ở bảng 5.1[43].
Bảng 5.1: So sánh kết cục lâm sàng giữa omecamtiv mecarbil so với giả dược[43].
| Kết cục lâm sàng | Omecativ Mecarbil
(n=4120) |
Giả dược
(n=4112) |
HR (KTC 95%);
P |
||
| Số BN
(%) |
Số biến cố mỗi 100 Bệnh nhân-Năm | Số BN
(%) |
Số biến cố mỗi 100 Bệnh nhân-Năm | ||
| Tiêu chí chính | 1523
(37) |
24.2 | 1607
(39.1) |
26.3 | 0.92 (0.86 to 0.99);
0.03 |
| Tử vong tim
mạch |
346
(8.4) |
371
(9.0) |
|||
| Nhập viện lần
đầu do suy tim |
1107 (26.9) | 1133 (27.6) | |||
| Đi khám sớm do
suy tim nặng lên |
70
(1.7) |
103
(2.5) |
|||
| Tiêu chí phụ | |||||
| Tổng số tử vong timmạch | 512 (20.3) | 16.0 | 534 (21.2) | 16.9 | 0.95 (0.84- 1.07);
0.38 |
| Thay đổi triệu chứng theo Kansas | 0.03 | ||||
| Nội trú | 23.7±0.7 | 21.2±0.7 | 2.5 (0.5 to 4.5) | ||
| Ngoại trú | 5.8±0.3 | 6.3±0.3 | −0.5 (−1.4 to 0.5) | ||
| Tử vong do mọi
nguyên nhân |
1067 (25.9) | 14.4 | 1065 (25.9) | 14.4 | 1.00 (0.92 to 1.09) |
Tác động của omecativ mecarbil giúp giảm tỉ lệ biến cố chính về tử vong tim mạch hay suy tim tuy nhiên độ giảm nguy cơ tương đối chỉ ở mức vừa phải 8% (P=0.03). Sự khác biệt thấy rõ ràng ở nhóm có PSTM <28%. Không có sự khác biệt về tử vong tim mạch, tử vong do mọi nguyên nhân, nhập viện do suy tim. Sử dụng OM dường như chỉ cải thiện chất lượng sống theo đánh giá của bảng câu hỏi Kansas trong nhóm điều trị nội trú, là những bệnh nhân có điểm ban đầu thấp hơn nhóm ngoại trú.
Trong nghiên cứu này, dù ghi nhận có sự tăng nhẹ nồng độ troponin trong nhóm dùng omecamtiv (chỉ khoảng 4 ng/L – tương đương với khi hoạt động thể dục gắng sức mạnh), tuy nhiên không có sự khác biệt về tần suất thiếu máu cơ tim, loạn nhịp thất hay tử vong giữa 2 nhóm omecamtiv và giả dược. Ngoài ra, không có tác dụng phụ ngoại ý nào về huyết áp, nhịp tim, kali máu hay chức năng thận khi bệnh nhân dùng omecamtiv [43].
Vậy liệu rằng nhóm thuốc tác động đến myosin cơ tim này sẽ đứng đâu trong điều trị suy tim PSTM giảm? Bằng chứng từ nghiên cứu GALACTIC-HF thấy rằng nhóm thuốc này có hiệu quả lớn hơn trên nhóm bệnh nhân nhập viện và người có PSTM thấp hơn, có thể mong đợi rằng các tác động có lợi sẽ rõ ràng hơn trên nhóm bệnh nhân suy tim nặng hơn (ví dụ NYHA IV). Tuy nhiên, hầu như rất ít bệnh nhân trong thử nghiệm lâm sàng này có NYHA IV. Bên cạnh đó, nghiên cứu này cũng ít mang tính phổ quát do tỉ lệ phân bố không đồng đều, ví dụ loại trừ bệnh nhân trên 85 tuổi, nữ chỉ chiếm 21%, sắc tộc da đen chỉ có 7% dân số nghiên cứu. Ngoài ra, thuốc ức chế SGLT2 gần đây đã được chứng minh có lợi ích rõ rệt trên nhóm bệnh nhân suy tim cũng chưa được dùng nhiều tại thời điểm diễn ra nghiên cứu GALACTIC-HF, chỉ 2.6% được dùng theo chỉ định đái tháo đường kèm theo. Cho đến thời điểm hiện tại, vẫn cần thêm nhiều dữ liệu hơn về nhóm thuốc này trước khi có thể đưa ra khuyến cáo thực hành trên lâm sàng. Dù vậy, với tín hiệu đáng mừng từ nghiên cứu GALACTIC-HF, lần đầu tiên sau hàng chục năm, một nhóm thuốc tăng sức co bóp cơ tim có thể cải thiện tiên lượng bệnh nhân suy tim PSTM giảm mà không làm tăng tỉ lệ thiếu máu cơ tim, loạn nhịp thất nguy hiểm. Đây sẽ là một thuốc mới đầy hứa hẹn trong điều trị suy tim PSTM giảm trong tương lai, dù vẫn cần thêm nhiều bằng chứng rõ ràng hơn nữa.
- KẾT LUẬN
Suy tim vẫn là 1 gánh nặng về sức khỏe và y tế toàn cầu. Hiện nay dù đã có nhiều thuốc và phương tiện hiện đại điều trị cho bệnh nhân, tuy nhiên họ vẫn phải đối mặt với các nguy cơ bị các biến cố tim mạch trong quá trình điều trị, đặc biệt là tử vong tim mạch và tái nhập viện do suy tim. Bệnh suất và tử suất còn cao, với tỉ lệ sống còn 5 năm sau nhập viện vì suy tim PSTM giảm chỉ khoảng 25%.[40]
Các tiến bộ gần đây về thuốc điều trị suy tim, bên cạnh nhóm thuốc ức chế hệ RAA, như thuốc ức chế SGLT2 (empagliflozin, dapagliflozin), thuốc kích hoạt trực tiếp men guanylate cyclase (vericiguat), thuốc kích hoạt chọn lọc myosin cơ tim (omecamtiv mecarbil) đã giúp cải thiện ngoạn mục hơn nữa tiên lượng cho bệnh nhân suy tim PSTM giảm. Tuy nhiên, khi có nhiều lựa chọn cho các bác sĩ lâm sàng về các thuốc giúp cải thiện tiên lượng, thì việc lựa chọn thuốc phù hợp với từng giai đoạn suy tim cũng như cách phối hợp, thêm thuốc với nhau cũng là một câu hỏi cần được làm sáng tỏ thêm. Chúng ta hi vọng rằng những vấn đề đặt ra khi ứng dụng trong thực tế lâm sàng của các nhóm thuốc mới này sẽ được trả lời bởi các thử nghiệm lâm sàng cũng như số liệu từ khảo sát thế giới thực (real-world) trong tương lai.
TÀI LIỆU THAM KHẢO
- Armstrong P. W., Pieske B., Anstrom K. J., et al. (2020), “Vericiguat in Patients with Heart Failure and Reduced Ejection Fraction”, New England Journal of Medicine.
- Butler J., Anstrom K. J., Armstrong P. W. (2020), “Comparing the Benefit Of Novel Therapies Across Clinical Trials: Insights from the VICTORIA Trial”, Circulation.
- Gheorghiade M., Greene S. J., Butler J., et al. (2015), “Effect of Vericiguat, a Soluble Guanylate Cyclase Stimulator, on Natriuretic Peptide Levels in Patients With Worsening Chronic Heart Failure and Reduced Ejection Fraction: The SOCRATES-REDUCED Randomized Trial”, JAMA, 314 (21), pp. 2251-2262.
- McMurray J. J. V., Packer M., Desai A. S., et al. (2014), “Angiotensin–Neprilysin Inhibition versus Enalapril in Heart Failure”, New England Journal of Medicine, 371 (11), pp. 993-1004.
- McMurray J. J. V., Solomon S. D., Inzucchi S. E., et al. (2019), “Dapagliflozin in Patients with Heart Failure and Reduced Ejection Fraction”, New England Journal of Medicine, 381 (21), pp. 1995-2008.
- Bayes-Genis A., Prickett T. C., Richards A. M., et al. (2016), “Soluble neprilysin retains catalytic activity in heart failure”, J Heart Lung Transplant, 35 (5), pp. 684-5.
- Bhatt D. L., Szarek M., Steg P. G., et al. (2021), “Sotagliflozin in Patients with Diabetes and Recent Worsening Heart Failure”, New England Journal of Medicine, 384 (2), pp. 117-128.
- Braunwald E. (2015), “The war against heart failure: the Lancet lecture”, Lancet, 385 (9970), pp. 812-24.
- Burnstock G. (1969), “Evolution of the autonomic innervation of visceral and cardiovascular systems in vertebrates”, Pharmacol Rev, 21 (4), pp. 247-324.
- Clouthier D. E., Hosoda K., Richardson J. A., et al. (1998), “Cranial and cardiac neural crest defects in endothelin-A receptor-deficient mice”, Development, 125 (5), pp. 813-24.
- Cullington D., Goode K. M., Zhang J., et al. (2014), “Is heart rate important for patients with heart failure in atrial fibrillation?”, JACC Heart Fail, 2 (3), pp. 213-20.
- Filippatos G., Anker S. D., Böhm M., et al. (2016), “A randomized controlled study of finerenone vs. eplerenone in patients with worsening chronic heart failure and diabetes mellitus and/or chronic kidney disease”, Eur Heart J, 37 (27), pp. 2105-14.
- Flather M. D., Yusuf S., Køber L., et al. (2000), “Long-term ACE-inhibitor therapy in patients with heart failure or left-ventricular dysfunction: a systematic overview of data from individual patients. ACE-Inhibitor Myocardial Infarction Collaborative Group”, Lancet, 355 (9215), pp. 1575-81.
- Funder J. W. (2010), “Aldosterone and mineralocorticoid receptors in the cardiovascular system”, Progress in cardiovascular diseases, 52 (5), pp. 393-400.
- Gheorghiade M., Böhm M., Greene S. J., et al. (2013), “Effect of aliskiren on postdischarge mortality and heart failure readmissions among patients hospitalized for heart failure: the ASTRONAUT randomized trial”, Jama, 309 (11), pp. 1125-35.
- Gould P. A., Esler M. D., Kaye D. M. (2008), “Atrial fibrillation is associated with decreased cardiac sympathetic response to isometric exercise in CHF in comparison to sinus rhythm”, Pacing Clin Electrophysiol, 31 (9), pp. 1125-9.
- Jarcho J. A. (2020), “More Evidence for SGLT2 Inhibitors in Heart Failure”, New England Journal of Medicine, 383 (15), pp. 1481-1482.
- Kelland N. F., Webb D. J. (2007), “Clinical trials of endothelin antagonists in heart failure: publication is good for the public health”, Heart (British Cardiac Society), 93 (1), pp. 2-4.
- Kiowski W., Sütsch G., Hunziker P., et al. (1995), “Evidence for endothelin-1-mediated vasoconstriction in severe chronic heart failure”, Lancet, 346 (8977), pp. 732-6.
- Kirchhof P., Benussi S., Kotecha D., et al. (2016), “2016 ESC Guidelines for the management of atrial fibrillation developed in collaboration with EACTS”, European Heart Journal, 37 (38), pp. 2893-2962.
- Kostis J. B., Packer M., Black H. R., et al. (2004), “Omapatrilat and enalapril in patients with hypertension: the Omapatrilat Cardiovascular Treatment vs. Enalapril (OCTAVE) trial”, Am J Hypertens, 17 (2), pp. 103-11.
- Kotecha D., Holmes J., Krum H., et al. (2014), “Efficacy of β blockers in patients with heart failure plus atrial fibrillation: an individual-patient data meta-analysis”, Lancet, 384 (9961), pp. 2235-43.
- Kotecha D., Manzano L., Krum H., et al. (2016), “Effect of age and sex on efficacy and tolerability of β blockers in patients with heart failure with reduced ejection fraction: individual patient data meta-analysis”, Bmj, 353, pp. i1855.
- Krum H. (2001), “New and emerging pharmacological strategies in the management of chronic heart failure”, Curr Opin Pharmacol, 1 (2), pp. 126-33.
- Lerman A., Kubo S. H., Tschumperlin L. K., et al. (1992), “Plasma endothelin concentrations in humans with end-stage heart failure and after heart transplantation”, J Am Coll Cardiol, 20 (4), pp. 849-53.
- Lopaschuk Gary D., Verma S. (2020), “Mechanisms of Cardiovascular Benefits of Sodium Glucose Co-Transporter 2 (SGLT2) Inhibitors”, JACC: Basic to Translational Science, 5 (6), pp. 632-644.
- Mangiafico S., Costello-Boerrigter L. C., Andersen I. A., et al. (2013), “Neutral endopeptidase inhibition and the natriuretic peptide system: an evolving strategy in cardiovascular therapeutics”, Eur Heart J, 34 (12), pp. 886-893c.
- McMurray J. J. V., Krum H., Abraham W. T., et al. (2016), “Aliskiren, Enalapril, or Aliskiren and Enalapril in Heart Failure”, New England Journal of Medicine, 374 (16), pp. 1521-1532.
- Messerli F. H., Nussberger J. (2000), “Vasopeptidase inhibition and angio-oedema”, Lancet, 356 (9230), pp. 608-9.
- Neal B., Perkovic V., Mahaffey K. W., et al. (2017), “Canagliflozin and Cardiovascular and Renal Events in Type 2 Diabetes”, New England Journal of Medicine, 377 (7), pp. 644-657.
- O’Meara E., McDonald M., Chan M., et al. (2020), “CCS/CHFS Heart Failure Guidelines: Clinical Trial Update on Functional Mitral Regurgitation, SGLT2 Inhibitors, ARNI in HFpEF, and Tafamidis in Amyloidosis”, Can J Cardiol, 36 (2), pp. 159-169.
- Packer M., Anker S. D., Butler J., et al. (2020), “Cardiovascular and Renal Outcomes with Empagliflozin in Heart Failure”, New England Journal of Medicine, 383 (15), pp. 1413-1424.
- Packer M., Califf R. M., Konstam M. A., et al. (2002), “Comparison of omapatrilat and enalapril in patients with chronic heart failure: the Omapatrilat Versus Enalapril Randomized Trial of Utility in Reducing Events (OVERTURE)”, Circulation, 106 (8), pp. 920-6.
- Parving H.-H., Brenner B. M., McMurray J. J. V., et al. (2012), “Cardiorenal End Points in a Trial of Aliskiren for Type 2 Diabetes”, New England Journal of Medicine, 367 (23), pp. 2204-2213.
- Perkovic V., Jardine M. J., Neal B., et al. (2019), “Canagliflozin and Renal Outcomes in Type 2 Diabetes and Nephropathy”, New England Journal of Medicine, 380 (24), pp. 2295-2306.
- Pitt B., Zannad F., Remme W. J., et al. (1999), “The effect of spironolactone on morbidity and mortality in patients with severe heart failure. Randomized Aldactone Evaluation Study Investigators”, N Engl J Med, 341 (10), pp. 709-17.
- Rouleau J. L., Pfeffer M. A., Stewart D. J., et al. (2000), “Comparison of vasopeptidase inhibitor, omapatrilat, and lisinopril on exercise tolerance and morbidity in patients with heart failure: IMPRESS randomised trial”, Lancet, 356 (9230), pp. 615-20.
- Rubattu S., Sciarretta S., Valenti V., et al. (2008), “Natriuretic peptides: an update on bioactivity, potential therapeutic use, and implication in cardiovascular diseases”, Am J Hypertens, 21 (7), pp. 733-41.
- Seferovic P. M., Ponikowski P., Anker S. D., et al. (2019), “Clinical practice update on heart failure 2019: pharmacotherapy, procedures, devices and patient management. An expert consensus meeting report of the Heart Failure Association of the European Society of Cardiology”, European Journal of Heart Failure, 21 (10), pp. 1169-1186.
- Shah K. S., Xu H., Matsouaka R. A., et al. (2017), “Heart Failure With Preserved, Borderline, and Reduced Ejection Fraction: 5-Year Outcomes”, J Am Coll Cardiol, 70 (20), pp. 2476-2486.
- Solomon S. D., McMurray J. J. V., Anand I. S., et al. (2019), “Angiotensin–Neprilysin Inhibition in Heart Failure with Preserved Ejection Fraction”, New England Journal of Medicine, 381 (17), pp. 1609-1620.
- Stasch J. P., Pacher P., Evgenov O. V. (2011), “Soluble guanylate cyclase as an emerging therapeutic target in cardiopulmonary disease”, Circulation, 123 (20), pp. 2263-73.
- Teerlink J. R., Diaz R., Felker G. M., et al. (2020), “Cardiac Myosin Activation with Omecamtiv Mecarbil in Systolic Heart Failure”, New England Journal of Medicine, 384 (2), pp. 105-116.
- Teerlink J. R., Diaz R., Felker G. M., et al. (2020), “Omecamtiv Mecarbil in Chronic Heart Failure With Reduced Ejection Fraction: Rationale and Design of GALACTIC-HF”, JACC Heart Fail, 8 (4), pp. 329-340.
- Teerlink J. R., Felker G. M., McMurray J. J., et al. (2016), “Chronic Oral Study of Myosin Activation to Increase Contractility in Heart Failure (COSMIC-HF): a phase 2, pharmacokinetic, randomised, placebo-controlled trial”, Lancet, 388 (10062), pp. 2895-2903.
- Tota B., Cerra M. C., Gattuso A. (2010), “Catecholamines, cardiac natriuretic peptides and chromogranin A: evolution and physiopathology of a ‘whip-brake’ system of the endocrine heart”, The Journal of Experimental Biology, 213 (18), pp. 3081.
- von Lueder T. G., Atar D., Krum H. (2014), “Current role of neprilysin inhibitors in hypertension and heart failure”, Pharmacol Ther, 144 (1), pp. 41-9.
- von Lueder T. G., Wang B. H., Kompa A. R., et al. (2015), “Angiotensin receptor neprilysin inhibitor LCZ696 attenuates cardiac remodeling and dysfunction after myocardial infarction by reducing cardiac fibrosis and hypertrophy”, Circ Heart Fail, 8 (1), pp. 71-8.
- Wiviott S. D., Raz I., Bonaca M. P., et al. (2018), “Dapagliflozin and Cardiovascular Outcomes in Type 2 Diabetes”, New England Journal of Medicine, 380 (4), pp. 347-357.
- Yancy Clyde W., Jessup M., Bozkurt B., et al. (2016), “2016 ACC/AHA/HFSA Focused Update on New Pharmacological Therapy for Heart Failure: An Update of the 2013 ACCF/AHA Guideline for the Management of Heart Failure: A Report of the American College of Cardiology/American Heart Association Task Force on Clinical Practice Guidelines and the Heart Failure Society of America”, Circulation, 134 (13), pp. e282-e293.
- Yancy C. W., Jessup M., Bozkurt B., et al. (2017), “2017 ACC/AHA/HFSA Focused Update of the 2013 ACCF/AHA Guideline for the Management of Heart Failure: A Report of the American College of Cardiology/American Heart Association Task Force on Clinical Practice Guidelines and the Heart Failure Society of America”, Circulation, 136 (6), pp. e137-e161.
- Zelniker T. A., Wiviott S. D., Raz I., et al. (2019), “SGLT2 inhibitors for primary and secondary prevention of cardiovascular and renal outcomes in type 2 diabetes: a systematic review and meta-analysis of cardiovascular outcome trials”, Lancet, 393 (10166), pp. 31-39.
- Zinman B., Wanner C., Lachin J. M., et al. (2015), “Empagliflozin, Cardiovascular Outcomes, and Mortality in Type 2 Diabetes”, New England Journal of Medicine, 373 (22), pp. 2117-2128.







