5. Điều chỉnh các rối loạn nhịp thất và phòng ngừa đột tử tim trong bệnh mạch vành
5.1 Hội chứng mạch vành cấp tính
5.1.1 Loạn nhịp thất liên quan đến hội chứng mạch vành cấp
TS Phạm Hữu Văn
Mặc dù có giảm rõ rệt về tỷ lệ SCD qua tái thông mạch máu tốt hơn và phòng ngừa CAD thông qua việc bỏ thuốc lá và điều trị statin, hội chứng mạch vành cấp (ACS) và rối loạn nhịp trễ sau nhồi máu cơ tim cấp tính vẫn là một nguyên nhân phổ biến của SCD (xem phần 3.1). Một số lượng đáng kể các biến cố SCD xảy ra trong giai đoạn trước nhập bệnh viện của ACS, nhấn mạnh vai trò quan trọng của chương trình sàng lọc để xác định bệnh nhân có nguy cơ. Tỷ lệ VA trong giai đoạn bệnh viện của ACS đã giảm trong những thập kỷ gần đây, chủ yếu là nhờ vào chiến lược tái thông mạch máu sớm và tích cực cũng như sớm hướng dẫn điều trị nội khoa đầy đủ. Tuy nhiên, trên 6% bệnh nhân với ACS phát triển VT hoặc VF trong vòng 48 giờ đầu tiên sau khi khởi phát triệu chứng, thường trước hoặc trong quá trình tái tưới máu. Ngoài tái thông mạch vành nhanh chóng và đầy đủ, các can thiệp không dùng thuốc (sốc điện, khử rung tim, tạo nhịp và triệt phá qua catheter) cũng như điều trị bằng thuốc (thuốc không chống loạn nhịp tim và chống loạn nhịp tim) có thể cần thiết để kiểm soát VAs trong tình huống này. Thực hiên chẩn đoán ở bệnh nhân VAs dai dẳng trong bối cảnh của ACS được minh họa trong hình 3.
5.1.2 Phòng ngừa và điều chỉnh đột tử tim liên quan với hội chứng mạch vành cấp: Giai đoạn trước bệnh viện
Phòng ngừa đột tử do tim liên quan với hội chứng mạch vành cấp: Giai đoạn trước bệnh viện
|
Các khuyến cáo |
Classa |
Levelb |
Ref.c |
|
Ở bệnh nhân đau ngực, người ta khuyến cáo để giảm sự chậm trễ cả từ khởi phát triệu chứng đến liên hệ y tế đầu tiên và từ liên lạc y tế đầu tiên đến tái tưới máu.. |
I |
A |
244 |
|
Người ta khuyến cáo các đội xe cứu thương được đào tạo và trang bị để xác định ACS (với việc sử dụng máy ghi điện tim và từ xa khi cần thiết) và điều trị ngừng tim bằng thực hiện hỗ trợ sống cơ bản và khử rung tim. |
I |
IB |
178 |
|
Người ta khuyến cáo hỗ trợ sống cơ bản và tăng cường được thực hiện theo các giao thức thuật toán xác định do Hội đồng hồi sức châu Âu hoặc các nhóm chuyên gia hồi sức quốc gia hoặc quốc tế. |
I |
C |
17 |
|
Người ta khuyến cáo chăm sóc sau hồi sức được thực hiện tại các trung tâm chuyên gia trình độ cao khả năng cung cấp điều trị chăm sóc đặc biệt đa ngành, trong đó có biện pháp can thiệp mạch vành tiên phát, điện sinh lý, thiết bị hỗ trợ tim, phẫu thuật tim, mạch máu và điều trị hạ thân nhiệt. |
I |
B |
245, 246 |
|
Việc tạo ra các mạng lưới khu vực để điều trị ngừng tim cần được xem xét để cải thiện kết quả |
. IIa |
B |
245 |
ACS = hội chứng mạch vành cấp; ECG = điện tâm đồ.
aClass khuyến cáo
b Mức độ bằng chứng.
cTài liệu tham khảo ủng hộ khuyến cáo.
Mặc dù tỷ lệ tử vong trong bệnh viện do nhồi máu cơ tim ST chênh lên (STEMI) đã được giảm đáng kể thông qua việc sử dụng các liệu pháp tái tưới máu hiện đại, tỷ lệ tử vong ngắn hạn về tổng thể vẫn là mối quan tâm. Nhồi máu biểu hiện như đột tử trong vài giờ đầu tiên sau khi khởi phát triệu chứng hiện nay là nguyên nhân chính gây tử vong trong nhồi máu cơ tim cấp.
5.1.3 Phòng ngừa đột tử tim liên quan với hội chứng mạch vành cấp: trong giai đoạn bệnh viện
Phòng ngừa và điều chỉnh đột tử tim liên quan với hội chứng mạch vành cấp: trong giai đoạn bệnh viện. Chỉ định tái thông mạch máu
|
Các khuyến cáo |
Classa |
Levelb |
Ref.c |
|
Tái tưới máu khẩn cấp được khuyến cáo ở những bệnh nhân có STEMI. |
I |
A |
247– 249 |
|
Tái thông mạch vành được khuyến cáo ở những bệnh nhân có NSTEMI hoặc đau thắt ngực không ổn định theo hướng dẫn NSTEMI của ESC. |
I |
C |
13,250 |
|
Chụp mạch vành tiếp sau, nếu cần thiết, do nong mạch vành trong vòng 2 giờ sau khi nhập viện được khuyến cáo ở những bệnh nhân NSTEMI có nguy cơ cao, gồm cả VA đe dọa tính mạng. |
I |
C |
13,250 |
|
Tái thông mạch vành nhanh chóng và đầy đủ được khuyến cáo để điều trị thiếu máu cục bộ cơ tim có thể biểu hiện ở những bệnh nhân có VT hoặc VF tái phát. |
I |
C |
251, 252 |
|
Mở các mạch máu nhồi máu nhanh chóng được khuyến cáo để phục hồi rối loạn dẫn truyền AV thiếu máu cục bộ mới khởi phát. Điều này đặc biệt đúng đối với blốc AV do nhồi máu thành dưới, ngay cả trong trường hợp đến muộn (>12 h) . |
I |
C |
253 |
|
Nhập trực tiếp các Cathlab được khuyến cáo cho các người sống sót bị hôn mê do ngừng tim ngoài bệnh viện có các tiêu chí trên điện tâm đồ cho STEMI trên ECG sau hồi sức. |
I |
B |
251, 252 |
|
Dừng lại đơn vị chăm sóc tích cực nên được xem xét ở những người sống sót bị hôn mê ngừng tim ngoài bệnh viện không có tiêu chí trên điện tâm đồ ST chênh lên trên ECG sau hồi sức để loại trừ nguyên nhân không phải mạch vành và trong trường hợp không có rõ ràng nguyên nhân không phải mạch vành gây ra, chụp mạch vành nên được xem xét càng sớm càng tốt (2 h), đặc biệt ở những bệnh nhân huyết động không ổn định. |
Iia(cho cả hai khuyến cáo) |
B |
251, 252 |
|
Cấy thiết bị hỗ trợ LV hoặc hỗ trợ cuộc sống bên ngoài cơ thể cần được xem xét ở những bệnh nhân không ổn định có VT tái phát không ổn định huyết động hoặc VF mặc dù điều trị tối ưu. |
IIa |
B |
254 |
|
Hỗ trợ giúp tim và tái thông mạch máu ở các trung tâm chuyên ngành có thể được xem xét ở những bệnh nhân ngừng tim trơ. |
IIb |
C |
255, 256 |
ACS = hội chứng mạch vành cấp; AV = nhĩ thất; ECG = điện tâm đồ; ESC = Hội tim mạch châu Âu; LV = thất trái; NSTEMI = nhồi máu cơ tim ST không chênh lên; SCD = đột tử tim; STEMI = nhối máu cơ tim ST chênh lên; VA = loạn nhịp thất; VF = rung thất; VT = nhịp nhanh thất
aClass khuyến cáo
b Mức độ bằng chứng.
cTài liều tham khảo ủng hộ khuyến cáo.
Ngăn ngừa và điều chỉnh đột tử tim kết hợp với hội chứng mạch vành cấp: giai đoạn bệnh viện. Khử rung/chuyển nhịp/thuốc/triệt phá qua catheter
|
Các khuyến cáo |
Classa |
Levelb |
Ref.c |
|
Điều trị beta-blocker được khuyến cáo cho VT đa hình tái phát. |
I |
B |
257 |
|
Amiodarone tiêm tĩnh mạch được khuyến khích cho việc điều trị VT đa hình. |
I |
C |
258 |
|
Sốc điện ngay lập tức hoặc khử rung tim được khuyến cáo ở những bệnh nhân có VT dai dẳng hoặc VF. |
I |
C 180 |
C 180 |
|
Chụp động mạch vành cấp cứu tiếp theo khi được chỉ định, do tái thông mạch máu được khuyến cáo ở những bệnh nhân có VT tái phát hay VF khi thiếu máu cơ tim không thể được loại trừ. |
I |
C |
251, 252 |
|
Sửa chữa mất cân bằng điện giải được khuyến cáo ở những bệnh nhân có VT tái phát hay VF. |
I |
C |
179 |
|
Điều trị bằng uống beta-blockers cần được xem xét trong thời gian nằm viện và tiếp tục sau đó trong tất cả các bệnh nhân ACS mà không chống chỉ định. |
IIa |
B |
130, 257, 259, 260 |
|
Triệt phá bằng năng lượng tần số radio qua catheter tại trung tâm triệt phá chuyên biệt tiếp theo là cấy ICD cần được xem xét ở những bệnh nhân với VT tái phát, VF hay bão điện mặc dù tái tuần hoàn máu đầy đủ và điều trị thuốc tối ưu. |
IIa |
C |
261– 267 |
|
Kích thích vượt tần số qua catheter tĩnh mạch nên được xem xét nếu VT tái phát thường xuyên mặc dù sử dụng các thuốc chống loạn nhịp tim và triệt phá qua catheter là không thể. |
IIa C |
IIa C |
|
|
Lidocaine tiêm tĩnh mạch có thể được xem xét để điều trị VT dai dẳng tái phát hoặc VF không đáp ứng với thuốc chẹn bêta hoặc amiodarone hoặc có các chống chỉ định với amiodarone. |
IIb |
C |
268 |
|
Điều trị dự phòng bằng thuốc chống loạn nhịp tim (trừ beta-blockers) không được khuyến cáo. |
III |
B 269, 270 |
B 269, 270 |
ACS = hội chứng mạch vành cấp; ICD = máy khử rung tim có thể cấy; SCD = đột tử tim; VF = rung thất; VT = nhịp nhanh thất.
a Class khuyến cáo.
b Mức độ bằng chứng.
cTài liệu tham khảo ủng hộ khuyến cáo.
Phòng ngừa và điều chỉnh đột tử tim liên quan với hội chứng mạch vành cấp: giai đoạn trong bệnh viện. Tạo nhịp / máy khử rung tim cấy vào cơ thể
|
Khuyến cáo |
Classa |
Levelb |
Ref.c |
|
Tạo nhịp tạm thời qua tĩnh mạch được khuyến cáo ở những bệnh nhân nhịp xoang chậm có triệu chứng mặc dù điều trị bằng thuốc tăng nhịp tim (positive chronotropic medication). |
I |
C |
271 |
|
Tạo nhịp tạm thời qua tĩnh mạch được khuyến cáo ở những bệnh nhân blốc AV cao độ có triệu chứng không có nhịp thoát ổn định. |
I |
C |
271 |
|
Chụp động mạch khẩn cấp được khuyến cáo ở những bệnh nhân blốc AV cao độ có triệu chứng đã không nhận được tái tưới máu. |
I |
C |
271 |
|
Lập trình lại ICD đã cấy trước được khuyến cáo cho bệnh nhân có điều trị ICD không thích hợp tái phát. |
I |
C |
272 |
|
Lập trình lại một ICD đã được cấy trước cần được xem xét để tránh những sốc ICD không cần thiết. |
IIa |
C |
272 |
|
Cấy ICD hoặc tạm thời sử dụng WCD có thể được xem xét, sau nhồi máu cơ tim <40 ngày ở những bệnh nhân được lựa chọn (tái tuần hoàn máu không đầy đủ, d có rối loạn chức năng LVEF từ trước, xuất hiện loạn nhịp tim > 48 h sau khi sự khởi đầu ACS, VT đa hình hoặc VF) . |
IIb |
C |
170, 273 |
|
Cấy ICD phòng ngừa SCD tiên phát thường không được chỉ định < 40 ngày sau khi nhồi máu cơ tim. |
III |
A |
274, 275 |
ACS = hội chứng mạch vành cấp; AV = nhĩ thất; ICD = máy khử rung tim cấy vào cơ thể; LVEF = phân suất tống máu; SCD = đột tử tim; VF = rung thất; VT = nhịp nhanh thất; WCD = máy khử rung tim có thể mặc.
a Class khuyến cáo.
b Mức độ bằng chứng.
cTài liệu tham khảo ủng hộ khuyến cáo.
dTái tuần hoàn không hoàn toàn được qui cho thất bại điều trị tổn thương thủ phạm hoặc có mặt của các tổn thương không phải thủ phạm không thể điều trị được
Hướng dẫn ESC để điều trị ACS có hoặc không có đoạn ST chênh lên và tái tuần hoàn máu vành đã được xuất bản và tất cả các thông tin có liên quan đến việc chẩn đoán của ACS, NSTEMI hoặc STEMI và các khuyến cáo điều trị đã được cung cấp chi tiết.[13,250,271] Phần này tập trung vào vai trò cụ thể của tái tưới máu và / hoặc tái tuần hoàn máu để phòng ngừa và điều trị VT hay VF ở bệnh nhân ACS.
Do việc thực hiện các chương trình nâng cao nhận thức của công chúng về SCD, ngày càng có nhiều người sống sót sau ngừng tim ngoài bệnh viện đang được đưa vào bệnh viện. Nếu đoạn ST chênh lên trước khi hồi sức hoặc ECG sớm sau hồi sức hiện diện, chụp động mạch khẩn cấp và tái tuần hoàn máu được khuyến cáo ở tất cả các bệnh nhân STEMI. [251] Tuy nhiên, sự vắng mặt đoạn ST chênh lên không loại trừ tắc nghẽn hoặc thậm chí tổn thương huyết khối vành ‘thủ phạm’, trong đó có thể có mặt trong 25-58% các trường hợp. [251.252] với tỷ lệ cao tắc nghẽn mạch vành và khó khăn tiềm tàng trong việc giải thích các điện tâm đồ ở bệnh nhân sau khi ngừng tim, chụp mạch vành nên được xem xét ở những người sống sót do ngừng tim ngoài bệnh viện ngừng tim sau lưu lại khoa cấp cứu hoặc đơn vị chăm sóc tích cực để loại trừ sự hiện diện các nguyên nhân ngừng tim không phải tim [276]
Trong các bối cảnh ACS và VT dai dẳng tái phát và / hoặc phù hợp về mặt huyết động học hoặc VF, tái tuần hoàn máu nhanh chóng thành công là chìa khóa để tiếp tục phòng ngừa rối loạn nhịp tim và nên được tiến hành ngay lập tức [13.250.271].
5.1.3.1 Loạn nhịp thất trong hội chứng mạch vành cấp
Thiếu máu cấp tính gây ra sự mất ổn định điện, kích động VA ở bệnh nhân ACS [266]. Sử dụng sớm các thuốc chẹn beta trong các bối cảnh ACS làm giảm VT / VF và do đó được khuyến cáo [257.269]. Sửa chữa giảm magiê và hạ kali máu có thể giúp ở những bệnh nhân được lựa chọn. Liệu pháp statin làm giảm tỷ lệ tử vong ở những bệnh nhân có CAD, chủ yếu là thông qua việc phòng chống các biến cố mạch vành tái phát và do đó là một phần của các loại thuốc thông thường được khuyến cáo [250.271].
5.1.3.2 Sử dụng thuốc chống loạn nhịp tim trong hội chứng mạch vành cấp – xem xét chung
Sốc điện hoặc khử rung là can thiệp lựa chọn để cắt cấp thời VAs ở bệnh nhân ACS [1, 271]. Sử dụng sớm (có thể iv) beta-blockers có thể giúp ngăn ngừa loạn nhịp tim tái phát [257.269.271]. Điều trị bằng thuốc chống loạn nhịp với amiodarone chỉ nên được xem xét nếu các cơn VT hay VF thường xuyên và không còn có thể được kiểm soát bằng cách sốc điện hoặc khử rung tim tiếp [1271]. Lidocaine tiêm tĩnh mạch có thể được xem xét cho VT dai dẳng tái phát hoặc VF không đáp ứng với thuốc chẹn bêta hoặc amiodarone hoặc trong các trường hợp chống chỉ định amiodarone. Ở những bệnh nhân VT tái phát hoặc VF kích hoạt bằng phức hợp thất sớm (PVC) phát sinh từ các sợi Purkinje tổn thương một phần, triệt phá qua catheter là rất hiệu quả và nên được xem xét [261-265] (xem phần 6.3.2).
5.1.3.3 Bệnh nhân bị hội chứng mạch vành cấp và không có rối loạn nhịp thất
Điều trị beta-blocker được khuyến cáo để ngăn ngừa VA [257.271]. Điều trị dự phòng bằng thuốc chống loạn nhịp tim đã không được chứng minh có lợi và thậm chí có thể có hại và do đó không được chỉ định [257.269].
5.1.3.4 Các phức hợp thất sớm (PVC)
PVC và nhịp nhanh thất tạm thời (NSVT) thường xuyên xảy ra ở những bệnh nhân với ACS, đặc biệt trong quá trình can thiệp mạch vành qua da tiên phát cho STEMI (được gọi là rối loạn nhịp tái tưới máu). Chúng rất hiếm khi liên quan đến huyết động và không cần điều trị chuyên biệt. phức hợp thất ngoại vị thường xuyên và kéo dài có thể là một dấu hiệu cho thấy tái tuần hoàn máu tiếp theo (ví dụ như can thiệp chụp mạch vành qua da lại) là cần thiết. [250.271] Trong NSVT có liên quan đến huyết động, amiodarone (300 mg iv bolus) nên được xem xét [1271].
5.1.3.5 VT dai dẳng và VF
VT dai dẳng tái phát, đặc biệt khi VT đa hình hoặc VF tái phát có thể là dấu hiệu của tái tưới máu không hoàn toàn hoặc tái phát của thiếu máu cấp tính. Do đó, ngay lập tức chụp động mạch vành cần được xem xét [250.271]. VT đai hình tái phát thoái hóa thành VF có thể đáp ứng với beta-blockers. Ngoài ra, giảm đau sâu có thể hữu ích để giảm cơn VT hoặc VF. Amiodarone (150-300 mg iv bolus) cần được xem xét để ngăn chặn cấp tính VAs có liên quan đến huyến động. Việc sử dụng các thuốc chống loạn nhịp khác trong ACS (ví dụ như procainamide, propafenone, ajmaline, flecainide) không được khuyến cáo [1.269.271].
5.1.3.6 Triệt phá qua catheter nhịp tim nhanh thất dai dẳng tái phát, rung thất tái phát và bão điện
Ở những bệnh nhân VT tái phát hoặc VF mặc dù tái tuần hoàn máu đầy đủ và điều trị thuốc tối ưu, triệt phá bằng năng lượng tần số radio qua catheter nên được xem xét. Các cơn VF tái phát có thể được kích hoạt do các PVC phát sinh từ các sợi Purkinje tổn thương một phần hoặc cơ tâm thất bị tổn thương do thiếu máu cục bộ và / hoặc tái tưới máu. Trong hầu hết các trường hợp, các nền có thể được đánh giá từ nội tâm mạc. Lập bản đồ chính xác và triệt phá các khởi kích cho VT hoặc VF thành công, hoặc nền cơ tim duy trì VT hoặc VF, là một thủ thuật phức tạp và đòi hỏi khắt khe. Do đó lựa chọn sớm các bệnh nhân có VT hay bão VF đến các trung tâm chuyên khoa về triệt phá nên được xem xét [261-265].
5.1.3.7 Thiết bị hỗ trợ ngoài cơ thể (Extracorporeal support devices)
Trong các trường hợp VT tái phát hoặc VF được lựa chọn hoặc VF không thể được điều chỉnh với các khuyến nghị điều trị đưa ra ở trên, cấy thiết bị hỗ trợ LV hoặc hỗ trợ cuộc sống ngoài cơ thể cần được xem xét để ổn định huyết động. Can thiệp như vậy cũng có thể tạo ra các cửa sổ thời gian cho phép can thiệp mạch vành trong sốc tim do VT tái phát hoặc VF. Mặc dù ổn định huyết động có thể đạt được với các thiết bị hỗ trợ tâm thất, khả năng VT hoặc VF tái phát là cao và điều trị can thiệp là rất khó. [254]
5.1.3.8 Nhịp tim chậm và blốc tim
Nhịp tim chậm và blốc tim có thể xảy ra và được kết hợp với tỷ lệ tử vong bệnh viện tăng lên. Blốc AV thường do tắc gần động mạch vành phải hoặc động mạch mũ chiếm ưu thế. Tái tuần hoàn vành nhanh chóng thường được giải quyết dẫn truyền. [253] Khi nhịp tim chậm dẫn đến tổn thương huyết động học nặng (thường với blốc tim tiến triển hay hoàn toàn trong trường hợp không ổn nhịp thoát bộ nối) hoặc khi nó vẫn tồn tại mặc dù tái tuần hoàn máu vành, tạo nhịp tạm thời bằng điện cực đặt qua da vào thất phải, có thể cần thiết [271] Trong nhịp tim chậm hoặc blốc tim kéo dài, tạo nhịp vĩnh viễn có thể là cần thiết và cần được thực hiện theo các hướng dẫn tạo nhịp hiện hành [10].
5.1.4 Vai trò tiên lượng của rung thất sớm
VF sớm (tức là xảy ra trong vòng 48 h) trong ACS được liên kết với tăng tử suất ở bệnh viện lên trên 5 lằn [277] và có thể nhận diện các nguy cơ tử suất dài hạn. Không phải tất cả các trường hợp tử vong sau đó là đột tử và quyết định cho điều trị khử rung tim cần phải được dựa trên sự hiện diện của các yếu tố nguy cơ bổ sung thêm vào VF hoặc VT trong các bối cảnh của ACS. [278.279]
5.2 Thời gian sớm sau nhồi máu cơ tim
5.2.1 Phân tầng nguy cơ của đột tử tim
Phân tầng nguy cơ đột tử do tim sớm (trong vòng 10 ngày) sau khi nhồi máu cơ tim
|
Khuyến cáo |
Classa |
Levelb |
Ref.c |
|
PVS có thể được xem xét sớm sau nhồi máu cơ tim ở bệnh nhân LVEF giảm (≤40%) để đánh giá nguy cơ đột tử. |
IIb |
B |
280– 282 |
|
Các xét nghiệm không xâm lấn (như sự thay đổi vi sóng T, Test rối loạn tự trị hoặc SA-ECG) không được khuyến cáo cho phân tầng nguy cơ trong giai đoạn sớm sau nhồi máu cơ tim |
III |
B |
283, 284 |
LVEF = phân suất tống máu thất trái; PVS = kích thích thất có chương trình; SA-ECG = điện tâm đồ tín hiệu trung bình.
aClass khuyến cáo.
bMức độ bằng chứng.
cCác tài liệu ủng hộ cho khuyến cáo.
SCD là một nguyên nhân quan trọng của tử vong sau nhồi máu cơ tim cấp tính và thường là do nhồi máu tái phát. Tuy nhiên, cấy máy khử rung tim sớm sau nhồi máu không cải thiện tiên lượng, có thể là do các nguyên nhân của tử vong [274,275]. Tái tuần hoàn máu tối ưu và điều trị nội khoa (bao gồm cả betablockers, điều trị kháng tiểu cầu kép và statin) và phòng chống và điều trị HF được khuyến cáo và là trụ cột của phòng ngừa đột tử ở nhóm bệnh nhân này. Trong khi một số chỉ dấu nguy cơ không xâm lấn cho đột tử tim đã được thử nghiệm và bị bỏ sót trong nhóm này, một số dữ liệu hỗ trợ việc sử dụng kích thích có chương trình sớm ở những người nhồi máu cơ tim cấp sống sót với LVEF giảm, như những người không tạo ra VT đơn hình có nguy cơ thấp cho đột tử tiếp theo [285]. Các nghiên cứu ngẫu nhiên là cần thiết để kết luận xác định vai trò của kích thích có chương trình cho phân tầng nguy cơ sớm sau nhồi máu cơ tim cấp tính.
5.2.2 Chọn thời gian cấy máy khử rung tim sau nhồi máu cơ tim, đánh giá rối loạn chức năng thất trái trước và sau khi xuất viện
Chọn thời gian cấy máy khử rung tim sau nhồi máu cơ tim. Đánh giá phân suất tống máu
|
Các khuyến cáo |
Classa |
Levelb |
Ref.c |
|
Đánh giá sơm (trước khi xuất viện) LVEF được khuyến cáo ở tất cả các bệnh nhân bị nhồi máu cơ tim cấp tính. |
I |
C |
286– 288 |
|
Đánh giá lại LVEF 6-12 tuần sau nhồi máu cơ tim được khuyến cáo để đánh giá nhu cầu tiềm tàng cho cấy ICD ngừa tiên phát. |
I |
C |
286– 288 |
ICD = máy khử rung tim cấy vào cơ thể; LVEF = phân suất tống máu.
aClass của khuyến cáo.
bMức độ chứng cứ.
cTài liệu tham khảo ủng hộ khuyến cáo
Cấy ICD sớm (<40 ngày) hoặc sử dụng WCD tạm thời (<40 ngày) sử dụng có thể được xem xét khi có mặt các điều kiện cụ thể như LVEF giảm có tồn tại trước, tái tuần hoàn máu không đầy đủ và rối loạn nhịp tim xảy ra 48 h sau khi sự khởi phát ACS. Các loại VA phải được đánh giá (VT đơn hình, đa hình, nhiều hình dạng (pleomorphic) hoặc VF) cũng như độ dài chu kỳ VT (các cơn tạm thời ngắn [non-sustained short runs] hoặc các cơn tạm thời dài [non-sustained long runs]). Nếu kích thích có chương trình đã được thực hiện, khả năng tạo ra và cả các type loạn nhịp được tạo ra (VT đơn hinh, đa hình,VF) nên được đánh giá. [274.275]
LVEF nên được đánh giá 6-12 tuần sau khi nhồi máu cơ tim ở bệnh nhân ổn định và ở những người dùng thuốc HF tối ưu để đánh giá khả năng chỉ định cấy ICD dự phòng đột tử tiên phát. Việc đánh giá này cần được thực hiện và được áp dụng cho tất cả các bệnh nhân. [271.286 – 288]
5.3 Bệnh động mạch vành ổn định sau nhồi máu cơ tim với phân suất tống máu bảo tồn
Tái tuần hoàn máu hiện đại và điều trị phòng ngừa thứ phát cho phép bảo tồn LVEF ở hầu hết các bệnh nhân đến sớm với một nhồi máu cơ tim cấp tính. Mặc dù nguy cơ SCD ở những bệnh nhân này là thấp hơn đáng kể so với những bệnh nhân LVEF suy giảm nghiêm trọng, số lượng tuyệt đối các nạn nhân SCD với LVEF bảo tồn là cao. Các chiến lược phát hiện nguy cơ SCD được cải thiện ở quần thể trung gian có nguy cơ là cần thiết.
5.3.1 Phân tầng nguy cơ
Phân tầng nguy cơ ở bệnh nhân bị bệnh mạch vành ổn định sau nhồi máu cơ tim có phân suất tống máu bảo tồn
|
Khuyến cáo |
Classa |
Levelb |
Ref.c |
|
PVS nên được xem xét ở những người nhồi máu cơ tim sống sót có chức năng LV bảo tồn và ngất không giải thích được. |
IIa |
C |
280– 282 |
LV = thất trái; PVS = kích thích thất có chương trình
aClass của khuyến cáo.
bMức độ chứng cứ.
cTài liệu tham khảo ủng hộ khuyến cáo
Hầu hết các nghiên cứu đã đánh giá tính hữu ích của phân tầng nguy cơ không xâm lấn đã được thực hiện ở những bệnh nhân có LVEF suy giảm nghiêm trọng (<40%) hoặc trong các quần thể hỗn hợp. Trong những nghiên cứu này, một trong hai kết quả trong nhóm các bệnh nhân với LVEF> 40% đã không được báo cáo hoặc các phân nhóm này quá nhỏ để cho phép phân tích và giải thích các dữ liệu. Đến nay, ở bệnh nhân nhồi máu cơ tim thoáng qua (remote) và LVEF bảo tồn, không có kỹ thuật phân tầng nguy cơ không xâm lấn được chứng minh đủ đặc hiệu và nhạy cảm.
Có bằng chứng hạn chế từ các phân nhóm nghiên cứu quy mô lớn được kích thích thất có chương trình là hữu ích cho phân tầng nguy cơ ở bệnh nhân sau nhồi máu cơ tim với giá trị LVEF trung gian hoặc với LVEF> 40%.. [280-282] Câu hỏi này hiện đang được đề cập đến đang diễn ra trong nghiên cứu Phân tầng Nguy cơ Bệnh nhân có Phân uất Tống máu Bảo tồn (PRESERVE-EF) (NCT02124018).
5.3.2 Các khuyến cáo cho chiến lược tối ưu
Tái thông mạch máu ở những bệnh nhân bị bệnh mạch vành ổn định sau nhồi máu cơ tim với phân suất tống máu bảo tồn
|
Khuyến cáo |
Classa |
Levelb |
Ref.c |
|
Tái thông mạch vành được khuyên cáo để giảm nguy cơ SCD ở những bệnh nhân với VF khi thiếu máu cục bộ cơ tim cấp tính đi trước khởi phát VF. |
I |
B |
289, 290 |
SCD = Đột tử tim; VF = rung thất.
aClass của khuyến cáo.
bMức độ chứng cứ.
cTài liệu tham khảo ủng hộ khuyến cáo
Hướng dẫn tái thông mạch vành đã được công bố gần đây. [13] Chúng cung cấp thông tin điều chỉnh rõ ràng và người đọc được giới thiệu đến các nguồn tài liệu để biết chi tiết.
Ở những bệnh nhân CAD và VAs, đánh giá bệnh mạch vành tắc nghẽn và thiếu máu là rất cần thiết. Tái thông mạch máu bằng phẫu thuật có thể làm tăng tỷ lệ sống còn và ngăn chặn SCD. Cấy ICD điện cực thượng tâm mạc tại thời điểm bắc cầu mạch vành không có liên kết với lợi ích tử suất toàn bộ. Can thiệp mạch vành qua da cũng được kết hợp với suy giảm đáng kể tỷ lệ tử vong tim mạch do tử vong do nhồi máu cơ tim hay đột tử.ít hơn.
Tái thông mạch máu có thể liên quan với sự gia tăng LVEF ≥ 5-6% ở 15-65% bệnh nhân ổn định. Điều này đặc biệt đúng đối với những người có bằng chứng thiếu máu cơ tim cục bộ hay cơ tim ngủ đông (hibernating) trên nghiên cứu hình ảnh trước phẫu thuật. [291.292] Đa số các bệnh nhân biểu hiện LVEF giảm nặng ngay sau STEMI được cải thiện đáng kể chức năng tâm thu sau 3 tháng. [286] LVEF nên được đánh giá lại 6- 12 tuần sau khi tái thông mạch vành để đánh giá khả năng chỉ định cấy ICD phòng ngừa tiên phát.
Ở những bệnh nhân sống sót sau SCD, tái thông mạch máu có thể làm giảm tái phát rối loạn nhịp đe dọa tính mạng và SCD và cũng cải thiện kết cục của bệnh nhân, đặc biệt nếu có bằng chứng thiếu máu cục bộ trước SCD. VT đơn hình dai dẳng ở bệnh nhân nhồi máu cơ tim trước đó ít có khả năng bị ảnh hưởng do tái thông mạch máu. Tái thông mạch máu cơ tim có thể ngăn chặn tái phát SCD ở bệnh nhân có sẹo cơ tim rộng lớn và LVEF giảm đáng kể.
5.3.3 Sử dụng các thuốc chống loạn nhịp
Sử dụng các thuốc chống loạn nhịp
|
Các khuyến cáo |
Classa |
Levelb |
Ref.c |
|
Amiodaron có thể được xem xét để giảm các triệu chứng do VAs ở những người nhồi máu cơ tim sống sót, nhưng không có tác dụng trên tử suất. |
IIb |
B |
293, 294 |
|
Điều trị bằng thuốc chẹn kênh natri (class IC) không được khuyến cáo để dự phòng đột tử ở những bệnh nhân có CAD hoặc những người nhồi máu cơ tim sống sót. |
III |
B |
131 |
CAD = bệnh mạch vành; VA = Loạn nhịp thất
aClass của khuyến cáo.
bMức độ chứng cứ.
cTài liệu tham khảo ủng hộ khuyến cáo
Vai trò của các thuốc chống loạn nhịp tim trong dự phóng SCD ở bệnh nhân sau nhồi máu cơ có phân suất tống máu bảo tồn bị hạn chế. Hầu hết các dữ liệu đến từ các nghiên cứu CAST, [129] cho thấy thuốc ức chế kênh natri (các thuốc class IA và IC) tăng tỷ lệ tử vong sau nhồi máu cơ tim. Các thuốc class II (beta-blockers) có một vai trò đã được tính toán trong giảm tử vong ở bệnh nhân nhồi máu cơ tim với LVEF giảm và vai trò bảo vệ này cũng có thể có ở những bệnh nhân có LVEF bảo tồn, nhưng ảnh hưởng của chúng lên SCD còn chưa được chứng minh. Cuối cùng, các thuốc amiodarone class III đã không cho thấy giảm SCD ở bệnh nhân nhồi máu cơ tim với LVEF bảo tồn. Tuy nhiên, nó có thể có một vai trò trong việc làm giảm các triệu chứng và giảm các cơn loạn nhịp tim ở nhóm bệnh nhân này.
Đối với chứng loạn nhịp tim có triệu chứng nhưng không đe dọa tính mạng (PVC hoặc NSVT ngắn và chậm), amiodarone là thuốc được lựa chọn vì nó ức chế loạn nhịp tim mà không xấu đi tiên lượng [293.294].
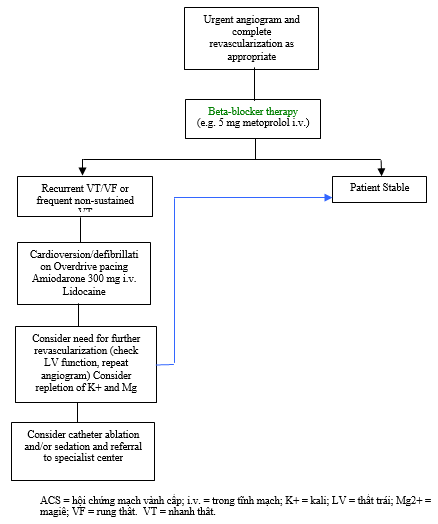
Hình 3Thực hiện chẩn đoán ở các bệnh nhân có loạn nhịp thất dai dẳng và hội chứng mạch vành cấp.
5.3.4 Triệt phá qua catheter
VT xảy ra trễ ở 1-2% bệnh nhân sau nhồi máu cơ tim, thường sau một khoảng thời gian vài năm. VT tái phát có thể được điều trị hiệu quả bằng triệt phá qua catheter, làm giảm đáng kể VT tái phát hàng loạt nhỏ các bệnh nhân điều trị tại các trung tâm chuyên ngành. Cho dù triệt phá trước tiên các VT đơn hình dai dẳng dung nạp tốt ở những bệnh nhân có LVEF < 40% mà không có ICD dự phóng là tương xứng lợi ích đáng được nghiên cứu tiếp theo. Cho đến khi đó, cấy ICD nên được xem xét ở những người sống sót sau nhồi máu cơ tim có VT dai dẳng hay VF không cho thấy thiếu máu cục bộ cấp tính, ngay cả sau khi triệt phá qua catheter thành công. [261-265]
6. Điều trị các bệnh nhân rối loạn chức năng thất trái có hoặc không có suy tim
VAs có mặt trong hầu hết các bệnh nhân suy tim và đột tử là phổ biến trong dân số này. [1,8,295,296]
Sự hiện diện và mức độ nghiêm trọng của VAs tăng lên cùng với mức độ nghiêm trọng của suy tim, nhưng giá trị của chúng để dự đoán đột tử không rõ ràng. [297-300]
Thật vậy, việc xác định các nguy cơ đột tử ở bệnh nhân suy tim đã trở nên rất khó khăn và chỉ tổ chức hội đoàn – độc lập nhất quán đã được thông báo với rối loạn chức năng LV hoặc LVEF nặng.
6.1 Dự phòng đột tử tim tiên phát
6.1.1 Các thuốc
Sử dụng thuốc ở bệnh nhân rối loạn chức năng thất trái
|
Các khuyến cáo |
Classa |
Levelb |
Ref.c |
|
Điều trị thuốc tối ưu bằng ức chế ACE (hoặc, khi không dung nạp bằng ARBs), beta-blockers và MRA được khuyến cáo ở những bệnh nhân có rối loạn chức năng tâm thu có HF (LVEF ≤ 35- 40%) để giảm tỉ lệ tử vong và SCD. |
I |
A |
301– 304 |
ACE = enzyme chuyển angiotensin; ARB = angiotensin II receptor blocker; HF = suy tim; LVEF = phân suất tống máu thất trái; MRA = chẹn thụ thể corticoide khoáng (mineralocorticoid receptor antagonist); SCD = đột tử tim.
aClass của khuyến cáo.
bMức độ chứng cứ.
cTài liệu tham khảo ủng hộ khuyến cáo
Các chất ức chế men chuyển, thuốc chẹn bêta và MRA được khuyến cáo ở những bệnh nhân suy tim có rối loạn tâm thu (LVEF ≤35-40%) vì chúng làm giảm tử suất do tất cả các nguyên nhân và đột tử [8] (xem phần 5).
Chất ức chế ACE làm giảm 15-25% tử vong do tất cả các nguyên nhân và được khuyến cáo trong tất cả các bệnh nhân LVEF giảm. [8, 305] Beta-blockers làm giảm tỷ lệ tử vong 35% và có đặc tính chống thiếu máu cục bộ, dẫn đến tác dụng chống loạn nhịp tim rõ rệt, và các thuốc này làm giảm một cách rõ rệt tỷ lệ đột tử.[8] Các tư liệu mới đây từ Beta-Blockers in Heart Failure Collaborative Group đã được thử thách các giả định lâm sàng về beta-blockers cải thiện tiên lượng ở bệnh nhân suy tim và AF và họ biện hộ để các bác sĩ nên chọn điều trị cho phân nhóm bệnh nhân suy tim một cách phù hợp. [306] Để tìm hiểu thêm quan sát hứng khở này, các tác giả nói ‘dữ liệu thử nghiệm đặc biệt ở những bệnh nhân suy tim và AF đang khẩn trương cần thiết và háo hức mong đợi “(‘trial data specifically in patients with HF and AF are urgently needed and eagerly anticipated’). [307]
MRA giảm tỷ lệ tử vong và giảm tỷ lệ đột tử ở những bệnh nhân suy tim được sử dụng các chất ức chế ACE và điều trị betablocker. [143.308.309] Trong các thử nghiệm gần đây nhất liên quan đến eplerenone, 20% bệnh nhân cũng đã cấy thiết bị (ICD hoặc CRT), nhưng thuốc hiệu quả tương đương ở bệnh nhân như những người không điều trị thiết bị. [309] Ảnh hưởng có lợi này của MRA về tỉ lệ SCD ở bệnh nhân có rối loạn chức năng tâm thu LV đã được xác nhận từ một phân tích gộp của sáu nghiên cứu cho thấy những bệnh nhân được điều trị với MRA có tỷ lệ chênh thấp hơn 23% của trải nghiệm SCD so với nhóm chứng [OR 0,77 (95% CI 0.66, 0.89), P = 0,001]. [310] Các thuốc lợi tiểu và digoxin vẫn được sử dụng do nhiều bệnh nhân suy tim, nhưng chúng không làm giảm giá tử suất toàn bộ do các nguyên nhân hoặc đột tử. Chẹn thụ thể angiotensin và Ivabradine chỉ được khuyến cáo ở các phân nhóm bệnh nhân với HF.[8] Amiodarone không ảnh hưởng đến hậu quả ở những bệnh nhân suy tim, [132] và dẫn đến tỷ lệ nhiễm độc thuốc cao, [8] nó không được khuyến khích sử dụng phổ biến ở những bệnh nhân này. Tuy nhiên, trong trường hợp nhịp nhanh thất có triệu chứng ở bệnh nhân suy tim (ví dụ như những người phải chịu những cú sốc từ máy khử rung tim hoặc từ VAs tạm thời gây ra triệu chứng), amiodarone là tác nhân chống loạn nhịp tim lựa chọn do nó không làm trầm trọng thêm hậu quả. [ 132] Các thuốc chống loạn nhịp khác không được khuyến cáo ở những bệnh nhân suy tim vì lo ngại tính an toàn.[8] Trong 10 năm qua đã có sự gia tăng nhận thức về nhiều bệnh nhân có các dấu hiệu và triệu chứng của suy tim có phân suất tống máu bình thường hoặc bảo tồn (HFpEF). [8, 311] Nhiều trong số các phương pháp điều trị đã cải thiện sống sót trong HF với phân suất tống máu giảm (HFrEF) lại ít hiệu quả trong HFpEF. Một tỷ lệ tương đối cao của các bệnh nhân có đồng bệnh tật không phải tim mạch, nhưng đột tử là phổ biến, [312] đã không có những nghiên cứu với ICDs hoặc CRT đủ thuyết phục. Hầu hết các thử nghiệm thuốc quy mô lớn trong HF đã được tiến hành trước khi kết quả tích cực từ những thử nghiệm mang tính bước ngoặt với ICD [63,64] và CRT [313.314] đã trở nên có khả năng (trong năm 2005); bằng chứng từ các thử nghiệm này đã dẫn đến khuyến cáo mạnh mẽ trong các hướng dẫn HF và gia tăng rất lớn trong việc sử dụng các hướng dẫn. [7315]
6.1.2 Máy khử rung tim có thể cấy
Máy khử rung tim có thể cấy ở các bệnh nhân có rối loạn chức năng thất trái
|
Các khuyến cáo |
Classa |
Levelb |
Ref.c |
|
Điều trị ICD được khuyến cáo để giảm SCD ở bệnh nhân suy tim có triệu chứng (NYHA II-III) và LVEF ≤ 35% sau ≥3 tháng điều trị nội tối ưu, người được hy vọng sống sót ít nhất 1 năm với tình trạng chức năng tốt: |
|
|
|
|
– Căn nguyên thiếu máu cục bộ (ít nhất 6 tuần sau nhồi máu cơ tim). |
I |
A |
63,64 |
|
– Căn nguyên không do thiếu máu cục. |
I |
B |
64,316, 317 |
HF = suy tim; ICD = máy khử rung tim có thể cấy; LVEF = phân suất tống máu; NYHA = New York Heart Association; SCD = đột tử tim.
aClass của khuyến cáo.
bMức độ chứng cứ.
cTài liệu tham khảo ủng hộ khuyến cáo
Nghiên cứu ban đầu về giá trị của ICD trong rối loạn chức năng LV đã được tiến hành ở những bệnh nhân bị ngừng tim trước đó (nghĩa là phòng ngừa thứ phát) hoặc ở người đòi hỏi có tiêu chuẩn điện sinh thêm vào. [1] Hai thử nghiệm lớn đã cung cấp dữ liệu về phòng ngừa SCD tiên phát bằng ICD ở bệnh nhân suy tim và LVEF giảm: các [l64] nghiên cứu SCD-HeFT và nghiên cứu Cấy Máy khử rung Đa trung tâm II (Multicenter Automatic Defibrillator Implantation Trial II: MADIT-II) [63,318]. Trong SCD-HeFT, sử dụng ICD đã được liên kết với giảm nguy cơ tử vong 23% [ tỷ số nguy cơ (HR) 0,77 (95% CI 0.62, 0.96), P = 0,007] và giảm tuyệt đối 7% trong tỷ lệ tử vong sau 5 năm (từ 29 đến 22%). Có giảm 60% SCD về phương diện cấy ICD [319]. Các hiệu quả trên tử suất do tất cả các nguyên nhân không thay đổi tùy theo HF do nguyên nhân thiếu máu cục bộ hoặc không thiếu máu cục bộ, nhưng có một sự khác biệt theo NYHA: ICD rất hiệu quả ở bệnh nhân class II nhưng không có tác dụng rõ ràng về tỷ lệ tử vong trong class III. Trong MADIT-II, bệnh nhân trong nhóm ICD đã giảm 31% tử suất do tất cả các nguyên nhân [HR 0,69 (95% CI 0.51, 0.93), P = 0,016], và một phân tích sau đó từ nghiên cứu này cho thấy lợi ích của ICD trong dân số này là phụ thuộc thời gian, [318] với một lợi ích lớn hơn ở những bệnh nhân có chỉ số nhồi máu cơ tim chênh lệch hơn từ ngẫu nhiên.
Trong khi có rất nhiều dữ liệu ủng hộ việc sử dụng ICD ở những người nhồi máu cơ tim sống sót (tức là nguyên nhân thiếu máu cục bộ), ở những bệnh nhân HFrEF với bệnh căn không thiếu máu cục bộ giảm tử suất do tất cả các nguyên nhân và tỷ lệ tử vong do loạn nhịp cũng được ủng hộ. Trong nghiên cứu Khử rung trong Đánh giá điều trị bệnh cơ tim Không do Thiếu máu (Defibrillator In NonIschemic cardiomyopathy treatment Evaluation: DEFINITE), [316] xu hướng trong giảm tử suất được quan sát thấy ở nhóm ICD [HR 0,65 (95% CI 0.40, 1.06), P = 0.08], trong khi đột tử tim đã giảm một cách có ý nghĩa [HR 0.20 (95% CI 0.06, 0.71), P = 0,006]. Trong nghiên cứu SCD-HeFT, [63] xu hướng giảm tử vong do mọi nguyên nhân [HR 0,73 (95% CI 0.50, 1.07), P = 0.06] được quan sát thấy ở những bệnh nhân không bị nhồi máu trước đó (và HF không thiếu máu cục bộ). Trong thử nghiệm tương tự cũng với bệnh nhân có nguyên nhân thiếu máu cục bộ, chỉ có một xu hướng trong việc giảm tử vong do mọi nguyên nhân [HR 0,79 (95% CI 0.60, 1.04), P = 0,05], chúng gợi ý có lẽ hai nhóm là quá nhỏ để đạt ý nghĩa thống kê [63]. Do đó, một phân tích gộp [317] năm thử nghiệm phòng ngừa tiên phát do Desai và cộng sự thực hiện liên quan đến 1.854 bệnh nhân suy tim không do thiếu máu cục bộ, sử dụng ICD đã được liên quan với giảm có ý nghĩa 31% trong tử suất toàn bộ [HR 0,69 (95% CI 0.55, 0.87), P = 0,002]. Điều trị ICD không được khuyến cáo ở những bệnh nhân HF giai đoạn cuối (NYHA IV) và ở những bệnh nhân có tuổi thọ được tính toán < 1 năm.
Hiện nay không có RCTs (các nghiên cứu ngẫy nhiên có đối chứng) chứng minh giá trị của ICD ở những bệnh nhân không có triệu chứng (NYHA I) với rối loạn chức năng tâm thu (LVEF ≤35-40%) hoặc ở những bệnh nhân suy tim và có chức năng tâm thu thất trái bảo tồn (LVEF > 40-45%), vì vậy ICD không được khuyến cáo phòng ngừa tiên phát ở những bệnh nhân này.
6.1.3 Máy khử rung tim có thể cấy ở các bệnh nhân có NYHA class IV được giành cho ghép tim
Máy khủ rung tim có thể cấy ở các bệnh nhân có New York Heart Association class IV giành cho ghép tim
|
Các khuyến cáo |
Classa |
Levelb |
Ref.c |
|
ICD cấy cần được xem xét để phòng ngừa SCD tiên phát và thứ phát ở những bệnh nhân được dự kiến cho ghép tim |
IIa |
C |
320, 321 |
ICD = máy khử rung có thể cấy; SCD = đột tử tim.
a Class của khuyến cáo.
bMức độ chứng cứ.
cTài liệu tham khảo ủng hộ khuyến cáo
Không có dữ liệu thử nghiệm ngẫu nhiên về giá trị của ICD ở bệnh nhân suy tim NYHA IV. Người ta thường chấp nhận điều trị ICD không được khuyến cáo ở những bệnh nhân nặng, có triệu chứng trơ với thuốc không phải là ứng cử viên cho CRT, một thiết bị hỗ trợ tâm thất hay nghép tim. [8,11] Tuy nhiên, tình trạng đối với các bệnh nhân class IV có thể đi lại được sắp xếp cho ghép tim có thể khác nhau. Những bệnh nhân này thường phải chờ ít nhất 1 năm và nguy cơ đột tử cao. Dữ liệu từ hai nghiên cứu quan sát cùng khám gần 2.000 bệnh nhân, một trong số nghiên cứu gần đây [320] và một nghiên cứu trước đây (trong đó việc sử dụng beta-blockers đạt thấp), [321] đã gợi ý các bệnh nhân này được cấy ICD là có lợi ích sống còn.
6.1.4 Điều trị tái đồng bộ tim
6.1.4.1 Suy tim có phân suất tống máu thất trái giảm và NYHA class III/class IV thay đổi
Bảng A. Điều trị tái đồng bộ tim dự phòng tiên phát đột tử ở các bệnh nhân nhịp xoang và NYHA chức năng class II/class IV thay đổi
|
Các khuyến cáo |
Classa |
Levelb |
Ref.c |
|
CRT được khuyến cáo để giảm tử suất do mọi nguyên nhân ở bệnh nhân có LVEF ≤35% và LBBB mặc dù điều trị nội khoa tối ưu ít nhất 3 tháng, người dự kiến sẽ sống sót ít nhất 1 năm với tình trạng chức năng tốt: |
|
|
322– 326 |
|
– Có QRS rộng > 150 ms |
I |
A |
313, 314, 327– 329 |
|
– Có QRS rộng 120–150 ms |
I |
B |
313, 314 |
|
CRT nên hoặc có thể được xem xét để giảm tử suất do mọi nguyên nhân ở bệnh nhân có LVEF ≤35% không LBBB mặc dù điều trị nội khoa tối ưu ít nhất là 3 tháng, người dự kiến sẽ sống sót ít nhất 1 năm với tình trạng chức năng tốt: |
|
|
326 323– 325 |
|
– Có QRS rộng > 150 ms |
IIa |
B |
313, 314 |
|
– Có QRS rộng 120–150 ms |
IIb |
B |
313, 314 |
CRT = điều trị tái đồng bộ tim; LBBB = blốc nhánh bố trái; LVEF = phân suất tống máu thất trái; ms = milliseconds.
aClass của khuyến cáo.
bMức độ chứng cứ.
cTài liệu tham khảo ủng hộ khuyến cáo
Bảng B.Điều trị tái đồng bộ tim trong dự phòng đột tử tiên phát ở các bệnh nhân có rung nhĩ mạn tính với NYHA chức năng class III/class IV thay đổi
|
Các khuyến cáo |
Classa |
Levelb |
Ref.c |
|
CRT cần được xem xét để giảm tử suất do mọi nguyên nhân ở bệnh nhân suy tim mạn tính, QRS ≥120 ms và LVEF ≤ 35% với NYHA chức năng class III / class IV thay đổi mặc dù điều trị nội khoa tối ưu ít nhất là 3 tháng, người đang hy vọng sống sót ít nhất là 1 năm với tình trạng chức năng tốt, được cung cấp tạo nhịp 2 thất càng sát nhau càng tốt có thể đạt đến 100%. |
IIa |
B |
330, 331 |
|
Triệt phá bộ nối AV cần được xem xét ở trường hợp tạo nhịp hai thất không hoàn toàn. |
B |
B |
332, 333 |
AV = nhĩ thất; CRT = điều trị tái đồng bộ tim; HF = suy tim; LVEF = phân suất tống máu; ms = milliseconds; NYHA = Hội Tim Mạch New York.
aClass của khuyến cáo.
bMức độ chứng cứ.
cTài liệu tham khảo ủng hộ khuyến cáo
Đối với bệnh nhân nhịp xoang, kiến nghị được để nghị liên quan đến LBBB đối lại với hình thái không phải dạng LBBB và cũng liên quan đến thời gian QRS (120-150 ms so với > 150 ms) [10] (Bảng A trong phần này). Đối với bệnh nhân RN, kiến nghị được trình bày ở bảng B trong phần này.
Hai RCT lớn (Comparison of Medical Therapy, Pacing, and Defibrillation in Heart failure Trial: COMPANION. Cardiac Resynchronization – Heart Failure Trial: CARE-HF)) [313] về So sánh Điều trị Nội khoa, Tạo nhịp tim và Khử rung tim trong Suy tim và Tái đồng bộ tim trong Suy timl 314] ở những bệnh nhân HF vừa đến nặng (class III-IV) và nhịp xoang đã cho thất CRT làm giảm tỷ lệ bệnh suất và tử suất ở quần thể này.
So Sánh liên quan đến bệnh nhân HFrEF có thời gian QRS ≥120 ms. Khi so sánh với các bệnh nhân điều trị nội khoa tối ưu đơn thuần, xu hướng giảm tử suất do mọi nguyên nhân đã được quan sát với tạo nhịp tim CRT (CRT-P) [HR 0,76 (95% CI 0.58, 1.01), P = 0,059] và giảm 36% đã được nhân thấy với CRT-D [HR 0,64 (95% CI 0.48, 0.86), P = 0,003], làm giảm tỷ lệ SCD trong nghiên cứu này, nhưng không phải CRT-P.
Trong khi các tiêu chí cho thời gian QRS cũng là ≥120 ms trong CARE-HF, tiêu chí bổ sung cho rối loạn đồng bộ phải được đáp ứng ở những bệnh nhân có khoảng thời gian QRS 120-149 ms. CRT-P giảm tử suất do mọi nguyên nhân tử vong bằng 36% [HR 0,64 (9536% CI 0.48, 0.85), P <0,002]. [64] Trong một báo cáo được mở rộng từ thử nghiệm CARE-HF (có nghĩa là theo dõi 37 tháng), CRT-P cũng giảm 46% đột tử [HR 0,54 (9536% CI 0.35, 0.84), P = 0,005], với việc giảm tỉ lệ tử vong tại thời điểm đó là 40% [HR 0.60 (9536% CI 0.47, 0.77) , P <0,001]. [335].
COMPANION và CARE-HF cùng nhau cung cấp bằng chứng mạnh mẽ ủng hộ việc sử dụng CRT (CRT-P hoặc CRT-D) ở những bệnh nhân HfrEF có các triệu chứng từ vừa đến nặng có khoảng thời gian QRS kéo dài, đặc biệt là ở những người có dạng LBBB. Một số nghiên cứu khác, đăng ký và phân tích gộp đã giải quyết vấn đề đáp ứng với CRT dựa trên hình thái QRS và đa số ủng hộ quan điểm vể hình thái QRS với dạng LBBB xác định nhóm các bệnh nhân với lợi ích gia tăng; phác thảo ngắn của nghiên cứu chính, đăng ký và phân tích gộp đã được báo cáo ở đây.
Các tư liệu từ Medicare ICD Registry, [326] trong đó gồm 14 946 bệnh nhân, cho thấy CRT-D đã không có hiệu quả ở bệnh nhân RBBB, khi cho thấy tử suất đã tăng lên trong 3 năm ở RBBB so với LBBB [HR 1.37 (95% CI 1,26 , 1,49), P <0,001]. Nghiên cứu Tái đồng bộ Làm đảo ngược Tái cấu trúc (REsynchronization reVErses Remodeling in Systolic left vEntricular dysfunction: REVERSE) [336] khẳng định việc giảm tiêu chí lâm sàng hỗ hợp chỉ ở những bệnh nhân với LBBB (OR 0,53, P <0,0032) và cho thấy không có lợi ích ở những bệnh nhân không LBBB (OR 0,74, P = 0,21). Tương tự như vậy, phân tích hình thái học QRS trong nghiên cứu MADIT-CRT [322] cho thấy giảm tiêu chí đầu tiên ở những bệnh nhân có hình thái QRS LBBB (HR 0,47, P <0,001), nhưng không phải ở những bệnh nhân không có hình thái QRS LBBB (HR 1,24, P = 0,257 ). Cũng đáng chú ý, các nguy cơ của VT, VF và tử vong đã giảm đáng kể chỉ có ở những bệnh nhân với LBBB. Một phân tích dài hạn liên quan tới các bệnh nhân trong MADIT-CRT đã được công bố gần đây, [148] khẳng định sau 7 năm theo dõi các lợi ích sống còn của CRT-D đã được quan sát thấy ở những bệnh nhân với hình thái QRS LBBB [HR 0,59 (95% CI 0.43, 0,80), P <0,001] trong khi bệnh nhân không có hình thái LBBB cho thấy không có hiệu quả và có thể có hại liên quan với CRT-D [HR 1,57 (95% CI 1.03, 2.39) P = 0.04]. Khi tư liệu từ nghiên cứu Tái đồng bộ – Khử rung cho Suy tim Có thể đi lại được (Resynchronization–Defibrillation for Ambulatory Heart Failure Trial: RAFT) được phân tích, trên cơ sở dữ liệu hình thái QRS, điều trị CRT cho thấy lợi ích lớn hơn ở những bệnh nhân có LBBB đối lại không có hình thái LBBB. [323] Điều thú vị là bệnh nhân không có hình thái QRS LBBB QRS với thời gian QRS 0,160 ms thấy giảm khiêm tốn trong các hậu quả đầu tiên [HR 0,52 (95% CI 0.29, 096), P = 0,033]. Mặc dù thực tế chỉ có 53 bệnh nhân đã có mặt trong nhóm này, các lợi ích tiềm tàng của CRT trong không có hình thái QRS LBBBi trong sự có mặt của QRS giãn rộng đáng kể (QRS ≥160 ms) là giá trị đánh giá. Quan sát này được hỗ trợ bằng các kết quả phân tích gộp của Cleland và cộng sự, [334] liên quan đến tư liệu từ CARE-HF, MIRACLE ICD (Multicenter InSync ICD Randomized Clinical Evaluation) và RAFT. Mặc dù có một lợi ích rõ ràng của CRT ở bệnh nhân LBBB trong phân tích đơn biến, kết quả trong mô hình đa biến cho thấy chỉ có thời gian QRS được dự đoán phạm vi hiệu quả của CRT trên kết quả. Nery và cộng sự. [324] đã báo cáo một phân tích tổng hợp các thử nghiệm lâm sàng CRT nhắm mục tiêu đến 485 bệnh nhân có hình thái QRS RBBB và cho thấy không có lợi ích của điều trị tái đồng bộ [HR 2.04 (95% CI 1.32, 3.15), P = 0,001]; tiếc là không có dữ liệu về thời gian QRS đã được cung cấp.
. Sipahi và cộng sự [325] thực hiện phân tích gộp trong đó họ đã kiểm tra 33 thử nghiệm lâm sàng điều tra hiệu quả của hình thái QRS trên CRT, nhưng chỉ có bốn (COMPANION, CARE-HF, MADIT-CRT and RAFT) bao gồm các kết quả theo hình thái QRS. Khi họ đánh giá hiệu quả của CRT trên các biến cố lâm sàng bất lợi hỗn hợp ở 3349 bệnh nhân LBBB lúc ban đầu, người ta nhận thấy giảm 36% nguy cơ với việc sử dụng CRT [RR 0.64 (9536% CI 0.52, 0.77), P <0.00001]. Tuy nhiên, lợi ích như vậy đã không được quan sát thấy ở những bệnh nhân không bất thường dẫn truyền LBBB [RR 0.97 (9536% CI 0,82, 1,15), P = 0,75]. [325] Điều thú vị là, khi phân tích được giới hạn đối với thử nghiệm không ICD (CARE-HF và COMPANION), lợi ích của CRT vẫn chỉ quan sát được ở những bệnh nhân có LBBB (P <0.000001).
Trong phân tích gộp lớn gần đây của 6 RCT (COMPANION, CARE-HF, MADIT-CRT, MIRACLE, RAFT và REVERSE), [337] trong đó có 6914 người tham gia (1683 không có hình thái QRS LBBB QRS), CRT không liên quan với giảm tử vong và / hoặc nhập viện do HF ở bệnh nhân không có hình thái QRS LBBB [HR 1.09 (9536% CI 0.85, 1.39)]. [337]
Do đó QRS rộng với không có hình thái LBBB vẫn còn là một khu vực không chắc chắn cho CRT. Dựa trên những tư liệu này, mặc dù thực tế hầu hết các bệnh nhân ở châu Âu nhận được với CRT-D [314] khuyến nghị của chúng tôi được thể hiện CRT thông thường.
Có sự khác biệt trong văn bản trước đây [American College of Cardiology Foundation/AHA guidelines and the consensus document on pacing from the European Heart Rhythm Association (EHRA)/ESC] về các class của khuyến cáo cho CRT ở những bệnh nhân có QRS giữa 120 và 150 ms. Dựa trên phân tích gộp của Sipahi và cộng sự, [328] CRT làm giảm một cách có ý nghĩa tử suất do mọi nguyên nhân hay nhập viện ở bệnh nhân có thời gian QRS ≥150 ms [RR 0.60 (9536% CI 0.53, 0.67), P <0,001], nhưng không phải ở những bệnh nhân có thời gian QRS 120-150 ms [RR 0.95 (9536% CI 0.82, 1.10), P = 0,49]. Tuy nhiên, mối quan tâm về phương pháp luận do sự đa dạng của các phân tích trong nghiên cứu của Sipahi và cộng sự. đã được chỉ ra, [338] và do đó kết luận CRT chỉ có hiệu quả đối với bệnh nhân có QRS ≥150 ms nên tại thời điểm này được coi chỉ là một khám phá.[338]. CRT không được khuyến cáo ở những bệnh nhân suy tim có thời gian QRS < 120 ms. [339]
Ở bệnh nhân RN, CRT cần được xem xét ở những người LVEF giảm đáng kể, nhưng điều này đã không được chứng minh là làm giảm tỷ lệ tử vong hoặc tử vong đột ngột ở những bệnh nhân này. [8340] Trong thử nghiệm RAFT 229 (hoặc 13% tổng dân số 1798) bệnh nhân có AF hay cuống nhĩ ban đầu. [327] Mặc dù đã có chính thức không có tương tác đáng kể giữa nhịp cơ bản và hiệu quả điều trị (ICD đối lại với CRT-D, P = 0,14), số lượng bệnh nhân trong nghiên cứu này là nhỏ và các hiệu quả ở bệnh nhân rung nhĩ hoặc cuồng nhĩ xuất hiện ít hơn so với những người ở nhịp xoang. Thành công của CRT ở bệnh nhân rung nhĩ là, đối với phần lớn, xác định bằng mức độ của tạo nhịp hai thất, và điều này chỉ có thể được thực hiện bằng phương pháp triệt phá bộ nối AV ở nhiều bệnh nhân. [10]
Mặc dù quyết định để thực hiện triệt phá bộ nối AV ở những bệnh nhân này vẫn còn là một vấn đề gây tranh cãi, dữ liệu gần đây cho thấy sống sót lâu dài sau khi CRT trong số bệnh nhân AF được thực hiện triệt phá nút AV tương tự như những người được quan sát ở bệnh nhân nhịp xoang. [333] Trong bản tóm tắt, CRT có thể được xem xét ở những bệnh nhân suy tim, AF vĩnh viễn và có LVEF ≤35% if (i) tạo nhịp tâm thất được đòi hỏi hoặc các bệnh nhân khác đáp ứng tiểu chuẩn CRT và (ii) gần 100% tạo nhịp thất đạt được với CRT với triệt phá nút AV hoặc kiểm soát tần số bằng thuốc (class IIA – mức chứng cứu B).
6.1.4.2 Suy tim có phân suất tống máu thất trái giảm nhưng triệu chứng nhẹ (New York Heart Association class II)
Bảng C.Điều trị tái đồng bộ – khử rung tim trong phòng ngừa đột tử tim tiên phát ở các bệnh nhân còn nhịp xoang với suy tim nhẹ (New York Heart Association class II)
|
Các khuyến cáo |
Classa |
Levelb |
Ref.c |
|
CRT-D được khuyến cáo để giảm tử suất toàn bộ ở các bệnh nhân có khoảng QRS ≥130 ms, có LVEF ≤30% và LBBB mặc dù điều trị thuốc tối ưu ít nhất 3 tháng và mong muốn sống sót ít nhất 1 năm với trạng thái chức năng tốt. |
I |
A |
148, 322, 323, 325, 327, 329 |
|
CRT-D có thể xem xét để phóng ngừa nhập viện cho HF ở các bệnh nhân có khoảng QRS ≥150 ms, bất chấp hình dạng QRS, LVEF ≤35% mặc dù điều trị nội tối ưu ít nhất 3 tháng với bệnh nhân mong muốn sống sót với trạng thái chức năng tốt ít nhất 1 năm. |
IIb |
IA |
148, 327– 329, 334 |
CRT-D = điều trị tái đồng bộ khử rung tim; HF = suy tim; LBBB = blốc bó nhánh trái; LVEF = phân suất tống máu thất trái; ms = milliseconds.
a Đây là khuyến cáo chuyên biệt cho CRT-D, từ các nghiên cứu về hiệu quả tái đồng bộ ở bệnh nhân có NYHA class II chỉ sử dụng CRT-D.
bClass khuyến cáo
c Mức độ bằng chứng.
dTài liệu tham khảo ủng hộ khuyến cáo.
Hai nghiên cứu ngẫu nhiên có đối chứng 3618 bệnh nhân suy tim nhẹ đưa vào điều trị thuốc cộng với ICD hoặc điều trị thuốc tối ưu cộng với CRT-D. [327.329] Các nghiên cứu MADIT-CRT [329] 1820 bệnh nhân có triệu chứng nhẹ (NYHA I hoặc II) và những người đã có LVEF ≤30% với thời gian QRS ≥130 ms. Các báo cáo ban đầu cho thấy giảm 34% trong tiêu chí đầu tiên của tử vong do mọi nguyên nhân hoặc biến cố HF [25.3% vs. 17.2% cho ICD đối lại CRT-D; HR 0.66 (95% CI 0.52, 0.84), P = 0.001].. Trong thông báo theo dõi dài hạn từ MADIT- CRT (theo dõi trung bình 7 năm), [148] CRT-D làm giảm tử suất một cách có ý nghĩa [HR 0,59 (9536% CI 0.43, 0.80), P <0,001] so với chỉ ICD, tuy nhiên, chúng được thực hiện trên cơ sở với bệnh nhân có LBBB, trong khi không có hiệu quả lợi ích được quan sát ở những bệnh nhân không có LBBB (P <0,001 cho tác dụng lẫn nhau) (Bảng C trong phần này).
Nghiên cứu RAFT [327] ở 1798 bệnh nhân HF nhẹ đến trung bình (NYHA II hoặc III), LVEF ≤30% và thời gian QRS ≥120 ms (hoặc thời gian QRS nhịp độ ≥200 ms). So với các bệnh nhân với ICD đơn độc, nhóm CRT-D cho thấy giảm 25% RR trong tử suất do tất cả các nguyên nhân [HR 0.75 (95% CI 0,62, 0,91), P = 0,003], minh chứng việc sử dụng hệ thống điều trị CRT ở bệnh nhân HFrEF có triệu chứng nhẹ.
6.2 Các phức hợp thất sớm ở những bệnh nhân có bệnh tim thực thể / rối loạn chức năng thất trái
Điều trị bệnh nhân rối loạn chức năng thất trái và phức hợp thất sớm
|
Khuyến cáo |
Classa |
Levelb |
Ref.c |
|
Ở các bệnh nhân có PVC hoặc NSVT thường xuyên có triệu chứng: |
|
|
|
|
– Amiodarone cần được xem xét. |
IIa |
B |
64 |
|
– Triệt phá qua Catheter cần được xem xét |
IIa |
B |
341-343 |
|
– Triệt phá qua Catheter cần được xem xét ở các bệnh nhân rối loạn chức năng LV có PVCs. |
IIa |
B |
341– 343 |
LV = thất trái; NSVT = nhịp nhanh thất tạm thời; PVC = phức bộ thất sớm.
aClass khuyến cáo.
bMức độ biến chứng.
cTài liệu ủng hộ các khuyến cáo.
PVC và các cơn NSVT rất phổ biến ở những bệnh nhân có rối loạn chức LV và có thể là hậu quả hoặc gây rối loạn chức năng LV. PVC và các cơn NSVT ở người có bệnh tim thực thể góp phần vào tăng nguy cơ tử vong, > 10 PVCs mỗi giờ hoặc các cơn NSVT là một dấu hiệu nguy cơ tăng lên có thể được thừa nhận. [[344]] Nếu bệnh nhân có triệu chứng do PVC hoặc NSVTs, hoặc nếu PVC hoặc NSVTs góp phần giảm LVEF (‘tim đập nhanh gây ra bệnh cơ tim), amiodarone hoặc catheter ablation nên được xem xét.
Một gánh nặng PVC cao (.> 24%) ở những bệnh nhân có rối loạn chức năng LV và một khoảng ghép ngắn hơn của các PVC (<300 ms) gợi ý bệnh cơ tim do PVC gây ra. [[342]] Ở những bệnh nhân như vậy, triệt phá qua catheter có thể ngăn chặn các PVC và phục hồi chức năng LV. [341]
6.3 Nhịp nhanh thất dai dẳng
6.3.1 Điều trị thuốc
Điều trị bệnh nhân rối loạn chức năng thất trái và nhịp nhanh thất đơn hình tái phát dai dẳng.
|
Khuyến cáo |
Classa |
Levelb |
Ref.c |
|
Tối ưu hóa thuốc điều trị HF theo hướng dẫn HF hiện hành được khuyến cáo ở những bệnh nhân có rối loạn chức LV và VT dai dẳng. |
I |
C |
8 |
|
Điều trị Amiodarone nên được xem xét để ngăn chặn ở các bệnh nhân có hoặc không có ICD. |
IIa |
C |
64 |
HF = suy tim; LV = thất trái; ICD = máy khử rung tim có thể cấy; VT = nhịp nhanh thất.
a Class khuyến cáo.
bMức độ bằng chứng.
c Tài liệu ủng hộ khuyến cáo.
Bệnh nhân có rối loạn chức năng LV có hoặc không có HF biểu hiện VT dai dẳng cần được điều trị theo hướng dẫn HF xuất bản gần đây, tương tự như những bệnh nhân có rối loạn chức năng LV mà không VT. [8] Ngoài ra, điều trị bằng thuốc nội khoa cho VT dai dẳng nên nhắm mục tiêu phong tỏa tối đa giao cảm. Trong nghiên cứu MADIT-II, bệnh nhân với ICD điều trị với liều cao nhất beta-blockers đã cho thấy giảm một cách có ý nghĩa các cơn tái phát của VT hay VF đòi can thiệp ICD so với bệnh nhân không dùng beta-blockers [HR 0.48 (95% CI 0.26, 0.89), P = 0.02]. [8]. Điều trị thuốc tối ưu trong nghiên cứu OPTIC (Optimal Pharmacological Therapy in Cardioverter Defibrillator Patients (OPTIC) study) đã so sánh sử dụng beta-blockers, sotalol và beta-blockers cộng với amiodarone cho dự phòng chống các sốc ICD. [156] Điều trị Amiodarone cộng beta-blocker giảm một cách có ý nghĩa nguy cơ sốc so với điều trị betablocker [HR 0.27 (95% CI 0.14, 0.52), P <0,001] và sotalol đơn thuần [HR 0.43 (95% CI 0.22, 0.85), P = 0.02]. Tuy nhiên, khi ngừng thuốc các bệnh nhân dùng sotalol và phối hợp amiodarone và beta blockers thường xuyên hơn.. Tần số nghiên cứu ngưng thuốc trong 1 năm là 18,2% đối với amiodarone, 23,5% cho sotalol và 5,3% đối với beta-blocker đơn thuần.
Trong nghiên cứu SCD-HeFT, bệnh nhân có rối loạn chức năng LV và NYHA II hoặc HF III nhận được điều trị HF thông thường, liệu pháp thông thường cộng với amiodarone hoặc liệu pháp thông thường và ICD một buồng. [64] So với điều trị suy tim thông thường, việc bổ sung các amiodarone không tăng tỷ lệ tử vong.
6.3.2 Triệt phá qua catheter
Phòng ngừa tái phát nhịp nhanh thất ở bệnh nhân rối loạn chức năng thất trái và nhịp nhanh thất dai dẳng.
|
Khuyến cáo |
Classa |
Levelb |
Ref.c |
|
Triệt phá qua catheter cấp cứu ở những trung tâm chuyên khoa hoặc có kinh nghiệm được khuyến cáo ở các bệnh nhân có VT liên hồi hoặc bão điện do sốc ICD. |
I |
B |
183 |
|
Amiodarone hoặc triệt phá qua catheter được khuyến cáo ở các BN có sốc ICD tái phát do VT dai dẳng. |
I |
B |
64,156, 184– 186 |
|
ICD cấy được khuyến cáo ở những bệnh nhân trải qua triệt phá qua catheter bất cứ khi nào họ đáp ứng đủ tiêu chuẩn cho ICD. |
I |
C |
|
|
Ý kiến này của các chuyên gia Amiodarone hoặc triệt phá qua catheter cần được xem xét sau khi tập đầu tiên của VT bền vững ở những bệnh nhân với một ICD. |
IIa |
B |
64, 184– 186 |
ICD = Máy khử rung tim có thể cấy; VT = nhịp nhanh thât.
aClass của các khuyến cáo.
bMức độ bằng chứng.
cTài liệu ủng hộ khuyến cáo.
Tùy thuộc vào các bệnh nền, triệt phá qua catheter cho VT dai dẳng có thể tạo ra kết quả cắt cơn cấp thời, giảm các cơn VT tái phát ở bệnh nhân bệnh tim cấu trúc.
6.3.2.1 Bệnh nhân rối loạn chức năng thất trái
Ở những bệnh nhân có rối loạn chức LV và VT dai dẳng, vào lại qua trung gian sẹo là cơ chế sinh lý bệnh phổ biến và triệt phá nhằm dích eo giới hạn trong phạm vi vòng vào lại. VT chủ yếu là đơn hình. Nếu ECG 12 chuyển đạo của VT lâm sàng không có sẵn ở những bệnh nhân ICD, độ dài chu kỳ của điện đồ ICD được lưu trong quá trình VT có thể dễ nhận biết VT lâm sàng trong quá trình nghiên cứu điện sinh lý. Triệt phá qua catheter tưới rửa (Irrigated) thường được sử dụng, trong đó tạo điều kiện hình thành tổn thương sâu hơn và làm giảm nguy cơ hình thành than cháy trong suốt thời gian phóng năng lượng.
Hiện nay, các chiến lược triệt phá tốt nhất là không rõ. Còn thiếu RCT so sánh triệt phá qua cahteter trong quá trình VT với một cách tiếp cận dựa trên nền bệnh cơ bản. Ngoài ra, không có sự đồng thuận đối với tiêu chỉ thủ thật lý tương. Trong khi loại bỏ tất cả VTs lâm sàng cần nỗ lực, không có khả năng tạo ra của bất kỳ VT sau khi triệt phá có thể là tiêu chí thử thuật được ưa chuộng.
Bệnh nhân có thể có bão điện. Triệt phá qua catheter có thể ngăn chặn biến cố có khả năng nguy hiển đến tính mạng này một cách cấp thời và đã được chứng minh là làm giảm tỷ lệ các cơn bão điện tái phát khi so sánh với chỉ điều trị bằng thuốc. [183] Bệnh nhân VT liên quan đến sẹo sau cơ tim có xu hướng có kết quả tốt hơn sau triệt phá qua catheter so với bệnh nhân VT do bệnh cơ tim không do thiếu máu cục bộ. Năm nghiên cứu tiền cứu đã đánh giá vai trò của triệt phá qua catheter trong điều trị VT dai dẳng. [184-188] Nghiên cứu Nhiệt lạnh Đa trung tâm (Multicenter Thermocool study) báo cáo tỷ lệ thành công cấp thời, được xác định khi xóa bỏ tất cả VTs có thể tạo ra là 49% và không bị các cơn VT 53% qua theo dõi 6 tháng. [185] Trong nghiên cứu Nhóm Khám phá Tần số Radio được Làm lạnh Đa trung tâm (Cooled RF Multi Center Investigators Group study), thành công cấp thời, được xác định khi loại bỏ tất cả các VTs có thể được tạo ra, đạt được ở 41% bệnh nhân. [184] Không bị VA tái phát được nghi nhận ở 46% bệnh nhân trong vòng 8 ± 5 tháng theo dõi. Trong nghiên cứu tiền cứu Euro-VT, triệt phá thành công cấp thời ở 81% bệnh nhân và không bị VT tái phát đã đạt được ở 51% bệnh nhân. [186] Nghiên cứu Lập bản đồ Nền bệnh và Triệt phá ở Nhịp xoang với Nhịp nhanh Thất Không đồng đều (Halt) (Substrate Mapping and Ablation in Sinus Rhythm to Halt Ventricular Tachycardia Trial: SMASH-VT) đã đánh giá vai trò của triệt phá qua catheter ở bệnh nhân nhồi máu cơ tim trước đó và LVEF giảm. [187] Các bệnh nhân trải qua cấy ICD cho VF, VT huyết động không ổn định hoặc ngất do VT có thể tạo ra trong quá trình nghiên cứu điện sinh lý xâm lấn. Về phương diện đối chứng chỉ trải qua cấy ICD. Không ai trong số các bệnh nhân nhận thuốc chống loạn nhịp. Triệt phá qua catheter được thực hiện bằng cách sử dụng phương pháp tiếp cận mục tiêu là các điện thế thất bất thường được hướng dẫn bằng nền bệnh cơ bản trong quá trình nhịp xoang không cần tạo ra VT. Quá trình theo dõi trung bình 23 ± 6 tháng đã giảm một cách có ý nghĩa tỷ lệ các cơn VT, từ 33% trong nhóm đối chứng tới 12% ở nhóm được triệt phá. Hơn nữa, tần số các sốc ICD phù hợp giảm từ 31% xuống 9% sau triệt phá qua catheter.
Nghiên cứu Triệt phá Nhịp nhanh Thất trong Bệnh Tim Mạch vành (Ventricular Tachycardia Ablation in Coronary Heart Disease: VTACH) tiền cứu ngẫu nhiên các bệnh nhân có nhồi máu cơ tim trước đó, phân suất tống máu giảm (≤50%) và VT ổn định về huyết động học để triệt phá qua catheter hoặc không điều trị bổ xung, ngoài ICD tiếp theo. [188] Tiểu chi đầu tiên là thời gian tái phát VT hoặc VF đầu tiên. Tần số sống sót do không bị VT tái phát qua 24 tháng là cao hơn ở nhóm triệt phá so với nhóm chứng [47%, so với 29%, HR 0.61 (95% CI 0.37, 0.99), P = 0,045]. Số lượng trung bình các sốc ICD thích hợp cho mỗi bệnh nhân mỗi năm giảm từ 3,4 ± 9,2-0,6 ± 2,1 ở bệnh nhân trải qua triệt phá qua catheter (P = 0,018). Triệt phá qua catheter không ảnh hưởng đến tử suất.
Nhìn chung, tỷ lệ thành công triệt phá qua catheter cho VT được xác định bởi số lượng giới hạn sẹo nhồi máu liên quan, biểu hiện là vùng điện thế thấp trên hệ thống lập bản đồ điện giải phẫu, [209] trong khi thiết bị chuyên dụng để điều trị các bệnh nhân trải qua triệt phá qua catheter của VT có thể tác động đến kết qua một cách tích cực.
6.3.2.2 Nhịp nhanh vào lại nhánh bó
Dự phòng tái phát nhịp nhanh thất ở bệnh nhân có nhịp nhanh vào lại nhánh bó.
|
Các khuyến cáo |
Classa |
Levelb |
Ref.c |
|
Triệt phá qua catheter như là điều trị đầu tiên được khuyến cáo ở các bệnh nhân biểu hiện nhịp nhanh vào lại nhánh bó |
C |
C |
345, 346 |
aClass của các khuyến cáo.
bMức độ bằng chứng.
cTài liệu ủng hộ khuyến cáo.
Nhịp nhanh nhánh bó là nhịp nhanh vào lại vòng lớn hiếm gặp thường liên quan đến các nhánh bên phải là đường xuôi và nhánh còn lại là đường ngược. Trên ECG bề mặt 12 chuyển đạo, hinh thái LBBB với trục lệch trái được nhận thấy. Vào lại nhánh bó thường được gắn liền với bệnh cơ tim. [347] Triệt phá qua catheter một trong những nhánh bó là điều trị, mặc dù các nhánh bên phải là mục tiêu ưa thích, vì nó có thể dễ dàng tiếp cận hơn triệt phá.[347]. Khi các cấu trúc bất thường cơ bản vẫn không thay đổi, đặt đồng thời một ICD cần mạnh mẽ xem xét. [347]
6.3.3 Máy khử rung tim có thể cấy
Cấy ICD ở bệnh nhân VT dai dẳng đã tăng sự sống sót so với điều trị bằng thuốc chống loạn nhịp. Cho đến nay, không có thử nghiệm được tiến hành so sánh triệt phá qua catheter cho VT dai dẳng nhưng không cấy ICD và chỉ cấy ICD. Theo quan điểm về sự hiếm có các dữ liệu và tốc độ khá cao tái phát sau triệt phá qua catheter cho VT dai dẳng, Cấy ICD nên được xem xét trong tất cả các bệnh nhân có rối loạn chức năng LV (phân suất tống máu < 45%) và VT dai dẳng.
(Còn nữa )
Tài liệu tham khảo
1. Zipes DP, Camm AJ, Borggrefe M, Buxton AE, Chaitman B, Fromer M, Gregoratos G, Klein G, Moss AJ, Myerburg RJ, Priori SG, Quinones MA, Roden DM, Silka MJ, Tracy C, Blanc JJ, Budaj A, Dean V, Deckers JW, Despres C, Dickstein K, Lekakis J, McGregor K, Metra M, Morais J, Osterspey A, Tamargo JL, Zamorano JL, Smith SC Jr, Jacobs AK, Adams CD, Antman EM, Anderson JL, Hunt SA, Halperin JL, Nishimura R, Ornato JP, Page RL, Riegel B. ACC/AHA/ESC 2006 guidelines for management of patients with ventricular arrhythmias and the prevention of sudden cardiac death – executive summary: a report of the American College of Cardiology/American Heart Association Task Force and the European Society of Cardiology Committee for Practice Guidelines (Writing Committee to Develop Guidelines for Management of Patients with Ventricular Arrhythmias and the Prevention of Sudden Cardiac Death) Developed in collaboration with the European Heart Rhythm Association and the Heart Rhythm Society. Eur Heart J 2006;27: 2099–2140.
2. Aliot EM, Stevenson WG, Almendral-Garrote JM, Bogun F, Calkins CH, Delacretaz E, Bella PD, Hindricks G, Jais P, Josephson ME, Kautzner J, Kay GN, Kuck KH, Lerman BB, Marchlinski F, Reddy V, Schalij MJ, Schilling R, Soejima K, Wilber D, European Heart Rhythm Association, European Society of Cardiology, Heart Rhythm Society. EHRA/HRS Expert Consensus on Catheter Ablation of Ventricular Arrhythmias: developed in a partnership with the European Heart Rhythm Association (EHRA), a Registered Branch of the European Society of Cardiology (ESC), and the Heart Rhythm Society (HRS); in collaboration with the American College of Cardiology (ACC) and the American Heart Association (AHA). Europace 2009;11: 771–817.
3. Pedersen CT, Kay GN, Kalman J, Borggrefe M, Della-Bella P, Dickfeld T, Dorian P, Huikuri H, Kim YH, Knight B, Marchlinski F, Ross D, Sacher F, Sapp J, Shivkumar K, Soejima K, Tada H, Alexander ME, Triedman JK, Yamada T, Kirchhof P, Document R, Lip GY, Kuck KH, Mont L, Haines D, Indik J, Dimarco J, Exner D, Iesaka Y, Savelieva I. EHRA/HRS/APHRS expert consensus on ventricular arrhythmias. Europace 2014;16:1257–1283.
4. Vardas PE, Auricchio A, Blanc JJ, Daubert JC, Drexler H, Ector H, Gasparini M, Linde C, Morgado FB, Oto A, Sutton R, Trusz-Gluza M, European Society of Cardiology, European Heart Rhythm Association. Guidelines for cardiac pacing and cardiac resynchronization therapy. The Task Force for Cardiac Pacing and Cardiac Resynchronization Therapy of the European Society of Cardiology. Developed in collaboration with the European Heart Rhythm Association. Europace 2007;9: 959–998.
5. Epstein AE, DiMarco JP, Ellenbogen KA, Estes NA 3rd, Freedman RA, Gettes LS, Gillinov AM, Gregoratos G, Hammill SC, Hayes DL, Hlatky MA, Newby LK, Page RL, Schoenfeld MH, Silka MJ, Stevenson LW, Sweeney MO, Smith SC Jr, Jacobs AK, Adams CD, Anderson JL, Buller CE, Creager MA, Ettinger SM, Faxon DP, Halperin JL, Hiratzka LF, Hunt SA, Krumholz HM, Kushner FG, Lytle BW, Nishimura RA, Ornato JP, Page RL, Riegel B, Tarkington LG, Yancy CW. ACC/AHA/HRS 2008 Guidelines for Device-Based Therapy of Cardiac Rhythm Abnormalities: a report of the American College of Cardiology/ American Heart Association Task Force on Practice Guidelines (Writing Committee to Revise the ACC/AHA/NASPE 2002 Guideline Update for Implantation of Cardiac Pacemakers and Antiarrhythmia Devices) developed in collaboration with the American Association for Thoracic Surgery and Society of Thoracic Surgeons. J Am Coll Cardiol 2008;51:e1–62.
6. Goldberger JJ, Cain ME, Hohnloser SH, Kadish AH, Knight BP, Lauer MS, Maron BJ, Page RL, Passman RS, Siscovick D, Stevenson WG, Zipes DP. American Heart Association/American College of Cardiology Foundation/Heart Rhythm Society scientific statement on noninvasive risk stratification techniques for identifying patients at risk for sudden cardiac death: a scientific statement from the American Heart Association Council on Clinical Cardiology Committee on Electrocardiography and Arrhythmias and Council on Epidemiology and Prevention. Circulation 2008;118:1497–1518
7. Dickstein K, Vardas PE, Auricchio A, Daubert JC, Linde C, McMurray J, Ponikowski P, Priori SG, Sutton R, van Veldhuisen DJ. 2010 focused update of ESC Guidelines on device therapy in heart failure: an update of the 2008 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure and the 2007 ESC Guidelines for cardiac and resynchronization therapy. Developed with the special contribution of the Heart Failure Association and the European Heart Rhythm Association. Eur J Heart Fail 2010;12:1143–1153.
8. McMurray JJ, Adamopoulos S, Anker SD, Auricchio A, Bohm M, Dickstein K, Falk V, Filippatos G, Fonseca C, Gomez-Sanchez MA, Jaarsma T, Kober L, Lip GY, Maggioni AP, Parkhomenko A, Pieske BM, Popescu BA, Ronnevik PK, Rutten FH, Schwitter J, Seferovic P, Stepinska J, Trindade PT, Voors AA, Zannad F, Zeiher A. ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure 2012: The Task Force for the Diagnosis and Treatment of Acute and Chronic Heart Failure 2012 of the European Society of Cardiology. Developed in collaboration with the Heart Failure Association (HFA) of the ESC. Eur Heart J 2012;33:1787–1847.
9. Yancy CW, Jessup M, Bozkurt B, Butler J, Casey DE Jr, Drazner MH, Fonarow GC, Geraci SA, Horwich T, Januzzi JL, Johnson MR, Kasper EK, Levy WC, Masoudi FA, McBride PE, McMurray JJ, Mitchell JE, Peterson PN, Riegel B, Sam F, Stevenson LW, Tang WH, Tsai EJ, Wilkoff BL. 2013 ACCF/AHA guideline for the management of heart failure: executive summary: a report of the American College of Cardiology Foundation/American Heart Association Task Force on practice guidelines. Circulation 2013;128:1810–1852.
10. Brignole M, Auricchio A, Baron-Esquivias G, Bordachar P, Boriani G, Breithardt OA, Cleland J, Deharo JC, Delgado V, Elliott PM, Gorenek B, Israel CW, Leclercq C, Linde C, Mont L, Padeletti L, Sutton R, Vardas PE, Zamorano JL, Achenbach S, Baumgartner H, Bax JJ, Bueno H, Dean V, Deaton C, Erol C, Fagard R, Ferrari R, Hasdai D, Hoes AW, Kirchhof P, Knuuti J, Kolh P, Lancellotti P, Linhart A, Nihoyannopoulos P, Piepoli MF, Ponikowski P, Sirnes PA, Tamargo JL, Tendera M, Torbicki A, Wijns W, Windecker S, Document R, Kirchhof P, Blomstrom-Lundqvist C, Badano LP, Aliyev F, Bansch D, Baumgartner H, Bsata W, Buser P, Charron P, Daubert JC, Dobreanu D, Faerestrand S, Hasdai D, Hoes AW, Le Heuzey JY, Mavrakis H, McDonagh T, Merino JL, Nawar MM, Nielsen JC, Pieske B, Poposka L, Ruschitzka F, Tendera M, Van Gelder IC, Wilson CM. 2013 ESC Guidelines on cardiac pacing and cardiac resynchronization therapy: the Task Force on cardiac pacing and resynchronization therapy of the European Society of Cardiology (ESC). Developed in collaboration with the European Heart Rhythm Association (EHRA). Eur Heart J 2013;34:2281–2329.
11. Epstein AE, DiMarco JP, Ellenbogen KA, Estes NA 3rd, Freedman RA, Gettes LS, Gillinov AM, Gregoratos G, Hammill SC, Hayes DL, Hlatky MA, Newby LK, Page RL, Schoenfeld MH, Silka MJ, Stevenson LW, Sweeney MO, American College of Cardiology Foundation, American Heart Association Task Force on Practice Guidelines, Heart Rhythm Society. 2012 ACCF/AHA/HRS focused update incorporated into the ACCF/AHA/HRS 2008 guidelines for device-based therapy of cardiac rhythm abnormalities: a report of the American College of Cardiology Foundation/American Heart Association Task Force on Practice Guidelines and the Heart Rhythm Society. Circulation 2013;127:e283–352.
12. Kusumoto FM, Calkins H, Boehmer J, Buxton AE, Chung MK, Gold MR, Hohnloser SH, Indik J, Lee R, Mehra MR, Menon V, Page RL, Shen WK, Slotwiner DJ, Stevenson LW, Varosy PD, Welikovitch L. HRS/ACC/AHA expert consensus statement on the use of implantable cardioverter-defibrillator therapy in patients who are not included or not well represented in clinical trials. J Am Coll Cardiol 2014;64:1143–1177.
13. Windecker S, Kolh P, Alfonso F, Collet JP, Cremer J, Falk V, Filippatos G, Hamm C, Head SJ, Juni P, Kappetein AP, Kastrati A, Knuuti J, Landmesser U, Laufer G, Neumann FJ, Richter DJ, Schauerte P, Sousa Uva M, Stefanini GG, Taggart DP, Torracca L, Valgimigli M, Wijns W, Witkowski A. 2014 ESC/EACTS Guidelines on myocardial revascularization: the Task Force on Myocardial Revascularization of the European Society of Cardiology (ESC) and the European Association for Cardio-Thoracic Surgery (EACTS) developed with the special contribution of the European Association of Percutaneous Cardiovascular Interventions (EAPCI). Eur Heart J 2014;35:2541–2619.
14. Priori SG, Wilde AA, Horie M, Cho Y, Behr ER, Berul C, Blom N, Brugada J, Chiang CE, Huikuri H, Kannankeril P, Krahn A, Leenhardt A, Moss A, Schwartz PJ, Shimizu W, Tomaselli G, Tracy C. Executive summary: HRS/ EHRA/APHRS expert consensus statement on the diagnosis and management of patients with inherited primary arrhythmia syndromes. Europace 2013;15: 1389–1406.
15. Fishman GI, Chugh SS, Dimarco JP, Albert CM, Anderson ME, Bonow RO, Buxton AE, Chen PS, Estes M, Jouven X, Kwong R, Lathrop DA, Mascette AM, Nerbonne JM, ORourke B, Page RL, Roden DM, Rosenbaum DS, Sotoodehnia N, Trayanova NA, Zheng ZJ. Sudden cardiac death prediction and prevention: report from a National Heart, Lung, and Blood Institute and Heart Rhythm Society Workshop. Circulation 2010;122:2335–2348.
16. Byard RW, Ranson D, Krous HF, Workshop P. National Australian workshop consensus on the definition of SIDS and initiation of a uniform autopsy approach to unexpected infant and early childhood death. Forensic Sci Med Pathol 2005;1: 289–292.
17. Basso C, Burke M, Fornes P, Gallagher PJ, de Gouveia RH, Sheppard M, Thiene G, van der Wal A, Association for European Cardiovascular P. Guidelines for autopsy investigation of sudden cardiac death. Virchows Arch 2008;452:11–18.
18. Priori S, Schwartz P, Bardy G, Bigger JJ, Borggrefe M, Camm A, Cobb L, Ewy G, Hauer R, Kuck K, Lane R, Lazzara R, Marcus F, Muller J, Myerburg R, Touboul P, Verrier R, Wellens H, Zipes D. Survivors of out-of-hospital cardiac arrest with apparently normal heart. Need for definition and standardized clinical evaluation. Consensus Statement of the Joint Steering Committees of the Unexplained Cardiac Arrest Registry of Europe and of the Idiopathic Ventricular Fibrillation Registry of the United States. Circulation 1997;95:265–272.
19. Niemeijer MN, van den Berg ME, Leening MJ, Hofman A, Franco OH, Deckers JW, Heeringa J, Rijnbeek PR, Stricker BH, Eijgelsheim M. Declining incidence of sudden cardiac death from 1990–2010 in a general middle-aged and elderly population: the Rotterdam Study. Heart Rhythm 2015;12:123–129.
20. Mendis SPP, Norrving B. Global Atlas on Cardiovascular Disease Prevention and Control. Geneva: World Health Organization, 2011. 21. Eckart RE, Shry EA, Burke AP, McNear JA, Appel DA, Castillo-Rojas LM, Avedissian L, Pearse LA, Potter RN, Tremaine L, Gentlesk PJ, Huffer L, Reich SS, Stevenson WG, Department of Defense Cardiovascular Death Registry G. Sudden death in young adults: an autopsy-based series of a population undergoing active surveillance. J Am Coll Cardiol 2011;58:1254–1261.
22. Maron BJ, Gohman TE, Aeppli D. Prevalence of sudden cardiac death during competitive sports activities in Minnesota high school athletes. J Am Coll Cardiol 1998; 32:1881–1884.
23. van der Werf C, Hendrix A, Birnie E, Bots ML, Vink A, Bardai A, Blom MT, Bosch J, Bruins W, Das CK, Koster RW, Naujocks T, Schaap B, Tan HL, de Vos R, de Vries P, Woonink F, Doevendans PA, van Weert HC, Wilde AA, Mosterd A, van Langen IM. Improving usual care after sudden death in the young with focus on inherited cardiac diseases (the CAREFUL study): a community-based intervention study. Europace 2015 Apr 1. pii: euv 059 [Epub ahead of print].
24. United Nations Economic Commission for Europe. UNECE statistical database. Available at http://w3.unece.org/pxweb.
25. Van Camp SP, Bloor CM, Mueller FO, Cantu RC, Olson HG. Nontraumatic sports death in high school and college athletes. Med Sci Sports Exerc 1995;27:641–647.
26. Corrado D, Basso C, Rizzoli G, Schiavon M, Thiene G. Does sports activity enhance the risk of sudden death in adolescents and young adults? J Am Coll Cardiol 2003;42:1959–1963.
27. Maron BJ, Doerer JJ, Haas TS, Tierney DM, Mueller FO. Sudden deaths in young competitive athletes: analysis of 1866 deaths in the United States, 1980–2006. Circulation 2009;119:1085–1092.
28. Choi K, Pan YP, Pock M, Chang RK. Active surveillance of sudden cardiac death in young athletes by periodic Internet searches. Pediatr Cardiol 2013;34:1816–1822.
29. Suarez-Mier MP, Aguilera B, Mosquera RM, Sanchez-de-Leon MS. Pathology of sudden death during recreational sports in Spain. Forensic Sci Int 2013;226: 188–196.
30. Maron BJ, Haas TS, Murphy CJ, Ahluwalia A, Rutten-Ramos S. Incidence and causes of sudden death in U.S. college athletes. J Am Coll Cardiol 2014;63: 1636–1643.
31. Topaz O, Edwards JE. Pathologic features of sudden death in children, adolescents, and young adults. Chest 1985;87:476–482. 32. Drory Y, Turetz Y, Hiss Y, Lev B, Fisman EZ, Pines A, Kramer MR. Sudden unexpected death in persons less than 40 years of age. Am J Cardiol 1991;68: 1388–1392.
33. Wisten A, Forsberg H, Krantz P, Messner T. Sudden cardiac death in 15–35-year olds in Sweden during 1992–99. J Intern Med 2002;252:529–536.
34. Eckart RE, Scoville SL, Campbell CL, Shry EA, Stajduhar KC, Potter RN, Pearse LA, Virmani R. Sudden death in young adults: a 25-year review of autopsies in military recruits. Ann Intern Med 2004;141:829–834.
35. Puranik R, Chow CK, Duflou JA, Kilborn MJ, McGuire MA. Sudden death in the young. Heart Rhythm 2005;2:1277–1282. 36. di Gioia CR, Autore C, Romeo DM, Ciallella C, Aromatario MR, Lopez A, Pagannone E, Giordano C, Gallo P, dAmati G. Sudden cardiac death in younger adults: autopsy diagnosis as a tool for preventive medicine. Hum Pathol 2006;37: 794–801.
37. Papadakis M, Sharma S, Cox S, Sheppard MN, Panoulas VF, Behr ER. The magnitude of sudden cardiac death in the young: a death certificate-based review in England and Wales. Europace 2009;11:1353–1358.
38. Morris VB, Keelan T, Leen E, Keating J, Magee H, ONeill JO, Galvin J. Sudden cardiac death in the young: a 1-year post-mortem analysis in the Republic of Ireland. Ir J Med Sci 2009;178:257–261.
39. Lim Z, Gibbs K, Potts JE, Sanatani S. A review of sudden unexpected death in the young in British Columbia. Can J Cardiol 2010;26:22–26.
40. Winkel BG, Holst AG, Theilade J, Kristensen IB, Thomsen JL, Ottesen GL, Bundgaard H, Svendsen JH, Haunso S, Tfelt-Hansen J. Nationwide study of sudden cardiac death in persons aged 1–35 years. Eur Heart J 2011;32:983–990.
41. Margey R, Roy A, Tobin S, OKeane CJ, McGorrian C, Morris V, Jennings S, Galvin J. Sudden cardiac death in 14- to 35-year olds in Ireland from 2005 to 2007: a retrospective registry. Europace 2011;13:1411–1418.
42. Pilmer CM, Porter B, Kirsh JA, Hicks AL, Gledhill N, Jamnik V, Faught BE, Hildebrandt D, McCartney N, Gow RM, Goodman J, Krahn AD. Scope and nature of sudden cardiac death before age 40 in Ontario: a report from the cardiac death advisory committee of the office of the chief coroner. Heart Rhythm 2013;10: 517–523.
43. de Noronha SV, Behr ER, Papadakis M, Ohta-Ogo K, Banya W, Wells J, Cox S, Cox A, Sharma S, Sheppard MN. The importance of specialist cardiac histopathological examination in the investigation of young sudden cardiac deaths. Europace 2014;16:899–907.
44. Risgaard B, Winkel BG, Jabbari R, Behr ER, Ingemann-Hansen O, Thomsen JL, Ottesen GL, Gislason GH, Bundgaard H, Haunso S, Holst AG, Tfelt-Hansen J. Burden of sudden cardiac death in persons aged 1 to 49 years: nationwide study in Denmark. Circ Arrhythm Electrophysiol 2014;7:205–211.
45. Winkel BG, Risgaard B, Sadjadieh G, Bundgaard H, Haunso S, Tfelt-Hansen J. Sudden cardiac death in children (1–18 years): symptoms and causes of death in a nationwide setting. Eur Heart J 2014;35:868–875.
46. Pilmer CM, Kirsh JA, Hildebrandt D, Krahn AD, Gow RM. Sudden cardiac death in children and adolescents between 1 and 19 years of age. Heart Rhythm 2014;11: 239–245.
47. Vassalini M, Verzeletti A, Restori M, De Ferrari F. An autopsy study of sudden cardiac death in persons aged 1-40 years in Brescia (Italy). J Cardiovasc Med 2015;16: [Epub ahead of print].
48. Mazzanti A, ORourke S, Ng K, Miceli C, Borio G, Curcio A, Esposito F, Napolitano C, Priori SG. The usual suspects in sudden cardiac death of the young: a focus on inherited arrhythmogenic diseases. Expert Rev Cardiovasc Ther 2014;12: 499–519.
49. Maron BJ. Sudden death in young athletes. N Engl J Med 2003;349:1064–1075. 50. Basso C, Carturan E, Pilichou K, Rizzo S, Corrado D, Thiene G. Sudden cardiac death with normal heart: molecular autopsy. Cardiovasc Pathol 2010;19:321–325.
51. Tester DJ, Medeiros-Domingo A, Will ML, Haglund CM, Ackerman MJ. Cardiac channel molecular autopsy: insights from 173 consecutive cases of autopsynegative sudden unexplained death referred for postmortem genetic testing. Mayo Clin Proc 2012;87:524–539.
52. Ackerman MJ, Priori SG, Willems S, Berul C, Brugada R, Calkins H, Camm AJ, Ellinor PT, Gollob M, Hamilton R, Hershberger RE, Judge DP, Le Marec H, McKenna WJ, Schulze-Bahr E, Semsarian C, Towbin JA, Watkins H, Wilde A, Wolpert C, Zipes DP. HRS/EHRA expert consensus statement on the state of genetic testing for the channelopathies and cardiomyopathies. Europace 2011; 13:1077–1109.
53. Wellens HJ, Schwartz PJ, Lindemans FW, Buxton AE, Goldberger JJ, Hohnloser SH, Huikuri HV, Kaab S, La Rovere MT, Malik M, Myerburg RJ, Simoons ML, Swedberg K, Tijssen J, Voors AA, Wilde AA. Risk stratification for sudden cardiac death: current status and challenges for the future. Eur Heart J 2014;35:1642–1651.
54. Myerburg RJ, Kessler KM, Castellanos A. Sudden cardiac death. Structure, function, and time-dependence of risk. Circulation 1992;85:I2–10. 55. Lloyd-Jones DM, Wilson PW, Larson MG, Beiser A, Leip EP, DAgostino RB, Levy D. Framingham risk score and prediction of lifetime risk for coronary heart disease. Am J Cardiol 2004;94:20–24.
56. Perk J, De Backer G, Gohlke H, Graham I, Reiner Z, Verschuren M, Albus C, Benlian P, Boysen G, Cifkova R, Deaton C, Ebrahim S, Fisher M, Germano G, Hobbs R, Hoes A, Karadeniz S, Mezzani A, Prescott E, Ryden L, Scherer M, Syvanne M, Scholte op Reimer WJ, Vrints C, Wood D, Zamorano JL, Zannad F. European Guidelines on cardiovascular disease prevention in clinical practice (version 2012). The Fifth Joint Task Force of the European Society of Cardiology and Other Societies on Cardiovascular Disease Prevention in Clinical Practice (constituted by representatives of nine societies and by invited experts). Eur Heart J 2012;33:1635–1701.
57. Jouven X, Desnos M, Guerot C, Ducimetiere P. Predicting sudden death in the population: the Paris Prospective Study I. Circulation 1999;99:1978–1983.
58. Friedlander Y, Siscovick DS, Weinmann S, Austin MA, Psaty BM, Lemaitre RN, Arbogast P, Raghunathan TE, Cobb LA. Family history as a risk factor for primary cardiac arrest. Circulation 1998;97:155–160.
59. Dekker LR, Bezzina CR, Henriques JP, Tanck MW, Koch KT, Alings MW, Arnold AE, de Boer MJ, Gorgels AP, Michels HR, Verkerk A, Verheugt FW, Zijlstra F, Wilde AA. Familial sudden death is an important risk factor for primary ventricular fibrillation: a case-control study in acute myocardial infarction patients. Circulation 2006;114:1140–1145.
60. Kaikkonen KS, Kortelainen ML, Linna E, Huikuri HV. Family history and the risk of sudden cardiac death as a manifestation of an acute coronary event. Circulation 2006;114:1462–1467.
61. Bezzina CR, Pazoki R, Bardai A, Marsman RF, de Jong JS, Blom MT, Scicluna BP, Jukema JW, Bindraban NR, Lichtner P, Pfeufer A, Bishopric NH, Roden DM, Meitinger T, Chugh SS, Myerburg RJ, Jouven X, Kaab S, Dekker LR, Tan HL, Tanck MW, Wilde AA. Genome-wide association study identifies a susceptibility locus at 21q21 for ventricular fibrillation in acute myocardial infarction. Nat Genet 2010;42:688–691.
62. Arking DE, Junttila MJ, Goyette P, Huertas-Vazquez A, Eijgelsheim M, Blom MT, Newton-Cheh C, Reinier K, Teodorescu C, Uy-Evanado A, Carter-Monroe N, Kaikkonen KS, Kortelainen ML, Boucher G, Lagace C, Moes A, Zhao X, Kolodgie F, Rivadeneira F, Hofman A, Witteman JC, Uitterlinden AG, Marsman RF, Pazoki R, Bardai A, Koster RW, Dehghan A, Hwang SJ, Bhatnagar P, Post W, Hilton G, Prineas RJ, Li M, Kottgen A, Ehret G, Boerwinkle E, Coresh J, Kao WH, Psaty BM, Tomaselli GF, Sotoodehnia N, Siscovick DS, Burke GL, Marban E, Spooner PM, Cupples LA, Jui J, Gunson K, Kesaniemi YA, Wilde AA, Tardif JC, ODonnell CJ, Bezzina CR, Virmani R, Stricker BH, Tan HL, Albert CM, Chakravarti A, Rioux JD, Huikuri HV, Chugh SS. Identification of a sudden cardiac death susceptibility locus at 2q24.2 through genome-wide association in European ancestry individuals. PLoS Genet 2011;7:e1002158.
63. Moss AJ, Zareba W, Hall WJ, Klein H, Wilber DJ, Cannom DS, Daubert JP, Higgins SL, Brown MW, Andrews ML. Prophylactic implantation of a defibrillator in patients with myocardial infarction and reduced ejection fraction. N Engl J Med 2002;346:877–883.
64. Bardy GH, Lee KL, Mark DB, Poole JE, Packer DL, Boineau R, Domanski M, Troutman C, Anderson J, Johnson G, McNulty SE, Clapp-Channing N, Davidson-Ray LD, Fraulo ES, Fishbein DP, Luceri RM, Ip JH, Sudden Cardiac Death in Heart Failure Trial (SCD-HeFT) Investigators. Amiodarone or an implantable cardioverter-defibrillator for congestive heart failure. N Engl J Med 2005;352: 225–237.
65. Scott PA, Barry J, Roberts PR, Morgan JM. Brain natriuretic peptide for the prediction of sudden cardiac death and ventricular arrhythmias: a meta-analysis. Eur J Heart Fail 2009;11:958–966.
66. Levine YC, Rosenberg MA, Mittleman M, Samuel M, Methachittiphan N, Link M, Josephson ME, Buxton AE. B-type natriuretic peptide is a major predictor of ventricular tachyarrhythmias. Heart Rhythm 2014;11:1109–1116.
67. Priori SG, Schwartz PJ, Napolitano C, Bloise R, Ronchetti E, Grillo M, Vicentini A, Spazzolini C, Nastoli J, Bottelli G, Folli R, Cappelletti D. Risk stratification in the long-QT syndrome. N Engl J Med 2003;348:1866–1874.
68. Spirito P, Bellone P, Harris KM, Bernabo P, Bruzzi P, Maron BJ. Magnitude of left ventricular hypertrophy and risk of sudden death in hypertrophic cardiomyopathy. N Engl J Med 2000;342:1778–1785.
69. Barsheshet A, Goldenberg I, O-Uchi J, Moss AJ, Jons C, Shimizu W, Wilde AA, McNitt S, Peterson DR, Zareba W, Robinson JL, Ackerman MJ, Cypress M, Gray DA, Hofman N, Kanters JK, Kaufman ES, Platonov PG, Qi M, Towbin JA, Vincent GM, Lopes CM. Mutations in cytoplasmic loops of the KCNQ1 channel and the risk of life-threatening events: implications for mutation-specific response to beta-blocker therapy in type 1 long-QT syndrome. Circulation 2012;125: 1988–1996.
70. Moss AJ, Zareba W, Kaufman ES, Gartman E, Peterson DR, Benhorin J, Towbin JA, Keating MT, Priori SG, Schwartz PJ, Vincent GM, Robinson JL, Andrews ML, Feng C, Hall WJ, Medina A, Zhang L, Wang Z. Increased risk of arrhythmic events in long-QT syndrome with mutations in the pore region of the human ether-a-go-go-related gene potassium channel. Circulation 2002;105:794–799.
71. van Rijsingen IA, Arbustini E, Elliott PM, Mogensen J, Hermans-van Ast JF, van der Kooi AJ, van Tintelen JP, van den Berg MP, Pilotto A, Pasotti M, Jenkins S, Rowland C, Aslam U, Wilde AA, Perrot A, Pankuweit S, Zwinderman AH, Charron P, Pinto YM. Risk factors for malignant ventricular arrhythmias in lamin a/c mutation carriers a European cohort study. J Am Coll Cardiol 2012;59:493–500.
72. Yoshinaga M, Ushinohama H, Sato S, Tauchi N, Horigome H, Takahashi H, Sumitomo N, Kucho Y, Shiraishi H, Nomura Y, Shimizu W, Nagashima M. Electrocardiographic screening of 1-month-old infants for identifying prolonged QT intervals. Circ Arrhythm Electrophysiol 2013;6:932–938.
73. Yoshinaga M, Kucho Y, Sarantuya J, Ninomiya Y, Horigome H, Ushinohama H, Shimizu W, Horie M. Genetic characteristics of children and adolescents with long-QT syndrome diagnosed by school-based electrocardiographic screening programs. Circ Arrhythm Electrophysiol 2014;7:107–112.
74. Schwartz PJ, Stramba-Badiale M, Crotti L, Pedrazzini M, Besana A, Bosi G, Gabbarini F, Goulene K, Insolia R, Mannarino S, Mosca F, Nespoli L, Rimini A, Rosati E, Salice P, Spazzolini C. Prevalence of the congenital long-QT syndrome. Circulation 2009;120:1761–1767.
75. Corrado D, Pelliccia A, Bjornstad HH, Vanhees L, Biffi A, Borjesson M, Panhuyzen-Goedkoop N, Deligiannis A, Solberg E, Dugmore D, Mellwig KP, Assanelli D, Delise P, van-Buuren F, Anastasakis A, Heidbuchel H, Hoffmann E, Fagard R, Priori SG, Basso C, Arbustini E, Blomstrom-Lundqvist C, McKenna WJ, Thiene G. Cardiovascular pre-participation screening of young competitive athletes for prevention of sudden death: proposal for a common European protocol. Consensus Statement of the Study Group of Sport Cardiology of the Working Group of Cardiac Rehabilitation and Exercise Physiology and the Working Group of Myocardial and Pericardial Diseases of the European Society of Cardiology. Eur Heart J 2005;26:516–524.
76. Maron BJ, Thompson PD, Ackerman MJ, Balady G, Berger S, Cohen D, Dimeff R, Douglas PS, Glover DW, Hutter AM Jr, Krauss MD, Maron MS, Mitten MJ, Roberts WO, Puffer JC. Recommendations and considerations related to preparticipation screening for cardiovascular abnormalities in competitive athletes: 2007 update: a scientific statement from the American Heart Association Council on Nutrition, Physical Activity, and Metabolism: endorsed by the American College of Cardiology Foundation. Circulation 2007;115:1643–1455.
77. Ljungqvist A, Jenoure P, Engebretsen L, Alonso JM, Bahr R, Clough A, De Bondt G, Dvorak J, Maloley R, Matheson G, Meeuwisse W, Meijboom E, Mountjoy M, Pelliccia A, Schwellnus M, Sprumont D, Schamasch P, Gauthier JB, Dubi C, Stupp H, Thill C. The International Olympic Committee (IOC) consensus statement on periodic health evaluation of elite athletes, March 2009. Br J Sports Med 2009;43:631–643.
78. Steinvil A, Chundadze T, Zeltser D, Rogowski O, Halkin A, Galily Y, Perluk H, Viskin S. Mandatory electrocardiographic screening of athletes to reduce their risk for sudden death proven fact or wishful thinking? J Am Coll Cardiol 2011;57: 1291–1296.
79. Narain R, Dhutia H, Merghani A, Myers J, Malhotra A, Millar L, Sheikh N, Sharma S, Papadakis M. Preventing sudden cardiac death in the young: results from a population-based screening program in the UK. European Journal of Preventive Cardiology 2014;21:suppl S1–S6.
80. Kaltman JR, Thompson PD, Lantos J, Berul CI, Botkin J, Cohen JT, Cook NR, Corrado D, Drezner J, Frick KD, Goldman S, Hlatky M, Kannankeril PJ, Leslie L, Priori S, Saul JP, Shapiro-Mendoza CK, Siscovick D, Vetter VL, Boineau R, Burns KM, Friedman RA. Screening for sudden cardiac death in the young: report from a national heart, lung, and blood institute working group. Circulation 2011; 123:1911–1918.
81. James CA, Bhonsale A, Tichnell C, Murray B, Russell SD, Tandri H, Tedford RJ, Judge DP, Calkins H. Exercise increases age-related penetrance and arrhythmic risk in arrhythmogenic right ventricular dysplasia/cardiomyopathy-associated desmosomal mutation carriers. J Am Coll Cardiol 2013;62:1290–1297.
82. Sawant AC, Bhonsale A, te Riele ASJM, Tichnell C, Murray B, Russell SD, Tandri H, Tedford RJ, Judge DP, Calkins H, James CA. Exercise has a disproportionate role in the pathogenesis of arrhythmogenic right ventricular dysplasia/cardiomyopathy in patients without desmosomal mutations. J Am Heart Assoc 2014;3:e001471.
83. Behr ER, Dalageorgou C, Christiansen M, Syrris P, Hughes S, Tome Esteban MT, Rowland E, Jeffery S, McKenna WJ. Sudden arrhythmic death syndrome: familial evaluation identifies inheritable heart disease in the majority of families. Eur Heart J 2008;29:1670–1680.
84. Charron P, Arad M, Arbustini E, Basso C, Bilinska Z, Elliott P, Helio T, Keren A, McKenna WJ, Monserrat L, Pankuweit S, Perrot A, Rapezzi C, Ristic A, Seggewiss H, van Langen I, Tavazzi L, European Society of Cardiology Working Group on Myocardial and Pericardial Diseases. Genetic counselling and testing in cardiomyopathies: a position statement of the European Society of Cardiology Working Group on Myocardial and Pericardial Diseases. Eur Heart J 2010;31: 2715–2726.
85. Christiaans I, Birnie E, Bonsel GJ, Wilde AA, van Langen IM. Uptake of genetic counselling and predictive DNA testing in hypertrophic cardiomyopathy. Eur J Hum Genet 2008;16:1201–1207. 86. Ormondroyd E, Oates S, Parker M, Blair E, Watkins H. Pre-symptomatic genetic testing for inherited cardiac conditions: a qualitative exploration of psychosocial and ethical implications. Eur J Hum Genet 2014;22:88–93.
87. Ingles J, Yeates L, Hunt L, McGaughran J, Scuffham PA, Atherton J, Semsarian C. Health status of cardiac genetic disease patients and their at-risk relatives. Int J Cardiol 2013;165:448–453.
88. Battista RN, Blancquaert I, Laberge AM, van Schendel N, Leduc N. Genetics in health care: an overview of current and emerging models. Public Health Genomics 2012;15:34–45.
89. Ingles J, Lind JM, Phongsavan P, Semsarian C. Psychosocial impact of specialized cardiac genetic clinics for hypertrophic cardiomyopathy. Genet Med 2008;10: 117–120.
90. Christiaans I, van Langen IM, Birnie E, Bonsel GJ, Wilde AA, Smets EM. Quality of life and psychological distress in hypertrophic cardiomyopathy mutation carriers: a cross-sectional cohort study. Am J Med Genet A 2009;149A:602–612.
91. McGorrian C, Constant O, Harper N, ODonnell C, Codd M, Keelan E, Green A, ONeill J, Galvin J, Mahon NG. Family-based cardiac screening in relatives of victims of sudden arrhythmic death syndrome. Europace 2013;15:1050–1058.
92. Moya A, Sutton R, Ammirati F, Blanc JJ, Brignole M, Dahm JB, Deharo JC, Gajek J, Gjesdal K, Krahn A, Massin M, Pepi M, Pezawas T, Ruiz Granell R, Sarasin F, Ungar A, van Dijk JG, Walma EP, Wieling W. Guidelines for the diagnosis and management of syncope. Eur Heart J 2009;30:2631–2671.
93. George S, Rodriguez I, Ipe D, Sager PT, Gussak I, Vajdic B. Computerized extraction of electrocardiograms from continuous 12-lead Holter recordings reduces measurement variability in a thorough QT study. J Clin Pharmacol 2012;52: 1891–1900.
94. de Asmundis C, Conte G, Sieira J, Chierchia GB, Rodriguez-Manero M, Di Giovanni G, Ciconte G, Levinstein M, Baltogiannis G, Saitoh Y, Casado-Arroyo R, Brugada P. Comparison of the patient-activated event recording system vs. traditional 24 h Holter electrocardiography in individuals with paroxysmal palpitations or dizziness. Europace 2014;16:1231–1235.
95. Volosin K, Stadler RW, Wyszynski R, Kirchhof P. Tachycardia detection performance of implantable loop recorders: results from a large real-life patient cohort and patients with induced ventricular arrhythmias. Europace 2013;15:1215–1222.
96. Kamath GS, Zareba W, Delaney J, Koneru JN, McKenna W, Gear K, Polonsky S, Sherrill D, Bluemke D, Marcus F, Steinberg JS. Value of the signal-averaged electrocardiogram in arrhythmogenic right ventricular cardiomyopathy/dysplasia. Heart Rhythm 2011;8:256–262.
97. Nava A, Folino AF, Bauce B, Turrini P, Buja GF, Daliento L, Thiene G. Signal-averaged electrocardiogram in patients with arrhythmogenic right ventricular cardiomyopathy and ventricular arrhythmias. Eur Heart J 2000;21:58–65.
98. Gibbons RJ, Balady GJ, Bricker JT, Chaitman BR, Fletcher GF, Froelicher VF, Mark DB, McCallister BD, Mooss AN, OReilly MG, Winters WL, Gibbons RJ, Antman EM, Alpert JS, Faxon DP, Fuster V, Gregoratos G, Hiratzka LF, Jacobs AK, Russell RO, Smith SC. ACC/AHA 2002 guideline update for exercise testing: summary article. A report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines (Committee to Update the 1997 Exercise Testing Guidelines). J Am Coll Cardiol 2002;40:1531–1540.
99. Podrid PJ, Graboys TB. Exercise stress testing in the management of cardiac rhythm disorders. Med Clin North Am 1984;68:1139–1152.
100. Prastaro M, DAmore C, Paolillo S, Losi M, Marciano C, Perrino C, Ruggiero D, Gargiulo P, Savarese G, Trimarco B, Perrone Filardi P. Prognostic role of transthoracic echocardiography in patients affected by heart failure and reduced ejection fraction. Heart Fail Rev 2015;20:305–316.
101. Chiu DT, Shapiro NI, Sun BC, Mottley JL, Grossman SA. Are echocardiography, telemetry, ambulatory electrocardiography monitoring, and cardiac enzymes in emergency department patients presenting with syncope useful tests? A preliminary investigation. J Emerg Med 2014;47:113–118.
102. Zellweger MJ, Hachamovitch R, Kang X, Hayes SW, Friedman JD, Germano G, Berman DS. Threshold, incidence, and predictors of prognostically high-risk silent ischemia in asymptomatic patients without prior diagnosis of coronary artery disease. J Nucl Cardiol 2009;16:193–200.
103. Kang X, Berman DS, Lewin H, Miranda R, Erel J, Friedman JD, Amanullah AM. Comparative ability of myocardial perfusion single-photon emission computed tomography to detect coronary artery disease in patients with and without diabetes mellitus. Am Heart J 1999;137:949–957.
104. Zelias A, Stepinska J, Andres J, Trabka-Zawicki A, Sadowski J, Zmudka K. Ten-year experience of an invasive cardiology centre with out-of-hospital cardiac arrest patients admitted for urgent coronary angiography. Kardiol Pol 2014;72:687–699.
105. Zaman S, Narayan A, Thiagalingam A, Sivagangabalan G, Thomas S, Ross DL, Kovoor P. Significance of repeat programmed ventricular stimulation at electrophysiology study for arrhythmia prediction after acute myocardial infarction. Pacing Clin Electrophysiol 2014;37:795–802.
106. Brembilla-Perrot B, Suty-Selton C, Houriez P, Claudon O, Beurrier D, de la Chaise AT. Value of non-invasive and invasive studies in patients with bundle branch block, syncope and history of myocardial infarction. Europace 2001;3: 187–194.
107. Dechering DG, Kochhauser S, Wasmer K, Zellerhoff S, Pott C, Kobe J, Spieker T, Piers SR, Bittner A, Monnig G, Breithardt G, Wichter T, Zeppenfeld K, Eckardt L. Electrophysiological characteristics of ventricular tachyarrhythmias in cardiac sarcoidosis versus arrhythmogenic right ventricular cardiomyopathy. Heart Rhythm 2013;10:158–164.
108. Marine JE, Shetty V, Chow GV, Wright JG, Gerstenblith G, Najjar SS, Lakatta EG, Fleg JL. Prevalence and prognostic significance of exercise-induced nonsustained ventricular tachycardia in asymptomatic volunteers: BLSA (Baltimore Longitudinal Study of Aging). J Am Coll Cardiol 2013;62:595–600.
109. Cheitlin MD, Armstrong WF, Aurigemma GP, Beller GA, Bierman FZ, Davis JL, Douglas PS, Faxon DP, Gillam LD, Kimball TR, Kussmaul WG, Pearlman AS, Philbrick JT, Rakowski H, Thys DM. ACC/AHA/ASE 2003 guideline update for the clinical application of echocardiography-summary article: a report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines (ACC/AHA/ASE Committee to Update the 1997 Guidelines for the Clinical Application of Echocardiography). J Am Coll Cardiol 2003;42: 954–970.
110. Summitt J, Rosenheck S, Kou WH, Schmaltz S, Kadish AH, Morady F. Effect of basic drive cycle length on the yield of ventricular tachycardia during programmed ventricular stimulation. Am J Cardiol 1990;65:49–52.
111. Denes P, Uretz E, Ezri MD, Borbola J. Clinical predictors of electrophysiologic findings in patients with syncope of unknown origin. Arch Intern Med 1988;148: 1922–1928.
112. Brignole M, Menozzi C, Moya A, Garcia-Civera R, Mont L, Alvarez M, Errazquin F, Beiras J, Bottoni N, Donateo P, International Study on Syncope of Uncertain Etiology (ISSUE) Investigators. Mechanism of syncope in patients with bundle branch block and negative electrophysiological test. Circulation 2001;104:2045–2050.
113. Roguin A, Bomma CS, Nasir K, Tandri H, Tichnell C, James C, Rutberg J, Crosson J, Spevak PJ, Berger RD, Halperin HR, Calkins H. Implantable cardioverterdefibrillators in patients with arrhythmogenic right ventricular dysplasia/cardiomyopathy. J Am Coll Cardiol 2004;43:1843–1852.
114. Bhonsale A, James CA, Tichnell C, Murray B, Gagarin D, Philips B, Dalal D, Tedford R, Russell SD, Abraham T, Tandri H, Judge DP, Calkins H. Incidence and predictors of implantable cardioverter-defibrillator therapy in patients with arrhythmogenic right ventricular dysplasia/cardiomyopathy undergoing implantable cardioverter-defibrillator implantation for primary prevention. J Am Coll Cardiol 2011;58:1485–1496.
115. Goldberger JJ, Subacius H, Patel T, Cunnane R, Kadish AH. Sudden cardiac death risk stratification in patients with nonischemic dilated cardiomyopathy. J Am Coll Cardiol 2014;63:1879–1889.
116. Elliott PM, Anastasakis A, Borger MA, Borggrefe M, Cecchi F, Charron P, Hagege AA, Lafont A, Limongelli G, Mahrholdt H, McKenna WJ, Mogensen J, Nihoyannopoulos P, Nistri S, Pieper PG, Pieske B, Rapezzi C, Rutten FH, Tillmanns C, Watkins H. 2014 ESC Guidelines on diagnosis and management of hypertrophic cardiomyopathy: The Task Force for the Diagnosis and Management of Hypertrophic Cardiomyopathy of the European Society of Cardiology (ESC). Eur Heart J 2014;35:2733–2779.
117. Bhandari AK, Shapiro WA, Morady F, Shen EN, Mason J, Scheinman MM. Electrophysiologic testing in patients with the long QT syndrome. Circulation 1985;71: 63–71.
118. Giustetto C, Schimpf R, Mazzanti A, Scrocco C, Maury P, Anttonen O, Probst V, Blanc JJ, Sbragia P, Dalmasso P, Borggrefe M, Gaita F. Long-term follow-up of patients with short QT syndrome. J Am Coll Cardiol 2011;58:587–595.
119. Mazzanti A, Kanthan A, Monteforte N, Memmi M, Bloise R, Novelli V, Miceli C, ORourke S, Borio G, Zienciuk-Krajka A, Curcio A, Surducan AE, Colombo M, Napolitano C, Priori SG. Novel insight into the natural history of short QT syndrome. J Am Coll Cardiol 2014;63:1300–1308.
120. Brugada J, Brugada R, Brugada P. Determinants of sudden cardiac death in individuals with the electrocardiographic pattern of Brugada syndrome and no previous cardiac arrest. Circulation 2003;108:3092–3096.
121. Middlekauff HR, Stevenson WG, Stevenson LW, Saxon LA. Syncope in advanced heart failure: high risk of sudden death regardless of origin of syncope. J Am Coll Cardiol 1993;21:110–116.
122. Surawicz B, Knilas T. Chous Electrocardiography in Clinical Practice. Philadelphia, PA: Saunders Elsevier, 2008. 123. Amiodarone Trials Meta Analysis Investigators. Effect of prophylactic amiodarone on mortality after acute myocardial infarction and in congestive heart failure: meta-analysis of individual data from 6500 patients in randomised trials. Lancet 1997;350:1417–1424.
124. Boutitie F, Boissel JP, Connolly SJ, Camm AJ, Cairns JA, Julian DG, Gent M, Janse MJ, Dorian P, Frangin G. Amiodarone interaction with beta-blockers: analysis of the merged EMIAT (European Myocardial Infarct Amiodarone Trial) and CAMIAT (Canadian Amiodarone Myocardial Infarction Trial) databases. The EMIAT and CAMIAT Investigators. Circulation 1999;99:2268–2275.
125. Ray WA, Murray KT, Meredith S, Narasimhulu SS, Hall K, Stein CM. Oral erythromycin and the risk of sudden death from cardiac causes. N Engl J Med 2004;351: 1089–1096.
126. Mosholder AD, Mathew J, Alexander JJ, Smith H, Nambiar S. Cardiovascular risks with azithromycin and other antibacterial drugs. N Engl J Med 2013;368: 1665–1668.
127. Belardinelli L, Giles WR, Rajamani S, Karagueuzian HS, Shryock JC. Cardiac late Na(+) current: proarrhythmic effects, roles in long QT syndromes, and pathological relationship to CaMKII and oxidative stress. Heart Rhythm 2015;12: 440–448.
128. Sarganas G, Garbe E, Klimpel A, Hering RC, Bronder E, Haverkamp W. Epidemiology of symptomatic drug-induced long QT syndrome and torsade de pointes in Germany. Europace 2014;16:101–108.
129. Cardiac Arrhythmia Suppression Trial (CAST) Investigators. Preliminary report: effect of encainide and flecainide on mortality in a randomized trial of arrhythmia suppression after myocardial infarction. N Engl J Med 1989;321:406–412.
130. Kontos MC, Diercks DB, Ho PM, Wang TY, Chen AY, Roe MT. Treatment and outcomes in patients with myocardial infarction treated with acute beta-blocker therapy: results from the American College of Cardiologys NCDRw. Am Heart J 2011;161:864–870.
131. Echt DS, Liebson PR, Mitchell LB, Peters RW, Obias-Manno D, Barker AH, Arensberg D, Baker A, Friedman L, Greene HL, Huther ML, Richardson DW, CAST Investigators. Mortality and morbidity in patients receiving encainide, flecainide, or placebo. The Cardiac Arrhythmia Suppression Trial. N Engl J Med 1991;324:781–788.
132. Singh SN, Fletcher RD, Fisher SG, Singh BN, Lewis HD, Deedwania PC, Massie BM, Colling C, Lazzeri D. Amiodarone in patients with congestive heart failure and asymptomatic ventricular arrhythmia. Survival Trial of Antiarrhythmic Therapy in Congestive Heart Failure. N Engl J Med 1995;333:77–82.
133. Piccini JP, Berger JS, OConnor CM. Amiodarone for the prevention of sudden cardiac death: a meta-analysis of randomized controlled trials. Eur Heart J 2009; 30:1245–1253.
134. Singh BN, Singh SN, Reda DJ, Tang XC, Lopez B, Harris CL, Fletcher RD, Sharma SC, Atwood JE, Jacobson AK, Lewis HD Jr, Raisch DW, Ezekowitz MD, Sotalol Amiodarone Atrial Fibrillation Efficacy Trial (SAFE-T) Investigators. Amiodarone versus sotalol for atrial fibrillation. N Engl J Med 2005;352:1861–1872.
135. Lafuente-Lafuente C, Longas-Tejero MA, Bergmann JF, Belmin J. Antiarrhythmics for maintaining sinus rhythm after cardioversion of atrial fibrillation. Cochrane Database Syst Rev 2012;5:CD005049.
136. Kuhlkamp V, Mewis C, Mermi J, Bosch RF, Seipel L. Suppression of sustained ventricular tachyarrhythmias: a comparison of d,l-sotalol with no antiarrhythmic drug treatment. J Am Coll Cardiol 1999;33:46–52.
137. Waldo AL, Camm AJ, deRuyter H, Friedman PL, MacNeil DJ, Pauls JF, Pitt B, Pratt CM, Schwartz PJ, Veltri EP. Effect of d-sotalol on mortality in patients with left ventricular dysfunction after recent and remote myocardial infarction. The SWORD Investigators. Survival With Oral d-Sotalol. Lancet 1996;348:7–12.
138. Hohnloser SH, Dorian P, Roberts R, Gent M, Israel CW, Fain E, Champagne J, Connolly SJ. Effect of amiodarone and sotalol on ventricular defibrillation threshold: the optimal pharmacological therapy in cardioverter defibrillator patients (OPTIC) trial. Circulation 2006;114:104–109.
139. Bunch TJ, Mahapatra S, Murdock D, Molden J, Weiss JP, May HT, Bair TL, Mader KM, Crandall BG, Day JD, Osborn JS, Muhlestein JB, Lappe DL, Anderson JL. Ranolazine reduces ventricular tachycardia burden and ICD shocks in patients with drug-refractory ICD shocks. Pacing Clin Electrophysiol 2011;34: 1600–1606.
140. Pacifico A, Hohnloser SH, Williams JH, Tao B, Saksena S, Henry PD, Prystowsky EN. Prevention of implantable-defibrillator shocks by treatment with sotalol. N Engl J Med 1999;340:1855–1862. 141. Goyal A, Spertus JA, Gosch K, Venkitachalam L, Jones PG, Van den Berghe G, Kosiborod M. Serum potassium levels and mortality in acute myocardial infarction. JAMA 2012;307:157–164.
142. Alberte C, Zipes DP. Use of nonantiarrhythmic drugs for prevention of sudden cardiac death. J Cardiovasc Electrophysiol 2003;14:S87–S95. 143. Pitt B, Remme W, Zannad F, Neaton J, Martinez F, Roniker B, Bittman R, Hurley S, Kleiman J, Gatlin M, Eplerenone Post-Acute Myocardial Infarction Heart Failure Efficacy and Survival Study Investigators. Eplerenone, a selective aldosterone blocker, in patients with left ventricular dysfunction after myocardial infarction. N Engl J Med 2003;348:1309–1321.
144. Dries DL, Domanski MJ, Waclawiw MA, Gersh BJ. Effect of antithrombotic therapy on risk of sudden coronary death in patients with congestive heart failure. Am J Cardiol 1997;79:909–913.
145. Mitchell LB, Powell JL, Gillis AM, Kehl V, Hallstrom AP. Are lipid-lowering drugs also antiarrhythmic drugs? An analysis of the Antiarrhythmics versus Implantable Defibrillators (AVID) trial. J Am Coll Cardiol 2003;42:81–87.
146. Smith T, Jordaens L, Theuns DA, van Dessel PF, Wilde AA, Hunink MG. The costeffectiveness of primary prophylactic implantable defibrillator therapy in patients with ischaemic or non-ischaemic heart disease: a European analysis. Eur Heart J 2013;34:211–219.
147. Goldenberg I, Gillespie J, Moss AJ, Hall WJ, Klein H, McNitt S, Brown MW, Cygankiewicz I, Zareba W, Executive Committee of the Multicenter Automatic Defibrillator Implantation Trial II. Long-term benefit of primary prevention with an implantable cardioverter-defibrillator: an extended 8-year follow-up study of the Multicenter Automatic Defibrillator Implantation Trial II. Circulation 2010;122: 1265–1271.
148. Goldenberg I, Kutyifa V, Klein HU, Cannom DS, Brown MW, Dan A, Daubert JP, Estes NA 3rd, Foster E, Greenberg H, Kautzner J, Klempfner R, Kuniss M, Merkely B, Pfeffer MA, Quesada A, Viskin S, McNitt S, Polonsky B, Ghanem A, Solomon SD, Wilber D, Zareba W, Moss AJ. Survival with cardiac-resynchronization therapy in mild heart failure. N Engl J Med 2014;370: 1694–1701.
149. Garnreiter JM, Pilcher TA, Etheridge SP, Saarel EV. Inappropriate ICD shocks in pediatrics and congenital heart disease patients: Risk factors and programming strategies. Heart Rhythm 2015;12:937–942. 150. van der Heijden AC, Borleffs CJ, Buiten MS, Thijssen J, van Rees JB, Cannegieter SC, Schalij MJ, van Erven L. The clinical course of patients with implantable defibrillators: Extended experience on clinical outcome, device replacements, and device-related complications. Heart Rhythm 2015;12:1169–1176.
151. Connolly SJ, Gent M, Roberts RS, Dorian P, Roy D, Sheldon RS, Mitchell LB, Green MS, Klein GJ, OBrien B. Canadian implantable defibrillator study (CIDS): a randomized trial of the implantable cardioverter defibrillator against amiodarone. Circulation 2000;101:1297–1302.
152. Kuck KH, Cappato R, Siebels J, Ruppel R. Randomized comparison of antiarrhythmic drug therapy with implantable defibrillators in patients resuscitated from cardiac arrest: the Cardiac Arrest Study Hamburg (CASH). Circulation 2000;102: 748–754.
153. The Antiarrhythmics versus Implantable Defibrillators (AVID) Investigators. A comparison of antiarrhythmic-drug therapy with implantable defibrillators in patients resuscitated from near-fatal ventricular arrhythmias. N Engl J Med 1997;337: 1576–1583.
154. Connolly SJ, Hallstrom AP, Cappato R, Schron EB, Kuck KH, Zipes DP, Greene HL, Boczor S, Domanski M, Follmann D, Gent M, Roberts RS. Meta-analysis of the implantable cardioverter defibrillator secondary prevention trials. AVID, CASH and CIDS studies. Antiarrhythmics vs Implantable Defibrillator study. Cardiac Arrest Study Hamburg. Canadian Implantable Defibrillator Study. Eur Heart J 2000;21:2071–2078.
155. CASCADE Investigators. Randomized antiarrhythmic drug therapy in survivors of cardiac arrest (the CASCADE Study). Am J Cardiol 1993;72:280–287.
156. Connolly SJ, Dorian P, Roberts RS, Gent M, Bailin S, Fain ES, Thorpe K, Champagne J, Talajic M, Coutu B, Gronefeld GC, Hohnloser SH, Optimal Pharmacological Therapy in Cardioverter Defibrillator Patients (OPTIC) Investigators. Comparison of beta-blockers, amiodarone plus beta-blockers, or sotalol for prevention of shocks from implantable cardioverter defibrillators: the OPTIC Study: a randomized trial. JAMA 2006;295:165–171.
157. Weiss R, Knight BP, Gold MR, Leon AR, Herre JM, Hood M, Rashtian M, Kremers M, Crozier I, Lee KL, Smith W, Burke MC. Safety and efficacy of a totally subcutaneous implantable-cardioverter defibrillator. Circulation 2013;128: 944–953.
158. Lambiase PD, Barr C, Theuns DA, Knops R, Neuzil P, Johansen JB, Hood M, Pedersen S, Kaab S, Murgatroyd F, Reeve HL, Carter N, Boersma L. Worldwide experience with a totally subcutaneous implantable defibrillator: early results from the EFFORTLESS S-ICD Registry. Eur Heart J 2014;35:1657–1665.
159. Bardy GH, Smith WM, Hood MA, Crozier IG, Melton IC, Jordaens L, Theuns D, Park RE, Wright DJ, Connelly DT, Fynn SP, Murgatroyd FD, Sperzel J, Neuzner J, Spitzer SG, Ardashev AV, Oduro A, Boersma L, Maass AH, Van Gelder IC, Wilde AA, van Dessel PF, Knops RE, Barr CS, Lupo P, Cappato R, Grace AA. An entirely subcutaneous implantable cardioverter-defibrillator. N Engl J Med 2010;363:36–44.
160. Jarman JW, Lascelles K, Wong T, Markides V, Clague JR, Till J. Clinical experience of entirely subcutaneous implantable cardioverter-defibrillators in children and adults: cause for caution. Eur Heart J 2012;33:1351–1359.
161. Dabiri Abkenari L, Theuns DA, Valk SD, Van Belle Y, de Groot NM, Haitsma D, Muskens-Heemskerk A, Szili-Torok T, Jordaens L. Clinical experience with a novel subcutaneous implantable defibrillator system in a single center. Clin Res Cardiol 2011;100:737–744.
162. Olde Nordkamp LR, Dabiri Abkenari L, Boersma LV, Maass AH, de Groot JR, van Oostrom AJ, Theuns DA, Jordaens LJ, Wilde AA, Knops RE. The entirely subcutaneous implantable cardioverter-defibrillator: initial clinical experience in a large Dutch cohort. J Am Coll Cardiol 2012;60:1933–1939.
163. Aydin A, Hartel F, Schluter M, Butter C, Kobe J, Seifert M, Gosau N, Hoffmann B, Hoffmann M, Vettorazzi E, Wilke I, Wegscheider K, Reichenspurner H, Eckardt L, Steven D, Willems S. Shock efficacy of subcutaneous implantable cardioverterdefibrillator for prevention of sudden cardiac death: initial multicenter experience. Circ Arrhythm Electrophysiol 2012;5:913–919.
164. Jarman JW, Todd DM. United Kingdom national experience of entirely subcutaneous implantable cardioverter-defibrillator technology: important lessons to learn. Europace 2013;15:1158–1165.
165. Kobe J, Reinke F, Meyer C, Shin DI, Martens E, Kaab S, Loher A, Amler S, Lichtenberg A, Winter J, Eckardt L. Implantation and follow-up of totally subcutaneous versus conventional implantable cardioverter-defibrillators: a multicenter case-control study. Heart Rhythm 2013;10:29–36.
166. Burke MC, Gold MR, Knight BP, Barr CS, Theuns DA, Boersma LV, Knops RE, Weiss R, Leon AR, Herre JM, Husby M, Stein KM, Lambiase PD. Safety and efficacy of the totally subcutaneous implantable defibrillator: 2-year results from a pooled analysis of the IDE Study and EFFORTLESS Registry. J Am Coll Cardiol 2015;65: 1605–1615.
167. Adler A, Halkin A, Viskin S. Wearable cardioverter-defibrillators. Circulation 2013; 127:854–860.
168. Auricchio A, Klein H, Geller CJ, Reek S, Heilman MS, Szymkiewicz SJ. Clinical ef- ficacy of the wearable cardioverter-defibrillator in acutely terminating episodes of ventricular fibrillation. Am J Cardiol 1998;81:1253–1256.
169. Chung MK, Szymkiewicz SJ, Shao M, Zishiri E, Niebauer MJ, Lindsay BD, Tchou PJ. Aggregate national experience with the wearable cardioverter-defibrillator: event rates, compliance, and survival. J Am Coll Cardiol 2010;56:194–203.
170. Epstein AE, Abraham WT, Bianco NR, Kern KB, Mirro M, Rao SV, Rhee EK, Solomon SD, Szymkiewicz SJ. Wearable cardioverter-defibrillator use in patients perceived to be at high risk early post-myocardial infarction. J Am Coll Cardiol 2013; 62:2000–2007.
171. Klein HU, Goldenberg I, Moss AJ. Risk stratification for implantable cardioverter defibrillator therapy: the role of the wearable cardioverter-defibrillator. Eur Heart J 2013;34:2230–2242.
172. Kao AC, Krause SW, Handa R, Karia D, Reyes G, Bianco NR, Szymkiewicz SJ, Wearable defibrillator use In heart Failure (WIF) Investigators. Wearable defibrillator use in heart failure (WIF): results of a prospective registry. BMC Cardiovasc Disord 2012;12:123.
173. Hallstrom AP, Ornato JP, Weisfeldt M, Travers A, Christenson J, McBurnie MA, Zalenski R, Becker LB, Schron EB, Proschan M. Public-access defibrillation and survival after out-of-hospital cardiac arrest. N Engl J Med 2004;351:637–646.
174. Capucci A, Aschieri D, Piepoli MF, Bardy GH, Iconomu E, Arvedi M. Tripling survival from sudden cardiac arrest via early defibrillation without traditional education in cardiopulmonary resuscitation. Circulation 2002;106:1065–1070.
175. de Vreede-Swagemakers JJ, Gorgels AP, Dubois-Arbouw WI, van Ree JW, Daemen MJ, Houben LG, Wellens HJ. Out-of-hospital cardiac arrest in the 1990s: a population-based study in the Maastricht area on incidence, characteristics and survival. J Am Coll Cardiol 1997;30:1500–1505.
176. Moriwaki Y, Tahara Y, Iwashita M, Kosuge T, Suzuki N. Risky locations for out-of-hospital cardiopulmonary arrest in a typical urban city. J Emerg Trauma Shock 2014;7:285–294.
177. Bardy GH, Lee KL, Mark DB, Poole JE, Toff WD, Tonkin AM, Smith W, Dorian P, Yallop JJ, Packer DL, White RD, Longstreth W, Anderson J, Johnson G, Bischoff E, Munkers CD, Brown A, McNulty S, Ray LD, Clapp-Channing NE, Rosenberg Y, Salive M, Schron EB. Rationale and design of the Home Automatic External De- fibrillator Trial (HAT). Am Heart J 2008;155:445–454.
178. Weisfeldt ML, Sitlani CM, Ornato JP, Rea T, Aufderheide TP, Davis D, Dreyer J, Hess EP, Jui J, Maloney J, Sopko G, Powell J, Nichol G, Morrison LJ. Survival after application of automatic external defibrillators before arrival of the emergency medical system: evaluation in the resuscitation outcomes consortium population of 21 million. J Am Coll Cardiol 2010;55:1713–1720.
179. Nolan JP, Soar J, Zideman DA, Biarent D, Bossaert LL, Deakin C, Koster RW, Wyllie J, Bottiger B, Group ERCGW. European Resuscitation Council Guidelines for Resuscitation 2010 Section 1. Executive summary. Resuscitation 2010;81: 1219–1276.
180. Zafari AM, Zarter SK, Heggen V, Wilson P, Taylor RA, Reddy K, Backscheider AG, Dudley SC Jr. A program encouraging early defibrillation results in improved inhospital resuscitation efficacy. J Am Coll Cardiol 2004;44:846–852.
181. Nolan JP, Hazinski MF, Billi JE, Boettiger BW, Bossaert L, de Caen AR, Deakin CD, Drajer S, Eigel B, Hickey RW, Jacobs I, Kleinman ME, Kloeck W, Koster RW, Lim SH, Mancini ME, Montgomery WH, Morley PT, Morrison LJ, Nadkarni VM, OConnor RE, Okada K, Perlman JM, Sayre MR, Shuster M, Soar J, Sunde K, Travers AH, Wyllie J, Zideman D. Part 1: Executive summary: 2010 International Consensus on Cardiopulmonary Resuscitation and Emergency Cardiovascular Care Science With Treatment Recommendations. Resuscitation 2010;81(Suppl 1): e1–25.
182. Griffith MJ, Garratt CJ, Rowland E, Ward DE, Camm AJ. Effects of intravenous adenosine on verapamil-sensitive “idiopathic” ventricular tachycardia. Am J Cardiol 1994;73:759–764.
183. Carbucicchio C, Santamaria M, Trevisi N, Maccabelli G, Giraldi F, Fassini G, Riva S, Moltrasio M, Cireddu M, Veglia F, Della Bella P. Catheter ablation for the treatment of electrical storm in patients with implantable cardioverter-defibrillators: short- and long-term outcomes in a prospective single-center study. Circulation 2008;117:462–469.
184. Calkins H, Epstein A, Packer D, Arria AM, Hummel J, Gilligan DM, Trusso J, Carlson M, Luceri R, Kopelman H, Wilber D, Wharton JM, Stevenson W. Catheter ablation of ventricular tachycardia in patients with structural heart disease using cooled radiofrequency energy: results of a prospective multicenter study. Cooled RF Multi Center Investigators Group. J Am Coll Cardiol 2000;35: 1905–1914.
185. Stevenson WG, Wilber DJ, Natale A, Jackman WM, Marchlinski FE, Talbert T, Gonzalez MD, Worley SJ, Daoud EG, Hwang C, Schuger C, Bump TE, Jazayeri M, Tomassoni GF, Kopelman HA, Soejima K, Nakagawa H. Irrigated radiofrequency catheter ablation guided by electroanatomic mapping for recurrent ventricular tachycardia after myocardial infarction: the multicenter thermocool ventricular tachycardia ablation trial. Circulation 2008;118:2773–2782.
186. Tanner H, Hindricks G, Volkmer M, Furniss S, Kuhlkamp V, Lacroix D, C DEC, Almendral J, Caponi D, Kuck KH, Kottkamp H. Catheter ablation of recurrent scar-related ventricular tachycardia using electroanatomical mapping and irrigated ablation technology: results of the prospective multicenter Euro-VT-study. J Cardiovasc Electrophysiol 2010;21:47–53.
187. Reddy VY, Reynolds MR, Neuzil P, Richardson AW, Taborsky M, Jongnarangsin K, Kralovec S, Sediva L, Ruskin JN, Josephson ME. Prophylactic catheter ablation for the prevention of defibrillator therapy. N Engl J Med 2007;357:2657–2665.
188. Kuck KH, Schaumann A, Eckardt L, Willems S, Ventura R, Delacretaz E, Pitschner HF, Kautzner J, Schumacher B, Hansen PS. Catheter ablation of stable ventricular tachycardia before defibrillator implantation in patients with coronary heart disease (VTACH): a multicentre randomised controlled trial. Lancet 2010; 375:31–40.
189. Poole JE, Johnson GW, Hellkamp AS, Anderson J, Callans DJ, Raitt MH, Reddy RK, Marchlinski FE, Yee R, Guarnieri T, Talajic M, Wilber DJ, Fishbein DP, Packer DL, Mark DB, Lee KL, Bardy GH. Prognostic importance of defibrillator shocks in patients with heart failure. N Engl J Med 2008;359:1009–1017.
190. Kamphuis HC, de Leeuw JR, Derksen R, Hauer RN, Winnubst JA. Implantable cardioverter defibrillator recipients: quality of life in recipients with and without ICD shock delivery: a prospective study. Europace 2003;5:381–389.
191. de Bakker JM, van Capelle FJ, Janse MJ, Tasseron S, Vermeulen JT, de Jonge N, Lahpor JR. Slow conduction in the infarcted human heart. Zigzag course of activation. Circulation 1993;88:915–926.
192. de Chillou C, Lacroix D, Klug D, Magnin-Poull I, Marquie C, Messier M, Andronache M, Kouakam C, Sadoul N, Chen J, Aliot E, Kacet S. Isthmus characteristics of reentrant ventricular tachycardia after myocardial infarction. Circulation 2002;105:726–731.
193. Littmann L, Svenson RH, Gallagher JJ, Selle JG, Zimmern SH, Fedor JM, Colavita PG. Functional role of the epicardium in postinfarction ventricular tachycardia. Observations derived from computerized epicardial activation mapping, entrainment, and epicardial laser photoablation. Circulation 1991;83:1577–1591.
194. Berruezo A, Mont L, Nava S, Chueca E, Bartholomay E, Brugada J. Electrocardiographic recognition of the epicardial origin of ventricular tachycardias. Circulation 2004;109:1842–1847.
195. Daniels DV, Lu YY, Morton JB, Santucci PA, Akar JG, Green A, Wilber DJ. Idiopathic epicardial left ventricular tachycardia originating remote from the sinus of Valsalva: electrophysiological characteristics, catheter ablation, and identification from the 12-lead electrocardiogram. Circulation 2006;113:1659–1666.
196. Bazan V, Gerstenfeld EP, Garcia FC, Bala R, Rivas N, Dixit S, Zado E, Callans DJ, Marchlinski FE. Site-specific twelve-lead ECG features to identify an epicardial origin for left ventricular tachycardia in the absence of myocardial infarction. Heart Rhythm 2007;4:1403–1410.
197. Valles E, Bazan V, Marchlinski FE. ECG criteria to identify epicardial ventricular tachycardia in nonischemic cardiomyopathy. Circ Arrhythm Electrophysiol 2010;3: 63–71.
198. Arenal A, Perez-David E, Avila P, Fernandez-Portales J, Crisostomo V, Baez C, Jimenez-Candil J, Rubio-Guivernau JL, Ledesma-Carbayo MJ, Loughlin G, Bermejo J, Sanchez-Margallo FM, Fernandez-Aviles F. Noninvasive identification of epicardial ventricular tachycardia substrate by magnetic resonance-based signal intensity mapping. Heart Rhythm 2014;11:1456–1464.
199. Perez-David E, Arenal A, Rubio-Guivernau JL, del Castillo R, Atea L, Arbelo E, Caballero E, Celorrio V, Datino T, Gonzalez-Torrecilla E, Atienza F, Ledesma-Carbayo MJ, Bermejo J, Medina A, Fernandez-Aviles F. Noninvasive identification of ventricular tachycardia-related conducting channels using contrast-enhanced magnetic resonance imaging in patients with chronic myocardial infarction: comparison of signal intensity scar mapping and endocardial voltage mapping. J Am Coll Cardiol 2011;57:184–194.
200. Bansch D, Bocker D, Brunn J, Weber M, Breithardt G, Block M. Clusters of ventricular tachycardias signify impaired survival in patients with idiopathic dilated cardiomyopathy and implantable cardioverter defibrillators. J Am Coll Cardiol 2000;36:566–573.
201. Haissaguerre M, Extramiana F, Hocini M, Cauchemez B, Jais P, Cabrera JA, Farre J, Leenhardt A, Sanders P, Scavee C, Hsu LF, Weerasooriya R, Shah DC, Frank R, Maury P, Delay M, Garrigue S, Clementy J. Mapping and ablation of ventricular fibrillation associated with long-QT and Brugada syndromes. Circulation 2003;108: 925–928.
202. Berruezo A, Fernandez-Armenta J, Mont L, Zeljko H, Andreu D, Herczku C, Boussy T, Tolosana JM, Arbelo E, Brugada J. Combined endocardial and epicardial catheter ablation in arrhythmogenic right ventricular dysplasia incorporating scar dechanneling technique. Circ Arrhythm Electrophysiol 2012;5:111–121.
203. Marchlinski FE, Callans DJ, Gottlieb CD, Zado E. Linear ablation lesions for control of unmappable ventricular tachycardia in patients with ischemic and nonischemic cardiomyopathy. Circulation 2000;101:1288–1296.
204. Jais P, Maury P, Khairy P, Sacher F, Nault I, Komatsu Y, Hocini M, Forclaz A, Jadidi AS, Weerasooryia R, Shah A, Derval N, Cochet H, Knecht S, Miyazaki S, Linton N, Rivard L, Wright M, Wilton SB, Scherr D, Pascale P, Roten L, Pederson M, Bordachar P, Laurent F, Kim SJ, Ritter P, Clementy J, Haissaguerre M. Elimination of local abnormal ventricular activities: a new end point for substrate modification in patients with scar-related ventricular tachycardia. Circulation 2012;125:2184–2196.
205. Di Biase L, Santangeli P, Burkhardt DJ, Bai R, Mohanty P, Carbucicchio C, Dello Russo A, Casella M, Mohanty S, Pump A, Hongo R, Beheiry S, Pelargonio G, Santarelli P, Zucchetti M, Horton R, Sanchez JE, Elayi CS, Lakkireddy D, Tondo C, Natale A. Endo-epicardial homogenization of the scar versus limited substrate ablation for the treatment of electrical storms in patients with ischemic cardiomyopathy. J Am Coll Cardiol 2012;60:132–141.
206. Cano O, Hutchinson M, Lin D, Garcia F, Zado E, Bala R, Riley M, Cooper J, Dixit S, Gerstenfeld E, Callans D, Marchlinski FE. Electroanatomic substrate and ablation outcome for suspected epicardial ventricular tachycardia in left ventricular nonischemic cardiomyopathy. J Am Coll Cardiol 2009;54:799–808.
207. Bai R, Di Biase L, Shivkumar K, Mohanty P, Tung R, Santangeli P, Saenz LC, Vacca M, Verma A, Khaykin Y, Mohanty S, Burkhardt JD, Hongo R, Beheiry S, Dello Russo A, Casella M, Pelargonio G, Santarelli P, Sanchez J, Tondo C, Natale A. Ablation of ventricular arrhythmias in arrhythmogenic right ventricular dysplasia/ cardiomyopathy: arrhythmia-free survival after endo-epicardial substrate based mapping and ablation. Circ Arrhythm Electrophysiol 2011;4:478–485.
208. Dinov B, Fiedler L, Schonbauer R, Bollmann A, Rolf S, Piorkowski C, Hindricks G, Arya A. Outcomes in catheter ablation of ventricular tachycardia in dilated nonischemic cardiomyopathy compared with ischemic cardiomyopathy: results from the Prospective Heart Centre of Leipzig VT (HELP-VT) Study. Circulation 2014; 129:728–736.
209. Kojodjojo P, Tokuda M, Bohnen M, Michaud GF, Koplan BA, Epstein LM, Albert CM, John RM, Stevenson WG, Tedrow UB. Electrocardiographic left ventricular scar burden predicts clinical outcomes following infarct-related ventricular tachycardia ablation. Heart Rhythm 2013;10:1119–1124.
210. Della Bella P, Baratto F, Tsiachris D, Trevisi N, Vergara P, Bisceglia C, Petracca F, Carbucicchio C, Benussi S, Maisano F, Alfieri O, Pappalardo F, Zangrillo A, Maccabelli G. Management of ventricular tachycardia in the setting of a dedicated unit for the treatment of complex ventricular arrhythmias: long-term outcome after ablation. Circulation 2013;127:1359–1368.
211. Peichl P, Wichterle D, Pavlu L, Cihak R, Aldhoon B, Kautzner J. Complications of catheter ablation of ventricular tachycardia: a single-center experience. Circ Arrhythm Electrophysiol 2014;7:684–690.
212. Mukaddirov M, Demaria RG, Perrault LP, Frapier JM, Albat B. Reconstructive surgery of postinfarction left ventricular aneurysms: techniques and unsolved problems. Eur J Cardiothorac Surg 2008;34:256–261.
213. Sartipy U, Albage A, Insulander P, Lindblom D. Surgery for ventricular tachycardia in patients undergoing surgical ventricular restoration: the Karolinska approach. J Interv Card Electrophysiol 2007;19:171–178.
214. Moran JM, Kehoe RF, Loeb JM, Lichtenthal PR, Sanders JH Jr, Michaelis LL. Extended endocardial resection for the treatment of ventricular tachycardia and ventricular fibrillation. Ann Thorac Surg 1982;34:538–552.
215. ONeill JO, Starling RC, Khaykin Y, McCarthy PM, Young JB, Hail M, Albert NM, Smedira N, Chung MK. Residual high incidence of ventricular arrhythmias after left ventricular reconstructive surgery. J Thorac Cardiovasc Surg 2005;130:1250–1256.
216. Rastegar H, Link MS, Foote CB, Wang PJ, Manolis AS, Estes NA 3rd. Perioperative and long-term results with mapping-guided subendocardial resection and left ventricular endoaneurysmorrhaphy. Circulation 1996;94:1041–1048.
217. Page PL, Cardinal R, Shenasa M, Kaltenbrunner W, Cossette R, Nadeau R. Surgical treatment of ventricular tachycardia. Regional cryoablation guided by computerized epicardial and endocardial mapping. Circulation 1989;80:I124–134.
218. Josephson ME, Harken AH, Horowitz LN. Endocardial excision: a new surgical technique for the treatment of recurrent ventricular tachycardia. Circulation 1979;60:1430–1439.
219. Krishnan SC, Josephson ME. Surgery for postinfarction ventricular tachycardia: is it obsolete? Pacing Clin Electrophysiol 2000;23:1295–1301. 220. Iwa T, Misaki T, Kawasuji M, Matsunaga Y, Tsubota M, Matsumoto Y. Long-term results of surgery for non-ischemic ventricular tachycardia. Eur J Cardiothorac Surg 1991;5:191–197.
221. Karamlou T, Silber I, Lao R, McCrindle BW, Harris L, Downar E, Webb GD, Colman JM, Van Arsdell GS, Williams WG. Outcomes after late reoperation in patients with repaired tetralogy of Fallot: the impact of arrhythmia and arrhythmia surgery. Ann Thorac Surg 2006;81:1786–1793.
222. Tilz RR, Makimoto H, Lin T, Rillig A, Deiss S, Wissner E, Mathew S, Metzner A, Rausch P, Kuck KH, Ouyang F. Electrical isolation of a substrate after myocardial infarction: a novel ablation strategy for unmappable ventricular tachycardiasfeasibility and clinical outcome. Europace 2014;16:1040–1052.
223. Schron EB, Exner DV, Yao Q, Jenkins LS, Steinberg JS, Cook JR, Kutalek SP, Friedman PL, Bubien RS, Page RL, Powell J. Quality of life in the antiarrhythmics versus implantable defibrillators trial: impact of therapy and influence of adverse symptoms and defibrillator shocks. Circulation 2002;105:589–594.
224. Irvine J, Dorian P, Baker B, OBrien BJ, Roberts R, Gent M, Newman D, Connolly SJ. Quality of life in the Canadian Implantable Defibrillator Study (CIDS). Am Heart J 2002;144:282–289.
225. Koopman HM, Vrijmoet-Wiersma CM, Langius JN, van den Heuvel F, Clur SA, Blank CA, Blom NA, ten Harkel AD. Psychological functioning and disease-related quality of life in pediatric patients with an implantable cardioverter defibrillator. Pediatr Cardiol 2012;33:569–575.
226. Berg SK, Higgins M, Reilly CM, Langberg JJ, Dunbar SB. Sleep quality and sleepiness in persons with implantable cardioverter defibrillators: outcome from a clinical randomized longitudinal trial. Pacing Clin Electrophysiol 2012;35:431–443.
227. Vazquez LD, Kuhl EA, Shea JB, Kirkness A, Lemon J, Whalley D, Conti JB, Sears SF. Age-specific differences in women with implantable cardioverter defibrillators: an international multi center study. Pacing Clin Electrophysiol 2008;31:1528–1534.
228. Magyar-Russell G, Thombs BD, Cai JX, Baveja T, Kuhl EA, Singh PP, Montenegro Braga Barroso M, Arthurs E, Roseman M, Amin N, Marine JE, Ziegelstein RC. The prevalence of anxiety and depression in adults with implantable cardioverter defi- brillators: a systematic review. J Psychosom Res 2011;71:223–231.
229. Braunschweig F, Boriani G, Bauer A, Hatala R, Herrmann-Lingen C, Kautzner J, Pedersen SS, Pehrson S, Ricci R, Schalij MJ. Management of patients receiving implantable cardiac defibrillator shocks: recommendations for acute and long-term patient management. Europace 2010;12:1673–1690.
230. Hoogwegt MT, Kupper N, Theuns DA, Zijlstra WP, Jordaens L, Pedersen SS. Undertreatment of anxiety and depression in patients with an implantable cardioverter-defibrillator: impact on health status. Health Psychol 2012;31: 745–753.
231. Lang S, Becker R, Wilke S, Hartmann M, Herzog W, Lowe B. Anxiety disorders in patients with implantable cardioverter defibrillators: frequency, course, predictors, and patients requests for treatment. Pacing Clin Electrophysiol 2014;37: 35–47.
232. Kapa S, Rotondi-Trevisan D, Mariano Z, Aves T, Irvine J, Dorian P, Hayes DL. Psychopathology in patients with ICDs over time: results of a prospective study. Pacing Clin Electrophysiol 2010;33:198–208.
233. Morken IM, Bru E, Norekval TM, Larsen AI, Idsoe T, Karlsen B. Perceived support from healthcare professionals, shock anxiety and post-traumatic stress in implantable cardioverter defibrillator recipients. J Clin Nurs 2014;23:450–460.
234. Versteeg H, Theuns DA, Erdman RA, Jordaens L, Pedersen SS. Posttraumatic stress in implantable cardioverter defibrillator patients: the role of preimplantation distress and shocks. Int J Cardiol 2011;146:438–439.
235. Morken IM, Isaksen K, Karlsen B, Norekval TM, Bru E, Larsen AI. Shock anxiety among implantable cardioverter defibrillator recipients with recent tachyarrhythmia. Pacing Clin Electrophysiol 2012;35:1369–1376.
236. Pedersen SS, van den Broek KC, Erdman RA, Jordaens L, Theuns DA. Preimplantation implantable cardioverter defibrillator concerns and type D personality increase the risk of mortality in patients with an implantable cardioverter de- fibrillator. Europace 2010;12:1446–1452.
237. Mastenbroek MH, Versteeg H, Jordaens L, Theuns DA, Pedersen SS. Ventricular tachyarrhythmias and mortality in patients with an implantable cardioverter defibrillator: impact of depression in the MIDAS cohort. Psychosom Med 2014;76: 58–65.
238. Dunbar SB, Dougherty CM, Sears SF, Carroll DL, Goldstein NE, Mark DB, McDaniel G, Pressler SJ, Schron E, Wang P, Zeigler VL. Educational and psychological interventions to improve outcomes for recipients of implantable cardioverter defibrillators and their families: a scientific statement from the American Heart Association. Circulation 2012;126:2146–2172.
239. Vijgen J, Botto G, Camm J, Hoijer CJ, Jung W, Le Heuzey JY, Lubinski A, Norekval TM, Santomauro M, Schalij M, Schmid JP, Vardas P. Consensus statement of the European Heart Rhythm Association: updated recommendations for driving by patients with implantable cardioverter defibrillators. Europace 2009;11:1097–1107.
240. Johansson I, Stromberg A. Experiences of driving and driving restrictions in recipients with an implantable cardioverter defibrillator-the patient perspective. J Cardiovasc Nurs 2010;25:E1–E10.
241. Steinke EE, Gill-Hopple K, Valdez D, Wooster M. Sexual concerns and educational needs after an implantable cardioverter defibrillator. Heart Lung 2005;34: 299–308.
242. Steinke EE, Jaarsma T, Barnason SA, Byrne M, Doherty S, Dougherty CM, Fridlund B, Kautz DD, Martensson J, Mosack V, Moser DK. Sexual counselling for individuals with cardiovascular disease and their partners: a consensus document from the American Heart Association and the ESC Council on Cardiovascular Nursing and Allied Professions (CCNAP). Eur Heart J 2013;34:3217–3235.
243. Zeigler VL, Nelms T. Almost normal: experiences of adolescents with implantable cardioverter defibrillators. J Spec Pediatr Nurs 2009;14:142–151.
244. Steg PG, Cambou JP, Goldstein P, Durand E, Sauval P, Kadri Z, Blanchard D, Lablanche JM, Gueret P, Cottin Y, Juliard JM, Hanania G, Vaur L, Danchin N. Bypassing the emergency room reduces delays and mortality in ST elevation myocardial infarction: the USIC 2000 registry. Heart 2006;92:1378–1383.
245. Soholm H, Wachtell K, Nielsen SL, Bro-Jeppesen J, Pedersen F, Wanscher M, Boesgaard S, Moller JE, Hassager C, Kjaergaard J. Tertiary centres have improved survival compared to other hospitals in the Copenhagen area after out-of-hospital cardiac arrest. Resuscitation 2013;84:162–167.
246. Xiao G, Guo Q, Shu M, Xie X, Deng J, Zhu Y, Wan C. Safety profile and outcome of mild therapeutic hypothermia in patients following cardiac arrest: systematic review and meta-analysis. Emerg Med J 2013;30:91–100.
247. Boersma E, Maas AC, Deckers JW, Simoons ML. Early thrombolytic treatment in acute myocardial infarction: reappraisal of the golden hour. Lancet 1996;348: 771–775.
248. Boersma E, Primary Coronary Angioplasty vs. Thrombolysis Group. Does time matter? A pooled analysis of randomized clinical trials comparing primary percutaneous coronary intervention and in-hospital fibrinolysis in acute myocardial infarction patients. Eur Heart J 2006;27:779–788.
249. Keeley EC, Boura JA, Grines CL. Comparison of primary and facilitated percutaneous coronary interventions for ST-elevation myocardial infarction: quantitative review of randomised trials. Lancet 2006;367:579–588.
250. Roffi M, Patrono C, Collet JP, Mueller C, Valgimigli M, Andreotti F, Bax JJ, Borger MA, Brotons C, Chew DP, Gencer B, Hasenfuss G, Kjeldsen K, Lancellotti P, Landmesser U, Mehilli J, Mukherjee D, Storey RF, Windecker S. 2015 ESC Guidelines for the Management of Acute Coronary Syndromes in Patients Presenting Without Persistent ST-Segment Elevation. Eur Heart J 2015. doi:10.1093/eurheartj/ehv320.
251. Spaulding CM, Joly LM, Rosenberg A, Monchi M, Weber SN, Dhainaut JF, Carli P. Immediate coronary angiography in survivors of out-of-hospital cardiac arrest. N Engl J Med 1997;336:1629–1633.
252. Dumas F, Cariou A, Manzo-Silberman S, Grimaldi D, Vivien B, Rosencher J, Empana JP, Carli P, Mira JP, Jouven X, Spaulding C. Immediate percutaneous coronary intervention is associated with better survival after out-of-hospital cardiac arrest: insights from the PROCAT (Parisian Region Out of hospital Cardiac ArresT) registry. Circ Cardiovasc Interv 2010;3:200–207.
253. Bowers TR, ONeill WW, Grines C, Pica MC, Safian RD, Goldstein JA. Effect of reperfusion on biventricular function and survival after right ventricular infarction. N Engl J Med 1998;338:933–940.
254. Reddy YM, Chinitz L, Mansour M, Bunch TJ, Mahapatra S, Swarup V, Di Biase L, Bommana S, Atkins D, Tung R, Shivkumar K, Burkhardt JD, Ruskin J, Natale A, Lakkireddy D. Percutaneous left ventricular assist devices in ventricular tachycardia ablation: multicenter experience. Circ Arrhythm Electrophysiol 2014;7:244–250.
255. Lamhaut L, Jouffroy R, Soldan M, Phillipe P, Deluze T, Jaffry M, Dagron C, Vivien B, Spaulding C, An K, Carli P. Safety and feasibility of prehospital extra corporeal life support implementation by non-surgeons for out-of-hospital refractory cardiac arrest. Resuscitation 2013;84:1525–1529.
256. Wang CH, Chou NK, Becker LB, Lin JW, Yu HY, Chi NH, Hunag SC, Ko WJ, Wang SS, Tseng LJ, Lin MH, Wu IH, Ma MH, Chen YS. Improved outcome of extracorporeal cardiopulmonary resuscitation for out-of-hospital cardiac arrest-a comparison with that for extracorporeal rescue for in-hospital cardiac arrest. Resuscitation 2014;85:1219–1224.
257. Piccini JP, Hranitzky PM, Kilaru R, Rouleau JL, White HD, Aylward PE, Van de Werf F, Solomon SD, Califf RM, Velazquez EJ. Relation of mortality to failure to prescribe beta blockers acutely in patients with sustained ventricular tachycardia and ventricular fibrillation following acute myocardial infarction (from the VALsartan In Acute myocardial iNfarcTion trial [VALIANT] Registry). Am J Cardiol 2008;102:1427–1432.
258. Wolfe CL, Nibley C, Bhandari A, Chatterjee K, Scheinman M. Polymorphous ventricular tachycardia associated with acute myocardial infarction. Circulation 1991; 84:1543–1551.
259. Chatterjee S, Chaudhuri D, Vedanthan R, Fuster V, Ibanez B, Bangalore S, Mukherjee D. Early intravenous beta-blockers in patients with acute coronary syndrome—a meta-analysis of randomized trials. Int J Cardiol 2013; 168:915–921.
260. Bangalore S, Makani H, Radford M, Thakur K, Toklu B, Katz SD, DiNicolantonio JJ, Devereaux PJ, Alexander KP, Wetterslev J, Messerli FH. Clinical outcomes with beta-blockers for myocardial infarction: a meta-analysis of randomized trials. Am J Med 2014;127:939–953.
261. Enjoji Y, Mizobuchi M, Muranishi H, Miyamoto C, Utsunomiya M, Funatsu A, Kobayashi T, Nakamura S. Catheter ablation of fatal ventricular tachyarrhythmias storm in acute coronary syndrome—role of Purkinje fiber network. J Interv Card Electrophysiol 2009;26:207–215.
262. Frankel DS, Mountantonakis SE, Robinson MR, Zado ES, Callans DJ, Marchlinski FE. Ventricular tachycardia ablation remains treatment of last resort in structural heart disease: argument for earlier intervention. J Cardiovasc Electrophysiol 2011;22:1123–1128.
263. Peichl P, Cihak R, Kozeluhova M, Wichterle D, Vancura V, Kautzner J. Catheter ablation of arrhythmic storm triggered by monomorphic ectopic beats in patients with coronary artery disease. J Interv Card Electrophysiol 2010;27:51–59.
264. Deneke T, Lemke B, Mugge A, Shin DI, Grewe PH, Horlitz M, Balta O, Bosche L, Lawo T. Catheter ablation of electrical storm. Expert Rev Cardiovasc Ther 2011;9: 1051–1058.
265. Deneke T, Shin DI, Lawo T, Bosche L, Balta O, Anders H, Bunz K, Horlitz M, Grewe PH, Lemke B, Mugge A. Catheter ablation of electrical storm in a collaborative hospital network. Am J Cardiol 2011;108:233–239.
266. Gorenek B, Blomstrom Lundqvist C, Brugada Terradellas J, Camm AJ, Hindricks G, Huber K, Kirchhof P, Kuck KH, Kudaiberdieva G, Lin T, Raviele A, Santini M, Tilz RR, Valgimigli M, Vos MA, Vrints C, Zeymer U, Lip GY, Potpara T, Fauchier L, Sticherling C, Roffi M, Widimsky P, Mehilli J, Lettino M, Schiele F, Sinnaeve P, Boriani G, Lane D, Savelieva I. Cardiac arrhythmias in acute coronary syndromes: position paper from the joint EHRA, ACCA, and EAPCI task force. Europace 2014;16:1655–1673.
267. Shaw DJ, Davidson JE, Smilde RI, Sondoozi T, Agan D. Multidisciplinary team training to enhance family communication in the ICU. Crit Care Med 2014;42:265–271.
268. Piccini JP, Schulte PJ, Pieper KS, Mehta RH, White HD, Van de Werf F, Ardissino D, Califf RM, Granger CB, Ohman EM, Alexander JH. Antiarrhythmic drug therapy for sustained ventricular arrhythmias complicating acute myocardial infarction. Crit Care Med 2011;39:78–83.
269. Huikuri HV, Castellanos A, Myerburg RJ. Sudden death due to cardiac arrhythmias. N Engl J Med 2001;345:1473–1482.
270. Hine LK, Laird N, Hewitt P, Chalmers TC. Meta-analytic evidence against prophylactic use of lidocaine in acute myocardial infarction. Arch Intern Med 1989;149: 2694–2698.
271. Steg PG, James SK, Atar D, Badano LP, Blomstrom-Lundqvist C, Borger MA, Di Mario C, Dickstein K, Ducrocq G, Fernandez-Aviles F, Gershlick AH, Giannuzzi P, Halvorsen S, Huber K, Juni P, Kastrati A, Knuuti J, Lenzen MJ, Mahaffey KW, Valgimigli M, vant Hof A, Widimsky P, Zahger D. ESC Guidelines for the management of acute myocardial infarction in patients presenting with ST-segment elevation. Eur Heart J 2012;33:2569–2619.
272. Borne RT, Varosy PD, Masoudi FA. Implantable cardioverter-defibrillator shocks: epidemiology, outcomes, and therapeutic approaches. JAMA Intern Med 2013;173: 859–865.
273. Liang JJ, Hodge DO, Mehta RA, Russo AM, Prasad A, Cha YM. Outcomes in patients with sustained ventricular tachyarrhythmias occurring within 48 h of acute myocardial infarction: when is ICD appropriate? Europace 2014;16:1759–1766.
274. Hohnloser SH, Kuck KH, Dorian P, Roberts RS, Hampton JR, Hatala R, Fain E, Gent M, Connolly SJ, Investigators D. Prophylactic use of an implantable cardioverter-defibrillator after acute myocardial infarction. N Engl J Med 2004; 351:2481–2488.
275. Steinbeck G, Andresen D, Seidl K, Brachmann J, Hoffmann E, Wojciechowski D, Kornacewicz-Jach Z, Sredniawa B, Lupkovics G, Hofgartner F, Lubinski A, Rosenqvist M, Habets A, Wegscheider K, Senges J, IRIS Investigators. Defibrillator implantation early after myocardial infarction. N Engl J Med 2009;361:1427–1436.
276. Noc M, Fajadet J, Lassen JF, Kala P, MacCarthy P, Olivecrona GK, Windecker S, Spaulding C. Invasive coronary treatment strategies for out-of-hospital cardiac arrest: a consensus statement from the European Association for Percutaneous Cardiovascular Interventions (EAPCI)/Stent for Life (SFL) groups. EuroIntervention 2014;10:31–37.
277. Bougouin W, Marijon E, Puymirat E, Defaye P, Celermajer DS, Le Heuzey JY, Boveda S, Kacet S, Mabo P, Barnay C, Da Costa A, Deharo JC, Daubert JC, Ferrieres J, Simon T, Danchin N. Incidence of sudden cardiac death after ventricular fibrillation complicating acute myocardial infarction: a 5-year cause-of-death analysis of the FAST-MI 2005 registry. Eur Heart J 2014;35:116–122.
278. Avezum A, Piegas LS, Goldberg RJ, Brieger D, Stiles MK, Paolini R, Huang W, Gore JM. Magnitude and prognosis associated with ventricular arrhythmias in patients hospitalized with acute coronary syndromes (from the GRACE Registry). Am J Cardiol 2008;102:1577–1582.
279. Piccini JP, White JA, Mehta RH, Lokhnygina Y, Al-Khatib SM, Tricoci P, Pollack CV Jr, Montalescot G, Van de Werf F, Gibson CM, Giugliano RP, Califf RM, Harrington RA, Newby LK. Sustained ventricular tachycardia and ventricular fibrillation complicating non-ST-segment-elevation acute coronary syndromes. Circulation 2012;126:41–49.
280. Buxton AE, Lee KL, DiCarlo L, Gold MR, Greer GS, Prystowsky EN, OToole MF, Tang A, Fisher JD, Coromilas J, Talajic M, Hafley G. Electrophysiologic testing to identify patients with coronary artery disease who are at risk for sudden death. Multicenter Unsustained Tachycardia Trial Investigators. N Engl J Med 2000;342: 1937–1945.
281. Buxton AE, Lee KL, Hafley GE, Pires LA, Fisher JD, Gold MR, Josephson ME, Lehmann MH, Prystowsky EN. Limitations of ejection fraction for prediction of sudden death risk in patients with coronary artery disease: lessons from the MUSTT study. J Am Coll Cardiol 2007;50:1150–1157.
282. Gatzoulis KA, Tsiachris D, Arsenos P, Archontakis S, Dilaveris P, Vouliotis A, Sideris S, Skiadas I, Kallikazaros I, Stefanadis C. Prognostic value of programmed ventricular stimulation for sudden death in selected high risk patients with structural heart disease and preserved systolic function. Int J Cardiol 2014;176: 1449–1451.
283. Exner DV, Kavanagh KM, Slawnych MP, Mitchell LB, Ramadan D, Aggarwal SG, Noullett C, Van Schaik A, Mitchell RT, Shibata MA, Gulamhussein S, McMeekin J, Tymchak W, Schnell G, Gillis AM, Sheldon RS, Fick GH, Duff HJ. Noninvasive risk assessment early after a myocardial infarction the REFINE study. J Am Coll Cardiol 2007;50:2275–2284.
284. Malik M, Camm AJ, Janse MJ, Julian DG, Frangin GA, Schwartz PJ. Depressed heart rate variability identifies postinfarction patients who might benefit from prophylactic treatment with amiodarone: a substudy of EMIAT (the European Myocardial Infarct Amiodarone Trial). J Am Coll Cardiol 2000;35:1263–1275.
285. Zaman S, Narayan A, Thiagalingam A, Sivagangabalan G, Thomas S, Ross DL, Kovoor P. Long-term arrhythmia-free survival in patients with severe left ventricular dysfunction and no inducible ventricular tachycardia after myocardial infarction. Circulation 2014;129:848–854.
286. Soholm H, Lonborg J, Andersen MJ, Vejlstrup N, Engstrom T, Moller JE, Hassager C. Repeated echocardiography after first ever ST-segment elevation myocardial infarction treated with primary percutaneous coronary intervention—is it necessary? Eur Heart J Acute Cardiovasc Care 2014 Oct 15. pii: 2048872614556000 [Epub ahead of print].
287. Allman KC, Shaw LJ, Hachamovitch R, Udelson JE. Myocardial viability testing and impact of revascularization on prognosis in patients with coronary artery disease and left ventricular dysfunction: a meta-analysis. J Am Coll Cardiol 2002;39: 1151–1158.
288. St John Sutton M, Pfeffer MA, Plappert T, Rouleau JL, Moye LA, Dagenais GR, Lamas GA, Klein M, Sussex B, Goldman S. Quantitative two-dimensional echocardiographic measurements are major predictors of adverse cardiovascular events after acute myocardial infarction. The protective effects of captopril. Circulation 1994; 89:68–75.
289. Kelly P, Ruskin JN, Vlahakes GJ, Buckley MJ Jr, Freeman CS, Garan H. Surgical coronary revascularization in survivors of prehospital cardiac arrest: its effect on inducible ventricular arrhythmias and long-term survival. J Am Coll Cardiol 1990;15: 267–273.
290. van der Burg AE, Bax JJ, Boersma E, Pauwels EK, van der Wall EE, Schalij MJ. Impact of viability, ischemia, scar tissue, and revascularization on outcome after aborted sudden death. Circulation 2003;108:1954–1959.
291. Bax JJ, Visser FC, Poldermans D, Elhendy A, Cornel JH, Boersma E, van Lingen A, Fioretti PM, Visser CA. Time course of functional recovery of stunned and hibernating segments after surgical revascularization. Circulation 2001;104:I314–I318.
292. Funaro S, La Torre G, Madonna M, Galiuto L, Scara A, Labbadia A, Canali E, Mattatelli A, Fedele F, Alessandrini F, Crea F, Agati L. Incidence, determinants, and prognostic value of reverse left ventricular remodelling after primary percutaneous coronary intervention: results of the Acute Myocardial Infarction Contrast Imaging (AMICI) multicenter study. Eur Heart J 2009;30:566–575.
293. Cairns JA, Connolly SJ, Roberts R, Gent M. Randomised trial of outcome after myocardial infarction in patients with frequent or repetitive ventricular premature depolarisations: CAMIAT. Canadian Amiodarone Myocardial Infarction Arrhythmia Trial Investigators. Lancet 1997;349:675–682.
294. Julian DG, Camm AJ, Frangin G, Janse MJ, Munoz A, Schwartz PJ, Simon P. Randomised trial of effect of amiodarone on mortality in patients with left-ventricular dysfunction after recent myocardial infarction: EMIAT. European Myocardial Infarct Amiodarone Trial Investigators. Lancet 1997;349:667–674.
295. Solomon SD, Wang D, Finn P, Skali H, Zornoff L, McMurray JJ, Swedberg K, Yusuf S, Granger CB, Michelson EL, Pocock S, Pfeffer MA. Effect of candesartan on cause-specific mortality in heart failure patients: the Candesartan in Heart failure Assessment of Reduction in Mortality and morbidity (CHARM) program. Circulation 2004;110:2180–2183.
296. Cleland JG, Massie BM, Packer M. Sudden death in heart failure: vascular or electrical? Eur J Heart Fail 1999;1:41–45.
297. Gradman A, Deedwania P, Cody R, Massie B, Packer M, Pitt B, Goldstein S. Predictors of total mortality and sudden death in mild to moderate heart failure. Captopril-Digoxin Study Group. J Am Coll Cardiol 1989;14:564–570.
298. Szabo BM, van Veldhuisen DJ, Crijns HJ, Wiesfeld AC, Hillege HL, Lie KI. Value of ambulatory electrocardiographic monitoring to identify increased risk of sudden death in patients with left ventricular dysfunction and heart failure. Eur Heart J 1994;15:928–933.
299. Doval HC, Nul DR, Grancelli HO, Varini SD, Soifer S, Corrado G, Dubner S, Scapin O, Perrone SV. Nonsustained ventricular tachycardia in severe heart failure. Independent marker of increased mortality due to sudden death. GESICAGEMA Investigators. Circulation 1996;94:3198–3203.
300. Teerlink JR, Jalaluddin M, Anderson S, Kukin ML, Eichhorn EJ, Francis G, Packer M, Massie BM. Ambulatory ventricular arrhythmias in patients with heart failure do not specifically predict an increased risk of sudden death. PROMISE (Prospective Randomized Milrinone Survival Evaluation) Investigators. Circulation 2000;101: 40–46.
301. AlJaroudi WA, Refaat MM, Habib RH, Al-Shaar L, Singh M, Gutmann R, Bloom HL, Dudley SC, Ellinor PT, Saba SF, Shalaby AA, Weiss R, McNamara DM, Halder I, London B, Genetic Risk Assessment of Defibrillator Events Investigators. Effect of angiotensin-converting enzyme inhibitors and receptor blockers on appropriate implantable cardiac defibrillator shock in patients with severe systolic heart failure (from the GRADE Multicenter Study). Am J Cardiol 2015;115:924–931.
302. Pitt B, White H, Nicolau J, Martinez F, Gheorghiade M, Aschermann M, van Veldhuisen DJ, Zannad F, Krum H, Mukherjee R, Vincent J, EPHESUS Investigators. Eplerenone reduces mortality 30 days after randomization following acute myocardial infarction in patients with left ventricular systolic dysfunction and heart failure. J Am Coll Cardiol 2005;46:425–431.
303. Peck KY, Lim YZ, Hopper I, Krum H. Medical therapy versus implantable cardioverter-defibrillator in preventing sudden cardiac death in patients with left ventricular systolic dysfunction and heart failure: a meta-analysis of .35,000 patients. Int J Cardiol 2014;173:197–203.
304. Chatterjee S, Udell JA, Sardar P, Lichstein E, Ryan JJ. Comparable benefit of betablocker therapy in heart failure across regions of the world: meta-analysis of randomized clinical trials. Can J Cardiol 2014;30:898–903.
305. Garg R, Yusuf S. Overview of randomized trials of angiotensin-converting enzyme inhibitors on mortality and morbidity in patients with heart failure. Collaborative Group on ACE Inhibitor Trials. JAMA 1995;273:1450–1456.
306. Kotecha D, Holmes J, Krum H, Altman DG, Manzano L, Cleland JG, Lip GY, Coats AJ, Andersson B, Kirchhof P, von Lueder TG, Wedel H, Rosano G, Shibata MC, Rigby A, Flather MD, Beta-Blockers in Heart Failure Collaborative Group. Efficacy of beta blockers in patients with heart failure plus atrial fibrillation: an individual-patient data meta-analysis. Lancet 2014;384:2235–2243.
307. Kotecha D, Altman DG, Manzano L, Flather MD, Beta-Blockers in Heart Failure Collaborative Group. beta blockers in patients with heart failure and atrial fibrillation—authors reply. Lancet 2015;385:1618–1619.
308. Pitt B, Zannad F, Remme WJ, Cody R, Castaigne A, Perez A, Palensky J, Wittes J. The effect of spironolactone on morbidity and mortality in patients with severe heart failure. Randomized Aldactone Evaluation Study Investigators. N Engl J Med 1999;341:709–717.
309. Zannad F, McMurray JJ, Krum H, van Veldhuisen DJ, Swedberg K, Shi H, Vincent J, Pocock SJ, Pitt B. Eplerenone in patients with systolic heart failure and mild symptoms. N Engl J Med 2011;364:11–21.
310. Bapoje SR, Bahia A, Hokanson JE, Peterson PN, Heidenreich PA, Lindenfeld J, Allen LA, Masoudi FA. Effects of mineralocorticoid receptor antagonists on the risk of sudden cardiac death in patients with left ventricular systolic dysfunction: a meta-analysis of randomized controlled trials. Circ Heart Fail 2013;6:166–173.
311. Borlaug BA, Paulus WJ. Heart failure with preserved ejection fraction: pathophysiology, diagnosis, and treatment. Eur Heart J 2011;32:670–679.
312. Chan MM, Lam CS. How do patients with heart failure with preserved ejection fraction die? Eur J Heart Fail 2013;15:604–613.
313. Bristow MR, Saxon LA, Boehmer J, Krueger S, Kass DA, De Marco T, Carson P, DiCarlo L, DeMets D, White BG, DeVries DW, Feldman AM, Comparison of Medical Therapy, Pacing, and Defibrillation in Heart Failure (COMPANION) Investigators. Cardiac-resynchronization therapy with or without an implantable defibrillator in advanced chronic heart failure. N Engl J Med 2004;350:2140–2150.
314. Cleland JG, Daubert JC, Erdmann E, Freemantle N, Gras D, Kappenberger L, Tavazzi L. The effect of cardiac resynchronization on morbidity and mortality in heart failure. N Engl J Med 2005;352:1539–1549.
315. van Veldhuisen DJ, Maass AH, Priori SG, Stolt P, van Gelder IC, Dickstein K, Swedberg K. Implementation of device therapy (cardiac resynchronization therapy and implantable cardioverter defibrillator) for patients with heart failure in Europe: changes from 2004 to 2008. Eur J Heart Fail 2009;11:1143–1151.
316. Kadish A, Dyer A, Daubert JP, Quigg R, Estes NA, Anderson KP, Calkins H, Hoch D, Goldberger J, Shalaby A, Sanders WE, Schaechter A, Levine JH, Defibrillators in Non-Ischemic Cardiomyopathy Treatment Evaluation Investigators. Prophylactic defibrillator implantation in patients with nonischemic dilated cardiomyopathy. N Engl J Med 2004;350:2151–2158.
317. Desai AS, Fang JC, Maisel WH, Baughman KL. Implantable defibrillators for the prevention of mortality in patients with nonischemic cardiomyopathy: a meta-analysis of randomized controlled trials. JAMA 2004;292:2874–2879.
318. Goldenberg I, Moss AJ, McNitt S, Zareba W, Hall WJ, Andrews ML, Wilber DJ, Klein HU. Time dependence of defibrillator benefit after coronary revascularization in the Multicenter Automatic Defibrillator Implantation Trial (MADIT)-II. J Am Coll Cardiol 2006;47:1811–1817.
319. Packer DL, Prutkin JM, Hellkamp AS, Mitchell LB, Bernstein RC, Wood F, Boehmer JP, Carlson MD, Frantz RP, McNulty SE, Rogers JG, Anderson J, Johnson GW, Walsh MN, Poole JE, Mark DB, Lee KL, Bardy GH. Impact of implantable cardioverter-defibrillator, amiodarone, and placebo on the mode of death in stable patients with heart failure: analysis from the sudden cardiac death in heart failure trial. Circulation 2009;120:2170–2176.
320. Frohlich GM, Holzmeister J, Hubler M, Hubler S, Wolfrum M, Enseleit F, Seifert B, Hurlimann D, Lehmkuhl HB, Noll G, Steffel J, Falk V, Luscher TF, Hetzer R, Ruschitzka F. Prophylactic implantable cardioverter defibrillator treatment in patients with end-stage heart failure awaiting heart transplantation. Heart 2013;99: 1158–1165.
321. Sandner SE, Wieselthaler G, Zuckermann A, Taghavi S, Schmidinger H, Pacher R, Ploner M, Laufer G, Wolner E, Grimm M. Survival benefit of the implantable cardioverter-defibrillator in patients on the waiting list for cardiac transplantation. Circulation 2001;104:I171–I176.
322. Zareba W, Klein H, Cygankiewicz I, Hall WJ, McNitt S, Brown M, Cannom D, Daubert JP, Eldar M, Gold MR, Goldberger JJ, Goldenberg I, Lichstein E, Pitschner H, Rashtian M, Solomon S, Viskin S, Wang P, Moss AJ, Investigators M-C. Effectiveness of Cardiac Resynchronization Therapy by QRS Morphology in the Multicenter Automatic Defibrillator Implantation Trial–Cardiac Resynchronization Therapy (MADIT-CRT). Circulation 2011;123:1061–1072.
323. Birnie DH, Ha A, Higginson L, Sidhu K, Green M, Philippon F, Thibault B, Wells G, Tang A. Impact of QRS morphology and duration on outcomes after cardiac resynchronization therapy: results from the Resynchronization-Defibrillation for Ambulatory Heart Failure Trial (RAFT). Circ Heart Fail 2013;6:1190–1198.
324. Nery PB, Ha AC, Keren A, Birnie DH. Cardiac resynchronization therapy in patients with left ventricular systolic dysfunction and right bundle branch block: a systematic review. Heart Rhythm 2011;8:1083–1087.
325. Sipahi I, Chou JC, Hyden M, Rowland DY, Simon DI, Fang JC. Effect of QRS morphology on clinical event reduction with cardiac resynchronization therapy: meta-analysis of randomized controlled trials. Am Heart J 2012;163:260–267.
326. Bilchick KC, Kamath S, DiMarco JP, Stukenborg GJ. Bundle-branch block morphology and other predictors of outcome after cardiac resynchronization therapy in Medicare patients. Circulation 2010;122:2022–2030.
327. Tang AS, Wells GA, Talajic M, Arnold MO, Sheldon R, Connolly S, Hohnloser SH, Nichol G, Birnie DH, Sapp JL, Yee R, Healey JS, Rouleau JL, ResynchronizationDefibrillation for Ambulatory Heart Failure Trial (RAFT) Investigators. Cardiac-resynchronization therapy for mild-to-moderate heart failure. N Engl J Med 2010;363:2385–2395.
328. Sipahi I, Carrigan TP, Rowland DY, Stambler BS, Fang JC. Impact of QRS duration on clinical event reduction with cardiac resynchronization therapy: meta-analysis of randomized controlled trials. Arch Intern Med 2011;171:1454–1462.
329. Moss AJ, Hall WJ, Cannom DS, Klein H, Brown MW, Daubert JP, Estes NA 3rd, Foster E, Greenberg H, Higgins SL, Pfeffer MA, Solomon SD, Wilber D, Zareba W, MADIT-CRT Trial Investigators. Cardiac-resynchronization therapy for the prevention of heart-failure events. N Engl J Med 2009;361:1329–1338.
330. Linde C, Leclercq C, Rex S, Garrigue S, Lavergne T, Cazeau S, McKenna W, Fitzgerald M, Deharo JC, Alonso C, Walker S, Braunschweig F, Bailleul C, Daubert JC. Long-term benefits of biventricular pacing in congestive heart failure: results from the MUltisite STimulation in cardiomyopathy (MUSTIC) study. J Am Coll Cardiol 2002;40:111–118.
331. Doshi RN, Daoud EG, Fellows C, Turk K, Duran A, Hamdan MH, Pires LA, PAVE Study Group. Left ventricular-based cardiac stimulation post AV nodal ablation evaluation (the PAVE study). J Cardiovasc Electrophysiol 2005;16:1160–1165.
332. Ganesan AN, Brooks AG, Roberts-Thomson KC, Lau DH, Kalman JM, Sanders P. Role of AV nodal ablation in cardiac resynchronization in patients with coexistent atrial fibrillation and heart failure a systematic review. J Am Coll Cardiol 2012;59: 719–726.
333. Gasparini M, Leclercq C, Lunati M, Landolina M, Auricchio A, Santini M, Boriani G, Lamp B, Proclemer A, Curnis A, Klersy C, Leyva F. Cardiac resynchronization therapy in patients with atrial fibrillation: the CERTIFY study (Cardiac Resynchronization Therapy in Atrial Fibrillation Patients Multinational Registry). JACC Heart Fail 2013;1:500–507.
334. Cleland JG, Abraham WT, Linde C, Gold MR, Young JB, Claude Daubert J, Sherfesee L, Wells GA, Tang AS. An individual patient meta-analysis of five randomized trials assessing the effects of cardiac resynchronization therapy on morbidity and mortality in patients with symptomatic heart failure. Eur Heart J 2013; 34:3547–3556.
335. Cleland JG, Daubert JC, Erdmann E, Freemantle N, Gras D, Kappenberger L, Tavazzi L. Longer-term effects of cardiac resynchronization therapy on mortality in heart failure [the CArdiac REsynchronization-Heart Failure (CARE-HF) trial extension phase]. Eur Heart J 2006;27:1928–1932.
336. Gold MR, Thebault C, Linde C, Abraham WT, Gerritse B, Ghio S, St John Sutton M, Daubert JC. Effect of QRS duration and morphology on cardiac resynchronization therapy outcomes in mild heart failure: results from the Resynchronization Reverses Remodeling in Systolic Left Ventricular Dysfunction (REVERSE) study. Circulation 2012;126:822–829.
337. Cunnington C, Kwok CS, Satchithananda DK, Patwala A, Khan MA, Zaidi A, Ahmed FZ, Mamas MA. Cardiac resynchronisation therapy is not associated with a reduction in mortality or heart failure hospitalisation in patients with nonleft bundle branch block QRS morphology: meta-analysis of randomised controlled trials. Heart 2015 Feb 12. doi:10.1136/heartjnl-2014-306811 [Epub ahead of print].
338. Magee CD, Byars LA, DeZee KJ. Limitations of subgroup analyses in meta-analysis of cardiac resynchronization therapy by QRS duration. Arch Intern Med 2012;172: 375.
339. Ruschitzka F, Abraham WT, Singh JP, Bax JJ, Borer JS, Brugada J, Dickstein K, Ford I, Gorcsan J 3rd, Gras D, Krum H, Sogaard P, Holzmeister J, Echo CRTSG. Cardiac-resynchronization therapy in heart failure with a narrow QRS complex. N Engl J Med 2013;369:1395–1405.
340. Camm AJ, Kirchhof P, Lip GY, Schotten U, Savelieva I, Ernst S, Van Gelder IC, Al-Attar N, Hindricks G, Prendergast B, Heidbuchel H, Alfieri O, Angelini A, Atar D, Colonna P, De Caterina R, De Sutter J, Goette A, Gorenek B, Heldal M, Hohloser SH, Kolh P, Le Heuzey JY, Ponikowski P, Rutten FH. Guidelines for the management of atrial fibrillation: the Task Force for the Management of Atrial Fibrillation of the European Society of Cardiology (ESC). Eur Heart J 2010;31:2369–2429.
341. Deyell MW, Park KM, Han Y, Frankel DS, Dixit S, Cooper JM, Hutchinson MD, Lin D, Garcia F, Bala R, Riley MP, Gerstenfeld E, Callans DJ, Marchlinski FE. Predictors of recovery of left ventricular dysfunction after ablation of frequent ventricular premature depolarizations. Heart Rhythm 2012;9:1465–1472.
342. Baman TS, Lange DC, Ilg KJ, Gupta SK, Liu TY, Alguire C, Armstrong W, Good E, Chugh A, Jongnarangsin K, Pelosi F Jr., Crawford T, Ebinger M, Oral H, Morady F, Bogun F. Relationship between burden of premature ventricular complexes and left ventricular function. Heart Rhythm 2010;7:865–869.
343. Ban JE, Park HC, Park JS, Nagamoto Y, Choi JI, Lim HE, Park SW, Kim YH. Electrocardiographic and electrophysiological characteristics of premature ventricular complexes associated with left ventricular dysfunction in patients without structural heart disease. Europace 2013;15:735–741.
344. Maggioni AP, Zuanetti G, Franzosi MG, Rovelli F, Santoro E, Staszewsky L, Tavazzi L, Tognoni G. Prevalence and prognostic significance of ventricular arrhythmias after acute myocardial infarction in the fibrinolytic era. GISSI-2 results. Circulation 1993;87:312–322.
345. Blanck Z, Dhala A, Deshpande S, Sra J, Jazayeri M, Akhtar M. Bundle branch reentrant ventricular tachycardia: cumulative experience in 48 patients. J Cardiovasc Electrophysiol 1993;4:253–262. 346. Caceres J, Jazayeri M, McKinnie J, Avitall B, Denker ST, Tchou P, Akhtar M. Sustained bundle branch reentry as a mechanism of clinical tachycardia. Circulation 1989;79:256–270.
347. Tchou P, Jazayeri M, Denker S, Dongas J, Caceres J, Akhtar M. Transcatheter electrical ablation of right bundle branch. A method of treating macroreentrant ventricular tachycardia attributed to bundle branch reentry. Circulation 1988;78: 246–257.
348. Elliott P, Andersson B, Arbustini E, Bilinska Z, Cecchi F, Charron P, Dubourg O, Kuhl U, Maisch B, McKenna WJ, Monserrat L, Pankuweit S, Rapezzi C, Seferovic P, Tavazzi L, Keren A. Classification of the cardiomyopathies: a position statement from the European Society Of Cardiology Working Group on Myocardial and Pericardial Diseases. Eur Heart J 2008;29:270–276.
349. Taylor MR, Carniel E, Mestroni L. Familial dilated cardiomyopathy. Orphanet J Rare Dis 2006;1:27.
350. Towbin JA, Lowe AM, Colan SD, Sleeper LA, Orav EJ, Clunie S, Messere J, Cox GF, Lurie PR, Hsu D, Canter C, Wilkinson JD, Lipshultz SE. Incidence, causes, and outcomes of dilated cardiomyopathy in children. JAMA 2006;296:1867–1876.
351. Petretta M, Pirozzi F, Sasso L, Paglia A, Bonaduce D. Review and metaanalysis of the frequency of familial dilated cardiomyopathy. Am J Cardiol 2011;108: 1171–1176.
352. Haas J, Frese KS, Peil B, Kloos W, Keller A, Nietsch R, Feng Z, Muller S, Kayvanpour E, Vogel B, Sedaghat-Hamedani F, Lim WK, Zhao X, Fradkin D, Kohler D, Fischer S, Franke J, Marquart S, Barb I, Li DT, Amr A, Ehlermann P, Mereles D, Weis T, Hassel S, Kremer A, King V, Wirsz E, Isnard R, Komajda M, Serio A, Grasso M, Syrris P, Wicks E, Plagnol V, Lopes L, Gadgaard T, Eiskjaer H, Jorgensen M, Garcia-Giustiniani D, Ortiz-Genga M, Crespo-Leiro MG, Deprez RH, Christiaans I, van Rijsingen IA, Wilde AA, Waldenstrom A, Bolognesi M, Bellazzi R, Morner S, Bermejo JL, Monserrat L, Villard E, Mogensen J, Pinto YM, Charron P, Elliott P, Arbustini E, Katus HA, Meder B. Atlas of the clinical genetics of human dilated cardiomyopathy. Eur Heart J 2015;36:1123–1135.
353. Hershberger RE, Lindenfeld J, Mestroni L, Seidman CE, Taylor MR, Towbin JA. Genetic evaluation of cardiomyopathy—a Heart Failure Society of America practice guideline. J Card Fail 2009;15:83–97.
354. Strickberger SA, Hummel JD, Bartlett TG, Frumin HI, Schuger CD, Beau SL, Bitar C, Morady F, Investigators A. Amiodarone versus implantable cardioverterdefibrillator:randomized trial in patients with nonischemic dilated cardiomyopathy and asymptomatic nonsustained ventricular tachycardia— AMIOVIRT. J Am Coll Cardiol 2003;41:1707–1712.
355. Proietti R, Essebag V, Beardsall J, Hache P, Pantano A, Wulffhart Z, Juta R, Tsang B, Joza J, Nascimento T, Pegoraro V, Khaykin Y, Verma A. Substrate-guided ablation of haemodynamically tolerated and untolerated ventricular tachycardia in patients with structural heart disease: effect of cardiomyopathy type and acute success on long-term outcome. Europace. 2015;17:461–467.
356. Kober L, Torp-Pedersen C, McMurray JJ, Gotzsche O, Levy S, Crijns H, Amlie J, Carlsen J, Dronedarone Study G. Increased mortality after dronedarone therapy for severe heart failure. N Engl J Med 2008;358:2678–2687.
357. Connolly SJ, Camm AJ, Halperin JL, Joyner C, Alings M, Amerena J, Atar D, Avezum A, Blomstrom P, Borggrefe M, Budaj A, Chen SA, Ching CK, Commerford P, Dans A, Davy JM, Delacretaz E, Di Pasquale G, Diaz R, Dorian P, Flaker G, Golitsyn S, Gonzalez-Hermosillo A, Granger CB, Heidbuchel H, Kautzner J, Kim JS, Lanas F, Lewis BS, Merino JL, Morillo C, Murin J, Narasimhan C, Paolasso E, Parkhomenko A, Peters NS, Sim KH, Stiles MK, Tanomsup S, Toivonen L, Tomcsanyi J, Torp-Pedersen C, Tse HF, Vardas P, Vinereanu D, Xavier D, Zhu J, Zhu JR, Baret-Cormel L, Weinling E, Staiger C, Yusuf S, Chrolavicius S, Afzal R, Hohnloser SH. Dronedarone in highrisk permanent atrial fibrillation. N Engl J Med 2011;365:2268–2276.
358. Castelli G, Fornaro A, Ciaccheri M, Dolara A, Troiani V, Tomberli B, Olivotto I, Gensini GF. Improving survival rates of patients with idiopathic dilated cardiomyopathy in Tuscany over 3 decades: impact of evidence-based management. Circ Heart Fail 2013;6:913–921.
359. Alexander PM, Daubeney PE, Nugent AW, Lee KJ, Turner C, Colan SD, Robertson T, Davis AM, Ramsay J, Justo R, Sholler GF, King I, Weintraub RG. Long-term outcomes of dilated cardiomyopathy diagnosed during childhood: results from a national population-based study of childhood cardiomyopathy. Circulation 2013;128:2039–2046.
360. Kuruvilla S, Adenaw N, Katwal AB, Lipinski MJ, Kramer CM, Salerno M. Late gadolinium enhancement on cardiac magnetic resonance predicts adverse cardiovascular outcomes in nonischemic cardiomyopathy: a systematic review and meta-analysis. Circ Cardiovasc Imaging 2014;7:250–258.
361. Bansch D, Antz M, Boczor S, Volkmer M, Tebbenjohanns J, Seidl K, Block M, Gietzen F, Berger J, Kuck KH. Primary prevention of sudden cardiac death in idiopathic dilated cardiomyopathy: the Cardiomyopathy Trial (CAT). Circulation 2002; 105:1453–1458.
362. Roden DM. Drug-induced prolongation of the QT interval. N Engl J Med 2004; 350:1013–1022.
363. Chamberlain DA, Jewitt DE, Julian DG, Campbell RW, Boyle DM, Shanks RG. Oral mexiletine in high-risk patients after myocardial infarction. Lancet 1980;2: 1324–1327.
364. Elliott PM, Gimeno JR, Thaman R, Shah J, Ward D, Dickie S, Tome Esteban MT, McKenna WJ. Historical trends in reported survival rates in patients with hypertrophic cardiomyopathy. Heart 2006;92:785–791.
365. OMahony C, Jichi F, Pavlou M, Monserrat L, Anastasakis A, Rapezzi C, Biagini E, Gimeno JR, Limongelli G, McKenna WJ, Omar RZ, Elliott PM. A novel clinical risk prediction model for sudden cardiac death in hypertrophic cardiomyopathy (HCM risk-SCD). Eur Heart J 2014;35:2010–2020.
366. Pelliccia A, Fagard R, Bjornstad HH, Anastassakis A, Arbustini E, Assanelli D, Biffi A, Borjesson M, Carre F, Corrado D, Delise P, Dorwarth U, Hirth A, Heidbuchel H, Hoffmann E, Mellwig KP, Panhuyzen-Goedkoop N, Pisani A, Solberg EE, van-Buuren F, Vanhees L, Blomstrom-Lundqvist C, Deligiannis A, Dugmore D, Glikson M, Hoff PI, Hoffmann A, Horstkotte D, Nordrehaug JE, Oudhof J, McKenna WJ, Penco M, Priori S, Reybrouck T, Senden J, Spataro A, Thiene G. Recommendations for competitive sports participation in athletes with cardiovascular disease: a consensus document from the Study Group of Sports Cardiology of the Working Group of Cardiac Rehabilitation and Exercise Physiology and the Working Group of Myocardial and Pericardial Diseases of the European Society of Cardiology. Eur Heart J 2005;26:1422–1445.
367. OMahony C, Tome-Esteban M, Lambiase PD, Pantazis A, Dickie S, McKenna WJ, Elliott PM. A validation study of the 2003 American College of Cardiology/European Society of Cardiology and 2011 American College of Cardiology Foundation/American Heart Association risk stratification and treatment algorithms for sudden cardiac death in patients with hypertrophic cardiomyopathy. Heart 2013;99:534–541.
368. OMahony C, Lambiase PD, Quarta G, Cardona M, Calcagnino M, Tsovolas K, Al-Shaikh S, Rahman SM, Arnous S, Jones S, McKenna W, Elliott P. The long-term survival and the risks and benefits of implantable cardioverter defibrillators in patients with hypertrophic cardiomyopathy. Heart 2012;98:116–125.
369. Elliott PM, Sharma S, Varnava A, Poloniecki J, Rowland E, McKenna WJ. Survival after cardiac arrest or sustained ventricular tachycardia in patients with hypertrophic cardiomyopathy. J Am Coll Cardiol 1999;33:1596–1601.
370. Cecchi F, Maron BJ, Epstein SE. Long-term outcome of patients with hypertrophic cardiomyopathy successfully resuscitated after cardiac arrest. J Am Coll Cardiol 1989;13:1283–1288.
371. Maron BJ, Spirito P, Shen WK, Haas TS, Formisano F, Link MS, Epstein AE, Almquist AK, Daubert JP, Lawrenz T, Boriani G, Estes NA 3rd, Favale S, Piccininno M, Winters SL, Santini M, Betocchi S, Arribas F, Sherrid MV, Buja G, Semsarian C, Bruzzi P. Implantable cardioverter-defibrillators and prevention of sudden cardiac death in hypertrophic cardiomyopathy. JAMA 2007;298:405–412.
372. Syska P, Przybylski A, Chojnowska L, Lewandowski M, Sterlinski M, Maciag A, Gepner K, Pytkowski M, Kowalik I, Maczynska-Mazuruk R, Ruzyllo W, Szwed H. Implantable cardioverter-defibrillator in patients with hypertrophic cardiomyopathy: efficacy and complications of the therapy in long-term follow-up. J Cardiovasc Electrophysiol 2010;21:883–889.
373. Monserrat L, Elliott PM, Gimeno JR, Sharma S, Penas-Lado M, McKenna WJ. Nonsustained ventricular tachycardia in hypertrophic cardiomyopathy: an independent marker of sudden death risk in young patients. J Am Coll Cardiol 2003;42: 873–879.
374. Adabag AS, Casey SA, Kuskowski MA, Zenovich AG, Maron BJ. Spectrum and prognostic significance of arrhythmias on ambulatory Holter electrocardiogram in hypertrophic cardiomyopathy. J Am Coll Cardiol 2005;45:697–704.
375. OHanlon R, Grasso A, Roughton M, Moon JC, Clark S, Wage R, Webb J, Kulkarni M, Dawson D, Sulaibeekh L, Chandrasekaran B, Bucciarelli-Ducci C, Pasquale F, Cowie MR, McKenna WJ, Sheppard MN, Elliott PM, Pennell DJ, Prasad SK. Prognostic significance of myocardial fibrosis in hypertrophic cardiomyopathy. J Am Coll Cardiol 2010;56:867–874.
376. Gimeno JR, Tome-Esteban M, Lofiego C, Hurtado J, Pantazis A, Mist B, Lambiase P, McKenna WJ, Elliott PM. Exercise-induced ventricular arrhythmias and risk of sudden cardiac death in patients with hypertrophic cardiomyopathy. Eur Heart J 2009; 30:2599–2605.
377. Inada K, Seiler J, Roberts-Thomson KC, Steven D, Rosman J, John RM, Sobieszczyk P, Stevenson WG, Tedrow UB. Substrate characterization and catheter ablation for monomorphic ventricular tachycardia in patients with apical hypertrophic cardiomyopathy. J Cardiovasc Electrophysiol 2011;22:41–48.
378. Maron BJ, McKenna WJ, Danielson GK, Kappenberger LJ, Kuhn HJ, Seidman CE, Shah PM, Spencer WH 3rd, Spirito P, Ten Cate FJ, Wigle ED. American College of Cardiology/European Society of Cardiology Clinical Expert Consensus Document on Hypertrophic Cardiomyopathy. A report of the American College of Cardiology Foundation Task Force on Clinical Expert Consensus Documents and the European Society of Cardiology Committee for Practice Guidelines. Eur Heart J 2003;24:1965–1991.
379. Gersh BJ, Maron BJ, Bonow RO, Dearani JA, Fifer MA, Link MS, Naidu SS, Nishimura RA, Ommen SR, Rakowski H, Seidman CE, Towbin JA, Udelson JE, Yancy CW, American College of Cardiology Foundation/American Heart Association Task Force on Practice Guidelines, American Association for Thoracic Surgery, American Society of Echocardiography, American Society of Nuclear Cardiology, Heart Failure Society of America, Heart Rhythm Society, Society for Cardiovascular Angiography and Interventions, Society of Thoracic Surgeons. 2011 ACCF/AHA guideline for the diagnosis and treatment of hypertrophic cardiomyopathy: a report of the American College of Cardiology Foundation/American Heart Association Task Force on Practice Guidelines. Circulation 2011;124: e783–e831.
380. McKenna WJ, Oakley CM, Krikler DM, Goodwin JF. Improved survival with amiodarone in patients with hypertrophic cardiomyopathy and ventricular tachycardia. Br Heart J 1985;53:412–416.
381. Melacini P, Maron BJ, Bobbo F, Basso C, Tokajuk B, Zucchetto M, Thiene G, Iliceto S. Evidence that pharmacological strategies lack efficacy for the prevention of sudden death in hypertrophic cardiomyopathy. Heart 2007;93:708–710.
382. Marcus FI, McKenna WJ, Sherrill D, Basso C, Bauce B, Bluemke DA, Calkins H, Corrado D, Cox MG, Daubert JP, Fontaine G, Gear K, Hauer R, Nava A, Picard MH, Protonotarios N, Saffitz JE, Sanborn DM, Steinberg JS, Tandri H, Thiene G, Towbin JA, Tsatsopoulou A, Wichter T, Zareba W. Diagnosis of arrhythmogenic right ventricular cardiomyopathy/dysplasia: proposed modification of the task force criteria. Eur Heart J 2010;31:806–814.
383. Basso C, Corrado D, Marcus FI, Nava A, Thiene G. Arrhythmogenic right ventricular cardiomyopathy. Lancet 2009;373:1289–1300.
384. Sen-Chowdhry S, Syrris P, Prasad SK, Hughes SE, Merrifield R, Ward D, Pennell DJ, McKenna WJ. Left-dominant arrhythmogenic cardiomyopathy: an under-recognized clinical entity. J Am Coll Cardiol 2008;52:2175–2187.
385. Basso C, Corrado D, Thiene G. Cardiovascular causes of sudden death in young individuals including athletes. Cardiol Rev 1999;7:127–135.
386. Tabib A, Loire R, Chalabreysse L, Meyronnet D, Miras A, Malicier D, Thivolet F, Chevalier P, Bouvagnet P. Circumstances of death and gross and microscopic observations in a series of 200 cases of sudden death associated with arrhythmogenic right ventricular cardiomyopathy and/or dysplasia. Circulation 2003;108: 3000–3005.
387. Schinkel AF. Implantable cardioverter defibrillators in arrhythmogenic right ventricular dysplasia/cardiomyopathy: patient outcomes, incidence of appropriate and inappropriate interventions, and complications. Circ Arrhythm Electrophysiol 2013;6:562–568.
388. Ruwald AC, Marcus F, Estes NA 3rd, Link M, McNitt S, Polonsky B, Calkins H, Towbin JA, Moss AJ, Zareba W. Association of competitive and recreational sport participation with cardiac events in patients with arrhythmogenic right ventricular cardiomyopathy: results from the North American multidisciplinary study of arrhythmogenic right ventricular cardiomyopathy. Eur Heart J 2015;36:1735–43.
389. Corrado D, Leoni L, Link MS, Della Bella P, Gaita F, Curnis A, Salerno JU, Igidbashian D, Raviele A, Disertori M, Zanotto G, Verlato R, Vergara G, Delise P, Turrini P, Basso C, Naccarella F, Maddalena F, Estes NA 3rd, Buja G, Thiene G. Implantable cardioverter-defibrillator therapy for prevention of sudden death in patients with arrhythmogenic right ventricular cardiomyopathy/dysplasia. Circulation 2003;108:3084–3091.
390. Marcus GM, Glidden DV, Polonsky B, Zareba W, Smith LM, Cannom DS, Estes NA 3rd, Marcus F, Scheinman MM, Multidisciplinary Study of Right Ventricular Dysplasia Investigators. Efficacy of antiarrhythmic drugs in arrhythmogenic right ventricular cardiomyopathy: a report from the North American ARVC Registry. J Am Coll Cardiol 2009;54:609–615.
391. Wichter T, Borggrefe M, Haverkamp W, Chen X, Breithardt G. Efficacy of antiarrhythmic drugs in patients with arrhythmogenic right ventricular disease. Results in patients with inducible and noninducible ventricular tachycardia. Circulation 1992;86:29–37.
392. Philips B, Madhavan S, James C, Tichnell C, Murray B, Dalal D, Bhonsale A, Nazarian S, Judge DP, Russell SD, Abraham T, Calkins H, Tandri H. Outcomes of catheter ablation of ventricular tachycardia in arrhythmogenic right ventricular dysplasia/cardiomyopathy. Circ Arrhythm Electrophysiol 2012;5:499–505.
393. Dalal D, Jain R, Tandri H, Dong J, Eid SM, Prakasa K, Tichnell C, James C, Abraham T, Russell SD, Sinha S, Judge DP, Bluemke DA, Marine JE, Calkins H. Long-term efficacy of catheter ablation of ventricular tachycardia in patients with arrhythmogenic right ventricular dysplasia/cardiomyopathy. J Am Coll Cardiol 2007;50:432–440.
394. Dalal D, Molin LH, Piccini J, Tichnell C, James C, Bomma C, Prakasa K, Towbin JA, Marcus FI, Spevak PJ, Bluemke DA, Abraham T, Russell SD, Calkins H, Judge DP. Clinical features of arrhythmogenic right ventricular dysplasia/cardiomyopathy associated with mutations in plakophilin-2. Circulation 2006;113:1641–1649.
395. Wichter T, Paul M, Wollmann C, Acil T, Gerdes P, Ashraf O, Tjan TD, Soeparwata R, Block M, Borggrefe M, Scheld HH, Breithardt G, Bocker D. Implantable cardioverter/defibrillator therapy in arrhythmogenic right ventricular cardiomyopathy: single-center experience of long-term follow-up and complications in 60 patients. Circulation 2004;109:1503–1508.
396. Nava A, Bauce B, Basso C, Muriago M, Rampazzo A, Villanova C, Daliento L, Buja G, Corrado D, Danieli GA, Thiene G. Clinical profile and long-term followup of 37 families with arrhythmogenic right ventricular cardiomyopathy. J Am Coll Cardiol 2000;36:2226–2233.
397. Nasir K, Bomma C, Tandri H, Roguin A, Dalal D, Prakasa K, Tichnell C, James C, Spevak PJ, Marcus F, Calkins H. Electrocardiographic features of arrhythmogenic right ventricular dysplasia/cardiomyopathy according to disease severity: a need to broaden diagnostic criteria. Circulation 2004;110:1527–1534.
398. Hamid MS, Norman M, Quraishi A, Firoozi S, Thaman R, Gimeno JR, Sachdev B, Rowland E, Elliott PM, McKenna WJ. Prospective evaluation of relatives for familial arrhythmogenic right ventricular cardiomyopathy/dysplasia reveals a need to broaden diagnostic criteria. J Am Coll Cardiol 2002;40:1445–1450.
399. Sen-Chowdhry S, Syrris P, Ward D, Asimaki A, Sevdalis E, McKenna WJ. Clinical and genetic characterization of families with arrhythmogenic right ventricular dysplasia/cardiomyopathy provides novel insights into patterns of disease expression. Circulation 2007;115:1710–1720.
400. Hoffmayer KS, Machado ON, Marcus GM, Yang Y, Johnson CJ, Ermakov S, Vittinghoff E, Pandurangi U, Calkins H, Cannom D, Gear KC, Tichnell C, Park Y, Zareba W, Marcus FI, Scheinman MM. Electrocardiographic comparison of ventricular arrhythmias in patients with arrhythmogenic right ventricular cardiomyopathy and right ventricular outflow tract tachycardia. J Am Coll Cardiol 2011;58:831–838.
401. Link MS, Laidlaw D, Polonsky B, Zareba W, McNitt S, Gear K, Marcus F, Estes NA 3rd. Ventricular arrhythmias in the North American multidisciplinary study of ARVC: predictors, characteristics, and treatment. J Am Coll Cardiol 2014;64: 119–125.
402. Ouyang F, Fotuhi P, Goya M, Volkmer M, Ernst S, Cappato R, Kuck K. Ventricular tachycardia around the tricuspid annulus in right ventricular dysplasia. Circulation 2001;103:913–914.
403. Heidbuchel H, Hoogsteen J, Fagard R, Vanhees L, Ector H, Willems R, Van Lierde J. High prevalence of right ventricular involvement in endurance athletes with ventricular arrhythmias. Role of an electrophysiologic study in risk stratification. Eur Heart J 2003;24:1473–1480.
404. Corrado D, Calkins H, Link MS, Leoni L, Favale S, Bevilacqua M, Basso C, Ward D, Boriani G, Ricci R, Piccini JP, Dalal D, Santini M, Buja G, Iliceto S, Estes NA 3rd, Wichter T, McKenna WJ, Thiene G, Marcus FI. Prophylactic implantable defibrillator in patients with arrhythmogenic right ventricular cardiomyopathy/dysplasia and no prior ventricular fibrillation or sustained ventricular tachycardia. Circulation 2010;122:1144–1152.
405. Peters S. Long-term follow-up and risk assessment of arrhythmogenic right ventricular dysplasia/cardiomyopathy: personal experience from different primary and tertiary centres. J Cardiovasc Med (Hagerstown) 2007;8:521–526.
406. Lemola K, Brunckhorst C, Helfenstein U, Oechslin E, Jenni R, Duru F. Predictors of adverse outcome in patients with arrhythmogenic right ventricular dysplasia/cardiomyopathy: long term experience of a tertiary care centre. Heart 2005;91: 1167–1172.
407. Rigato I, Bauce B, Rampazzo A, Zorzi A, Pilichou K, Mazzotti E, Migliore F, Marra MP, Lorenzon A, De Bortoli M, Calore M, Nava A, Daliento L, Gregori D, Iliceto S, Thiene G, Basso C, Corrado D. Compound and digenic heterozygosity predicts lifetime arrhythmic outcome and sudden cardiac death in desmosomal gene-related arrhythmogenic right ventricular cardiomyopathy. Circ Cardiovasc Genet 2013;6:533–542.
408. Kristen AV, Dengler TJ, Hegenbart U, Schonland SO, Goldschmidt H, Sack FU, Voss F, Becker R, Katus HA, Bauer A. Prophylactic implantation of cardioverterdefibrillator in patients with severe cardiac amyloidosis and high risk for sudden cardiac death. Heart Rhythm 2008;5:235–240.
409. Palladini G, Malamani G, Co F, Pistorio A, Recusani F, Anesi E, Garini P, Merlini G. Holter monitoring in AL amyloidosis: prognostic implications. Pacing Clin Electrophysiol 2001;24:1228–1233.
410. Dubrey SW, Bilazarian S, LaValley M, Reisinger J, Skinner M, Falk RH. Signal-averaged electrocardiography in patients with AL (primary) amyloidosis. Am Heart J 1997;134:994–1001.
411. Reisinger J, Dubrey SW, Lavalley M, Skinner M, Falk RH. Electrophysiologic abnormalities in AL (primary) amyloidosis with cardiac involvement. J Am Coll Cardiol 1997;30:1046–1051.
412. Ammash NM, Seward JB, Bailey KR, Edwards WD, Tajik AJ. Clinical profile and outcome of idiopathic restrictive cardiomyopathy. Circulation 2000;101: 2490–2496.
413. Dubrey SW. Amyloid heart disease: a brief review of treatment options. Postgrad Med J 2012;88:700–705. 414. Ruberg FL, Berk JL. Transthyretin (TTR) cardiac amyloidosis. Circulation 2012;126: 1286–1300.
415. Jaccard A, Comenzo RL, Hari P, Hawkins PN, Roussel M, Morel P, Macro M, Pellegrin JL, Lazaro E, Mohty D, Mercie P, Decaux O, Gillmore J, Lavergne D, Bridoux F, Wechalekar AD, Venner CP. Efficacy of bortezomib, cyclophosphamide and dexamethasone in treatment-naive patients with high-risk cardiac AL amyloidosis (Mayo Clinic stage III). Haematologica 2014;99:1479–1485.
416. Falk RH, Rubinow A, Cohen AS. Cardiac arrhythmias in systemic amyloidosis: correlation with echocardiographic abnormalities. J Am Coll Cardiol 1984;3:107–113.
417. Maskatia SA, Decker JA, Spinner JA, Kim JJ, Price JF, Jefferies JL, Dreyer WJ, Smith EO, Rossano JW, Denfield SW. Restrictive physiology is associated with poor outcomes in children with hypertrophic cardiomyopathy. Pediatr Cardiol 2012;33:141–149.
418. Rivenes SM, Kearney DL, Smith EO, Towbin JA, Denfield SW. Sudden death and cardiovascular collapse in children with restrictive cardiomyopathy. Circulation 2000;102:876–882.
419. Lipshultz SE, Orav EJ, Wilkinson JD, Towbin JA, Messere JE, Lowe AM, Sleeper LA, Cox GF, Hsu DT, Canter CE, Hunter JA, Colan SD. Risk stratification at diagnosis for children with hypertrophic cardiomyopathy: an analysis of data from the Pediatric Cardiomyopathy Registry. Lancet 2013;382:1889–1897.
420. Webber SA, Lipshultz SE, Sleeper LA, Lu M, Wilkinson JD, Addonizio LJ, Canter CE, Colan SD, Everitt MD, Jefferies JL, Kantor PF, Lamour JM, Margossian R, Pahl E, Rusconi PG, Towbin JA. Outcomes of restrictive cardiomyopathy in childhood and the influence of phenotype: a report from the Pediatric Cardiomyopathy Registry. Circulation 2012;126:1237–1244.
421. Kaski JP, Syrris P, Burch M, Tome-Esteban MT, Fenton M, Christiansen M, Andersen PS, Sebire N, Ashworth M, Deanfield JE, McKenna WJ, Elliott PM. Idiopathic restrictive cardiomyopathy in children is caused by mutations in cardiac sarcomere protein genes. Heart 2008;94:1478–1484.
422. Bhatia NL, Tajik AJ, Wilansky S, Steidley DE, Mookadam F. Isolated noncompaction of the left ventricular myocardium in adults: a systematic overview. J Card Fail 2011;17:771–778.
423. Oechslin E, Jenni R. Left ventricular non-compaction revisited: a distinct phenotype with genetic heterogeneity? Eur Heart J 2011;32:1446–1456.
424. Lofiego C, Biagini E, Pasquale F, Ferlito M, Rocchi G, Perugini E, Bacchi-Reggiani L, Boriani G, Leone O, Caliskan K, ten Cate FJ, Picchio FM, Branzi A, Rapezzi C. Wide spectrum of presentation and variable outcomes of isolated left ventricular noncompaction. Heart 2007;93:65–71.
425. Murphy RT, Thaman R, Blanes JG, Ward D, Sevdalis E, Papra E, Kiotsekoglou A, Tome MT, Pellerin D, McKenna WJ, Elliott PM. Natural history and familial characteristics of isolated left ventricular non-compaction. Eur Heart J 2005;26: 187–192.
426. Muratore CA, Batista Sa LA, Chiale PA, Eloy R, Tentori MC, Escudero J, Lima AM, Medina LE, Garillo R, Maloney J. Implantable cardioverter defibrillators and Chagas disease: results of the ICD Registry Latin America. Europace 2009;11: 164–168.
427. Martinelli M, de Siqueira SF, Sternick EB, Rassi A Jr, Costa R, Ramires JA, Kalil Filho R. Long-term follow-up of implantable cardioverter-defibrillator for secondary prevention in Chagas heart disease. Am J Cardiol 2012;110:1040–1045.
428. Cardinalli-Neto A, Bestetti RB, Cordeiro JA, Rodrigues VC. Predictors of all-cause mortality for patients with chronic Chagas heart disease receiving implantable cardioverter defibrillator therapy. J Cardiovasc Electrophysiol 2007;18:1236–1240.
429. Barbosa MP, da Costa Rocha MO, de Oliveira AB, Lombardi F, Ribeiro AL. Efficacy and safety of implantable cardioverter-defibrillators in patients with Chagas disease. Europace 2013;15:957–962.
430. Gali WL, Sarabanda AV, Baggio JM, Ferreira LG, Gomes GG, Marin-Neto JA, Junqueira LF. Implantable cardioverter-defibrillators for treatment of sustained ventricular arrhythmias in patients with Chagas heart disease: comparison with a control group treated with amiodarone alone. Europace 2014;16:674–680.
431. Schwartz PJ, Moss AJ, Vincent GM, Crampton RS. Diagnostic criteria for the long QT syndrome. An update. Circulation 1993;88:782–784.
432. Moss AJ, Schwartz PJ, Crampton RS, Tzivoni D, Locati EH, MacCluer J, Hall WJ, Weitkamp L, Vincent GM, Garson A Jr. The long QT syndrome. Prospective longitudinal study of 328 families. Circulation 1991;84:1136–1144.
433. Nguyen HL, Pieper GH, Wilders R. Andersen–Tawil syndrome: clinical and molecular aspects. Int J Cardiol 2013;170:1–16.
434. Schwartz PJ, Priori SG, Spazzolini C, Moss AJ, Vincent GM, Napolitano C, Denjoy I, Guicheney P, Breithardt G, Keating MT, Towbin JA, Beggs AH, Brink P, Wilde AA, Toivonen L, Zareba W, Robinson JL, Timothy KW, Corfield V, Wattanasirichaigoon D, Corbett C, Haverkamp W, Schulze-Bahr E, Lehmann MH, Schwartz K, Coumel P, Bloise R. Genotype-phenotype correlation in the long-QT syndrome: gene-specific triggers for life-threatening arrhythmias. Circulation 2001;103:89–95.
435. Priori SG, Napolitano C, Schwartz PJ, Grillo M, Bloise R, Ronchetti E, Moncalvo C, Tulipani C, Veia A, Bottelli G, Nastoli J. Association of long QT syndrome loci and cardiac events among patients treated with beta-blockers. JAMA 2004;292: 1341–1344.
436. Moss AJ, Zareba W, Hall WJ, Schwartz PJ, Crampton RS, Benhorin J, Vincent GM, Locati EH, Priori SG, Napolitano C, Medina A, Zhang L, Robinson JL, Timothy K, Towbin JA, Andrews ML. Effectiveness and limitations of beta-blocker therapy in congenital long-QT syndrome. Circulation 2000;101:616–623.
437. Zareba W, Moss AJ, Daubert JP, Hall WJ, Robinson JL, Andrews M. Implantable cardioverter defibrillator in high-risk long QT syndrome patients. J Cardiovasc Electrophysiol 2003;14:337–341.
438. Schwartz PJ, Spazzolini C, Priori SG, Crotti L, Vicentini A, Landolina M, Gasparini M, Wilde AA, Knops RE, Denjoy I, Toivonen L, Monnig G, Al-Fayyadh M, Jordaens L, Borggrefe M, Holmgren C, Brugada P, De Roy L, Hohnloser SH, Brink PA. Who are the long-QT syndrome patients who receive an implantable cardioverter-defibrillator and what happens to them?: data from the European Long-QT Syndrome Implantable Cardioverter-Defibrillator (LQTS ICD) Registry. Circulation 2010;122:1272–1282.
439. Jons C, Moss AJ, Goldenberg I, Liu J, McNitt S, Zareba W, Qi M, Robinson JL. Risk of fatal arrhythmic events in long QT syndrome patients after syncope. J Am Coll Cardiol 2010;55:783–788.
440. Schwartz PJ, Priori SG, Cerrone M, Spazzolini C, Odero A, Napolitano C, Bloise R, De Ferrari GM, Klersy C, Moss AJ, Zareba W, Robinson JL, Hall WJ, Brink PA, Toivonen L, Epstein AE, Li C, Hu D. Left cardiac sympathetic denervation in the management of high-risk patients affected by the long-QT syndrome. Circulation 2004;109:1826–1833.
441. Schwartz PJ, Priori SG, Locati EH, Napolitano C, Cantu F, Towbin JA, Keating MT, Hammoude H, Brown AM, Chen LS. Long QT syndrome patients with mutations of the SCN5A and HERG genes have differential responses to Na+ channel blockade and to increases in heart rate. Implications for gene-specific therapy. Circulation 1995;92:3381–3386.
442. Moss AJ, Windle JR, Hall WJ, Zareba W, Robinson JL, McNitt S, Severski P, Rosero S, Daubert JP, Qi M, Cieciorka M, Manalan AS. Safety and efficacy of flecainide in subjects with Long QT-3 syndrome (DeltaKPQ mutation): a randomized, double-blind, placebo-controlled clinical trial. Ann Noninvasive Electrocardiol 2005;10:59–66.
443. Moss AJ, Zareba W, Schwarz KQ, Rosero S, McNitt S, Robinson JL. Ranolazine shortens repolarization in patients with sustained inward sodium current due to type-3 long-QT syndrome. J Cardiovasc Electrophysiol 2008;19:1289–1293.
444. Liu JF, Jons C, Moss AJ, McNitt S, Peterson DR, Qi M, Zareba W, Robinson JL, Barsheshet A, Ackerman MJ, Benhorin J, Kaufman ES, Locati EH, Napolitano C, Priori SG, Schwartz PJ, Towbin J, Vincent M, Zhang L, Goldenberg I. Risk factors for recurrent syncope and subsequent fatal or near-fatal events in children and adolescents with long QT syndrome. J Am Coll Cardiol 2011;57:941–950.
445. Seth R, Moss AJ, McNitt S, Zareba W, Andrews ML, Qi M, Robinson JL, Goldenberg I, Ackerman MJ, Benhorin J, Kaufman ES, Locati EH, Napolitano C, Priori SG, Schwartz PJ, Towbin JA, Vincent GM, Zhang L. Long QT syndrome and pregnancy. J Am Coll Cardiol 2007;49:1092–1098.
446. Goldenberg I, Horr S, Moss AJ, Lopes CM, Barsheshet A, McNitt S, Zareba W, Andrews ML, Robinson JL, Locati EH, Ackerman MJ, Benhorin J, Kaufman ES, Napolitano C, Platonov PG, Priori SG, Qi M, Schwartz PJ, Shimizu W, Towbin JA, Vincent GM, Wilde AA, Zhang L. Risk for life-threatening cardiac events in patients with genotype-confirmed long-QT syndrome and normal-range corrected QT intervals. J Am Coll Cardiol 2011;57:51–59.
447. Gaita F, Giustetto C, Bianchi F, Wolpert C, Schimpf R, Riccardi R, Grossi S, Richiardi E, Borggrefe M. Short QT syndrome: a familial cause of sudden death. Circulation 2003;108:965–970.
448. Gaita F, Giustetto C, Bianchi F, Schimpf R, Haissaguerre M, Calo L, Brugada R, Antzelevitch C, Borggrefe M, Wolpert C. Short QT syndrome: pharmacological treatment. J Am Coll Cardiol 2004;43:1494–1499.
449. Fowler SJ, Priori SG. Clinical spectrum of patients with a Brugada ECG. Curr Opin Cardiol 2009;24:74–81.
450. Gehi AK, Duong TD, Metz LD, Gomes JA, Mehta D. Risk stratification of individuals with the Brugada electrocardiogram: a meta-analysis. J Cardiovasc Electrophysiol 2006;17:577–583.
451. Priori SG, Napolitano C, Gasparini M, Pappone C, Della Bella P, Giordano U, Bloise R, Giustetto C, De Nardis R, Grillo M, Ronchetti E, Faggiano G, Nastoli J. Natural history of Brugada syndrome: insights for risk stratification and management. Circulation 2002;105:1342–1347.
452. Fauchier L, Isorni MA, Clementy N, Pierre B, Simeon E, Babuty D. Prognostic value of programmed ventricular stimulation in Brugada syndrome according to clinical presentation: an updated meta-analysis of worldwide published data. Int J Cardiol 2013;168:3027–3029.
453. Maury P, Hocini M, Haissaguerre M. Electrical storms in Brugada syndrome: review of pharmacologic and ablative therapeutic options. Indian Pacing Electrophysiol J 2005;5:25–34.
454. Marquez MF, Bonny A, Hernandez-Castillo E, De Sisti A, Gomez-Flores J, Nava S, Hidden-Lucet F, Iturralde P, Cardenas M, Tonet J. Long-term efficacy of low doses of quinidine on malignant arrhythmias in Brugada syndrome with an implantable cardioverter-defibrillator: a case series and literature review. Heart Rhythm 2012; 9:1995–2000.
455. Nademanee K, Veerakul G, Chandanamattha P, Chaothawee L, Ariyachaipanich A, Jirasirirojanakorn K, Likittanasombat K, Bhuripanyo K, Ngarmukos T. Prevention of ventricular fibrillation episodes in Brugada syndrome by catheter ablation over the anterior right ventricular outflow tract epicardium. Circulation 2011;123:1270–1279.
456. Priori SG, Gasparini M, Napolitano C, Della Bella P, Ottonelli AG, Sassone B, Giordano U, Pappone C, Mascioli G, Rossetti G, De Nardis R, Colombo M. Risk stratification in Brugada syndrome: results of the PRELUDE (PRogrammed ELectrical stimUlation preDictive valuE) registry. J Am Coll Cardiol 2012;59:37–45.
457. Coumel P. Catecholamine-induced severe ventricular arrhythmias with AdamsStokes syndrome in children: a report of four cases. Br Heart J 1978;40:28–37.
458. Priori SG, Napolitano C, Memmi M, Colombi B, Drago F, Gasparini M, DeSimone L, Coltorti F, Bloise R, Keegan R, Cruz Filho FE, Vignati G, Benatar A, DeLogu A. Clinical and molecular characterization of patients with catecholaminergic polymorphic ventricular tachycardia. Circulation 2002;106: 69–74.
459. Marjamaa A, Hiippala A, Arrhenius B, Lahtinen AM, Kontula K, Toivonen L, Happonen JM, Swan H. Intravenous epinephrine infusion test in diagnosis of catecholaminergic polymorphic ventricular tachycardia. J Cardiovasc Electrophysiol 2012;23:194–199.
460. Leenhardt A, Lucet V, Denjoy I, Grau F, Ngoc DD, Coumel P. Catecholaminergic polymorphic ventricular tachycardia in children. A 7-year follow-up of 21 patients. Circulation 1995;91:1512–1519.
461. Hayashi M, Denjoy I, Extramiana F, Maltret A, Buisson NR, Lupoglazoff JM, Klug D, Takatsuki S, Villain E, Kamblock J, Messali A, Guicheney P, Lunardi J, Leenhardt A. Incidence and risk factors of arrhythmic events in catecholaminergic polymorphic ventricular tachycardia. Circulation 2009;119:2426–2434.
462. van der Werf C, Nederend I, Hofman N, van Geloven N, Ebink C, Frohn-Mulder IM, Alings AM, Bosker HA, Bracke FA, van den Heuvel F, Waalewijn RA, Bikker H, van Tintelen JP, Bhuiyan ZA, van den Berg MP, Wilde AA. Familial evaluation in catecholaminergic polymorphic ventricular tachycardia: disease penetrance and expression in cardiac ryanodine receptor mutation-carrying relatives. Circ Arrhythm Electrophysiol 2012;5:748–756.
463. Watanabe H, Chopra N, Laver D, Hwang HS, Davies SS, Roach DE, Duff HJ, Roden DM, Wilde AA, Knollmann BC. Flecainide prevents catecholaminergic polymorphic ventricular tachycardia in mice and humans. Nat Med 2009;15: 380–383. 464. Olde Nordkamp LR, Driessen AH, Odero A, Blom NA, Koolbergen DR, Schwartz PJ, Wilde AA. Left cardiac sympathetic denervation in the Netherlands for the treatment of inherited arrhythmia syndromes. Neth Heart J 2014;22: 160–166.
465. Hofferberth SC, Cecchin F, Loberman D, Fynn-Thompson F. Left thoracoscopic sympathectomy for cardiac denervation in patients with life-threatening ventricular arrhythmias. J Thorac Cardiovasc Surg 2014;147:404–409. 466. Roses-Noguer F, Jarman JW, Clague JR, Till J. Outcomes of defibrillator therapy in catecholaminergic polymorphic ventricular tachycardia. Heart Rhythm 2014;11: 58–66.
467. Haissaguerre M, Derval N, Sacher F, Jesel L, Deisenhofer I, de Roy L, Pasquie JL, Nogami A, Babuty D, Yli-Mayry S, De Chillou C, Scanu P, Mabo P, Matsuo S, Probst V, Le Scouarnec S, Defaye P, Schlaepfer J, Rostock T, Lacroix D, Lamaison D, Lavergne T, Aizawa Y, Englund A, Anselme F, ONeill M, Hocini M, Lim KT, Knecht S, Veenhuyzen GD, Bordachar P, Chauvin M, Jais P, Coureau G, Chene G, Klein GJ, Clementy J. Sudden cardiac arrest associated with early repolarization. N Engl J Med 2008;358:2016–2023.
468. Rosso R, Kogan E, Belhassen B, Rozovski U, Scheinman MM, Zeltser D, Halkin A, Steinvil A, Heller K, Glikson M, Katz A, Viskin S. J-point elevation in survivors of primary ventricular fibrillation and matched control subjects: incidence and clinical significance. J Am Coll Cardiol 2008;52:1231–1238.
469. Paul T, Marchal C, Garson A Jr. Ventricular couplets in the young: prognosis related to underlying substrate. Am Heart J 1990;119:577–582.
470. Beaufort-Krol GC, Dijkstra SS, Bink-Boelkens MT. Natural history of ventricular premature contractions in children with a structurally normal heart: does origin matter? Europace 2008;10:998–1003.
471. Pfammatter JP, Paul T. Idiopathic ventricular tachycardia in infancy and childhood: a multicenter study on clinical profile and outcome. Working Group on Dysrhythmias and Electrophysiology of the Association for European Pediatric Cardiology. J Am Coll Cardiol 1999;33:2067–2072.
472. Wang S, Zhu W, Hamilton RM, Kirsh JA, Stephenson EA, Gross GJ. Diagnosisspecific characteristics of ventricular tachycardia in children with structurally normal hearts. Heart Rhythm 2010;7:1725–1731.
473. Collins KK, Schaffer MS, Liberman L, Saarel E, Knecht M, Tanel RE, Bradley D, Dubin AM, Paul T, Salerno J, Bar-Cohen Y, Sreeram N, Sanatani S, Law IH, Blaufox A, Batra A, Moltedo JM, van Hare GF, Reed J, Ro PS, Kugler J, Anderson C, Triedman JK. Fascicular and nonfascicular left ventricular tachycardias in the young: an international multicenter study. J Cardiovasc Electrophysiol 2013;24:640–648.
474. Schneider HE, Kriebel T, Jung K, Gravenhorst VD, Paul T. Catheter ablation of idiopathic left and right ventricular tachycardias in the pediatric population using noncontact mapping. Heart Rhythm 2010;7:731–739.
475. Blaufox AD, Felix GL, Saul JP. Radiofrequency catheter ablation in infants ≤18 months old: when is it done and how do they fare?: short-term data from the pediatric ablation registry. Circulation 2001;104:2803–2808.
476. Lapage MJ, Bradley DJ, Dick M 2nd. Verapamil in infants: an exaggerated fear? Pediatr Cardiol 2013;34:1532–1534.
477. Nagashima M, Matsushima M, Ogawa A, Ohsuga A, Kaneko T, Yazaki T, Okajima M. Cardiac arrhythmias in healthy children revealed by 24-hour ambulatory ECG monitoring. Pediatr Cardiol 1987;8:103–108.
478. Southall DP, Richards J, Mitchell P, Brown DJ, Johnston PG, Shinebourne EA. Study of cardiac rhythm in healthy newborn infants. Br Heart J 1980;43:14–20.
479. Jacobsen JR, Garson A Jr, Gillette PC, McNamara DG. Premature ventricular contractions in normal children. J Pediatr 1978;92:36–38. 480. Tsuji A, Nagashima M, Hasegawa S, Nagai N, Nishibata K, Goto M, Matsushima M. Long-term follow-up of idiopathic ventricular arrhythmias in otherwise normal children. Jpn Circ J 1995;59:654–662.
481. Van Hare GF, Stanger P. Ventricular tachycardia and accelerated ventricular rhythm presenting in the first month of life. Am J Cardiol 1991;67:42–45.
482. Iwamoto M, Niimura I, Shibata T, Yasui K, Takigiku K, Nishizawa T, Akaike T, Yokota S. Long-term course and clinical characteristics of ventricular tachycardia detected in children by school-based heart disease screening. Circ J 2005;69: 273–276.
483. Roggen A, Pavlovic M, Pfammatter JP. Frequency of spontaneous ventricular tachycardia in a pediatric population. Am J Cardiol 2008;101:852–854.
484. Garson A Jr, Smith RT Jr, Moak JP, Kearney DL, Hawkins EP, Titus JL, Cooley DA, Ott DA. Incessant ventricular tachycardia in infants: myocardial hamartomas and surgical cure. J Am Coll Cardiol 1987;10:619–626.
485. Paul T, Bokenkamp R, Mahnert B, Trappe HJ. Coronary artery involvement early and late after radiofrequency current application in young pigs. Am Heart J 1997; 133:436–440.
486. Khairy P, Guerra PG, Rivard L, Tanguay JF, Landry E, Guertin MC, Macle L, Thibault B, Tardif JC, Talajic M, Roy D, Dubuc M. Enlargement of catheter ablation lesions in infant hearts with cryothermal versus radiofrequency energy: an animal study. Circ Arrhythm Electrophysiol 2011;4:211–217.
487. Saul JP, Hulse JE, Papagiannis J, Van Praagh R, Walsh EP. Late enlargement of radiofrequency lesions in infant lambs. Implications for ablation procedures in small children. Circulation 1994;90:492–499.
488. Khairy P, Harris L, Landzberg MJ, Viswanathan S, Barlow A, Gatzoulis MA, Fernandes SM, Beauchesne L, Therrien J, Chetaille P, Gordon E, Vonder Muhll I, Cecchin F. Implantable cardioverter-defibrillators in tetralogy of Fallot. Circulation 2008;117:363–370.
489. Khairy P, Harris L, Landzberg MJ, Fernandes SM, Barlow A, Mercier LA, Viswanathan S, Chetaille P, Gordon E, Dore A, Cecchin F. Sudden death and defi- brillators in transposition of the great arteries with intra-atrial baffles: a multicenter study. Circ Arrhythm Electrophysiol 2008;1:250–257.
490. Berul CI, Van Hare GF, Kertesz NJ, Dubin AM, Cecchin F, Collins KK, Cannon BC, Alexander ME, Triedman JK, Walsh EP, Friedman RA. Results of a multicenter retrospective implantable cardioverter-defibrillator registry of pediatric and congenital heart disease patients. J Am Coll Cardiol 2008;51:1685–1691.
491. Koyak Z, de Groot JR, Van Gelder IC, Bouma BJ, van Dessel PF, Budts W, van Erven L, van Dijk AP, Wilde AA, Pieper PG, Sieswerda GT, Mulder BJ. Implantable cardioverter defibrillator therapy in adults with congenital heart disease: who is at risk of shocks? Circ Arrhythm Electrophysiol 2012;5:101–110.
492. Zeppenfeld K, Schalij MJ, Bartelings MM, Tedrow UB, Koplan BA, Soejima K, Stevenson WG. Catheter ablation of ventricular tachycardia after repair of congenital heart disease: electroanatomic identification of the critical right ventricular isthmus. Circulation 2007;116:2241–2252.
493. Gallego P, Gonzalez AE, Sanchez-Recalde A, Peinado R, Polo L, Gomez-Rubin C, Lopez-Sendon JL, Oliver JM. Incidence and predictors of sudden cardiac arrest in adults with congenital heart defects repaired before adult life. Am J Cardiol 2012; 110:109–117.
494. Ghai A, Silversides C, Harris L, Webb GD, Siu SC, Therrien J. Left ventricular dysfunction is a risk factor for sudden cardiac death in adults late after repair of tetralogy of Fallot. J Am Coll Cardiol 2002;40:1675–1680.
495. Gatzoulis MA, Balaji S, Webber SA, Siu SC, Hokanson JS, Poile C, Rosenthal M, Nakazawa M, Moller JH, Gillette PC, Webb GD, Redington AN. Risk factors for arrhythmia and sudden cardiac death late after repair of tetralogy of Fallot: a multicentre study. Lancet 2000;356:975–981.
496. Khairy P, Landzberg MJ, Gatzoulis MA, Lucron H, Lambert J, Marcon F, Alexander ME, Walsh EP. Value of programmed ventricular stimulation after tetralogy of fallot repair: a multicenter study. Circulation 2004;109:1994–2000.
497. Koyak Z, Harris L, de Groot JR, Silversides CK, Oechslin EN, Bouma BJ, Budts W, Zwinderman AH, Van Gelder IC, Mulder BJ. Sudden cardiac death in adult congenital heart disease. Circulation 2012;126:1944–1954.
498. Kammeraad JA, van Deurzen CH, Sreeram N, Bink-Boelkens MT, Ottenkamp J, Helbing WA, Lam J, Sobotka-Plojhar MA, Daniels O, Balaji S. Predictors of sudden cardiac death after Mustard or Senning repair for transposition of the great arteries. J Am Coll Cardiol 2004;44:1095–1102.
499. van der Linde D, Konings EE, Slager MA, Witsenburg M, Helbing WA, Takkenberg JJ, Roos-Hesselink JW. Birth prevalence of congenital heart disease worldwide: a systematic review and meta-analysis. J Am Coll Cardiol 2011;58: 2241–2247.
500. Marelli AJ, Mackie AS, Ionescu-Ittu R, Rahme E, Pilote L. Congenital heart disease in the general population: changing prevalence and age distribution. Circulation 2007;115:163–172.
501. Silka MJ, Hardy BG, Menashe VD, Morris CD. A population-based prospective evaluation of risk of sudden cardiac death after operation for common congenital heart defects. J Am Coll Cardiol 1998;32:245–251.
502. Oechslin EN, Harrison DA, Connelly MS, Webb GD, Siu SC. Mode of death in adults with congenital heart disease. Am J Cardiol 2000;86:1111–1116. 503. Nieminen HP, Jokinen EV, Sairanen HI. Causes of late deaths after pediatric cardiac surgery: a population-based study. J Am Coll Cardiol 2007;50:1263–1271.
504. Murphy JG, Gersh BJ, Mair DD, Fuster V, McGoon MD, Ilstrup DM, McGoon DC, Kirklin JW, Danielson GK. Long-term outcome in patients undergoing surgical repair of tetralogy of Fallot. N Engl J Med 1993;329:593–599.
505. Moons P, Gewillig M, Sluysmans T, Verhaaren H, Viart P, Massin M, Suys B, Budts W, Pasquet A, De Wolf D, Vliers A. Long term outcome up to 30 years after the Mustard or Senning operation: a nationwide multicentre study in Belgium. Heart 2004;90:307–313.
506. Brown DW, Dipilato AE, Chong EC, Gauvreau K, McElhinney DB, Colan SD, Lock JE. Sudden unexpected death after balloon valvuloplasty for congenital aortic stenosis. J Am Coll Cardiol 2010;56:1939–1946.
507. Khairy P, Fernandes SM, Mayer JE Jr, Triedman JK, Walsh EP, Lock JE, Landzberg MJ. Long-term survival, modes of death, and predictors of mortality in patients with Fontan surgery. Circulation 2008;117:85–92.
508. Heersche JH, Blom NA, van de Heuvel F, Blank C, Reimer AG, Clur SA, Witsenburg M, ten Harkel AD. Implantable cardioverter defibrillator therapy for prevention of sudden cardiac death in children in the Netherlands. Pacing Clin Electrophysiol 2010;33:179–185.
509. Silka MJ, Kron J, Dunnigan A, Dick M 2nd. Sudden cardiac death and the use of implantable cardioverter-defibrillators in pediatric patients. The Pediatric Electrophysiology Society. Circulation 1993;87:800–807.
510. Etheridge SP, Sanatani S, Cohen MI, Albaro CA, Saarel EV, Bradley DJ. Long QT syndrome in children in the era of implantable defibrillators. J Am Coll Cardiol 2007; 50:1335–1340.
511. Maron BJ, Spirito P, Ackerman MJ, Casey SA, Semsarian C, Estes NA 3rd, Shannon KM, Ashley EA, Day SM, Pacileo G, Formisano F, Devoto E, Anastasakis A, Bos JM, Woo A, Autore C, Pass RH, Boriani G, Garberich RF, Almquist AK, Russell MW, Boni L, Berger S, Maron MS, Link MS. Prevention of sudden cardiac death with implantable cardioverter-defibrillators in children and adolescents with hypertrophic cardiomyopathy. J Am Coll Cardiol 2013;61: 1527–1535.
512. Radbill AE, Triedman JK, Berul CI, Fynn-Thompson F, Atallah J, Alexander ME, Walsh EP, Cecchin F. System survival of nontransvenous implantable cardioverter-defibrillators compared to transvenous implantable cardioverterdefibrillators in pediatric and congenital heart disease patients. Heart Rhythm 2010;7:193–198. 513. Burns KM, Evans F, Kaltman JR. Pediatric ICD utilization in the United States from 1997 to 2006. Heart Rhythm 2011;8:23–28.
514. Pahl E, Sleeper LA, Canter CE, Hsu DT, Lu M, Webber SA, Colan SD, Kantor PF, Everitt MD, Towbin JA, Jefferies JL, Kaufman BD, Wilkinson JD, Lipshultz SE, Pediatric Cardiomyopathy Registry I. Incidence of and risk factors for sudden cardiac death in children with dilated cardiomyopathy: a report from the Pediatric Cardiomyopathy Registry. J Am Coll Cardiol 2012;59:607–615.
515. Dimas VV, Denfield SW, Friedman RA, Cannon BC, Kim JJ, Smith EO, Clunie SK, Price JF, Towbin JA, Dreyer WJ, Kertesz NJ. Frequency of cardiac death in children with idiopathic dilated cardiomyopathy. Am J Cardiol 2009;104:1574–1577.
516. Hamilton RM, Dorian P, Gow RM, Williams WG. Five-year experience with implantable defibrillators in children. Am J Cardiol 1996;77:524–526.
517. Chatrath R, Porter CB, Ackerman MJ. Role of transvenous implantable cardioverter-defibrillators in preventing sudden cardiac death in children, adolescents, and young adults. Mayo Clin Proc 2002;77:226–231.
518. Lawrence D, Von Bergen N, Law IH, Bradley DJ, Dick M 2nd, Frias PA, Streiper MJ, Fischbach PS. Inappropriate ICD discharges in single-chamber versus dualchamber devices in the pediatric and young adult population. J Cardiovasc Electrophysiol 2009;20:287–290.
519. Celiker A, Olgun H, Karagoz T, Ozer S, Ozkutlu S, Alehan D. Midterm experience with implantable cardioverter-defibrillators in children and young adults. Europace 2010;12:1732–1738.
520. Shah MJ. Implantable cardioverter defibrillator-related complications in the pediatric population. Pacing Clin Electrophysiol 2009;32(Suppl 2):S71–S74.
521. Janson CM, Patel AR, Bonney WJ, Smoots K, Shah MJ. Implantable cardioverterdefibrillator lead failure in children and young adults: a matter of lead diameter or lead design? J Am Coll Cardiol 2014;63:133–140.
522. Atallah J, Erickson CC, Cecchin F, Dubin AM, Law IH, Cohen MI, Lapage MJ, Cannon BC, Chun TU, Freedenberg V, Gierdalski M, Berul CI, Pediatric and Congenital Electrophysiology Society (PACES). Multi-institutional study of implantable defibrillator lead performance in children and young adults: results of the Pediatric Lead Extractability and Survival Evaluation (PLEASE) study. Circulation 2013;127:2393–2402.
523. Janousek J, Gebauer RA, Abdul-Khaliq H, Turner M, Kornyei L, Grollmuss O, Rosenthal E, Villain E, Fruh A, Paul T, Blom NA, Happonen JM, Bauersfeld U, Jacobsen JR, van den Heuvel F, Delhaas T, Papagiannis J, Trigo C, Working Group for Cardiac Dysrhythmias and Electrophysiology of the Association for European Paediatric Cardiology. Cardiac resynchronisation therapy in paediatric and congenital heart disease: differential effects in various anatomical and functional substrates. Heart 2009;95:1165–1171.
524. van der Hulst AE, Delgado V, Blom NA, van de Veire NR, Schalij MJ, Bax JJ, Roest AA, Holman ER. Cardiac resynchronization therapy in paediatric and congenital heart disease patients. Eur Heart J 2011;32:2236–2246.
525. Morady F, Kadish AH, DiCarlo L, Kou WH, Winston S, deBuitlier M, Calkins H, Rosenheck S, Sousa J. Long-term results of catheter ablation of idiopathic right ventricular tachycardia. Circulation 1990;82:2093–2099.
526. Yamashina Y, Yagi T, Namekawa A, Ishida A, Sato H, Nakagawa T, Sakuramoto M, Sato E, Yambe T. Distribution of successful ablation sites of idiopathic right ventricular outflow tract tachycardia. Pacing Clin Electrophysiol 2009;32:727–733.
527. Ventura R, Steven D, Klemm HU, Lutomsky B, Mullerleile K, Rostock T, Servatius H, Risius T, Meinertz T, Kuck KH, Willems S. Decennial follow-up in patients with recurrent tachycardia originating from the right ventricular outflow tract: electrophysiologic characteristics and response to treatment. Eur Heart J 2007;28:2338–2345.
528. Krittayaphong R, Sriratanasathavorn C, Dumavibhat C, Pumprueg S, Boonyapisit W, Pooranawattanakul S, Phrudprisan S, Kangkagate C. Electrocardiographic predictors of long-term outcomes after radiofrequency ablation in patients with right-ventricular outflow tract tachycardia. Europace 2006;8:601–606.
529. Steven D, Roberts-Thomson KC, Seiler J, Inada K, Tedrow UB, Mitchell RN, Sobieszczyk PS, Eisenhauer AC, Couper GS, Stevenson WG. Ventricular tachycardia arising from the aortomitral continuity in structural heart disease: characteristics and therapeutic considerations for an anatomically challenging area of origin. Circ Arrhythm Electrophysiol 2009;2:660–666.
530. Hachiya H, Hirao K, Sasaki T, Higuchi K, Hayashi T, Tanaka Y, Kawabata M, Isobe M. Novel ECG predictor of difficult cases of outflow tract ventricular tachycardia: peak deflection index on an inferior lead. Circ J 2010;74:256–261.
531. Sacher F, Roberts-Thomson K, Maury P, Tedrow U, Nault I, Steven D, Hocini M, Koplan B, Leroux L, Derval N, Seiler J, Wright MJ, Epstein L, Haissaguerre M, Jais P, Stevenson WG. Epicardial ventricular tachycardia ablation a multicenter safety study. J Am Coll Cardiol 2010;55:2366–2372.
532. Ouyang F, Mathew S, Wu S, Kamioka M, Metzner A, Xue Y, Ju W, Yang B, Zhan X, Rillig A, Lin T, Rausch P, Deiss S, Lemes C, Tonnis T, Wissner E, Tilz RR, Kuck KH, Chen M. Ventricular arrhythmias arising from the left ventricular outflow tract below the aortic sinus cusps: mapping and catheter ablation via transseptal approach and electrocardiographic characteristics. Circ Arrhythm Electrophysiol 2014;7: 445–455.
533. Kamakura S, Shimizu W, Matsuo K, Taguchi A, Suyama K, Kurita T, Aihara N, Ohe T, Shimomura K. Localization of optimal ablation site of idiopathic ventricular tachycardia from right and left ventricular outflow tract by body surface ECG. Circulation 1998;98:1525–1533.
534. Callans DJ, Menz V, Schwartzman D, Gottlieb CD, Marchlinski FE. Repetitive monomorphic tachycardia from the left ventricular outflow tract: electrocardiographic patterns consistent with a left ventricular site of origin. J Am Coll Cardiol 1997;29:1023–1027.
535. Tada H, Hiratsuji T, Naito S, Kurosaki K, Ueda M, Ito S, Shinbo G, Hoshizaki H, Oshima S, Nogami A, Taniguchi K. Prevalence and characteristics of idiopathic outflow tract tachycardia with QRS alteration following catheter ablation requiring additional radiofrequency ablation at a different point in the outflow tract. Pacing Clin Electrophysiol 2004;27:1240–1249.
536. Yamada T, McElderry HT, Doppalapudi H, Murakami Y, Yoshida Y, Yoshida N, Okada T, Tsuboi N, Inden Y, Murohara T, Epstein AE, Plumb VJ, Singh SP, Kay GN. Idiopathic ventricular arrhythmias originating from the aortic root prevalence, electrocardiographic and electrophysiologic characteristics, and results of radiofrequency catheter ablation. J Am Coll Cardiol 2008;52:139–147.
537. Kanagaratnam L, Tomassoni G, Schweikert R, Pavia S, Bash D, Beheiry S, Neibauer M, Saliba W, Chung M, Tchou P, Natale A. Ventricular tachycardias arising from the aortic sinus of valsalva: an under-recognized variant of left outflow tract ventricular tachycardia. J Am Coll Cardiol 2001;37:1408–1414.
538. Ouyang F, Fotuhi P, Ho SY, Hebe J, Volkmer M, Goya M, Burns M, Antz M, Ernst S, Cappato R, Kuck KH. Repetitive monomorphic ventricular tachycardia originating from the aortic sinus cusp: electrocardiographic characterization for guiding catheter ablation. J Am Coll Cardiol 2002;39:500–508.
539. Tada H, Nogami A, Naito S, Fukazawa H, Horie Y, Kubota S, Okamoto Y, Hoshizaki H, Oshima S, Taniguchi K. Left ventricular epicardial outflow tract tachycardia: a new distinct subgroup of outflow tract tachycardia. Jpn Circ J 2001;65:723–730.
540. Yamada T, Litovsky SH, Kay GN. The left ventricular ostium: an anatomic concept relevant to idiopathic ventricular arrhythmias. Circ Arrhythm Electrophysiol 2008;1: 396–404.
541. Yamada T, McElderry HT, Doppalapudi H, Okada T, Murakami Y, Yoshida Y, Yoshida N, Inden Y, Murohara T, Plumb VJ, Kay GN. Idiopathic ventricular arrhythmias originating from the left ventricular summit: anatomic concepts relevant to ablation. Circ Arrhythm Electrophysiol 2010;3:616–623.
542. Ouyang F, Bansch D, Schaumann A, Ernst S, Linder C, Falk P, Hachiya H, Kuck KH, Antz M. Catheter ablation of subepicardial ventricular tachycardia using electroanatomic mapping. Herz 2003;28:591–597.
543. Kumagai K, Yamauchi Y, Takahashi A, Yokoyama Y, Sekiguchi Y, Watanabe J, Iesaka Y, Shirato K, Aonuma K. Idiopathic left ventricular tachycardia originating from the mitral annulus. J Cardiovasc Electrophysiol 2005;16:1029–1036.
544. Tada H, Tadokoro K, Miyaji K, Ito S, Kurosaki K, Kaseno K, Naito S, Nogami A, Oshima S, Taniguchi K. Idiopathic ventricular arrhythmias arising from the pulmonary artery: prevalence, characteristics, and topography of the arrhythmia origin. Heart Rhythm 2008;5:419–426.
545. Sekiguchi Y, Aonuma K, Takahashi A, Yamauchi Y, Hachiya H, Yokoyama Y, Iesaka Y, Isobe M. Electrocardiographic and electrophysiologic characteristics of ventricular tachycardia originating within the pulmonary artery. J Am Coll Cardiol 2005;45:887–895.
546. Timmermans C, Rodriguez LM, Crijns HJ, Moorman AF, Wellens HJ. Idiopathic left bundle-branch block-shaped ventricular tachycardia may originate above the pulmonary valve. Circulation 2003;108:1960–1967.
547. Krittayaphong R, Saiviroonporn P, Boonyasirinant T, Nakyen S, Thanapiboonpol P, Watanaprakarnchai W, Ruksakul K, Kangkagate C. Magnetic resonance imaging abnormalities in right ventricular outflow tract tachycardia and the prediction of radiofrequency ablation outcome. Pacing Clin Electrophysiol 2006;29:837–845.
548. Proclemer A, Basadonna PT, Slavich GA, Miani D, Fresco C, Fioretti PM. Cardiac magnetic resonance imaging findings in patients with right ventricular outflow tract premature contractions. Eur Heart J 1997;18:2002–2010.
549. Lerman BB, Belardinelli L, West GA, Berne RM, DiMarco JP. Adenosine-sensitive ventricular tachycardia: evidence suggesting cyclic AMP-mediated triggered activity. Circulation 1986;74:270–280.
550. Lerman BB. Response of nonreentrant catecholamine-mediated ventricular tachycardia to endogenous adenosine and acetylcholine. Evidence for myocardial receptor-mediated effects. Circulation 1993;87:382–390.
551. Sung RJ, Keung EC, Nguyen NX, Huycke EC. Effects of beta-adrenergic blockade on verapamil-responsive and verapamil-irresponsive sustained ventricular tachycardias. J Clin Invest 1988;81:688–699.
552. Wilber DJ, Baerman J, Olshansky B, Kall J, Kopp D. Adenosine-sensitive ventricular tachycardia. Clinical characteristics and response to catheter ablation. Circulation 1993;87:126–134.
553. Marchlinski FE, Deely MP, Zado ES. Sex-specific triggers for right ventricular out- flow tract tachycardia. Am Heart J 2000;139:1009–1013.
554. ODonnell D, Cox D, Bourke J, Mitchell L, Furniss S. Clinical and electrophysiological differences between patients with arrhythmogenic right ventricular dysplasia and right ventricular outflow tract tachycardia. Eur Heart J 2003;24:801–810.
555. Khasnis A, Jongnarangsin K, Abela G, Veerareddy S, Reddy V, Thakur R. Tachycardia-induced cardiomyopathy: a review of literature. Pacing Clin Electrophysiol 2005;28:710–721.
556. Ho YS. Overview of cardiac anatomy relevant to catheter ablation. In: Wilber D, Packer D, Stevenson W, eds. Catheter Ablation of Cardiac Arrhythmias, 3rd edn. Cambridge, MA: Blackwell Scientific; 2008:3–17.
557. McAlpine WA. Heart and Coronary Arteries. New York: Springer-Verlag; 1975.
558. Ito S, Tada H, Naito S, Kurosaki K, Ueda M, Hoshizaki H, Miyamori I, Oshima S, Taniguchi K, Nogami A. Development and validation of an ECG algorithm for identifying the optimal ablation site for idiopathic ventricular outflow tract tachycardia. J Cardiovasc Electrophysiol 2003;14:1280–1286.
559. Pons M, Beck L, Leclercq F, Ferriere M, Albat B, Davy JM. Chronic left main coronary artery occlusion: a complication of radiofrequency ablation of idiopathic left ventricular tachycardia. Pacing Clin Electrophysiol 1997;20:1874–1876.
560. Koruth JS, Aryana A, Dukkipati SR, Pak HN, Kim YH, Sosa EA, Scanavacca M, Mahapatra S, Ailawadi G, Reddy VY, dAvila A. Unusual complications of percutaneous epicardial access and epicardial mapping and ablation of cardiac arrhythmias. Circ Arrhythm Electrophysiol 2011;4:882–888.
561. Roberts-Thomson KC, Steven D, Seiler J, Inada K, Koplan BA, Tedrow UB, Epstein LM, Stevenson WG. Coronary artery injury due to catheter ablation in adults: presentations and outcomes. Circulation 2009;120:1465–1473.
562. Makimoto H, Zhang Q, Tilz RR, Wissner E, Cuneo A, Kuck KH, Ouyang F. Aborted sudden cardiac death due to radiofrequency ablation within the coronary sinus and subsequent total occlusion of the circumflex artery. J Cardiovasc Electrophysiol 2013;24:929–932.
563. Klein LS, Shih HT, Hackett FK, Zipes DP, Miles WM. Radiofrequency catheter ablation of ventricular tachycardia in patients without structural heart disease. Circulation 1992;85:1666–1674.
564. Lin D, Hsia HH, Gerstenfeld EP, Dixit S, Callans DJ, Nayak H, Russo A, Marchlinski FE. Idiopathic fascicular left ventricular tachycardia: linear ablation lesion strategy for noninducible or nonsustained tachycardia. Heart Rhythm 2005;2: 934–939.
565. Crijns HJ, Smeets JL, Rodriguez LM, Meijer A, Wellens HJ. Cure of interfascicular reentrant ventricular tachycardia by ablation of the anterior fascicle of the left bundle branch. J Cardiovasc Electrophysiol 1995;6:486–492.
566. Ohe T, Shimomura K, Aihara N, Kamakura S, Matsuhisa M, Sato I, Nakagawa H, Shimizu A. Idiopathic sustained left ventricular tachycardia: clinical and electrophysiologic characteristics. Circulation 1988;77:560–568.
567. Ouyang F, Cappato R, Ernst S, Goya M, Volkmer M, Hebe J, Antz M, Vogtmann T, Schaumann A, Fotuhi P, Hoffmann-Riem M, Kuck KH. Electroanatomic substrate of idiopathic left ventricular tachycardia: unidirectional block and macroreentry within the Purkinje network. Circulation 2002;105:462–469.
568. Nogami A, Naito S, Tada H, Taniguchi K, Okamoto Y, Nishimura S, Yamauchi Y, Aonuma K, Goya M, Iesaka Y, Hiroe M. Demonstration of diastolic and presystolic Purkinje potentials as critical potentials in a macroreentry circuit of verapamilsensitive idiopathic left ventricular tachycardia. J Am Coll Cardiol 2000;36:811–823.
569. Ma FS, Ma J, Tang K, Han H, Jia YH, Fang PH, Chu JM, Pu JL, Zhang S. Left posterior fascicular block: a new endpoint of ablation for verapamil-sensitive idiopathic ventricular tachycardia. Chin Med J (Engl) 2006;119:367–372.
570. Kottkamp H, Chen X, Hindricks G, Willems S, Haverkamp W, Wichter T, Breithardt G, Borggrefe M. Idiopathic left ventricular tachycardia: new insights into electrophysiological characteristics and radiofrequency catheter ablation. Pacing Clin Electrophysiol 1995;18:1285–1297.
571. Nogami A, Naito S, Tada H, Oshima S, Taniguchi K, Aonuma K, Iesaka Y. Verapamil-sensitive left anterior fascicular ventricular tachycardia: results of radiofrequency ablation in six patients. J Cardiovasc Electrophysiol 1998;9: 1269–1278.
572. Reithmann C, Hahnefeld A, Ulbrich M, Matis T, Steinbeck G. Different forms of ventricular tachycardia involving the left anterior fascicle in nonischemic cardiomyopathy: critical sites of the reentrant circuit in low-voltage areas. J Cardiovasc Electrophysiol 2009;20:841–849.
573. Bogun F, El-Atassi R, Daoud E, Man KC, Strickberger SA, Morady F. Radiofrequency ablation of idiopathic left anterior fascicular tachycardia. J Cardiovasc Electrophysiol 1995;6:1113–1116.
574. Mizusawa Y, Sakurada H, Nishizaki M, Ueda-Tatsumoto A, Fukamizu S, Hiraoka M. Characteristics of bundle branch reentrant ventricular tachycardia with a right bundle branch block configuration: feasibility of atrial pacing. Europace 2009;11: 1208–1213.
575. Nogami A. Purkinje-related arrhythmias part I: monomorphic ventricular tachycardias. Pacing Clin Electrophysiol 2011;34:624–650.
576. Doppalapudi H, Yamada T, McElderry HT, Plumb VJ, Epstein AE, Kay GN. Ventricular tachycardia originating from the posterior papillary muscle in the left ventricle: a distinct clinical syndrome. Circ Arrhythm Electrophysiol 2008;1:23–29.
577. Crawford T, Mueller G, Good E, Jongnarangsin K, Chugh A, Pelosi F Jr, Ebinger M, Oral H, Morady F, Bogun F. Ventricular arrhythmias originating from papillary muscles in the right ventricle. Heart Rhythm 2010;7:725–730.
578. Bogun F, Desjardins B, Crawford T, Good E, Jongnarangsin K, Oral H, Chugh A, Pelosi F, Morady F. Post-infarction ventricular arrhythmias originating in papillary muscles. J Am Coll Cardiol 2008;51:1794–1802.
579. Yeh SJ, Wen MS, Wang CC, Lin FC, Wu D. Adenosine-sensitive ventricular tachycardia from the anterobasal left ventricle. J Am Coll Cardiol 1997;30:1339–1345.
580. Kondo K, Watanabe I, Kojima T, Nakai T, Yanagawa S, Sugimura H, Shindo A, Oshikawa N, Masaki R, Saito S, Ozawa Y, Kanmatsuse K. Radiofrequency catheter ablation of ventricular tachycardia from the anterobasal left ventricle. Jpn Heart J 2000;41:215–225.
581. Tada H, Ito S, Naito S, Kurosaki K, Kubota S, Sugiyasu A, Tsuchiya T, Miyaji K, Yamada M, Kutsumi Y, Oshima S, Nogami A, Taniguchi K. Idiopathic ventricular arrhythmia arising from the mitral annulus: a distinct subgroup of idiopathic ventricular arrhythmias. J Am Coll Cardiol 2005;45:877–886.
582. Prystowsky EN, Padanilam BJ, Joshi S, Fogel RI. Ventricular arrhythmias in the absence of structural heart disease. J Am Coll Cardiol 2012;59:1733–1744.
583. Meissner MD, Lehmann MH, Steinman RT, Mosteller RD, Akhtar M, Calkins H, Cannom DS, Epstein AE, Fogoros RN, Liem LB, Marchlinski FE, Myerburg RJ, Veltri EP. Ventricular fibrillation in patients without significant structural heart disease: a multicenter experience with implantable cardioverter-defibrillator therapy. J Am Coll Cardiol 1993;21:1406–1412.
584. Haissaguerre M, Shah DC, Jais P, Shoda M, Kautzner J, Arentz T, Kalushe D, Kadish A, Griffith M, Gaita F, Yamane T, Garrigue S, Hocini M, Clementy J. Role of Purkinje conducting system in triggering of idiopathic ventricular fibrillation. Lancet 2002;359:677–678.
585. Bogun F, Good E, Reich S, Elmouchi D, Igic P, Tschopp D, Dey S, Wimmer A, Jongnarangsin K, Oral H, Chugh A, Pelosi F, Morady F. Role of Purkinje fibers in post-infarction ventricular tachycardia. J Am Coll Cardiol 2006;48:2500–2507.
586. Knecht S, Sacher F, Wright M, Hocini M, Nogami A, Arentz T, Petit B, Franck R, De Chillou C, Lamaison D, Farre J, Lavergne T, Verbeet T, Nault I, Matsuo S, Leroux L, Weerasooriya R, Cauchemez B, Lellouche N, Derval N, Narayan SM, Jais P, Clementy J, Haissaguerre M. Long-term follow-up of idiopathic ventricular fibrillation ablation: a multicenter study. J Am Coll Cardiol 2009;54:522–528.
587. Nogami A, Sugiyasu A, Kubota S, Kato K. Mapping and ablation of idiopathic ventricular fibrillation from the Purkinje system. Heart Rhythm 2005;2:646–649.
588. Haissaguerre M, Shoda M, Jais P, Nogami A, Shah DC, Kautzner J, Arentz T, Kalushe D, Lamaison D, Griffith M, Cruz F, de Paola A, Gaita F, Hocini M, Garrigue S, Macle L, Weerasooriya R, Clementy J. Mapping and ablation of idiopathic ventricular fibrillation. Circulation 2002;106:962–967.
589. Wever EF, Robles de Medina EO. Sudden death in patients without structural heart disease. J Am Coll Cardiol 2004;43:1137–1144.
590. Leenhardt A, Glaser E, Burguera M, Nurnberg M, Maison-Blanche P, Coumel P. Short-coupled variant of torsade de pointes. A new electrocardiographic entity in the spectrum of idiopathic ventricular tachyarrhythmias. Circulation 1994;89: 206–215.
591. Eisenberg SJ, Scheinman MM, Dullet NK, Finkbeiner WE, Griffin JC, Eldar M, Franz MR, Gonzalez R, Kadish AH, Lesh MD. Sudden cardiac death and polymorphous ventricular tachycardia in patients with normal QT intervals and normal systolic cardiac function. Am J Cardiol 1995;75:687–692.
592. Van den Branden B, Wever E, Boersma L. Torsade de pointes with short coupling interval. Acta Cardiol 2010;65:345–346.
593. Caforio AL, Pankuweit S, Arbustini E, Basso C, Gimeno-Blanes J, Felix SB, Fu M, Helio T, Heymans S, Jahns R, Klingel K, Linhart A, Maisch B, McKenna W, Mogensen J, Pinto YM, Ristic A, Schultheiss HP, Seggewiss H, Tavazzi L, Thiene G, Yilmaz A, Charron P, Elliott PM. Current state of knowledge on aetiology, diagnosis, management, and therapy of myocarditis: a position statement of the European Society of Cardiology Working Group on Myocardial and Pericardial Diseases. Eur Heart J 2013;34:2636–2648.
594. JCS Joint Working Group. Guidelines for diagnosis and treatment of myocarditis (JCS 2009): digest version. Circ J 2011;75:734–743.
595. Aoyama N, Izumi T, Hiramori K, Isobe M, Kawana M, Hiroe M, Hishida H, Kitaura Y, Imaizumi T. National survey of fulminant myocarditis in Japan: therapeutic guidelines and long-term prognosis of using percutaneous cardiopulmonary support for fulminant myocarditis (special report from a scientific committee). Circ J 2002;66:133–144.
596. Liberman L, Anderson B, Silver ES, Singh R, Richmond ME. Incidence and characteristics of arrhythmias in pediatric patients with myocarditis: a multicenter study. J Am Coll Cardiol 2014;63:A483.
597. Kindermann I, Kindermann M, Kandolf R, Klingel K, Bultmann B, Muller T, Lindinger A, Bohm M. Predictors of outcome in patients with suspected myocarditis. Circulation 2008;118:639–648.
598. Prochnau D, Surber R, Kuehnert H, Heinke M, Klein HU, Figulla HR. Successful use of a wearable cardioverter-defibrillator in myocarditis with normal ejection fraction. Clin Res Cardiol 2010;99:129–131.
599. Chung MK. The role of the wearable cardioverter defibrillator in clinical practice. Cardiol Clin 2014;32:253–270.
600. Kandolin R, Lehtonen J, Salmenkivi K, Raisanen-Sokolowski A, Lommi J, Kupari M. Diagnosis, treatment, and outcome of giant-cell myocarditis in the era of combined immunosuppression. Circ Heart Fail 2013;6:15–22.
601. Schumm J, Greulich S, Wagner A, Grun S, Ong P, Bentz K, Klingel K, Kandolf R, Bruder O, Schneider S, Sechtem U, Mahrholdt H. Cardiovascular magnetic resonance risk stratification in patients with clinically suspected myocarditis. J Cardiovasc Magn Reson 2014;16:14.
602. Rosenheck S, Weiss A, Sharon Z. Therapy success and survival in patients with valvular heart disease and implantable cardioverter defibrillator. Int J Cardiol 2010;144:103–104.
603. Yang F, Shah B, Iwai S, Markowitz SM, Lerman BB, Stein KM. ICD implantation and arrhythmia-free survival in patients with depressed LV function following surgery for valvular heart disease. Pacing Clin Electrophysiol 2008;31:1419–1424.
604. Valles AG, Khawaja FJ, Gersh BJ, Enriquez-Sarano M, Friedman PA, Park SJ, Hodge DO, Cha YM. Implantable cardioverter defibrillators in patients with valvular cardiomyopathy. J Cardiovasc Electrophysiol 2012;23:1326–1332.
605. Aranki SF, Santini F, Adams DH, Rizzo RJ, Couper GS, Kinchla NM, Gildea JS, Collins JJ Jr, Cohn LH. Aortic valve endocarditis. Determinants of early survival and late morbidity. Circulation 1994;90:II175–II182.
606. Johnson LL, Sciacca RR, Ellis K, Weiss MB, Cannon PJ. Reduced left ventricular myocardial blood flow per unit mass in aortic stenosis. Circulation 1978;57: 582–590.
607. Martinez-Rubio A, Schwammenthal Y, Schwammenthal E, Block M, Reinhardt L, Garcia-Alberola A, Sierra G, Shenasa M, Haverkamp W, Scheld HH, Breithardt G, Borggrefe M. Patients with valvular heart disease presenting with sustained ventricular tachyarrhythmias or syncope: results of programmed ventricular stimulation and long-term follow-up. Circulation 1997;96:500–508.
608. Narasimhan C, Jazayeri MR, Sra J, Dhala A, Deshpande S, Biehl M, Akhtar M, Blanck Z. Ventricular tachycardia in valvular heart disease: facilitation of sustained bundle-branch reentry by valve surgery. Circulation 1997;96:4307–4313.
609. Sagar S, Liu PP, Cooper LT Jr. Myocarditis. Lancet 2012;379:738–747.
610. Liu QN, Reddy S, Sayre JW, Pop V, Graves MC, Fiala M. Essential role of HIV type 1-infected and cyclooxygenase 2-activated macrophages and T cells in HIV type 1 myocarditis. AIDS Res Hum Retroviruses 2001;17:1423–1433.
611. Richardson P, McKenna W, Bristow M, Maisch B, Mautner B, OConnell J, Olsen E, Thiene G, Goodwin J, Gyarfas I, Martin I, Nordet P. Report of the 1995 World Health Organization/International Society and Federation of Cardiology Task Force on the Definition and Classification of Cardiomyopathies. Circulation 1996;93:841–842.
612. Ukena C, Mahfoud F, Kindermann I, Kandolf R, Kindermann M, Bohm M. Prognostic electrocardiographic parameters in patients with suspected myocarditis. Eur J Heart Fail 2011;13:398–405.
613. Kohno K, Aoyama N, Shimohama T, Yoshida M, Machida Y, Fukuda N, Aizaki T, Suzuki K, Kurosawa T, Izumi T. Resuscitation from fulminant myocarditis associated with refractory ventricular fibrillation. Jpn Circ J 2000;64:139–143.
614. McCarthy RE 3rd, Boehmer JP, Hruban RH, Hutchins GM, Kasper EK, Hare JM, Baughman KL. Long-term outcome of fulminant myocarditis as compared with acute (nonfulminant) myocarditis. N Engl J Med 2000;342:690–695.
615. Phillips M, Robinowitz M, Higgins JR, Boran KJ, Reed T, Virmani R. Sudden cardiac death in Air Force recruits. A 20-year review. JAMA 1986;256:2696–2699.
616. Basso C, Calabrese F, Corrado D, Thiene G. Myocarditis: an underestimated cause of sudden cardiac death. In: Aliot E, Clementy J, Prystowsky EN, eds. Fighting Sudden Cardiac Death: A Worldwide Challenge. Armonk, NY: Futura; 2000:447–458.
617. Basso C, Calabrese F, Corrado D, Thiene G. Postmortem diagnosis in sudden cardiac death victims: macroscopic, microscopic and molecular findings. Cardiovasc Res 2001;50:290–300.
618. Fabre A, Sheppard MN. Sudden adult death syndrome and other non-ischaemic causes of sudden cardiac death. Heart 2006;92:316–320.
619. Wesslen L, Pahlson C, Lindquist O, Hjelm E, Gnarpe J, Larsson E, Baandrup U, Eriksson L, Fohlman J, Engstrand L, Linglof T, Nystrom-Rosander C, Gnarpe H, Magnius L, Rolf C, Friman G. An increase in sudden unexpected cardiac deaths among young Swedish orienteers during 1979–1992. Eur Heart J 1996;17: 902–910.
620. DAmbrosio A, Patti G, Manzoli A, Sinagra G, Di Lenarda A, Silvestri F, Di Sciascio G. The fate of acute myocarditis between spontaneous improvement and evolution to dilated cardiomyopathy: a review. Heart 2001;85:499–504.
621. Kuhl U, Pauschinger M, Seeberg B, Lassner D, Noutsias M, Poller W, Schultheiss HP. Viral persistence in the myocardium is associated with progressive cardiac dysfunction. Circulation 2005;112:1965–1970.
622. Mazzone P, Tsiachris D, Della Bella P. Epicardial management of myocarditisrelated ventricular tachycardia. Eur Heart J 2013;34:244.
623. Wallace SM, Walton BI, Kharbanda RK, Hardy R, Wilson AP, Swanton RH. Mortality from infective endocarditis: clinical predictors of outcome. Heart 2002;88: 53–60.
624. Kumar S, Barbhaiya C, Nagashima K, Choi EK, Epstein LM, John RM, Maytin M, Albert CM, Miller AL, Koplan BA, Michaud GF, Tedrow UB, Stevenson WG. Ventricular tachycardia in cardiac sarcoidosis: characterization of ventricular substrate and outcomes of catheter ablation. Circ Arrhythm Electrophysiol 2015;8: 87–93.
625. Birnie DH, Sauer WH, Bogun F, Cooper JM, Culver DA, Duvernoy CS, Judson MA, Kron J, Mehta D, Cosedis Nielsen J, Patel AR, Ohe T, Raatikainen P, Soejima K. HRS expert consensus statement on the diagnosis and management of arrhythmias associated with cardiac sarcoidosis. Heart Rhythm 2014;11:1305–1323.
626. von Olshausen K, Schwarz F, Apfelbach J, Rohrig N, Kramer B, Kubler W. Determinants of the incidence and severity of ventricular arrhythmias in aortic valve disease. Am J Cardiol 1983;51:1103–1109.
627. Hochreiter C, Niles N, Devereux RB, Kligfield P, Borer JS. Mitral regurgitation: relationship of noninvasive descriptors of right and left ventricular performance to clinical and hemodynamic findings and to prognosis in medically and surgically treated patients. Circulation 1986;73:900–912.
628. Chizner MA, Pearle DL, deLeon AC Jr. The natural history of aortic stenosis in adults. Am Heart J 1980;99:419–424.
629. Sorgato A, Faggiano P, Aurigemma GP, Rusconi C, Gaasch WH. Ventricular arrhythmias in adult aortic stenosis: prevalence, mechanisms, and clinical relevance. Chest 1998;113:482–491.
630. Delahaye JP, Gare JP, Viguier E, Delahaye F, De Gevigney G, Milon H. Natural history of severe mitral regurgitation. Eur Heart J 1991;12(Suppl B):5–9.
631. Grigioni F, Enriquez-Sarano M, Ling LH, Bailey KR, Seward JB, Tajik AJ, Frye RL. Sudden death in mitral regurgitation due to flail leaflet. J Am Coll Cardiol 1999; 34:2078–2085.
632. Olafiranye O, Hochreiter CA, Borer JS, Supino PG, Herrold EM, Budzikowski AS, Hai OY, Bouraad D, Kligfield PD, Girardi LN, Krieger KH, Isom OW. Nonischemic mitral regurgitation: prognostic value of nonsustained ventricular tachycardia after mitral valve surgery. Cardiology 2013;124:108–115.
633. Groves P. Valve disease: Surgery of valve disease: late results and late complications. Heart 2001;86:715–721.
634. Blackstone EH, Kirklin JW. Death and other time-related events after valve replacement. Circulation 1985;72:753–767.
635. Hwang MH, Burchfiel CM, Sethi GK, Oprian C, Grover FL, Henderson WG, Hammermeister K. Comparison of the causes of late death following aortic and mitral valve replacement. VA Co-operative Study on Valvular Heart Disease. J Heart Valve Dis 1994;3:17–24.
636. Burke AP, Farb A, Sessums L, Virmani R. Causes of sudden cardiac death in patients with replacement valves: an autopsy study. J Heart Valve Dis 1994;3:10–16.
637. Food and Drug Administration. International Conference on Harmonisation; guidance on E14 Clinical Evaluation of QT/QTc Interval Prolongation and Proarrhythmic Potential for Non-Antiarrhythmic Drugs; availability. Notice. Fed Reg 2005;70:61134–61135.
638. Watanabe J, Suzuki Y, Fukui N, Ono S, Sugai T, Tsuneyama N, Someya T. Increased risk of antipsychotic-related QT prolongation during nighttime: a 24-hour Holter electrocardiogram recording study. J Clin Psychopharmacol 2012;32:18–22.
639. Wu CS, Tsai YT, Tsai HJ. Antipsychotic drugs and the risk of ventricular arrhythmia and/or sudden cardiac death: a nation-wide case-crossover study. J Am Heart Assoc 2015;4:e001568.
640. Sala M, Vicentini A, Brambilla P, Montomoli C, Jogia JR, Caverzasi E, Bonzano A, Piccinelli M, Barale F, De Ferrari GM. QT interval prolongation related to psychoactive drug treatment: a comparison of monotherapy versus polytherapy. Ann Gen Psychiatry 2005;4:1.
641. Fanoe S, Kristensen D, Fink-Jensen A, Jensen HK, Toft E, Nielsen J, Videbech P, Pehrson S, Bundgaard H. Risk of arrhythmia induced by psychotropic medications: a proposal for clinical management. Eur Heart J 2014;35:1306–1315.
642. Girardin FR, Gex-Fabry M, Berney P, Shah D, Gaspoz JM, Dayer P. Drug-induced long QT in adult psychiatric inpatients: the 5-year cross-sectional ECG Screening Outcome in Psychiatry study. Am J Psychiatry 2013;170:1468–1476.
643. Murray-Thomas T, Jones ME, Patel D, Brunner E, Shatapathy CC, Motsko S, Van Staa TP. Risk of mortality (including sudden cardiac death) and major cardiovascular events in atypical and typical antipsychotic users: a study with the general practice research database. Cardiovasc Psychiatry Neurol 2013;2013:247486.
644. Appleby L, Thomas S, Ferrier N, Lewis G, Shaw J, Amos T. Sudden unexplained death in psychiatric in-patients. Br J Psychiatry 2000;176:405–406.
645. Roden DM, Lazzara R, Rosen M, Schwartz PJ, Towbin J, Vincent GM. Multiple mechanisms in the long-QT syndrome. Current knowledge, gaps, and future directions. The SADS Foundation Task Force on LQTS. Circulation 1996;94: 1996–2012.
646. Ray WA, Meredith S, Thapa PB, Meador KG, Hall K, Murray KT. Antipsychotics and the risk of sudden cardiac death. Arch Gen Psychiatry 2001;58:1161–1167.
647. Ray WA, Chung CP, Murray KT, Hall K, Stein CM. Atypical antipsychotic drugs and the risk of sudden cardiac death. N Engl J Med 2009;360:225–235.
648. Haddad PM, Anderson IM. Antipsychotic-related QTc prolongation, torsade de pointes and sudden death. Drugs 2002;62:1649–1671.
649. Taylor DM. Antipsychotics and QT prolongation. Acta Psychiatr Scand 2003;107: 85–95.
650. Devinsky O. Sudden, unexpected death in epilepsy. N Engl J Med 2011;365: 1801–1811.
651. Annegers JF. United States perspective on definitions and classifications. Epilepsia 1997;38(Suppl):S9–S12.
652. Dasheiff RM. Sudden unexpected death in epilepsy: a series from an epilepsy surgery program and speculation on the relationship to sudden cardiac death. J Clin Neurophysiol 1991;8:216–222.
653. Donner EJ, Smith CR, Snead OC 3rd. Sudden unexplained death in children with epilepsy. Neurology 2001;57:430–434.
654. Ficker DM, So EL, Shen WK, Annegers JF, OBrien PC, Cascino GD, Belau PG. Population-based study of the incidence of sudden unexplained death in epilepsy. Neurology 1998;51:1270–1274.
655. Nashef L, Fish DR, Garner S, Sander JW, Shorvon SD. Sudden death in epilepsy: a study of incidence in a young cohort with epilepsy and learning difficulty. Epilepsia 1995;36:1187–1194.
656. Nilsson L, Ahlbom A, Farahmand BY, Tomson T. Mortality in a population-based cohort of epilepsy surgery patients. Epilepsia 2003;44:575–581.
657. Sperling MR, Feldman H, Kinman J, Liporace JD, OConnor MJ. Seizure control and mortality in epilepsy. Ann Neurol 1999;46:45–50.
658. Tomson T, Nashef L, Ryvlin P. Sudden unexpected death in epilepsy: current knowledge and future directions. Lancet Neurol 2008;7:1021–1031.
659. Tomson T, Walczak T, Sillanpaa M, Sander JW. Sudden unexpected death in epilepsy: a review of incidence and risk factors. Epilepsia 2005;46(Suppl 11):54–61.
660. Walczak TS, Leppik IE, DAmelio M, Rarick J, So E, Ahman P, Ruggles K, Cascino GD, Annegers JF, Hauser WA. Incidence and risk factors in sudden unexpected death in epilepsy: a prospective cohort study. Neurology 2001;56: 519–525.
661. Sandorfi G, Clemens B, Csanadi Z. Electrical storm in the brain and in the heart: epilepsy and Brugada syndrome. Mayo Clin Proc 2013;88:1167–1173.
662. Johnson JN, Hofman N, Haglund CM, Cascino GD, Wilde AA, Ackerman MJ. Identification of a possible pathogenic link between congenital long QT syndrome and epilepsy. Neurology 2009;72:224–231.
663. Rugg-Gunn FJ, Simister RJ, Squirrell M, Holdright DR, Duncan JS. Cardiac arrhythmias in focal epilepsy: a prospective long-term study. Lancet 2004;364: 2212–2219.
664. Ryvlin P, Nashef L, Lhatoo SD, Bateman LM, Bird J, Bleasel A, Boon P, Crespel A, Dworetzky BA, Hogenhaven H, Lerche H, Maillard L, Malter MP, Marchal C, Murthy JM, Nitsche M, Pataraia E, Rabben T, Rheims S, Sadzot B, Schulze-Bonhage A, Seyal M, So EL, Spitz M, Szucs A, Tan M, Tao JX, Tomson T. Incidence and mechanisms of cardiorespiratory arrests in epilepsy monitoring units (MORTEMUS): a retrospective study. Lancet Neurol 2013;12: 966–977.
665. Lund M, Diaz LJ, Ranthe MF, Petri H, Duno M, Juncker I, Eiberg H, Vissing J, Bundgaard H, Wohlfahrt J, Melbye M. Cardiac involvement in myotonic dystrophy: a nationwide cohort study. Eur Heart J 2014;35:2158–2164.
666. Groh WJ. Arrhythmias in the muscular dystrophies. Heart Rhythm 2012;9: 1890–1895.
667. Petri H, Vissing J, Witting N, Bundgaard H, Kober L. Cardiac manifestations of myotonic dystrophy type 1. Int J Cardiol 2012;160:82–88.
668. Lallemand B, Clementy N, Bernard-Brunet A, Pierre B, Corcia P, Fauchier L, Raynaud M, Pellieux S, Babuty D. The evolution of infrahissian conduction time in myotonic dystrophy patients: clinical implications. Heart 2012;98:291–296.
669. Groh WJ, Groh MR, Saha C, Kincaid JC, Simmons Z, Ciafaloni E, Pourmand R, Otten RF, Bhakta D, Nair GV, Marashdeh MM, Zipes DP, Pascuzzi RM. Electrocardiographic abnormalities and sudden death in myotonic dystrophy type 1. N Engl J Med 2008;358:2688–2697.
670. Roberts NK, Perloff JK, Kark RA. Cardiac conduction in the Kearns-Sayre syndrome (a neuromuscular disorder associated with progressive external ophthalmoplegia and pigmentary retinopathy). Report of 2 cases and review of 17 published cases. Am J Cardiol 1979;44:1396–1400.
671. Boriani G, Gallina M, Merlini L, Bonne G, Toniolo D, Amati S, Biffi M, Martignani C, Frabetti L, Bonvicini M, Rapezzi C, Branzi A. Clinical relevance of atrial fibrillation/ flutter, stroke, pacemaker implant, and heart failure in Emery-Dreifuss muscular dystrophy: a long-term longitudinal study. Stroke 2003;34:901–908.
672. Wahbi K, Meune C, Porcher R, Becane HM, Lazarus A, Laforet P, Stojkovic T, Behin A, Radvanyi-Hoffmann H, Eymard B, Duboc D. Electrophysiological study with prophylactic pacing and survival in adults with myotonic dystrophy and conduction system disease. JAMA 2012;307:1292–1301.
673. Laurent V, Pellieux S, Corcia P, Magro P, Pierre B, Fauchier L, Raynaud M, Babuty D. Mortality in myotonic dystrophy patients in the area of prophylactic pacing devices. Int J Cardiol 2011;150:54–58.
674. Meune C, Van Berlo JH, Anselme F, Bonne G, Pinto YM, Duboc D. Primary prevention of sudden death in patients with lamin A/C gene mutations. N Engl J Med 2006;354:209–210.
675. European Society of Gynecology (ESG), Association for European Paediatric Cardiology (AEPC), German Society for Gender Medicine (DGesGM), Regitz-Zagrosek V, Blomstrom Lundqvist C, Borghi C, Cifkova R, Ferreira R, Foidart JM, Gibbs JS, Gohlke-Baerwolf C, Gorenek B, Iung B, Kirby M, Maas AH, Morais J, Nihoyannopoulos P, Pieper PG, Presbitero P, Roos-Hesselink JW, Schaufelberger M, Seeland U, Torracca L, ESC Committee for Practice Guidelines. ESC Guidelines on the management of cardiovascular diseases during pregnancy: the Task Force on the Management of Cardiovascular Diseases during Pregnancy of the European Society of Cardiology (ESC). Eur Heart J 2011;32:3147–3197.
676. Rashba EJ, Zareba W, Moss AJ, Hall WJ, Robinson J, Locati EH, Schwartz PJ, Andrews M. Influence of pregnancy on the risk for cardiac events in patients with hereditary long QT syndrome. LQTS Investigators. Circulation 1998;97: 451–456.
677. Task Force on the Management of Cardiovascular Diseases During Pregnancy of the European Society of Cardiology. Expert consensus document on management of cardiovascular diseases during pregnancy. Eur Heart J 2003;24:761–781.
678. Dorian P, Cass D, Schwartz B, Cooper R, Gelaznikas R, Barr A. Amiodarone as compared with lidocaine for shock-resistant ventricular fibrillation. N Engl J Med 2002;346:884–890.
679. Siu SC, Sermer M, Colman JM, Alvarez AN, Mercier LA, Morton BC, Kells CM, Bergin ML, Kiess MC, Marcotte F, Taylor DA, Gordon EP, Spears JC, Tam JW, Amankwah KS, Smallhorn JF, Farine D, Sorensen S. Prospective multicenter study of pregnancy outcomes in women with heart disease. Circulation 2001;104: 515–521.
680. Drenthen W, Pieper PG, Roos-Hesselink JW, van Lottum WA, Voors AA, Mulder BJ, van Dijk AP, Vliegen HW, Yap SC, Moons P, Ebels T, van Veldhuisen DJ. Outcome of pregnancy in women with congenital heart disease: a literature review. J Am Coll Cardiol 2007;49:2303–2311.
681. Roos-Hesselink JW, Ruys TP, Stein JI, Thilen U, Webb GD, Niwa K, Kaemmerer H, Baumgartner H, Budts W, Maggioni AP, Tavazzi L, Taha N, Johnson MR, Hall R. Outcome of pregnancy in patients with structural or ischaemic heart disease: results of a registry of the European Society of Cardiology. Eur Heart J 2013;34: 657–665.
682. Wolbrette D, Naccarelli G, Curtis A, Lehmann M, Kadish A. Gender differences in arrhythmias. Clin Cardiol 2002;25:49–56.
683. Rodriguez-Manero M, Casado-Arroyo R, Sarkozy A, Leysen E, Sieira JA, Namdar M, Conte G, Levinstein M, Chierchia GB, de Asmundis C, Brugada P. The clinical significance of pregnancy in Brugada syndrome. Rev Esp Cardiol (Engl Ed) 2014;67:176–180.
684. Benito B, Berruezo A. Brugada syndrome and pregnancy: delving into the role of sex hormones in ion channelopathies. Rev Esp Cardiol (Engl Ed) 2014;67:165–167.
685. Shotan A, Ostrzega E, Mehra A, Johnson JV, Elkayam U. Incidence of arrhythmias in normal pregnancy and relation to palpitations, dizziness, and syncope. Am J Cardiol 1997;79:1061–1064.
686. Widerhorn J, Widerhorn AL, Rahimtoola SH, Elkayam U. WPW syndrome during pregnancy: increased incidence of supraventricular arrhythmias. Am Heart J 1992; 123:796–798.
687. Tawam M, Levine J, Mendelson M, Goldberger J, Dyer A, Kadish A. Effect of pregnancy on paroxysmal supraventricular tachycardia. Am J Cardiol 1993;72:838–840.
688. Lee SH, Chen SA, Wu TJ, Chiang CE, Cheng CC, Tai CT, Chiou CW, Ueng KC, Chang MS. Effects of pregnancy on first onset and symptoms of paroxysmal supraventricular tachycardia. Am J Cardiol 1995;76:675–678.
689. Brodsky M, Doria R, Allen B, Sato D, Thomas G, Sada M. New-onset ventricular tachycardia during pregnancy. Am Heart J 1992;123:933–941.
690. Silversides CK, Harris L, Haberer K, Sermer M, Colman JM, Siu SC. Recurrence rates of arrhythmias during pregnancy in women with previous tachyarrhythmia and impact on fetal and neonatal outcomes. Am J Cardiol 2006;97:1206–1212.
691. Sharif-Kazemi MB, Emkanjoo Z, Tavoosi A, Kafi M, Kheirkhah J, Alizadeh A, Sadr-Ameli MA. Electrical storm in Brugada syndrome during pregnancy. Pacing Clin Electrophysiol 2011;34:e18–e21.
692. Joglar JA, Page RL. Treatment of cardiac arrhythmias during pregnancy: safety considerations. Drug Saf 1999;20:85–94.
693. Cox JL, Gardner MJ. Treatment of cardiac arrhythmias during pregnancy. Prog Cardiovasc Dis 1993;36:137–178.
694. Tan HL, Lie KI. Treatment of tachyarrhythmias during pregnancy and lactation. Eur Heart J 2001;22:458–464.
695. Abello M, Peinado R, Merino JL, Gnoatto M, Mateos M, Silvestre J, Dominguez JL. Cardioverter defibrillator implantation in a pregnant woman guided with transesophageal echocardiography. Pacing Clin Electrophysiol 2003;26:1913–1914.
696. Natale A, Davidson T, Geiger MJ, Newby K. Implantable cardioverterdefibrillators and pregnancy: a safe combination? Circulation 1997;96:2808–2812.
697. Piper JM, Berkus M, Ridgway LE 3rd. Pregnancy complicated by chronic cardiomyopathy and an automatic implantable cardioverter defibrillator. Am J Obstet Gynecol 1992;167:506–507.
698. Sliwa K, Hilfiker-Kleiner D, Petrie MC, Mebazaa A, Pieske B, Buchmann E, Regitz-Zagrosek V, Schaufelberger M, Tavazzi L, van Veldhuisen DJ, Watkins H, Shah AJ, Seferovic PM, Elkayam U, Pankuweit S, Papp Z, Mouquet F, McMurray JJ. Current state of knowledge on aetiology, diagnosis, management, and therapy of peripartum cardiomyopathy: a position statement from the Heart Failure Association of the European Society of Cardiology Working Group on peripartum cardiomyopathy. Eur J Heart Fail 2010;12:767–778.
699. Cooper WO, Hernandez-Diaz S, Arbogast PG, Dudley JA, Dyer S, Gideon PS, Hall K, Ray WA. Major congenital malformations after first-trimester exposure to ACE inhibitors. N Engl J Med 2006;354:2443–2451.
700. Regitz-Zagrosek V, Blomstrom Lundqvist C, Borghi C, Cifkova R, Ferreira R, Foidart JM, Gibbs JS, Gohlke-Baerwolf C, Gorenek B, Iung B, Kirby M, Maas AH, Morais J, Nihoyannopoulos P, Pieper PG, Presbitero P, Roos-Hesselink JW, Schaufelberger M, Seeland U, Torracca L. ESC Guidelines on the management of cardiovascular diseases during pregnancy: the Task Force on the Management of Cardiovascular Diseases during Pregnancy of the European Society of Cardiology (ESC). Eur Heart J 2011;32:3147–3197.
701. Sliwa K, Fett J, Elkayam U. Peripartum cardiomyopathy. Lancet 2006;368:687–693. 702. Gunderson EP, Croen LA, Chiang V, Yoshida CK, Walton D, Go AS. Epidemiology of peripartum cardiomyopathy: incidence, predictors, and outcomes. Obstet Gynecol 2011;118:583–591.
703. Felker GM, Jaeger CJ, Klodas E, Thiemann DR, Hare JM, Hruban RH, Kasper EK, Baughman KL. Myocarditis and long-term survival in peripartum cardiomyopathy. Am Heart J 2000;140:785–791.
704. van Spaendonck-Zwarts KY, Posafalvi A, van den Berg MP, Hilfiker-Kleiner D, Bollen IA, Sliwa K, Alders M, Almomani R, van Langen IM, van der Meer P, Sinke RJ, van der Velden J, Van Veldhuisen DJ, van Tintelen JP, Jongbloed JD. Titin gene mutations are common in families with both peripartum cardiomyopathy and dilated cardiomyopathy. Eur Heart J 2014;35:2165–2173.
705. Sliwa K, Hilfiker-Kleiner D, Mebazaa A, Petrie MC, Maggioni AP, Regitz-Zagrosek V, Schaufelberger M, Tavazzi L, van Veldhuisen DJ, Roos-Hesslink JW, Shah AJ, Seferovic PM, Elkayam U, van Spaendonck-Zwarts K, Bachelier-Walenta K, Mouquet F, Kraigher-Krainer E, Hall R, Ponikowski P, McMurray JJ, Pieske B. EURObservational Research Programme: a worldwide registry on peripartum cardiomyopathy (PPCM) in conjunction with the Heart Failure Association of the European Society of Cardiology Working Group on PPCM. Eur J Heart Fail 2014;16:583–591.
706. Gowda RM, Khan IA, Mehta NJ, Vasavada BC, Sacchi TJ. Cardiac arrhythmias in pregnancy: clinical and therapeutic considerations. Int J Cardiol 2003;88:129–133.
707. Schaefer C. Angiotensin II-receptor-antagonists: further evidence of fetotoxicity but not teratogenicity. Birth Defects Res A Clin Mol Teratol 2003;67:591–594. 708. Trappe HJ, Pfitzner P. [Cardiac arrhythmias in pregnancy]. Z Kardiol 2001; 90(Suppl 4):36–44.
709. Mirshahi M, Ayani E, Nicolas C, Golestaneh N, Ferrari P, Valamanesh F, Agarwal MK. The blockade of mineralocorticoid hormone signaling provokes dramatic teratogenesis in cultured rat embryos. Int J Toxicol 2002;21:191–199.
710. Habli M, OBrien T, Nowack E, Khoury S, Barton JR, Sibai B. Peripartum cardiomyopathy: prognostic factors for long-term maternal outcome. Am J Obstet Gynecol 2008;199:415.e1–415.e5.
711. Simantirakis EN, Schiza SI, Marketou ME, Chrysostomakis SI, Chlouverakis GI, Klapsinos NC, Siafakas NS, Vardas PE. Severe bradyarrhythmias in patients with sleep apnoea: the effect of continuous positive airway pressure treatment: a longterm evaluation using an insertable loop recorder. Eur Heart J 2004;25: 1070–1076.
712. Gami AS, Olson EJ, Shen WK, Wright RS, Ballman KV, Hodge DO, Herges RM, Howard DE, Somers VK. Obstructive sleep apnea and the risk of sudden cardiac death: a longitudinal study of 10,701 adults. J Am Coll Cardiol 2013;62:610–616.
713. Young T, Palta M, Dempsey J, Skatrud J, Weber S, Badr S. The occurrence of sleepdisordered breathing among middle-aged adults. N Engl J Med 1993;328: 1230–1235.
714. Marshall NS, Wong KK, Liu PY, Cullen SR, Knuiman MW, Grunstein RR. Sleep apnea as an independent risk factor for all-cause mortality: the Busselton Health Study. Sleep 2008;31:1079–1085.
715. Young T, Finn L, Peppard PE, Szklo-Coxe M, Austin D, Nieto FJ, Stubbs R, Hla KM. Sleep disordered breathing and mortality: eighteen-year follow-up of the Wisconsin sleep cohort. Sleep 2008;31:1071–1078.
716. Kreuz J, Skowasch D, Horlbeck F, Atzinger C, Schrickel JW, Lorenzen H, Nickenig G, Schwab JO. Usefulness of sleep-disordered breathing to predict occurrence of appropriate and inappropriate implantable-cardioverter defibrillator therapy in patients with implantable cardioverter-defibrillator for primary prevention of sudden cardiac death. Am J Cardiol 2013;111:1319–1323.
717. Bitter T, Westerheide N, Prinz C, Hossain MS, Vogt J, Langer C, Horstkotte D, Oldenburg O. Cheyne-Stokes respiration and obstructive sleep apnoea are independent risk factors for malignant ventricular arrhythmias requiring appropriate cardioverter-defibrillator therapies in patients with congestive heart failure. Eur Heart J 2011;32:61–74.
718. Roche F, Xuong AN, Court-Fortune I, Costes F, Pichot V, Duverney D, Vergnon JM, Gaspoz JM, Barthelemy JC. Relationship among the severity of sleep apnea syndrome, cardiac arrhythmias, and autonomic imbalance. Pacing Clin Electrophysiol 2003;26:669–677.
719. Guilleminault C, Connolly SJ, Winkle RA. Cardiac arrhythmia and conduction disturbances during sleep in 400 patients with sleep apnea syndrome. Am J Cardiol 1983;52:490–494.
720. Becker HF, Koehler U, Stammnitz A, Peter JH. Heart block in patients with sleep apnoea. Thorax 1998;53(Suppl 3):S29–S32.
721. Grimm W, Hoffmann J, Menz V, Kohler U, Heitmann J, Peter JH, Maisch B. Electrophysiologic evaluation of sinus node function and atrioventricular conduction in patients with prolonged ventricular asystole during obstructive sleep apnea. Am J Cardiol 1996;77:1310–1314.
722. Mehra R, Benjamin EJ, Shahar E, Gottlieb DJ, Nawabit R, Kirchner HL, Sahadevan J, Redline S. Association of nocturnal arrhythmias with sleep-disordered breathing: the Sleep Heart Health Study. Am J Respir Crit Care Med 2006;173:910–916.
723. Hoffstein V, Mateika S. Cardiac arrhythmias, snoring, and sleep apnea. Chest 1994; 106:466–471.
724. Tilkian AG, Guilleminault C, Schroeder JS, Lehrman KL, Simmons FB, Dement WC. Sleep-induced apnea syndrome. Prevalence of cardiac arrhythmias and their reversal after tracheostomy. Am J Med 1977;63:348–358.
725. Ryan CM, Usui K, Floras JS, Bradley TD. Effect of continuous positive airway pressure on ventricular ectopy in heart failure patients with obstructive sleep apnoea. Thorax 2005;60:781–785.
726. Gami AS, Howard DE, Olson EJ, Somers VK. Day-night pattern of sudden death in obstructive sleep apnea. N Engl J Med 2005;352:1206–1214.
727. Gonzalez-Rothi RJ, Foresman GE, Block AJ. Do patients with sleep apnea die in their sleep? Chest 1988;94:531–538.
728. Seppala T, Partinen M, Penttila A, Aspholm R, Tiainen E, Kaukianen A. Sudden death and sleeping history among Finnish men. J Intern Med 1991;229:23–28.
729. Zeidan-Shwiri T, Aronson D, Atalla K, Blich M, Suleiman M, Marai I, Gepstein L, Lavie L, Lavie P, Boulos M. Circadian pattern of life-threatening ventricular arrhythmia in patients with sleep-disordered breathing and implantable cardioverter-defibrillators. Heart Rhythm 2011;8:657–662.
730. Harbison J, OReilly P, McNicholas WT. Cardiac rhythm disturbances in the obstructive sleep apnea syndrome: effects of nasal continuous positive airway pressure therapy. Chest 2000;118:591–595.
731. Grimm W, Koehler U, Fus E, Hoffmann J, Menz V, Funck R, Peter JH, Maisch B. Outcome of patients with sleep apnea-associated severe bradyarrhythmias after continuous positive airway pressure therapy. Am J Cardiol 2000;86:688–692.
732. Koehler U, Fus E, Grimm W, Pankow W, Schafer H, Stammnitz A, Peter JH. Heart block in patients with obstructive sleep apnoea: pathogenetic factors and effects of treatment. Eur Respir J 1998;11:434–439.
733. Stegman SS, Burroughs JM, Henthorn RW. Asymptomatic bradyarrhythmias as a marker for sleep apnea: appropriate recognition and treatment may reduce the need for pacemaker therapy. Pacing Clin Electrophysiol 1996;19:899–904.
734. Garrigue S, Pepin JL, Defaye P, Murgatroyd F, Poezevara Y, Clementy J, Levy P. High prevalence of sleep apnea syndrome in patients with long-term pacing: the European Multicenter Polysomnographic Study. Circulation 2007;115: 1703–1709.
735. Doherty LS, Kiely JL, Swan V, McNicholas WT. Long-term effects of nasal continuous positive airway pressure therapy on cardiovascular outcomes in sleep apnea syndrome. Chest 2005;127:2076–2084.
736. Garrigue S, Bordier P, Jais P, Shah DC, Hocini M, Raherison C, Tunon De Lara M, Haissaguerre M, Clementy J. Benefit of atrial pacing in sleep apnea syndrome. N Engl J Med 2002;346:404–412.
737. Simantirakis EN, Vardas PE. Cardiac pacing in sleep apnoea: diagnostic and therapeutic implications. Europace 2006;8:984–987.
738. Marin JM, Carrizo SJ, Vicente E, Agusti AG. Long-term cardiovascular outcomes in men with obstructive sleep apnoea-hypopnoea with or without treatment with continuous positive airway pressure: an observational study. Lancet 2005;365: 1046–1053.
739. Defaye P, de la Cruz I, Marti-Almor J, Villuendas R, Bru P, Senechal J, Tamisier R, Pepin JL. A pacemaker transthoracic impedance sensor with an advanced algorithm to identify severe sleep apnea: the DREAM European study. Heart Rhythm 2014;11:842–848.
740. Strollo PJ Jr, Soose RJ, Maurer JT, de Vries N, Cornelius J, Froymovich O, Hanson RD, Padhya TA, Steward DL, Gillespie MB, Woodson BT, Van de Heyning PH, Goetting MG, Vanderveken OM, Feldman N, Knaack L, Strohl KP. Upper-airway stimulation for obstructive sleep apnea. N Engl J Med 2014;370: 139–149.
741. Wyse DG, Friedman PL, Brodsky MA, Beckman KJ, Carlson MD, Curtis AB, Hallstrom AP, Raitt MH, Wilkoff BL, Greene HL. Life-threatening ventricular arrhythmias due to transient or correctable causes: high risk for death in follow-up. J Am Coll Cardiol 2001;38:1718–1724.
742. Monnig G, Kobe J, Loher A, Wasmer K, Milberg P, Zellerhoff S, Pott C, Zumhagen S, Radu R, Scheld HH, Haverkamp W, Schulze-Bahr E, Eckardt L. Role of implantable cardioverter defibrillator therapy in patients with acquired long QT syndrome: a long-term follow-up. Europace 2012;14:396–401.
743. Wolbrette DL. Risk of proarrhythmia with class III antiarrhythmic agents: sexbased differences and other issues. Am J Cardiol 2003;91:39D–44D.
744. Haverkamp W, Breithardt G, Camm AJ, Janse MJ, Rosen MR, Antzelevitch C, Escande D, Franz M, Malik M, Moss A, Shah R. The potential for QT prolongation and proarrhythmia by non-antiarrhythmic drugs: clinical and regulatory implications. Report on a policy conference of the European Society of Cardiology. Eur Heart J 2000;21:1216–1231.
745. Rao GA, Mann JR, Shoaibi A, Bennett CL, Nahhas G, Sutton SS, Jacob S, Strayer SM. Azithromycin and levofloxacin use and increased risk of cardiac arrhythmia and death. Ann Fam Med 2014;12:121–127.
746. Ray WA, Murray KT, Hall K, Arbogast PG, Stein CM. Azithromycin and the risk of cardiovascular death. N Engl J Med 2012;366:1881–1890.
747. Lapi F, Wilchesky M, Kezouh A, Benisty JI, Ernst P, Suissa S. Fluoroquinolones and the risk of serious arrhythmia: a population-based study. Clin Infect Dis 2012;55: 1457–1465.
748. Svanstrom H, Pasternak B, Hviid A. Use of clarithromycin and roxithromycin and risk of cardiac death: cohort study. BMJ 2014;349:g4930.
749. Fralick M, Macdonald EM, Gomes T, Antoniou T, Hollands S, Mamdani MM, Juurlink DN, Canadian Drug Safety and Effectiveness Research Network (CDSERN). Co-trimoxazole and sudden death in patients receiving inhibitors of renin-angiotensin system: population based study. BMJ 2014;349:g6196.
750. Tada H, Sticherling C, Oral H, Morady F. Brugada syndrome mimicked by tricyclic antidepressant overdose. J Cardiovasc Electrophysiol 2001;12:275.
751. Lipshultz SE, Lipsitz SR, Mone SM, Goorin AM, Sallan SE, Sanders SP, Orav EJ, Gelber RD, Colan SD. Female sex and drug dose as risk factors for late cardiotoxic effects of doxorubicin therapy for childhood cancer. N Engl J Med 1995; 332:1738–1743.
752. Steinherz LJ, Steinherz PG, Tan C. Cardiac failure and dysrhythmias 6-19 years after anthracycline therapy: a series of 15 patients. Med Pediatr Oncol 1995;24: 352–361.
753. Anand AJ. Fluorouracil cardiotoxicity. Ann Pharmacother 1994;28:374–378.
754. Gorgulu S, Celik S, Tezel T. A case of coronary spasm induced by 5-fluorouracil. Acta Cardiol 2002;57:381–383. 755. Pinter A, Dorian P, Newman D. Cesium-induced torsades de pointes. N Engl J Med 2002;346:383–384.
756. Gowda RM, Cohen RA, Khan IA. Toad venom poisoning: resemblance to digoxin toxicity and therapeutic implications. Heart 2003;89:e14.
757. Bain RJ. Accidental digitalis poisoning due to drinking herbal tea. Br Med J (Clin Res Ed) 1985;290:1624.
758. Eddleston M, Ariaratnam CA, Sjostrom L, Jayalath S, Rajakanthan K, Rajapakse S, Colbert D, Meyer WP, Perera G, Attapattu S, Kularatne SA, Sheriff MR, Warrell DA. Acute yellow oleander (Thevetia peruviana) poisoning: cardiac arrhythmias, electrolyte disturbances, and serum cardiac glycoside concentrations on presentation to hospital. Heart 2000;83:301–306.
759. Schnetzler B, Popova N, Collao Lamb C, Sappino AP. Coronary spasm induced by capecitabine. Ann Oncol 2001;12:723–724.
760. Welch KM, Saiers J, Salonen R. Triptans and coronary spasm. Clin Pharmacol Ther 2000;68:337–338.
761. Qasim A, Townend J, Davies MK. Ecstasy induced acute myocardial infarction. Heart 2001;85:E10. 762. Tzivoni D, Banai S, Schuger C, Benhorin J, Keren A, Gottlieb S, Stern S. Treatment of torsade de pointes with magnesium sulfate. Circulation 1988;77:392–397.
763. Hondeghem LM. Antiarrhythmic agents: modulated receptor applications. Circulation 1987;75:514–520.
764. Siebels J, Kuck KH. Implantable cardioverter defibrillator compared with antiarrhythmic drug treatment in cardiac arrest survivors (the Cardiac Arrest Study Hamburg). Am Heart J 1994;127:1139–1144.
765. Hellestrand KJ, Burnett PJ, Milne JR, Bexton RS, Nathan AW, Camm AJ. Effect of the antiarrhythmic agent flecainide acetate on acute and chronic pacing thresholds. Pacing Clin Electrophysiol 1983;6:892–899. 766. Echt DS, Black JN, Barbey JT, Coxe DR, Cato E. Evaluation of antiarrhythmic drugs on defibrillation energy requirements in dogs. Sodium channel block and action potential prolongation. Circulation 1989;79:1106–1117.
767. Torp-Pedersen C, Moller M, Bloch-Thomsen PE, Kober L, Sandoe E, Egstrup K, Agner E, Carlsen J, Videbaek J, Marchant B, Camm AJ. Dofetilide in patients with congestive heart failure and left ventricular dysfunction. Danish Investigations of Arrhythmia and Mortality on Dofetilide Study Group. N Engl J Med 1999;341: 857–865.
768. Lazzara R. Antiarrhythmic drugs and torsade de pointes. Eur Heart J 1993; 14(Suppl H):88–92. 769. Khan IA, Gowda RM. Novel therapeutics for treatment of long-QT syndrome and torsade de pointes. Int J Cardiol 2004;95:1–6.
770. Barra S, Agarwal S, Begley D, Providencia R. Post-acute management of the acquired long QT syndrome. Postgrad Med J 2014;90:348–358. 771. Borron SW, Bismuth C, Muszynski J. Advances in the management of digoxin toxicity in the older patient. Drugs Aging 1997;10:18–33.
772. Solomon RJ. Ventricular arrhythmias in patients with myocardial infarction and ischaemia. Relationship to serum potassium and magnesium. Drugs 1984;28(Suppl 1): 66–76.
773. Sjogren A, Edvinsson L, Fallgren B. Magnesium deficiency in coronary artery disease and cardiac arrhythmias. J Intern Med 1989;226:213–222.
774. Rasmussen HS, McNair P, Norregard P, Backer V, Lindeneg O, Balslev S. Intravenous magnesium in acute myocardial infarction. Lancet 1986;1:234–236.
775. Abraham AS, Rosenmann D, Kramer M, Balkin J, Zion MM, Farbstien H, Eylath U. Magnesium in the prevention of lethal arrhythmias in acute myocardial infarction. Arch Intern Med 1987;147:753–755.
776. Rajs J, Rajs E, Lundman T. Unexpected death in patients suffering from eating disorders. A medico-legal study. Acta Psychiatr Scand 1986;74:587–596. 777. Iseri LT, Freed J, Bures AR. Magnesium deficiency and cardiac disorders. Am J Med 1975;58:837–846.
778. Zwerling HK. Does exogenous magnesium suppress myocardial irritability and tachyarrhythmias in the nondigitalized patient? Am Heart J 1987;113:1046–1053.
779. Rosenqvist M, Beyer T, Block M, den Dulk K, Minten J, Lindemans F. Adverse events with transvenous implantable cardioverter-defibrillators: a prospective multicenter study. European 7219 Jewel ICD investigators. Circulation 1998;98: 663–670.
780. Martinez Sanchez J, Garcia Alberol A, Almendral Garrote J, Castellanos E, Perez Castellanos N, Ortiz Paton M, Sanchez Munoz JJ, Llamas Lazaro C, Ruiperez Abizanda JA, Valdes Chavarri M. [Ventricular arrhythmias induced by appropriate antibradycardia pacing in patients with implantable defibrillators]. Rev Esp Cardiol 2001;54:845–850.
781. Callans DJ, Hook BG, Kleiman RB, Mitra RL, Flores BT, Marchlinski FE. Unique sensing errors in third-generation implantable cardioverter-defibrillators. J Am Coll Cardiol 1993;22:1135–1140.
782. Chantranuwat C, Blakey JD, Kobashigawa JA, Moriguchi JD, Laks H, Vassilakis ME, Fishbein MC. Sudden, unexpected death in cardiac transplant recipients: an autopsy study. J Heart Lung Transplant 2004;23:683–689.
783. Vakil K, Taimeh Z, Sharma A, Abidi KS, Colvin M, Luepker R, Levy WC, Adabag S. Incidence, predictors, and temporal trends of sudden cardiac death after heart transplantation. Heart Rhythm 2014;11:1684–1690. 784. Tsai VW, Cooper J, Garan H, Natale A, Ptaszek LM, Ellinor PT, Hickey K, Downey R, Zei P, Hsia H, Wang P, Hunt S, Haddad F, Al-Ahmad A. The efficacy of implantable cardioverter-defibrillators in heart transplant recipients: results from a multicenter registry. Circ Heart Fail 2009;2:197–201.
785. Menafoglio A, Di Valentino M, Porretta AP, Foglia P, Segatto JM, Siragusa P, Pezzoli R, Maggi M, Romano GA, Moschovitis G, Gallino A. Cardiovascular evaluation of middle-aged individuals engaged in high-intensity sport activities: implications for workload, yield and economic costs. Br J Sports Med 2014 Nov 13. doi:10.1136/bjsports-2014-093857 [Epub ahead of print].
786. Borjesson M, Serratosa L, Carre F, Corrado D, Drezner J, Dugmore DL, Heidbuchel HH, Mellwig KP, Panhuyzen-Goedkoop NM, Papadakis M, Rasmusen H, Sharma S, Solberg EE, van Buuren F, Pelliccia A, writing group on behalf of the EACPR Section of Sports Cardiology. Consensus document regarding cardiovascular safety at sports arenas: position stand from the European Association of Cardiovascular Prevention and Rehabilitation (EACPR), section of Sports Cardiology. Eur Heart J 2011;32:2119–2124.
787. Conroy RM, Pyorala K, Fitzgerald AP, Sans S, Menotti A, De Backer G, De Bacquer D, Ducimetiere P, Jousilahti P, Keil U, Njolstad I, Oganov RG, Thomsen T, Tunstall-Pedoe H, Tverdal A, Wedel H, Whincup P, Wilhelmsen L, Graham IM, SCORE project group. Estimation of ten-year risk of fatal cardiovascular disease in Europe: the SCORE project. Eur Heart J 2003;24:987–1003.
788. Harmon KG, Drezner JA, Wilson MG, Sharma S. Incidence of sudden cardiac death in athletes: a state-of-the-art review. Heart 2014;100:1227–1234. 789. Schmied C, Borjesson M. Sudden cardiac death in athletes. J Intern Med 2014;275: 93–103.
790. Corrado D, Basso C, Pavei A, Michieli P, Schiavon M, Thiene G. Trends in sudden cardiovascular death in young competitive athletes after implementation of a preparticipation screening program. JAMA 2006;296:1593–1601.
791. Maron BJ, Araujo CG, Thompson PD, Fletcher GF, de Luna AB, Fleg JL, Pelliccia A, Balady GJ, Furlanello F, Van Camp SP, Elosua R, Chaitman BR, Bazzarre TL. Recommendations for preparticipation screening and the assessment of cardiovascular disease in masters athletes: an advisory for healthcare professionals from the working groups of the World Heart Federation, the International Federation of Sports Medicine, and the American Heart Association Committee on Exercise, Cardiac Rehabilitation, and Prevention. Circulation 2001;103:327–334.
792. Borjesson M, Urhausen A, Kouidi E, Dugmore D, Sharma S, Halle M, Heidbuchel H, Bjornstad HH, Gielen S, Mezzani A, Corrado D, Pelliccia A, Vanhees L. Cardiovascular evaluation of middle-aged/senior individuals engaged in leisure-time sport activities: position stand from the sections of exercise physiology and sports cardiology of the European Association of Cardiovascular Prevention and Rehabilitation. Eur J Cardiovasc Prev Rehabil 2011;18:446–458.
793. Pappone C, Vicedomini G, Manguso F, Saviano M, Baldi M, Pappone A, Ciaccio C, Giannelli L, Ionescu B, Petretta A, Vitale R, Cuko A, Calovic Z, Fundaliotis A, Moscatiello M, Tavazzi L, Santinelli V. Wolff–Parkinson–White syndrome in the era of catheter ablation: insights from a registry study of 2169 patients. Circulation 2014;130:811–819.
794. Obeyesekere MN, Leong-Sit P, Massel D, Manlucu J, Modi S, Krahn AD, Skanes AC, Yee R, Gula LJ, Klein GJ. Risk of arrhythmia and sudden death in patients with asymptomatic preexcitation: a meta-analysis. Circulation 2012;125: 2308–2315.
795. Munger TM, Packer DL, Hammill SC, Feldman BJ, Bailey KR, Ballard DJ, Holmes DR Jr, Gersh BJ. A population study of the natural history of Wolff–Parkinson–White syndrome in Olmsted County, Minnesota, 1953–1989. Circulation 1993;87:866–873.
796. Cohen MI, Triedman JK, Cannon BC, Davis AM, Drago F, Janousek J, Klein GJ, Law IH, Morady FJ, Paul T, Perry JC, Sanatani S, Tanel RE. PACES/HRS expert consensus statement on the management of the asymptomatic young patient with a Wolff–Parkinson–White (WPW, ventricular preexcitation) electrocardiographic pattern: developed in partnership between the Pediatric and Congenital Electrophysiology Society (PACES) and the Heart Rhythm Society (HRS). Endorsed by the governing bodies of PACES, HRS, the American College of Cardiology Foundation (ACCF), the American Heart Association (AHA), the American Academy of Pediatrics (AAP), and the Canadian Heart Rhythm Society (CHRS). Heart Rhythm 2012;9:1006–1024.
797. Soumerai SB, McLaughlin TJ, Spiegelman D, Hertzmark E, Thibault G, Goldman L. Adverse outcomes of underuse of beta-blockers in elderly survivors of acute myocardial infarction. JAMA 1997;277:115–121.
798. Kong MH, Al-Khatib SM, Sanders GD, Hasselblad V, Peterson ED. Use of implantable cardioverter-defibrillators for primary prevention in older patients: a systematic literature review and meta-analysis. Cardiol J 2011;18:503–514.
799. Santangeli P, Di Biase L, Dello Russo A, Casella M, Bartoletti S, Santarelli P, Pelargonio G, Natale A. Meta-analysis: age and effectiveness of prophylactic implantable cardioverter-defibrillators. Ann Intern Med 2010;153:592–599.
800. Healey JS, Hallstrom AP, Kuck KH, Nair G, Schron EP, Roberts RS, Morillo CA, Connolly SJ. Role of the implantable defibrillator among elderly patients with a history of life-threatening ventricular arrhythmias. Eur Heart J 2007;28: 1746–1749.
801. Chan PS, Nallamothu BK, Spertus JA, Masoudi FA, Bartone C, Kereiakes DJ, Chow T. Impact of age and medical comorbidity on the effectiveness of implantable cardioverter-defibrillators for primary prevention. Circ Cardiovasc Qual Outcomes 2009;2:16–24.
802. Brullmann S, Dichtl W, Paoli U, Haegeli L, Schmied C, Steffel J, Brunckhorst C, Hintringer F, Seifert B, Duru F, Wolber T. Comparison of benefit and mortality of implantable cardioverter-defibrillator therapy in patients aged ≥75 years versus those ,75 years. Am J Cardiol 2012;109:712–717.
803. Noyes K, Corona E, Zwanziger J, Hall WJ, Zhao H, Wang H, Moss AJ, Dick AW. Health-related quality of life consequences of implantable cardioverter defibrillators: results from MADIT II. Med Care 2007;45:377–385. 804. Lunney JR, Lynn J, Foley DJ, Lipson S, Guralnik JM. Patterns of functional decline at the end of life. JAMA 2003;289:2387–2392.
805. Padeletti L, Arnar DO, Boncinelli L, Brachman J, Camm JA, Daubert JC, Hassam SK, Deliens L, Glikson M, Hayes D, Israel C, Lampert R, Lobban T, Raatikainen P, Siegal G, Vardas P, Reviewers, Kirchhof P, Becker R, Cosio F, Loh P, Cobbe S, Grace A, Morgan J. EHRA Expert Consensus Statement on the management of cardiovascular implantable electronic devices in patients nearing end of life or requesting withdrawal of therapy. Europace 2010;12: 1480–1489.
806. Jaarsma T, Beattie JM, Ryder M, Rutten FH, McDonagh T, Mohacsi P, Murray SA, Grodzicki T, Bergh I, Metra M, Ekman I, Angermann C, Leventhal M, Pitsis A, Anker SD, Gavazzi A, Ponikowski P, Dickstein K, Delacretaz E, Blue L, Strasser F, McMurray J. Palliative care in heart failure: a position statement from the palliative care workshop of the Heart Failure Association of the European Society of Cardiology. Eur J Heart Fail 2009;11:433–443.
807. Goldstein NE, Lampert R, Bradley E, Lynn J, Krumholz HM. Management of implantable cardioverter defibrillators in end-of-life care. Ann Intern Med 2004; 141:835–838.
808. Wright GA, Klein GJ, Gula LJ. Ethical and legal perspective of implantable cardioverter defibrillator deactivation or implantable cardioverter defibrillator generator replacement in the elderly. Curr Opin Cardiol 2013;28:43–49.
809. Lampert R, Hayes DL, Annas GJ, Farley MA, Goldstein NE, Hamilton RM, Kay GN, Kramer DB, Mueller PS, Padeletti L, Pozuelo L, Schoenfeld MH, Vardas PE, Wiegand DL, Zellner R. HRS Expert Consensus Statement on the Management of Cardiovascular Implantable Electronic Devices (CIEDs) in patients nearing end of life or requesting withdrawal of therapy. Heart Rhythm 2010;7:1008–1026.







