TÓM TẮT
CƠ SỞ LÝ LUẬN
Bệnh động mạch ngoại biên có liên quan với nguy cơ thiếu máu cục bộ và chảy máu tăng cao ở bệnh nhân có tiền căn nhồi máu cơ tim.
(Bonaca MP, Bhatt DL, Storey RF, Steg PG, Cohen M, Kuder J, Goodrich E, Nicolau JC,
Parkhomenko A, López-Sendón J, Dellborg M, Dalby A, Špinar J, Aylward P,Corbalán R,
Abola MT, Jensen EC, Held P, Braunwald E, Sabatine MS. Ticagrelor forPrevention of ischemic Events After Myocardial Infarction in Patients WithPeripheral Artery Disease.
J Am Coll Cardiol. 2016 Jun 14;67(23):2719-28.)
Lược dịch: TS. BS. Chu Trọng Hiệp
MỤC TIÊU
Nghiên cứu này đánh giá hiệu quả và an toàn của Ticagrelor về các biến cố tim mạch nặng và các biến cố thiếu máu chi nặng ở bệnh nhân bệnh động mạch ngọai biên và nhồi máu cơ tim trước đây.
PHƯƠNG PHÁP
PEGASUS-TIMI 54 (Prevention of Cardiovascular Events in Patients With Prior Heart Attack Using Ticagrelor Compared to Placebo on a Background of Aspirin—Thrombolysis In Myocardial Infarction 54) nghiên cứu ngẫu nhiên 21.162 bệnh nhân có tiền sử NMCT (1-3 năm) dùng ticagrelor 90 mg hai lần mỗi ngày, dùng ticagrelor 60 mg hai lần mỗi ngày hoặc giả dược, tất cả trên một nền tảng của aspirin liều thấp. Tiền sử bệnh động mạch ngoại biên (PAD) được ghi nhận tại thời điểm bắt đầu tham gia nghiên cứu.Tỷ lệ các biến cố bất lợi tim mạch chính (MACE) (được định nghĩa như chết do nguyên nhân tim mạch, nhồi máu cơ tim hoặc đột quỵ) và các các biến cố bất lợi chính ở chi (MALE) (được định nghĩa như thiếu máu cục bộ chi cấp tính hoặc cần thiết tái thông mạch máu ngoại vi cho thiếu máu cục bộ) được ghi lại trong quá trình theo dõi
KẾT QUẢ
Tổng cộng có 1.143 bệnh nhân (5%) có bệnh động mạch ngoại biên (PAD) được nhận diện. Trong nhóm giả dược, những người có bệnh động mạch ngoại biên (PAD) (n = 404) có tỷ lệ cao hơn MACE tại thời điểm 3 năm so với những người không có (n = 6663; 19,3%, so với 8,4%; p <0,001), điều này vẫn đúng sau khi điều chỉnh các giới hạn khác nhau (HR điều chỉnh là 1,60; KTC 95%: 1,20-2,13; p = 0,0013), và có tỷ lệ cao hơn ở thiếu máu chi cấp tính 1,0% so với 0,1%) và phẫu thuật tái lưu thông mạch máu ngoại biên (9,15% so với 0,46%). Trong khi đó, giảm nguy cơ tương đối MACE với Ticagrelor cũng đồng nhất, bệnh nhân bệnh động mạch ngoại biên (PAD) có giảm nguy cơ tuyệt đối nhiều hơn đến 4,1% (number needed to treat là 25) do nguy cơ tuyệt đối của họ cao hơn. Tỷ lệ xuất huyết nặng theo TIMI tăng 0,12% (number needed to harm là 834). Liều 60 mg có kết quả đặc biệt thuận lợi cho tim mạch và tử vong do mọi nguyên nhân. Ticagrelor (liều gộp) làm giảm nguy cơ của MALE (HR = 0,65; KTC 95%: 0,44-0,95; p = 0,026).
KẾT LUẬN
Trong số bệnh nhân ổn định với tiền căn NMCT (MI), kèm theo bệnh mạch máu ngoại biên có nguy cơ thiếu máu cục bộtăng cao. Ở những bệnh nhân này Ticagrelor giảm MACE, giảm nguy cơ tuyệt đối lớn, và MALE.
——————————————————————————————-
Bệnh nhân bị bệnh động mạch ngoại biên (PAD) có nguy cơ cao của các biến cố tim mạch chính (MACE), bao gồm nhồi máu cơ tim (MI) và đột quỵ. Bệnh nhân bệnh mạch vành kèm theo bệnh động mạch ngoại biên có triệu chứng (bệnh tổn thương đa mạch máu), có tương quan với nguy cơ cao hơn nữa của thiếu máu cục bộ và tử vong liên quan đến bệnh có triệu chứng ở một trong hai giường mạch máu (động mạch vành hoặc động mạch ngoại vi) (1-4).
Chiến lược chống huyết khối chuyên sâu nhằm giảm nguy cơ MACE ở bệnh nhân PAD đã cho thấy kết quả khác nhau. Trong khi liệu pháp kháng tiểu cầu đơn độc đã được chứng minh là giảm nguy cơ thiếu máu cục bộ ở bệnh nhân bệnh động mạch ngoại biên (PAD) (4-6), sự kết hợp của aspirin và một chất ức chế P2Y12 ở bệnh nhân bệnh động mạch ngoại biên được phẫu thuật bắc cầu động mạch chi dưới không làm giảm kết cục chung tim mạch và chi (7). Tuy nhiên, các nghiên cứu lớn đánh giá sự kết hợp của aspirin và clopidogrel đã cho thấy xu hướng có lợi cho việc giảm MACE ở bệnh nhân có bệnh lý mạch máu có triệu chứng, bao gồm cả những người bị PAD (8,9). Gần đây, việc bổ sung các chất đối kháng PAR-1, vorapaxar, đã được chứng minh khả năng giảm nguy cơ MACE ở những bệnh nhân bị NMCT trước đây hoặc bệnh động mạch ngoại biên nhưng tăng lại làm tăng tỷ lệ xuất huyết từ vừa đến nặng theo GUSTO (Chiến lược để mở thông hoàn toàn động mạch tắc nghẽn Global Use of Strategies to Open Occluded Arteries)(10). Ngoài việc giảm MACE, vorapaxar được cho thấy giảm tỷ lệ thương tật ở chi, bao gồm thiếu máu cấp tính chi dưới (ALI) và tái thông mạch máu ngoại vi, khi kết hợp với aspirin và / hoặc clopidogrel (11,12). Những phát hiện này làm nổi bật tiềm năng của liệu pháp kháng đông để giảm tỷ lệ thương tật chi ở những bệnh nhân với bệnh động mạch ngoại vi.
Sự kết hợp của PAD đồng mắc với gia tăng nguy cơ thiếu máu cục bộ trở nên phức tạp bởi thực tế là PAD (Bệnh động mạch ngoại biên) cũng liên quan với tăng nguy cơ chảy máu (13). Có rất nhiều bệnh đi kèm làm tăng nguy cơ của cả PAD và chảy máu, bao gồm tuổi và rối loạn chức năng thận. Ngoài ra, các mạch máu bị bệnh ở bệnh nhân PAD dễ dàng bị chấn thương hoặc các gặp các biến chứng của can thiệp mạch dẫn đến chảy máu. Trong các thử nghiệm của chiến lược chống huyết khối mạnh để phòng ngừa trong PAD, đã có sự gia tăng đáng kể biến chứng xuất huyết, đặc biệt là với các thuốc chống đông máu liều đầy đủ (7, 8, 10, 14)
PEGASUS-TIMI 54 (Dự phòng các biến cố tim mạch trên bệnh nhân có tiền sử NMCT – Sử dụng Ticagrelor so với Placebotrên nền của Aspirin) Nghiên cứu cho thấy việc bổ sung Ticagrelor, một thuốc ức chế mạnh, có hồi phục P2Y12, làm giảm nguy cơ thiếu máu cục bộ dài hạn ở những bệnh nhân có tiền sử NMCT. Giảm nguy cơ thiếu máu cục bộ này được đi kèm với sự gia tăng chảy máu nặng theo TIMI. Do đó chúng tôi đã đánh giá nguy cơ thiếu máu cục bộ và chảy máu liên quan đến PAD (Bệnh động mạch ngoại biên) có triệu chứng kèm theo; và liệu những tác động của ticagrelor trên MACE và các biến cố chính ở chi (MALE) có bị thay đổi bởi sự hiện diện của PAD.
PHƯƠNG PHÁP NGHIÊN CỨU
Dân số nghiên cứu
Thử nghiệm PEGASUS-TIMI 54: nghiên cứu ngẫu trên nhiên bệnh nhân bị NMCT với ticagrelor 90 mg hai lần mỗi ngày, ticagrelor 60 mg hai lần mỗi ngày, hoặc giả dược, kết hợp với aspirin liều thấp. Thiết kế nghiên cứu (15) và kết quả chính của cuộc thử nghiệm đã được công bố (16). Sơ lược chúng tôi ghi nhận có 21.162 bệnh nhân có NMCT tự phát xảy ra 1-3 năm trước khi tuyển chọn vào nghiên cứucùng với ít nhất 1 yếu tố nguy cơ cao sau đây: tuổi ≥ 65; đái tháo đường đang điều trị thuốc; NMCT tái phát; bệnh mạch vành nhiều nhánh hoặc rối loạn chức năng thận mãn tính, được xác định khi độ thanh thải creatinin <60 ml / phút, theo ước tính của các phương trình Cockcroft-Gault. Bệnh nhân không đạt tiêu chuẩn tuyển chọn nếu được chỉ định sử dụng một chất đối kháng thụ thể P2Y12 hoặc điều trị chống đông trong thời gian nghiên cứu; nếu bệnh nhân đã có rối loạn chảy máu, hoặc có tiền sử đột quỵ thiếu máu cục bộ hoặc xuất huyết nội sọ, một khối u hệ thống thần kinh trung ương, hay sự bất thường mạch máu nội sọ; hoặc nếu họ đã có xuất huyết tiêu hóa trong vòng 6 tháng trước đó hoặc phẫu thuật lớn trong vòng 1 tháng trước đó. Bệnh động mạch ngoại biên được ghi nhận ở đặc điểm cơ bản của bệnh nhân. Ngoài ra, các bệnh nhân có bệnh động mạch ngoại biên đã được ghi nhận chỉ số mắt cá chân-cánh tay (ABI) ≤0.90, bệnh sử tái thông mạch máu ngoại vi, hoặc có tiền sử đau cách hồi chi dưới.
Tiêu chí của nghiên cứu
Tiêu chí hiệu quả chính là tỷ lệ biến cố gộp tử vong do tim mạch, NMCT hoặc đột quỵ (MACE). Tỷ lệ thiếu máu chi cấp (ALI) được thu thập và đánh giá thông qua định nghĩa đã được công bố trước đó: phải có các biểu hiện lâm sàng của thiếu máu cấp tính và có phát hiện bất thường trên thăm khám thực thể hoặc chẩn đoán hình ảnh. Tiêu chí về các biến cố chính ở chi (MALE) được định nghĩa là tỷ lệ biến cố gộp của ALI và tái thông mạch máu ngoại biên.Tiêu chí an toàn chính là tỷ lệ xuất huyết nặng theo TIMI. Đoạn chi được coi như là biến cố về tính an toàn, bao gồm đoạn chi do mọi nguyên nhân (ví dụ như chấn thương, nhiễm trùng, thiếu máu cục bộ…). Tiêu chí an toàn phụ gồm xuất huyết nhẹ theo TIMI, xuất huyết nội sọ (ICH), và xuất huyết gây tử vong.
KẾT QUẢ
Tổng cộng có 21.162 bệnh nhân tham gia vào thử nghiệm PEGASUS-TIMI 54 với tiền sử NMCT và 1.143 (5%) đã được biết có bệnh động mạch ngoại biên. Bệnh nhân bị bệnh động mạch ngoại biên chủ yếu có bệnh sử đau cách hồi (65%), với khoảng một phần ba (34%) có bệnh sử can thiệp tái thông mạch máu ngoại vi và chỉ có 48 người (~4%) với ABI bất thường duy nhất mà không tái thông mạch máu hoặckhông có triệu chứng (Bảng 1). Đặc điểm cơ bản ở những người có và không có bệnh động mạch ngoại biên được thể hiện trong Bảng1. Nhóm bệnh nhân có PAD thường liên quan đến các yếu tố như lớn tuổi, NMCT không ST chênh và không chênh, đái tháo đường, rối loạn chức năng thận, hút thuốc lá, suy tim, tiền sử đột quỵ hoặc cơn thoáng thiếu máu não, và thời gian từ liều cuối cùng của chất ức chế P2Y12 trước khi phân ngẫu nhiên (Bảng 1). Nhóm bệnh nhân có PAD thường ghi nhận có bệnh lý nhiều nhánh mạch vành và tiền sử CABG, ít tiền sử can thiệp mạch vành qua da (Bảng 1). Tỷ lệ sử dụng liệu pháp điều trị nền, bao gồm cả aspirin (99,9%), statin (93%), beta-blockers (83%), và thuốc ức chế men chuyển hoặc thuốc chẹn thụ thể angiotensin (80,5%) là cao và tương đồng, bất kể có bệnh động mạch ngoại biên hay không.
Bảng 1. Đặc điểm cơ bản (chụp từ tài liệu gốc)
|
|
No PAD |
PAD |
p Value |
|---|---|---|---|
|
Age, yrs |
65 (59–71) |
66 (60–73) |
0.0003 |
|
Age ≥75 yrs |
2,892 (14.45) |
191 (16.71) |
0.035 |
|
Female |
4,806 (24.01) |
254 (22.22) |
0.1682 |
|
Body mass index, kg/m2 |
27.8 (25.16–31.16) |
27.8 (24.84–31.14) |
0.0845 |
|
Caucasian |
17,260 (86.23) |
1,066 (93.26) |
<0.0001 |
|
History of hypertension |
15,441 (77.14) |
966 (84.51) |
<0.0001 |
|
History of hypercholesterolemia |
15,317 (76.53) |
924 (80.84) |
0.0008 |
|
Current smoker |
3,191 (15.95) |
345 (30.18) |
<0.0001 |
|
History of COPD |
444 (6.66) |
68 (16.83) |
<0.0001 |
|
eGFR <60 ml/min/1.73 m2 (MDRD) |
4,494 (22.73) |
355 (31.47) |
<0.0001 |
|
History of diabetes |
6,324 (31.59) |
482 (42.17) |
<0.0001 |
|
History of CHF |
3,888 (19.42) |
338 (29.57) |
<0.0001 |
|
History of stroke or TIA |
312 (1.56) |
35 (3.06) |
0.0001 |
|
History of second prior MI |
3,207 (16.02) |
292 (25.55) |
<0.0001 |
|
Multivessel coronary artery disease |
11,821 (59.07) |
736 (64.39) |
0.0004 |
|
Prior angina |
6,097 (30.46) |
458 (40.07) |
<0.0001 |
|
Prior CABG |
827 (4.13) |
148 (12.95) |
<0.0001 |
|
History of PCI with stenting |
16,028 (80.07) |
863 (75.5) |
<0.0001 |
|
ABI ≤0.90 |
0 |
217 (18.99) |
— |
|
Peripheral revascularization |
0 |
389 (34.03) |
— |
|
History of claudication |
0 |
747 (65.35) |
— |
|
Region |
|
|
<0.0001 |
|
North America |
3,669 (18.33) |
238 (20.82) |
|
|
South America |
2,342 (11.7) |
116 (10.15) |
|
|
Western Europe (including South Africa) |
5,819 (29.07) |
317 (27.73) |
|
|
Eastern Europe |
5,867 (29.31) |
423 (37.01) |
|
|
Asia/Australia/New Zealand |
2,320 (11.59) |
49 (4.29) |
|
|
Time from qualifying MI, yrs |
1.7 (1.24–2.33) |
1.7 (1.23–2.35) |
0.762 |
|
Qualifying MI type |
|
|
<0.0001 |
|
Unknown |
1,142 (5.71) |
81 (7.11) |
|
|
STEMI |
10,814 (54.09) |
515 (45.18) |
|
|
NSTEMI |
8,037 (40.2) |
544 (47.72) |
|
|
Qualifying MI ≥2 yrs prior |
7,707 (38.55) |
447 (39.21) |
0.6551 |
|
Time from last dose of P2Y12 inhibitor, days |
152 (16–418) |
86 (6.5–361.5) |
<0.0001 |
|
Aspirin use at baseline |
19,989 (99.86) |
1,142 (99.91) |
0.6414 |
|
Statin use at baseline |
18,537 (92.61) |
1,067 (93.35) |
0.3483 |
|
Beta-blocker use at baseline |
16,541 (82.63) |
944 (82.59) |
0.9688 |
|
ACE-I or ARB use at baseline |
16,093 (80.4) |
936 (81.89) |
0.2155 |
Hiệu quả và tính an toàn của ticagrelor cho biến cố tim mạch chính (MACE) ở những bệnh nhân tiền sử NMCT và bệnh động mạch ngoại biên
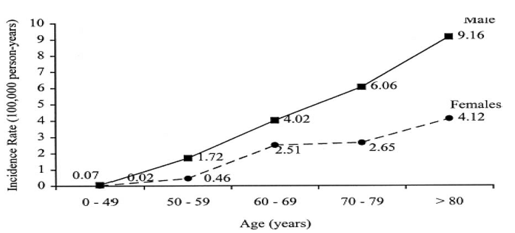
Có đồng nhất trong việc giảm nguy cơ tương đối của ticagrelor cho biến cố tim mạch chính (MACE) ở bệnh nhân có kèm bệnh động mạch ngoại biên tại thời điểm bắt đầu (P tương tác = 0,41). Tuy nhiên, do nguy cơ tuyệt đối của họ cao hơn, bệnh nhân bệnh động mạch ngoại biên (PAD) đã giảm nguy cơ tuyệt đối với số lượng lớn hơn tại thời điểm 3 năm (4,1%; 95% CI: -1,07% đến 9,29%) so với những người không có PAD (1,0%; 95% CI: 0,14% đến 1,9%). Hiệu quả so với giả dược nói chung là tương tự cho 2 liều ticagrelor, nhưng, đáng chú ý, liều 60 mg giảm đáng kể tử vong tim mạch (HR: 0,47; 95% CI: 0,25-0,86; p = 0,014) (bảng 2, hình 1), và cũng giảm tử vong do mọi nguyên nhân (HR: 0,52; 95% CI: 0,32-0,84; p = 0,0074).
Bảng 2. Hiệu quả và an toàn củaTicagrelor ở bệnh nhân bệnh lý động mạch ngoại biên (chụp từ tài liệu gốc)
|
|
Placebo n, % |
Ticagrelor 60 mg n, % |
Ticagrelor 90 mg n, % |
Ticagrelor 60 mg |
Ticagrelor 90 mg |
|---|---|---|---|---|---|
|
Efficacy outcomes, N |
404 |
368 |
371 |
|
|
|
CV death, MI, stroke |
71, 19.3 |
47, 14.1 |
54, 16.3 |
0.69 (0.47–0.99) |
0.81 (0.57–1.15) |
|
CV death |
34, 9.6 |
15, 4.2 |
26, 7.9 |
0.47 (0.25–0.86) |
0.83 (0.50–1.38) |
|
All-cause mortality |
51, 14.0 |
25, 8.2 |
41, 11.7 |
0.52 (0.32–0.84) |
0.88 (0.58–1.32) |
|
Stroke |
17, 4.0 |
8, 2.9 |
10, 3.1 |
0.49 (0.21–1.14) |
0.63 (0.29–1.38) |
|
Ischemic stroke |
16, 3.7 |
8, 2.9 |
7, 2.0 |
0.52 (0.22–1.22) |
0.47 (0.19–1.14) |
|
Safety outcomes, N |
399 |
363 |
368 |
|
|
|
TIMI major |
4, 1.6 |
4, 1.6 |
5, 1.8 |
1.18 (0.29–4.70) |
1.46 (0.39–5.43) |
|
TIMI major or minor |
6, 2.2 |
7, 3.2 |
8, 3.1 |
1.36 (0.46–4.05) |
1.57 (0.54–4.53) |
|
ICH or fatal bleeding |
3, 1.3 |
0, — |
1, 0.4 |
— |
0.39 (0.04–3.75) |
Ticagrelor làm tăng tỷ lệ chảy máu nặng theo TIMI ở cả nhóm bệnh nhân có PAD (pooled doses HR: 1.32; 95% CI: 0.41 to 4.29) và không có PAD (HR: 2.59; 95% CI: 1.91 to 3.52; p interaction = 0.28). Mặc dù bệnh nhân có PAD trong nhóm giả dược có nguy cơ xuất huyết tuyệt đối cao hơn, gia tăng nguy cơ xuất huyết tuyệt đối của ticagrelor sau 3 năm tương đối thấp hơn ở những bệnh nhân có PAD (0.12%; 95% CI: −1.79% to 2.04%) so với nhóm bệnh nhận không có PAD (1.46%; 95% CI: 1.01% to 1.91%). Tỷ lệ xuất huyết nội sọ và xuất huyết gây tử vong thấp hơn ở nhóm bệnh nhân có PAD.
MALE (Các biến cố bất lợi chính ở chi) với ticagrelor
Nhìn chung, ticagrelor giảm MALE (HR: 0,65; 95% CI: 0,44-0,95; p = 0,026), giảm nguy cơ tương đốilớn hơnở liều 90 mg (HR: 0,49; 95% CI: 0,30 0,81; p = 0,005) so với liều 60 mg (HR: 0,81; 95% CI: 0,53-1,24; p = 0,33) (Bảng 3). Hiệu quả này là phù hợp đối với việc giảm nguy cơ thiếu máu cấp ở chi (ALI) (HR: 0,56; 95% CI: 0,23-1,37) và tái thông mạch máu ngoại vi do thiếu máu cục bộ chi (HR: 0,63; 95% CI: 0,43-0,93). Kết quả tương tự ở phân nhóm các bệnh nhân có tiền sử bệnh lý động mạch ngoại biên cũng như khi phẫu thuật đoạn chi do bất kỳ nguyên do nào.
Bảng 3. Hiệu quả trên mạch máu chi của Ticagrelor (chụp từ tài liệu gốc)
|
|
Placebo |
Ticagrelor 60 mg |
Ticagrelor 90 mg |
Ticagrelor 60 mg |
Ticagrelor 90 mg |
|---|---|---|---|---|---|
|
Acute limb ischemia or peripheral revascularization for ischemia |
47, 0.71 |
38, 0.60 |
23, 0.32 |
0.81 (0.53–1.24) |
0.49 (0.30–0.81) |
|
Acute limb ischemia |
9, 0.13 |
6, 0.11 |
4, 0.06 |
0.67 (0.24–1.87) |
0.45 (0.14–1.45) |
|
Peripheral revascularization for ischemia |
46, 0.70 |
37, 0.59 |
21, 0.29 |
0.80 (0.52–1.24) |
0.46 (0.27–0.76) |
|
Peripheral revascularization |
60, 0.94 |
46, 0.74 |
38, 0.55 |
0.77 (0.52–1.13) |
0.63 (0.42–0.95) |
BÀN LUẬN
Nghiên cứu này chứng minh rằng bệnh nhân ngoại trú với tình trạng ổn định có tiền sử NMCT có kèm PAD có thể gặp nguy cơ gia tăng đáng kể các biến cố thiếu máu cục bộ hệ thống, thiếu máu cục bộ chi, chảy máu và tử vong do mọi nguyên nhân. Ngoài ra, lợi ích của ticagrelor cho việc giảm nguy cơ tương đối của MACE là đồng nhất, bất kể có hay không có PAD; tuy nhiên, do bản chất nguy cơ rất cao, các bệnh nhân PAD có thể giảm được nguy cơ tuyệt đối đặc biệt cao (Minh họa trung tâm). Cuối cùng, sự kết hợp của aspirin và ticagrelor giảm MALE so với aspirin đơn trị liệu.
Mối liên hệ giữa PAD với gia tăng nguy cơ MACE ở những bệnh nhân vốn đã có nguy cơ cao do có tiền sử PAD là tương đối phức tạp. Có thể lý giải là do có bệnh trong hơn 1 giường mạch máudẫn đến tình trạng nặng hơn của bệnh mạch máu xơ vữa động mạch. Ngoài ra, PAD có thể kết hợp với các yếu tố nguy cơ xơ vữa huyết khối khác như tuổi, rối loạn chức năng thận, tiểu đường, và hút thuốc. Tuy nhiên, sau khi điều chỉnh những khác biệt cơ bản, PAD vẫn là một dấu hiệu mạnh về nguy cơ thiếu máu cục bộ hệ thống. Bất kể PAD có là dấu hiệu của bệnh chứng mạch máu khác nghiêm trọng hơn hay không, một tổ hợp nhiều yếu tố nguy cơ bất lợi, hoặc cả hai, trong thực tế lâm sàng nó vẫn là một chỉ điểm dễ nhận biết và có độ mạnh cao cho các nguy cơ trong tương lai.Trong nghiên cứu này, tầm quan trọng của MACE cùng với đau cách hồitương tự với tiền sử tái thông mạch máu ngoại vi, sẽ là các chỉ số lâm sàng của PAD. Những phát hiện này nhấn mạnh tầm quan trọng của việc phải xác định PAD đồng mắc khi thăm khám để thông báo cho bệnh nhân những rủi ro trong tương lai của cả MACE và MALE.
MINH HỌA TRUNG TÂM: Ticagrelor với bệnh nhân có bệnh lý động mạch ngoại biên và tiền sử NMCT tại thời điểm 3 năm(chụp từ tài liệu gốc)
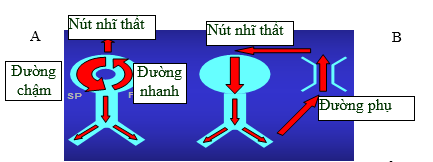
Việc xác định nguy cơ MACE cao là đặc biệt hữu ích khiđưa ra quyết địnhlâm sàng. Nghiên cứu PEGASUS-TIMI 54 chứng minh rằng ticagrelor có hiệu quả trong việc giảm MACE ở những bệnh nhân bị NMCT trước đó. Tuy nhiên, nhu cầu cân bằng giữa hiệu quả trên thiếu máu cục bộ và nguy cơ chảy máu đã tiền đề để khảo sát các phân nhóm trong đó ticagrelor có hiệu quả đặc biệt mạnh mẽ. Trong phân tích này, chúng tôi chứng minh rằng sự hiện diện của PAD không làm thay đổi hiệu quả tương đối của ticagrelor. Tuy nhiên, do nguy cơ MACE cao hơn gấp 2 lần, bệnh nhân PAD sẽ được hưởng lợi khi giảm nguy cơ tuyệt đối mạnh mẽ đến 4.1% trong 3 năm, giảm số trường hợp cần điều trị (NNT) đến 25 bệnh nhân (NNT hằng năm = 74). Mặc dù mỗi liều đã được thử nghiệm một cách độc lập so với giả dược, và không có sự tương tác chính thức giữa nào về hiệu quả của các liềucũng như tình trạng PAD ban đầu, lợi ích rõ ràng nhất là ở liều 60 mg, giảm nguy cơ tuyệt đối 5.2% với MACE và 20 cho NNT (NNThàng năm = 58), cũng như giảm đáng kể tỷ lệ tử vong do tim mạch và tỷ lệ tử vong do mọi nguyên nhân. Đồng thời, tỷ lệ chảy máu với ticagrelor là tương đương nhau ở các bệnh nhân có và không có PAD. Do đó, sự hiện diện của PAD có thể hữu ích cho các bác sĩ trong việc xác định bệnh nhân bị NMCT trước đó vì họ có thể được hưởng lợi ích mạnh mẽ với ticagrelor.
Ngoài nguy cơ MACE, bệnh nhân PAD trong nghiên cứu PEGASUS-TIMI 54 cũng có nguy cơ MALE cao. Tỷ lệ tái thông mạch máu chi do thiếu máu cục bộ là tương đương với NMCT và nhiều hơn gấp hai lần so với tỷ lệ đột quỵ ở những bệnh nhân PAD. Tiền sử tái thông mạch máu ngoại vi là một yếu tố dự báo của MALE ở bệnh nhân PAD trong phân tích này (11).
Cho đến nay, điều trị kháng tiểu cầu kép với aspirin và clopidogrel đã không cho thấy hiệu quả trong việc giảm các biến cố mạch máu chi ởbệnh nhân với PAD (7). Mặc dù không đủ hiệu lực để trả lời câu hỏi này, nghiên cứu này cho thấy rằng liệu pháp kháng tiểu cầu kép với aspirin và ticagrelor có thểcó hiệu quả trong việc giảm ALI nếu được tiến hành trong nghiên cứu đoàn hệ lớn hơn, và nguy cơ cao hơn. Ngoài ra, việc giảm tiêu chí phụ tái thông mạch máu ngoại vi do thiếu máu cục bộ cũng cho thấy lợi ích giảm huyết khối của ticagrelor trên tuần hoàn chi.
KẾT LUẬN
Ở những bệnh nhân có tiền sử NMCT, bệnh lý động mạch ngoại biên (PAD) đồng mắc có liên quan với tăng nguy cơ biến chứng mạch máu và tỷ lệ tử vong, thậm chí sau khi đã điều trị các bệnh lý đi kèm của họ. Ở những bệnh nhân này, sự kết hợp của ticagrelor và aspirin để phòng ngừa thứ cấp dài hạn dường nhưcó làm giảm nguy cơ thiếu máu cục bộ với việc giảm mạnh nguy cơ tuyệt đối , bao gồm giảm các biến cố tim mạch chính (MACE) và các biến cố mạch máu chi.
Điều trị kéo dài với ticagrelor làm giảm nguy cơ thiếu máu cục bộ và tăng nguy cơ xuất huyết ở bệnh nhân bị NMCT, và trong một phân tích phân nhóm, những người bị bệnh lý động mạch ngoại biêntrên nền thiếu máu cục bộcó lợi ích tuyệt đối lớn hơn những người không có bệnh lý động mạch ngoại biên.
TÀI LIỆU THAM KHẢO
1. D.L. Bhatt, P.G. Steg, E.M. Ohman, for theREACH Registry Investigators,et al.International prevalence, recognition, and treatment of cardiovascular risk factors in outpatients with atherothrombosis. JAMA, 295 (2006), pp. 180–189
2. D.L. Bhatt, K.A. Eagle, E.M. Ohman, for the REACH Registry Investigators,et al.Comparative determinants of 4-year cardiovascular event rates in stable outpatients at risk of or with Atherothrombosis. JAMA, 304 (2010), pp. 1350–1357
3. P.G. Steg, D.L. Bhatt, P.W. Wilson, for the REACH Registry Investigators,et al.One-year cardiovascular event rates in outpatients with atherothrombosis. JAMA, 297 (2007), pp. 1197–1206
4. Antithrombotic Trialists’ Collaboration. Collaborative meta-analysis of randomised trials of antiplatelet therapy for prevention of death, myocardial infarction, and stroke in high risk patients. BMJ, 324 (2002), pp. 71–86
5. CAPRIE Steering Committee. Arandomised, blinded, trial of clopidogrel versus aspirin in patients at risk of ischaemic events (CAPRIE). Lancet, 348 (1996), pp. 1329–1339
6. L. Janzon, D. Bergqvist, J. Boberg,et al.Prevention of myocardial infarction and stroke in patients with intermittent claudication; effects of ticlopidine. Results from STIMS, the Swedish Ticlopidine Multicentre Study. JIntern Med, 227 (1990), pp. 301–308
7. J.J.F. Belch, J. Dormandy, for the CASPAR Writing Committee. Results of the randomized, placebo-controlled clopidogrel and acetylsalicylic acid in bypass surgery for peripheral arterial disease (CASPAR) trial. JVasc Surg, 52 (2010), pp. 825–833 833.e1–2
8. D.L. Bhatt, M.D. Flather, W. Hacke, for the CHARISMA Investigators,et al.Patients with prior myocardial infarction, stroke, or symptomatic peripheral arterial disease in the CHARISMA trial. JAm Coll Cardiol, 49 (2007), pp. 1982–1988
9. P.P. Cacoub, D.L. Bhatt, P.G. Steg, for the CHARISMA Investigators,et al.Patients with peripheral arterial disease in the CHARISMA trial. Eur Heart J, 30 (2009), pp. 192–201
10. G. Magnani, M.P. Bonaca, E. Braunwald,et al.Efficacy and safety of vorapaxar as approved for clinical use in the United States. JAm Heart Assoc, 4 (2015), p. e001505
11. M.P. Bonaca, B.M. Scirica, M.A. Creager,et al.Vorapaxar in patients with peripheral artery disease: results from TRA2°P-TIMI 50. Circulation, 127 (2013), pp. 1522–1529 1529.e1–6
12. M.P. Bonaca, J.A. Gutierrez, M.A. Creager,et al.Acute limb ischemia and outcomes with vorapaxar in patients with peripheral artery disease: results from the Trial to Assess the Effects of Vorapaxar in Preventing Heart Attack and Stroke in Patients With Atherosclerosis–Thrombolysis In Myocardial Infarction 50 (TRA2°P-TIMI 50). Circulation, 133 (2016), pp. 997–1005
13. D.L. Bhatt, E.D. Peterson, R.A. Harrington, CRUSADE Investigators,et al.Prior polyvascular disease: risk factor for adverse ischaemic outcomes in acute coronary syndromes. Eur Heart J, 30 (2009), pp. 1195–1202
14. Warfarin Antiplatelet Vascular Evaluation Trial Investigators. Oral anticoagulant and antiplatelet therapy and peripheral arterial disease. NEngl J Med, 357 (2007), pp. 217–227
15. M.P. Bonaca, D.L. Bhatt, E. Braunwald,et al.Design and rationale for the Prevention of Cardiovascular Events in Patients With Prior Heart Attack Using Ticagrelor Compared to Placebo on a Background of Aspirin–Thrombolysis In Myocardial Infarction 54 (PEGASUS-TIMI 54) trial. Am Heart J, 167 (2014), pp. 437–444.e5
16. M.P. Bonaca, D.L. Bhatt, M. Cohen, for the PEGASUS-TIMI 54 Steering Committee and Investigators,et al.Long-term use of ticagrelor in patients with prior myocardial infarction. NEngl J Med, 372 (2015), pp. 1791–1800







