BS. TRẦN MINH ĐỨC*
BS. CKII. NGUYỄN THANH HIỀN
(*) Khoa Tim Mạch Can thiệp, BV ĐHYD TP. Hồ Chí Minh
Chú thích những từ viết tắt:
BN: Bệnh nhân; HCLK: Hội chứng lão khoa; NC: Nghiên cứu; NCT: Người cao tuổi; ST: Suy tim; THA: Tăng huyết áp.
- Giới thiệu.
Tần suất suy tim (ST) tăng dần theo tuổi, từ 6% ở nhóm 60 đến 79 tuổi và gấp đôi 12% ở nhóm>80 tuổi[1]. Tiên lượng ST ở người cao tuổi (NCT) vẫn còn kém với tỷ lệ tử vong cao trong 5 năm (54.4%), thường là do những nguyên nhân không do tim mạch (54.3%)[1]. Mối tương tác phức tạp giữa suy yếu, các bệnh đồng mắc, hoạt động nhận thức, chức năng, và vấn đề xã hội thúc đẩy kết cục sức khỏe kém ở NCTbị ST bất kể phân suất tống máu. Vai trò và mục tiêu chăm sóc của những yếu tố này là hết sức phù hợp trong việc quản lý bệnh nhân ST.
Suy yếu là một quá trình liên tục, trạng thái trung gian trước khi đi đến sự tàn phế, đặc trưng bởi giảm khả năng đáp ứng với căng thẳng do giảm dự trữ chức năng[2]. Có 2 cách tiếp cận chính trong suy yếu: (1) phương pháp tiếp cận sinh lý được đề xuất bởi Fried và cộng sự năm 2001, dựa trên 5 thang đo trực tiếp và tự đánh giá: sụt cân, kiệt sức, vận tốc dáng đi chậm, lực nắm tay yếu, hoạt động thể chất kém[3]; (2) phương pháp tiếp cận suy yếu được đề xuất bởi Rockwood và cộng sự dựa trên sự tích hợp của những khiếm khuyết bao gồm: hội chứng lão khoa (HCLK), những bệnh đồng mắc bao gồm tình trạng nhận thức hay những bệnh lý tim mạch làm giảm trữ lượng chức năng[4]. Hai cách tiếp cận suy yếu này nhận ra rằng những cá thể ở những thời điểm giảm trữ lượng chức năng khác nhau có lâm sàng và tiên lượng khác nhau. Thật vậy, kiểu suy yếu Fried xác định những cá thể ở thời điểm ban đầu của giảm trữ lượng chức năng, có sự tăng nguy cơ kết cục bất lợi khi có sự hiện diện của stress, và tỷ lệ tử vong trong 2 năm khoảng 10%[3],[5]. BN với thang điểm suy yếu Rockwood cao có tỷ lệ tử vong 2 năm cao, tương tự với BN tàn tật nặng[2], [6].
Bởi vì tính chất phức tạp và đa dạng nhiều mặt của suy yếu, hiểu biết về mối quan hệ giữa ST và suy yếu là mục tiêu quan trong hàng đầu trong quản lý và điều trị BN. Mục tiêu của bài viết này được đề xuất bởi các chuyên gia ST, tim mạch và lão khoa, để làm rõ mối quan hệ giữa ST và suy yếu, nhằm đề xuất phương pháp tầm soát sớm suy yếu bởi các bác sĩ không chuyên ngành lão khoa và lập kế hoạch quản lý suy yếu trên BN ST.
- Tần suất và ảnh hưởng suy yếu lên tiên lượng BN ST.
Ở trại dưỡng lão, tần suất suy yếu ở BN ≥65 tuổi là từ 3-23%[3], [7]. Mặc dù có sự khác biệt tần suất suy yếu ở các NC do khác nhau giữ các thang đo, tuy nhiên, tần suất suy yếu ở BN ST vẫn còn cao[8]. Ví dụ, một khảo sát trong 1727 BN cao tuổi ST theo cách tiếp cận Rockwood, có tới 94% BN có suy yếu đi kèm[9]. Những NC khác sử dụng nhiều công cụ tầm soát trong 487 BN, tần suất là từ 38 % đến 52%[10]. Đối với BN ST nhập viện, tần suất thay đổi từ 56% đến 76% độc lập với chức năng thất trái[11], [12]. Trong những tình huống đặc biệt như những BN có chỉ định cho cấy ghép dụng cụ hỗ trợ thất trái, theo NC của Tse và cộng sự, tần suất là 21% mặc dù dân số BN tương đối trẻ (57.5+/-15.3)[13].
Trên các phân type ở ST, tần suất suy yếu ở BN ST với phân suất tống máu bảo tồn (HFpEF) cao hơn ST với phân suất tống máu giảm (HFrEF), có tới 60% đến 90% BN HFpEF bị suy yếu, đó là do tuổi cao và nhiều bệnh đồng mắc hơn[71], [72]. Ở BN nội trú, tần suất suy yếu thậm chí còn cao hơn (56% đến 76%) và giống nhau giữa HFpEF và HFrEF. Tương tự như vậy, tần suất suy yếu cao hơn ở BN ST tiến triển (50% đến 65%) ở những NC đơn trung tâm nhỏ lẻ[73], [74].
BN ST có suy yếu đi kèm, có nhiều gánh nặng triệu chứng hơn, so với BN không suy yếu, nhóm này có gấp 2 lần triệu chứng khó thở, 75% mất ngủ, trầm cảm[75]. Chất lượng cuộc sống cũng kém có ý nghĩa ở BN suy yếu, bất kể ST cấp hay mạn[76]. Trên kết cục lâm sàng, trong NC đoàn hệ TOPCAT (Treatment of Preserved Cardiac Function Heart Failure with an Aldosterone Antagonist), ở nhóm HFpEF có chỉ số suy yếu cao (Frailty Index) có tỷ lệ nhập viện và tử vong cao hơn so với nhóm không suy yếu[61].
Giá trị tiên lượng của suy yếu cũng được chứng minh ở nhóm đợt cấp mất bù của ST. Volpato và cộng sự[77] cho rằng ở nhóm BN này, thang điểm SPPB (Short Physical Performance Battery) thấp kết hợp với thời gian nằm viện dài hơn, gánh nặng tàn tật lên các hoạt động cơ bản hằng ngày, tái nhập viện và tử vong[78]. Cùng với đó, đánh giá suy yếu có thể xác định BNST có yếu tố nguy cơ cao tàn tật và kết cục lâm sàng bất lợi ở mỗi thời điểm biểu hiện bệnh, từ đó đề xuất can thiệp nhằm cải thiện gánh nặng suy yếu và kết cục.
Mặc dù thiếu tiêu chuẩn định nghĩa và phương pháp đo (tiêu chuẩn Fried, Rockwood), những NC này đều cho rằng có mối quan hệ mạnh mẽ giữa suy yếu và tỷ lệ tử vong cao, nhập viện và suy giảm chức năng ở BNST.
- Cơ chế sinh lý học nền tảng của suy yếu trên BN ST[87].
Gánh nặng suy yếu trên BN ST thường là sự phối hợp của rối loạn chức năng nhiều hệ thống, bao gồm đáp ứng viêm, gánh nặng bệnh đồng mắc, tuổi già, bất thường hệ thống cơ xương. ST mạn thúc đẩy lão hóa kết hợp với sự suy giảm khối cơ, với sự bảo tồn và tích lũy khối mỡ, đưa đến tình trạng béo phì giảm cơ. ST mạn cũng thúc đẩy bất thường khối cơ (tích tụ mô mỡ gian cơ, thay đổi sợi cơ, giảm mật độ mao mạch), thúc đẩy làm giảm chức năng ty thể ở hệ thống cơ xương, giảm khả năng gắng sức, suy yếu thể chất. Hệ quả là đưa đến tình trạng tiền viêm, suy giảm chuyển hóa, và đề kháng insulin.
Bệnh đồng mắc thường gặp ở NCT mắc ST mạn, thúc đẩy tình trạng tiền viêm, đề kháng insulin, làm tiến triển bất lợi thành phần, kích thước, chức năng của cơ. Hơn thế nữa, những bất thường huyết động kết hợp với ST đưa đến tình trạng giảm oxy mô, chết tế bào, và viêm. Sung huyết mạn tính, quá tải thể tích tuần hoàn, giảm tưới máu mô có thể thúc đẩy thiếu máu nuôi ruột, sự di chuyển của vi khuẩn vào hệ thống tuần hoàn, điều hòa hướng lên đáp ứng viêm toàn thân, cùng với đó là con đường đáp ứng thần kinh thể dịch bị thay đổi cũng góp phần thúc đẩy tiền viêm, đưa đến suy giảm chuyển hóa, thay đổi cấu trúc và chức năng của hệ thống nhiều cơ quan, làm giảm trữ lượng sinh lý và tăng tính dễ nhạy cảm.
- Mối liên quan giữa suy yếu và ST.
Mối liên quan giữa suy yếu và ST còn chưa hiểu biết đầy đủ. Về một phương diện, ST mạn là yếu tố thúc đẩy suy yếu. ST là một trong những bệnh đồng mắc trong mô hình của Rockwood[4]. Thêm vào đó, suy yếu có thể thúc đẩy hoặc bắt đầu cho việc suy giảm nhận thức[24]. Mặc khác, BN suy yếu thường giảm khà năng đáp ứng với stress như trong ST cấp, khả năng chức năng tối đa giảm dưới ngưỡng đòi hỏi cho tình trạng stress cấp tính, tuy nhiên có thể đảo ngược lại khi phục hồi.
Có một mối quan hệ chặt chẽ giữa suy yếu và ST, và dường như việc tầm soát suy yếu trên BNST để tối ưu hóa quản lý ST, giúp tránh những đợt mất bù cấp, tránh tình trạng suy giảm chức năng có thể thúc đẩy tàn tật. Hơn nữa, lợi ích của việc can thiệp có thể làm giảm sự ảnh hưởng của suy yếu[25] (hình 1 và bảng 1).
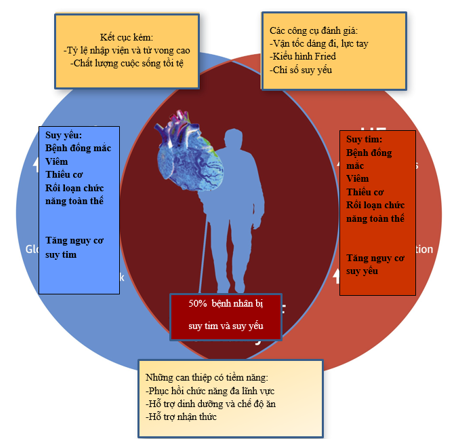
Hình 1: Mối liên quan giữa suy yếu và ST[87].
Bảng 1. Những NC được công bố về ảnh hưởng của suy yếu lên BN ST, từ 2018 đến 5/2021
| Tác giả | NC | Dân số NC | N | Những đặc điểm dân số NC | Kết cục | Thời gian theo dõi | HR hoặc OR (95% CI) P-value |
| Zheng, 2021[16] | NC đoàn hệ tiến cứu | BN nhập viện với ST cấp | 443 | Tuổi trung bình: 76.1, 50.8% là nam | Cộng gộp: tử vong và tái nhập viện | 6 tháng | HR = 1.78 (1.02–3.10) P = 0.041 |
| Weng, 2021[17] | NC đoàn hê hồi cứu | BN cao tuổi ở khoa Lão | 811 | Tuổi trung bình ở BNST: 82.7
73.5% là nam |
Tử vong | Thời gian theo dõi trung vị 3.2 năm | HR = 1.05 (1.0004–1.10) P <0.05 |
| Kohsaka, 2020[19] | NC đoàn hê hồi cứu | Cựu chiến binh bị ST | 163085 | Tuổi trung bình ở BN suy yếu: 77
97.2% là nam |
Cộng gộp: tử vong và tái nhập viện | 2 năm | OR = 1.71, (1.65–1.77) |
| Matsue, 2020[18] | NCđoàn hệ tiến cứu | BN nhập viện với ST cấp | 1180 | Tuổi trung bình: 55
57.4% là nam |
Cộng gộp: tử vong và tái nhập viện | 1 năm | HR = 2.04 (1.28–3.24) P = 0.003 |
| Dewan, 2020[20] | NC đoàn hệ tiến cứu | HF-rEF(PARADIGM) | 13265 | Tuổi trung bình: 65
22.2% là nữ |
Cộng gộp: tử vong và tái nhập viện | 26.6 tháng | HR = 1.71 (1.56–1.88) P <0.00 |
| Kwok, 2020[15] | NC đoàn hê hồi cứu | BN nhập viện với ST cấp | 11626400 | Tử vong nội viện | OR = 3,05 (2,57-3,62) P <0,00 |
||
| Newton, 2019[21] | NC đoàn hệ tiến cứu | BN nhập viện với ST cấp | 811 | Tuổi trung bình: 77 | Tử vong | 1 năm | HR = 1.98 (1.18–3.30) P <0.01 |
| McAlister, 2019[22] | NC đoàn hê hồi cứu | BN nhập viện với ST cấp | 26626 | Tuổi trung bình: 77.4 | Tử vong | 30 và 90 ngày | P <0.01 |
| Bottle, 2019[23] | NC đoàn hê hồi cứu | Chăm sóc tích cực | 6360 | 82% >65 tuổi
44.5% là nữ |
Nhập viện lần đầu | 1 năm | HR = 2.57 (1.69–3.90) P <0.001 |
| Yang, 2018[14] | Phân tích meta-analysis | BN nhập viện với ST cấp | 2645 | Tử vong | Thời gian theo dõi trung vị: 1.8 năm | HR = 1.54 (1.34–1.75) P <0.0 |
Hình 2. (A) Sơ đồ giải thích cơ chế suy yếu trên lão hóa. Khả năng chức năng tối đa (đường xanh da trời) giảm theo tuổi, cũng như trữ lượng chức năng. Suy yếu xảy ra khi khả năng chức năng tối đa giảm dưới ngưỡng đòi hỏi khi có tình trạng stress (mũi tên 2). Ở những người trẻ, khả năng chức năng là đủ để vượt qua stress.Đường cong suy giảm chức năng thay đổi theo cá nhân. Người mà suy giảm chậm biểu hiện lão hóa thành công và không suy yếu (đường xanh lá cây, mũi tên 3).Người có biểu hiện suy giảm nhanh có tốc độ lão hóa nhanh và suy yếu lớn hơn (đường đỏ và mũi tên 1).(B) STcó thể thay đổi khả năng chức năng thông qua việc giảm trữ lượng chức năng và tăng suy yếu (mũi tên 4 và 5). Mối liên quan giữa ST cấp và suy yếu có thể đảo ngược sau sự hồi phục.
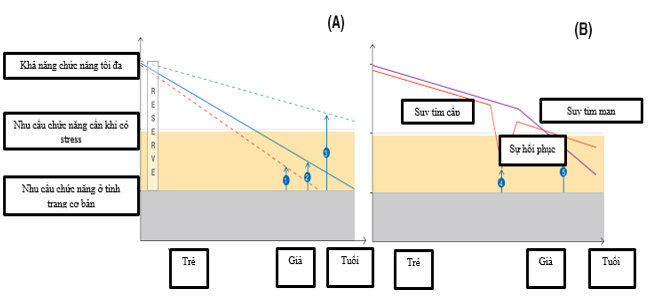
- Lợi ích của quản lý suy yếu.
Những BN có đồng thời ST và suy yếu đòi hỏi tiếp cận quản lý theo từng cá nhân. Bất kể định nghĩa suy yếu (theo kiểu Fried hay Rockwood), điều trị nên tiếp cận một cách đa chiều bao gồm điều trị dùng thuốc và không dùng thuốc (như chăm sóc tâm lý và xã hội).
Vào năm 1995, MW Rich và cộng sự, báo cáo 1 NC tiến cứu ngẫu nhiên về giá trị của sự phối hợp can thiệp đa ngành làm tăng chất lượng cuộc sống, giảm tỷ lệ tái nhập viện trong 90 ngày, giảm toàn bộ chi phí y khoa và tỷ lệ tử vong ở NCT mắc ST[26]. Và từ đó, những NC về việc quản lý suy yếu được công bố.NC phân tích meta-analysis của Chen và cộng sự (bao gồm 7 NC ngẫu nhiên) cho thấy ảnh hưởng tích cực của hoạt động thể chất lên test đi bộ 6 phút nhưng không ảnh hưởng đến tỷ lệ nhập viện và tử vong[27]. Tuy nhiên, NC ngẫu nhiên xác nhận vai trò của can thiệp phối hợp (lời khuyên về chế độ ăn, hỗ trợ tâm lý, phục hồi chức năng) với theo dõi chuyên biệt cho tối ưu hóa quản lý BNST có suy yếu so với điều trị chuẩn[28].
- Hướng dẫn thực hành tầm soát suy yếu ở BN ST
Một chương trình tầm soát không chỉ đơn thuần bao gồm 1 test đơn lẻ mà là một lộ trình để xác định dân số phù hợp cho tầm soát và dừng khi những can thiệp, điều trị và kết cục được báo cáo[1] (hình 2 và bảng 2, 3). Nhóm làm việc ST của hội Tim mạch Pháp, hội Lão Khoa và tích tuổi học Pháp tập trung vào kiểu hình suy yếu dựa trên tích hợp khiếm khuyết bao gồm HCLK, tình trạng bệnh đồng mắc và bệnh tim mạch làm giảm trữ lượng chức năng.
Hình 3. Phối hợp chăm sóc ở BN cao tuổi mắc ST.
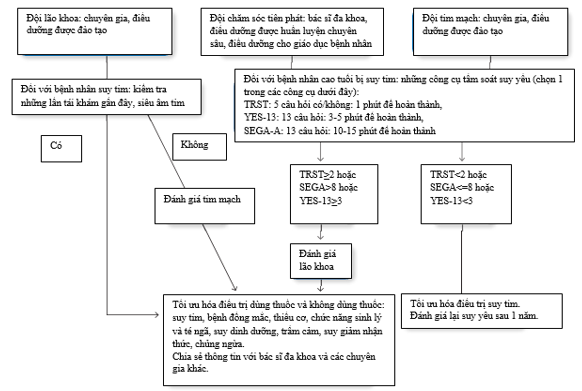
- Ai?
Liên quan đến tần suất cao suy yếu trên NCT mắc ST, bất chấp phân suất tống máu thất trái, ST cấp hay mạn, việc tầm soát và quản lý nên dành cho nhóm ST. Bởi vì tần suất suy yếu tăng với tuổi, có hay không có bệnh đồng mắc, những BN được chọn tầm soát suy yếu nên ≥75 tuổi[32], {33]. Nó dường như không phù hợp cho việc giới hạn dân số mục tiêu theo bệnh đồng mắc vì bản thân suy yếu có thể thứ phát sau ST. Thật vậy, ở BN phẫu thuật tim mạch, điều trị dụng cụ phẫu thuật hoặc không phẫu thuật, việc tầm soát nên được đề ra ở BN ≥65 tuổi hoặc đôi khi trẻ hơn[13]. Tránh việc tầm soát suy yếu ở BN được chăm sóc giảm nhẹ, ST giai đoạn cuối, phụ thuộc hoàn toàn các hoạt động sống cơ bản hằng ngày, chăm sóc cuối đời, không thể hồi phục khi có stress nhỏ.
- Khi nào?
STthường biểu hiện 2 tình huống lâm sàng khác biệt: BN ngoại trú với ST mạn, BN nội trú với ST cấp. Ở mỗi tình huống, việc tầm soát suy yếu là quan trọng, vì suy yếu làm tăng thêm kết cục tồi tệ ở BN ngoại trú và nội trú[14], [19], [23]. ST không ổn định thường đưa đến tái nhập viện thường xuyên với mỗi lần làm tăng suy yếuhơn [34]. Mỗi dụng cụ tầm soát suy yếu thay đổi theo tình huống chăm sóc hay khả năng của BN nội trú. Để có một thông điệp đơn giản nhất, các chuyên gia cần chọn một công cụ tầm soát đơn giản nhất dùng trong các tình huống khác nhau. Công cụ tầm soát không nên cần nhiều thời gian để hoàn thành[10]. Đối với BN nội trú, công cụ tầm soát có thể thực hiện bên ngoài khoa tim mạch hoặc đơn vị chăm sóc tích cực khi ST được thiết lập và tiên lượng được đánh giá. Tuy nhiên, cần thực hiện sớm, trong vòng 48 giờ đầu tiên, để đưa ra kế hoạch chăm sóc cho từng cá nhân trong và sau thời gian nằm viện, phụ thuộc vào nguồn nhân lực tại chỗ. Công cụ có thể thực hiện sau khi xuất viện bởi các chuyên gia tim mạch, bác sĩ nội trú, sinh viên y khoa hoặc điều dưỡng đã được đào tạo, bất kể thời gian trong quá trình theo dõi[35], [36], [37].
- Bằng cách nào?
Suy yếu được định nghĩa là tình trạng tích lũy những suy giảm bao gồm HCLK và bệnh đồng mắc, có thể được đánh giá bằng phương pháp lão khoa toàn diện. Các phương tiện đánh giá suy yếu: tiêu chuẩn Fried[3] hay thang điểm suy yếu lâm sàng Rockwood[4] cần nhiều thời gian và công cụ chuyên biệt, do đó cần một phương tiện để tầm soát thay vì để đánh giá. Nhiều phương pháp để tầm soát suy yếu trong dân số chung như: thang đo suy yếu lâm sàng, kiểu hình suy yếu, SHARE-FI, FRAIL… cũng như các thang đo đánh giá lão khoa như Short Emergency Geriactric Assesement (SEGA), Vulnerable Elders Survey-13 (VES-13) hay Triage Risk Screening Tool (TRST)[10], [35], [38].
Trong một bài đánh giá hệ thống vào năm 2018 bao gồm 20 NC, Mc Donagh J và cộng sự phân tích 8 công cụ tầm soát và đánh giá suy yếu ở BNST. Ngay cả khi suy yếu là một yếu tố tiên lượng quan trọng ở BN ST và cần tiến cận điều trị một cách tích cực hơn, những công cụ tầm soát này không có giá trị đầy đủ ở những BN này[35]. ỞNC khác theo dõi BNST, thanh điểm suy yếu lâm sàng Clinical Frailty Scale (CSF) có tương quan cao với những công cụ đánh giá[10]. Cần có những NC để xác định liệu những công cụ tầm soát suy yếu đơn giản có giá trị tiên lượng so với đánh giá suy yếu toàn diện ở BNST. Hội ST châu Âu của hội tim mạch châu Âu đề xuất 4 trụ cột chính (lâm sàng, nhận thức-tâm thần, chức năng và xã hội)[39].
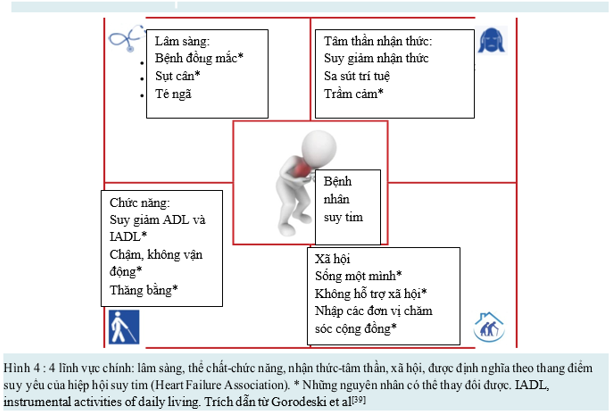
VES-13 (Vulnerable Elders Survey-13) là bộ 13 câu hỏi được phát triển ở Mỹ năm 2001[40], có thể phỏng vấn trực tiếp hoặc qua điện thoại trong vài phút bởi các nhà lâm sàng hoặc không phải lâm sàng. Công cụ có thể đánh giá ở BN ngoại trú và nội trú[41], [42].
SEGA-A (Short Emergency Geriactric Assesement) được đề xuất năm 2004 để đánh giá sớm HCLK trong khoa cấp cứu[43], [44]. Công cụ này có thuận lợi là có giá trị lớn (ngoại trú, nội trú, khoa cấp cứu), đơn giản và có thể lặp lại, nó tốn 5 phút để hoàn thành ngay cả với người không phải là bác sĩ[45].
TRST (Triage Risk Screening) là công cụ được phát triển ở khoa cấp cứu ở Cleveland năm 2003[46].Nó dự đoán tỷ lệ tái nhập viện và biến cố bất lợi, nhanh chóng, và cũng như SEGA-A và VES-13, nó có thể đánh giá lão khoa.
Giá trị dự đoán của các thang điểm để xác định NCT tăng nguy cơ suy giảm chức năng, nhập viện và tử vong được tóm tắt ở bảng 2.
Bảng 2. Những chi tiết và giá trị dự đoán của các công cụ tầm soát suy yếu: TRST, SEGA-A, VES-13
| SEGA-A | VES-13 | TRST | |
| Loại công cụ | Đánh giá BN | Bộ câu hỏi cho BN và người chăm sóc (phỏng vấn trực tiếp hay qua điện thoại) | Đánh giá BN |
| Thời gian (phút) | 10 | 3-5 | 1-5 |
| Số mục | 13 | 13 | 5 |
| Loại mục | Tuổi | Tuổi | Tiền căn hoặc có bằng chứng suy giảm nhận thức |
| Các thuốc | Cảm nhận bản thân về sức khỏe | Nhập viện gần đây hoặc cấp cứu | |
| Tâm trạng | Sự khó khăn khi thực hiện 6 hoạt động sinh lý | Rối loạn dáng đi hoặc té ngã | |
| Cảm nhận bản thân về sức khỏe | Sự giới hạn cho 5 hoạt động sống hằng ngày do vấn đề sức khỏe | Phụ thuộc các hoạt động sống hằng ngày, được thực hiện bởi điều dưỡng, ngược đãi người già, tài sản, không tuân thủ dùng thuốc | |
| Té ngã | |||
| Tình trạng dinh dưỡng | |||
| Bệnh đồng mắc | |||
| Tình dục | |||
| Cần giúp đỡ cho hoạt động hằng ngày | |||
| Chức năng nhận thức | |||
| Chấm điểm cho các mục và ngưỡng của thang đo | 3 mức độ
Ngưỡng>8 |
2-3 mức độ
Ngưỡng≥3 |
2 mức độ
Ngưỡng≥2 |
| Ngữ cảnh áp dụng | Cấp cứu, nằm viện | NCT ở nhà chăm sóc cộng đồng, nhập viện, phẫu thuật, BN mắc ung thư, cấp cứu, BN nằm khoa tim mạch | Cấp cứu, nằm viện |
| Giá trị tiên đoán (độ nhạy, độ đặc hiệu) cho | |||
| Tử vong | Có[45] | Có (nhạy: 87%, đặc hiệu: 47%)[42] | Có |
| Nhập nhà dưỡng lão | Có | Có (nhạy: 92%, đặc hiệu: 50%)[42] | Không |
| Nhập viện | Có | Không | Có (nhạy: 83%, đặc hiệu: 32%)[48] |
| Suy giảm chức năng | Có | Có (nhạy: 91%, đặc hiệu: 50%)[42] | Có (nhạy: 66%, đặc hiệu: 47%)[48] |
| Giá trị | Dự đoán nhiều kết cục | Có giá trị trong nhiều tình huống khác nhau
Công cụ tầm soát nhanh |
5 câu hỏi đơn giản
Công cụ tầm soát ngắn |
| Giới hạn | Đòi hỏi thời gian dài để hoàn thành | Không biết độ nhạy và độ đặc hiệu trong dự đoán nguy cơ nhập viện | Không biết độ nhạy và độ đặc hiệu trong dự đoán nguy cơn nhập nhà chăm sóc cộng đồng |
Chú thích: TRST: Triage Risk Screening Tool , SEGA: Short Emergency Geriactric Assesement,VES-13: Vulnerable Elders Survey-13 (VES-13)
- Sau tầm soát?
Sau khi tầm soát có suy yếu, cần thống nhất lộ trình chăm sóc và quản lý giữa chuyên gia tim mạch, các nhà lão khoa và các bác sĩ thực hành liên quan, mục đích là để đánh giá tim mạch-lão khoa toàn diện, đa yếu tố. Nếu BN không có suy yếu, đánh giá lại sau 1 năm.
- Hướng dẫn quản lý suy yếu ở BN ST.
Mục tiêu của sự phối hợp lão khoa và tim mạch là để tích hợp nhiều con đường chăm sóc làm giảm tỷ lệ tử vong, nhập viện và tái nhập viện ở BNST, cải thiện chất lượng cuộc sống và tình trạng chức năng ở BNST. Nó bao gồm cả tối ưu hóa điều trị thuốc và kế hoạch chăm sóc toàn diện[49], [50].
- Tối ưu hóa điều trị bằng thuốc và dụng cụ không phẫu thuật.
Điều trị ST dự trên khuyến cáo của hội tim châu Âu (European Society of Cardiology-ESC) trong việc chẩn đoán và điều trị ST cấp và mạn[29]. Đầu tiên, thật cần thiết cho BN cao tuổi được đánh giá bởi chuyên gia tim mạch với một bản siêu âm tim khi các bác sĩ đa khoa nghi ngờ có ST. Siêu âm tim là phương pháp được chọn để đánh giá chức năng tâm thu và tâm trương, và tìm kiếm các chẩn đoán phân biệt (bệnh van tim, bệnh cơ tim amyloidosis), mà điều trị chúng tùy vào chẩn đoán. Ở phương diện lão khoa, có gần 50% NCT mắc ST không được siêu âm tim tối thiểu một lần hoặc không biết chức năng tống máu thất trái (left ejection ventricular function-LVEF)[51]. Sự phân biêt giữa các BN có ST dự trên LVEF rất quan trọng do nguyên nhân gây bệnh, bệnh đồng mắc, đáp ứng điều trị (hướng dẫn ESC). Thứ hai, khuyến cáo điều trị dựa trên HFrEF cải thiện chức năng sống, giảm tử vong, nhập viện đột xuất. Việc bắt đầu điều trị hoặc và điều chỉnh liều thuốc (ức chế men chuyển (ACE inbihitors), chẹn beta giao cảm (beta-blockers), chẹn thụ thể angiotensin (angiotensin receptor blockers (ARBs), đối kháng thụ thể mineralocorticoid (MRAs), ức chế neprilysin thụ thể angiotensin (ARNI), ức chế kênh đồng vận chuyển natri-glucose (sodium glucose co transporter 2 inbitors-SGLT2i) có thể là thách thức đối với NCT bị suy yếu do nhiều lý do: yếu tố nguy cơ tác dụng phụ tăng theo bệnh đồng mắc (ví dụ suy thận), đa thuốc, tương tác thuốc, lợi ích đạt được và thời gian để đánh giá thì rất phức tạp do NCT bị loại trừ khỏi các NC gốc[52]. Do đó, cân bằng lợi ích, nguy cơ đôi khi khó đánh giá. Những công cụ giúp nhà lâm sàng đánh giá lại những thuốc phù hợp và có khả năng không phù hợp như STOPP và START[30]. Tuy nhiên, những NC ngẫu nhiên và NC quan sát lớn cho thấy những lợi ích của các thuốc này, bất chấp độ tuổi[53-58]. Gần đây, một đồng thuận của các nhà lão khoa và tích tuổi học Pháp nhấn mạnh quản lý BN rất cao tuổi bị ST có thể cải thiện bằng tối ưu hóa thuốc điều trị ST, đặc biệt HFrEF[59]. Bởi vì vấn đề điều trị dưới ngưỡng hoặc hạn chế kê toa các thuốc điều trị có thể làm tồi tệ tình trạng ST, cần thiết phải có sự thống nhất giữa các bác sĩ đa khoa, chuyên gia tim mạch và lão khoa. Tương tự vậy, điều trị dụng cụ không phẫu thuật như điều trị tái đồng bộ tim có thể cải thiện tiên lượng và chất lượng cuộc sống ở BN cao tuổi bị HFrEF, nhưng lợi ích ít rõ ràng hơn BN suy yếu[60]. Cuối cùng, đặc biệt BN có HFpEF, điều trị lợi tiểu có thể là thách thức trong phòng ngừa biến cố hội chứng tim thận.
Trong mọi tình huống, tối ưu hóa điều trị bệnh đồng mắc làm giảm nguy cơ ST mất bù và suy yếu. Khiếm khuyết sắt và vitamin D cần được đánh giá nhằm hiệu chỉnh bằng cách truyền sắt tĩnh mạch hoặc vitamin D uống[29], [31]. Cuối cùng, việc chủng ngừa cúm, phế cầu và SARS-CoV-2 cũng cần thiết do BN.
- Tối ưu hóa toàn diện BN với trung tâm là sinh học-tâm thần-xã hội dựa trên phối hợp lộ trình chăm sóc.
Điều trị không dùng thuốc là cần thiết đối với BN cao tuổi mắc ST. ỞBN ST với phân suất tống máu bảo tồn, tập thể dục tăng sức bền, như đạp xe đạp hoặc chạy bộ, có thể cải thiện khả năng gắng sức[61]. Tập thể dục nhịp điệu phối hợp sức bền có hiệu quả làm ngăn chặn thiếu cơ. Đối với NCT, chương trình tập thể dục bao gồm nhịp điệu, lực tay, thăng bằng là phương pháp hiệu quả nhất là tăng khối và lực cơ, giảm té ngã, cải thiện chất lượng cuộc sống[62]. Sử dụng các trò chơi trong tập thể dục cho những BN không thích phương pháp truyền thống[63]. Sự phối hợp giữa thể dục và dinh dưỡng là môt trong những phương pháp có giá trị quản lý thành phần sinh lý của suy yếu.Ở BNST, nhu cầu dinh dưỡng bị hạn chế do cảm giác no sớm, giảm cảm giác mùi và vị, bệnh đồng mắc như trầm cảm, chế độ hạn chế tùy theo bệnh. Và kết quả là, BN STlàm tăng nguy cơ khiếm khuyết và rối loạn dinh dưỡng. Không cung cấp đủ năng lượng làm cho chất lượng cuộc sống sau ra viện nghèo nàn và làm tăng gánh nặng cho tái nhập viện[64]. Sự thay đổi chế độ ăn, bao gồm những lời khuyên về dinh dưỡng, các chế phẩm giàu protein, cùng với tập thể dục nhằm cải thiện chất lượng cuộc sống của NCT[65]. Trong NC PICNIC và GOURTMET (Geriactric Out-of-Hospital Randomized Meal Trial in Heart Failure), chương trình can thiệp dinh dưỡng 6 tháng, cho thấy những lời khuyên tối ưu hóa dinh dưỡng làm giảm có ý nghĩa tử vong và tái nhập viện 1 năm[84], [85].Ở trong một tình huống khác, NC Kitzman và cộng sự trên BN HFpEF bị béo phì, giới hạn caloric và giảm cân góp phần cải thiện khả năng gắng sức, chất lượng cuộc sống, thành phần cơ thể và đáp ứng viêm hệ thống[86].
Bảng 3. Hiệu quả của những can thiệp để cải thiện chất lượng cuộc sống, hoạt động thể chất và khả năng gắng sức trên NCT mắc ST
| Thiết kế | Những chi tiết về can thiệp | Nhóm so sánh | Chất lượng cuộc sống | Chức năng thể chất, khả năng gắng sức | |
| Can thiệp dinh dưỡng[85] | RCT | DASH+ chế độ ăn giới hạn muối sau ra viện ở BNST (tuổi trung bình: 71 tuổi) | Chăm sóc thông thường | Cải thiện không có ý nghĩa thống kê thang điểm lâm sàng KCCQ | Không đánh giá |
| Giảm cân+ tập thể dục[86] | RCT (thử nghiệm thiết kế lũy thừa trong can thiệp dinh dưỡng và chế độ ăn) | Giảm caloric 400 kcal/ngày ở BNST EF bảo tồn (tuổi trung bình: 66 tuổi), 1 giờ theo dõi tập thể dục có giám sát, 3 lần/ 1 tuần trong 20 tuần | Chế độ ăn và hoặc tập thể dục, so với chăm sóc thông thường | Cải thiện chất lượng cuộc sống theo KCCQ và SF-36 theo can thiệp chế độ ăn | Cải thiện chất lượng cuộc sống ở cả cab thiệp chế độ ăn (V02 đỉnh+0.7MET) và tập thể dục (V02 đỉnh+0.8MET) |
| Phục hồi chức năng đa lĩnh vực[79] | RCT mở đầu | Can thiệp phục hồi chức năng thể chất đa lĩnh vực bắt đầu BN nhập viện với ST mất bù cấp (tuổi trung bình: 72) | Chăm sóc thông thường | Cải thiện chất lượng cuộc sống theo thang điểm KCCQ | Xu hướng cải thiện khả năng thực hiện SPPB (+1.1U) và test đi bộ 6 phút (+23m) |
| Đào tạo tập thể dục có giám sát[82] | Phân tích meta-analysis | Thể dục cường độ trung bình có theo dõi sát ở BN HFpEF mạn | Chăm sóc thông thường | Cải thiện chất lượng cuộc sống theo thanh điểm MLWHF | Cải thiện khả năng gắng sức (V02 đỉnh+ 0.8 MET) |
| Đào tạo tập thể dục tại nhà[83] | Phân tích meta-analysis | Đi bộ cường độ nhẹ đến vừa (40-75% tần số tim tối đa), thể dục liên tục, đào tạo sức bền | Chăm sóc thông thường | Cải thiện chất lượng cuộc sống | Cải thiện khả năng gắng sức (V02 đỉnh+ 1 MET) |
| Các tác nhân kháng viêm (IL-1)[80], [81] | RCT | Anakinra ở BN HFpEF (45-46 tuổi) và HFrEF (49-68 tuổi) | Chăm sóc thông thường | Không cải thiện chất lượng cuộc sống (theo thang điểm DASI và MLWHF) | Không cải thiện V02 đỉnh |
Chú giải: 6MWD:6-min walk distance: khoảng cách đi bộ 6 phút; ADHF: acute decompensated heart failure: ST mất bù cấp; DASH: Dietary Approaches to Stop Hypertension: những tiếp cận chế độ ăn để ngưng THA; DASI:Duke Activity Status Index: chỉ số tình trạng hoạt động Duke; HF: heart failure: ST; HFpEF: heart failurewith preserved ejection fraction: ST với phân suất tống máu bảo tồn; HFrEF: heart failure with reduced ejection fraction: ST với phân suất tống máu giảm; I:interlukin; KCCQ: Kansas City Cardiomyopathy Questionnaire: bộ câu hỏi bệnh cơ tim thành phố Kansas; MET:Metabolic equivalents: đương lượng chuyển hóa; MLWHF: Minnesota Living With Heart Failure; QOL: quality of life: chất lượng cuộc sống; peak VO2: peak exercise oxygen uptake: tiêu thụ oxy gắng sức đỉnh; RCT: randomized controlled trial: thử nghiệm ngẫu nhiên có đối chứng; SF-36: 36-item Short-Form Health Survey: khảo sát sức khỏe dạng ngắn 36 mục.
Cùng lúc đó, xác định HCLK là cần thiết nhằm có kế hoạch chăm sóc tối ưu, dựa trên thiếu cơ, suy dinh dưỡng, suy giảm chức năng sinh lý, trầm cảm, suy giảm nhận thức và chăm sóc xã hội[65]. Với mỗi bước tiếp cận được tóm lược ở bảng 3. Mỗi thành phần có liên quan với nhau, do đó phải tích hợp và đưa BN làm trung tâm.
Hơn thế nữa, ngay cả khi BNSTchưa suy yếu, việc ngăn chặn là cần thiết bởi vì mối liên quan giữa chúng. Các can thiệp được đề xuất nhằm ngăn chặn tình trạng suy giảm nhận thức được đề xuất ở bảng 4.
Bảng 4. Phòng chống tiên phát suy yếu và tối ưu hóa chăm sóc HCLK ở NCT dựa trên : ức chế men chuyển (ACE inbihitors), chẹn beta giao cảm (beta-blockers), chẹn thụ thể angiotensin (angiotensin receptor blockers (ARBs), đối kháng thụ thể mineralocorticoid (MRAs), ức chế neprilysin thụ thể angiotensin (ARNI), ức chế kênh đổng vận chuyển natri-glucose (sodium glucose co transporter 2 inbitors-SGLT2i).
| Phòng ngừa | Điều trị | |
| HFrEF | Điều trị các yếu tố nguy cơ như các bệnh lý tim mạch mạn tính: THA, đái tháo đường, rung nhĩ. | Tối ưu hóa điều trị (ACEi hoặc ARNI, BB, MRA, SGLT2i).[29]
Chuyển đến trung tâm có điều trị tái đồng bộ tim nếu có chỉ định. Tối ưu hóa điều trị lợi tiểu theo điều trị bệnh đồng mắc. Chương trình đào tạo tập thể dục, 2-3 lần/tuần. |
| HFpEF | ||
| Bệnh đồng mắc và đa thuốc | Liều điều trị theo độ thanh lọc cầu thận.
Cố gắng sử dụng một thuốc cho điều trị nhiều bệnh.[30] Thông tin BN và người chăm sóc về thuốc kê toa. |
Kiểm tra việc quản lý bệnh đồng mắc bao gồm thiếu sắt.
Đánh giá lại kê toa thuốc. Ưu tiên BN có đa bệnh lý. |
| Thiếu cơ | Thể dục thể chất đều đặn theo khả năng của BN. | Chương trình đào tạo tập thể dục, bao gồm thể dục nhịp điệu, lực cơ thể dục thăng bằng, 2-3 lần/tuần.
Phối hợp giữa dinh dưỡng và chương trình tập thể dục. |
| Suy dinh dưỡng | Theo dõi cân nặng.
Lượng protein cần nhập: 1-1.2g/kg/ngày. Thể dục thể chất đều đặn theo khả năng của BN. |
Nhu cầu năng lượng: 30-40 kcal/kg/ngày.
Nhu cầu protein: 1.2-1.5 g/kg/ngày. +-Chế phẩm dinh dưỡng đường miệng. Thể dục thể chất đều đặn theo khả năng của BN.
|
| Chức năng thể chất và té ngã | Tầm soát tụt huyết áp tư thế.
Cung cấp đủ nước. Thể dục thể chất đều đặn theo khả năng của BN. |
Xác định và điều trị các yếu tố nguy cơ bao gồm việc giảm các thuốc điều trị tâm thần.
Tầm soát các yếu tố nguy cơ có khả năng thúc đẩy. Cung cấp vitamin D.[31] Đánh giá môi trường xung quanh. Chương trình đào tạo tập thể dục, bao gồm thể dục nhịp điệu, lực cơ thể dục thăng bằng và linh động, 2-3 lần/tuần.
|
| Trầm cảm | Đấu tranh chống lại sự cô lập xã hội. | Thuốc điều trị nếu cần thiết: ức chế tái hấp thu chọn lọc serotonin.
Tâm lý trị liệu. |
| Suy giảm nhận thức | Điều trị bệnh đồng mắc như THAvà rung nhĩ để ngăn chặn suy giảm nhận thức.
Tham gia các hoạt động cộng đồng. |
Chú ý đến việc tuân trị thuốc.
Điều trị đặc hiệu và hỗ trợ xã hội. Kích thích nhận thức. |
| Chủng ngừa | Cúm, phế cầu, SARS-CoV2. | |
| Xã hội | Tầm soát cho việc tuân thủ trị. | Hỗ trợ xã hội.
Điều dưỡng cho điều trị. |
Lộ trình chăm sóc phụ thuộc vào tình huống tầm soát. Đầu tiên, các nhà thực hành cần nhận thức mối liên hệ giữa chúng. Sau bước tầm soát, nhiều hành động được đề xuất nhằm đánh giá lão khoa và tim mạch toàn diện được đề xuất ở hình 2. Trong nhiều tình huống phức tạp, cần có sự thống nhất giữa chuyên gia tim mạch và lão khoa để xác định ưu tiên trong kế hoạch chăm sóc[68], [69].
Kết luận
Có mối tương quan mạnh mẽ giữa suy yếu, ST và bệnh đồng mắc, do đó, cần tầm soát suy yếu ở BNST. Có nhiều công cụ tầm soát suy yếu. nhưng công cụ để đánh giá HCLK và các yếu tố chính của suy yếu là phù hợp nhất trong quản lý bước đầu BN. Từ đó, lợi ích can thiệp điều trị làm giảm gánh nặng suy yếu và kết cục ST. Tối ưu hóa điều trị BN cao tuổi bị ST gặp thách thức và cần lộ trình chuyên biệt, tuy nhiên, BN cũng hưởng được lợi ích từ các khuyên cáo điều trị tim mạch-lão khoa.
TÀI LIỆU THAM KHẢO
- Virani SS, Alonso A, Aparicio HJ, Benjamin EJ, Bittencourt MS, Callaway CW, Carson AP, Chamberlain AM, Cheng S, Delling FN, Elkind MSV, Evenson KR, Ferguson JF, Gupta DK, Khan SS, Kissela BM, Knutson KL, Lee CD, Lewis TT, Liu J, Loop MS, Lutsey PL, Ma J, Mackey J, Martin SS, Matchar DB, Mussolino ME, Navaneethan SD, Perak AM, Roth GA, et al. Heart Disease and Stroke Statistics-2021 Update: A Report From the American Heart Association. Circulation. 2021; 143: e254-e743.
- Hoogendijk EO, Afilalo J, Ensrud KE, Kowal P, Onder G, Fried LP. Frailty: implications for clinical practice and public health. Lancet. 2019; 394: 1365-1375.
- Fried LP, Tangen CM, Walston J, Newman AB, Hirsch C, Gottdiener J, Seeman T, Tracy R, Kop WJ, Burke G, McBurnie MA. Frailty in older adults: evidence for a phenotype. J Gerontol A Biol Sci Med Sci. 2001; 56: M146-M156.
- Rockwood K, Song X, MacKnight C, Bergman H, Hogan DB, McDowell I, Mitnitski A. A global clinical measure of fitness and frailty in elderly people. CMAJ. 2005; 173: 489-495.
- Guralnik JM, Ferrucci L, Simonsick EM, Salive ME, Wallace RB. Lower-extremity function in persons over the age of 70 years as a predictor of subsequent disability. N Engl J Med. 1995; 332: 556-561.
- Dunlay SM, Manemann SM, Chamberlain AM, Cheville AL, Jiang R, Weston SA, Roger VL. Activities of daily living and outcomes in heart failure. Circ Heart Fail. 2015; 8: 261-267.
- Santos-Eggimann B, Cuénoud P, Spagnoli J, Junod J. Prevalence of frailty in middle-aged and older community-dwelling Europeans living in 10 countries. J Gerontol A Biol Sci Med Sci. 2009; 64: 675-681.
- Dent E, Kowal P, Hoogendijk EO. Frailty measurement in research and clinical practice: A review. Eur J Intern Med. 2016; 31: 3-10.
- Sanders NA, Supiano MA, Lewis EF, Liu J, Claggett B, Pfeffer MA, Desai AS, Sweitzer NK, Solomon SD, Fang JC. The frailty syndrome and outcomes in the TOPCAT trial. Eur J Heart Fail. 2018; 20: 1570-1577.
- Sze S, Pellicori P, Zhang J, Weston J, Clark AL. Identification of Frailty in Chronic Heart Failure. JACC Heart Fail. 2019; 7: 291-302.
- Madan SA, Fida N, Barman P, Sims D, Shin J, Verghese J, Piña I, Jorde U, Patel SR. Frailty Assessment in Advanced Heart Failure. J Card Fail. 2016; 22: 840-844.
- Joyce E. Frailty in Advanced Heart Failure. Heart Fail Clin. 2016; 12: 363-374.
- Tse G, Gong M, Wong SH, Wu WKK, Bazoukis G, Lampropoulos K, Wong WT, Xia Y, Wong MCS, Liu T, Woo J. International Health Informatics Study (IHIS) Network. Frailty and Clinical Outcomes in Advanced Heart Failure Patients Undergoing Left Ventricular Assist Device Implantation: A Systematic Review and Meta-analysis. J Am Med Dir Assoc. 2018; 19: 255-261.e1.
- Yang X, Lupón J, Vidán MT, Ferguson C, Gastelurrutia P, Newton PJ, Macdonald PS, Bueno H, Bayés-Genís A, Woo J, Fung E. Impact of Frailty on Mortality and Hospitalization in Chronic Heart Failure: A Systematic Review and Meta-Analysis. J Am Heart Assoc. 2018; 7: e008251.
- Kwok CS, Zieroth S, Van Spall HGC, Helliwell T, Clarson L, Mohamed M, Mallen C, Duckett S, Mamas MA. The Hospital Frailty Risk Score and its association with in-hospital mortality, cost, length of stay and discharge location in patients with heart failure short running title: Frailty and outcomes in heart failure. Int J Cardiol. 2020; 300: 184-190.
- Zheng P-P, Yao S-M, He W, Wan Y-H, Wang H, Yang J-F. Frailty related all-cause mortality or hospital readmission among adults aged 65 and older with stage-B heart failure inpatients. BMC Geriatr. 2021; 21: 125.
- Weng S-C, Lin C-S, Tarng D-C, Lin S-Y. Physical frailty and long-term mortality in older people with chronic heart failure with preserved and reduced ejection fraction: a retrospective longitudinal study. BMC Geriatr. 2021; 21: 92.
- Matsue Y, Kamiya K, Saito H, Saito K, Ogasahara Y, Maekawa E, Konishi M, Kitai T, Iwata K, Jujo K, Wada H, Kasai T, Nagamatsu H, Ozawa T, Izawa K, Yamamoto S, Aizawa N, Yonezawa R, Oka K, Momomura S-I, Kagiyama N. Prevalence and prognostic impact of the coexistence of multiple frailty domains in elderly patients with heart failure: the FRAGILE-HF cohort study. Eur J Heart Fail. 2020; 22: 2112-2119.
- Kohsaka S, Sandhu AT, Parizo JT, Shoji S, Kumamamru H, Heidenreich PA. Association of Diagnostic Coding-Based Frailty and Outcomes in Patients With Heart Failure: A Report From the Veterans Affairs Health System. J Am Heart Assoc. 2020; 9: e016502.
- Dewan P, Jackson A, Jhund PS, Shen L, Ferreira JP, Petrie MC, Abraham WT, Desai AS, Dickstein K, Køber L, Packer M, Rouleau JL, Solomon SD, Swedberg K, Zile MR, McMurray JJV. The prevalence and importance of frailty in heart failure with reduced ejection fraction – an analysis of PARADIGM-HF and ATMOSPHERE. Eur J Heart Fail. 2020; 22: 2123-2133.
- Newton PJ, Si S, Reid CM, Davidson PM, Hayward CS, Macdonald PS, NSW HF Snapshot Investigators. Survival After an Acute Heart Failure Admission. Twelve-Month Outcomes From the NSW HF Snapshot Study. Heart Lung Circ. 2020; 29: 1032-1038.
- McAlister FA, Savu A, Ezekowitz JA, Armstrong PW, Kaul P. The hospital frailty risk score in patients with heart failure is strongly associated with outcomes but less so with pharmacotherapy. J Intern Med. 2020; 287: 322-332.
- Bottle A, Kim D, Hayhoe B, Majeed A, Aylin P, Clegg A, Cowie MR. Frailty and co-morbidity predict first hospitalisation after heart failure diagnosis in primary care: population-based observational study in England. Age Ageing. 2019; 48: 347-354.
- Cannon JA, Moffitt P, Perez-Moreno AC, Walters MR, Broomfield NM, McMurray JJV, Quinn TJ. Cognitive Impairment and Heart Failure: Systematic Review and Meta-Analysis. J Card Fail. 2017; 23: 464-475.
- Uchmanowicz I, Młynarska A, Lisiak M, Kałużna-Oleksy M, Wleklik M, Chudiak A, Dudek M, Migaj J, Hinterbuchner L, Gobbens R. Heart Failure and Problems with Frailty Syndrome: Why it is Time to Care About Frailty Syndrome in Heart Failure. Card Fail Rev. 2019; 5: 37-43.
- Rich MW, Beckham V, Wittenberg C, Leven CL, Freedland KE, Carney RM. A multidisciplinary intervention to prevent the readmission of elderly patients with congestive heart failure. N Engl J Med. 1995; 333: 1190-1195.
- Chen YM, Li Y. Safety and efficacy of exercise training in elderly heart failure patients: a systematic review and meta-analysis. Int J Clin Pract. 2013; 67: 1192-1198.
- Cameron ID, Fairhall N, Langron C, Lockwood K, Monaghan N, Aggar C, Sherrington C, Lord SR, Kurrle SE. A multifactorial interdisciplinary intervention reduces frailty in older people: randomized trial. BMC Med. 2013; 11: 65.
- McDonagh TA, Metra M, Adamo M, Gardner RS, Baumbach A, Böhm M, Burri H, Butler J, Čelutkienė J, Chioncel O, Cleland JGF, Coats AJS, Crespo-Leiro MG, Farmakis D, Gilard M, Heymans S, Hoes AW, Jaarsma T, Jankowska EA, Lainscak M, Lam CSP, Lyon AR, McMurray JJV, Mebazaa A, Mindham R, Muneretto C, Francesco Piepoli M, Price S, Rosano GMC, Ruschitzka F, et al. ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure. Eur Heart J. 2021: ehab368.
- O’Mahony D, O’Sullivan D, Byrne S, O’Connor MN, Ryan C, Gallagher P. STOPP/START criteria for potentially inappropriate prescribing in older people: version 2. Age Ageing. 2015; 44: 213-218.
- Annweiler C, Legrand E, Souberbielle J-C. Vitamin D in adults: update on testing and supplementation. Geriatr Psychol Neuropsychiatr Vieil. 2018; 16: 7-22.
- Morley JE, Vellas B, Kan GV, Anker SD, Bauer JM, Bernabei R, Cesari M, Chumlea WC, Doehner W, Evans J, Fried LP, Guralnik JM, Katz PR, Malmstrom TK, McCarter RJ, Gutierrez Robledo LM, Rockwood K, Von HS, Vandewoude MF, Walston J. Frailty consensus: a call to action. J Am Med Dir Assoc. 2013; 14: 392-397.
- Martín-Sánchez FJ, Rodríguez-Adrada E, Vidan MT, Llopis García G, González Del Castillo J, Rizzi MA, Alquezar A, Piñera P, Lázaro Aragues P, Llorens P, Herrero P, Jacob J, Gil V, Fernández C, Bueno H, Miró Ò. Representing the members of the OAK Register Investigators. Impact of Frailty and Disability on 30-Day Mortality in Older Patients With Acute Heart Failure. Am J Cardiol. 2017; 120: 1151-1157.
- Teixeira A, Arrigo M, Tolppanen H, Gayat E, Laribi S, Metra M, Seronde MF, Cohen-Solal A, Mebazaa A. Management of acute heart failure in elderly patients. Arch Cardiovasc Dis. 2016; 109: 422-430.
- McDonagh J, Martin L, Ferguson C, Jha SR, Macdonald PS, Davidson PM, Newton PJ. Frailty assessment instruments in heart failure: A systematic review. Eur J Cardiovasc Nurs. 2018; 17: 23-35.
- Kotsani M, Aromatario O, Labat C, Vançon G, Fréminet A, Mejri M, Lantieri O, Fantino B, Perret-Guillaume C, Epstein J, Benetos A. A Simple Questionnaire as a First-Step Tool to Detect Specific Frailty Profiles: The Lorraine Frailty-Profiling Screening Scale. J Nutr Health Aging. 2020; 24: 730-738.
- Ambagtsheer RC, Archibald MM, Lawless M, Kitson A, Beilby J. Feasibility and acceptability of commonly used screening instruments to identify frailty among community-dwelling older people: a mixed methods study. BMC Geriatr. 2020; 20: 152.
- Oviedo-Briones M, Laso ÁR, Carnicero JA, Cesari M, Grodzicki T, Gryglewska B, Sinclair A, Landi F, Vellas B, Checa-López M, Rodriguez-Mañas L. A Comparison of Frailty Assessment Instruments in Different Clinical and Social Care Settings: The Frailtools Project. J Am Med Dir Assoc. 2020.
- Vitale C, Jankowska E, Hill L, Piepoli M, Doehner W, Anker SD, Lainscak M, Jaarsma T, Ponikowski P, Rosano GMC, Seferovic P, Coats AJ. Heart Failure Association/European Society of Cardiology position paper on frailty in patients with heart failure. Eur J Heart Fail. 2019; 21: 1299-1305.
- Saliba D, Elliott M, Rubenstein LZ, Solomon DH, Young RT, Kamberg CJ, Roth C, MacLean CH, Shekelle PG, Sloss EM, Wenger NS. The Vulnerable Elders Survey: a tool for identifying vulnerable older people in the community. J Am Geriatr Soc. 2001; 49: 1691-1699.
- Wang J, Dietrich MS, Bell SP, Maxwell CA, Simmons SF, Kripalani S. Vanderbilt Inpatient Cohort Study (VICS). Changes in vulnerability among older patients with cardiovascular disease in the first 90 days after hospital discharge: A secondary analysis of a cohort study. BMJ Open. 2019; 9: e024766.
- Bongue B, Buisson A, Dupre C, Beland F, Gonthier R, Crawford-Achour É. Predictive performance of four frailty screening tools in community-dwelling elderly. BMC Geriatr. 2017; 17: 262.
- Schoevaerdt D, Biettlot S, Malhomme B, Cornette P, Vanpee D, Swine C. Identification précoce du profil gériatrique en salle d’urgences: présentation de la grille SEGA. La Revue de Gériatrie. 2004; 03: 169-178.
- Piffer I, Goetz C, Zevering Y, André E, Bourouis Z, Blettner N. Ability of Emergency Department Physicians Using a Functional Autonomy-Assessing Version of the Triage Risk Screening Tool to Detect Frail Older Patients Who Require Mobile Geriatric Team Consultation. J Nutr Health Aging. 2020; 24: 634-641.
- Oubaya N, Dramé M, Novella J-L, Quignard E, Cunin C, Jolly D, Mahmoudi R. Screening for frailty in community-dwelling elderly subjects: Predictive validity of the modified SEGA instrument. Arch Gerontol Geriatr. 2017; 73: 177-181.
- Meldon SW, Mion LC, Palmer RM, Drew BL, Connor JT, Lewicki LJ, Bass DM, Emerman CL. A brief risk-stratification tool to predict repeat emergency department visits and hospitalizations in older patients discharged from the emergency department. Acad Emerg Med. 2003; 10: 224-232.
- Comment réduire les réhospitalisations évitables des personnes âgées? Haute Autorité de Santé. https://www.has-sante.fr/jcms/c_1602735/fr/comment-reduire-les-rehospita…(24 February 2021)
- Carpenter CR, Shelton E, Fowler S, Suffoletto B, Platts-Mills TF, Rothman RE, Hogan TM. Risk Factors and Screening Instruments to Predict Adverse Outcomes for Undifferentiated Older Emergency Department Patients: A Systematic Review and Meta-analysis. Acad Emerg Med. 2015; 22: 1-21.
- Azad NA, Mielniczuk L. A Call for Collaboration: Improving Cardiogeriatric Care. Can J Cardiol. 2016; 32: 1041-1044.
- Goyal P, Gorodeski EZ, Flint KM, Goldwater DS, Dodson JA, Afilalo J, Maurer MS, Rich MW, Alexander KP, Hummel SL. Perspectives on Implementing a Multidomain Approach to Caring for Older Adults With Heart Failure. J Am Geriatr Soc. 2019; 67: 2593-2599.
- Boully C, Vidal J-S, Guibert E, Ghazali FN, Pesce A, Beauplet B, Roger J-D, Carrière I, Timbely B, Idiri H, Constensoux J-P, Durocher A-M, Dubail D, Fargier M, Jeandel C, Berrut G, Hanon O, SFGG study group. National survey on the management of heart failure in individuals over 80 years of age in French geriatric care units. BMC Geriatr. 2019; 19: 204.
- Cherubini A, Oristrell J, Pla X, Ruggiero C, Ferretti R, Diestre G, Clarfield AM, Crome P, Hertogh C, Lesauskaite V, Prada G-I, Szczerbinska K, Topinkova E, Sinclair-Cohen J, Edbrooke D, Mills GH. The persistent exclusion of older patients from ongoing clinical trials regarding heart failure. Arch Intern Med. 2011; 171: 550-556.
- Jhund PS, Fu M, Bayram E, Chen C-H, Negrusz-Kawecka M, Rosenthal A, Desai AS, Lefkowitz MP, Rizkala AR, Rouleau JL, Shi VC, Solomon SD, Swedberg K, Zile MR, McMurray JJV, Packer M, PARADIGM-HF Investigators and Committees. Efficacy and safety of LCZ696 (sacubitril-valsartan) according to age: insights from PARADIGM-HF. Eur Heart J. 2015; 36: 2576-2584.
- Flather MD, Shibata MC, Coats AJS, Van Veldhuisen DJ, Parkhomenko A, Borbola J, Cohen-Solal A, Dumitrascu D, Ferrari R, Lechat P, Soler-Soler J, Tavazzi L, Spinarova L, Toman J, Böhm M, Anker SD, Thompson SG, Poole-Wilson PA, SENIORS Investigators. Randomized trial to determine the effect of nebivolol on mortality and cardiovascular hospital admission in elderly patients with heart failure (SENIORS). Eur Heart J. 2005; 26: 215-225.
- Cohen-Solal A, McMurray JJV, Swedberg K, Pfeffer MA, Puu M, Solomon SD, Michelson EL, Yusuf S, Granger CB, CHARM Investigators. Benefits and safety of candesartan treatment in heart failure are independent of age: insights from the Candesartan in Heart failure-Assessment of Reduction in Mortality and morbidity programme. Eur Heart J. 2008; 29: 3022-3028.
- Komajda M, Hanon O, Hochadel M, Lopez-Sendon JL, Follath F, Ponikowski P, Harjola V-P, Drexler H, Dickstein K, Tavazzi L, Nieminen M. Contemporary management of octogenarians hospitalized for heart failure in Europe: Euro Heart Failure Survey II. Eur Heart J. 2009; 30: 478-486.
- Rodil Fraile R, Malafarina V, Tiberio LG. Sacubitril-valsartan in heart failure and multimorbidity patients. ESC Heart Fail. 2018; 5: 956-959.
- Sin DD, McAlister FA. The effects of beta-blockers on morbidity and mortality in a population-based cohort of 11,942 elderly patients with heart failure. Am J Med. 2002; 113: 650-656.
- Hanon O, Belmin J, Benetos A, Chassagne P, De Decker L, Jeandel C, Krolak-Salmon P, Nourhashemi F, Paccalin M. Consensus of experts from the French Society of Geriatrics and Gerontology on the management of heart failure in very old subjects. Arch Cardiovasc Dis. 2021; 114: 246-259.
- Kubala M, Guédon-Moreau L, Anselme F, Klug D, Bertaina G, Traullé S, Buiciuc O, Savouré A, Diouf M, Hermida J-S. Utility of Frailty Assessment for Elderly Patients Undergoing Cardiac Resynchronization Therapy. JACC Clin Electrophysiol. 2017; 3: 1523-1533.
- Pandey A, Kitzman DW, Brubaker P, Haykowsky MJ, Morgan T, Becton JT, Berry JD. Response to Endurance Exercise Training in Older Adults with Heart Failure with Preserved or Reduced Ejection Fraction. J Am Geriatr Soc. 2017; 65: 1698-1704.
- Billot M, Calvani R, Urtamo A, Sánchez-Sánchez JL, Ciccolari-Micaldi C, Chang M, Roller-Wirnsberger R, Wirnsberger G, Sinclair A, Vaquero-Pinto N, Jyväkorpi S, Öhman H, Strandberg T, Schols JMGA, Schols AMWJ, Smeets N, Topinkova E, Michalkova H, Bonfigli AR, Lattanzio F, Rodríguez-Mañas L, Coelho-Júnior H, Broccatelli M, D’Elia ME, Biscotti D, Marzetti E, Freiberger E. Preserving Mobility in Older Adults with Physical Frailty and Sarcopenia: Opportunities, Challenges, and Recommendations for Physical Activity Interventions. Clin Interv Aging. 2020; 15: 1675-1690.
- Verheijden Klompstra L, Jaarsma T, Strömberg A. Exergaming in older adults: a scoping review and implementation potential for patients with heart failure. Eur J Cardiovasc Nurs. 2014; 13: 388-398.
- Bilgen F, Chen P, Poggi A, Wells J, Trumble E, Helmke S, Teruya S, Catalan T, Rosenblum HR, Cornellier ML, Karmally W, Maurer MS, Hummel SL. Insufficient Calorie Intake Worsens Post-Discharge Quality of Life and Increases Readmission Burden in Heart Failure. JACC Heart Fail. 2020; 8: 756-764.
- Vest AR, Chan M, Deswal A, Givertz MM, Lekavich C, Lennie T, Litwin SE, Parsly L, Rodgers JE, Rich MW, Schulze PC, Slader A, Desai A. Nutrition, Obesity, and Cachexia in Patients With Heart Failure: A Consensus Statement from the Heart Failure Society of America Scientific Statements Committee. J Card Fail. 2019; 25: 380-400.
- Wiersinga JHI, Rhodius-Meester HFM, Kleipool EEF, Handoko L, Van RAC, Liem S, Trappenburg MC, Peters MJL, Muller M. Managing older patients with heart failure calls for a holistic approach. ESC Heart Fail. 2021; 8: 2111-2119.
- Gorodeski EZ, Goyal P, Hummel SL, Krishnaswami A, Goodlin SJ, Hart LL, Forman DE, Wenger NK, Kirkpatrick JN, Alexander KP, Geriatric Cardiology Section Leadership Council, American College of Cardiology. Domain Management Approach to Heart Failure in the Geriatric Patient: Present and Future. J Am Coll Cardiol. 2018; 71: 1921-1936.
- Mo Y, Chu M, Hu W, Wang H. Association between the nurse-led program with mental health status, quality of life, and heart failure rehospitalization in chronic heart failure patients. Medicine (Baltimore). 2021; 100: e25052.
- Kikuchi A, Taniguchi T, Nakamoto K, Sera F, Ohtani T, Yamada T, Sakata Y. Feasibility of home-based cardiac rehabilitation using an integrated telerehabilitation platform in elderly patients with heart failure: A pilot study. J Cardiol. 2021.
- Yang X, Lupon J, Vidan MT, et al. Impact of frailty on mortality and hospitalization in chronic heart failure: a systematic review and meta-analysis. J Am Heart Assoc2018;7:e008251.
- Sze S, Pellicori P, Zhang J, Weston J, Clark AL. Identification of frailty in chronic heart failure. J Am Coll Cardiol HF2019;7:291–302.
- Sanders NA, Supiano MA, Lewis EF, et al. The frailty syndrome and outcomes in the TOPCAT trial. Eur J Heart Fail2018;20:1570–7.
- Madan SA, Fida N, Barman P, et al. Frailty assessment in advanced heart failure. J Card Fail 2016;22:840–4.
- Joyce E Frailty in advanced heart failure. Heart Fail Clin2016;12:363–74.
- Denfeld QE, Winters-Stone K, Mudd JO, Hiatt SO, Lee CS. Identifying a relationship between physical frailty and heart failure symptoms. J Cardiovasc Nurs2018;33:E1–7.
- Denfeld QE, Winters-Stone K, Mudd JO, Gelow JM, Kurdi S, Lee CS. The prevalence of frailty in heart failure: a systematic review and meta-analysis. Int J Cardiol2017;236:283–9.
- Volpato S, Cavalieri M, Guerra G, et al. Performance-based functional assessment in older hospitalized patients: feasibility and clinical correlates. J Gerontol A Biol Sci Med Sci2008;63: 1393–8.
- Vidan MT, Blaya-Novakova V, Sanchez E, Ortiz J, Serra-Rexach JA, Bueno H. Prevalence and prognostic impact of frailty and its components in non-dependent elderly patients with heart failure. Eur J Heart Fail2016;18:869–75.
- Reeves GR, Whellan DJ, O’Connor CM, et al. A novel rehabilitation intervention for older patients with acute decompensated heart failure: the REHAB-HF Pilot Study. J Am Coll Cardiol HF 2017;5:359–66.
- Van Tassell BW, Canada J, Carbone S, et al. Interleukin-1 blockade in recently decompensated systolic heart failure: results from REDHART (Recently Decompensated Heart Failure Anakinra Response Trial). Circ Heart Fail2017;10.
- Van Tassell BW, Trankle CR, Canada JM, et al. IL-1 blockade in patients with heart failure with preserved ejection fraction. Circ Heart Fail2018; 11:e005036.
- Pandey A, Parashar A, Kumbhani D, et al. Exercise training in patients with heart failure and preserved ejection fraction: meta-analysis of randomized control trials. Circ Heart Fail2015;8: 33–40.
- Imran HM, Baig M, Erqou S, et al. Home-based cardiac rehabilitation alone and hybrid with center-based cardiac rehabilitation in heart failure: a systematic review and meta-analysis. J Am Heart Assoc 2019;8:e012779.
- Bonilla-Palomas JL, Gamez-Lopez AL, Castillo-Dominguez JC, et al. Nutritional intervention in malnourished hospitalized patients with heart failure. Arch Med Res2016;47:535–40.
- Hummel SL, Karmally W, Gillespie BW, et al. Home-delivered meals postdischarge from heart failure hospitalization. Circ Heart Fail2018;11:e004886.
- Kitzman DW, Brubaker P, Morgan T, et al. Effect of caloric restriction or aerobic exercise training on peak oxygen consumption and quality of life in obese older patients with heart failure with preserved ejection fraction: a randomized clinical trial. JAMA2016;315:36–46.
- A Pandey, et al. Frailty Is Intertwined With Heart Failure. JACC Heart Fail. 2019 Dec; 7(12): 1001–1011.







