PGS. TS. Phạm Nguyễn Vinh (**)
(*)- Khoa Tim Mạch Can Thiệp, BV Tim Tâm Đức
(**)- Giám đốc chuyên môn, BV Tim Tâm Đức
1. MỞ ĐẦU
Trong kỷ nguyên stent phủ thuốc hiện tại, ngày càng có nhiều bệnh nhân hẹp nhiều nhánh động mạch vành được điều trị tái tưới máu bằng phương pháp can thiệp động mạch vành qua da (Percutaneous Coronary Intervention- PCI). Tuy nhiên, can thiệp động mạch vành với stent phủ thuốc luôn phải đối mặt với những tai biến nhất định (bóc tách động mạch vành, không dòng chảy, tái hẹp trong stent, hoặc huyết khối muộn trong stent), và chi phí cho việc điều trị thường rất tốn kém. Do đó, việc chọn lựa tổn thương để đặt stent là rất quan trọng. Can thiệp đúng tổn thương gây thiếu máu cục bộ cơ tim sẽ cải thiện triệu chứng cơ năng và tiên lượng của bệnh nhân.
Ở bệnh nhân hẹp nhiều nhánh động mạch vành, trắc nghiệm gắng sức không xâm lấn trong một số trường hợp không giúp bác sĩ tim mạch xác định chính xác tổn thương gây thiếu máu cục bộ cơ tim. Cho đến hiện nay, mặc dù có những giới hạn nhất định, hình chụp động mạch vành cản quang vẫn là tiêu chuẩn quan trọng giúp bác sĩ lựa chọn tổn thương đặt stent. Phân suất dự trữ lưu lượng (Fractional Flow Reserve- FFR) động mạch vành là một chỉ số giúp đánh giá khả năng gây thiếu máu cục bộ cơ tim của một tổn thương gây hẹp lòng động mạch vành và ít bị ảnh hưởng bởi các yếu tố huyết động.
FFR được tính bằng tỷ số lưu lượng dòng chảy tối đa qua chỗ hẹp (Qs) chia cho lưu lượng dòng chảy tối đa bình thường (Qn). Trong điều kiện dãn mạch tối ưu, FFR được tính theo công thức FFR = Qs/Qn= Pd/Pa; trong đó Pa là áp lực động mạch chủ, đo được ở đầu ống thông can thiệp; Pd là áp lực động mạch vành đo được ở phía xa chỗ hẹp, đo được bằng dây dẫn đo áp lực (pressure wire).
Tổn thương hẹp động mạch vành có FFR < 0.75 được xem là hẹp có ý nghĩa, có khả năng gây thiếu máu cục bộ cơ tim và nên được tái tưới máu. FFR < 0.75 liên quan chặt chẽ với tình trạng thiếu máu cục bộ cơ tim và có tương quan có ý nghĩa với các phương pháp chẩn đoán thiếu máu cục bộ cơ tim không xâm nhập khác như trắc nghiệm gắng sức bằng xe đạp, xạ ký cơ tim bằng thallium và siêu âm tim gắng sức bằng dobutamine, với độ nhạy 88%, độ chuyên biệt 100% và khả năng tiên đoán chính xác 93% (1). Kết quả theo dõi 5 năm của nghiên cứu DEFER công bố năm 2007 cũng cho thấy sự an toàn của việc không can thiệp qua da động mạch vành ở các tổn thương có FFR ³ 0.75. Nhóm bệnh nhân này có tỉ lệ tử vong tim mạch và nhồi máu cơ tim rất thấp, < 1% năm. Ngược lại, trì hoãn can thiệp tổn thương có FFR < 0.75- 0.80 dẫn đến kết cục lâm sàng xấu cho bệnh nhân nếu so sánh với nhóm được can thiệp đặt stent (2).
Nghiên cứu FAME (Fractional Flow Reserve versus Angiography for Guiding Percutaneous Coronary Intervention) là thử nghiệm lâm sàng ngẫu nhiên, đa trung tâm và đa quốc gia đầu tiên so sánh FFR và hình chụp động mạch vành cản quang trong việc quyết định lựa chọn tổn thương cần đặt stent phủ thuốc ở bệnh nhân hẹp nhiều nhánh động mạch vành (3). Kết quả nghiên cứu được công bố lần đầu vào đầu năm 2009 và gần đây kết quả theo dõi 02 năm cũng đã được báo cáo.
2. THIẾT KẾ NGHIÊN CỨU FAME
Đối tượng nghiên cứu là bệnh nhân hẹp nhiều nhánh động mạch vành, được định nghĩa là hẹp ³ 50% ở ít nhất hai nhánh động mach vành thượng tâm mạc chính trên phim chụp cản quang động mạch vành, có chỉ định tái tưới máu bằng can thiệp động mạch vành qua da (PCI). Ngay sau khi được thu nhận vào nghiên cứu, bệnh nhân sẽ được phân ngẫu nhiên thành hai nhóm. Nhóm thứ nhất, bệnh nhân được can thiệp đặt stent ở tất cả các tổn thương hẹp động mạch vành. Nhóm thứ hai, tất cả các tổn thương được đo FFR bằng dây dẫn đo áp lực, tổn thương nào có FFR £ 0.80 sẽ được đặt stent. Tất cả stent sử dụng đều là stent phủ thuốc (Endeavor [Medtronic], Cypher [Cordis], hoặc Taxus [Boston Scientific], được lựa chọn tùy ý bác sĩ tim mạch can thiệp).
Tiêu chuẩn loại trừ bao gồm hẹp có ý nghĩa thân chung động mạch vành trái, tiền sử phẫu thuật bắc cầu động mạch vành, giải phẫu động mạch vành quá ngoằn ngoèo hoặc vôi hóa nặng, bệnh nhân mắc bệnh khác có thời gian sống dự kiến ít hơn 2 năm, bệnh nhân có chống chỉ định với stent phủ thuốc, phụ nữ có thai.
FFR được đo bằng dây dẫn đo áp lực (Radi Medical Systems) trong tình trạng dãn động mạch vành tối đa, được tạo ra bằng cách truyền tĩnh mạch Adenosine với liều 140 µg/kg/phút.
Tất cả bệnh nhân đều được điều trị bằng hai thuốc chống kết tập tiểu cầu là Aspirin và Clopidogrel trong ít nhất 1 năm sau thủ thuật can thiệp động mạch vành.
Tiêu chí đánh giá chính (Primary Endpoint) là tỷ lệ các biến cố tim mạch nặng sau 1 năm. Biến cố tim mạch nặng được định nghĩa bao gồm tử vong, nhồi máu cơ tim và làm lại tái tưới máu động mạch vành. Các tiêu chí phụ (Secondary Endpoints) bao gồm thòi gian thủ thuật; số lượng thuốc cản quang sử dụng; đau ngực tại thời điểm 1 năm đánh giá bằng thang điểm Canadian Cardiovascular Society; chất lượng cuộc sống đáng gía bằng thang điểm European Quality of Life- 5 Dimensions EQ- 5D; số lượng thuốc chống đau ngực sử dụng; các tiêu chí riêng biệt của tiêu chí chính; tỷ lệ các biến cố tim mạch nặng sau 30 ngày và 6 tháng; chi phí cho thủ thuật can thiệp.
Cỡ mẫu dự kiến cho mỗi nhóm là 426 bệnh nhân.
3. KẾT QUẢ NGHIÊN CỨU FAME
Từ 01.1006 đến 09.2007, tổng cộng 1005 bệnh nhân ở 20 trung tâm y khoa tại Mỹ và Châu Âu đã được thu nhận vào nghiên cứu; 496 bệnh nhân được phân vào nhóm can thiệp với hướng dẫn của hình chụp động mạch vành (Angiography-group), 509 bệnh nhân vào nhóm can thiệp với hướng dẫn của FFR (FFR-group). Không có sự khác biệt có ý nghĩa về đặc điểm dân số, về tổn thương động mạch vành ở hai nhóm (Bảng 1).
Bảng 1. Đặc điểm bệnh nhân
|
|
Angiography-group (N= 496) |
FFR-group (N= 509) |
p |
|
Dân số |
|
|
|
|
Tuổi (năm) |
64.2±10.2 |
64.6±10.3 |
0.47 |
|
Giới tính |
|
|
0.30 |
|
Nam |
360 (72.6) |
384 (75.4) |
|
|
Nữ |
136 (27.4) |
125 (24.6) |
|
|
Lâm sàng |
|
|
|
|
Phân độ đau ngực CCS |
|
|
0.13 |
|
I |
115 (23.2) |
132 (25.9) |
|
|
II |
165 (33.3) |
170 (33.4) |
|
|
III |
118 (23.8) |
132 (25.9) |
|
|
IV |
098 (19.8) |
075 (14.7) |
|
|
Nhồi máu cơ tim cũ |
180 (36.3) |
187 (36.7) |
0.84 |
|
Có PCI trước đây |
129 (26.0) |
146 (28.7) |
0.34 |
|
Tiểu đường |
125 (25.2) |
123 (24.2) |
0.65 |
|
Tăng huyết áp |
327 (65.9) |
312 (61.3) |
0.10 |
|
Tăng cholesterol máu |
362 (73.0) |
366 (71.9) |
0.62 |
|
Tiền căn gia đình |
190 (38.3) |
205 (40.3) |
0.49 |
|
Hút thuốc lá |
156 (31.5) |
138 (27.1) |
0.12 |
|
Cơn đau thắt ngực không ổn định |
|
|
|
|
Có thay đổi ECG |
091 (18.3) |
073 (14.3) |
0.09 |
|
Không thay đổi ECG |
087 (17.5) |
077 (15.1) |
0.29 |
|
Phân suất tống máu thất trái |
57.1±12.0 |
57.2±11.0 |
0.92 |
|
Thuốc điều trị |
|
|
|
|
Ức chế bêta |
377 (76.0) |
395 (77.6) |
0.55 |
|
Chẹn kênh canxi |
096 (19.4) |
121 (23.8) |
0.09 |
|
Nitrate |
179 (36.1) |
167 (32.8) |
0.27 |
|
UCMC hoặc UCTT |
255 (51.4) |
267 (52.5) |
0.74 |
|
Statin |
397 (80.0) |
417 (81.9) |
0.45 |
|
Aspirin |
454 (91.5) |
465 (91.4) |
0.92 |
|
Clopidogrel |
292 (58.9) |
310 (60.9) |
0.51 |
|
Đặc điểm tổn thương ĐMV |
|
|
|
|
Số tổn thương mỗi bệnh nhân |
2.7±0.9 |
2.8±1.0 |
0.34 |
|
Mức độ hẹp ĐMV (số tổn thương/tổng số tổn thương) |
|
|
|
|
50-70% |
550/1350 (40.7) |
624/1414 (44.1) |
|
|
71-90% |
553/1350 (41.0) |
530/1414 |
|
|
91-99% |
207/1350 (15.3) |
2 |
|
|
Tắc hoàn toàn |
040/1350 (03.0) |
058/1414 |
|
|
Số bệnh nhân có tổn thương tắc hoàn toàn |
37 (7.5) |
54 (10.6) |
|
|
Đo QCA |
|
|
|
|
Mức độ hẹp |
61.2±16.6 |
60.4±17.6 |
0.24 |
|
Đường kính lòng mạch nhỏ nhất |
1.0±0.4 |
1.0±0.5 |
0.35 |
|
Đường kính lòng mạch tham chiếu |
2.5±0.6 |
2.5±0.7 |
0.81 |
|
Chiều dài tổn thương |
12.6±6.9 |
12.5±6.5 |
0.42 |
|
Điểm SYNTAX |
14.5±8.8 |
14.5±8.6 |
0.95 |
|
Điểm EQ-5D |
64.7±19.2 |
66.5±18.3 |
0.24 |
Tổng cộng có 2415 stent đã được sử dụng, trong đó 96.9% là stent phủ thuốc. Các tổn thương được đặt stent thường (bare metal stent) liên quan đến vấn đề kỹ thuật. Nhóm Angiography-group có số stent trên bênh nhân nhiều hơn có ý nghĩa so với nhóm FFR-group (2.7±1.2 vs. 1.9±1.3, p<0.001). Trong nhóm FFR-group, 63% tổn thương có FFR #0.80 được đặt stent; 37% tổn thương có FFR >0.08 và không được đặt stent. Thời gian thực hiện thủ thuật tương đương nhau ở hai nhóm (70±44 phút vs. 71±43 phút, p=0.51). Số lượng thuốc cản quang sử dụng ở nhóm Angiography-group nhiền hơn hẳn nhóm FFR-group (302±127 ml vs. 272±133 ml, p<0.001) (Bảng 2).
|
|
Angiography-group (N= 496) |
FFR-group (N= 509) |
p |
|
Thời gian thủ thuật- phút |
70±44 |
71±43 |
0.51 |
|
Số lượng thuốc cản quang- ml |
302±127 |
272±133 |
<0.001 |
|
Số stent/ bệnh nhân |
2.7±1.2 |
1.9±1.3 |
<0.001 |
|
Chiều dài stent/bệnh nhân- mm |
51.9±24.6 |
37.9±27.8 |
<0.001 |
|
Kết quả FFR |
|
|
|
|
Số tổn thương đo FFR |
|
1329/1414 (94%) |
|
|
Giá trị FFR |
|
0.71±0.18 |
|
|
Tổn thương gây TMCB |
|
0.60±0.14 |
|
|
Tổn thương không gây TMCB |
|
0.88±0.05 |
|
|
Số tổn thương có FFR ≤0.80 |
|
874/1387 (63%) |
|
|
Số tổn thương có FFR >0.80 |
|
513/1387 (37%) |
|
|
|
|
|
|
|
Chi phí dụng cụ thủ thuật -USD |
6007±2819 |
5332±3261 |
<0.001 |
|
Số ngày nằm viện |
3.7±3.5 |
3.4±3.3 |
0.05 |
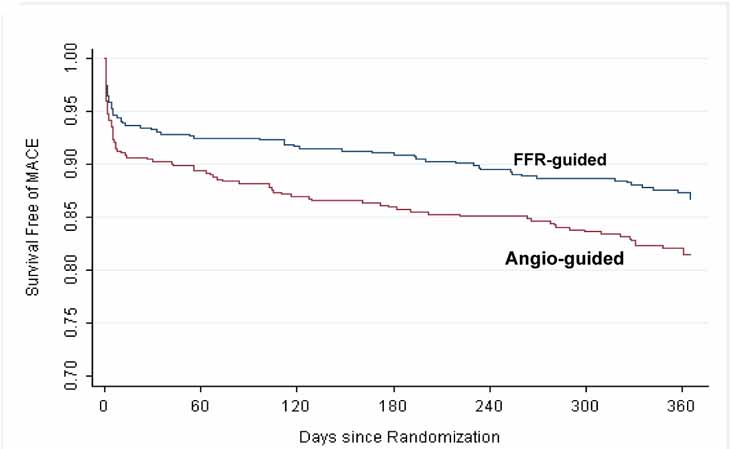
Tỷ lệ các biến cố tim mạch nặng (tiêu chí đánh giá chính) lần lượt là 18.3% và 13.2% ở hai nhóm Angiography-group và FFR-group, p=0.02. Không có sự khác biệt có ý nghĩa ở từng tiêu chí tử vong, nhối máu cơ tim hoặc làm lại tái tưới máu động mạch vành. Nếu tính gộp tỷ lệ tử vong và nhồi máu cơ tim thì có sự khác biệt có ý nghĩa giữa hai nhóm – 11.1% (55 bệnh nhân) ở nhóm Angiography-group và 7.3% (37 bệnh nhân) ở nhóm FFR-group, p=0.04 (Bảng 3).
Bảng 3. Kết quả các tiêu chí đánh giá của FAME tại thời điểm 1 năm
|
|
Angio-group (N= 496) |
FFR-group (N= 509) |
p |
RR (KTC 95%) |
|
Tiêu chí gộp- Tử vong/ NMCT/ Làm lại tái tưới máu động mạch vành |
91 (18.3) |
67 (13.2) |
0.02 |
0.72 (0.54-0.96) |
|
Tử vong |
15 (3.0) |
09 (1.8) |
0.19 |
0.58 (0.26-1.32) |
|
NMCT |
43 (8.7) |
29 (5.7) |
0.07 |
0.66 (0.42-1.04) |
|
Làm lại tái tưới máu ĐMV |
47 (9.5) |
33 (6.5) |
0.08 |
0.68 (0.45-1.05) |
|
Tử vong/ NMCT |
55 (11.1) |
37 (7.3) |
0.04 |
0.66 (0.44 |
|
|
|
|
|
|
|
Bn không bị biến cố tim mạch & không đau ngực |
326/482 (67.6) |
360/493 (73.0) |
0.07 |
|
|
Bn không đau ngực |
374/480 (77.9) |
399/491 (81.3) |
0.20 |
|
|
Số lượng thuốc chống đau thắt ngực |
1.23±0.74 |
1.20±0.76 |
0.48 |
|
Tại thời điểm 1 năm, 77.9% bệnh nhân ở nhóm Angiography-group không có triệu chứng đau thắt ngực, so với 831.3% ở nhóm FFR-group (p=0.20). Chi phí cho thủ thuật can thiệp ở hai nhóm Angiography-group và FFR- group lần lượt là 6007±2819 USD và 5332±3261 USD, p<0.001.
Hình 1. Đường biểu diễn Kaplan-Meier- Bệnh nhân không bị các biến cố tim mạch nặng
(MACE- Major Adverse Cardiac Event)
Kết quả theo dõi 2 năm của nghiên cứu FAME vừa được báo cáo vào cuối tháng 9/2009 tại hội nghị Transcatheter Cardiovascular Therapeutics (TCT) ở San Francisco. Tỷ lệ các biến cố tim mạch nặng (tiêu chí đánh giá chính) lần lượt là 22.2% và 17.7% ở hai nhóm Angiography-group và FFR-group, p=0.07. Nếu xét riêng tiêu chí lâm sàng, đo FFR thường quy trước khi đặt stent giảm một cách có ý nghĩa nguy cơ tử vong và nhồi máu cơ tim (Bảng 4). Sau 2 năm theo dõi, chỉ có 1/513 (0.2%) tổn thương không đặt stent do kết quả FFR là thủ phạm của nhồi máu cơ tim sau đó; 10/513 (1.9%) tổn thương không đặt stent do kết quả FFR tiếp tục tiến triển nặng thêm và cần tới tái tưới máu (4).
Bảng 4. Kết quả FAME tại thời điểm 2 năm
|
|
Angiography-group (N= 496) |
FFR-group (N= 509) |
p |
|
Tiêu chí gộp- Tử vong/ NMCT/ Làm lại tái tưới máu động mạch vành |
110 (22.2) |
90 (17.7) |
0.07 |
|
Tử vong |
19 (3.8) |
13 (2.6) |
0.25 |
|
NMCT |
48 (9.7) |
31 (6.1) |
0.03 |
|
Làm lại tái tưới máu ĐMV |
61 (12.3) |
53 (10.4) |
0.35 |
|
Tử vong/ NMCT |
63 (12.7) |
43 (8.4) |
0.03 |
4. Ý NGHĨA LÂM SÀNG CỦA NGHIÊN CỨU FAME
Ở bệnh nhân hẹp nhiều nhánh động mạch vành, đo FFR để hướng dẫn can thiệp đặt stent sẽ giảm được 28% nguy cơ tương đối các biến cố tim mạch nặng (tử vong, nhối máu cơ tim, làm lại tái tưới máu động mạch vành). Đo FFR ở 20 bệnh nhân sẽ ngăn ngừa được 1 biến cố tim mạch. Đó là kết quả chính của nghiên cứu FAME.
Kết quả của FAME cho thấy, tiên lượng của bệnh nhân đặt stent có thể được cải thiện nếu can thiệp đó được thực hiện với hướng dẫn của FFR. Cách thực hành này cũng giúp tiết kiệm chi phí thủ thuật và số lượng thuốc cản quang sử dụng và không làm kéo dài thời gian thủ thuật.
FFR cho bác sĩ tim mạch can thiệp một cách nhìn khách quan hơn
về khả năng gây thiếu máu cục bộ cơ tim của một tổn thương hẹp lòng động mạch vành. Các nghiên cứu trước đây cũng đã nhận định tái tưới máu không hoàn toàn sẽ dẫn đến kết cục lâm sàng không tốt (5,6). FAME chọn giới hạn <0.80 để chẩn đoán một tổn thương có khả năng gây thiếu máu cục bộ cơ tim (các nghiên cứu trước đây về FFR thường chọn giá trị <0.75); điều này giúp tránh bỏ sót các tổn thương và có thể giúp tái tưới máu động mạch vành hoàn toàn.
5. KẾT LUẬN
Đo FFR một cách thường quy để hướng dẫn can thiệp qua da với stent phủ thuốc có thể cải thiện tiên lượng của bệnh nhân hẹp nhiều nhánh động mạch vành. Kết quả nghiên cứu FAME ủng hộ quan điểm, “Tái tưới máu động mạch vành hoàn toàn các tổn thương gây thiếu máu cục bộ cơ tim; điều trị nội khoa các tổn thương không gây thiếu máu cục bộ cơ tim”.
Tài liệu tham khảo
1. Pijls NHJ, De Bruyne B, Peels K, et al. Measurement of fractional flow reserve to assess the functional severity of coronary artery stenosis. N Engl J Med 1996;334:1703-1708.
2. Bech GJW, De Bruyne B, Bonnier HJRM, et al. Long-term follow-up after deferral of percutaneous transluminal coronary angioplasty of intermediate stenosis on the basis of coronary pressure measurement. J Am Coll Cardiol 1998;31:841-847.
3. Tonino PAL, De Bruyne B, Pijls NHJ, et al. Fractional Flow Reserve versus Angiography for Guiding Percutaneous Coronary Intervention. N Engl J Med 2009;360:213-24.
4. http://www.clinical trialresults.org/Slides/FAME%202%20yr%20 LBT%20TCT2009.ppt
5. Hannan EL, Racz M, Holmes DR, et al. Impact of completeness of percutaneous coronary intervention on long-term outcomes in the stent era. Circulation 2006;113:2406-12.
6. Teirstein PS. The dueling hazards of incomplete revascularization and incomplete data. Circulation 2006;113:2380-2.