NGUYỄN DƯƠNG KHANG
NGUYỄN THANH HIỀN
I. Định nghĩa và phân loại suy tim
Cùng với việc nhận ra sự cần thiết phải chuẩn hóa định nghĩa suy tim, tiêu chuẩn toàn cầu về định nghĩa và phân loại suy tim đã ra đời. Theo đó, suy tim là một hội chứng lâm sàng với các triệu chứng và/hoặc dấu hiệu bây giờ hoặc trước đây, do bất thường cấu trúc và/hoặc chức năng của tim và có liên quan với tăng nồng độ natriuretic peptide (NP) hoặc các bằng chứng trực tiếp của sung huyết phổi hoặc sung huyết hệ thống do tim[1]. Cũng theo đó, phân loại giai đoạn suy tim cũng được cập nhật, với “Có nguy cơ suy tim” (trước đây là giai đoạn A) là những bệnh nhân có nguy cơ suy tim nhưng hiện tại hoặc trước đây không có triệu chứng hoặc dấu hiệu của suy tim và không có các thay đổi bệnh tim cấu trúc hoặc tăng dấu ấn sinh học bệnh tim. “Tiền suy tim” (trước đây là giai đoạn B) là những bệnh nhân hiện tại hoặc tiền căn không có dấu hiệu hoặc triệu chứng của suy tim nhưng có bằng chứng của bệnh tim cấu trúc, bất thường chức năng tim, tăng nồng độ NP hoặc tăng nồng độ troponin tim. “Suy tim” (trước đây là giai đoạn C) dành cho những bệnh nhân có triệu chứng; và “Suy tim nặng” (trước đây là giai đoạn D) dành cho những bệnh nhân có triệu chứng và/hoặc dấu hiệu suy tim nặng. Phân loại theo phân suất tống máu cũng có một số hiệu chỉnh: suy tim phân suất tống máu giảm (HFrEF) khi LVEF ≤ 40%; suy tim với phân suất tống máu giảm nhẹ (HFmrEF) khi LVEF 41 – 49%; suy tim với phân suất tống máu bảo tồn (HFpEF): LVEF > 50%; và suy tim với phân suất tống máu cải thiện (HFimpEF): suy tim với LVEF nền ≤ 40%, có tăng LVEF ≥ 10% so với nền, và trị số LVEF sau tăng là > 40%. Trong định nghĩa toàn cầu về suy tim, họ cũng nhấn mạnh việc dùng “suy tim trường diễn” thay vì “suy tim ổn định” với những bệnh nhân còn triệu chứng/dấu hiệu suy tim; và “suy tim đang thuyên giảm” thay vì “suy tim hồi phục” dành cho những bệnh nhân có sự phục hồi triệu chứng và dấu hiệu suy tim hoặc có sự phục hồi về bệnh tim cấu trúc/chức năng. Một định nghĩa thay thế và đơn giản hơn khi nói về suy tim là dựa vào NP, tuy vậy, hạn chế của cách tiếp cận này là việc nồng độ NP thay đổi nhiều theo tuổi, giới, khối lượng cơ thể, chức năng thận và rung nhĩ; cũng như thiếu tính đặc hiệu cũng như thiếu bằng chứng trong việc tiếp cận điều trị dựa trên dấu ấn sinh học [2].
II. Chẩn đoán và phân tầng nguy cơ
Với HFrEF, tiêu chuẩn chẩn đoán chính vẫn là LVEF ≤ 40% [3]. Còn những phân loại khác thì vẫn có những tranh cãi. Pieske và cộng sự [4] đưa ra một tiêu chuẩn chẩn đoán mới, bao gồm các số đo trên siêu âm tim, NP và nếu vẫn chưa đưa ra được chẩn đoán chắc chắn thì tiến hành các nghiệm pháp gắng sức và/hoặc thăm dò huyết động học.
Hiện nay, người ta ngày càng nhận ra rằng các phương phép chẩn đoán cổ điển không còn chính xác trong những bệnh lý phức tạp đa yếu tố với nhiều nguyên nhân và yếu tố khởi phát; và gần đây, nhiều nghiên cứu đã đặt ra vấn đề rằng liệu một phương thức tiếp cận mới, sử dụng những dữ liệu lớn được truy vấn bởi các công thức trên máy tính có ưu việt hơn trong chẩn đoán hay không. Những kỹ thuật này bao gồm học máy (machine learning – ML) và trí thông minh nhân tạo (artificial intelligence – AI). Peyster và cộng sự [5] sử dụng phân tích hình ảnh tự động để phát hiện thải ghép sau ghép tim và ghi nhận rằng “Computer-Assisted Cardiac Histologic Evaluation (CACHE)-Grader” không thua kém so với phân loại phân suất tống máu bằng các nhà giải phẫu bệnh độc lập. Một mảng nghiên cứu khác mà AI cung cấp là công cụ phân loại những bệnh nhân được chẩn đoán suy tim. Verdonschot và cộng sự [6] nghiên cứu 795 bệnh nhân bệnh cơ tim dãn với dữ liệu về nguyên nhân và bệnh đi kèm, hình ảnh học và sinh thiết nội mạc cơ tim, và xác định được 4 thể bệnh riêng biệt. Woolley và cộng sự [7] sử dụng một mô hình dựa trên 363 dấu ấn sinh học để phân loại, từ đó 429 bệnh nhân HFpEF được phân thành 4 nhóm với các chỉ số lâm sàng khác nhau và quan trọng là tiên lượng cũng khác nhau.
AI/ML có thể đặc biệt hữu ích trong chẩn đoán HF. Kwon và cộng sự đánh giá dữ liệu từ 34103 bệnh nhân được siêu âm tim và đo điện tâm đồ, từ đó thiết lập ra một thuật toán ML có thể phát hiện HFpEF. Segar và cộng sự [8] cũng áp dụng các công thức ML vào trong dự đoán các nguy cơ dựa trên chủng tộc trong chẩn đoán HF.
Trong tương lai gần, chúng ta sẽ có nhiều công cụ AL/ML có triển vọng hơn nữa vì càng ngày nhu cầu tiếp cận và xử trí dựa trên cá thể hóa ngày càng rõ rệt hơn [9]. Tuy vậy, điểm mấu chốt là phải có khuyến cáo về việc dữ liệu đầu vào tối thiểu cho các mô hình này là gì, cũng như các mô hình này cũng phải được thử nghiệm trong các bối cảnh độc lập. Hơn nữa, các quyết định điều trị dựa trên các mô hình thuật toán cũng phải được thử nghiệm theo cách phân nhóm ngẫu nhiên kinh điển [10].
* Hình ảnh học và dấu ấn sinh học
Hướng dẫn của ESC [3] khuyến cáo việc dùng thường quy các dấu hiệu và triệu chứng, hỗ trợ bằng hình ảnh học và dấu ấn sinh học. Hình ảnh học chủ yếu dựa trên siêu âm tim và MRI tim; còn dấu ấn sinh học thì NP và troponin siêu nhạy là các dấu ấn được ưu tiên sử dụng. Cách phân loại phức tạp dựa trên hỗ trợ của hình ảnh học và dấu ấn sinh học có thể giúp phân nhóm bệnh học chính xác hơn[6], [11] và các hình ảnh học không tại tim khác như mô mỡ cũng có thể giúp phân nhóm bệnh học suy tim[12], [13]. Hơn nữa, các phân tích về di truyền gần đây đã cho thấy khả năng tiên lượng [14] và chẩn đoán[15, 16] trong suy tim. Một bài báo gần đây cũng đề cập đến các chỉ định của sinh thiết nội mạc cơ tim [16].
III. Các tình huống cụ thể
- Suy tim cấp
Hướng dẫn của ESC 2021 không có nhiều thay đổi đáng kể trong khuyến cáo về suy tim cấp, ngoại trừ việc dùng opioids đã bị đưa xuống Class III [3]. Các bằng chứng tiếp tục ủng hộ việc sử dụng natri niệu trong đánh giá biến cố trong suy tim cấp [17], [18].
- Sốc tim
Tử suất trong sốc tim vẫn còn cao, và các thử nghiệm ngẫu nhiên đánh giá các phương thức điều trị là còn ít ỏi; trong đó một nghiên cứu ngẫu nhiên đơn trung tâm ở những bệnh nhân sốc tim chia thành nhóm dùng milrinone hoặc nhóm dobutamine lại không có kết quả khác biệt nào ở cả biến cố chính và phụ [19]. Khi theo dõi nghiên cứu IMPRESS ở những bệnh nhân sốc tim, người ta ghi nhận không có sự khác biệt trong tỉ lệ tử vong khi so sánh giữa việc dùng bóng đối xung nội động mạch chủ hay Impella sau 5 năm [20]. Việc dùng gộp các dấu ấn sinh học được chứng minh là tốt hơn các thang điểm nguy cơ cho sốc tim khác. Thang điểm gộp này gồm 4 dấu ấn sinh học: Cystatin C, Lactate, Interleukin-6 và NT-proBNP [21].
- Dụng cụ hỗ trợ thất trái và ghép tim
Một nghiên cứu sổ bộ ghi nhận kết cục của HeartMate III (HMIII) tốt hơn nhóm chứng đã giúp thúc đẩy việc tiến hành các nghiên cứu ngẫu nhiên [22]. Tần suất đột quỵ với HMIII thấp hơn dụng cụ hỗ trợ thất trái Heartware (HVAD) – cũng là một trong số những nguyên nhân HVAD bị rút khỏi thị trường [23]. Nhưng thất vọng là việc dùng LVAD không giúp cải thiện xơ hóa cơ tim cũng như việc thang điểm nguy cơ mới không giúp cải thiện dự đoán suy thất phải sau LVAD. Nhưng nhìn về mặt tươi sáng hơn, những bệnh nhân lớn tuổi có thể có lợi trong cải thiện chất lượng cuộc sống và khả năng gắng sức với LVADs [24], [25], [26]. Các phương pháp không xâm lấn dự đoán về thải ghép ở bệnh nhân ghép tim còn chưa rõ ràng, nhưng các nghiên cứu sử dụng DNA không tế bào ở máu ngoại biên đã cho một số kết quả sớm đáng mong đợi [27].
- Thai phụ/những bệnh nhân bệnh cơ tim chu sinh
Những phụ nữ đã biết bệnh cơ tim trước đó hoặc có nguy cơ suy tim và đang dự định mang thai, hoặc có biểu hiện suy tim trong hoặc sau thai kỳ đều cần được đánh giá và tư vấn cá thể hóa trước, trong và sau thai kỳ [28].
Những bệnh nhân bệnh cơ tim chu sinh có nguy cơ biến cố nặng [29], [30] nhưng thường hồi phục sau HFrEF. Gần đây, đã có nhưng nghiên cứu đánh giá giá trị của các bất thường trên ECG trong dự đoán kết quả siêu âm tim và vai trò của tăng huyết áp trong thai kỳ [31], [32].
- Bệnh cơ tim phì đại/amyloidosis
Trong nghiên cứu EXPLORER-HCM, mavacamten cải thiện rõ rệt tình trạng của những bệnh nhân bệnh cơ tim phì đại tắc nghẽn có triệu chứng (HCM) khi so với nhóm chứng [33]. Pelliccia và cộng sự [34] đã tổng hợp lại các điểm còn thiếu trong bằng chứng về phân nhóm nguy cơ đột tử do tim ở bệnh nhân HCM. Trong một nghiên cứu của Marston và cộng sự [35] sử dụng sổ bộ Sarcomeric Human Cardiomyopathy, những bệnh nhân khởi phát HCM thời thơ ấu sẽ dễ mắc bệnh lý sarcomeric hơ, có nguy cơ rối loạn nhịp thất đe dọa tính màng hơn, và cần đa số cần được điều trị suy tim tích cực. Trong một thông cáo của Hội Tim Đức, Yilmaz và cộng sự [36] đưa ra một sơ đồ chẩn đoán để phát hiện amyloidosis tim, để xác định chính xác mức độ tiến triển, và để xác định chính xác subtype của amyloidosis, từ đó đưa ra trị liệu trúng đích phù hợp.
- Ung thư
Suy tim thường làm phức tạp trị liệu ung thư, và đồng thời một thông cáo gần đây đã đưa ra các tiêu chuẩn về độc tính trên tim mạch của các phương pháp trị liệu ung thư [37]. Kinh điển thì hóa trị và xạ trị đều được xem là các yếu tố nguy cơ, nhưng trong thập kỷ gần đây, liệu pháp dùng miễn dịch cũng như các thuốc ức chế điểm miễn dịch (ICIs) đã trở thành phương pháp điều trị ung thư chủ yếu. Tuy nhiên, ICI lại cũng mang nguy cơ tác dụng phụ trên tim mạch. D’Souza và cộng sự [38] đã báo cáo nguy cơ này trong sổ bộ Đan Mạch và cho thấy ICI liên quan với 1.8% nguy cơ 1 năm của viêm cơ tim (± màng ngoài tim), và với gần 10% nguy cơ của biến cố tim mạch bất kỳ. Vì việc sử dụng ICIs ngày càng tăng, vấn đề này sẽ cần các hướng dẫn lâm sàng và các nghiên cứu sâu hơn, vì ICIs có tác động trên nhiều mô và tế bào [39], [40]. Đã có những báo cáo hướng dẫn điều trị viêm cơ tim do ICI [41], [42].
Lãnh vực này đã làm tăng nhận thức rằng ung thư thường gặp ở những bệnh nhân suy tim [43], và suy tim cùng ung thư có thể có mối liên hệ gần hơn chúng ta vẫn nghĩ. Ren và cộng sự [44] ghi nhận rằng việc dùng statin giúp giảm nguy cơ xuất hiện ung thư. Cuối cùng, một bài báo của Zannad và cộng sự [45] đã đưa ra bàn luận về các mặt của một nghiên cứu về ung thư có thể áp dụng được trong nghiên cứu về suy tim, với mục tiêu thúc đẩy tiến trình nghiên cứu lâm sàng và giảm thời gian cũng như chi phí để đưa các liệu pháp điều trị an toàn, hiệu quả đến với bệnh nhân suy tim.
IV. Điều trị dùng thuốc
- Lưu đồ điều trị dùng thuốc mới cho suy tim phân suất tống máu giảm
Hướng dẫn 2021 của ESC về suy tim đưa ra khuyến cáo Class I cho các điều trị dùng thuốc ở tất cả các bệnh nhân HFrEF với phối hợp 1 loại ức chế men chuyển (ACEi) hoặc ức chế thụ thể neprilysin angiotensin (ARNi), một loại chẹn beta, một loại đối vận thụ thể mineralcorticoid (MRA), và một loại ức chế kênh đồng vận Na-Glucose (SGLT2i) [3]. Hướng dẫn này vẫn khuyến cáo việc dùng ARNi là một lựa chọn thay thế cho ACEi; tuy vậy, ARNi cũng có thể được cân nhắc là lựa chọn đầu tay thay vì ACEi. Hướng dẫn này cũng khuyến cáo rằng 4 loại thuốc này nên được khởi đầu cùng 1 khoảng thời gian [3], [46]. Theo một phân tích của Vaduganathan và cộng sự (2020), việc dùng chiến lược 4 thuốc ở một bệnh nhân HfrEF 55 tuổi sẽ mang lại 8,3 năm không bị tử vong tim mạch hoặc nhập viện lần đầu vì suy tim; và thêm 6,3 năm sống còn so với việc dùng kết hợp thông thường là một ACEi và một chẹn beta. Có một lưu đồ dùng thuốc tiếp nối cũng có nhiều tiềm năng là lưu đồ của McMurray và Packer [47] với chẹn beta và SGLT2i là các thuốc khởi đầu. Tuy vậy, mặc dù đứng về mặt sinh lý bệnh thì có vẻ hấp dẫn nhưng lưu đồ này vẫn chưa được hỗ trợ bởi các bằng chứng khoa học.
Một đồng thuận gần đây của HFA/ESC đã xác định 9 nhóm bệnh nhân phù hợp vơi các điều trị suy tim của ESC, với các yếu tố được đưa vào cân nhắc gồm tần số tim, rung nhĩ, huyết áp thấp có triệu chứng, độ lọc cầu thận ước đoán, hay tăng Kali máu. Sử dụng các phương thức tiếp cận cá thể hóa này có thể giúp có những điều trị tốt hơn và hiệu quả hơn cho mỗi bệnh nhân [48].
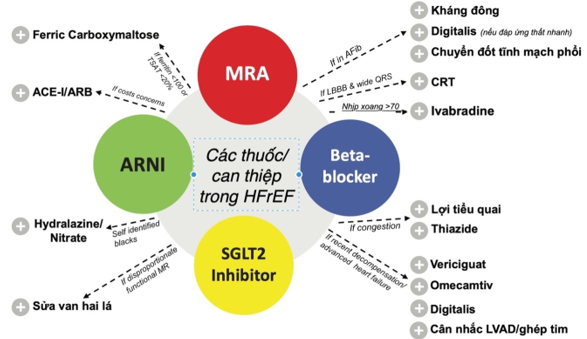
Hình 1. Thuốc và các can thiệp điều trị suy tim phân suất tống máu giảm [52]
- Ức chế men chuyển
ACEi vẫn là nền tảng trong điều trị và phòng ngừa suy tim trong nhiều năm qua, tuy vậy, tác động của loại thuốc này trong điều trị suy tim ở những bệnh nhân bị loạn dưỡng cơ Duchenne là còn chưa rõ ràng. Một sổ bộ lớn tại Pháp cho thấy việc điều trị dự phòng với ACEi ở những bệnh nhân không có suy chức năng thất trái có thể giúp ngăn ngừa việc tiến triển thành suy tim và cải thiện tiên lượng sống còn ở những bệnh nhân loạn dưỡng cơ Duchenne [49].
- ARNi (PARAGON, PARADIGM, PARALLAX, PARADISE-MI, LIFE)
Nghiên cứu PARADIGM-HF đã cho thấy việc khởi đầu sacubitril/valsartan, ngay cả khi tăng đến liều đích, không làm thay đổi liều hay làm ngưng dùng các thuốc có lợi trong suy tim khác và cũng không làm ảnh hưởng đến việc dùng MRA [50]. Trong thế giới thực, sacubitril/valsartan được chứng minh là có hiệu quả, an toàn và dung nạp tốt [51], [52], [53], [54]. Sacubitril/valsartan cũng được chứng minh có lợi trong điều trị tăng huyết áp kháng trị ở bệnh nhân HFpEF trong nghiên cứu PARAGON-HF khi so sánh với valsartan [55]. Trong nghiên cứu PROVE-HF, những bệnh nhân HFrEF thì có 32% cải thiện EF đến > 35% sau 6 tháng và 62% cải thiện > 35% sau 12 tháng khởi đầu sacubitril/valsartan [56]. Ở những bệnh nhân có suy chức năng tâm thu thất trái không triệu chứng muộn sau nhồi máu cơ tim, việc dùng sacubitril/valsartan không làm cải thiện tái cấu trúc có tim so với valsartan [57], [58]. Trong nghiên cứu PARADISE-MI [59], sacubitril/valsartan không làm giảm đáng kể tần suất tử vong tim mạch, nhập viện do suy tim hay điều trị suy tim ngoại trú ở những bệnh nhân LVEF ≤ 40% và/hoặc sung huyết phổi sau nhồi máu cơ tim cấp khi so sánh với ramipril. Trong nghiên cứu LIFE-HF thu nhận bệnh nhân suy tim NYHA IV và LVEF ≤ 35%, sacubitril/valsartan không cải thiện kết cục lâm sàng gộp. Nghiên cứu PARALLAX sẽ cho kết quả liệu sacubitril/valsartan có cải thiện nồng độ NT-proBNP, khả năng gắng sức, chất lượng cuộc sống và gánh nặng triệu chứng ở những bệnh nhân suy tim EF > 40% hay không [60].
Trong Hướng dẫn đầu năm 2022 của Hội Tim Hoa Kỳ về quản lý bệnh nhân suy tim, việc dùng ARNi được khuyến cáo để giảm bệnh suất và tử suất ở nhóm bệnh nhân HFrEF có NYHA II – III [61].
- Ức chế đồng vận Na-Glucose 2 (EMPEROR-Reduced, EMPEROR-Preserved, DAPA-HF, SOLOIST)
SGLT2i đang nhanh chóng trở thành thuốc quan trọng trong toàn bộ thể bệnh chuyển hóa tim mạch và thận. Trong những nghiên cứu về đái tháo đường type 2 (T2DM), tác dụng có lợi về kết cục tim mạch nói chung đã được chứng minh, còn tác động có lợi trên suy tim là rất đáng kể. Những tác động này đã được kiểm định ở nhóm bệnh nhân HFrEF trong nghiên cứu DAPA-HF và sau đó 1 năm là nghiên cứu EMPEROR-Reduced. Một số phân tích dưới nhóm từ các nghiên cứu này cũng đã được công bố vào năm 2021.
Đầu tiên, bên cạnh tác động có lợi trên các kết cục chính, càng ngày, tác động trên chức năng sống và triệu chứng ở các bệnh nhân HFrEF càng được ghi nhận [62]. Các tác động có lợi này đều được quan sát trong hai nghiên cứu DAPA-HF và EMPEROR-Reduced [63], [64], dù một nghiên cứu nhỏ hơn với empagliflozin lại không ghi nhận cải thiện chức năng sống [65]. Một số phân tích dưới nhóm cho thấy không có tương tác giữa SGLT2i với các thuốc suy tim thông thường, như MRAs, và quan trọng nhất là với sacubitril/valsartan [66], [67]. Hơn nữa, các tác động này đều tương tự khi phân tích ở nhiều quốc gia và nhiều chủng tộc [68]. Một lợi ích đáng kể nữa của dapagliflozin là giảm tần suất đái tháo đường mới mắc [69]. Lợi ích của dapagliflozin trên kết cục chính gồm tử vong tim mạch hoặc suy tim nặng lên và các kết cục phụ là tương tự nhau ở nhóm bệnh nhân có dùng hoặc không dùng sacubitril/valsartan. Tựu trung lại, đến thời điểm này, chúng ta chưa thấy bất kỳ phân tích nào cho thấy SGLT2i kém hiệu quả trong điều trị HfrEF. Do đó, việc của các bác sĩ bây giờ là bắt đầu sử dụng nhóm thuốc này trong thực hành lâm sàng.
Khác với nhóm HfrEF, hiệu quả của nhóm ức chế SGLT2 còn chưa rõ rệt ở dân số HfpEF. Tuy vậy, kết quả của nghiên cứu EMPEROR-Preserved trình bày tại ESC 2021 cho thấy empagliflozin làm giảm kết cục gộp gồm tử vong do tim mạch và nhập viện vì suy tim ở gần 6000 bệnh nhân HfpEF. Những dữ kiện này vô cùng quan trọng và đưa đến hi vọng cho hàng triệu bệnh nhân HfpEF, cũng là nhóm dân số chưa từng có trị liệu nào được chứng minh hiệu quả. Trong thời gian theo dõi trung bình 26 tháng, kết cục chính xảy ra ở 13,8% nhóm dân số empagliflozin và ở 17,1% nhóm dân số chứng (HR: 0,79; 95% CI: ,69 – 0,90, P < 0,001). Empagliflozin rất hiệu quả trong giảm nhập viện do suy tim, nhưng không làm giảm tử vong chung. Hiệu quả của empagliflozin là đồng nhất ở nhóm có hay không có đái tháo đường [65]. Nghiên cứu của dapagliflozin trong nhóm dân số HfpEF, DELIVER, cũng sẽ được công bố trong thời gian gần nhất [70].
Thuốc ức chế SGLT2 cũng được thử nghiệm trong nhóm bệnh nhân suy tim cấp hoặc ngay sau đợt mất bù cấp của suy tim. Nghiên cứu SOLOIST [71], với stagliflozin là thuốc ức chế SGLT 1/2, thu nhận 1244 bệnh nhân T2DM và vừa nhập viện vì suy tiim nặng lên cho thấy tác dụng có lợi của thuốc, khởi động trước hoặc ngay sau xuất viện, với giảm đáng kể con số tử vong do tim mạch và nhập viện do suy tim và tái khám sớm vì suy tim. Nghiên cứu EMPULSE đã cho thấy ở những bệnh nhân nhập viện vì đợt mất bù cấp suy tim, empagliflozin có liên quan với cải thiện kết cục lâm sàng đáng kể so với nhóm chứng tại thời điểm 90 ngày [72]. Nghiên cứu này thu nhận những bệnh nhân bất kể phân suất tống máu và bất kể có đái tháo đường hay không. Empagliflozin còn làm giảm tử vong, cải thiện chất lượng cuộc sống, và giảm số kg cân nặng đáng kể. Một điểm đặc sắc nữa là không có lo ngại gì về độ an toàn của empagliflozin.
Thuốc ức chế SGLT2 còn có lợi trong nhóm bệnh thận. Sau khi nghiên cứu CREDENCE và DAPA-CKD công bố kết quả; trong năm 2021, nghiên cứu SCORED cũng thu nhận nhóm bệnh nhân T2DM và bệnh thận mạn, phân nhóm sotagliflozin hoặc nhóm chứng, cho thấy giảm 37% kết cục chính gồm tử vong do tim mạch và biến cố suy tim (HR 0,74; 95% CI: 0,63 – 0,88; P < 0,001). Tuy vậy, sotagliflozin có liên quan với các tác dụng phụ như tiêu chảy, nhiễm khuẩn niệu dục, mất dịch và nhiễm toan ceton đái tháo đường.
- Đối kháng thụ thể mineralcorticoid (FIDELIO, FIGARO, HOMAGE)
Thuốc đối kháng thụ thể mineralcorticoid là nhóm thuốc đầu tay trong điều trị HfrEF và cũng có thể được cân nhắc trong nhóm HfmrEF [3]. Các thuốc MRA không steroid mới như finerenone khác biệt với các thuốc MRA steroid ở đặc điểm phân bố vào mô, gắn kết với thụ thể, kích hoạt các loại đồng vận, và giảm biểu hiện gen [73]. Trong nghiên cứu FIDELIO-DKD, finerenone cải thiện kết cục tim mạch và thận ở nhóm bệnh nhân bệnh thận mạn và T2D bất kể tình trạng suy tim nền. Trong nghiên cứu FIGARO-DKD, finerenone làm giảm các kết cục chính gồm tử vong do nguyên nhân tim mạch, nhồi máu cơ tim không tử vong, đột quỵ không tử vong, hoặc nhập viện vì suy tim với lợi ích chủ yếu đến từ giảm tần suất nhập viện vì suy tim [74]. Trong nghiên cứu HOMAGE, những bệnh nhân đã có, hoặc nguy cơ cao, bệnh mạch vành và tăng nồng độ natriuretic peptides, thì không ghi nhận tương tác nào giữa galectin-3 trong máu hay thay đổi procollagen collagen khi điều trị với spironolactone. Tuy vậy, spironolactone giúp giảm huyết áp và NT-proBNP [75].
- Kích hoạt soluble guanylate cyclase (VICTORIA)
Thuốc hoạt hoá soluble guanylate cyclase mới, vericiguat, trong một phân tích dưới nhóm của nghiên cứu VICTORIA đã không làm giảm được tỉ lệ rung nhĩ mới xuất hiện. Tuy vậy, rung nhĩ đã có trước đó không ảnh hưởng đến tác động có lợi của vericiguat trên kết cục gộp chính (thời gian đến tử vong do tim mạch hoặc nhập viện vì suy tim đầu tiên) hoặc từng thành phần trong kết cục đó [76]. Tương tự như vậy, tác động có lợi của vericiguat là tương đồng trong tất cả các phân nhóm dựa trên chức năng thận [77].
- Hoạt hoá myosin tim
Một phân nhóm của nghiễn cứu GALACTIC-HF trên bệnh nhân HfrEF cho thấy thuốc này làm giảm kết cục chính gồm nhập viện vì suy tim và tử vong do tim mạch càng nhiều khi EF càng giảm, với giảm 17% trong nhóm EF =< 22% và không có lợi ở nhóm EF >= 33%.
- Ferric carboxymaltose (AFFIRM-AHF; IRON-CRT)
Thiếu sắt có liên quan với kết cục xấu trong suy tim. Nghiên cứu AFFIRM-AHF cho thấy ở những bệnh nhân có LVEF <40% và thiếu sắt sau một lần nhập viện vì suy tim cấp thì điều trị ferric carboxymaltose đường tĩnh mạch không chỉ làm giảm nhập viện vì suy tim mà còn đưa đến tác động có lợi đáng kể trên lâm sàng về chất lượng cuộc sống [78]. Trong nhóm dân số HFrEFF có thiếu sắt và LVEF < 45% trường diễn sau khi tái đồng bộ tim (IRON-CRT) thì ferric carboxymaltose IV giúp cải thiện cấu trúc và chức năng thất, cũng như chất lượng cuộc sống [79].
Thiếu sắt cũng góp phần vào kháng trị với erythropoietin, cũng là một nguyên nhân quan trọng gây thiếu máu trong suy tim.
- Khác
Trong một nghiên cứu lâm sàng nhỏ, CDR132L, là một loại thuốc antisense oligonucleotide tác động trực tiếp trên miR-132 cho thấy tính dung nạp tốt và dường như cải thiện chức năng tim ở bệnh nhân suy tim [80], [81], [82].
Trong 50 bệnh nhân bệnh cơ tim dãn mạn tính vô căn và có nhiễm parvovirus B19, liệu pháp miễn dịch IV không cải thiện đáng kể chức năng tâm thu thất trái hoặc khả năng gắng sức hơn điều trị nội khoa tiêu chuẩn [43].
V. Dung mạo bệnh nhân suy tim và hướng điều trị
- Bệnh nhân có huyết áp thấp và tần số tim cao
Chưa có định nghĩa rõ rệt thế nào là huyết áp thấp trong suy tim. Dù vậy, trị số < 90mHg vẫn thường được xem là huyết áp tâm thu thấp. Tuy nhiên, ở những bệnh nhân có bệnh mạch vành sẵn có, khuyến cáo giữ huyết áp tâm thu > 120 mmHg [83]. Hình thái huyết áp thấp và tần số tim cao là hình thái hiếm gặp ở ngoại trú, và cần được đánh giá các nguyên nhân gây huyết áp thấp khác, như thiếu dịch, chảy máu hay nhiễm trùng. Tất cả các thuốc không dùng cho suy tim đều cần được đánh giá lại, như việc dùng nitrates, chẹn kênh calci hay các thuốc giãn mạch khác. Nếu bệnh nhân bình thể tích, việc giảm hoặc ngưng lợi tiểu có thể được cân nhắc, và cần theo dõi sát trong các ngày tiếp theo để tránh ứ dịch. Điều chỉnh các thuốc trong bộ 4 và liều của các thuốc này chỉ nên xem xét nếu bệnh nhân có tụt huyết áp có triệu chứng. Tần số tim thấp có liên quan với cải thiện sống còn trong HfrEF và nhịp xoang, và kết cục có lợi nhất được quan sát thấy ở nhóm tần số tim khoảng 60 lần/phút [84]. Thuốc chẹn beta là một phần cốt lõi của điều trị HfrEF, và nên được tăng liều đến liều tối đa hoặc tối ưu theo nghiên cứu. Trong nghiên cứu COPERNICUS, ở những bệnh nhân có huyết áp tâm thu 85 – 95mmhg, chưa ghi nhận bằng chứng của huyết áp giảm thêm khi dùng chẹn beta so với nhóm chứng. Những bệnh nhân này thuộc nhóm nguy cơ cao nhất gặp biến cố, và sẽ nhận được lợi ích tuyệt đối nhiều nhất từ việc dùng chẹn beta [85]. Trong nghiên cứu CARVIVA HF, việc phối hợp một chẹn beta với ivabradine cho phép bệnh nhân đạt được liều cao hơn của từng thuốc, hơn là tăng liều từng loại thuốc [49]. Trong nhóm bệnh nhân tụt huyết áp có triệu chứng, và sau khi cần nhắc ngưng các thuốc hạ áp không cần thiết, việc giảm hoặc thậm chí ngưng chẹn beta có thể sẽ cần thiết. Trong tình huống này, ivabradine là một lựa chọn quan trọng. MRAs và SGLT2i có tác động rất ít trên huyết áp, nên việc ngưng thuốc sẽ không cần thiết [86], [87], [88]. Việc dùng sacubitril/valsartan là chống chỉ định trong nhóm bệnh nhân có huyết áp tâm thu < 100mmHg.
- Bệnh nhân có huyết áp thấp và tần số tim thấp
Cần cân nhắc các nguyên nhân gây tụt huyết áp khác và các thuốc khác như trong mục V.1. Việc thay đổi điều trị bộ 4 chỉ nên được xem xét khi tụt huyết áp có triệu chứng. MRAs và SGLT2i có tác động rất ít trên huyết áp, nên việc ngưng thuốc là không cần thiết. Việc giảm liều BB có thể cần thiết nếu tần số tim < 50 l/p, hoặc khi nhịp chậm có triệu chứng.
- Bệnh nhân có huyết áp bình thường và tần số tim thấp
Thuốc có tác động giảm tần số tim nên được cân nhắc lại kỹ lưỡng và nếu có thể thì ngưng, như chẹn kênh calci non-DHP (diltiazem và verapamil), digoxin hoặc thuốc chống rối loạn nhịp. Nếu bệnh nhân đang dùng ivabradine thì nên giảm liều hoặc ngưng nếu tần số tim < 50 l/p hoặc bệnh nhân có nhịp chậm có triệu chứng. Tiếp theo đó, những bệnh nhân có nhịp chậm hoặc tần số tim < 50 l/p nên được giảm liều BB.
- Bệnh nhân có huyết áp bình thường và tần số tim cao
Những bệnh nhân này nên được điều trị với BB ở liều đích. Nếu tần số tim > 70 l/p và nhịp xoang thì việc dùng BB phối hợp với ivabradine sẽ dễ kiểm soát tần số tim hơn và đỡ tăng liều BB hơn với tác dụng phụ thấp hơn. ACEi/ARB hoặc ARNI nên được tăng liều đến liều đích ở những bệnh nhân HfrEF vì liều cao hơn sẽ mang thêm lợi ích so với liều thấp hơn. Ở những bệnh nhân nội trú, chúng ta nên cân nhắc khởi động vericiguat trước xuất viện.
- Bệnh nhân rung nhĩ và huyết áp bình thường
Tần số thất khi nghỉ tối ưu ở những bệnh nhân suy tim rung nhĩ vẫn chưa được xác định chính xác, tuy vậy sẽ nằm trong khoảng 60 – 80 l/p [89]. Ngược với các bệnh nhân nhịp xoang, tần số tim không phải yếu tố tiên lượng tử vong trong những bệnh nhân HfrEF rung nhĩ. Chưa có chứng cứ rõ ràng về lợi ích trong tiên lượng khi dùng BB ở những bệnh nhân suy tim rung nhĩ [90], [91]. Các nỗ lực tăng liều BB đến liều tối đa có thể dung nạp được có thể đưa đến tác động có hại, vì tần số thất < 70 l/p được ghi nhận đưa đến kết cục xấu. Kháng đông luôn được chỉ định ở những bệnh nhân rung nhĩ trừ khi nguy cơ vượt quá lợi ích hoặc khi những thuốc này có chống chỉ định tuyệt đối.
- Bệnh nhân rung nhĩ và huyết áp thấp
Như đã đề cập, những bằng chứng về lợi ích của BB trên bệnh suất và tử suất thì kém mạnh hơn, nên BB có thể được ngưng hoặc giảm liều nếu cần thiết. Digoxin có thể dùng trong những tình huống này thay cho BB để kiểm soát tần số thất vì nó không có ảnh hưởng trên huyết áp. Nên duy trì một tần số tim > 70 l/p. Chiến lược này có thể giúp khởi động hoặc tăng liều thuốc có tác động trên bệnh suất và tử suất, như ACEi hoặc ARNI. MRAs và SGLT2i có tác động rất ít trên huyết áp, do vậy không cần thiết ngưng các loại thuốc này. Bệnh nhân suy tim có rung nhĩ luôn nên được dùng kháng đông, ưu tiên NOAC trừ khi có chống chỉ định.
- Bệnh nhân bệnh thận mạn
Hầu như tất cả RCTs đều loại trừ các bệnh nhân CKD nặng, làm hạn chế các bằng chứng về lợi ích và tính an toàn của các thuốc trong bối cảnh này. Dữ liệu sổ bộ cho thấy những bệnh nhân được lợi từ bộ 4 bị loại trừ khỏi các nghiên cứu vì những lý do đặc biệt, như CKS với eGFR > 30 mL/phút/1,73m2. ACEi/ARB/ARNI chỉ nên ngừng khi creatinine tăng > 100% hoặc > 3,5 mg/dL, hoặc eGFR < 20 mL/phút/1,73m2. BB có thể dùng an toàn với bệnh nhân có eGFR xuống tới 30 mL/phút/1,73m2, với lợi ích trên sống còn rõ rệt. MRAs có thể dùng khi eGFR >30 mL/phút/1,73m2 với Kali =< 5,0 mEq/L, với nguy cơ tăng Kali máu và tăng creatinine máu thấp. Kiểm tra Kali máu nên được tiến hành 1 – 4 tuần sau khi khởi động hoặc tăng liều MRA, và hàng tháng sau đó. Sacubitril/valsartan có thể dùng đến khi eGFR < 30 mL/phút/1,73m2. Dapagliflozin và empagliflozin được chứng minh có lợi và an toàn trong cải thiện kết cục về tim mạch và thận ở bệnh nhân có eGFR >20 – 25 mL/phút/1,73m2. Tuy vậy, có bằng chứng hiệu quả của dapagliflozin ở cả nhóm bệnh nhân eGFR < 20 mL/phút/1,73m2. Việc giảm nhẹ eGFR trong những ngày đầu sau khởi động một SGLT2i không nên là lý do để ngưng thuốc, vì hiện tượng giảm eGFR này lại liên quan với lợi ích lâu dài trên chức năng thận [92]. Thuốc mới như vericiguat và omecamtiv mecarbil có thể lần lượt dùng cho bệnh nhân eGFR >15 mL/phút/1,73m2 và eGFR >20 mL/phút/1,73m2. Các thuốc khác có thể làm tệ hơn chức năng thận (như NSAIDs) do đó điều quan trọng là đảm bảo những thuốc này không được dùng khi không có chỉ định. Thuốc gắn Kali (patiromer và sodium zirconium cyclosilicate) đã cho thấy hiệu quả trong giảm Kali máu ở những bệnh nhân suy tim và CKS được dùng RAASi[93], [94]. Tuy vậy, vẫn chưa có bằng chứng về tác động có lợi trên tiên lượng của các loại thuốc này.
- Bệnh nhân trước xuất viện
Trong thời gian nằm viện, những bệnh nhân này có thể đã được điều trị ổn định nhưng vẫn còn sung huyết nhẹ. Một tỉ lệ 30% những bệnh nhân suy tim nhập viện được xuất viện với triệu chứng lâm sàng của sung huyết tồn lưu, đặc biệt ở những người có hở van 3 lá, đái tháo đường, hay thiếu máu [95]. Nếu những bệnh nhân này chưa được dùng BB tại thời điểm hiện tại, thì không nên đưa BB vào điều trị đầu tay, vì khởi động BB ở bệnh nhân sung huyết có thể dẫn tới lâm sàng nặng nề hơn. ACEi hoặc ARNI ở những bệnh nhân đã được dùng ACEi với liều phù hợp rồi, nên được khởi động ở những bệnh nhân có huyết áp tâm thu lần lượt là > 90 hoặc > 100 mmHg. MRAs và SGLTs có thể được dùng an toàn, ngay cả ở những bệnh nhân sung huyết và huyết áp thấp.
Empagliflozin dung nạp tốt ở những bệnh nhân này, và làm giảm kết cục gộp gồm suy tim nặng lên, tái nhập viện vì suy tim hoặc tử vong trong 60 ngày. Ở những bệnh nhân đái tháo đường nhập viện vì suy tim [71], sotagliflozin và Empagliflozin làm giảm kết cục gộp gồm tử vong tim mạch, nhập viện hay tái khám sớm vì suy tim, nếu được khởi động trước hoặc ngay sau xuất viện.
- Bệnh nhân huyết áp cao dù đã dùng bộ 4
Ở những bệnh nhân tăng huyết áp, quan trọng là phải đảm bảo bệnh nhân không dùng bất kỳ thuốc nào có thể làm tăng huyết áp (như NSAID, corticoid hay dãn phế quản). Việc tuân thủ dùng thuốc cần được kiểm tra, và có thể cân nhắc dùng liều cao hơn. Nếu bệnh nhân vẫn còn tăng huyết áp dù đã dùng bộ 4 ở liều tối ưu thì phối hợp ISDN/Hydralazine có thể được dùng để đạt mục tiêu kiểm soát huyết áp. Nếu không cải thiện, có thể phối hợp với ưc chế kênh calcium dihydro-pyridine (amlordipine, folodipine…)
VI. Can thiệp và dụng cụ
- CRT
Ở bệnh nhân suy tim, rung nhĩ và QRS hẹp có tỉ lệ tử vong và nhập viện vì suy tim giảm đi khi cắt đốt nút nhĩ thất và đặt CRT so với việc điều trị nội khoa đơn thuần; tác động có lợi này là tương tự ở cả nhóm LVEF =< 35% và > 35% [96]. Tuy vậy, vẫn còn nhiều tranh cãi về việc dùng ICD thêm vào CRT có cho lợi ích hơn nữa về mặt sống còn hay không, đặc biệt ở nhóm bệnh nhân suy tim không do thiếu máu cục bộ [97].
- Sửa van hai lá qua da
Khuyến cáo của Hoa Kỳ cũng như của châu Âu về bệnh van tim gần đây đã nâng bậc khuyến cáo thay van hai lá qua ống thông (TEER) cho hở van hai lá thứ phát (cơ năng) lên thành IIa với những bệnh nhân thoả tiêu chí COAPT [98], [99]. Kết quả sau 3 năm của nghiên cứu COAPT cho thấy lợi ích liên tục của TEER. Một phân tích dứoi nhóm quan trọng của COAPT còn cho thấy hở van 2 lá thứ phát tồn lưu 3 – 4+ là yếu tố nguy cơ mạnh mẽ nhất của kết cục xấu trong cả nhóm TEER và nhóm điều trị nội khoa [100]. Với những bệnh nhân rung nhĩ, TEER làm giảm nguy cơ đột quỵ [101].
- Theo dõi huyết động dưới da
Nghiên cứu GUIDE-HF đánh giá quản lý bệnh nhân dựa trên huyết động học để giảm nhập viện do suy tim và tử vong ở những bệnh nhân NYHA II-IV và mọi phân suất tống máu. Phân tích tổng qua cho kết quả âm tính nhưng khi COVID-19 được đưa vào phân tích thì có giảm đáng kể nhập viện vì suy tim ở những bệnh nhân NYHA II-III đã có nhập viện vì suy tim trước đây hoặc có tăng natriuretic peptides [102].
VII. Suy tim trong dịch bệnh COVID-19
Biến cố suy tim cấp được ghi nhận là biến chứng trong 2%, tổn thương cơ tim trong 10% số bệnh nhân nhập viện vì COVID-19. NT-proBNP lúc nhập viện tăng cũng có liên quan với tăng tử vong [103], và các microRNAs đặc hiệu cho tim được tăng biểu hiện ở những bệnh nhân COVID-19 nguy kịch cũng chỉ ra tác động trên tim trong dịch bệnh này. Giảm tỉ lệ nhập viện chung vì suy tim [104] và tỉ lệ tử vong ngoại viện tăng cao [105] trong thời gian giãn cách xã hội là những vấn đề báo động, thể hiện sự thiếu tiếp cận với y tế ở những bệnh nhân suy tim đã biết. Các nghiên cứu ngẫu nhiên đã cho thấy việc tiếp tục dùng ACEi hay ARB ở những bệnh nhân nhập viện vì COVID-19 là vẫn an toàn. Dapagliflozin không làm giảm đáng kể suy chức năng cơ quan hay tử vong, nhưng dung nạp tốt ở những bệnh nhân nhập viện vì COVID-19 (DARE-19) [106]. Viêm cơ tim nổi lên là một biến chứng hiếm gặp của việc tiêm vaccine COVID-19 loại mRNA, đặc biệt ở nam trẻ [107]. Đánh giá lợi ích – nguy cơ của việc tiêm vaccine COVID-19 là nghiêng về lợi ích ở mọi lứa tuổi và giới tính; và gần như mọi bệnh nhân viêm cơ tim đều hồi phục triệu chứng sau ăn. Các biến chứng lâu dài của nhiễm SARS-CoV-2 bao gồm nhịp nhanh xoang kéo dài, hội chứng nhịp nhanh kịch phát tư thế đứng, rối loạn nhịp nhĩ, và bệnh cơ tim [108]. Với những vận động viên hồi phục sau nhiễm COVID-19, những nghiên cứu sử dụng MRI tim có báo cáo nhiều tỉ lệ cũng như nhiều mức độ bất thường tim nghĩ viêm cơ tim khác nhau [109], [110]. Tầm soát bằng troponin, ECG, siêu âm tim, và MRI tim và/hoặc siêu âm tim gắng sức nếu bất thường, trả về kết quả chỉ có 0,6% những vận động viên bị cấm quay trở lại thi đấu, cũng như không có ai bị biến cố tim mạch trong thời gian theo dõi. Mặc dù tổn thương cơ tim trong COVID-19 là thường gặp, và RNA SARS-CoV-2 có thể được phát hiện trong tim thì viêm cơ tim vẫn là một chẩn đoán về mặt giải phẫu bệnh hiếm gặp, chỉ trong 4,5% các trường hợp rất chọn lọc được tử thiết hoặc sinh thiết cơ tim.
TÀI LIỆU THAM KHẢO
- Bozkurt B, Coats AJS, Tsutsui H, Abdelhamid CM, Adamopoulos S, Albert N, et al. Universal definition and classification of heart failure: a report of the Heart Failure Society of America, Heart Failure Association of the European Society of Cardiology, Japanese Heart Failure Society and Writing Committee of the Universal Definition of Heart Failure: Endorsed by the Canadian Heart Failure Society, Heart Failure Association of India, Cardiac Society of Australia and New Zealand, and Chinese Heart Failure Association. Eur J Heart Fail. 2021;23(3):352-80. Epub 2021/02/20. PubMed PMID: 33605000.
- Cleland JGF, Pfeffer MA, Clark AL, Januzzi JL, McMurray JJV, Mueller C, et al. The struggle towards a Universal Definition of Heart Failure-how to proceed? Eur Heart J. 2021;42(24):2331-43. Epub 2021/04/02. PubMed PMID: 33791787.
- McDonagh TA, Metra M, Adamo M, Gardner RS, Baumbach A, Böhm M, et al. 2021 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure. Eur Heart J. 2021;42(36):3599-726. Epub 2021/08/28. PubMed PMID: 34447992.
- Pieske B, Tschöpe C, de Boer RA, Fraser AG, Anker SD, Donal E, et al. How to diagnose heart failure with preserved ejection fraction: the HFA-PEFF diagnostic algorithm: a consensus recommendation from the Heart Failure Association (HFA) of the European Society of Cardiology (ESC). Eur Heart J. 2019;40(40):3297-317. Epub 2019/09/11. PubMed PMID: 31504452.
- Peyster EG, Arabyarmohammadi S, Janowczyk A, Azarianpour-Esfahani S, Sekulic M, Cassol C, et al. An automated computational image analysis pipeline for histological grading of cardiac allograft rejection. Eur Heart J. 2021;42(24):2356-69. Epub 2021/05/14. PubMed PMID: 33982079; PubMed Central PMCID: PMCPMC8216729.
- Verdonschot JAJ, Merlo M, Dominguez F, Wang P, Henkens M, Adriaens ME, et al. Phenotypic clustering of dilated cardiomyopathy patients highlights important pathophysiological differences. Eur Heart J. 2021;42(2):162-74. Epub 2020/11/07. PubMed PMID: 33156912; PubMed Central PMCID: PMCPMC7813623.
- Woolley RJ, Ceelen D, Ouwerkerk W, Tromp J, Figarska SM, Anker SD, et al. Machine learning based on biomarker profiles identifies distinct subgroups of heart failure with preserved ejection fraction. Eur J Heart Fail. 2021;23(6):983-91. Epub 2021/03/03. PubMed PMID: 33651430; PubMed Central PMCID: PMCPMC8360080.
- Segar MW, Jaeger BC, Patel KV, Nambi V, Ndumele CE, Correa A, et al. Development and Validation of Machine Learning-Based Race-Specific Models to Predict 10-Year Risk of Heart Failure: A Multicohort Analysis. Circulation. 2021;143(24):2370-83. Epub 2021/04/14. PubMed PMID: 33845593.
- Hamdani N, Costantino S, Mügge A, Lebeche D, Tschöpe C, Thum T, et al. Leveraging clinical epigenetics in heart failure with preserved ejection fraction: a call for individualized therapies. Eur Heart J. 2021;42(20):1940-58. Epub 2021/05/06. PubMed PMID: 33948637; PubMed Central PMCID: PMCPMC8921660.
- Fraser AG, Tschöpe C, de Boer RA. Diagnostic recommendations and phenotyping for heart failure with preserved ejection fraction: knowing more and understanding less? Eur J Heart Fail. 2021;23(6):964-72. Epub 2021/05/01. PubMed PMID: 33928729.
- Raafs AG, Verdonschot JAJ, Henkens MTHM, Adriaans BP, Wang P, Derks K, et al. The combination of carboxy-terminal propeptide of procollagen type I blood levels and late gadolinium enhancement at cardiac magnetic resonance provides additional prognostic information in idiopathic dilated cardiomyopathy – A multilevel assessment of myocardial fibrosis in dilated cardiomyopathy. European Journal of Heart Failure. 2021;23(6):933-44.
- Sorimachi H, Obokata M, Takahashi N, Reddy YNV, Jain CC, Verbrugge FH, et al. Pathophysiologic importance of visceral adipose tissue in women with heart failure and preserved ejection fraction. Eur Heart J. 2021;42(16):1595-605. Epub 2020/11/24. PubMed PMID: 33227126; PubMed Central PMCID: PMCPMC8060057.
- Withaar C, Meems LMG, de Boer RA. Fighting HFpEF in women: taking aim at belly fat. Eur Heart J. 2021;42(16):1606-8. Epub 2020/12/15. PubMed PMID: 33313678.
- Assmus B, Cremer S, Kirschbaum K, Culmann D, Kiefer K, Dorsheimer L, et al. Clonal haematopoiesis in chronic ischaemic heart failure: prognostic role of clone size for DNMT3A- and TET2-driver gene mutations. Eur Heart J. 2021;42(3):257-65. Epub 2020/11/27. PubMed PMID: 33241418.
- Garnier S, Harakalova M, Weiss S, Mokry M, Regitz-Zagrosek V, Hengstenberg C, et al. Genome-wide association analysis in dilated cardiomyopathy reveals two new players in systolic heart failure on chromosomes 3p25.1 and 22q11.23. Eur Heart J. 2021;42(20):2000-11. Epub 2021/03/08. PubMed PMID: 33677556; PubMed Central PMCID: PMCPMC8139853.
- Seferović PM, Tsutsui H, McNamara DM, Ristić AD, Basso C, Bozkurt B, et al. Heart Failure Association, Heart Failure Society of America, and Japanese Heart Failure Society Position Statement on Endomyocardial Biopsy. J Card Fail. 2021;27(7):727-43. Epub 2021/05/23. PubMed PMID: 34022400.
- Tersalvi G, Dauw J, Gasperetti A, Winterton D, Cioffi GM, Scopigni F, et al. The value of urinary sodium assessment in acute heart failure. Eur Heart J Acute Cardiovasc Care. 2021;10(2):216-23. Epub 2021/02/24. PubMed PMID: 33620424; PubMed Central PMCID: PMCPMC8294841.
- Biegus J, Zymliński R, Fudim M, Testani J, Sokolski M, Marciniak D, et al. Spot urine sodium in acute heart failure: differences in prognostic value on admission and discharge. ESC Heart Fail. 2021;8(4):2597-602. Epub 2021/05/02. PubMed PMID: 33932273; PubMed Central PMCID: PMCPMC8318409.
- Gibson LE, Chang MG, Berra L. Milrinone as Compared with Dobutamine in the Treatment of Cardiogenic Shock. N Engl J Med. 2021;385(22):2108. Epub 2021/11/25. PubMed PMID: 34818494.
- Karami M, Eriksen E, Ouweneel DM, Claessen BE, Vis MM, Baan J, et al. Long-term 5-year outcome of the randomized IMPRESS in severe shock trial: percutaneous mechanical circulatory support vs. intra-aortic balloon pump in cardiogenic shock after acute myocardial infarction. Eur Heart J Acute Cardiovasc Care. 2021;10(9):1009-15. Epub 2021/07/31. PubMed PMID: 34327527; PubMed Central PMCID: PMCPMC8648392.
- Ceglarek U, Schellong P, Rosolowski M, Scholz M, Willenberg A, Kratzsch J, et al. The novel cystatin C, lactate, interleukin-6, and N-terminal pro-B-type natriuretic peptide (CLIP)-based mortality risk score in cardiogenic shock after acute myocardial infarction. Eur Heart J. 2021;42(24):2344-52. Epub 2021/03/02. PubMed PMID: 33647946.
- Schmitto JD, Mariani S, Li T, Dogan G, Hanke JS, Bara C, et al. Five-year outcomes of patients supported with HeartMate 3: a single-centre experience. Eur J Cardiothorac Surg. 2021;59(6):1155-63. Epub 2021/02/16. PubMed PMID: 33585913.
- Cho SM, Mehaffey JH, Meyers SL, Cantor RS, Starling RC, Kirklin JK, et al. Cerebrovascular Events in Patients With Centrifugal-Flow Left Ventricular Assist Devices: Propensity Score-Matched Analysis From the Intermacs Registry. Circulation. 2021;144(10):763-72. Epub 2021/07/29. PubMed PMID: 34315231.
- Kassner A, Oezpeker C, Gummert J, Zittermann A, Gärtner A, Tiesmeier J, et al. Mechanical circulatory support does not reduce advanced myocardial fibrosis in patients with end-stage heart failure. Eur J Heart Fail. 2021;23(2):324-34. Epub 2020/10/11. PubMed PMID: 33038287.
- Rivas-Lasarte M, Kumar S, Derbala MH, Ferrall J, Cefalu M, Rashid SMI, et al. Prediction of right heart failure after left ventricular assist implantation: external validation of the EUROMACS right-sided heart failure risk score. Eur Heart J Acute Cardiovasc Care. 2021;10(7):723-32. Epub 2021/05/30. PubMed PMID: 34050652.
- Emerson D, Chikwe J, Catarino P, Hassanein M, Deng L, Cantor RS, et al. Contemporary Left Ventricular Assist Device Outcomes in an Aging Population: An STS INTERMACS Analysis. J Am Coll Cardiol. 2021;78(9):883-94. Epub 2021/08/28. PubMed PMID: 34446160.
- Agbor-Enoh S, Shah P, Tunc I, Hsu S, Russell S, Feller E, et al. Cell-Free DNA to Detect Heart Allograft Acute Rejection. Circulation. 2021;143(12):1184-97. Epub 2021/01/14. PubMed PMID: 33435695; PubMed Central PMCID: PMCPMC8221834.
- Sliwa K, van der Meer P, Petrie MC, Frogoudaki A, Johnson MR, Hilfiker-Kleiner D, et al. Risk stratification and management of women with cardiomyopathy/heart failure planning pregnancy or presenting during/after pregnancy: a position statement from the Heart Failure Association of the European Society of Cardiology Study Group on Peripartum Cardiomyopathy. Eur J Heart Fail. 2021;23(4):527-40. Epub 2021/02/21. PubMed PMID: 33609068.
- Sliwa K, Petrie MC, van der Meer P, Mebazaa A, Hilfiker-Kleiner D, Jackson AM, et al. Clinical presentation, management, and 6-month outcomes in women with peripartum cardiomyopathy: an ESC EORP registry. Eur Heart J. 2020;41(39):3787-97. Epub 2020/08/26. PubMed PMID: 32840318; PubMed Central PMCID: PMCPMC7846090.
- Farhan HA, Yaseen IF. Peripartum cardiomyopathy in Iraq: initial registry-based data and 6 month outcomes. ESC Heart Failure. 2021;8(5):4048-54.
- Mbakwem AC, Bauersachs J, Viljoen C, Hoevelmann J, van der Meer P, Petrie MC, et al. Electrocardiographic features and their echocardiographic correlates in peripartum cardiomyopathy: results from the ESC EORP PPCM registry. ESC Heart Fail. 2021;8(2):879-89. Epub 2021/01/17. PubMed PMID: 33453082; PubMed Central PMCID: PMCPMC8006717.
- Jackson AM, Petrie MC, Frogoudaki A, Laroche C, Gustafsson F, Ibrahim B, et al. Hypertensive disorders in women with peripartum cardiomyopathy: insights from the ESC EORP PPCM Registry. Eur J Heart Fail. 2021;23(12):2058-69. Epub 2021/06/12. PubMed PMID: 34114268; PubMed Central PMCID: PMCPMC9311416.
- Olivotto I, Oreziak A, Barriales-Villa R, Abraham TP, Masri A, Garcia-Pavia P, et al. Mavacamten for treatment of symptomatic obstructive hypertrophic cardiomyopathy (EXPLORER-HCM): a randomised, double-blind, placebo-controlled, phase 3 trial. Lancet. 2020;396(10253):759-69. Epub 2020/09/02. PubMed PMID: 32871100.
- Pelliccia F, Gersh BJ, Camici PG. Gaps in Evidence for Risk Stratification for Sudden Cardiac Death in Hypertrophic Cardiomyopathy. Circulation. 2021;143(2):101-3.
- Marston NA, Han L, Olivotto I, Day SM, Ashley EA, Michels M, et al. Clinical characteristics and outcomes in childhood-onset hypertrophic cardiomyopathy. Eur Heart J. 2021;42(20):1988-96. Epub 2021/03/27. PubMed PMID: 33769460; PubMed Central PMCID: PMCPMC8139852.
- Yilmaz A, Bauersachs J, Bengel F, Büchel R, Kindermann I, Klingel K, et al. Diagnosis and treatment of cardiac amyloidosis: position statement of the German Cardiac Society (DGK). Clin Res Cardiol. 2021;110(4):479-506. Epub 2021/01/19. PubMed PMID: 33459839; PubMed Central PMCID: PMCPMC8055575.
- Herrmann J, Lenihan D, Armenian S, Barac A, Blaes A, Cardinale D, et al. Defining cardiovascular toxicities of cancer therapies: an International Cardio-Oncology Society (IC-OS) consensus statement. Eur Heart J. 2022;43(4):280-99. Epub 2021/12/15. PubMed PMID: 34904661; PubMed Central PMCID: PMCPMC8803367.
- D’Souza M, Nielsen D, Svane IM, Iversen K, Rasmussen PV, Madelaire C, et al. The risk of cardiac events in patients receiving immune checkpoint inhibitors: a nationwide Danish study. Eur Heart J. 2021;42(16):1621-31. Epub 2020/12/09. PubMed PMID: 33291147.
- Totzeck M, Lutgens E, Neilan TG. Are we underestimating the potential for cardiotoxicity related to immune checkpoint inhibitors? Eur Heart J. 2021;42(16):1632-5. Epub 2020/12/09. PubMed PMID: 33291139; PubMed Central PMCID: PMCPMC8088813.
- de Wit S, de Boer RA. From Studying Heart Disease and Cancer Simultaneously to Reverse Cardio-Oncology. Circulation. 2021;144(2):93-5.
- Michel L, Helfrich I, Hendgen-Cotta UB, Mincu RI, Korste S, Mrotzek SM, et al. Targeting early stages of cardiotoxicity from anti-PD1 immune checkpoint inhibitor therapy. Eur Heart J. 2022;43(4):316-29. Epub 2021/08/15. PubMed PMID: 34389849.
- Lehmann LH, Cautela J, Palaskas N, Baik AH, Meijers WC, Allenbach Y, et al. Clinical Strategy for the Diagnosis and Treatment of Immune Checkpoint Inhibitor-Associated Myocarditis: A Narrative Review. JAMA Cardiol. 2021;6(11):1329-37. Epub 2021/07/08. PubMed PMID: 34232253.
- de Boer RA, Hulot JS, Tocchetti CG, Aboumsallem JP, Ameri P, Anker SD, et al. Common mechanistic pathways in cancer and heart failure. A scientific roadmap on behalf of the Translational Research Committee of the Heart Failure Association (HFA) of the European Society of Cardiology (ESC). Eur J Heart Fail. 2020;22(12):2272-89. Epub 2020/10/24. PubMed PMID: 33094495; PubMed Central PMCID: PMCPMC7894564.
- Ren QW, Yu SY, Teng TK, Li X, Cheung KS, Wu MZ, et al. Statin associated lower cancer risk and related mortality in patients with heart failure. Eur Heart J. 2021;42(32):3049-59. Epub 2021/06/23. PubMed PMID: 34157723; PubMed Central PMCID: PMCPMC8380061.
- Zannad F, Cotter G, Alonso Garcia A, George S, Davison B, Figtree G, et al. What can heart failure trialists learn from oncology trialists? Eur Heart J. 2021;42(24):2373-83. Epub 2021/06/03. PubMed PMID: 34076243.
- Bauersachs J. Heart failure drug treatment: the fantastic four. Eur Heart J. 2021;42(6):681-3. Epub 2021/01/16. PubMed PMID: 33447845; PubMed Central PMCID: PMCPMC7878007.
- McMurray JJV, Packer M. How Should We Sequence the Treatments for Heart Failure and a Reduced Ejection Fraction?: A Redefinition of Evidence-Based Medicine. Circulation. 2021;143(9):875-7. Epub 2020/12/31. PubMed PMID: 33378214.
- Rosano GMC, Moura B, Metra M, Böhm M, Bauersachs J, Ben Gal T, et al. Patient profiling in heart failure for tailoring medical therapy. A consensus document of the Heart Failure Association of the European Society of Cardiology. Eur J Heart Fail. 2021;23(6):872-81. Epub 2021/05/02. PubMed PMID: 33932268.
- Porcher R, Desguerre I, Amthor H, Chabrol B, Audic F, Rivier F, et al. Association between prophylactic angiotensin-converting enzyme inhibitors and overall survival in Duchenne muscular dystrophy-analysis of registry data. Eur Heart J. 2021;42(20):1976-84. Epub 2021/03/23. PubMed PMID: 33748842.
- Bhatt AS, Vaduganathan M, Claggett BL, Liu J, Packer M, Desai AS, et al. Effect of sacubitril/valsartan vs. enalapril on changes in heart failure therapies over time: the PARADIGM-HF trial. Eur J Heart Fail. 2021;23(9):1518-24. Epub 2021/06/09. PubMed PMID: 34101308; PubMed Central PMCID: PMCPMC9291580.
- Tsutsui H, Momomura SI, Saito Y, Ito H, Yamamoto K, Sakata Y, et al. Efficacy and Safety of Sacubitril/Valsartan in Japanese Patients With Chronic Heart Failure and Reduced Ejection Fraction - Results From the PARALLEL-HF Study. Circ J. 2021;85(5):584-94. Epub 2021/03/19. PubMed PMID: 33731544.
- Proudfoot C, Studer R, Rajput T, Jindal R, Agrawal R, Corda S, et al. Real-world effectiveness and safety of sacubitril/valsartan in heart failure: A systematic review. Int J Cardiol. 2021;331:164-71. Epub 2021/02/06. PubMed PMID: 33545266.
- Giovinazzo S, Carmisciano L, Toma M, Benenati S, Tomasoni D, Sormani MP, et al. Sacubitril/valsartan in real-life European patients with heart failure and reduced ejection fraction: a systematic review and meta-analysis. ESC Heart Fail. 2021;8(5):3547-56. Epub 2021/08/03. PubMed PMID: 34338429; PubMed Central PMCID: PMCPMC8497227.
- Volpe M, Bauersachs J, Bayés-Genís A, Butler J, Cohen-Solal A, Gallo G, et al. Sacubitril/valsartan for the management of heart failure: A perspective viewpoint on current evidence. Int J Cardiol. 2021;327:138-45. Epub 2020/12/11. PubMed PMID: 33301829.
- Jackson AM, Jhund PS, Anand IS, Düngen HD, Lam CSP, Lefkowitz MP, et al. Sacubitril-valsartan as a treatment for apparent resistant hypertension in patients with heart failure and preserved ejection fraction. Eur Heart J. 2021;42(36):3741-52. Epub 2021/08/16. PubMed PMID: 34392331; PubMed Central PMCID: PMCPMC8455346.
- Felker GM, Butler J, Ibrahim NE, Piña IL, Maisel A, Bapat D, et al. Implantable Cardioverter-Defibrillator Eligibility After Initiation of Sacubitril/Valsartan in Chronic Heart Failure: Insights From PROVE-HF. Circulation. 2021;144(2):180-2. Epub 2021/07/13. PubMed PMID: 34251893; PubMed Central PMCID: PMCPMC8270225.
- Docherty KF, Campbell RT, Brooksbank KJM, Dreisbach JG, Forsyth P, Godeseth RL, et al. Effect of Neprilysin Inhibition on Left Ventricular Remodeling in Patients With Asymptomatic Left Ventricular Systolic Dysfunction Late After Myocardial Infarction. Circulation. 2021;144(3):199-209. Epub 2021/05/14. PubMed PMID: 33983794; PubMed Central PMCID: PMCPMC8284373.
- Docherty KF, Campbell RT, Brooksbank KJM, Godeseth RL, Forsyth P, McConnachie A, et al. Rationale and methods of a randomized trial evaluating the effect of neprilysin inhibition on left ventricular remodelling. ESC Heart Fail. 2021;8(1):129-38. Epub 2020/12/12. PubMed PMID: 33305513; PubMed Central PMCID: PMCPMC7835504.
- Jering KS, Claggett B, Pfeffer MA, Granger C, Køber L, Lewis EF, et al. Prospective ARNI vs. ACE inhibitor trial to DetermIne Superiority in reducing heart failure Events after Myocardial Infarction (PARADISE-MI): design and baseline characteristics. Eur J Heart Fail. 2021;23(6):1040-8. Epub 2021/04/14. PubMed PMID: 33847047.
- Shah SJ, Cowie MR, Wachter R, Szecsödy P, Shi V, Ibram G, et al. Baseline characteristics of patients in the PARALLAX trial: insights into quality of life and exercise capacity in heart failure with preserved ejection fraction. Eur J Heart Fail. 2021;23(9):1541-51. Epub 2021/06/26. PubMed PMID: 34170062; PubMed Central PMCID: PMCPMC8448949.
- Heidenreich PA, Bozkurt B, Aguilar D, Allen LA, Byun JJ, Colvin MM, et al. 2022 AHA/ACC/HFSA Guideline for the Management of Heart Failure: A Report of the American College of Cardiology/American Heart Association Joint Committee on Clinical Practice Guidelines. Circulation. 2022;145(18):e895-e1032.
- Spertus JA. Quality of life in EMPEROR-Reduced: emphasizing what is important to patients while identifying strategies to support more patient-centred care. Eur Heart J. 2021;42(13):1213-5. Epub 2021/02/18. PubMed PMID: 33595088.
- Kosiborod MN, Jhund PS, Docherty KF, Diez M, Petrie MC, Verma S, et al. Effects of Dapagliflozin on Symptoms, Function, and Quality of Life in Patients With Heart Failure and Reduced Ejection Fraction: Results From the DAPA-HF Trial. Circulation. 2020;141(2):90-9. Epub 2019/11/19. PubMed PMID: 31736335; PubMed Central PMCID: PMCPMC6964869.
- Butler J, Anker SD, Filippatos G, Khan MS, Ferreira JP, Pocock SJ, et al. Empagliflozin and health-related quality of life outcomes in patients with heart failure with reduced ejection fraction: the EMPEROR-Reduced trial. Eur Heart J. 2021;42(13):1203-12. Epub 2021/01/10. PubMed PMID: 33420498; PubMed Central PMCID: PMCPMC8014525.
- Abraham WT, Lindenfeld J, Ponikowski P, Agostoni P, Butler J, Desai AS, et al. Effect of empagliflozin on exercise ability and symptoms in heart failure patients with reduced and preserved ejection fraction, with and without type 2 diabetes. Eur Heart J. 2021;42(6):700-10. Epub 2020/12/23. PubMed PMID: 33351892.
- Solomon SD, Jhund PS, Claggett BL, Dewan P, Køber L, Kosiborod MN, et al. Effect of Dapagliflozin in Patients With HFrEF Treated With Sacubitril/Valsartan: The DAPA-HF Trial. JACC Heart Fail. 2020;8(10):811-8. Epub 2020/07/13. PubMed PMID: 32653447.
- Packer M, Anker SD, Butler J, Filippatos G, Ferreira JP, Pocock SJ, et al. Influence of neprilysin inhibition on the efficacy and safety of empagliflozin in patients with chronic heart failure and a reduced ejection fraction: the EMPEROR-Reduced trial. Eur Heart J. 2021;42(6):671-80. Epub 2021/01/19. PubMed PMID: 33459776; PubMed Central PMCID: PMCPMC7878011.
- Lam CSP, Ferreira JP, Pfarr E, Sim D, Tsutsui H, Anker SD, et al. Regional and ethnic influences on the response to empagliflozin in patients with heart failure and a reduced ejection fraction: the EMPEROR-Reduced trial. Eur Heart J. 2021;42(43):4442-51. Epub 2021/06/30. PubMed PMID: 34184057; PubMed Central PMCID: PMCPMC8599078.
- Inzucchi SE, Docherty KF, Køber L, Kosiborod MN, Martinez FA, Ponikowski P, et al. Dapagliflozin and the Incidence of Type 2 Diabetes in Patients With Heart Failure and Reduced Ejection Fraction: An Exploratory Analysis From DAPA-HF. Diabetes Care. 2021;44(2):586-94. Epub 2020/12/24. PubMed PMID: 33355302.
- Solomon SD, de Boer RA, DeMets D, Hernandez AF, Inzucchi SE, Kosiborod MN, et al. Dapagliflozin in heart failure with preserved and mildly reduced ejection fraction: rationale and design of the DELIVER trial. Eur J Heart Fail. 2021;23(7):1217-25. Epub 2021/05/30. PubMed PMID: 34051124; PubMed Central PMCID: PMCPMC8361994.
- Bhatt DL, Szarek M, Steg PG, Cannon CP, Leiter LA, McGuire DK, et al. Sotagliflozin in Patients with Diabetes and Recent Worsening Heart Failure. N Engl J Med. 2021;384(2):117-28. Epub 2020/11/18. PubMed PMID: 33200892.
- Tromp J, Ponikowski P, Salsali A, Angermann CE, Biegus J, Blatchford J, et al. Sodium-glucose co-transporter 2 inhibition in patients hospitalized for acute decompensated heart failure: rationale for and design of the EMPULSE trial. Eur J Heart Fail. 2021;23(5):826-34. Epub 2021/02/21. PubMed PMID: 33609072; PubMed Central PMCID: PMCPMC8358952.
- Agarwal R, Kolkhof P, Bakris G, Bauersachs J, Haller H, Wada T, et al. Steroidal and non-steroidal mineralocorticoid receptor antagonists in cardiorenal medicine. Eur Heart J. 2021;42(2):152-61. Epub 2020/10/26. PubMed PMID: 33099609; PubMed Central PMCID: PMCPMC7813624.
- Pitt B, Filippatos G, Agarwal R, Anker SD, Bakris GL, Rossing P, et al. Cardiovascular Events with Finerenone in Kidney Disease and Type 2 Diabetes. N Engl J Med. 2021;385(24):2252-63. Epub 2021/08/28. PubMed PMID: 34449181.
- Cleland JGF, Ferreira JP, Mariottoni B, Pellicori P, Cuthbert J, Verdonschot JAJ, et al. The effect of spironolactone on cardiovascular function and markers of fibrosis in people at increased risk of developing heart failure: the heart ‘OMics’ in AGEing (HOMAGE) randomized clinical trial. Eur Heart J. 2021;42(6):684-96. Epub 2020/11/21. PubMed PMID: 33215209; PubMed Central PMCID: PMCPMC7878013.
- Ponikowski P, Alemayehu W, Oto A, Bahit MC, Noori E, Patel MJ, et al. Vericiguat in patients with atrial fibrillation and heart failure with reduced ejection fraction: insights from the VICTORIA trial. Eur J Heart Fail. 2021;23(8):1300-12. Epub 2021/07/01. PubMed PMID: 34191395.
- Voors AA, Mulder H, Reyes E, Cowie MR, Lassus J, Hernandez AF, et al. Renal function and the effects of vericiguat in patients with worsening heart failure with reduced ejection fraction: insights from the VICTORIA (Vericiguat Global Study in Subjects with HFrEF) trial. Eur J Heart Fail. 2021;23(8):1313-21. Epub 2021/05/18. PubMed PMID: 33999486; PubMed Central PMCID: PMCPMC8453520.
- Jankowska EA, Kirwan BA, Kosiborod M, Butler J, Anker SD, McDonagh T, et al. The effect of intravenous ferric carboxymaltose on health-related quality of life in iron-deficient patients with acute heart failure: the results of the AFFIRM-AHF study. Eur Heart J. 2021;42(31):3011-20. Epub 2021/06/04. PubMed PMID: 34080008; PubMed Central PMCID: PMCPMC8370759.
- Martens P, Dupont M, Dauw J, Nijst P, Herbots L, Dendale P, et al. The effect of intravenous ferric carboxymaltose on cardiac reverse remodelling following cardiac resynchronization therapy-the IRON-CRT trial. Eur Heart J. 2021;42(48):4905-14. Epub 2021/06/30. PubMed PMID: 34185066; PubMed Central PMCID: PMCPMC8691806.
- Täubel J, Hauke W, Rump S, Viereck J, Batkai S, Poetzsch J, et al. Novel antisense therapy targeting microRNA-132 in patients with heart failure: results of a first-in-human Phase 1b randomized, double-blind, placebo-controlled study. Eur Heart J. 2021;42(2):178-88. Epub 2020/11/28. PubMed PMID: 33245749; PubMed Central PMCID: PMCPMC7954267.
- Devaux Y, Badimon L. CDR132L: another brick in the wall towards the use of miRNAs to treat cardiovascular disease. Eur Heart J. 2021;42(2):202-4. Epub 2020/11/05. PubMed PMID: 33147612.
- Baker AH, Giacca M. Antagonism of miRNA in heart failure: first evidence in human. Eur Heart J. 2021;42(2):189-91. Epub 2020/12/19. PubMed PMID: 33338200; PubMed Central PMCID: PMCPMC7816691.
- Williams B, Mancia G, Spiering W, Agabiti Rosei E, Azizi M, Burnier M, et al. 2018 ESC/ESH Guidelines for the management of arterial hypertension. Eur Heart J. 2018;39(33):3021-104. Epub 2018/08/31. PubMed PMID: 30165516.
- Swedberg K, Komajda M, Böhm M, Borer JS, Ford I, Dubost-Brama A, et al. Ivabradine and outcomes in chronic heart failure (SHIFT): a randomised placebo-controlled study. Lancet. 2010;376(9744):875-85. Epub 2010/08/31. PubMed PMID: 20801500.
- Fowler MB. Carvedilol prospective randomized cumulative survival (COPERNICUS) trial: carvedilol in severe heart failure. Am J Cardiol. 2004;93(9A):35B-9B. PubMed PMID: 15144935.
- Pitt B, Zannad F, Remme WJ, Cody R, Castaigne A, Perez A, et al. The effect of spironolactone on morbidity and mortality in patients with severe heart failure. Randomized Aldactone Evaluation Study Investigators. N Engl J Med. 1999;341(10):709-17. Epub 1999/09/02. PubMed PMID: 10471456.
- Packer M, Anker SD, Butler J, Filippatos G, Pocock SJ, Carson P, et al. Cardiovascular and Renal Outcomes with Empagliflozin in Heart Failure. N Engl J Med. 2020;383(15):1413-24. Epub 2020/09/01. PubMed PMID: 32865377.
- Wiviott SD, Raz I, Bonaca MP, Mosenzon O, Kato ET, Cahn A, et al. Dapagliflozin and Cardiovascular Outcomes in Type 2 Diabetes. N Engl J Med. 2019;380(4):347-57. Epub 2018/11/13. PubMed PMID: 30415602.
- Bauersachs J, Veltmann C. Heart rate control in heart failure with reduced ejection fraction: the bright and the dark side of the moon. Eur J Heart Fail. 2020;22(3):539-42. Epub 2020/01/09. PubMed PMID: 31912648.
- Kotecha D, Holmes J, Krum H, Altman DG, Manzano L, Cleland JG, et al. Efficacy of β blockers in patients with heart failure plus atrial fibrillation: an individual-patient data meta-analysis. Lancet. 2014;384(9961):2235-43. Epub 2014/09/07. PubMed PMID: 25193873.
- Cleland JGF, Bunting KV, Flather MD, Altman DG, Holmes J, Coats AJS, et al. Beta-blockers for heart failure with reduced, mid-range, and preserved ejection fraction: an individual patient-level analysis of double-blind randomized trials. Eur Heart J. 2018;39(1):26-35. Epub 2017/10/19. PubMed PMID: 29040525; PubMed Central PMCID: PMCPMC5837435.
- Heerspink HJL, Stefánsson BV, Correa-Rotter R, Chertow GM, Greene T, Hou FF, et al. Dapagliflozin in Patients with Chronic Kidney Disease. N Engl J Med. 2020;383(15):1436-46. Epub 2020/09/25. PubMed PMID: 32970396.
- Rosano GMC, Tamargo J, Kjeldsen KP, Lainscak M, Agewall S, Anker SD, et al. Expert consensus document on the management of hyperkalaemia in patients with cardiovascular disease treated with renin angiotensin aldosterone system inhibitors: coordinated by the Working Group on Cardiovascular Pharmacotherapy of the European Society of Cardiology. Eur Heart J Cardiovasc Pharmacother. 2018;4(3):180-8. Epub 2018/05/05. PubMed PMID: 29726985.
- Pitt B, Anker SD, Bushinsky DA, Kitzman DW, Zannad F, Huang IZ. Evaluation of the efficacy and safety of RLY5016, a polymeric potassium binder, in a double-blind, placebo-controlled study in patients with chronic heart failure (the PEARL-HF) trial. Eur Heart J. 2011;32(7):820-8. Epub 2011/01/07. PubMed PMID: 21208974; PubMed Central PMCID: PMCPMC3069389.
- Chioncel O, Mebazaa A, Maggioni AP, Harjola VP, Rosano G, Laroche C, et al. Acute heart failure congestion and perfusion status – impact of the clinical classification on in-hospital and long-term outcomes; insights from the ESC-EORP-HFA Heart Failure Long-Term Registry. Eur J Heart Fail. 2019;21(11):1338-52. Epub 2019/05/28. PubMed PMID: 31127678.
- Brignole M, Pentimalli F, Palmisano P, Landolina M, Quartieri F, Occhetta E, et al. AV junction ablation and cardiac resynchronization for patients with permanent atrial fibrillation and narrow QRS: the APAF-CRT mortality trial. Eur Heart J. 2021;42(46):4731-9. Epub 2021/08/29. PubMed PMID: 34453840.
- Schrage B, Lund LH, Melin M, Benson L, Uijl A, Dahlström U, et al. Cardiac resynchronization therapy with or without defibrillator in patients with heart failure. EP Europace. 2022;24(1):48-57.
- Otto CM, Nishimura RA, Bonow RO, Carabello BA, Erwin JP, Gentile F, et al. 2020 ACC/AHA Guideline for the Management of Patients With Valvular Heart Disease: A Report of the American College of Cardiology/American Heart Association Joint Committee on Clinical Practice Guidelines. Circulation. 2021;143(5):e72-e227.
- Vahanian A, Beyersdorf F, Praz F, Milojevic M, Baldus S, Bauersachs J, et al. 2021 ESC/EACTS Guidelines for the management of valvular heart disease. Eur J Cardiothorac Surg. 2021;60(4):727-800. Epub 2021/08/29. PubMed PMID: 34453161.
- Kar S, Mack MJ, Lindenfeld J, Abraham WT, Asch FM, Weissman NJ, et al. Relationship Between Residual Mitral Regurgitation and Clinical and Quality-of-Life Outcomes After Transcatheter and Medical Treatments in Heart Failure: COAPT Trial. Circulation. 2021;144(6):426-37. Epub 2021/05/28. PubMed PMID: 34039025.
- Gertz ZM, Herrmann HC, Lim DS, Kar S, Kapadia SR, Reed GW, et al. Implications of Atrial Fibrillation on the Mechanisms of Mitral Regurgitation and Response to MitraClip in the COAPT Trial. Circ Cardiovasc Interv. 2021;14(4):e010300. Epub 2021/03/16. PubMed PMID: 33719505.
- Lindenfeld J, Zile MR, Desai AS, Bhatt K, Ducharme A, Horstmanshof D, et al. Haemodynamic-guided management of heart failure (GUIDE-HF): a randomised controlled trial. Lancet. 2021;398(10304):991-1001. Epub 2021/08/31. PubMed PMID: 34461042.
- Yoo J, Grewal P, Hotelling J, Papamanoli A, Cao K, Dhaliwal S, et al. Admission NT-proBNP and outcomes in patients without history of heart failure hospitalized with COVID-19. ESC Heart Fail. 2021;8(5):4278-87. Epub 2021/08/05. PubMed PMID: 34346182; PubMed Central PMCID: PMCPMC8426942.
- Charman SJ, Velicki L, Okwose NC, Harwood A, McGregor G, Ristic A, et al. Insights into heart failure hospitalizations, management, and services during and beyond COVID-19. ESC Heart Fail. 2021;8(1):175-82. Epub 2020/11/25. PubMed PMID: 33232587; PubMed Central PMCID: PMCPMC7753441.
- Butt JH, Fosbøl EL, Gerds TA, Andersson C, Kragholm K, Biering-Sørensen T, et al. All-cause mortality and location of death in patients with established cardiovascular disease before, during, and after the COVID-19 lockdown: a Danish Nationwide Cohort Study. Eur Heart J. 2021;42(15):1516-23. Epub 2021/02/25. PubMed PMID: 33624011; PubMed Central PMCID: PMCPMC7928991.
- Kosiborod MN, Esterline R, Furtado RHM, Oscarsson J, Gasparyan SB, Koch GG, et al. Dapagliflozin in patients with cardiometabolic risk factors hospitalised with COVID-19 (DARE-19): a randomised, double-blind, placebo-controlled, phase 3 trial. Lancet Diabetes Endocrinol. 2021;9(9):586-94. Epub 2021/07/25. PubMed PMID: 34302745; PubMed Central PMCID: PMCPMC8294807 JRLS, FT, SLW, OM, VC, RVPS, VG, PEL, FSS, and MP declare no competing interests. MNK has received a research grant for the conduct of this study from AstraZeneca. He has also received grant and research support from AstraZeneca. He has received a grant and honoraria from Boehringer-Ingelheim, and honoraria from Sanofi, Amgen, Novo Nordisk, Merck (Diabetes), Janssen, Bayer, Novartis, Eli Lilly, and Vifor Pharma. OB reports grants from AstraZeneca, Novartis, Bayer, Amgen, Boehringer-Ingelheim, and Pfizer. GGK is the Principal Investigator of a biostatistics grant from AstraZeneca. He is also the Principal Investigator for biostatistics grants from other biopharmaceutical sponsors that have no relationship to the submitted work. SV reports receiving grants, speaker honoraria and consulting fees from Boehringer-Ingelheim, AstraZeneca, and Janssen. He has received speaker honoraria and consulting fees from Eli Lilly, and speaker honoraria from EOCI Pharmacomm Ltd, Sun Pharmaceuticals, and Toronto Knowledge Translation Working Group. He has also received grants and consulting fees from Amgen; grants, speaker honoraria and consulting fees from Bayer, and from Merck; grants from Bristol-Myers Squibb; speaker honoraria and consulting fees from HLS Therapeutics, Novo Nordisk, and Sanofi; and speaker honoraria from Novartis. AJ received research support for this study from AstraZeneca. He has stock options in DexCom, and has a pending patent for fusion protein nanodiscs for the treatment of heart failure. RF reports research grants and personal fees from AstraZeneca, Bayer and Servier; and research grants from Pfizer, EMS, Aché, Brazilian Ministry of Health, University Health Network, and Lemann Foundation Reseach Fellowship. MN is a consultant for Roche, Vifor, and Amgen, and has received speaking honoraria from Abbott. RE, JO, SBG, JB, AML, and PA are employees and stockholders of AstraZeneca.
- Bozkurt B, Kamat I, Hotez PJ. Myocarditis With COVID-19 mRNA Vaccines. Circulation. 2021;144(6):471-84.
- Huang C, Huang L, Wang Y, Li X, Ren L, Gu X, et al. 6-month consequences of COVID-19 in patients discharged from hospital: a cohort study. Lancet. 2021;397(10270):220-32. Epub 2021/01/12. PubMed PMID: 33428867; PubMed Central PMCID: PMCPMC7833295.
- Rajpal S, Tong MS, Borchers J, Zareba KM, Obarski TP, Simonetti OP, et al. Cardiovascular Magnetic Resonance Findings in Competitive Athletes Recovering From COVID-19 Infection. JAMA Cardiol. 2021;6(1):116-8. Epub 2020/09/12. PubMed PMID: 32915194; PubMed Central PMCID: PMCPMC7489396 Myocardial Solutions, and Cook Medical outside the submitted work. No other disclosures were reported.
- Clark DE, Parikh A, Dendy JM, Diamond AB, George-Durrett K, Fish FA, et al. COVID-19 Myocardial Pathology Evaluation in Athletes With Cardiac Magnetic Resonance (COMPETE CMR). Circulation. 2021;143(6):609-12.







