Đặt vấn đề
Điều trị kháng thụ thể P2Y12 được khuyến cáo phối hợp với ASA kéo dài đến 1 năm sau hội chứng mạch vành cấp để giảm các biến cố do thiếu máu cục bộ. Ngược lại, lợi ích của điều trị kháng tiểu cầu kép dài hơn 1 năm vẫn chưa rõ ràng.
TS.BS. Hoàng Văn Sỹ
(lược dịch)
Ticagrelor là chất đối kháng thụ thể P2Y12 mạnh, gắn kết có phục hồi đã được chứng minh tốt hơn clopidogrel ở bệnh nhân có hội chứng mạch vành cấp được điều trị tới 1 năm.
Thiết kế nghiên cứu
Nghiên cứu PEGASUS-TIMI 54 là một thử nghiệm lâm sàng ngẫu nhiên đa quốc gia, mù đôi, đối chứng giả dược, được thiết kế để đánh giá hiệu quả và an toàn của ticagrelor khi phối hợp với aspirin (75-150 mg) nhằm ngăn ngừa các biến cố tim mạch chính ở những bệnh nhân có tiền sử nhồi máu cơ tim và yếu tố nguy cơ tim mạch. Bệnh nhân có tiền sử nhồi máu cơ tim tự phát trong vòng 1-3 năm được chọn ngẫu nhiên theo tỉ lệ 1: 1: 1 tương ứng với ticagrelor 90 mg hai lần mỗi ngày, ticagrelor 60 mg hai lần mỗi ngày, hoặc cân đối với giả dược, tất cả đều đang uống ASA liều thấp, cho đến khi kết thúc nghiên cứu. Tiêu chí chính bao gồm tử vong tim mạch, nhồi máu cơ tim hoặc đột quỵ. Tuyển bệnh bắt đầu vào tháng 10/2010 và hoàn thành vào 04/2013 với cỡ mẫu trên 21.000 bệnh nhân. Thử nghiệm được lên kế hoạch tiếp tục cho đến khi tích lũy1360 tiêu chí chính hoặc bệnh nhân cuối cùng được phân ngẫu nhiên theo dõi ít nhất 12 tháng.
Kết luận
PEGASUS-TIMI 54 đang nghiên cứu xem liệu việc phối hợp điều trị kháng tiểu cầu mạnh ticagrelor với aspirin liều thấp có làm giảm biến cố tim mạch chính ở những bệnh nhân nguy cơ cao có tiền sử nhồi máu cơ tim hay không. (Am J Heart 2014; 167:437-444.e5)
Nghiên cứu được thực hiện bởi Marc P. Bonaca và cộng sự – trong nhóm nghiên cứu TIMI,chuyên ngành tim mạch, khoa y, bệnh viện Brighamand Women’s,trường Y Harvard, Boston.
Nghiên cứu PEGASUS-TIMI 54 được tài trợ bởi công ty Dược phẩm AstraZeneca.
Sự hoạt hóa tiểu cầu là một yếu tố quan trọng trong sinh bệnh học của biến cố mạch vành cấp. Aspirin đã được chứng minh có hiệu quả trong việc giảm nguy cơ thiếu máu cục bộ ở bệnh nhân có tiền căn nhồi máu cơ tim (NMCT). Sự phối hợp một chất đối kháng thụ thể P2Y12 với aspirin, được gọi là điều trị kháng tiểu cầu kép (DAPT), đã được chứng minh giảm hơn nữa nguy cơ bị các biến cố thiếu máu cục bộ ở những bệnh nhân bị hội chứng mạch vành cấp. Tầm quan trọng của điều trị kháng tiểu cầu mạnh hơn trong bệnh cảnh này đã được đánh giá hơn nữa khi điều trị thuốc đối kháng thụ thể P2Y12 thế hệ mới có hiệu lực mạnh hơn và ổn định hơn đã chứng minh hiệu quả vượt trội so với clopidogrel.
Tuy nhiên thời gian tối ưu của DAPT sau NMCT vẫn chưa được biết. Mặc dù các phân tích bản lề chứng minh lợi ích cộng dồn tiếp tục sau giai đoạn cấp của hội chứng mạch vành cấp, nhưng thời gian thử nghiệm ACS chỉ khoảng 1 năm. Một thử nghiệm chuyên biệt lâu dài về ức chế thụ thể P2Y12 với clopidogrel trên một nền aspirin trong dân số bệnh nhân xơ vữa động mạch hoặc yếu tố nguy cơ tim mạch không cho thấy một lợi ích quan trọng có ý nghĩa thống kê, mặc dù, trong một phân tích post-hoc trên bệnh nhân có tiền căn biến cố tim mạch, và đặc biệt tiền căn NMCT, có sự giảm đáng kể tỉ lệ các biến chứng do thiếu máu cục bộ.
Ticagrelor là một chất đối kháng thụ thể P2Y12 mạnh, hoạt động trực tiếp, gắn kết có phục hồi, đại diện cho một nhóm hóa chất khác biệt với các thienopyridine. Lợi thế của thuốc này bao gồm: thuốc không phải là một tiền chất và do đó không cần giai đoạn chuyển hóa, khởi phát hiệu quả kháng tiểu cầu nhanh (trong vòng 2 giờ), sự thay đổi hiệu quả thuốc trong từng cá thể thấp, và có khả năng phục hồi do vậy hết tác động nhanh hơn khi so sánh với thienopyridine.Thử nghiệm PLATO đã tiến hành nghiên cứu ticagrelor liều nạp 180mg sau đó liều duy trì 90 mg hai lần mỗi ngày so với clopidogrel liều nạp 300mg – 600mg sau đó duy trì 75 mg mỗi ngày phối hợp với aspirin ở những bệnh nhân bị hội chứng mạch vành cấp.
Kết quả chính của nghiên cứu PLATO đã chứng minh tính ưu việt của ticagrelor trong việc làm giảm tiêu chí chính về tử vong tim mạch, NMCT hay đột quỵ (9,8% so với 11,7%, HR 0,84, 95% CI 0,77-0,92, P < 0,001) với cân bằng “nguy cơ – lợi ích” chấp nhận được so với clopidogrel (tỉ lệ xuất huyết nặng chung trong nghiên cứu PLATO 11,6% so với 11,2%, P = 0,43; xuất huyết nặng trong nhóm không phẫu thuật bắc cầu động mạch vành (non-CABG) theo TIMI là 2,8%, so với 2,2%, P = 0,03; xuất huyết nội sọ (ICH) 0,3% so với 0,2%, P = 0,06). Biến cố huyết khối do thiếu máu cục bộ giảm rõ ràng trong vòng 30 ngày đầu tiên và kéo dài trong suốt thời gian theo dõi. Một kết quả quan trọng là giảm mạnh tử vong do nguyên nhân mạch máu (HR 0,79, P = 0,001) và tử vong do mọi nguyên nhân (HR 0,78, P < 0,001).
Thử nghiệm PEGASUS-TIMI 54 sẽ đánh giá xem điều trị lâu dài với ticagrelor khi phối hợp với aspirin có làm giảm nguy cơ các biến cố tim mạch quan trọng ở những bệnh nhân ổn định có tiền căn NMCT so với giả dược. Ngoài ra, thử nghiệm PEGASUS-TIMI 54 cũng sẽ đánh giá cường độ điều trị kháng tiểu cầu trong đó liều ticagrelor 90 mg hai lần mỗi ngày như trong nghiên cứu PLATO, cũng như liều thấp hơn, 60 mg hai lần mỗi ngày, để xem xét liệu cường độ thấp hơn ở giai đoạn điều trị lâu dài có thể tối ưu hóa sự cân bằng về hiệu quả và chảy máu, cũng như nguy cơ các biến cố tái phát có giảm theo thời gian hay không sau nhồi máu cơ tim cấp.
Thiết kế nghiên cứu và dân số nghiên cứu
Nghiên cứu PEGASUS-TIMI 54 là một thử nghiệm lâm sàng ngẫu nhiên đa quốc gia, mù đôi, đối chứng giả dược, được thiết kế để đánh giá hiệu quả và an toàn của ticagrelor khi phối hợp với aspirin liều thấp bệnh nhân ổn định có tiền sử nhồi máu cơ tim. Giả thuyết chính là việc bổ sung ticagrelor với điều trị chuẩn sẽ làm giảm tỷ lệ mắc các biến cố tim mạch chính trong quá trình theo dõi lâu dài (hình).
Bệnh nhân nghiên cứu phải có tiền căn NMCT tự phát xảy ra trong vòng 1-3 năm trước khi nhận vào nghiên cứu cũng như có ít nhất một yếu tố nguy cơ cao kết hợp (Bảng I). Đáng chú ý, ban đầu trong quá trình nghiên cứu (trong vòng 6 tháng đầu tiên nhân bệnh vào nghiên cứu, < 400 bệnh nhân được phân ngẫu nhiên), dựa trên dữ liệu từ các thử nghiệm và nghiên cứu sổ bộ khác (không liên quan đến ticagrelor) cho thấy có tăng nguy cơ xuất huyết nội sọ với điều trị kháng tiểu cầu mạnh hơn ở những bệnh nhân có tiền sử đột quỵ do thiếu máu cục bộ, những bệnh nhân như vậy cũng bị loại khỏi nghiên cứu PEGASUS-TIMI 54. Tuy nhiên, cần lưu ý rằng trong nghiên cứu PLATO, không có bằng chứng về sự không đồng nhất nguy cơ dựa trên tiền sử đột quỵ do thiếu máu cục bộ.
Khoảng 21.000 bệnh nhân đủ điều kiện được phân ngẫu nhiên theo tỷ lệ 1:1:1 để nhận hoặc ticagrelor 90 mg hai lần mỗi ngày, ticagrelor 60 mg hai lần mỗi ngày, hoặc giả dược. Bệnh nhân đầu tiên được chọn ngẫu nhiên vào ngày 29 tháng 10, năm 2010. Phân ngẫu nhiên được thực hiện bằng cách sử dụng một điện thoại vi tính hóa trung tâm hay hệ thống dựa trên web. Phân bổ điều trị mù đôi. Bệnh nhân được phân ngẫu nhiên sẽ được theo dõi tất cả các kết cục lâm sàng và các biến cố bất lợi nghiêm trọng cho đến khi kết thúc nghiên cứu khi mà có sự tích lũy 1.360 biến cố chính (tử vong tim mạch, NMCT, hay đột quỵ) được xác nhận bởi hội đồng trung tâm hoặc theo dõi ít nhất là 12 tháng đối với các bệnh nhân cuối cùng được phân ngẫu nhiên. Thời gian theo dõi trung bình cho bệnh nhân ngẫu nhiên được dự đoán sẽ dài hơn 2 năm.
Nghiên cứu được thực hiện theo nguyên tắc đạo đức phù hợp với Tuyên bố Helsinki, hướng dẫn thực hành lâm sàng tốt ICH, và các quy định hiện hành. Phác đồ nghiên cứu cuối cùng và bản cam kết đồng ý tham gia nghiên cứu đã được xem xét và chấp thuận của cơ quan y tế tương ứng và cơ quan IRBs về đạo đức cho tất cả các trung tâm nghiên cứu tham gia. Bệnh nhân đồng ý ký cam kết tham gia thử nghiệm.
Phác đồ điều trị và theo dõi các thủ thuật
Lựa chọn liều điều trị
Dựa trên các kết quả của thử nghiệm PLATO, ticagrelor 90 mg hai lần mỗi ngày là một liều hợp lý để được sử dụng trong PEGASUS-TIMI 54. Tuy nhiên, người ta nhận thấy rằng trong trường hợp điều trị kéo dài, mức độ ức chế tiểu cầu tối ưu khi điều trị lâu dài chưa được biết và có thể thấp hơn so với khi điều trị trong bệnh cảnh cấp tính, do vậy một nhánh nghiên cứu sử dụng ticagrelor 60 mg hai lần mỗi ngày đã được thêm vào, mà trong đó, dựa trên mô hình dược động học và dược lực học, chế độ này sẽ có sự ức chế tiểu cầu ít hơn so với liều 90 mg hai lần mỗi ngày, nhưng sự ức chế tiểu cầu trung bình vẫn lớn hơn và biến đổi ít hơn so với clopidogrel 75 mg mỗi ngày.
Bởi vì dân số nghiên cứu ổn định, do vậy không sử dụng liều tải trong nghiên cứu. Tất cả bệnh nhân uống 2 viên hai lần mỗi ngày, một 90 mg cân đối với giả dược, và một 60 mg cân đối với giả dược. Chỉ có một trong 2 viên được uống ở bất cứ lần nào là ticagrelor có hoạt tính, hoặc không có viên nào có hoạt tính ticagrelor nếu bệnh nhân được phân bổ vào nhóm dùng giả dược. Trong nghiên cứu này người ta dự đoán rằng một số bệnh nhân sẽ xuất hiện một chỉ định sử dụng ức chế thụ thể P2Y12. Một lựa chọn điều trị nghiên cứu điều chỉnh trong tình huống này là chuyển bệnh nhân đã được phân ngẫu nhiên hoặc cho ticagrelor liều tải 180 mg sau đó 90 mg hai lần mỗi ngày hoặc chuyển giả dược sang clopidogrel (Hình 2).
Các phương pháp điều trị đồng thời
Tất cả bệnh nhân trong PEGASUS-TIMI 54 được khuyến cáo tiếp tục điều trị phòng ngừa thứ phát chuẩn bao gồm aspirin < 150 mg mỗi ngày, phù hợp với khuyến cáo về phòng ngừa thứ phát và với liều được chấp thuận cho điều trị với ticagrelor. Điều trị chống huyết khối thêm bị cấm bao gồm thuốc kháng thụ thể P2Y12 khác, thuốc chống đông kéo dài ở liều điều trị, và thuốc ức chế tiểu cầu khác. Chi tiết được mô tả trong Phụ lục A.
Các khuyến cáo cho các bệnh nhân trải qua thủ thuật
Bệnh nhân trải qua các thủ thuật chương trình lớn không do tim mạch được khuyến cáo nên ngừng điều trị thuốc nghiên cứu 5 ngày trước thủ thuật và sử dụng lại khi xác định thích hợp bởi bác sĩ điều trị. Quản lý điều trị nghiên cứu trong bối cảnh tiểu phẫu hoặc thủ thuật xâm lấn là theo quyết định của bác sĩ điều trị.
Lịch trình thăm bệnh và theo dõi
Bệnh nhân tái khám mỗi 4 tháng trong năm đầu tiên và mỗi 6 tháng sau đó cho đến khi kết thúc nghiên cứu. Trong quá trình theo dõi bệnh nhân được đánh giá các biến cố bất lợi, máu và nước tiểu được lấy mẫu để xét nghiệm trong phòng thí nghiệm trung tâm. Tất cả bệnh nhân sắp kết thúc điều trị được thăm khám khi ngừng điều trị vĩnh viễn và theo dõi khoảng 2 tuần sau liều thuốc nghiên cứu cuối cùng. Khuyến cáo tất cả các bệnh nhân ngẫu nhiên đều được thăm khám lần kết thúc nghiên cứu dù có hay không đang điều trị nghiên cứu ngẫu nhiên. Đánh giá tình trạng sống còn sẽ được thực hiện trong tất cả các bệnh nhân vào cuối thử nghiệm.
Tiêu chí nghiên cứu
Tiêu chí chính bao gồm tử vong tim mạch, nhồi máu cơ tim hoặc đột quỵ. Tiêu chí phụ bao gồm tử vong tim mạch và tử vong do mọi nguyên nhân. Tiêu chí hiệu quả khác bao gồm: phức hợp tử vong tim mạch hoặc nhập viện vì huyết khối động mạch vành hoặc mạch máu não (được định nghĩa là nhồi máu cơ tim, đột quỵ, hoặc nhập viện do tái thông mạch vành khẩn cấp, đau thắt ngực không ổn định, hoặc cơn thiếu máu cục bộ thoáng qua); phức hợp tử vong do bệnh mạch vành, NMCT hoặc đột quỵ; huyết khối stent động mạch vành; và chất lượng cuộc sống được đo bằng thang điểm EQ-5D của Châu Âu. Định nghĩa tiêu chí hiệu quả được nêu chi tiết trong Phụ lục B.
Tiêu chí an toàn chính là chảy máu theo định nghĩa phân loại trong TIMI, PLATO, GUSTO, và Hiệp hội quốc tế về nghẽn mạch và cầm máu (ISTH) với tập trung cụ thể vào các biến cố hội đủ điều kiện như xuất huyết nặng theo TIMI, xuất huyết nặng hoặc nhẹ theo TIMI, và xuất huyết nặng theo PLATO (phụ lục B trực tuyến). An toàn cũng sẽ được đánh giá thông qua sự chứng minh đạt chuẩn các biến cố bất lợi được báo cáo từ các nơi nghiên cứu cũng như qua việc đo lường tại trung tâm các đánh giá an toàn trong phòng thí nghiệm.
Tất cả tiêu chí hiệu quả và an toàn được báo cáo tại chỗ trong trang web dựa trên hệ thống chụp điện tử với ứng dụng duyệt trình hỗ trợ tiếp cận tài liệu nguồn. Đánh giá mỗi biến cố được thực hiện theo định nghĩa trong PEGASUS-TIMI 54 bởi Ủy ban đánh giá tiêu chí lâm sàng (Phụ lục B trực tuyến). Đây là Ủy ban đánh giá tiêu chí lâm sàng độc lập, mù đôi, và đã qua đào tạo có chứng nhận của hội đồng quản trị trong lĩnh vực tim mạch hoặc thần kinh tùy thuộc vào loại biến cố.
Thống kê
Phân tích hiệu quả chính của PEGASUS-TIMI 54 sẽ được dựa trên thời gian từ khi chuyển điều trị ngẫu nhiên đến khi sự xuất hiện đầu tiên bất kỳthành phần nào của tiêu chí gộp chính bao gồm tử vongtim mạch, NMCT, hoặc đột quỵ.Ở mỗi liều điều trị (tức là 90 mg hai lần mỗi ngày hoặc 60 mg hai lần mỗi ngày) sẽ được đánh giá một cách độc lập so với giả dược. Để kiểm soát sai số loại I chung ở mức 5%, alpha sẽ được phân bổ đồng đều cho mỗi liều ticagrelor với so sánh giả dược.
Tiêu chí phụ (bao gồm cả thời gian từ lúc phân ngẫu nhiên đến khi tử vong tim mạch và thời gian từlúc phân ngẫu nhiên đếnkhi tử vong do mọi nguyên nhân) sẽ được đánh giá một cách có thứ bậc cho mỗi liều ticagrelor nếu tiêu chí chính được xác nhận cho liều đó. Một phân tích thăm dò hiệu quả cho cả hai liều kết hợp so với giả dược cũng sẽ được thực hiện. Tất cả các phân tích hiệu quả sẽ được thực hiện theo một nguyên tắc từ chủ định tới điều trị trong tất cả các bệnh nhân ngẫu nhiên không phụ thuộc vào việc tuân thủ phác đồ hoặc thời gian tiếp xúc với điều trị nghiên cứu. Đánh giá an toàn sẽ bao gồm tất cả bệnh nhân ngẫu nhiên nhận được ít nhất một liều điều trị nghiên cứu và dữ liệu sau điều trị có sẵn.
Xác định cỡ mẫu nghiên cứu đã được thực hiện với các giả định tỉ lệ biến cố tiêu chí chính trong nhóm dùng giả dược là 3,5% mỗi năm, dựa trên các nghiên cứu trước đó trong các quần thể nghiên cứu tương tự và giảm nguy cơ tương đối mục tiêu đối với liều 90 mg là 20% và khoảng 19% cho liều 60 mg so với giả dược. Ước tính cho việc giảm nguy cơ tương đối dựa trên những quan sát trong nghiên cứu so sánh DAPT với đơn trị liệu trong dân số ổn định giống nhau. Giảm nguy cơ với liều ticagrelor thấp hơn được mô hình hóa bằng cách ức chế kết tập tiểu cầu từ dữ liệu của thử nghiệm DISPERE và giả định rằng tỉ số rủi ro về kết cục lâm sàng là tỷ lệ thuận với tỷ lệ ức chế kết tập tiểu cầu trung bình ở liều 60 mg so với liều 90 mg.
Dựa trên những giả định này người ta ước tính rằng tổng cộng 1.360 biến cố trong tiêu chí chính sẽ tạo ra khoảng 90% độ mạnh thống kê cho liều 90 mg và khoảng 83% độ mạnh thống kê cho liều 60 mg khi so sánh với giả dược một cách độc lập. Sự ngẫu nhiên hóa của 21.000 bệnh nhân trong 2-3 năm với khoảng hơn 1 năm theo dõi từ bệnh nhân cuối cùng được phân ngẫu nhiên sẽ cho phép dự kiến có 1.360 biến cố chính cộng dồn xảy ra, tuy nhiên, theo dõi sẽ tiếp tục cho đến khi số mục tiêu của tiêu chí đạt được, dự kiến sẽ xảy ra trong nửa sau của năm 2014. Ban chấp hành sẽ theo dõi tốc độ dữ liệu các biến cố tổng hợp mù cũng như các số liệu thử nghiệm khác và có thể điều chỉnh thử nghiệm để duy trì sức mạnh đầy đủ để đánh giá giả thuyết chính của nghiên cứu, hoặc thời gian theo dõi để đạt được số mục tiêu các biến cố.
Một ủy ban giám sát dữ liệu độc lập (IDMC) có trách nhiệm theo dõi sựan toàn trong suốt quá trình thử nghiệm và ngoài ra sẽ thực hiện ít nhất một phân tích tạm thời về hiệu quả khi khoảng một nửa số biến cố của tiêu chí chính dự kiếncộng dồn và đánh giá. IDMC theo quyết định của mình có thể thực hiện các trạng thái hiệu quả bổ sung. alpha sẽ điều chỉnh ở phân tích thống kê giữa kỳ và phân tích cuối cùng để kiểm soát sai số loại I chung khoảng5%.
Nghiên cứu dưới nhóm
Một loạt các nghiên cứu dưới nhóm được lên kế hoạch trong các nhóm bệnh nhân được phân ngẫu nhiên ở một số nước chọn lọc, trong đó có đo chỉ dấu sinh học huyết tương và huyết thanh trạng thái cơ bản và 4 tháng, dược lý học gen, dược động học, cũng như xét nghiệm chức năng tiểu cầu, dược lực học, kinh tế y tế và chất lượng cuộc sống.
Tổ chức nghiên cứu
Thử nghiệm PEGASUS-TIMI 54 thử nghiệm đang được tiến hành trong 31quốc gia và hơn 1145 trung tâm. Nhận bệnh nhân vào nghiên cứu bắt đầu ở Mỹ trong tháng 10 năm 2010 và hoàn thành vào tháng 04 năm 2013. Đặc điểm cơ bản ban đầu của nhóm nghiên cứu được trình bày trong Bảng II.
Nhóm hoạt động thử nghiệm là một quan hệ đối tác gồm các thành viên của nhóm nghiên cứu TIMI và Astra Zeneca, nhà tài trợ thử nghiệm (Phụ lục C trực tuyến). Một ủy ban giám sát hoạt động diễn ra trong thử nghiệm. Một ủy ban chỉ đạo gồm các chuyên gia học thuật và các nhà nghiên cứu chính quốc gia cho mỗi nước chịu trách nhiệm về phác đồ và thực hiện phác đồ. IDMC chịu trách nhiệm đánh giá khoảng thời gian an toàn bệnh nhân trong suốt quá trình thử nghiệm.
Thử nghiệm PEGASUS-TIMI 54 được thiết kế bởi nhóm nghiên cứu TIMI phối hợp với nhà tài trợ thử nghiệm và ủy ban điều hành và ủy ban chỉ đạo. Phân tích dữ liệu sẽ được thực hiện bởi nhóm nghiên cứu TIMI có xác nhận của nhà tài trợ thử nghiệm. Nhóm nghiên cứu TIMI sẽ tự do và có đầy đủ quyền truy cập vào tất cả dữ liệu thử nghiệm và sẽ đệ trình kết quả nghiên cứu để công bố trên tạp chí y khoa đánh giá ngang hàng.
Thử nghiệm PEGASUS-TIMI 54 thử nghiệm đã được đăng ký theo số NCT01225562. Thử nghiệm PEGASUS-TIMI 54 được hỗ trợ bởi một khoản trợ cấp nghiên cứu của AstraZeneca. Các tác giả hoàn toàn chịu trách nhiệm cho việc thiết kế và tiến hành nghiên cứu này, phân tích tất cả nghiên cứu, soạn thảo và biên tập bản thảo, và nội dung cuối cùng của nó.
Bàn luận
Thử nghiệm PEGASUS-TIMI 54 sẽ xác định vai trò của điều trị kháng tiểu cầu kép, aspirin và ticagrelor, ở những bệnh nhân ổn định có tiền sử NMCT từ 1 đến 3 năm trước đây và có ít nhất một yếu tố nguy cơ xơ vữa huyết khối kết hợp. Mặc dù điều trị nền đã được cải thiện, bệnh nhân có tiền sử NMCT vẫn có nguy cơ cao tái phát biến cố. Điều trị lâu dài mới là cần thiết cho nhóm nguy cơ cao này.
Việc phối hợp thuốc đối kháng thụ thể P2Y12 được khuyến cáo thống nhất theo các hướng dẫn chuyên nghiệp trong suốt 12 tháng điều trị sau khi NMCT. Việc mở rộng chiến lược điều trị này vượt quá khung thời gian đó chưa được chứng minh. Một loạt các thử nghiệm ngẫu nhiên đã không chứng tỏ lợi ích khi cho DAPT kéo dài sau can thiệp mạch vành qua da (PCI) (bao gồm cả sau ACS), nhưng các nghiên cứu đã thực hiện tương đối nhỏ và nhận vào bệnh nhân có nguy cơ tương đối thấp. Nghiên cứu đang thực hiện sẽ giúp cung cấp thêm bằng chứng rõ ràng về thời gian tối ưu của DAPT ở những bệnh nhân trải qua PCI có đặt stent, nhưng chủ yếu cho chỉ định chương trình.
Đối với các bệnh nhân ổn định có tiền căn NMCT, cho đến nay, 2 đánh giá quy mô lớn nghiêm ngặt về các lợi ích và nguy cơ của điều trị kháng tiểu cầu mạnh kéo dài đã được thực hiện. Trong thử nghiệm CHARISMA, hơn 15.000 bệnh nhân ổn định có bệnh mạch máu do huyết tắc xơ vữa hoặc có yếu tố nguy cơ xơ vữa động mạch nhưng không biết bệnh được chọn ngẫu nhiên để cho clopidogrel kết hợp với aspirin so với đơn trị liệu aspirin. Mặc dù thử nghiệm tổng thể không cho thấy lợi ích (RR 0.93, 95% CI 0,83-1,05, P = 0,22), đã có một xu hướng rõ ràng về lợi ích dựa trên nguy cơ của bệnh nhân, với giảm nguy cơ tương đối tử vong tim mạch, NMCT, hay đột quỵ 7% trong nhóm tổng thể, 12% ở những bệnh nhân có bằng chứng huyết tắc xơ vữa rõ ràng trên lâm sàng, 17% ở những người có tiền sử NMCT, đột quỵ, hoặc bệnh mạch máu ngoại biên, và 23% ở những người có tiền sử NMCT.
Trong thử nghiệm TRA2P-TIMI 50, hơn 26.000 bệnh nhân bị bệnh mạch máu ổn định được chọn ngẫu nhiên để cho vorapaxar hoặc giả dược, một thuốc kháng tiểu cầu mới ức chế hoạt động của thrombin trên các thụ thể kích hoạt protease. Trong nhóm hơn 17.000 bệnh nhân tiền sử NMCT, điều trị kháng tiểu cầu mạnh hơn làm giảm nguy cơ tử vong tim mạch, NMCT hoặc đột quỵ 20% (8,1% so với 9,7%, HR 0,80, 95% CI 0,72-0,89, P < 0,0001), với kết quả hằng định trong cả thời gian hơn 6 tháng kể về chỉ số NMCT cũng như thời gian hơn 1 năm sau khi phân ngẫu nhiên. Hơn nữa, nghiên cứu TRILOGY báo cáo gần đây so điều trị Prasugrel với Clopidogrel với thời gian trung bình 17 tháng ở những bệnh nhân ACS được điều trị nội khoa. Mặc dù thử nghiệm tổng thể cũng không cho thấy lợi ích, nó gợi ý rằng điều trị kháng tiểu cầu mạnh hơn có thể có lợi hơn 1 năm ở những người có bệnh động mạch vành được chẩn đoán trên chụp mạch vành cản quang.
Kết hợp lại, những dữ liệu này ủng hộ giả thuyết rằng kéo dài điều trị kháng tiểu cầu mạnh hơn sẽ làm giảm tử vong tim mạch và các biến chứng thiếu máu cục bộ ở những bệnh nhân nguy cơ cao có tiền sử NMCT.
Tóm tắt
Thử nghiệm PEGASUS-TIMI 54 đang nghiên cứu xem liệu bổ sung ticagrelor trên nền aspirin có làm giảm biến cố tim mạch bất lợi chính ở những bệnh nhân ổn định có tiền sử nhồi máu cơ tim hay không.
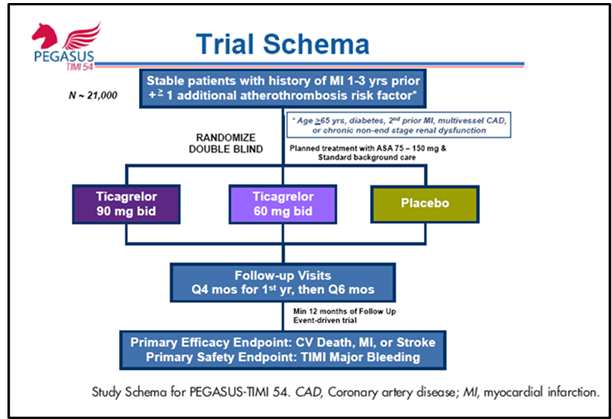
Hình 1. Sơ đồ nghiên cứu PEGASUS-TIMI 54. CAD: Coronary artery disease; MI: myocardial infarction.
Bảng 1. Tiêu chuẩn nhận bệnh và loại trừ
|
Tiêu chuẩn nhận bệnh |
Tiêu chuẩn loại trừ |
|
Ít nhất 50 tuổi NMCT tự phát trong 1-3 năm trước và có ít nhất một trong các yếu tố nguy cơ sau:
Đang uống 75-150 mg mỗi ngày Biện pháp tránh thai ở phụ nữ tiềm năng sinh đẻ Đồng ý viết cam kết tham gia nghiên cứu |
Kế hoạch sử dụng thuốc ức chế thụ thể ADP, dipyridamole hay cilostazol Kế hoạch tái thông mạch máu (mạch vành, ngoại vi, mạch máu não) Đang điều trị thuốc chống đông mạn Rối loạn chảy máu hay đông máu đã biết Nguy cơ chảy máu tăng:
Tiền căn đột quỵ thiếu máu cục bộ Bệnh nhân có nguy cơ biến cố do mạch chậm (hội chứng xoang hay blốc nhĩ thất độ hai hoặc độ ba) trừ khi đã được đặt máy tạo nhịp tim vĩnh viễn Phẫu thuật bắc cầu chủ vành trong 5 năm qua Bệnh gan nặng được biết Suy thận cần chạy thận nhân tạo Phụ nữ có thai hoặc cho con bú Kỳ vọng sống < 1 năm Bất kỳ tình trạng nào được đánh giá bởi các nhà nghiên cứu cho thấy tham gia vào nghiên cứu không an toàn cho bệnh nhân Không có khả năng thực hiện phác đồ nghiên cứu Đã tham tham gia trong một thử nghiệm với ticagrelor trước đây (nếu được điều trị bằng ticagrelor) Tham gia vào kế hoạch, tiến hành nghiên cứu Tham gia vào một nghiên cứu lâm sàng khác với một sản phẩm thuốc nghiên cứu Trong thời gian 30 ngày trước |
Bảng 2. Đặc điểm cơ bản của bệnh nhân nghiên cứu
|
Đặc điểm bệnh nhân |
N = 21.162 |
|
Tuổi, năm, trung bình (IQR) |
65 (59-71) |
|
Giới nữ |
24% |
|
Da trắng |
87% |
|
Cân nặng, kg, trung bình (IQR) |
81 (70-92) |
|
BMI, trung bình (IQR) |
28 (25-31) |
|
Vùng thu nhận bệnh nhân |
|
|
11% |
|
59% |
|
18% |
|
12% |
|
Phân loại biến cố và tiền sử tim mạch |
|
|
1,7 (1,2) |
|
41% |
|
54% |
|
5% |
|
83% |
|
5% |
|
5% |
|
Phân loại yếu tố nguy cơ |
|
|
55% |
|
28% |
|
17% |
|
59% |
|
6% |
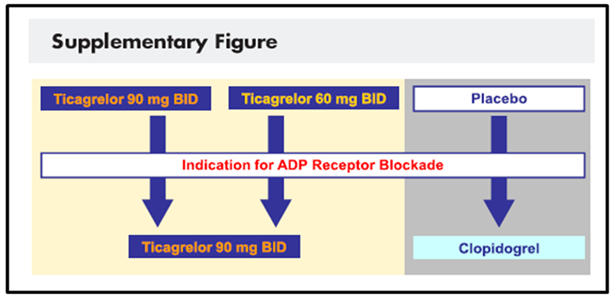
Hình 2. Thay đổi điều trị thuốc nghiên cứu
Tài liệu tham khảo
Marc P. Bonaca, BhattDL, BraunwaldE et al. Design and rationale for the Prevention ofCardiovascular Events in Patients With Prior HeartAttack Using Ticagrelor Compared to Placebo on aBackground of Aspirin–Thrombolysis in MyocardialInfarction 54 (PEGASUS-TIMI 54) trial. AmHeart J 2014;167:437-444.e5.







