MỞ ĐẦU
Đối với các bệnh nhân rung nhĩ đang điều trị warfarin và cần phẫu thuật chương trình hoặc thủ thuật chương trình xâm lấn khác, nhu cầu kháng đông bắc cầu trong thời gian ngưng điều trị warfarin chu phẫu vẫn còn chưa chắc chắn [1-3].
ThS.BS TRẦN CÔNG DUY
Bộ Môn Nội Tổng Quát
Đại Học Y Dược TP. Hồ Chí Minh
Bệnh cảnh lâm sàng phổ biến này ảnh hưởng khoảng 1/6 bệnh nhân rung nhĩ điều trị warfarin mỗi năm [4],[5]. Điều trị warfarin điển hình được ngưng 5 ngày trước phẫu thuật chương trình để làm mất tác dụng kháng đông và sử dụng lại sau phẫu thuật khi cầm máu an toàn với 5 – 10 ngày điều trị để đạt được mục tiêu kháng đông [6],[7]. Trong thời gian ngưng điều trị warfarin, liệu pháp kháng đông bắc cầu với heparin trọng lượng phân tử thấp có thể giảm thiểu nguy cơ thuyên tắc động mạch chu phẫu như đột quỵ [6].
Nhiều nghiên cứu quan sát đã đánh giá thời gian và liều của kháng đông bắc cầu chu phẫu với heparin trọng lượng phân tử thấp [8-15]. Tuy nhiên, câu hỏi quan trọng là kháng đông bắc cầu có cần thiết trong thời gian ngưng warfarin chu phẫu vẫn chưa được trả lời [16-18]. Do thiếu chứng cớ nên các hướng dẫn thực hành cung cấp các khuyến cáo yếu và mâu thuẫn về nhu cầu kháng đông bắc cầu [19-21].
Thử nghiệm BRIDGE (the Bridging Anticoagulation in Patients who Require Temporary Interruption of Warfarin Therapy for an Elective Invasive Procedure or Surgery trial) được thiết kế để trả lời một câu hỏi đơn giản: ở các bệnh nhân rung nhĩ, kháng đông bắc cầu có cần thiết trong thời gian ngưng điều trị warfarin trước và sau phẫu thuật hoặc thủ thuật xâm lấn khác không? Nghiên cứu giả thuyết rằng chiến lược không bắc cầu sẽ không thua kém chiến lược bắc cầu với heparin trọng lượng phân tử thấp trong phòng ngừa thuyên tắc huyết khối động mạch chu phẫu và tốt hơn về kết cục xuất huyết nặng.
PHƯƠNG PHÁP
Thiết kế nghiên cứu
Nghiên cứu BRIDGE là một thử nghiệm ngẫu nhiên, mù đôi, có đối chứng giả dược. Viện Nghiên Cứu Lâm Sàng Duke quản lý nghiên cứu. Trung tâm điều phối lâm sàng có trách nhiệm sắp xếp dữ liệu, phân nhóm ngẫu nhiên và phân bố thuốc nghiên cứu. Trung tâm điều phối dữ liệu duy trì cơ sở dữ liệu, phê chuẩn và phân tích dữ liệu. Eisai tài trợ dalteparin, và Đại học Dược Iowa chuẩn bị giả dược. Eisai không có vai trò thiết kế hoặc chỉ đạo nghiên cứu, phân tích dữ liệu hoặc chuẩn bị bản thảo.
Đối tượng bệnh nhân
Bệnh nhân thích hợp tham gia nghiên cứu nếu lớn hơn hoặc bằng 18 tuổi; có rung nhĩ hoặc cuồng nhĩ mạn (vĩnh viễn hoặc kịch phát) được xác định bằng phương tiện điện tâm đồ trước đó hoặc thẩm vấn về máy tạo nhịp (các bệnh nhân rung nhĩ liên quan bệnh van tim, bao gồm bệnh van hai lá); điều trị warfarin trong 3 tháng hoặc lâu hơn với mục tiêu điều trị của tỉ số bình thường hóa quốc tế (INR) 2,0 – 3,0; sắp trải qua phẫu thuật chương trình hoặc thủ thuật chương trình xâm lấn khác cần ngưng warfarin; có ít nhất một trong các yếu tố nguy cơ đột quỵ của CHADS2: suy tim sung huyết hoặc rối loạn chức năng thất trái, tăng huyết áp, tuổi lớn hơn hoặc bằng 75, đái tháo đường, tiền sử đột quỵ thiếu máu não, thuyên tắc hệ thống hoặc cơn thoáng thiếu máu não. Bệnh nhân không được chọn lựa nếu có một hoặc nhiều hơn các yếu tố sau: van tim cơ học; đột quỵ, thuyên tắc hệ thống hoặc cơn thoáng thiếu máu não trong vòng 12 tuần trước; độ thanh lọc creatinine dưới 30 ml/ph; tiểu cầu dưới 100.000/mm3; hoặc phẫu thuật tim, nội sọ hoặc trong tủy sống đã được lập kế hoạch. Tất cả người tham gia nghiên cứu được cung cấp giấy cam kết đồng ý.
Thủ thuật
Các bệnh nhân được phân ngẫu nhiên để nhận điều trị kháng đông bắc cầu với dalteparin sodium (100 UI/kg tiêm dưới da hai lần mỗi ngày) hoặc không điều trị bắc cầu (tiêm dưới da giả dược) từ 3 ngày trước thủ thuật cho đến 24 giờ trước thủ thật và trong 5 đến 10 ngày sau thủ thuật. Sự phân nhóm ngẫu nhiên được thực hiện theo trung tâm nghiên cứu bằng cách sử dụng hệ thống phản ứng giọng nói tương tác với số điện thoại và mã truy cập hoặc qua Internet. Các thuốc nghiên cứu được cung cấp trong các lọ giống nhau.
Quản lý thuốc nghiên cứu thực hiện theo đề cương quản lý chu phẫu được chuẩn hóa (Hình 1). Điều trị warfarin được ngưng 5 ngày trước thủ thuật và bắt đầu sử dụng thuốc nghiên cứu (daltepatin hoặc giả dược) 3 ngày trước thủ thuật. Liều cuối cùng trước thủ thuật của dalteparin hoặc giả dược được cho vào buổi sáng khoảng 24 giờ trước thủ thuật [22],[23]. Warfarin được bắt đầu lại vào buổi tối hoặc ngày sau thủ thuật với liều thông thường của bệnh nhân. Dalteparin hoặc giả dược được sử dụng lại 12 đến 24 giờ sau thủ thuật nhỏ (hoặc nguy cơ xuất huyết thấp) và 48 đến 72 giờ sau thủ thuật lớn (hoặc nguy cơ xuất huyết cao) [8],[10]. Bệnh nhân tiếp tục sử dụng thuốc nghiên cứu đến khi INR lớn hơn hoặc bằng 2. Bệnh nhân được theo dõi mỗi tuần bằng điện thoại với lần theo dõi cuối cùng 30 đến 37 ngày sau thủ thuật. Điều trị kháng tiểu cầu chu phẫu do người nghiên cứu quyết định.
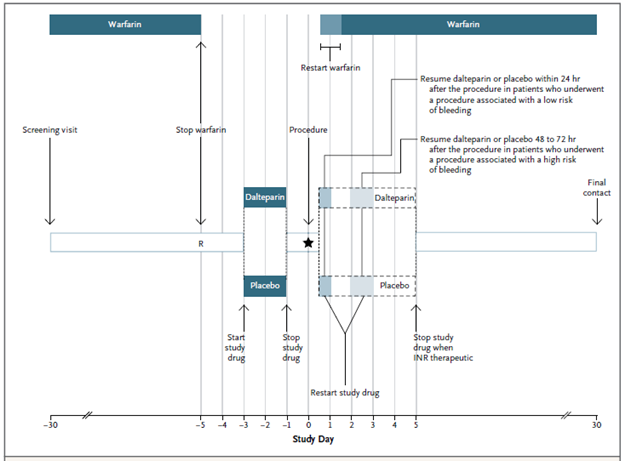
Hình 1. Thiết kế nghiên cứu BRIDGE.Khám sàng lọc bệnh nhân từ 30 đến 5 ngày trước phẫu thuật chương trình, và phân nhóm ngẫu nhiên 5 ngày trước phẫu thuật. Ngưng điều trị warfarin 5 ngày trước phẫu thuật, và sử dụng thuốc nghiên cứu 3 ngày trước phẫu thuật. Điều trị lại warfarin vào buổi tối hoặc một ngày sau phẫu thuật, và sử dụng lại thuốc nghiên cứu vào 12 đến 24 giờ sau phẫu thuật nhỏ (nguy cơ xuất huyết thấp) và 48 đến 72 giờ sau phẫu thuật lớn (nguy cơ xuất huyết cao). Tiếp tục thuốc nghiên cứu sau phẫu thuật đến khi INR lớn hơn hoặc bằng 2 vào một lần đo. Lần theo dõi bệnh nhân cuối cùng vào 30 ngày sau phẫu thuật.
Kết cục nghiên cứu
Tất cả kết cục nghiên cứu được đánh giá vào 37 ngày sau thủ thuật. Kết cục hiệu quả tiên phát là thuyên tắc động mạch bao gồm đột quỵ (thiếu máu não hoặc xuất huyết não), cơn thoáng thiếu máu não và thuyên tắc hệ thống, và kết cục an toàn tiên phát là xuất huyết nặng. Các kết cục hiệu quả thứ phát là nhồi máu cơ tim cấp, huyết khối tĩnh mạch sâu, thuyên tắc phổi và tử vong, và kết cục an toàn thứ phát là xuất huyết nhẹ. Tất cả kết cục nghiên cứu được xém xét độc lập và làm mù.
Phân tích thống kê
Kết cục hiệu quả tiên phát là thuyên tắc động mạch vào 30 ngày. Ước đoán cở mẫu bàn đầu đối với thuyên tắc huyết khối động mạch dựa vào kết quả của các nghiên cứu đoàn hệ đương thời với tỉ lệ ở nhóm bắc cầu là 1,0% [8-10],[24],[25]. Nhóm nghiên cứu cũng cho tỉ lệ ở nhóm không bắc cầu là 1,0%. Phân tích hiệu quả tiên phát là phân tích không thua kém (noninferiority) với test một đuôi ở mức 0,025. Giới hạn không thua kém được đặt ở 1,0%. Nhóm nghiên cứu quyết định rằng giả thuyết không thua kém sẽ bị loại bỏ nếu giới hạn trên của khoảng tin cậy 95% với sự khác biệt tỉ lệ dưới điểm 1 phần trăm-tuổi. Khoảng tin cậy 95% đối với sự khác biệt tỉ lệ biến cố được tính bằng phương pháp dựa vào test Barnard [26], bởi vì test này cho phép tính khoảng tin cậy khi phân tích cở mẫu nhỏ. Các giá trị khoảng tin cậy được tính bằng cách sử dụng phần mềm StatXact, phiên bản 9 (Cytel) [27].
Kết cục an toàn tiên phát là xuất huyết nặng vào 30 ngày sau thủ thuật. Giả thuyết không về sự không khác biệt tỉ lệ xuất huyết nặng được kiểm tra bằng test hai đuôi ở mức 0,05. Tỉ lệ xuất huyết dự đoán là 1,0% ở nhánh không bắc cầu và 3,0% ở nhánh bắc cầu. Giá trị P được tính bằng mid-P test Fisher như khi thực hiện trong phần mềm SAS, phiên bản 9.3, và khoảng tin cậy 95% là khoảng tin cậy tỉ số nguy cơ được tính bằng cùng phiên bản SAS.
Nhóm nghiên cứu tính cở mẫu 1641 bệnh nhân mỗi nhóm cho độ mạnh 80% để phát hiện sự không thua kém của liệu pháp không bắc cầu, với tỉ lệ thuyên tắc huyết khối động mạch 1,0% ở mỗi nhóm và giới hạn không thua kém 1,0%, mức alpha một đuôi 0,025 đối với thuyên tắc huyết khối động mạch và mức alpha hai đuôi 0,05 đối với xuất huyết. Với mức cho phép 10% bệnh nhân rút khỏi nghiên cứu, cở mẫu yêu cầu là 1813 bệnh nhân mỗi nhóm. Nhóm nghiên cứu tính rằng cở mẫu này sẽ cho độ mạnh hơn 99% để phát hiện sự khác biệt dự đoán về tỉ lệ xuất huyết.
Sau khi nhận vào khoảng 850 bệnh nhân, tỉ lệ thuyên tắc huyết khối động mạch dưới 0,5%, nhóm nghiên cứu quyết định cở mẫu sửa đổi là 2526 cho phép độ mạnh ít nhất 90% đối với mỗi kết cục tiên phát. Sau khi nhận vào 1720 bệnh nhân, tỉ lệ thuyên tắc huyết khối động mạch là 0,46% và tỉ lệ xuất huyết là 2,3% trong toàn bộ dân số. Cở mẫu nghiên cứu sửa đổi 1882 được tính dựa vào cở sở ước đoán độ mạnh gần 90% đối với hai kết cục tiên phát.
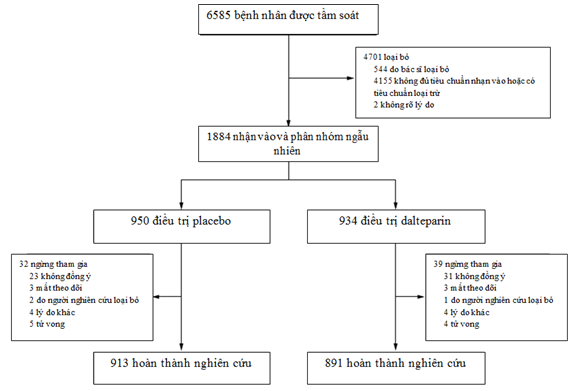
Hình 2. Sàng lọc, phân nhóm ngẫu nhiên và theo dõi
KẾT QUẢ
Như trình bày ở Hình 2, nghiên cứu nhận vào 1884 bệnh nhân trong khoảng thời gian từ tháng 7/2009 đến 12/2014 tại 108 trung tâm ở Hoa Kỳ và Canada; 950 bệnh nhân được phân vào nhóm giả dược (không bắc cầu) và 934 bệnh nhân được điều trị bắc cầu với dalteparin (nhóm bắc cầu). Bảng 1 cho thấy các đặc điểm ban đầu của bệnh nhân. Tuổi trung bình của bệnh nhân là 71,7 và 73,4% bệnh nhân là nam; cân nặng trung bình là 95,8 kg. Điểm số CHADS (điểm số CHADS2 từ 1 đến 6, với điểm càng cao cho thấy nguy cơ đột quỵ càng cao) trung bình là 2,3; 38,3% bệnh nhân có điểm CHADS2 lớn hơn hoặc bằng 3. Tổng 34,7% bệnh nhân đang dùng aspirin, và 7,2% bệnh nhân đang sử dụng thuốc kháng tiểu cầu khác.
Bảng 1. Đặc điểm ban đầu của bệnh nhân
|
Đặc điểm |
Không bắc cầu (N=950) |
Bắc cầu (N=934) |
|
Tuổi – năm Giới nam – số BN (%) Chủng tộc – số BN (%) Da trắng Không Da trắng Không rõ Cân nặng – kg Điểm CHADS2 Trung bình Phân bố – số BN (%) 0 1 2 3 4 5 6 Suy tim trái hoặc rối loạn chức năng thất trái – số BN (%) Tăng huyết áp – số BN (%) Đái tháo đường – số BN (%) Đột quỵ – số BN (%) Cơn thoáng thiếu máu não – số BN (%) Bệnh van hai lá – số BN (%) Hẹp Hở Sa van Nhồi máu cơ tim – số BN (%) Bệnh thận – số BN (%) Bệnh ác tính tạng đặc – số BN (%) Xét nghiệm Hemoglobin – g/dL Tiểu cầu – tế bào/mm3 INR Creatinine huyết thanh – mg/dL Độ thanh lọc creatinine – ml/ph Sử dụng thuốc – số BN (%) Aspirin Clopidogrel Kháng viêm nonsteroid Ức chế COX-2 |
71,8±8,74 696 (73,3)
860 (90,5) 88 (9,3) 2 (0,2) 96,2±24,87
2,3±1,03
1 (0,1) 216 (22,7) 382 (40,2) 229 (24,1) 96 (10,1) 23 (2,4) 3 (0,3) 289 (30,4) 833 (87,7) 390 (41,1) 79 (8,3) 79 (8,3) 165 (17,4) 19 (2,0) 142 (14,9) 13 (1,4) 138 (14,5) 108 (11,4) 68 (7,2)
13,8±1,67 209.300±592.900 2,4±0,57 1,1±0,32 88,1±39,50 324 (34,1) 30 (3,2) 34 (3,6) 8 (0,8)
|
71,6±8,88 686 (73,4)
849 (90,9) 82 (8,8) 3 (0,3) 95,4±23,50
2,4±1,07
1 (0,1) 212 (22,7) 351 (37,6) 232 (24,8) 106 (11,3) 27 (2,9) 5 (0,5) 310 (33,2) 806 (86,3) 382 (40,9) 99 (10,6) 77 (8,2) 142 (15,2) 10 (1,1) 133 (14,2) 5 (0,5) 155 (16,6) 92 (9,9) 52 (5,6)
13,8±1,62 209.200±580.500 2,4±0,57 1,1±0,32 87,6±40,14 329 (35,2) 21 (2,2) 25 (2,7) 13 (1,4)
|
Trong số 1884 bệnh nhân được nhận vào thử nghiệm, 1722 bệnh nhân thực sự trải qua phẫu thuật chương trình và 162 không thực hiện phẫu thuật. Các phẫu thuật phổ biến nhất là tiêu hóa (44,0%), tim – lồng ngực (17,2%), và chỉnh hình (9,2%). Nhìn chung, 89,4% bệnh nhân trải qua phẫu thuật nhỏ (nguy cơ xuất huyết thấp) theo phân loại đã xác định trước; tuy nhiên, 69,1% được điều trị như có nguy cơ xuất huyết thấp bởi người nghiên cứu.
Điều trị kháng đông chu phẫu
Số liều trung bình của thuốc nghiên cứu là 5,0 ± 1,1 trước phẫu thuật và 16,0 ± 7,9 sau phẫu thuật (Bảng 2). Liều trung bình của dalteparin là 9093 ± 2240 IU tiêm dưới da hai lần mỗi ngày. 86,5% trường hợp trước phẫu thuật và 96,5% sau phẫu thuật tuân theo đề cương thuốc nghiên cứu.
Bảng 2. Điều trị kháng đông chu phẫu
|
Biến số |
Không bắc cầu (N=950) |
Bắc cầu (N=934) |
Giá trị P |
|
Điều trị warfarin Thời gian tiền phẫu không sử dụng warfarin Số bệnh nhân có dữ liệu Trung bình – ngày Thời gian dùng liều warfarin đầu tiên hậu phẫu Số bệnh nhân có dữ liệu Trung bình – ngày Heparin trọng lượng phân tử thấp hoặc giả dược Liều tiền phẫu Số bệnh nhân có dữ liệu Trung bình – ngày Bệnh nhân có liều cuối cùng vào sáng ngày phẫu thuật – số/tổng số (%) Thời gian dùng liều hậu phẫu đầu tiên Phẫu thuật hoặc thủ thuật lớn (nguy cơ xuất huyết cao) Số bệnh nhân có dữ liệu Trung bình – giờ Phẫu thuật hoặc thủ thuật nhỏ (nguy cơ xuất huyết thấp) Số bệnh nhân có dữ liệu Trung bình – giờ Liều hậu phẫu Số bệnh nhân có dữ liệu Số liều trung bình Điều trị aspirin – số/tổng số (%) Ngưng ≥ 7 ngày trước phẫu thuật Ngưng < 7 ngày trước phẫu thuật Không ngưng |
872 5,2±1,4
735 1,5±1,3
796 5,0±0,7 778/796 (97,7)
235 53,3±31,6
526 53,3±31,6
764 15,7±7,4
92/324 (28,4) 41/324 (12,7) 191/324 (59,0) |
839 5,3±1,8
696 1,4±1,0
768 5,0±1,4 734/768 (95,6)
223 51,3±27,9
497 21,0±2,4
721 16,1±8,4
92/329 (28,0) 33/329 (10,0) 204/329 (62,0) |
0,28
0,40
0,61
0,02
0,74
0,74
0,74
0,53
|
Kết cục nghiên cứu
Trong 1884 bệnh nhân được nhận vào nghiên cứu, 71 bệnh nhân ngừng tham gia và không cung cấp dữ liệu kết cục; do đó dữ liệu từ 1813 bệnh nhân được dùng để phân tích (Hình 2). Vào 30 ngày sau thủ thuật, tỉ lệ hiện mắc của thuyên tắc huyết khối động mạch là 0,4% (bốn biến cố trong 918 bệnh nhân) ở nhóm không bắc cầu và 0,3% (ba biến cố trong 895 bệnh nhân) ở nhóm bắc cầu (sự khác biệt trung bình giữa các nhóm 0,1 phần trăm điểm; khoảng tin cậy 95%, -0,6 – 0,8; p=0,01 đối với tính không thua kém; p=0,73 đối với tính vượt trội) (Bảng 3). Trong phân tích các trường hợp được điều trị, tỉ lệ thuyên tắc huyết khối động mạch là 0,3% (ba biến cố trong 875 bệnh nhân) ở nhóm không bắc cầu và 0,4% (ba biến cố trong 847 bệnh nhân) ở nhóm bắc cầu (sự khác biệt trung bình giữa các nhóm 0,0% phần trăm điểm; khoảng tin cậy 95% -0,7 – 0,7; p = 0,006 về tính không thua kém). Các bệnh nhân với thuyên tắc huyết khối động mạch có điểm CHADS2 trung bình là 2,6 (từ 1 đến 4), và năm trong bảy biến cố xảy ra sau phẫu thuật nhỏ. Thời gian trung vị xảy ra biến cố thuyên tắc huyết khối động mạch sau phẫu thuật là 19,0 ngày (khoảng tứ phân vị 6,0 – 23,0).
Xuất huyết nặng xảy ra ở 1,3% bệnh nhân (12 trong 918) ở nhóm không bắc cầu và 3,2% (29 trong 895) ở nhóm bắc cầu, cho thấy nhóm không bắc cầu bị xuất huyết nặng nhiều hơn nhóm bắc cầu (nguy cơ tương đối 0,41; khoảng tin cậy 95%, 0,20 đến 0,78; p=0,005). Không có trường hợp xuất huyết nặng tử vong. Nhóm không bắc cầu liên quan với nguy cơ xuất huyết nhẹ thấp hơn nhóm bắc cầu (12,0% so với 20,9%, p < 0,001). Thời gian trung bình xảy ra biến cố xuất huyết nặng sau phẫu thuật là 7,0 ngày (khoảng tứ phân vị, 4,0 đến 18,0).
Không có sự khác biệt ý nghĩa giữa các nhóm về tỉ lệ nhồi máu cơ tim cấp, huyết khối tĩnh mạch sâu, thuyên tắc phổi hoặc tử vong.
Bảng 3. Kết cục nghiên cứu
|
Kết cục |
Không bắc cầu (N=918) |
Bắc cầu (N=895) |
Giá trị P |
|
Số bệnh nhân (%) |
|||
|
Tiên phát |
|
|
|
|
Thuyên tắc huyết khối động mạch |
4 (0,4) |
3 (0,3) |
0,01*; 0,73ǂ |
|
Đột quỵ |
2 (0,2) |
3 (0,3) |
|
|
Cơn thoáng thiếu máu não |
2 (0,2) |
0 |
|
|
Thuyên tắc hệ thống |
0 |
0 |
|
|
Xuất huyết nặng |
12 (1,3) |
29 (3,2) |
0,005ǂ |
|
Thứ phát |
|
|
|
|
Tử vong |
5 (0,5) |
4 (0,4) |
0,88ǂ |
|
Nhồi máu cơ tim |
7 (0,8) |
14 (1,6) |
0,10ǂ |
|
Huyết khối tĩnh mạch sâu |
0 |
1 (0,1) |
0,25ǂ |
|
Thuyên tắc phổi |
0 |
1 (0,1) |
0,25ǂ |
|
Xuất huyết nhẹ |
110 (12,0) |
187 (20,9) |
<0,001ǂ |
|
*P đối với tính không thua kém ǂ P đối với tính vượt trội |
|||
BÀN LUẬN
Ở các bệnh nhân rung nhĩ cần ngưng điều trị warfarin chu phẫu đối với phẫu thuật chương trình, chiến lược ngưng warfarin mà không sử dụng kháng đông bắc cầu không thua kém sử dụng kháng đông bắc cầu về phòng ngừa thuyên tắc huyết khối động mạch. Ngoài ra, điều trị bắc cầu có nguy cơ xuất huyết nặng gần gấp ba nhóm không bắc cầu, và cũng có ít trường hợp xuất huyết nhẹ hơn. Không có sự khác biệt ý nghĩa giữa hai nhóm về nhồi máu cơ tim, thuyên tắc huyết khối tĩnh mạch, hoặc tử vong. Các phát hiện này cho thấy lợi ích lâm sàng thiên về chiến lược không bắc cầu so với bắc cầu bằng heparin trọng lượng phân tử thấp.
Các phát hiện trong thử nghiệm này phù hợp với kết quả từ các nghiên cứu so sánh không ngẫu nhiên giữa các chiến lược này. Một phân tích gộp các nghiên cứu quan sát bao gồm 12278 bệnh nhân rung nhĩ hoặc van tim cơ học có hoặc không điều trị bắc cầu với heparin trọng lượng thấp cho thấy không có sự khác biệt ý nghĩa về tỉ lệ thuyên tắc huyết khối động mạch (tỉ số số chênh với bắc cầu 0,80; khoảng tin cậy 95% 0,42 đến 1,54) nhưng tỉ lệ xuất huyết nặng cao hơn (tỉ số số chênh 3,60; khoảng tin cậy 95% 1,52 đến 8,50) ở nhóm bắc cầu [28]. Trong nghiên cứu dưới nhóm của RELY (the Randomized Evaluation of Long-Term Anticoagulation Therapy) [29], trong đó các bệnh nhân rung nhĩ được phân ngẫu nhiên điều trị warfarin hoặc dabigatran ở hình thức nhãn mở, kháng đông bắc cầu liên quan với tỉ lệ xuất huyết nặng nhiều hơn nhóm không bắc cầu (6,8% so với 1,6%, p < 0,001) trong 1424 bệnh nhân ngưng điều trị warfarin đối với phẫu thuật chương trình, và không có ảnh hưởng đối với thuyên tắc huyết khối động mạch (0,5% so với 0,2%, p=0,32) [30]. Nghiên cứu ORBIT-AF (the Outcome Registry for Better Informed Treatment of Atrial Fibrillation) bao gồm 2200 bệnh nhân rung nhĩ cần phẫu thuật chương trình cũng có tỉ lệ xuất huyết cao hơn nếu sử dụng kháng đông bắc cầu trong thời gian ngưng điều trị warfarin chu phẫu [31].
Cơ sở của việc sử dụng kháng đông bắc cầu được đặt ra dựa vào giả thuyết rằng nguy cơ xuất huyết cao hơn có thể chấp nhận về mặt lâm sàng nhưng bù lại nguy cơ thuyên tắc huyết khối động mạch chu phẫu thấp hơn [32]. Các phát hiện từ thử nghiệm BRIDGE cũng như các nghiên cứu không ngẫu nhiên cho thấy nguy cơ thuyên tắc huyết khối động mạch chu phẫu ở các bệnh nhân rung nhĩ trong thời gian ngưng điều trị warfarin có thể được khẳng định quá mức và có thể không được giảm bởi kháng đông bắc cầu. Thực ra, cơ chế của thuyên tắc huyết khối động mạch chu phẫu có thể liên quan chặt chẽ với các yếu tố như loại phẫu thuật [33] và sự thay đổi huyết áp trong phẫu thuật [34]. Giả thuyết rằng ngưng warfarin dẫn đến tăng đông dội ngược và phẫu thuật dẫn đến tình trạng tiền đông, gây ra thuyên tắc huyết khối động mạch không được ủng bộ bởi kết quả của các nghiên cứu này [35-37].
Có một số hạn chế của thử nghiệm BRIDGE. Trước hết, mặc dù nhóm nghiên cứu có mục đích nhận vào mẫu đại diện gồm các bệnh nhân rung nhĩ được xem xét kháng đông bắc cầu nhưng một số nhóm nhất định không đại diện. Ít bệnh nhân có điểm CHADS2 5 hoặc 6, mặc dù điểm trung bình 2,3 tương tự các bệnh nhân rung nhĩ được đánh giá trong các thử nghiệm gần đây với điểm trung bình từ 2,1 đến 2,8 [29],[38-40]. Các bệnh nhân trải qua phẫu thuật lớn liên quan với tỉ lệ thuyên tắc huyết khối động mạchvà xuất huyết (như gỡ bỏ nội mạc động mạch cảnh, phẫu thuật ung thư lớn, phẫu thuật tim hoặc phẫu thuật thần kinh) [19],[33]không đại diện trong thử nghiệm này, mặc dù các phẫu thuật được thực hiện đại diện cho các can thiệp phổ biến nhất mà bệnh nhân trải qua khi ngưng điều trị kháng đông, phần lớn là các phẫu thuật nguy cơ thấp [4],[5],[41]. Ngoài ra, các kết quả không nên áp dụng cho các bệnh nhân có van tim cơ học vì đã loại trừ khỏi nghiên cứu.
Thứ hai, tỉ lệ toàn bộ của thuyên tắc huyết khối động mạch thấp hơn dự đoán nên ảnh hưởng đến độ mạnh của thử nghiệm trong việc phát hiện lợi ích liên quan với bắc cầu. Mặc dù nhóm nghiên cứu đã dự đoán tỉ lệ thuyên tắc huyết khối động mạchkhoảng 1,0% [8],[9],[12],[24] nhưng tỉ lệ quan sát được (0,4%) tương tự tỉ lệ trong các nghiên cứu gần đây bao gồm các bệnh nhân ngưng điều trị warfarin chu phẫu [4],[5],[31],[42]. Ngoài ra, giới hạn không thua kém nhóm nghiên cứu chọn có vẻ lớn so với tỉ lệ biến cố quan sát, nó phản ánh ước đoán ban đầu của tỉ lệ biến cố đã xác định trong đề cương nghiên cứu.
Thứ ba, tỉ lệ quan sát của xuất huyết nặng ở nhóm bắc cầu (3,2%, không có trường hợp tử vong) ở mức trung bình. Tuy nhiên, đề cương điều trị bắc cầu của nhóm nghiên cứu được thiết kế để giảm thiểu xuất huyết, và tỉ lệ xuất huyết cao hơn ở các nghiên cứu khác về kháng đông bắc cầu có thể phản ánh điều trị bắc cầu quá sớm sau các phẫu thuật với nguy cơ xuất huyết cao [10],[43]hoặc thiếu các đề cương điều trị bắc cầu được chuẩn hóa [28],[30].
Thứ tư, việc giảm cở mẫu nghiên cứu có thể gây ra mối bận tâm. Việc giảm cở mẫu do tỉ lệ toàn bộ của thuyên tắc huyết khối động mạchthấp hơn với điều kiện là duy trì độ mạnh đề cập đến giả thuyết nghiên cứu tiên phát. Dù việc mở rộng thử nghiệm được xem xét nhưng không thực hiện do độ mạnh thống kê thêm vào sẽ không thích hợp và chọn lựa bệnh nhân gặp khó khăn trong quá trình nghiên cứu.
Cuối cùng, một số người có thể cho rằng các phát hiện của nghiên cứu này ítý nghĩa do tình trạng giảm sử dụng warfarin trong điều trị các bệnh nhân rung nhĩ, thay bằng sự sẵn có của các thuốc kháng đông trực tiếp mới đường uống [6]. Tuy nhiên, warfarin vẫn còn được sử dụng rộng rãi ở các bệnh nhân rung nhĩ [44-46]. Hơn nữa, các kết quả của nghiên cứu cũng có thể áp dụng đối với các thuốc kháng đôngmới hơn. Trong nghiên cứu dưới nhóm của thử nghiệm RELY, bệnh nhân ngừng điều trị dabigatran vì phẫu thuật chương trình bị xuất huyết nặng nhiều hơn ở nhóm bắc cầu so với nhóm không bắc cầu, và không có ảnh hưởng ý nghĩa đối với thuyên tắc huyết khối động mạch[30].
KẾT LUẬN
Tóm lại, trong thử nghiệm BRIDGE, đối với các bệnh nhân rung nhĩ cần ngưng tạm thời điều trị warfarin do phẫu thuật chương trình hoặc thủ thuật chương trình xâm lấn khác, chiến lược không sử dụng kháng đông bắc cầu không thua kém chế độ bắc cầu với heparin trọng lượng phân tử thấp trong phòng ngừa thuyên tắc huyết khối động mạch. Chiến lược không điều trị bắc cầu cũng giảm nguy cơ xuất huyết nặng.
TÀI LIỆU THAM KHẢO
1. Kearon C, Hirsh J. Management of anticoagulation before and after elective surgery. N Engl J Med 1997; 336: 1506-11.
2. Piazza G, Goldhaber SZ. Perioperative management of the chronically anticoagluated patient: critical pathways for bridging therapy. Crit Pathw Cardiol 2003; 2: 96-103.
3. Gallego P, et al. Bridging evidence-based pratice and pratice-based evidence in periprocedural anticoagulation. Circulation 2012; 126: 1573-6.
4. Healey JS, et al. Periprocedural bleeding and thromboembolic events with dabigatran compared with warfarin: results from the Randomized Evaluation of Long-Term Anticoagulation Therapy (RE-LY) randomized trial. Circulation 2012; 126 (10): e160J.
5. Garcia D, et al. Management and clinical outcomes in patients treated with apixaban vs warfarin undergoing procedures. Blood 2014; 124: 3692-8.
6. Baron TH, et al. Management of antithrombotic therapy in patients undergoing invasive procedures. N Engl J Med 2013; 368: 2113-24.
7. Schulman S, et al. Loading dose vs. Maintainance dose of warfarin for reinitiation after invasive procedures: a randomized trial. J Thromb Haemost 2014; 12: 1254-9.
8. Douketis JD, et al. Low-molecular-weight heparin as bridging anticoagulation during interruption of warfarin: assessment of a standardized periprocedural anticoagulation regimen. Arch Intern Med 2004; 164: 1319-26.
9. Kovacs MJ, et al. Single-arm study of bridging therapy with low-molecular-weight heparin for parients at risk of arterial embolism who require temporary interruption of warfarin. Circulation 2004; 110: 1658-63.
10. Dunn AS, et al. Bridging therapy in patients on long-term oral anticoagulants who require surgery: the Prospective Peri-operative Enoxaparin Cohort Trial (PROSPECT). J Thromb Haemost 2007; 5: 2211-8.
11. Halbritter KM, et al. Bridging anticoagulation for patients on long-term vitamin-K-antagonists: a prospective 1 year registry of 311 episodes. J Thromb Haemost 2005; 3: 2823-5.
12. Spyropoulos AC, et al. Clinical outcomes with unfractionated heparin or low-molecular-weight heparin as bridging therapy in patients on long-term oral anticoagulants: the REGIMEN registry. J Thromb Haemost 2006; 4: 1246-52.
13. Wysokinski WE, et al. Periprocedural anticoagulation management of patients with nonvalvular atrial fibrillation. Mayo Clin Proc 2008; 83: 639-45.
14. Pengo V, et al. Standardized low-molecular-weight heparin bridging regimen in outpatients on oral anticoagulants undergoing invasive procedure or surgery: an inception cohort management study. Circulation 2009; 119: 2920-7.
15. Malato A, et al. Patients requiring interruption of long-term oral anticoagulant therapy: the use of fixed sub-therapeutic doses of low-molecular-weight heparin. J Thromb Haemost 2010; 8: 107-13.
16. Ansell JE. The perioperative management of warfarin therapy. Arch Intern Med 2003; 163: 881-3.
17. BRIDGE Study Investigators. Bridging therapy anticoagulation: is it needed when warfarin is interrupted around the time of a surgery or procedure? Circulation 2012; 125(12): e496-e498.
18. Patel JP, Arya R. The current status of bridging anticoagulation. Br J Haematol 2014; 164: 619-29.
19. Douketis JD, et al. The perioperative management of antithrombotic therapy: American College of Chest Physician Evidence-Based Clinical Practice Guideline (8th Edition). Chest 2008; 133: Suppl: 299S-339S.
20. Fuster V, et al. 2011 ACCF/AHA/HRS focused updated incorporated into the ACC/AHA/ESC 2006 Guidelines for the management of patients with atrial fibrillation: a report of the American College of Cardiology Foundation/American Heart Association Task Force on Practice Guidelines developed in partnership with the European Society of Cardiology and in collaboration with the European Heart Rhythm Association and the Heart Rhythm Society. J Am Coll Cardiol 2011; 57(11): e101-e198.
21. Douketis JD, et al. Perioperative management of antithrombotic therapy: Antithrombotic Therapy and Prevention of Thrombosis, 9th ed: American College of Chest Physicians Evidence-Based Clinical Practice Guidelines. Chest 2012; 141: Suppl: e326S-e350S.
22. ODonnell MJ, et al. Brief communication: perioperative anticoagluant activity after bridging low-molecular-weight heparin for temporary interruption of warfarin. Ann Intern Med 2007; 146:184-7.
23. Douketis JD, et al. Bridging anticoagulation with low-molecular-weight heparin after interruption of warfarin therapy is associated with a residual anticoagulant effect prior to surgery. Thromb Haemost 2005; 94: 528-31.
24. Dunn AS, Turpie AG. Perioperative management of patients receiving oral anticoagulants: a systematic review. Arch Intern Med 2003; 163: 901-8.
25. Garcia A, et al. Risk of thromboembolism with short-term interruption of warfarin therapy. Arch Intern Med 2008; 168: 63-9.
26. Barnard GA. Significance tests for 2 x 2 tables. Biometrika 1947; 34: 123-38.
27. StatXact Version 9 with Cytel Studio. Cambridge, MA: CYTEL software, 2010.
28. Siegal D, et al. Periprocedural heparin bridging therapy in patients receiving vitamin K antagonists: systematic review and meta-analysis of bleeding and thromboembolic rates. Circulation 2012; 126: 1630-9.
29. Connolly SJ,et al. Dabigatran versus warfarin in patients with atrial fibrillation. N Engl J Med 2009; 361: 1139-51.
30. Douketis JD, et al. Perioperative bridging anticoagulation during dabigatran or warfarin interruption among patients who had an elective surgery or procedure: substudy of the RE-LY trial. Thromb Haemost 2015; 113: 625-32.
31. Steinberg BA, et al. Use and outcomes associated with bridging during anticoaglution interruptions in patients with atrial fibrillation: findings from the Outcomes Registry for Better Informed Treatment of Atrial Fibrillation (ORBIT-AF). Circulation 2015; 131: 488-94.
32. Spyropoulos AC. Pro: “Bridging anticoagulation is needed during warfarin interruption in patients who require elective surgery”. Thromb Haemost 2012; 108: 213-6.
33. Kaatz S, et al. Risk of stroke after surgery in patients with and without chronic atrial fibrillation. J Thromb Haemost 2010; 8: 884-90.
34. Cheung CC, et al. Predictors of intraoperative hypotension and bradycardia. Am J Med 2015; 128: 532-8.
35. Grip L, et al. Hypercoagulable state and thromboembolism following warfarin withdrawal in post-myocardial-infarction patients. Eur Heart J 1991;12: 1255-33.
36. Palareti, Legnanai C. Warfarin withdrawal: pharmacokinetic-pharmacodynamic considerations. Clin Pharmacokinet 1996; 30: 300-13.
37. Kosir MA, et al. Prospective double-arm study of fibrinolysis in surgical patients. J Surg Res 1998; 74: 96-101.
38. Granger CB, et al. Apixaban versus warfarin in patients with atrial fibrillion. N Eng J Med 2011; 365: 981-92.
39. Giugliano RP, et al. Edoxaban versus warfarin in patients with atrial fibrillion. N Eng J Med 2013; 369: 2093-104.
40. Graham DJ, et al. Cardiovacular, bleeding and mortality risks in elderly Medicare patients treated with dabigatran or warfarin for nonvalvular atrial fibrillation. Circulation 2015; 131: 157-64.
41. Beyer-Westendorf J, et al. Peri-interventional management of novel oral anticoagulants in daily care: results from the prospective Dresden NOAC registry. Eur Heart J 2014; 35: 1888-96.
42. Sherwood MV, et al. Outcomes of temporary interruption of rivaroxaban compared with warfarin in patients with nonvalvular atrial fibrillation: results from the Rivaroxaban Once Daily, Oral, Direct Factor Xa Inhibition Compared with Vitamin K Antagonism for Prevention of Stroke and Embolism Trial in Atrial Fibrillation (ROCKET AF). Circulation 2014; 129: 1850-9.
43. Birnie DH, et al. Pacemaker or defibrillator surgery without interruption of anticoagulation. N Engl J Med 2013; 368: 2084-93.
44. Xu Y, et al. Prescribing patterns of novel oral anticoagulants following regulatory approval for atrial fibrillation in Ontario, Canada: a population-based descriptive analysis. CAMJ Open 2013; 1: E115-9.
45. Desai NR, et al. Patterns of initiation of oral anticoagulants in patients with atrial fibrillation – quality and cost implications. Am J Med 2014; 127 (11):1075.e1-1028.e1.
46. Olesen JB, et al. Non-vitamin K antagonist oral anticoagultion agents in aticoagulant naive atrial fibrillation patients: Danish nation-wide descriptive data 2011-2013. Europace 2015; 17: 187-93.







