Ercole Tagliamonte, Teresa Cyril, Fausto Rigo, Constantine Astarita, Antonino Coppola, Carlo Romano, Nicola Capuano
Người dịch: THS. BS. ĐẶNG QUANG TOÀN
Bệnh Viện Chợ Rẫy
Hiệu đính: BS. CKII. LÊ HOÀI NAM
Đại học Y Dược TP.HCM
TÓM TẮT
Giới thiệu: Dự trữ vận tốc dòng chảy động mạch vành (DTVTDCĐMV) là một dấu hiệu tiên lượng quan trọng ở những bệnh nhân mắc bệnh động mạch vành ổn định (BĐMV). Thuốc chẹn beta và ivabradine đã được chứng minh là cải thiện DTVTDCĐMV ở những bệnh nhân có BĐMV ổn định, nhưng tác dụng của chúng không bao giờ được so sánh. Mục đích của nghiên cứu hiện tại là so sánh tác dụng của bisoprolol và ivabradine đối với DTVTDCĐMV ở những bệnh nhân có BĐMV ổn định.
Phương pháp: Bệnh nhân nhịp xoang với BĐMV ổn định được đưa vào thử nghiệm tiến cứu, phân nhóm ngẫu nhiên, mù đôi này. Bệnh nhân phải ở trong tình trạng ổn định với điều trị thường ngày của họ trong ít nhất 15 ngày trước khi đăng ký. Những bệnh nhân đang dùng thuốc chẹn bêta hoặc ivabradine bước vào giai đoạn loại bỏ hiệu ứng thuốc 2 tuần khỏi các loại thuốc này trước khi phân nhóm ngẫu nhiên. DTVTDCĐMV qua siêu âm tim Doppler qua thành ngực được đánh giá ở động mạch vành xuống trước trái và được tính là tỷ số vận tốc dòng chảy động mạch vành đỉnh/đáy. Vận tốc dòng chảy động mạch vành đỉnh thu được bằng cách sử dụng dipyridamole theo quy trình thông thường. Sau khi đánh giá DTVTDCĐMV, bệnh nhân được chọn ngẫu nhiên vào nhóm sử dụng ivabradine hoặc bisoprolol và bước vào giai đoạn tăng liều, và DTVTDCĐMV được đánh giá lại 1 tháng sau khi kết thúc giai đoạn tăng liều.
Kết quả: 59 bệnh nhân (38 nam, 21 nữ; trung bình 69 ± 9 tuổi) tham gia nghiên cứu. Đánh giá vận tốc dòng chảy động mạch vành qua siêu âm Doppler và DTVTDCĐMV được thực hiện thành công ở tất cả các bệnh nhân. Các đặc điểm cơ bản là tương tự giữa các nhóm bisoprolol và ivabradine. Không có bệnh nhân nào bỏ tham gia trong quá trình nghiên cứu. Lúc ban đầu, vận tốc dòng chảy động mạch vành đỉnh và DTVTDCĐMV khi nghỉ ngơi không khác biệt đáng kể trong các nhóm ivabradine và bisoprolol. Sau khi điều trị, vận tốc dòng chảy động mạch vành đỉnh khi nghỉ ngơi giảm đáng kể ở cả nhóm ivabradine và bisoprolol, nhưng không có sự khác biệt đáng kể giữa các nhóm (nhóm ivabradine 20,7 ± 4,6 so với 22,8 ± 5,2, P<0,001; nhóm bisoprolol 20,1 ± 4,1 so với 22,1 ± 4,3, P<0,001). Tuy nhiên, vận tốc dòng chảy động mạch vành đỉnh tăng đáng kể ở cả hai nhóm, nhưng ở mức độ lớn hơn ở những bệnh nhân được điều trị bằng ivabradine (ivabradine: 70,7 ± 9,4 so với 58,8 ± 9,2, P < 0,001; bisoprolol: 65 ± 8,3 so với 58,7 ± 8,2, P<0,001). Theo đó, DTVTDCĐMV tăng đáng kể ở cả hai nhóm (ivabradine 3,52 ± 0,64 so với 2,67 ± 0,55, P<0,001; bisoprolol 3,35 ± 0,70 so với 2,72 ± 0,55, P<0,001), nhưng cao hơn đáng kể ở nhóm ivabradine, mặc dù tần số tim giảm tương tự (63 ± 7 so với 61 ± 6; P không đạt sự khác biệt có ý nghĩa thống kê).
Kết luận: Ivabradine cải thiện vận tốc dòng chảy động mạch vành đỉnh và DTVTDCĐMV ở mức độ lớn hơn bisoprolol ở những bệnh nhân có BĐMV ổn định, mặc dù nhịp tim giảm tương tự. Những dữ liệu này chứng minh rằng lợi ích từ liệu pháp ivabradine vượt ra ngoài nhịp tim. Điều này có thể là do một cơ chế khác nhau như thời gian tưới máu tâm trương, thư giãn tâm thất đồng thể tích, áp lực cuối tâm trương, và tuần hoàn bàng hệ.
Tài trợ: Servier.
Từ khóa: Bisoprolol; Tim mạch; Bệnh động mạch vành; Dự trữ vận tốc dòng chảy động mạch vành; Vận tốc dòng chảy mạch vành; Dipyridamole; Nhịp tim; Ivabradine
GIỚI THIỆU
Tần số tim khi nghỉ cao được coi là một dấu hiệu của nguy cơ tim mạch trong dân số nói chung và ở những bệnh nhân mắc bệnh tim mạch. Nó có liên quan đến nguy cơ mắc bệnh tim mạch và tử vong ở những người khỏe mạnh [1], và ở những bệnh nhân bị tăng huyết áp [2], bệnh động mạch vành (BĐMV) [3] và suy tim mãn tính (ST) [4-6]. Giá trị tiên lượng xấu của tần số tim tăng dường như độc lập với các yếu tố nguy cơ tim mạch truyền thống [1, 3, 4, 6, 7].
Một số thuốc giảm tần số tim đã được chứng minh là cải thiện kết quả lâm sàng, mặc dù liệu giảm tần số tim có phải là cơ chế lợi ích duy nhất hay không rất khó để chứng minh và khu trú. Ivabradine làm giảm tần số tim mà không ảnh hưởng đến huyết áp hoặc chức năng tâm thu thất trái bằng cách ức chế dòng If trong nút xoang nhĩ. Ở những bệnh nhân bị rối loạn chức năng tâm thu thất trái, nó được chứng minh là làm giảm tỷ lệ bệnh nhân phải nhập viện để tái thông mạch vành hay nhồi máu cơ tim (NMCT) [8]. Hơn nữa, nó có thể cải thiện kết quả ở những bệnh nhân có tần số tim 70 nhịp mỗi phút trở lên.
Dự trữ vận tốc dòng chảy động mạch vành (DTVTDCĐMV) được định nghĩa là tỷ lệ tăng tốc so với dòng vận tốc đỉnh cơ bản và phản ánh khả năng chức năng thích ứng của vi tuần hoàn mạch vành trong quá trình tim co bóp. Nó phụ thuộc vào tác động kết hợp của hẹp mạch vành nặng và rối loạn chức năng vi tuần hoàn. Siêu âm tim Doppler qua thành ngực cho phép đánh giá DTVTDCĐMV không xâm lấn ở động mạch vành xuống trước trái [9–12]. Đo DTVTDCĐMV bằng siêu âm tim doppler qua thành ngực không chỉ hữu ích để chẩn đoán hẹp động mạch vành tắc nghẽn [13, 14], mà còn hữu ích để đánh giá chức năng vi mạch [15, 16]. Các báo cáo trước đây đã chỉ ra rằng giảm DTVTDCĐMV là một dấu hiệu tiên lượng quan trọng ở những bệnh nhân có BĐMV không tắc nghẽn [17-20]. Thuốc chẹn beta và ivabradine đã được chứng minh là cải thiện DTVTDCĐMV ở những bệnh nhân có BĐMV ổn định [21-23], nhưng tác dụng của chúng không bao giờ được so sánh. Mục đích của nghiên cứu này là so sánh tác dụng của bisoprolol và ivabradine đối với vận tốc dòng chảy mạch vành và DTVTDCĐMV ở những bệnh nhân có BĐMV ổn định và hiểu rõ hơn về tác dụng của các loại thuốc này đối với dòng chảy mạch vành.
PHƯƠNG PHÁP
Thiết kế nghiên cứu
Đây là thử nghiện tiến cứu, phân nhóm ngẫu nhiên, mù đôi trên những bệnh nhân có nhịp xoang với BĐMV ổn định. BĐMV ổn định được định nghĩa là có NMCT trước đó ít nhất 6 tháng trước khi phân nhóm ngẫu nhiên, phẫu thuật trước đó hoặc can thiệp mạch vành qua da (ít nhất 6 tháng) hoặc có bằng chứng hẹp mạch vành nhánh chính ít nhất 50%.
Các tiêu chí loại trừ gồm: không hợp tác hay không chắc chắn trong nghiên cứu; mang thai hoặc cho con bú; NMCT hoặc tái thông mạch vành gần đây (<6 tháng); tiền sử đột quỵ hoặc thiếu máu cục bộ thoáng qua gần đây (<3 tháng); phẫu thuật hoặc can thiệp mạch vành qua da theo chương trình; ít nhất một tiêu chí sau đây: có máy tạo nhịp tim hoặc máy khử rung được cấy ghép, phẫu thuật theo chương trình cho bệnh lý van tim, hội chứng suy nút xoang, blốc xoang nhĩ, hội chứng QT dài bẩm sinh, blốc nhĩ thất hoàn toàn hay tăng huyết áp cấp cứu hoặc không kiểm soát được (huyết áp tâm thu > 180 mmHg và/ hoặc huyết áp tâm trương > 110 mmHg).
Sau khi ký phiếu đồng ý tham gia nghiên cứu, bệnh nhân bước vào giai đoạn loại bỏ hiệu thuốc 2 tuần khỏi thuốc chẹn beta hoặc liệu pháp ivabradine để xác nhận đủ điều kiện và trình trạng ổn định lâm sàng. Vào cuối giai tiền nghiên cứu, bệnh nhân phải trên 18 tuổi, trong nhịp xoang với tần số tim ≥ 60 lần/phút khi nghỉ ngơi, phân suất tống máu thất trái bảo tồn (≥ 50%), và trong tình trạng ổn định trong ít nhất 15 ngày. Nếu đủ điều kiện và sự ổn định lâm sàng được xác nhận trong giai đoạn chạy trong giai đoạn tiền nghiên cứu, bệnh nhân được chỉ định ngẫu nhiên, trong một giao thức mù đôi, để nhận ivabradine với liều khởi đầu là 2,5 mg hai lần mỗi ngày hoặc bisoprolol với liều khởi đầu là 1,25 mg hai lần mỗi ngày. Cả hai loại thuốc đều được tăng liều hàng tuần dựa theo tần số tim, với liều dung nạp cao nhất (liều tối đa: 7,5 mg hai lần mỗi ngày đối với ivabradine và 5 mg hai lần mỗi ngày đối với bisoprolol). Sau giai đoạn tăng liều, bệnh nhân nhận được ivabradine hoặc bisoprolol trong một tháng nữa. Bệnh nhân được điều trị các thuốc nền ổn định theo hướng dẫn hiện hành. Nghiên cứu đã được Ủy ban Đạo đức Nội bộ phê duyệt. Tất cả các thủ tục theo sau đều phù hợp với Tuyên bố Helsinki năm 1964, được sửa đổi vào năm 2013.
Dự trữ dòng chảy mạch vành
Siêu âm tim Doppler đánh giá lưu lượng dòng chảy mạch vành và DTVTDCĐMV được thực hiện ở thời điểm ban đầu và sau 1 tháng điều trị, sử dụng hệ thống siêu âm VividTM 7 (GE Healthcare). Dòng chảy mạch vành được đánh giá qua đoạn xa của động mạch vành xuống trước trái qua mặt cắt 2 buồng từ mỏm hiệu chỉnh. Vận tốc tâm trương đỉnh được đo ở thời điểm trước và sau khi truyền dipyridamole (0,84 mg / kg trong 6 phút), như được dự kiến bởi một quy trình chuẩn [24, 25]. Vận tốc tâm trương đỉnh cơ sở và tăng cao thu được từ ba chu kỳ tim liên tiếp, và DTVTDCĐMV được tính là tỷ lệ vận tốc tâm trương tăng cao so với vận tốc tâm trương đỉnh cơ bản. Tất cả các phép đo đã được thực hiện ngoại tuyến, sử dụng Phần mềm máy trạm lâm sàng EchoPACTM (GE Healthcare), bởi hai nhà siêu âm tim có kinh nghiệm, bị mù với tất cả dữ liệu lâm sàng. Sự thay đổi trong và liên quan sát của các phép đo lần lượt là 4% và 6%, và được đánh giá ở 10 bệnh nhân liên tiếp.
PHÂN TÍCH THỐNG KÊ
Các đặc điểm cơ bản được biểu thị dưới dạng trung bình và độ lệch chuẩn cho các biến liên tục và dưới dạng số và tỷ lệ phần trăm cho các biến phân loại. Phép kiểm T-test không ghép gặp được sử dụng để phân tích sự khác biệt trong các biến liên tục giữa các nhóm; Phép kiểm T-test ghép cặp được sử dụng để phân tích sự khác biệt trong các nhóm. Phân tích các biến phân loại được thực hiện bằng cách sử dụng phép kiểm Chi Bình phương. Tất cả các thử nghiệm của các giả thuyết là hai mặt và giá trị P < 0,05 được coi là có ý nghĩa thống kê. Phần mềm thống kê SPSS (V22.0, IBM, NY, Hoa Kỳ) được sử dụng để phân tích thống kê.
KẾT QUẢ
Tổng cộng, có 59 bệnh nhân (38 nam, 21 nữ) tham gia nghiên cứu. Các đặc điểm cơ bản là tương tự nhau ở hai nhóm (Bảng 1).
Bảng 1. Đặc điểm lâm sàng ban đầu
| Đặc điểm | Ivabradine | Bisoprolol | p |
| Tuổi (năm) | 70 ± 7 | 68 ± 7 | Không có ý nghĩa thống kê |
| Giới (nữ) | 10 (33) | 11 (37) | Không có ý nghĩa thống kê |
| Chỉ số khối cơ thể (kg/m2) | 23.6 ± 4,2 | 24.1 ± 4,1 | Không có ý nghĩa thống kê |
| Tăng huyết áp | 20 (66) | 18 (62) | Không có ý nghĩa thống kê |
| Đái tháo đường | 4 (13) | 4 (14) | Không có ý nghĩa thống kê |
| Hút thuốc lá | 7 (23) | 7 (24) | Không có ý nghĩa thống kê |
| Rối loạn mỡ máu | 14 (46) | 12 (41) | Không có ý nghĩa thống kê |
| Nhồi máu cơ tim trước đó | 7 (23) | 6 (21) | Không có ý nghĩa thống kê |
| Tái tưới máu trước dó | 10 (33) | 11 (38) | Không có ý nghĩa thống kê |
| Đau ngực khi gắng sức | 11 (36) | 9 (31) | Không có ý nghĩa thống kê |
| Huyết áp tâm thu (mmHg) | 126 ± 11 | 129 ± 14 | Không có ý nghĩa thống kê |
| Huyết áp tâm trương (mmHg) | 74 ± 7 | 77 ± 8 | Không có ý nghĩa thống kê |
| Tần số tim lúc nghỉ (lần/phút) | 73 ± 10 | 71 ± 9 | Không có ý nghĩa thống kê |
| Phân suất tống máu thất trái (%) | 58 ± 6 | 60 ± 5 | Không có ý nghĩa thống kê |
Dân số nghiên cứu có độ tuổi trung bình là 69 ± 9 tuổi (35,6% nữ) và tần số tim lúc nghỉ là 72,2 ± 9,3 lần/phút. Nhìn chung, 22% bệnh nhân có NMCT trước đó, 36% đã tái thông mạch vành trước đó, trong khi 34% bị đau thắt ngực. Hai mươi bốn bệnh nhân (41%) có bằng chứng mạch hẹp ít nhất 50% mạch vành chính: 11 bệnh nhân bị hẹp mạch vành động mạch vành xuống trước trái (4 bệnh nhân hẹp từ 70% đến 80% được chọn ngẫu nhiên như nhau để phân nhóm vào ivabradine hoặc bisoprolol để tránh gây nhiều), 9 bệnh nhân động mạch mũ trái và 7 bệnh nhân động mạch vành phải. Bệnh nhân đã được điều trị BĐMV theo hướng dẫn hiện hành một cách thích hợp khi đăng ký thử nghiệm. Liều lượng trung bình của thuốc là 6,3 ± 1,1 mg hai lần mỗi ngày ở nhóm ivabradine và 5,8 ± 0,8 mg hai lần mỗi ngày ở nhóm bisoprolol. Một tháng sau khi kết thúc giai đoạn tăng liều, tần số tim là giảm đáng kể có nghĩa thống kê, như mong đợi ở cả hai nhóm, mà không có sự khác biệt đáng kể giữa các nhóm (từ 73 ± 10 đến 63 ± 7 lần/phút trong nhóm ivabradine, P < 0.001; từ 71 ± 9 đến 61 ± 6 bpm trong nhóm bisoprolol, P<0.001; Bảng 2). Truyền dipyridamole được dung nạp tốt và DTVTDCĐMV đã được thực hiện thành công ở tất cả các bệnh nhân. Các thông số Doppler của vận tốc dòng chảy mạch vành và DTVTDCĐMV được đưa ra trong Bảng 2. Ở mức nền, vận tốc dòng chảy mạch vành đỉnh khi nghỉ ngơi cũng như DTVTDCĐMV không khác biệt có ý nghĩa thống kê giữa các nhóm sử dụng ivabradine và bisoprolol. Sau khi điều trị, vận tốc dòng chảy mạch vành đỉnh nghỉ ngơi giảm đáng kể ở cả nhóm ivabradine và bisoprolol, nhưng không có sự khác biệt có ý nghĩa thống kê giữa chúng. Tuy nhiên, vận tốc dòng chảy mạch vành đỉnh tăng đáng kể ở cả hai nhóm, nhưng ở mức độ lớn hơn trong nhóm ivabradine. Theo đó, DTVTDCĐMV tăng đáng kể ở cả hai nhóm, nhưng ở mức độ lớn hơn ở nhóm ivabradine (Biểu đồ 1).
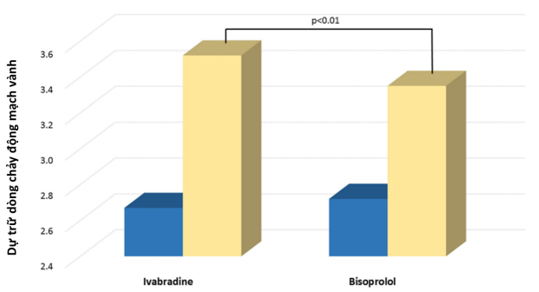
Biểu đồ 1. Dự trữ dòng chảy động mạch vành lúc ban đầu (xanh) và sau điều trị (vàng)
Tất cả những kết quả này đã thu được mặc dù giảm tần số tim tương tự (63 ± 7 so với 61 ± 6 bpm, P không khác biệt có ý nghĩa thống kê; Bảng 2; Biểu đồ 2). Không có bệnh nhân nào bị loại khỏi trong quá trình nghiên cứu.
Bảng 2. Thông số Doppler và tần số tim trước và sau điều trị
| Thông số | Ivabradine | Bisoprolol |
| Trước điều trị | ||
| Vận tốc dòng chảy tâm trương ban đầu (cm/giây) | 22.8 ± 5.2 | 22.1 ± 4.3 |
| Vận tốc dòng chảy tâm trương đỉnh (cm/giây) | 58.8 ± 9.2 | 58.7 ± 8.2 |
| Dự trữ dòng chảy động mạch vành | 2.67 ± 0.55 | 2.72 ± 0.55 |
| Tần số tim (lần/phút) | 73 ± 10 | 71 ± 9 |
| Sau điều trị | ||
| Vận tốc dòng chảy tâm trương ban đầu (cm/giây) | 20.7 ± 4.6* | 20.1 ± 4.1* |
| Vận tốc dòng chảy tâm trương đỉnh (cm/giây) | 70.7 ± 9.4*, # | 65.0 ± 8.3* |
| Dự trữ dòng chảy động mạch vành | 3.52 ± 0.64*,# | 3.35 ± 0.70* |
| Tần số tim (lần/phút) | 63 ± 7* | 61 ± 6* |
| Dữ liệu biểu thị dưới dạng trung bình ± độ lệch chuẩn
* P<0.01 với nhóm tương tự trước điều trị # P<0.01 với bisoprolol |
||
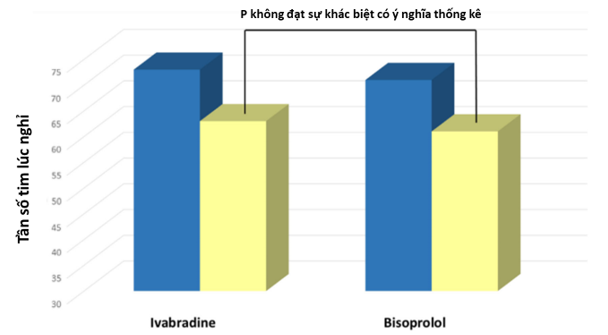
Biểu đồ 2. Tác động của bisoprolol và ivabradine trên tần số tim lúc nghỉ (lần/phút). Ban đầu (xanh), sau điều trị (vàng)
BÀN LUẬN
Nghiên cứu này đã chứng minh rằng ivabradine làm tăng vận tốc dòng chảy mạch vành đỉnh và DTVTDCĐMV ở mức độ lớn hơn bisoprolol, mặc dù giảm tần số tim tương tự. Cơ chế cơ bản của sự khác biệt giữa ivabradine và thuốc chẹn bêta trên vận tốc dòng chảy mạch vành và DTVTDCĐMV dù là giả thuyết nhưng cực kỳ thú vị.
Tần số tim lúc nghỉ là một yếu tố nguy cơ quan trọng và độc lập với các tác động tiên lượng quan trọng, như một yếu tố dự báo về tỷ lệ tử vong và bệnh tim mạch độc lập với các yếu tố nguy cơ khác [1-7]. Do đó, một số phương pháp điều trị dược lý đã được đề xuất để giảm tần số tim nhằm cải thiện kết cục của bệnh nhân bị BĐMV và ST. Tuy nhiên, khi nói rằng mọi tác dụng của các loại thuốc này chỉ là do giảm tần số tim là chưa đầy đủ. Ivabradine là một chất ức chế chọn lọc của kênh If, lần đầu tiên được mô tả bởi Thollon et al. [26] vào năm 1997.
Ức chế kênh f (“funny channel”), kênh kiểm soát điện hoạt động tạo nhịp tim trong nút xoang nhĩ, ivabradine gây giảm tần số tim ở bệnh nhân có nhịp xoang, cả khi nghỉ ngơi và khi gắng sức. Tần số tim thấp sẽ làm kéo dài thời kỳ tâm trương và cải thiện đổ đầy thất, dẫn đến việc tiêu thụ oxy cơ tim ít hơn và cho phép tăng lưu lượng mạch vành và tưới máu cơ tim [27]. Không giống như các tác nhân giảm tần số tim khác như thuốc chẹn bêta hoặc thuốc chẹn kênh canxi, ivabradine không làm giảm huyết áp hệ thống[28], không ức chế co bóp cơ tim [28, 29], và không gây ra bất thường dẫn truyền nhĩ thất [30]. Cụ thể, nó không làm thay đổi khoảng QT hoặc thời gian tái cực cũng như độ dẫn điện hoặc độ trơ của tâm thất, hệ thống His-Purkinje, nút nhĩ thất và tâm nhĩ [30]. Bốn đồng phân của gen kênh If được xác định trong tim động vật [31, 32] và HCN2, có nồng độ cao hơn trong nút xoang [33], được coi là đồng phân chiếm ưu thế. Ivabradine làm giảm sự xâm nhập của natri vào các tế bào cơ, đưa đến sự giảm canxi cytosolic, và cải thiện sự tái hấp thu canxi của lưới tế bào chất, dẫn đến cải thiện thư giãn thất [34, 35].
Ivabradine và Thuốc chẹn bêta
Ivabradine và thuốc chẹn bêta thường vẫn xem là có tác dụng hạ tần số tim như nhau. Trong các thử nghiệm lâm sàng lớn, ivabradine đã được nghiên cứu như một giải pháp thay thế cho thuốc chẹn beta, khi các tác nhân này không thể dung nạp hoặc chống chỉ định, hoặc ngoài ra, khi tần số tim không được kiểm soát đầy đủ với liều thuốc chẹn beta dung nạp cao nhất.
Nhưng chúng ta nên tự hỏi liệu tác dụng của chúng có thực sự giống nhau như vậy không. Gần đây, nhiều cơ chế đã được đề xuất để giải thích sự khác biệt giữa ivabradine và thuốc chẹn bêta. Một số nghiên cứu thực nghiệm đã báo cáo một tác dụng có lợi của ivabradine ít nhất là một phần độc lập về tần số tim và hỗ trợ tính tác động đa hình của ivabradine [36-39]. Do đó, đâu là chìa khóa để hiểu rõ hơn về sự khác biệt giữa ivabradine và bisoprolol trên dòng chảy mạch vành?
Lưu lượng máu mạch vành xảy ra chủ yếu trong thời kì tâm trương, khi có sự giảm chèn ép các mạch vành bởi các sợi tim cơ xung quanh so với thời kỳ tâm thu. Rõ ràng là thời gian tưới máu tâm trương chủ yếu ảnh hưởng đến lưu lượng máu dưới nội mạc. Hơn nữa, lưu lượng mạch vành có thể bị ảnh hưởng bởi độ dốc áp suất giữa áp suất tâm trương trung bình trong gốc động mạch chủ và áp suất tâm trương. Độ chênh áp suất này và thời gian tâm trương được tích hợp vào tích phân áp suất tâm trương -thời gian [40], và bất cứ điều gì làm thay đổi tích phân áp suất tâm trương sẽ thay đổi lưu lượng máu mạch vành: ở đây chúng ta có thể tìm thấy chìa khóa của sự khác biệt giữa ivabradine và bisoprolol trên lưu lượng máu mạch vành.
Tác dụng của ivabradine và atenolol, một thuốc chẹn bêta, đối với thời gian tâm trương đã được so sánh trong hai thực nghiệm [41, 42]. Ivabradine làm tăng thời gian tâm trương cả khi nghỉ ngơi và trong khi gắng sức trên máy chạy bộ ở mức độ lớn hơn atenolol, mặc dù tần số tim tương tự với cả hai loại thuốc. Kết quả là, ivabradine gây ra sự gia tăng lưu lượng máu mạch vành khi gắng sức lớn hơn để giảm tần số tim tương tự so với thuốc chẹn bêta (như đã được chứng minh trong các thực nghiệm), do thời gian đổ đầy tâm trương của động mạch vành kéo dài hơn.
Thuốc chẹn bêta, với tác dụng giãn cơ tim bất lợi của chúng, trái ngược với ivabradine, làm suy giảm quá trình thư giãn tâm thất đồng thể tích, bù đắp một phần lợi ích của thời gian tâm trương kéo dài, và đây có thể là một lý do khác cho sự khác biệt giữa ivabradine và bisoprolol trên vận tốc dòng chảy mạch vành và DTVTDCĐMV [43].
Hơn nữa, với ivabradine không có sự gia tăng hoặc tác động co mạch vành của alpha-adrenergic, so với thuốc chẹn bêta, trong động mạch vành thượng tâm mạc và thậm chí nhiều hơn trong vi tuần hoàn mạch vành [44].
Cuối cùng, sự hình thành các tuần hoàn bàng hệ biểu hiện cho một cơ chế tự nhiên để bù đắp cho sự hạn chế của dòng chảy mạch vành với hẹp mạch vành ngày càng tiến triển và là bảo vệ thuận lợi mô cơ tim khỏi thiếu máu cục bộ. Patel và cộng sự đã chứng minh rằng có mối liên hệ giữa tần số tim thấp và sự phát triển của các động mạch bang hệ ở những bệnh nhân bị BĐMV tắc nghẽn. Có ý kiến cho rằng các tác nhân giảm tần số tim có thể hữu ích cho việc thúc đẩy sự phát triển của động mạch bàng hệ ở bệnh nhân mắc bệnh xơ vữa động mạch. Gần đây, Gloekler và cộng sự đã đánh giá tác động của ivabradine đối với lưu thông hệ tuần hoàn bàng hệ mạch vành ở người. Kết quả của nghiên cứu lâm sàng ngẫu nhiên, kiểm soát với giả dược lần đầu tiên này đã chứng minh rằng ivabradine cải thiện chức năng mạch vành bàng hệ ở những bệnh nhân có BĐMV ổn định. Về mặt lý thuyết, chức năng bang hệ mạch vành được cải thiện có thể ảnh hưởng đến dự trữ dòng chảy mạch vành qua siêu âm tim Doppler, mặc dù các thử nghiệm cụ thể sẽ xác nhận giả thuyết này.
HẠN CHẾ
Không phải tất cả bệnh nhân đều trải qua chụp động mạch vành ngay trước khi tham gia. Cỡ mẫu nghiên cứu nhỏ và do đó không có dữ liệu thống kê về các kết cục lâm sàng đã thu được. Hơn nữa, không có dữ liệu về bất kỳ việc tái thông mạch máu tiếp theo được thu thập khi đã ngưng theo dõi sau khi đánh giá dòng chảy mạch vành.
KẾT LUẬN
Nghiên cứu này lần đâu tiên cho thấy ở người rằng ivabradine cải thiện đáng kể vận tốc dòng chảy mạch vành đỉnh và DTVTDCĐMV ở mức độ cao hơn so với thuốc chẹn bêta, ở những bệnh nhân có BĐMV ổn định,nghiên chứng minh rằng ivabradine không chỉ có tác dụng chống đau ngực mà còn có tác dụng chống thiếu máu cục bộ. Giảm tần số tim tương tự thu được với cả hai loại thuốc cho thấy rằng hiệu quả của điều trị ivabradine vượt ra ngoài tần số tim. Sự khác biệt giữa ivabradine và bisoprolol có thể là do tác dụng khác nhau về thời gian tưới máu tâm trương và thư giãn tâm thất đồng thể tích, cũng như chỉ ra tính chất co mạch vành qua alpha-adrenergic của thuốc chẹn beta. Về mặt lý thuyết, sự cải thiện tổng thể chức năng tâm trương và tác động tích cực đến chức năng bang hệ mạch vành có thể giải thích thêm sự khác biệt giữa thuốc chẹn ivabradine và beta trên vận tốc dòng chảy mạch vành và DTVTDCĐMV. Các câu hỏi tiếp theo mà cộng đồng y tế phải trả lời như sau: Ivabradine có lợi thế hơn thuốc chẹn bêta không? Ivabradine có tác dụng điều trị khác ngoài việc giảm tần số tim khiến nó trở thành một tác nhân thích hợp hơn không?
XÁC NHẬN
Tài trợ, phí xử lý bài viết và phí truy cập mở cho nghiên cứu này được tài trợ bởi Servier. Tất cả các tác giả đều có quyền truy cập đầy đủ vào tất cả dữ liệu trong nghiên cứu này và chịu trách nhiệm hoàn toàn về tính toàn vẹn của dữ liệu và độ chính xác của phân tích dữ liệu. Tất cả các tác giả được nêu tên đều đáp ứng các tiêu chí của Ủy ban Biên tập Tạp chí Y khoa Quốc tế (ICMJE) về quyền tác giả cho bản thảo này, chịu trách nhiệm về tính toàn vẹn của tác phẩm nói chung và đã phê duyệt cuối cùng cho phiên bản được xuất bản.
Xung đột lợi ích. Ercole Tagliamonte, Teresa Cirillo, Fausto Rigo, Costantino Astarita, Antonino Coppola, Carlo Romano và Nicola Capuano không có xung đột lợi ích.
Tuân thủ các nguyên tắc đạo đức. Tất cả các thủ tục theo sau đều phù hợp với các tiêu chuẩn đạo đức của ủy ban có trách nhiệm về thử nghiệm của con người (thể chế và quốc gia) và với Tuyên bố Helsinki năm 1964, được sửa đổi vào năm 2013. Có được sự đồng ý thông báo từ tất cả các bệnh nhân để được đưa vào nghiên cứu.
Nguồn mở. Bài viết này được phân phối theo các điều khoản của Giấy phép quốc tế Creative Commons Attribution-NonCommercial 4.0
(http://creativecommons.org/licenses/ by-nc/4.0/), cho phép bất kỳ việc sử dụng, phân phối và sao chép phi thương mại nào trong bất kỳ phương tiện nào, miễn là bạn cung cấp tín dụng thích hợp cho (các) tác giả gốc và nguồn, cung cấp liên kết đến giấy phép Creative Commons và cho biết nếu có thay đổi.
TÀI LIỆU THAM KHẢO
- Jouven X, Empana JP, Schwartz PJ, Desnos M, Courbon D, Ducimetiere P. Heart-rate profile during exercise as a predictor of sudden death. N Engl J Med. 2005;352:1951–8.
- Palatini P, Benetos A, Julius S. Impact of increased heart rate on clinical outcomes in hypertension: implications for antihypertensive drug therapy. Drugs. 2006;66:133–44.
- Diaz A, Bourassa MG, Guertin MC, Tardif JC. Long-term prognostic value of resting heart rate in patients with suspected or proven coronary flow velocity. Eur Heart J. 2005;26:967–74.
- Fox K, Ford I, Steg PG, Tendera M, Robertson M. Ferrari R; BEAUTIFUL investigators. Heart rate as a prognostic risk factor in patients with coronary artery disease and left-ventricular systolic dysfunction (BEAUTIFUL): a subgroup analysis of a randomised controlled trial. Lancet. 2008;372:817–21.
- Swedberg K, Komajda M, Bohm M, et al. Ivabradine and outcomes in chronic heart failure (SHIFT): a randomized placebo-controlled study. Lancet. 2010;376:875–85.
- Bohm M, Swedberg K, Komajda M, et al. Heart rate as a risk factor in chronic heart failure (SHIFT): the association between heart rate and outcomes in a randomised placebo-controlled trial. Lancet. 2010;376:886–94.
- Fox K, Borer JS, Camm AJ, et al. Resting heart rate in cardiovascular disease. J Am Coll Cardiol. 2007;50:823–30.
- Fox K, Ford I, Steg PG, Tendera M, Robertson M, Ferrari R. BEAUTIFUL investigators. Ivabradine for patients with stable coronary artery disease and left-ventricular systolic dysfunction (BEAUTIFUL): a randomised, double-blind, placebo-controlled trial. Lancet. 2008;372:807–16.
- Caiati C, Montaldo C, Zedda N, Bina A, Iliceto S. New non invasive method for coronary flow reserve assessment: contrast-enhanced transthoracic second harmonic echo Doppler. Circulation. 1999;99:771–8.
- Daimon M, Watanabe H, Yamagishi H, et al. Physiologic assessment of coronary artery stenosis by coronary flow reserve measurements with transthoracic Doppler echocardiography: comparison with exercise thallium-201 single piston emission computed tomography. J Am Coll Cardiol. 2001;37:1310–5.
- Takeuchi M, Miyazaki C, Yoshitani H, Otani S, Sakamoto K, Yoshikawa J. Assessment of coronary flow velocity with transthoracic Doppler echocardiography during dobutamine stress echocardiography. J Am Coll Cardiol. 2001;38:117–23.
- Hozumi T, Yoshida K, Akasaka T, et al. Noninvasive assessment of coronary flow velocity and coronary flow velocity reserve in the left anterior descending coronary artery by Doppler echocardiography: comparison with invasive technique. J Am Coll Cardiol. 1998;32:1251–9.
- Rigo F, Richieri M, Pasanisi E, et al. Usefulness of coronary flow reserve over regional wall motion when added to dual-imaging dipyridamole echocardiography. Am J Cardiol. 2003;91:269–73.
- Nohtomi Y, Takeuchi M, Nagasawa K, Arimura K, Miyata K, Kuwata K. Simultaneous assessment of wall motion and coronary flow velocity in the left anterior descending coronary artery during dipyridamole stress echocardiography. J Am Soc Echocardiogr. 2003;16:457–63.
- Lee DH, Youn HJ, Choi YS, et al. Coronary flow reserve is a comprehensive indicator of cardiovascular risk factors in subjects with chest pain and normal coronary angiogram. Circ J. 2010;74:1405–14.
- Cortigiani L, Rigo F, Gherardi S, Bovenzi F, Picano E, Sicari R. Implication of the continuous prognostic spectrum of Doppler echocardiographic derived coronary flow reserve on left anterior descending artery. Am J Cardiol. 2010;105:158–62.
- Cortigiani L, Rigo F, Gherardi S, et al. Additional prognostic value of coronary flow reserve in diabetic and nondiabetic patients with negative dipyridamole stress echocardiography by wall motion criteria. J Am Coll Cardiol. 2007;50:1354–61.
- Sicari R, Rigo F, Cortigiani L, Gherardi S, Galderisi M, Picano E. Additive prognostic value of coronary flow reserve in patients with chest pain syndrome and normal or near-normal coronary arteries. Am J Cardiol. 2009;103:626–31.
- Rigo F, Sicari R, Gherardi S, Djordjevic-Dikic A, Cortigiani L, Picano E. Prognostic value of coronary flow reserve in medically treated patients with left anterior descending coronary disease with stenosis 51% to 75% in diameter. Am J Cardiol. 2007;100:1527–31.
- Rigo F, Sicari R, Gherardi S, Djordjevic-Dikic A, Cortigiani L, Picano E. The additive prognostic value of wall motion abnormalities and coronary flow reserve during dipyridamole stress echo. Eur Heart J. 2008;29:79–88.
- Billinger M, Seiler C, Fleisch M, Eberli FR, Meier B, Hess OM. Do beta-adrenergic blocking agents increase coronary flow reserve? J Am Coll Cardiol. 2001;38:1866–71.
- Togni M, Vigorito F, Windecker S, et al. Does the beta-blocker nebivolol increase coronary flow reserve? Cardiovasc Drugs Ther. 2007;21:99–108.
- Skalidis EI, Hamilos MI, Chlouverakis G, Zacharis EA, Vardas E. Ivabradine improves coronary flow reserve in patients with stable coronary artery disease. Atherosclerosis. 2011;1:160–5.
- Armstrong WF, Pellikka PA, Ryan T, Crouse L, Zoghbi WA. Stress echocardiography: recommendations for performance and interpretation of stress echocardiography. Stress Echocardiography Task Force of the Nomenclature and Standards Committee of the American Society of Echocardiography. J Am Soc Echocardiogr. 1998;11:97–104.
- Sicari R, Nihoyannopoulos P, Evangelista A, et al. European Association of Echocardiography. Stress echocardiography expert consensus statement: European Association of Echocardiography (EAE) (a registered branch of the ESC). Eur J Echocardiogr. 2008;9:415–37.
- Thollon C, Bidouard JP, Cambarrat C, et al. Stereospecific in vitro and in vivo effects of the new sinus node inhibitor (?)-S 16257. Eur J Pharmacol. 1997;339:43–51.
- Di Francesco D, Camm JA. Heart rate lowering by specific and selective I(f) current inhibition with ivabradine: a new therapeutic perspective in cardiovascular disease. Drugs. 2004;64(16):1757–65.
- Joannides R, Moore N, Iacob M, et al. Comparative effects of ivabradine, a selective heart rate-lowering agent, and propranolol on systemic and cardiac haemodynamics at rest and during exercise. Br J Clin Pharmacol. 2006;61(2):127–37.
- Manz M, Reuter M, Lauck G, Omran H, Jung W. A single intravenous dose of ivabradine, a novel I(f) inhibitor, lowers heart rate but does not depress left ventricular function in patients with left ventricular dysfunction. Cardiology. 2003;100(3):149–55.
- Camm AJ, Lau CP. Electrophysiological effects of a single intravenous administration of ivabradine (S 16257) in adult patients with normal baseline electrophysiology. Drugs. 2003;4(2):83–9.
- Accili EA, Proenza C, Baruscotti M, Di Francesco D. From funny current to HCN channels: 20 years of excitation. News Physiol Sci. 2002;17:32–7.
- Ludwig A, Zong X, Jeglitsch M, Hofmann F, Biel M. A family of hyperpolarization-activated mammalian cation channels. Nature. 1998;393:587–91.
- Shi W, Wymore R, Yu H, et al. Distribution and prevalence of hyperpolarization-activated cation channel (HCN) mRNA expression in cardiac tissues. Circ Res. 1999;85:e1–6.
- Ceconi C, Cargnoni A, Francolini G, Parinello G, Ferrari R. Heart rate reduction with ivabradine improves energy metabolism and mechanical function of isolated ischaemic rabbit heart. Cardiovasc Res. 2009;84:72–82.
- Gewirtz H. ‘Funny’ current: if heart rate slowing is not the best answer, what might be? Cardiovasc Res. 2009;84:9–10.
- Heusch G, Skyschally A, Gres P, van Caster P, Schilawa D, Schulz R. Improvement of regional myocardial blood flow and function and reduction of infarct size with ivabradine: protection beyond heart rate reduction. Eur Heart J. 2008;29:2265–75.
- Fox K, Ford I, Steg PG, Tendera M, Robertson M, Ferrari R, BEAUTIFUL Investigators. Relationship between ivabradine treatment and cardiovascular outcomes in patients with stable coronary artery disease and left ventricular systolic dysfunction with limiting angina: a subgroup analysis of the randomized, controlled BEAUTIFUL trial. Eur Heart J. 2009;30:2337–45.
- Heusch G. A BEAUTIFUL lesson—ivabradine protects from ischaemia, but not from heart failure: through heart rate reduction or more? Eur Heart J. 2009;30:2300–1.
- Heusch G. Pleiotropic action(s) of the bradycardic agent ivabradine: cardiovascular protection beyond heart rate reduction. Br J Pharmacol. 2008;155:970–1.
- Buckberg GD, Fixler DE, Archie JP Jr, Hoffman JIE. Experimental subendocardial ischemia in dogs with normal coronary arteries. Circ Res. 1972;30:67–81.
- Colin P, Ghaleh B, Monnet X, et al. Contributions of heart rate and contractility to myocardial oxygen balance during exercise. Am J Physiol Heart Circ Physiol. 2003;284:H676–82.
- Colin P, Ghaleh B, Monnet X, Hittinger L, Berdeaux A. Effect of graded heart rate reduction with Ivabradine on myocardial oxygen consumption and diastolic time in exercising dogs. J Pharmacol Exp Ther. 2004;308:236–40.
- Colin P, Ghaleh B, Hittinger L, et al. Differential effects of heart rate reduction and beta-blockade on left ventricular relaxation during exercise. Am J Physiol Heart Circ Physiol. 2002;282:H672–9.
- Monnet X, Ghaleh B, Colin P, Parent De Curzon O, Giudicelli J-F, Berdeaux A. Effects of heart rate reduction with ivabradine on exercise induced myocardial ischemia and stunning. J Pharmacol Exp Ther. 2001;299:1133–9.
- Patel SR, Breall JA, Diver DJ, Gersh BJ, Levy AP. Bradycardia is associated with development of coronary collateral vessels in humans. Coron Artery Dis. 2000;11(6):467–72.
- Gloekler S, Traupe T, Stoller M, et al. The effect of heart rate reduction by Ivabradine on collateral function in patients with chronic stable coronary artery disease. Heart. 2014;100(2):160–6.







