BS. HUỲNH ANH KIỆT*
BS. NGUYỄN THANH HIỀN
*Khoa nội TM, BV Đại Học Y Dược, Tp Hồ Chí Minh
MỞ ĐẦU:
Bệnh van động mạch chủ phổ biến ở các nước công nghiệp hóa và tỷ lệ mắc bệnh dự kiến sẽ tăng theo tuổi thọ. Hẹp động mạch chủ do thoái hóa là bệnh lý van tim phổ biến nhất cần điều trị.
Thập kỷ qua chứng kiến sự ra đời của kỹ thuật thay van động mạch chủ qua ống thông (TAVR), cách mạng hóa điều trị hẹp động mạch chủ. TAVR hiện được khuyến cáo ở bệnh nhân có triệu chứng > 80 tuổi với kỳ vọng sống từ 1–10 năm, bệnh nhân có triệu chứng từ 65–80 tuổi nếu không có chống chỉ định với TAVR và bệnh nhân có triệu chứng ở mọi lứa tuổi có nguy cơ phẫu thuật cao với kỳ vọng sống lâu hơn hơn 12 tháng.1
Bất kể loại van động mạch chủ nhân tạo nào được chọn, cả van nhân tạo SAVR (thay van bằng phẫu thuật và TAVR đều có thể bị rối loạn chức năng van, bao gồm viêm nội tâm mạc, huyết khối, thoái hóa van nhân tạo sinh học và hở cạnh van.2,3bài viết này tập trung vào xử trí huyết khối van nhân tạo.
I. ĐỊNH NGHĨA
Huyết khối van nhân tạo được định nghĩa là sự hình thành huyết khối tại van nhân tạo được bắt đầu bởi quá trình nội mạc hóa không hoàn toàn hoặc sự nứt vỡ nội mô thứ phát do các yếu tố khởi kích, chẳng hạn như viêm nội tâm mạc, thoái hóa hoặc hình thành pannus.
Hiệp hội Nghiên cứu Học thuật Van Tim 3 (VARC3) đã phân loại các giai đoạn của huyết khối van nhân tạo gồm 3 giai đoạn: tổn thương về mặt hình thái mà không có thay đổi đáng kể huyết động (giai đoạn 1), suy sụphuyết động trung bình (giai đoạn 2) và suy sụp huyết động trầm trọng (giai đoạn 3).
Huyết khối van tim dưới lâm sàng được định nghĩa là các biểu hiện về hình thái gợi ý huyết khối van tim có thay đổi huyết động nhẹ hoặc không đáng kể và không có triệu chứng lâm sàng hoặc bằng chứng về biến cố thuyên tắc dohuyết khối.2,3
II. DỊCH TỄ HỌC
Huyết khối van tim nhân tạo là một biến chứng của thay van tim nhân tạo bằng phẫu thuật hoặc ống thông. Tỷ lệ huyết khối van tim nhân tạo tùy thuộc vào nhóm bệnh nhân, thuốc chống huyết khối bệnh nhân dùng sau thủ thuật, tiêu chuẩn chẩn đoán và định nghĩa huyết khối. Tỷ lệ huyết khối van nhân tạo ghi nhận 4% sau SAVRvà 13% sau TAVI.Tỷ lệ huyết khối van nhân tạo rõ ràng trên lâm sàng (các triệu chứng liên quan đến hẹp van và tăng độ chênh áp qua van) thấp hơn nhiều (0,6-2,8%), mặc dù cao đáng kể ở bệnh nhân TAVI van trong van (Valve in Valve TAVI: nghĩa là bệnh nhân đã được thay van tim sinh học bằng phẫu thuật mở ngực trước đó, nay van nhân tạo bị thoái hoá gây hẹp, mình đặt thêm 1 valve sinh học qua đường ống thông TAVI chồng lên van sinh học cũ trước đó, còn gọi là thay van ĐMC qua da trên van nhân tạo có sẵn-7,6%)
Ba nghiên cứu quan sát lớn nhất ghi nhận tỷ lệhuyết khối van tim lâm sàng và dưới lâm sàng ở bệnh nhân sau TAVRlà 7-12%.Các yếu tố nguy cơ huyết khối van nhân tạo bao gồm kích thước van lớn và nong van bằng bóng. Kết quả của 20 nghiên cứu với hơn 12.000 bệnh nhân cho thấy tỷ lệ huyết khối van tim dưới lâm sàng và lâm sàng ở bệnh nhân TAVR lần lượt là 15,1% và 1,2%.4
III. SINH LÝ BỆNH
Nguyên nhân của huyết khối van nhân tạo vẫn chưa sáng tỏ hoàn toàn, nhưng sự hình thành huyết khối van nhân tạo là kết quả của tương tác phức tạp giữa các yếu tố liên quan đến thiết bị, các yếu tố đôngcầm máu, huyết động, và bệnh kèm theo của từng bệnh nhân.4
1. Yếu tố liên quan đến thiết bị
Bề mặt van nhân tạo chủ yếu bao gồm collagen tiếp xúc với dòng máu chảy, dẫn đến kích hoạt quá trình đông máu. Các protein như yếu tố von Willebrand, fibrinogen và fibronectin được hấp thụ trên bề mặt van nhân tạo và gây ra sự tích tụ trên van, sau đó là sự kết dính tiểu cầu và bạch cầu, kích hoạt và kết tập tiểu cầu hơn nữa, tạo ra huyết khối. Điều này cuối cùng dẫn đến sự lắng đọng huyết khối giàu tiểu cầu được kết dính lại với nhau bằng các sợi fibrin trên bề mặt van nhân tạo. Quá trình nội mạc hóa van nhân tạo sinh học thường xảy ra khoảng 3 tháng sau khi thay, nhưng huyết khối van vẫn tiếp tục xảy ra sau khoảng thời gian này. Van cơ học thì phải uống kháng đông suốt đời.
Kỹ thuật thay van động mạch chủ qua da cũng có thể làm tăng nguy cơ huyết khối van. Việc gấp mép các lá van nhân tạo sinh học vào hệ thống di chuyển, van nở không hoàn toàn, van giãn nở sau và áp không hoàn toàn vào thành động mạch chủ được cho là những nguyên nhân góp phần gây ra huyết khối van nhân tạo sau đó.
Do đó, tất cả các van nhân tạo đều cần điều trị ngắn hạn và dài hạn bằng thuốc kháng vitamin K và/hoặc thuốc kháng kết tập tiểu cầu để quá trình nội mạc hóa vật liệu nhân tạo không bị gián đoạn.
2. Yếu tố liên quan dòng chảy
Dòng chảy tĩnh hoặc ngưng trệ dẫn đến kích hoạt quá trình đông máu, trong khi dòng chảy hỗn loạn có thể dẫn đến kích hoạt tiểu cầu, tổn thương và gián đoạn tân tạo nội mạc, đồng thời có thể làm tăng khả năng hình thành huyết khối cục bộ. Van nở không hoàn toàn hoặc gắn van nhân tạo vào van động mạch chủ tự nhiên có thể tạo ra các mô hình dòng chảy cục bộ phức tạp, thúc đẩy sự lắng đọng fibrin, kích hoạt tiểu cầu và tạo huyết khối.
Lực căng lên thành động mạch cao từ đáy đến phía đầu lá van, nơi có tốc độ dòng chảy tối đa có thể thúc đẩy qúa trình kích hoạt tiểu cầu. Máu tiếp xúc kéo dài với nơi có sức căng thành cao kết hợp với dòng chảy tuần hoàn có thể kích thích quá trình tạo huyết khối cục bộ.
Khu vực giữa khung van nhân tạo và các lá van tự nhiên được đặt trong stent cũng được ghi nhận là khu vực có lực căng thành thấp nhưng tiềm ẩn các dạng dòng chảy rối có thể tạo ra môi trường tiền huyết khối. Người ta cũng đề xuất rằng việc đặt van nhân tạo ở trên van, thay vì trong vòng van, có thể làm giảm nguy cơ huyết khối lá van.
3. Yếu tố liên quan huyết học
Bất kể yếu tố kích hoạt nào (chẳng hạn như các yếu tố lưu biến hoặc kích hoạt tiếp xúc), kết quả cuối cùng là kích hoạt cả quá trình kết tập tiểu cầu và dòng thác đông máu; tuy nhiên, các khiếm khuyết nội tại đường đông máu thúc đẩy tình trạng tăng đông máu cũng có thể dẫn đến huyết khối van. Các bệnh lý đông máu di truyền hoặc mắc phải đều có khuynh hướng tăng xảy ra các biến cố huyết khối. Một minh chứng cho vai trò quan trọng của con đường đông máu trong huyết khốivan tim là nó được xử trí bằng thuốc kháng đông và thuốc kháng đôngcũng được biết là giúp cải thiện lá van bị hạn chế di động.
4. Các yếu tố liên quan đến bệnh nhân
Phần lớn bệnh nhân TAVI là người cao tuổi, thường có nhiều bệnh đi kèm làm tăng nguy cơ huyết khối sau TAVI. Các yếu tố liên quan đến bệnh nhân làm tăng xu hướng hình thành huyết khối bao gồm rung nhĩ, tuổi cao, tình trạng bất động, bệnh ác tính, hút thuốc lá và suy thận,với rung nhĩ có lẽ là yếu tố nguy cơ được công nhận nhiều nhất. Hầu hết bệnh nhân trải qua TAVI có nguy cơ đột quỵ từ trung bình đến cao trong bối cảnh rung nhĩ có thêm nguy cơ liên quan đến tuổi tác, thường đi kèm với bệnh động mạch hoặc tăng huyết áp, rất phổ biến ở những bệnh nhân này. Rung nhĩ thường được quan sát thấy trong đoàn hệ này và rung nhĩ mới khởi phát được báo cáo ở 14% sau TAVI.
IV. BIỂU HIỆN LÂM SÀNG
Bệnh nhân mang van nhân tạo nên được theo dõi thường xuyên và tư vấn về các triệu chứng gợi ý rối loạn chức năng van nhân tạo.
Tùy thuộc vào khoảng thời gian sau khi thay van, rối loạn chức năng van nhân tạo do hậu quả của sự hình thành huyết khối có thể xảy ra trong tình trạng cấp tính, bán cấp hoặc mạn tính. Trong khi sự hình thành huyết khối mới là một thực thể trong giai đoạn cấp tính (3 ngày đầu tiên sau khi cấy ghép van), sự hình thành huyết khối có tổ chức bao gồm các lớp khác nhau được tìm thấy trong huyết khối van nhân tạo bán cấp (3 tháng đầu) và mạn tính (hơn 1 năm). Do đó, biểu hiện lâm sàng của huyết khối van nhân tạo thay đổi tùy thuộc vào vị trí, kích thước, ảnh hưởng huyết động và mức độ tắc nghẽn của van.4
Khi nào nghi ngờ huyết khối van nhân tạo hoặc tắc nghẽn
Huyết khối van nhân tạo và/hoặc tắc nghẽn nên được nghi ngờ ở bệnh nhân thay van nhân tạo có âm thổi mới hoặc thay đổi tính chất âm thổi, hoặc có triệu chứng cơ năng và thực thể suy tim (ví dụ khó thở, mệt mỏi, ran ẩm ở phổi, ngất, sốc tim).
Bệnh cảnh lâm sàng của huyết khối van nhân tạo có thể phát hiện tình cờ ở bệnh nhân không có triệu chứng, biểu hiện lâm sàng phổ biến nhất có lẽ là triệu chứng khó thở tăng dần, thậm chí ngất, suy tim cấp và nặng nề nhất là sốc tim do tắc nghẽn cơ học. Các triệu chứng của huyết khối van nhân tạo bao gồm các triệu chứng suy tim liên quan đến hẹp hoặc hở van nhân tạo, và các triệu chứng liên quan biến cố thuyên tắc huyết khối (chẳng hạn như cơn thiếu máu não thoáng qua/đột quỵ, đau bụng không rõ nguyên nhân hoặcthiếu máu chi cục bộ).
Cần loại trừ viêm nội tâm mạc nhiễm trùng và rung nhĩ là yếu tốquan trọng khởi kích huyết khối van nhân tạo.5
V. CẬN LÂM SÀNG
1. Xét nghiệm
Các xét nghiệm ban đầu gồm công thức máu toàn bộ, INR ở những bệnh nhân đã được điều trị bằng warfarin và điện tâm đồ ở bệnh nhân suy tim hoặc có dấu hiệu của hội chứng mạch vành cấp.
Nếu mức độ huyết sắc tố thấp, việc đánh giá tình trạng thiếu máu nên thêm xét nghiệm về tán huyết (đánh giá phết máu ngoại vi, số lượng hồng cầu lưới và nồng độ lactate dehydrogenase (LDH) trong huyết thanh, bilirubin, huyết sắc tố tự do và haptoglobin). Tắc nghẽn hoặc hở van sinh học đôi khi liên quan đến tán huyết.
Xét nghiệm bổ sung cho bệnh nhân nghi ngờ HF, bao gồm đánh giá nồng độ natriuretic peptide ([BNP] hoặc NT-proBNP).
2. Điện tâm đồ
Điện tâm đồ được chỉ định ở những bệnh nhân có các triệu chứng gợi ý HF (ví dụ: khó thở, phù), hội chứng mạch vành cấp tính (ví dụ: đau ngực) hoặc đột quỵ. Điện tâm đồ thường không chẩn đoán đượcbệnh nhân huyết khối van nhân tạo hoặc huyết khối tắc mạch. Tuy nhiên, điện tâm đồ có thể giúp xác định các nguyên nhân khác của bệnh lý liên quan như hội chứng mạch vành cấp hoặc rối loạn nhịp tim (ví dụ, rung nhĩ), thuyên tắc mạch vành do huyết khối van nhân tạo là một nguyên nhân hiếm gặp của nhồi máu cơ tim cấp.
3. HÌNH ẢNH HỌC
Siêu âm tim
Siêu âm tim qua thành ngực là phương tiện chẩn đoán hình ảnh đầu tiên được khuyến cáo để đánh giá chức năngvan tim nhân tạo, giúp đánh giá kích thước, chức năng tâm thu thất trái, đường thoát thất trái, độ dày và độ di động van nhân tạo.
Cục máu đông, sùi, thoái hóa, khối u hoặc vết khâu có thể khó phân biệt trên siêu âm tim qua thành ngực nên cần sử dụng thêm các phương tiện hình ảnh học khác. Siêu âm Doppler đánh giá huyết động van nhân tạo nên được thực hiện ngay từ đầu để có thể so sánh với sự thay đổi sau đó. Bất kỳ hở van tim nhân tạo xuất hiện đều cần phải khảo sát về sự tắc nghẽn van.
Các thông số siêu âm tim gợi ý tắc nghẽn van nhân tạo gồm vận tốc đỉnh >3 m/s, chênh áp trung bình >20 mmHg, DVI <0,3, diện tích lỗ van hiệu quả (EOA) <1,2 cm, thời gian gia tốc (AT) >80 ms và đường viền dòng phụt phổ Doppler tròn. Trong đánh giá so sánh, chênh áp qua van trung bình tăng hơn 50% so với ban đầu hoặc >10 mmHg được coi là bệnh lý khi không có cung lượng tim cao để giải thích sự gia tăng bất thường này.2
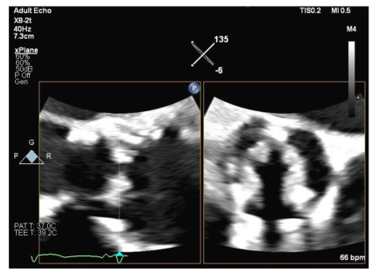
Hình 1. Huyết khối van động mạch chủ nhân tạo.
Siêu âm tim qua thực quản hai bình diện (TEE) ở mức van động mạch chủ cho thấy sự dày lên rõ rệt của các lá van động mạch chủ nhân tạo sinh học, phù hợp với huyết khối tại van.6
Đánh giá van động mạch chủ nhân tạo bằng siêu âm tim qua thực quản có thể cung cấp thêm thông tin về độ dày của lá van, tính di động của lá van và sự hiện diện của sùi hoặc huyết khối, ngoài sự hiện diện của hở van hoặc hở cạnh van. Tuy nhiên, hình ảnh của van có thể bị ảnh hưởng bất lợi bởi bóng lưng, đặc biệt là van động mạch chủ nhân tạo cơ học.
Mặc dù siêu âm tim qua thực quản đã được chứng minh là một công cụ tuyệt vời trong đánh giá huyết động của van hai lá, nhưng nó có những hạn chế trong việc đánh giá huyết động học của van động mạch chủ do vị trí phía trước của van và tầm nhìn hạn chế của van động mạch chủ và đường ra thất trái từ cácgóc nhìn sâu xuyên dạ dày.
Bất chấp những hạn chế, siêu âm tim qua thực quản có thể cung cấp thông tin giá trị khi phân biệt pannus với huyết khối. Pannus trên siêu âm tim qua thực quản có xu hướng nhỏ và tăng âm so với huyết khối. Tuy nhiên, những phát hiện về huyết động cung cấp rất ít giá trị trong việc phân biệt pannus với thương tổn huyết khối.
Bệnh nhân có van nhân tạo nên được đánh giá ban đầu chi tiết về van nhân tạo để xác định huyết động cơ bản (khuyến cáo nhóm I). Hình ảnh học như siêu âm tim qua thành ngực được khuyến cáo thực hiện hàng năm để theo dõi bệnh nhân thay van động mạch chủ qua catheter (khuyến cáo nhóm IIa), sau 5 và 10 năm, sau đó hàng năm ở những bệnh nhân phẫu thuật thay van sinh học (khuyến cáo nhóm IIa). Bất kỳ thay đổi nào về tình trạng lâm sàng của bệnh nhân nên bắt đầu đánh giá nhanh chóng bằng siêm âm tim qua thành ngực, nếu cần, có thể đánh giá thêm bởi siêu âm tim qua thực quản và CT đa đầu dò (khuyến cáo nhóm I).
Một số bệnh nhân không thể kết luận trên siêu âm tim qua thành ngực, siêu âm tim gắng sức có thể thực hiện để đánh giá thay đổi chênh áp qua van nhân tạo và làm tái hiện các triệu chứng lâm sàng. Nhìn chung,tăng chênh áp qua van nhân tạo gợi ý cótắc nghẽn van nhân tạo nên cần kết hợp bệnh cảnh lâm sàng và cần đánh giá thêm về hình ảnh học.5

Hình 2. Chênh áp qua van trên siêu âm tim qua thành ngực. Siêu âm tim qua thành ngực cho thấy chênh áp qua van tăng đáng kể (PG tối đa 126 mm Hg; PG trung bình 74 mm Hg).7
Bảng 1 Đặc điểm lâm sàng và hình ảnh gợi ý huyết khối van nhân tạo2
| Đặc điểm lâm sàng và hình ảnh học | Đặc điểm gợi ý tắc nghẽn van động mạch chủ nhân tạo |
| Biểu hiện lâm sàng | · Khởi phát suy tim mới
· Biến cố thuyên tắc huyết khối |
| Siêu âm tim qua thành ngực | · Chênh áp trung bình >20 mmHg
· Chỉ số vận tốc không thứ nguyên <0,3 · Diện tích lỗ vanhiệu quả <1,2 cm · Đường viền dòng phụt ngược Doppler tròn và đối xứng · Thời gian tăng tốc >80 ms · Dòng phụt ngược qua van mới xuất hiện |
| CT | · Hiển thị huyết khối với Hounsfield <145
· Giảm chuyển động của lá van · Lá vandày hơnvàgiảm đậm độ |
| Soi huỳnh quang | · Cử động giới hạn của các đĩacơ học
· Đĩa bất động · Thay đổi góc mở và đóng so với thông số kỹ thuật/mô tả của nhà sản xuất |
Soi huỳnh quang
Soi huỳnh quang cung cấp thông tin đáng tin cậy nhất về sự di động của lá van nhưng không cho phép đánh giá mô mềm (ví dụ: huyết khối hoặc pannus) liên quan đến van. Soi huỳnh quang thường được thực hiện tốt nhất bởi người có kinh nghiệm ở phòng thông tim. Soi huỳnh quang có thể được sử dụng để đánh giá mức độ di động của lá van, nhưng siêu âm tim qua thực quản thường được ưa chuộng hơn vì nó cho phép đánh giá thêm tính chất của khối trên lá van.2
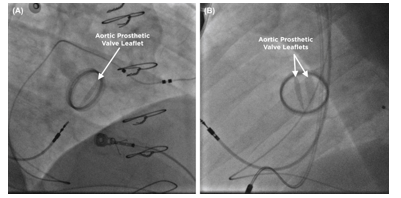
Hình 3. Soi huỳnh quang. (A) Hình ảnh khung van nhân tạo động mạch chủ thì tâm thu của bệnh nhân. Chỉ một trong hai lá van mở. (B) Khung van nhân tạo động mạch chủ thì tâm thu sau khi xử trí huyết khối hoàn toàn bằng liệu pháp tiêu sợi huyết.8
Chụp cắt lớp vi tính
Chụp cắt lớp vi tính đa đầu dò (MDCT, multidetector computed tomography) — CT đa đầu dò cho phép đánh giá hình dạng và chuyển động của lá van nhân tạo cũng như các đặc điểm của huyết khối. CT đa đầu dò và soi huỳnh quang tương quan tốt trong việc xác định chuyển động của lá van bị hạn chế, nhưng CT đa đầu dò còn cho phép đánh giá các khối cạnh van. CT đa đầu dò cũng hữu ích trong việc xác định các chẩn đoán thay thế (tương tự như TEE), vì nó có thể phát hiện sùi với độ chính xác gần bằng siêu âm tim qua thực quản và CT đa đầu dò có thể xác định huyết khối nhĩ với độ chính xác gần bằng siêu âm tim qua thực quản. Tuy nhiên, các khối mỏng, di động cao có thể khó phát hiện bằng CT đa đầu dò do độ phân giải theo thời gian.
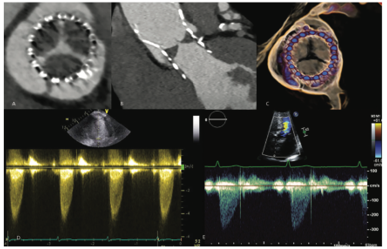
Hình 4. Hình ảnh CT cho thấy huyết khối>75% các lá van động mạch chủ nhân tạo sinh học thay qua ống thông (A, B và C) và vận tốc đỉnh tăng>4 m/s (D). Vận tốc đỉnh qua van nhân tạo sinh học 30 ngày sau khi điều trị kháng đông cải thiện đáng kể (E)2.
VI. CHẨN ĐOÁN PHÂN BIỆT
Đối với tắc nghẽn van động mạch mạch chủ
Đối với tắc nghẽn van nhân tạo, cần phân biệt tắc nghẽn van với các nguyên nhân khác gây tắc nghẽn đường ra thất trái hoặc tăng chênh áp qua van nhân tạo, chẳng hạn như sự không phù hợp giữa bệnh nhân và van nhân tạo, hở van nhân tạo, viêm nội tâm mạc và tăng thể tích nhát bóp (ví dụ, tình trạng cung lượng tim cao).
Loại trừ viêm nội tâm mạc do van nhân tạo
Đối với những bệnh nhân có hình dạng hoặc tính di động của van nhân tạo bất thường, điều quan trọng là cần loại trừ viêm nội tâm mạc van nhân tạo, thường có các dấu hiệu và triệu chứng của nhiễm trùng xâm lấn.
Phân biệt nguyên nhân chính gây tắc nghẽn do huyết khối và pannus
Ở những bệnh nhân có biểu hiện tắc nghẽn van nhân tạo, một khi viêm nội tâm mạc đã được loại trừ, điều quan trọng là phải phân biệt huyết khối với pannus do khác biệt trong phương pháp điều trị.
Đặc điểm gợi ý huyết khối:
- Đặc điểm lâm sàng – Các triệu chứng khởi phát cấp tính hơn và bệnh sử không tuân thủ dùng thuốc kháng đông.
- Hạn chế di động của lá van.
- Phát hiện khối phù hợp với huyết khối gợi ý huyết khối, nhưng nếu không thấy khối cũng không được loại trừ huyết khối. Huyết khối nằm ở hạ lưu của van (phía tâm thất trái, phía động mạch chủ đối với van bán nguyệt được thay) thường rất khó thấy qua siêu âm tim hoặc CT.9
Các đặc điểm sau gợi ý huyết khối trên siêu âm tim:
- Độ phản âm thấp hơn so với pannus. Mặc dù mật độ phản âm của huyết khối và pannus chồng lấp lên nhau, các khối có tỷ lệ cường độcản âm thấp nhất (tỷ lệ cản âm của khối trên siêu âm so vớivan nhân tạo <0,45) là huyết khối.
- Huyết khối có thể có hình dạng bất thường và bám vào các lá van tim nhân tạo hoặc các điểm bản lề.
- Một khối di động thường gặp ở bệnh nhân có huyết khối hoặc huyết khối kèm theo pannus.7
Đặc điểm gợi ý pannus:
- Thường độ cản âmlớn hơn huyết khối.
- Độ di động của lá van có thể bình thường hoặc bị hạn chế. Ở một bệnh nhân mới bị tắc van cơ học, nếu siêu âm tim qua thực quản thấy rõ di động của lá van bình thường, thì có khả năng là pannus.
- Bệnh nhân có pannus có thể không thấy trên siêu âm 2 D qua thực quản.
- Khối nằm dọc theo vòng van.7
VII. ĐIỀU TRỊ
Điều trị huyết khối van nhân tạo bao gồm điều trị giai đoạn cấp tính và điều trị lâu dài. Các phương pháp điều trị bao gồm điều trị nội khoa suy tim, thuốc chống huyết khối (tiêu sợi huyết, thuốc kháng đông và kháng kết tập tiểu cầu) và điều trị phẫu thuật thay van tim.10 Yếu tố chính cần cân nhắc là đánh giá tắc nghẽn van nhân tạo cơ học tập trung vào việc phân biệt hai nguyên nhân này vì huyết khối có thể được điều trị bằng thuốc kháng đông, tiêu sợi huyết hoặc phẫu thuật van (lấy huyết khối hoặc thay van lại), trong khi pannus chỉ có thể được điều trị bằng phẫu thuật.12
1. Điều trị nội khoa suy tim
Trong số những bệnh nhân bị tắc nghẽn van nhân tạo có triệu chứng, điều trị nội khoa suy tim như một biện pháp đầu tiên và giảm nhẹ trong thời gian chờ điều trị nguyên nhân gây tắc nghẽn. Điều trị nội khoa cần thận trọng khi dùng thuốc lợi tiểu và các thuốc khác (ví dụ như thuốc ức chế men chuyển angiotensin), do tăng nguy cơ tác dụng phụ khi cố gắng điều trị.11
2. Điều trị chống huyết khối tối ưu
Đối với những bệnh nhân có huyết khối van nhân tạo không gây tắc nghẽn <0,8 cm2, các tác giả khuyến cáo điều trị kháng đông tối ưu (với heparin không phân đoạn truyền tĩnh mạch, sau đó là thuốc kháng vitamin K) kết hợp với aspirin 75 đến 100 mg/ngày, theo dõi bằng siêu âm tim, dựa trên bằng chứng hạn chế từ các nghiên cứu quan sát. Các nghiên cứu quan sát này đã báo cáo giải quyết một phần huyết khối bằng thuốc kháng đông (có hoặc không có aspirin) trong một tuần ở 72 đến 100% bệnh nhân bị huyết khối van nhân tạo không tắc nghẽn. Các nghiên cứu nhỏ đã gợi ý rằng nguy cơ biến chứng nặng (đột quỵ hoặc tắc nghẽn) thấp hơn ở những bệnh nhân có huyết khối nhỏ (<5 mm) so với huyết khối lớn hơn.11,13
3. Tiêu sợi huyết
Phác đồ dùng tiêu sợi huyết
Đối với bệnh nhân huyết khối van nhân tạo có chỉ định tiêu sợi huyết (còn được gọi là tiêu huyết khối), các tác giả đề xuất phác đồ liều thấp truyền cực chậm dựa trên các nghiên cứu quan sát. Dùng hình ảnh học theo dõi để đánh giá hiệu quả của tiêu sợi huyết bằng siêu âm tim qua thành ngực (TTE) thường được sử dụng để xác định ảnh hưởng đến độ chênh áp qua van nhân tạo trong các trường hợp tắc nghẽn và siêu âm tim qua thực quản (TEE) thường được sử dụng để xác định kích thước huyết khối và hình dạng của van nhân tạo.14
- Đánh giá các chống chỉ định của liệu pháp tiêu sợi huyết (tương tự như trong trường hợp nhồi máu cơ tim)
- Nếu bệnh nhân có chống chỉ định dùng thuốc tiêu sợi huyết thì nên tiến hành phẫu thuật thay van tim (cắt huyết khối hoặc thay van lại).
- Nếu không có chống chỉ định tiêu sợi huyết, ngưng thuốc chống đông trong quá trình điều trị tiêu sợi huyết và chờ đến khi INR <2,5 (hoặc aPTT<50 giây nếu bệnh nhân đang dùng heparin không phân đoạn) trước khi bắt đầu điều trị tiêu sợi huyết.
- Truyền tĩnh mạch 25 mg alteplase trong 25 giờ mà không cần dùng liều tải. Tiếp theo là truyền heparin không phân đoạn trong 6 giờ (70 đơn vị/kg bolus và 16 đơn vị/kg/giờ [tối đa 1000 đơn vị/giờ] với aPTT mục tiêu từ 1,5 đến 2,0 lần giá trị chứng.
- Đối với bệnh nhân bị tắc nghẽn van nhân tạo, siêu âm tim qua thành ngực giúp đánh giá độ chênh áp qua van nhân tạo.
- Nếu độ chênh áp giảm, thực hiện siêu âm tim qua thực quản:
- Nếu siêu âm tim qua thực quản (TEE) cho thấy huyết khối đã phân giải một phần (giảm kích thước <75 phần trăm),truyền 25 mg alteplase lặp lại trong 25 giờ, sau đó truyền UFH trong 6 giờ, sau đó lặp lại siêu âm tim qua thực quản.
- Nếu TEE cho thấy huyết khối đã phân giải (kích thước giảm ≥75 phần trăm), dừng alteplase và bắt đầu dùng heparin không phân đoạn và kháng vitamin K.
- Nếu độ chênh áp không cải thiện, truyền 25 mg alteplase lặp lại trong 25 giờ, sau đó truyền UFH trong 6 giờ, sau đó lặp lại siêu âm tim qua thực quản.
- Đối với bệnh nhân bị huyết khối không tắc nghẽn, lặp lại siêu âm tim qua thực quản.
- Nếu huyết khối được điều trị hiệu quả (kích thước giảm ≥75 phần trăm), dừng alteplase và bắt đầu heparin không phân đoạn và kháng vitamin K.
- Nếu huyết khối không thay đổi hoặc chỉ hiệu quả một phần (giảm kích thước <75 phần trăm), lặp lại truyền 25 mg alteplase trong 25 giờ, sau đó truyền UFH trong 6 giờ, sau đó lặp lại siêu âm tim qua thực quản.
- Đối với những bệnh nhân bị huyết khối dai dẳng khi thực hiện TEE lặp lại, có thể truyền 25 mg alteplase lặp lại trong 25 giờ (tiếp theo là truyền heparin không phân đoạn trong 6 giờ) nếu cần (đánh giá bằng siêu âm tim qua thực quản sau dùng mỗi liều) cho đến liều tích lũy tối đa là 200 mg của alteplase. Hầu hết bệnh nhân cần truyền không quá ba lần.
Khi tiêu sợi huyết thành công, bệnh nhân bắt đầu dùngheparin không phân đoạn và kháng vitamin K. Heparin không phân đoạn tiếp tục dùng cho đến khi kháng vitamin K đạt INR mục tiêu trong hai ngày liên tiếp.10,11
Bằng chứng khi dùng tiêu sợi huyết
Bằng chứng để hướng dẫn tiêu sợi huyết ở bệnh nhân huyết khối van nhân tạo còn hạn chế. Chỉ có dữ liệu quan sát về hiệu quả và độ an toàn của phác đồ điều trị tiêu sợi huyết đối với huyết khối van nhân tạo. Dữ liệu so sánh đối đầu giữa các cách dùng tiêu sợi huyết khác nhau còn thiếu, hầu hết các nghiên cứu chỉ giới hạn ở kinh nghiệm đơn trung tâm. Hầu hết các bằng chứng được công bố về quá trình tiêu sợi huyết đối với huyết khối van nhân tạo liên quan đến alteplase và chủ yếu tập trung vào huyết khối bên trái. Các nghiên cứu sử dụng phương pháp truyền chậm hoặc siêu chậm dưới sự hướng dẫn của siêu âm tim, phác đồ tiêu sợi huyết liều thấp đã chứng minh tỷ lệ hiệu quả cao (85 đến 90 phần trăm hoặc cao hơn) với tỷ lệ biến chứng tương đối thấp (ví dụ: 10,5 phần trăm bao gồm cả không tử vong khi truyền trong 6 giờ; 6,7% [bao gồm tỷ lệ tử vong 0,8%] với truyền trong 25 giờ). Kết quả với các chế độ điều trị chậm hoặc siêu chậm liều thấp thuận lợi hơn so với kết quả quan sát trong các nghiên cứu tiêu sợi huyết trước đó (trước năm 2013) với tốc độ truyền nhanh và liều cao hơn (tỷ lệ thành công về huyết động là 75%, tỷ lệ tử vong trong 30 ngày là 7%, tỷ lệ thuyên tắc huyết khối 13%, và tỷ lệ chảy máu nặng là 6%).15
Một nghiên cứu về 120 lượt bị huyết khối van nhân tạo ở 114 bệnh nhân với độ tuổi trung bình là 49, phác đồ truyền cực chậm 25 mg alteplase trong 25 giờ mà không cần liều tải (dựa trên kết quả TTE/TEE lặp lại đến 8 lần, tổng cộng 200 mg) đã thành công ở 90% bệnh nhân, với tỷ lệ biến chứng 6,7% (0,8% tử vong, 3,3% biến chứng nặng không gây tử vong và 2,5% biến chứng nhẹ). Số lần truyền tiêu sợi huyết trung bình là 2 (từ 1 đến 8). NYHA III/IV là yếu tố dự báo độc lập duy nhất thất bại điều trị tiêu sợi huyết. Các yếu tố dự đoán biến chứng là rung nhĩ, diện tích huyết khối lớn (>1 cm2) và phân loại NYHA cao; tỷ lệ biến chứng cao nhất ở những bệnh nhân có triệu chứng NYHA IV (75%). Một bệnh nhân tử vong có triệu chứng suy tim với phân độ chức năng NYHA IV.14
4. Phẫu thuật
Dữ liệu quan sát về vai trò của phẫu thuật bệnh nhân bị tắc van nhân tạo hoặc huyết khối còn giới hạn. Phẫu thuật điều trị tắc nghẽn hoặc huyết khối van nhân tạo (thay van hoặc phẫu thuật lấy huyết khối) liên quan đến tỷ lệ tử vong phẫu thuật cao (tỷ lệ tử vong chung trong 30 ngày từ 10 đến 15%) phần lớn liên quan đến phân độ chức năng suy tim (ví dụ: 17,5% ở bệnh nhân có các triệu chứng NYHA loại IV so với 4,7 phần trăm với các triệu chứng NYHA loại I đến III khi khảo sát 106 bệnh nhân). Tỷ lệ tử vong cao đến 35% đã được ghi nhận ở những bệnh nhân có tình trạng bệnh trầm trọng.10,16
So sánh phẫu thuật với tiêu sợi huyết
Bằng chứng để so sánh kết quả giữa phẫu thuật và tiêu sợi huyết ở bệnh nhân huyết khối van nhân tạo còn hạn chế.
Một phân tích tổng hợp gồm 48 nghiên cứu về phẫu thuật và/hoặc tiêu sợi huyết ở 2302 bệnh nhân huyết khối van tim nhân tạo. Tỷ lệ tử vong ở những bệnh nhân được điều trị bằng phẫu thuật cao hơn đáng kể so với những bệnh nhân được điều trị bằng liệu pháp tiêu sợi huyết (18,1% so với 6,6%). Phẫu thuật có biến chứng thuyên tắc huyết khối thấp hơn đáng kể (4,6 so với 12,8%), nhưng tỷ lệ đột quỵ (4,3 so với 5,6%) và chảy máu (4,6 so với 6,8%) ở hai nhóm là như nhau.17
Mặc dù còn thiếu dữ liệu được kiểm chứng, nhưng một số khuyến cáo đề nghị đánh giá cá nhân hóa các yếu tố lâm sàng nhằm lựa chọn phương pháp điều trị phù hợp (ví dụ: phẫu thuật lấy huyết khối lớn hơn và tiêu sợi huyết ở bệnh nhân có huyết khối nhỏ).10
5. Điều trị tùy theo loại van
Van động mạch chủ nhân tạo cơ học
Những bệnh nhân nghi ngờ có huyết khối van cơ học với triệu chứng khởi phát cấp tính gợi ý suy tim, sốc hoặc biến cố thuyên tắc huyết khối, hình ảnh học khẩn cấp được khuyến cáo để đánh giá độ lớn của huyết khối và rối loạn chức năng van.2
Trong các trường hợp huyết khối van nhân tạo cơ học đã được xác định chẩn đoán, quyết định điều trị tối ưu bằng phẫu thuật cấp cứu hoặc truyền chậm tiêu sợi huyết dựa trên nhiều yếu tố sau đây:
Bảng 2. Chọn lựa giữa phẫu thuật và tiên sợi huyết
| Các yếu tố thích hợp phẫu thuật cấp cứu | Các yếu tố thích hợp dùng tiêu sợi huyết |
| • Triệu chứng phân độ chức năng NYHA IV
• Kích thước cục máu đông lớn (>0.8 cm2) • Có huyết khối nhĩ trái • Huyết khối van timtái phát • Chống chỉ định tiêu sợi huyết • Chuyên môn phẫu thuật sẳn có • Cópannus • Nguy cơ phẫu thuật thấp • Bệnh cần phẫu thuật do bệnh lý tim khác |
• Triệu chứng NYHA I, II hoặc III.
• Kích thước cục máu đông nhỏ (≤0,8 cm2) • Không có huyết khối nhĩ trái • Lần đầu bị huyết khối van nhân tạo • Không có chống chỉ định tiêu sợi huyết • Không có kinh nghiệm về phẫu thuật tim • Bệnh nhân nguy cơ cao khi phẫu thuật |
Truyền chậm tiêu sợi huyết 25 mg trong 25 giờ có tỷ lệ thành công về huyết động học >90% với nguy cơ tắc mạch và chảy máu nặng <2% ở những bệnh nhân thoả tiêu chí lựa chọn. Hình ảnh học được thực hiện để đánh giá chênh áp qua van nhân tạo và hiệu quả của tiêu sợi huyết. Hình sau minh họa một trường hợp huyết khối van cơ học được điều trị thành công bằng tiêu sợi huyết đường tĩnh mạch2.
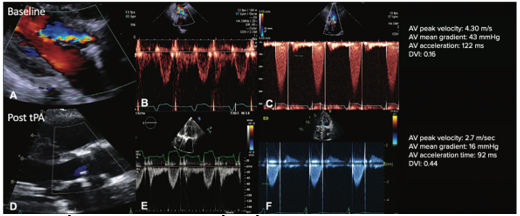
Hình 5. Kết quả siêu âm tim huyết khối van động mạch chủ cơ học trước và sau điều trị tiêu sợi huyết. Hình ảnh ban đầu cho thấy hở van động mạch chủ nhân tạo vừa phải (A) với tăng vận tốc đỉnh, chênh áp trung bình, thời gian tăng tốc và DVI giảm (B và C). Xử trí hoàn toàn huyết khối van nhân tạo, không có thêm bằng chứng hở van động mạch chủ ở hình (D), và bình thường hóa vận tốc Doppler và huyết động học qua van nhân tạo ở hình (E và F)2.
Phẫu thuật thay van nhân tạo sinh học và thay van động mạch chủ qua ống thông
Ở những bệnh nhân nghi ngờ có huyết khối van nhân tạo sinh học, hình ảnh học chi tiết nhằm đánh giá đầy đủ chức năng van nhân tạo và khả năng di động van tim. Với huyết khối van nhân tạo sinh học chẩn đoán xác định hoặc nghi ngờ cao, nên điều trị bằng thuốc kháng vitamin K (khuyến cáo nhóm IIa).
Các nghiên cứu nhỏ đã đánh giá thời điểm và thời gian điều trị kháng đông. Nhìn chung, có rất ít dữ liệu về thời gian điều trị kháng đông đối với huyết khối van nhân tạo sinh học. Tuy nhiên, phân tích hình ảnh học sau điều trị cho thấy huyết khối đã được xử trí trong vòng 14 ngày kể từ ngày bắt đầu điều trị, được minh chứng bằng giảm độ chênh áp qua van. Cho đến nay chưa có hướng dẫn về thời gian dùng kháng đông tối ưu.2
Dùng kháng đông bằng kháng vitamin K được khuyến cáo ưu tiên hơn so với thuốc kháng đông đường uống trực tiếp.Hiện tại, dữ liệu về kháng đông còn hạn chế ở bệnh nhân lá van dầy giảm đậm độ và lá van giảm di động.
6. Điều trị dài hạn sau biến cố tắc van nhân tạo do huyết khối
Khi huyết khối van nhân tạo xảy ra mặc dù đã điều trị bằng thuốc chống huyết khối, bước đầu tiên quan trọng là xác định thuốc chống huyết khối nào (ví dụ: warfarin và/hoặc aspirin) mà bệnh nhân đang dùng và mức độ hiệu quả của thuốc kháng đông(bao gồm thời gian đạt mục tiêu điều trị gần đây). Nguy cơ biến chứng chảy máu khi tăng liều kháng đông cũng nên được đánh giá. Liệu pháp chống huyết khối tiêu chuẩn cho van cơ học bao gồm aspirin liều thấp (75 đến 100 mg/ngày) kết hợp với thuốc kháng đông (thuốc kháng vitamin K hoặc heparin). Thuốc kháng đông đường uống trực tiếp (thuốc ức chế thrombin trực tiếp đường uống và thuốc ức chế yếu tố Xa) không được khuyến cáo sử dụng cho bệnh nhân có van nhân tạo cơ học.
Nếu liệu pháp chống huyết khối không đủ trước khi xảy ra huyết khối van nhân tạo hoặc thuyên tắc huyết khối, cần tiến hành liệu pháp thích hợp, bao gồm tối ưu hóa khoảng thời gian INR đạt mục tiêu (ví dụ: giáo dục bệnh nhân, theo dõi thường xuyên hơn, quản lý bởi phòng khám kháng đông chuyên nghiệp do dược sĩ hướng dẫn hoặc bệnh nhân tự giám sát), nên là bước điều trị đầu tiên.18,19
Cách tiếp cận sau đây được đề xuất cho những bệnh nhân có van nhân taọ cơ học đã được điều trị huyết khối van tim:
- Đối với bệnh nhân thuyên tắc huyết khối đã được điều trị kháng đông đầy đủ bằng VKA (ví dụ: warfarin) nhưng không dùng aspirin, có thể thêm aspirin (75 đến 100 mg/ngày).
- Đối với bệnh nhân thuyên tắc huyết khối hoặc huyết khối van trong khi điều trị kháng đông đạt mục tiêu INR là 2,5 (ví dụ: bệnh nhân thay van động mạch chủ cơ học mà không có các yếu tố nguy cơ khác) và đang dùng aspirin, tăng mục tiêu INR lên 3,0.
- Đối với bệnh nhân thuyên tắc huyết khối hoặc huyết khối van khi điều trị kháng đông đạt mục tiêu INR là 3,0 cộng với aspirin, mục tiêu INR có thể cần tăng lên 4,0.19
VIII. DỰ PHÒNG
Van động mạch chủ nhân tạo cơ học
Phòng ngừa huyết khối van động mạch chủ cơ học là điều cần thiết , những bệnh nhân này cần điều trị kháng đông suốt đời bằng kháng vitamin K với mục tiêu INRcụ thể.
Mục tiêu INR là 2,5 (2–3) được khuyến cáo cho những bệnh nhân không có yếu tố nguy cơ thuyên tắc huyết khối nào khác. Ở những bệnh nhân có các yếu tố nguy cơ thuyên tắc huyết khối bao gồm rung nhĩ, tiền sử thuyên tắc huyết khối trước đó, tình trạng tăng đông, van cơ học thế hệ cũ và rối loạn chức năng tâm thu thất trái, mục tiêu INR là 3 (2,5–3,5).
Kết hợp kháng kết tập tiểu cầu và kháng vitanin K làm tăng nguy cơ chảy máu. Tuy nhiên, ở những bệnh nhân có van động mạch chủ nhân tạo cần dùng kháng kết tập tiểu cầu, nên dùng aspirin liều thấp (75–100 mg) (khuyến cáo nhóm IIa).10
Van nhân tạo sinh học
Trong trường hợp không có các yếu tố nguy cơ chảy máu, bệnh nhân thay van động mạch chủ sinh học bằng phẫu thuật được điều trị bằng kháng vitamin K trong ít nhất 3 tháng và tối đa 6 tháng (khuyến cáo nhóm IIa).
Điều trị bằng kháng vitamin K có thể được chuyển sang thuốc chống đông đường uống trực tiếp sau 6 tháng nếu cần tiếp tục điều trị kháng đông (ví dụ như trong rung nhĩ). Nếu không cần dùng kháng đông đường uống, khuyến cáo điều trị suốt đời bằng aspirin liều thấp cho nhóm bệnh nhân này (khuyến cáo nhóm IIa).10
Thay van động mạch chủ qua ống thông
Điều trị bệnh nhân sau TAVR vẫn còn tranh cãi và nhiều nghiên cứu đang được tiến hành để giải quyết nhu cầu điều trị kháng đông ở bệnh nhân thay van ĐMCqua ống thông.
Trong các hướng dẫn hiện tại về điều trị bệnh van tim, các thuốc kháng tiểu cầu đơn được ưu tiên ở những bệnh nhân TAVR và không có chỉ định nào khác cần dùng kháng đông hoặc kháng kết tập tiểu cầu kép (khuyến cáo nhóm IIa). Hiện nay, phác đồ dùng kháng tiểu cầu kép khuyến cáo nhóm IIb vì tăng nguy cơ chảy máu.
Ở những bệnh nhân nghi ngờ có huyết khối TAVR hoặc huyết khối dưới lâm sàng và bệnh nhân cần dùng thuốc kháng đông cho các chỉ định khác, kháng vitamin Kđược ưu tiên hơn thuốc kháng đông đường uống trực tiếp (khuyến cáo nhóm IIb).20
KẾT LUẬN
Thay van động mạch chủ nhân tạo qua phẫu thuật và qua ống thông đều có thể bị huyết khối. Khi bệnh nhân có thay đổi về lâm sàng hoặc huyết động học của van nhân tạo nênnghi ngờ về rối loạn chức năng van nhân tạo, bao gồm cả tắc nghẽn van nhân tạo. Hình ảnh học,đặc biệt là CT đa đầu dò, như chìa khóa để xác định chẩn đoán.
Chiến lược điều trị tối ưu phụ thuộc vào loại van, bên cạnh các yếu tố khác nhau liên quan đến bệnh nhân và hình ảnh cụ thể. Điều trị kháng đông hoặc kháng kết tập tiểu cầu sau phẫu thuật nên được chú trọng ởbệnh nhân thay van động mạch chủ nhân tạo để giảm nguy cơ huyết khối van.
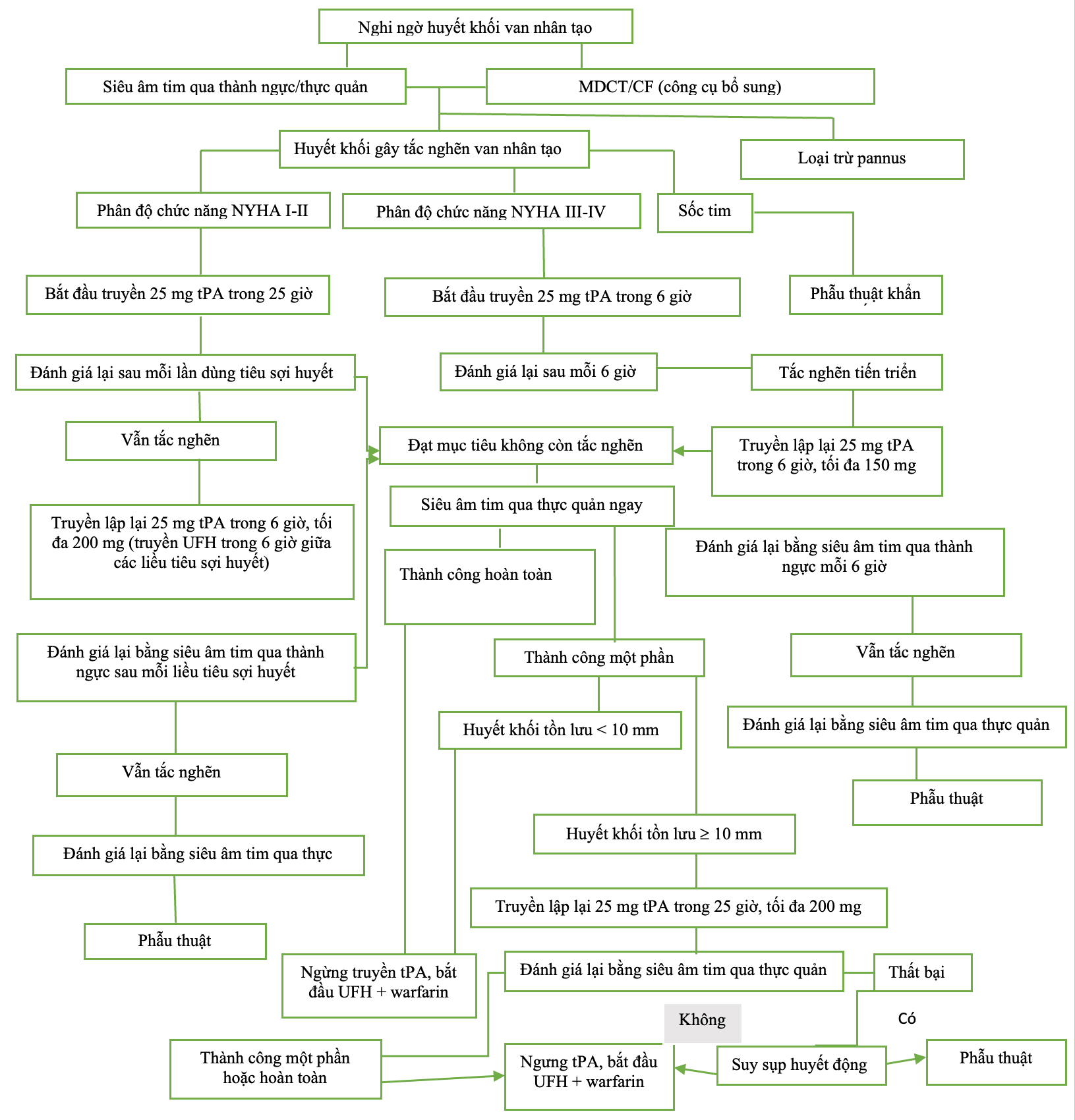
Hình 6: Lưu đồ xử trí tắc nghẽn van nhân tạo do huyết khối. CF= nội soi huỳnh quang; MDCT= chụp cắt lớp vi tính đa đầu dò; NYHA= Hiệp hội Tim mạch New York; PVT = huyết khối van nhân tạo; TEE = siêu âm tim qua thực quản; t-PA = chất kích hoạt plasminogen mô; TT = điều trị bằng tiêu sợi huyết; TTE = siêu âm tim qua thành ngực; UFH = heparin không phân đoạn16.
Tài liệu tham khảo
- Mirsadraee S, Sellers S, Duncan A, Hamadanchi A, Gorog DA. Bioprosthetic valve thrombosis and degeneration following transcatheter aortic valve implantation (TAVI). Clin Radiol. Jan 2021;76(1):73.e39-73.e47. doi:10.1016/j.crad.2020.08.015
- Pournazari P, Chang SM, Little SH, Goel S, Faza NN. Prosthetic Aortic Valve Thrombosis. US Cardiology Review 2022;16:e17. 2022;doi:10.15420/usc.2021.19
- Cahill TJ, Chen M, Hayashida K, et al. Transcatheter aortic valve implantation: current status and future perspectives. Eur Heart J. Jul 21 2018;39(28):2625-2634. doi:10.1093/eurheartj/ehy244
- Abdel-Wahab M, Simonato M, Latib A, et al. Clinical Valve Thrombosis After Transcatheter Aortic Valve-in-Valve Implantation. Circulation: Cardiovascular Interventions. 2018;11(11):e006730. doi:doi:10.1161/CIRCINTERVENTIONS.118.006730
- Shahinian JH, Chan V, Pislaru SV. Chronic thrombosis of bioprostheses: Diagnosis and management. Prog Cardiovasc Dis. May-Jun 2022;72:15-20. doi:10.1016/j.pcad.2022.06.008
- Alexander SA, Fergus IV, Lerakis S. Bioprosthetic Valve Thrombosis Associated With COVID-19 Infection. Circ Cardiovasc Imaging. May 2021;14(5):e012118. doi:10.1161/circimaging.120.012118
- Tanis W, Habets J, van den Brink RB, Symersky P, Budde RP, Chamuleau SA. Differentiation of thrombus from pannus as the cause of acquired mechanical prosthetic heart valve obstruction by non-invasive imaging: a review of the literature. Eur Heart J Cardiovasc Imaging. Feb 2014;15(2):119-29. doi:10.1093/ehjci/jet127
- Noohi F, Sadeghpour A, Alizadehasl A. Chapter 30 – Valvular Heart Disease. In: Maleki M, Alizadehasl A, Haghjoo M, eds. Practical Cardiology (Second Edition). Elsevier; 2022:527-571.
- Suchá D, Symersky P, Tanis W, et al. Multimodality Imaging Assessment of Prosthetic Heart Valves. Circ Cardiovasc Imaging. Sep 2015;8(9):e003703. doi:10.1161/circimaging.115.003703
- Otto CM, Nishimura RA, Bonow RO, et al. 2020 ACC/AHA Guideline for the Management of Patients With Valvular Heart Disease: A Report of the American College of Cardiology/American Heart Association Joint Committee on Clinical Practice Guidelines. Circulation. Feb 2 2021;143(5):e72-e227. doi:10.1161/cir.0000000000000923
- Vahanian A, Beyersdorf F, Praz F, et al. 2021 ESC/EACTS Guidelines for the management of valvular heart disease. Eur Heart J. Feb 12 2022;43(7):561-632. doi:10.1093/eurheartj/ehab395
- Biteker M, Altun I, Basaran O, Dogan V, Yildirim B, Ergun G. Treatment of Prosthetic Valve Thrombosis: Current Evidence and Future Directions. J Clin Med Res. Dec 2015;7(12):932-6. doi:10.14740/jocmr2392w
- Laplace G, Lafitte S, Labèque JN, et al. Clinical significance of early thrombosis after prosthetic mitral valve replacement: a postoperative monocentric study of 680 patients. J Am Coll Cardiol. Apr 7 2004;43(7):1283-90. doi:10.1016/j.jacc.2003.09.064
- Özkan M, Gündüz S, Gürsoy OM, et al. Ultraslow thrombolytic therapy: A novel strategy in the management of PROsthetic MEchanical valve Thrombosis and the prEdictors of outcomE: The Ultra-slow PROMETEE trial. Am Heart J. Aug 2015;170(2):409-18. doi:10.1016/j.ahj.2015.04.025
- Özkan M, Çakal B, Karakoyun S, et al. Thrombolytic therapy for the treatment of prosthetic heart valve thrombosis in pregnancy with low-dose, slow infusion of tissue-type plasminogen activator. Circulation. Jul 30 2013;128(5):532-40. doi:10.1161/circulationaha.113.001145
- Özkan M, Gündüz S, Güner A, et al. Thrombolysis or Surgery in Patients With Obstructive Mechanical Valve Thrombosis. Journal of the American College of Cardiology. 2022/03/15 2022;79(10):977-989. doi:10.1016/j.jacc.2021.12.027
- Castilho FM, De Sousa MR, Mendonça AL, Ribeiro AL, Cáceres-Lóriga FM. Thrombolytic therapy or surgery for valve prosthesis thrombosis: systematic review and meta-analysis. J Thromb Haemost. Aug 2014;12(8):1218-28. doi:10.1111/jth.12577
- Sondergaard L, De Backer O, Kofoed KF, et al. Natural history of subclinical leaflet thrombosis affecting motion in bioprosthetic aortic valves. Eur Heart J. Jul 21 2017;38(28):2201-2207. doi:10.1093/eurheartj/ehx369
- Petrescu I, Egbe AC, Ionescu F, et al. Long-Term Outcomes of Anticoagulation for Bioprosthetic Valve Thrombosis. J Am Coll Cardiol. Mar 3 2020;75(8):857-866. doi:10.1016/j.jacc.2019.12.037
- Dangas GD, Tijssen JGP, Wöhrle J, et al. A Controlled Trial of Rivaroxaban after Transcatheter Aortic-Valve Replacement. New England Journal of Medicine. 2019;382(2):120-129. doi:10.1056/NEJMoa1911425







