Đột tử do tim (SCD) chiếm > 300.000 ca tử vong ở Mỹ mỗi năm. [1] Mặc dù đa số các trường hợp tử vong xảy ra trong nhóm có nguy cơ thấp [2], trong đó biện pháp can thiệp tích cực là không thực tế, một số quần thể nguy cơ cao hơn đã được thiết lập ở các can thiệp bệnh nhân với cấy máy khử rung (ICD) đã được chứng minh trong các thử nghiệm ngẫu nhiên để giảm tỷ lệ tử vong.
TS Phạm Hữu Văn
[3-7] Ngoài ra, có một số bệnh nhân có thể hưởng lợi từ khử rung tim khẩn cấp tự động nhưng không được coi là ứng viên phù hợp cho cấy ICD tại thời điểm có biểu hiện. Nhóm này được xác định ở 2 quần thể. Phân nhóm thứ nhất gồm những người có nguy cơ được nhận biết nhưng có thể có hy vọng để cải thiện lâm sàng (ví dụ, bệnh nhân ngay sau khi tái thông mạch máu hoặc những người có chẩn đoán nhồi máu cơ tim – MI – và bệnh cơ tim vừa mới xẩy ra). Nói cách khác, việc điều trị tối ưu những bệnh nhân này có nguy cơ (hay rủi ro đã được biết) trong khoảng thời gian chờ đợi trước khi ICD được chỉ định còn chưa rõ. Phân nhóm thứ hai bao gồm những người có chỉ định rõ ràng cho ICD nhưng có chống chỉ định cấy ICD cấp thời (ví dụ, nhiễm trùng đang hoạt động hoặc tiên lượng chưa biết).
Áo khử rung tim(wearble cardiovertor difibrilator: WCD) là một thiết bị được thiết kế cho những bệnh nhân có nguy cơ SCD song không phải là ứng viên ngay lập tức cho điều trị ICD. Bằng cách cung cấp liệu pháp tự động, WCD không phụ thuộc vào một người thứ hai để đánh sốc, khi được đòi hỏi với khử rung tim bằng tay hoặc tự động ngoài (AED). Không có khả năng (gồm cả hai đường tĩnh mạch và dưới da), WCD không cần phẫu thuật, có thể cung cấp cho một khoảng thời gian ngắn, chỉ tạm thời và có thể dễ dàng gỡ bỏ. Những đặc tính của WCD, cùng với dữ liệu an toàn và hiệu quả được trình bày cho FDA (Food and Drug Administration), đã được phê chuẩn ở HK năm 2002,[8] Ở Việt Nam chúng ta, cho đến nay, chưa cơ một cơ sở y tế nào được trang bị áo khử rung tim. Việc soạn bài này, chúng tôi hy vọng cung cấp những thông tim quan trọng, để chúng ta có thể trang bị cho các cơ sở y tế có thêm một thiết bị ngăn ngừa đột tử.
Do việc sử dụng ngày càng tăng WCD và sự không chắc chắn của các chỉ định thực hành của các chuyên gia sức khỏe tim mạch, tư vấn khoa học này đã được Hội Tim Mạch Hoa Kỳ (AHA) chuẩn bị. Trong thông báo này, người ta mô tả WCD trong bối cảnh công nghệ độc đáo, thích hợp lâm sàng và liệu pháp lựa chọn. Người ta xem xét các tài liệu có sẵn để hỗ trợ hiệu quả và tính an toàn của WCDs và khám phá những dấu hiệu cho thấy có thể cho sử dụng công nghệ này. Cuối cùng, trên cơ sở phân tích và chờ đợi các nghiên cứu xác định, người ta cung cấp hướng dẫn tương đối cho việc sử dụng WCD trong thực hành lâm sàng theo phương pháp Hiệp hội Tim mạch Hoa Kỳ phân loại sự nhất trí về sự chắc chắn của chúng và mức độ (chất lượng) của bằng chứng có sẵn (Bảng 1). Bảng 1 cung cấp tóm tắt các khái niệm chính được trình bày trong tư vấn khoa học này.
Do có một số lượng ít ỏi các dữ liệu tiền cứu hỗ trợ việc sử dụng của WCD, đặc biệt không có bất kỳ các thử nghiệm lâm sàng ngẫu nhiên xuất bản, các đề nghị trong tư vấn này không nhằm đề ra qui tắc hoặc đề nghị một phương pháp tiếp cận dựa trên bằng chứng cho việc điều chỉnh bệnh nhân có dấu hiệu được FDA chấp thuận cho sử dụng. Thay vào đó, đây là các khuyến cáo được cung cấp để cung cấp hướng các nhà lâm sàng khi thảo luận về liệu pháp này với bệnh nhân. Đó là ý kiến của các tác giả, quyết định cuối cùng về việc sử dụng của WCD nên dựa vào việc ra quyết định chia sẻ, trong đó sẽ bao gồm một cuộc thảo luận thẳng thắn nguy cơ lợi ích giữa các thày thuốc và bệnh nhân thừa nhận sự không chắc chắn xung quanh hiệu quả và tính an toàn của WCD.
Dịch tễ học và ngăn ngừa đột tử tim
Một phần ba (1/3) ngừng tim ngoài bệnh viện do nhịp nhanh thất (VT) hoặc rung thất (VF).[1] Mặc dù hiệu quả của khử rung tim nhanh, hầu hết bệnh nhân có ngừng tim do VT/VF đã không nhận được khử rung kịp thời. Mặc dù kết quả rất khác nhau giữa các cộng đồng ở Bắc Mỹ, theo tính toàn, sống sót từ ngừng tim do VT / VF tính trung bình và trong đó chức năng thất trái suy đáng kể.[10] Nhóm cuối cùng bao gồm những bệnh nhân có bệnh tim thiếu máu cục bộ hoặc không do thiếu máu cục bộ và phân suất tống máu tâm thất trái giảm một cách không hồi phục (LVEF) ≤0.35 kết hợp với suy tim NYHA class II đến III, mặc dù điều trị nội khoa theo hướng dẫn kéo dài hoặc MI trước đó có EF ≤ 0.30 không có suy tim nặng (NYHA chức năng class IV ) và những người MI> 40 ngày.[3-5] Những chỉ định này được FDA chấp thuận dựa trên sự ủng hộ bằng các thử nghiệm quan trọng được khẳng định một lợi ích sống còn của ICD ở các quần thể này.[3,4] Các phân tích gộp các nghiên cứu lớn cho thấy giảm nguy cơ tương đối cơ bản giữa 20% và 30% .[11,12] Mặc dù các chỉ dẫn cho đặt ICD được chấp nhận rộng rãi, điều chỉnh tối ưu của những bệnh nhân được coi là có nguy cơ cao trong thời gian chờ đợi (trước khi cấy ICD chắc chắn có lợi) vẫn còn bàn cãi.[13,14] Giai đoạn chờ đợi này được xem xét là 90 ngày sau chẩn đoán, trong khi điều trị nội khoa theo hướng dẫn được thực hiện và tối ưu.
Bảng 1.Các khái niệm mấu chốt
|
SCD vẫn là một nguyên nhân quan trọng và có thể ngăn ngừa nguyên nhân tử vong |
|
Mặc dù có lợi ích rõ ràng của chúng, công nghệ máy khử rung tim hiện nay có những hạn chế và rủi ro |
|
Chống chỉ tạm thời đối với điều trị cấy thiết bị thường phát sinh trong thực hành lâm sàng. |
|
WCDs có thể đáp ứng như là một phương pháp tạm thời ngăn ngừa tử vong loạn nhịp mà không cần người bên ngoài phản ứng với ngừng tim. |
|
WCDs sử dụng phân tích vector các tín hiệu điện tâm đồ bề mặt để phát hiện rối loạn nhịp thất đe dọa tính mạng. |
|
Tuân thủ của bệnh nhân là một phần không thể thiếu trong điều trị thành công WCD |
|
Các dữ liệu quan sát cho WCD có thể nhận biết và cắt cơn loạn nhịp thất thành công. |
|
WCD sử dụng là hợp lý khi có một chỉ định rõ ràng cho ICD trong sự hiện diện của một chống chỉ tạm thời ICD. |
|
WCD sử dụng có thể thích hợp trong hoàn cảnh lâm sàng liên quan với tăng nguy cơ loạn nhịp tạm thời. |
|
Tư vấn nguy cơ và thảo luận về sở thích bệnh nhân là bộ phận không tách rời của chăm sóc bệnh nhân và điều trị WCD. |
ICD chỉ máy khử rung tim cấy vào cơ thể; SCD chỉ đột tử tim, WCD chỉ máy khử rung tim mặc.
Đi đầu trong các cuộc tranh luận là những thành tích của phòng ngừa đột tử ở những bệnh nhân có nguy cơ cao trong giai đoạn đầu phục hồi từ nhồi máu cơ tim cấp (AMI) hoặc với một bệnh cơ tim không do thiếu máu cục bộ mới được chẩn đoán. Các lý do để trì hoãn đặt ICD trong những trường hợp này là một phần đáng kể của bệnh nhân sẽ trải qua sự phục hồi cơ tim và cải thiện chức năng thất trái đáng kể. Ngoài ra, nhiều bệnh nhân trải qua cải thiện sau khi thực hiện các điều trị nội tối ưu hoặc điều trị can thiệp liệu pháp y tế tối ưu hoặc liệu pháp can thiệp, như vậy sự cần thiết dự phòng ICD được ngăn lại. Ví dụ, phục hồi một phần hoặc toàn bộ LVEF đã được quan sát thấy trong hơn một nửa (1/2) số bệnh nhân trong 3 tháng từ khi AMI, khi bắt đầu các điều trị nội theo hướng dẫn với β blockers và kháng hệ thống renin angiotensin aldosterone trong giai đoạn sớm sau chẩn đoán bệnh cơ tim không do thiếu máu có thể tạo ra chức năng thất được cải thiện và nguy cơ SCD tiếp theo giảm đi; 50% bệnh nhân mới được chẩn đoán bệnh cơ tim không do thiếu máu sẽ được chứng minh cải thiện 10% trong LVEF với khởi đầu điều trị nội khoa. [21,22]
Mặc dù lý luận phân tích và lý do để trì hoãn cấy ICD cấy là hợp lý, các cơ sở bằng chứng hiện nay là chưa đầy đủ. Ví dụ, đột tử tim trong Nghiên cứu Suy Tim (SCD-HeFT) đã loại trừ các bệnh nhân với chẩn đoán bệnh cơ tim <3 tháng và những người đã không nhận được điều trị nội khoa theo hướng dẫn. Không có thử nghiệm ngẫu nhiên có sẵn so sánh cấy ICD sớm (có nghĩa, trong vòng 3 tháng) với thuốc điều trị chuẩn trong bệnh cơ tim không do thiếu máu. Hơn nữa, mặc dù các thử nghiệm lâm sàng cấy ICD sớm sau khi MI đã cho thấy không có lợi ích, những thử nghiệm đã tuyển các bệnh nhân lựa chọn rất kỹ, những người thường xuyên có các yếu tố nguy cơ bổ sung để tăng tỷ lệ tử vong do mọi nguyên nhân. Ví dụ, Nghiên cứu Phân tầng Nguy cơ Cải thiện Sống sót ngay bắt buộc LVEF ≤ 40% và tần số tim lúc nghỉ ngơi > 90 bpm hoặc VT tạm thời > 150 bpm trên theo dõi Holter. 62.944 bệnh nhân sau MI không được lựa chọn được tầm soát IRIS để ghi danh 898 (1,4% tổng số được tầm soát). Như vậy, khả năng khái quát những kết quả thử nghiệm trong câu hỏi.
Một mối quan tâm thường được nhắc đến về các tiêu chuẩn ICD hiện nay là nguy cơ của VT/VF nguy hiểm trong thời gian chờ đợi. Nghiên cứu Valsartan trong nhồi máu cơ tim cấp (Valsartan in Acute Myocardial Infarction Trial: VALIANT) cho thấy: trong số các bệnh nhân có EF ≤ 0,30 sau MI được theo dõi thời gian trung bình 24,7 tháng, 21% đột tử hoặc biến cố ngừng tim được cứu sống xuất hiện trong phạm vi 30 ngày đầu tiên sau khi AMI.[23] Mặc dù kết quả khám nghiệm tử thi đã chứng minh nhiều người trong số đột tử không do loạn nhịp thực sự, một phần đáng kể (51%) do loạn nhịp.[24] Đáng chú ý, phần lớn các bệnh nhân đột tử hoặc được cứu sống trong VALIANT trong vòng 1 tháng AMI cũng đã được đánh giá trong tình trạng lâm sàng ổn định khi xuất viện.
Nghiên cứu các Máy khử rung trong đánh giá điều trị bệnh cơ tim không do thiếu máu cục bộ (Defibrillators in Non-Ischemic Cardiomyopathy Treatment Evaluation: DEFINITE), [25] phân tích phân nhóm những người có chẩn đoán bệnh cơ tim mới, tỷ lệ tử vong thấp hơn 48% người nhận ICD ngẫu nhiên trong vòng 9 tháng khởi đầu chẩn đoán (9,2% so với 17,7 %; P = 0,058) [26]. Tóm lại, những phát hiện cho thấy lợi ích từ ICD phòng ngừa ban đầu không phụ thuộc thời gian hoặc trong bệnh cơ tim không do thiếu máu hoặc sau AMI và nguy cơ có thể so sánh với rối loạn nhịp đe dọa sự sống có thể tồn tại cho những bệnh nhân này ở hầu như tất cả các cửa sổ thời gian sau sự kiện ghi nhân của họ hoặc chẩn đoán. Phải thừa nhận, hầu hết các thử nghiệm điều trị ICD dự phòng tiên phát so với điều trị nội khoa theo hướng dẫn chứng minh lợi ích sống sót không thực được nhận thấy cho đến khi ≈ 1 năm sau khi cấy, làm cho khó khăn hơn để xác định ảnh hưởng của việc điều trị được giới hạn trong khoảng thời gian sớm hơn và ngắn hơn. [3,4]
Mặc dù cấy ICD sớm đưa đến giảm SCD, lợi ích sống còn tổng thể từ đặt ICD sớm sau MI hoặc bệnh cơ tim mới được chẩn đoán đã không được chứng minh. Ví dụ, những gợi ý trong DEFINITE sống sót được cải thiện ở những người nhận được ICD có bệnh cơ tim mới được chẩn đoán là hồi cứu và không kết luận có ý nghĩa thống kê. Trong Nghiên cứu Bệnh cơ tim (Cardiomyopathy Trial: CAT), bệnh nhân mới được chẩn đoán bệnh cơ tim giãn (LVEF < 0,30) được ghi nhận không có lợi ích có thể đo lường từ ICD.[27]. Các máy khử rung tim và nhồi máu cơ tim cấp tính (Defibrillator and Acute Myocardial Infarction: Dinamit) và nghiên cứu IRIS bệnh nhân hồi cứu ngẫu nhiên với chức năng thất suy yếu đáng kể (EF <0,35 và <0,40, tương ứng), cùng với các yếu tố nguy cơ khác, để nhận được ICD ngay (có nghĩa là, 18 và 13 ngày, tương ứng) sau AMI.[28,29] Trong cả hai thử nghiệm, tỷ lệ SD thấp hơn ở phương diện ICD đã song hành với tăng đồng thời tỷ lệ tử vong không do loạn nhịp, như vậy tử suất toàn bộ cuối cùng đã không khác nhau ở các nhóm điều trị ICD và điều trị thuốc. Cùng với nhau, những phát hiện này không hỗ trợ một lợi ích sống còn từ cấy sớm/đặt máy khử rung tim vĩnh viễn cho phòng ngừa tiên phát trong trường hợp bệnh nhân có nguy cơ cao.
Kỹ thuật Khử rung và Hạn chế
Thời gian để khử rung tim là rất quan trọng trong hồi sức ngừng tuần hoàn do VT/VF.[30] Các khả năng sống sót trong ngừng tuần hoàn do VT/VF giảm từ 7% đến 10% cho mỗi phút khử rung tim bị trì hoãn không cần hồi sức tim phổi và 3%/phút đến 4%/ phút với hồi sức tim phổi. Sự phát triển của khử rung tự động ngoài (AED) đã có tầm quan trọng để cải thiện sự sống còn trong trường hợp ngừng tuần hoàn do chính VT/VF.[31] AED dễ dàng thực hiện ngắn chặn sự cần thiết chờ đợi để kích hoạt các hệ thống ứng phó khẩn cấp y tế và sự xuất hiện của nhân viên hồi sức tăng cường với khử rung xách tay. Khả năng của AED cho phép khử rung tim sớm hơn do nhân viện phản ứng y tế chuyên biệt hoặc do người tại chỗ nếu AED được định khu một cách chiến lược gần hiện trường ngừng tim (những gì đã trở nên biết rõ như khử rung được thực hiện công cộng).[32] Máy khử rung tim ngoài có hiệu quả cao trong điều trị ngừng tim do nhịp nhanh thất.[33] Tuy nhiên, hiệu quả tổng thể của chúng trong việc cải thiện sống sót sau ngừng tim phụ thuộc vào thời gian cần thiết để triển khai chúng ở hiện trường do các nhà cung cấp dịch vụ chăm sóc khẩn cấp hoặc sự sẵn có của AED và sự hiện diện của người ngoài sẵn sàng và có khả năng sử dụng điều trị khi cần thiết. Một thử nghiệm lâm sàng ngẫu nhiên của AED sử dụng tại nhà sau AMI đã thất bại trong việc xác định lợi ích sống còn.[34]
Ở tương đối nhỏbệnh nhân nhưng quan trọng, ở họ nguy cơ ngừng tim tăng lên có thể dự báo trên cơ sở các yếu tố nguy cơ lâm sàng, cấy máy khử rung dự phòng cung cấp các lợi thế riêng biệt. ICD liên tục theo dõi nhịp của bệnh nhân, mang đến lợi ích chậm trễ tối thiểu giữa sự khởi đầu của nhịp nhanh có khả năng gây tử vong và điều trị được thực hiện một cách tự động. Về hạn chế của chúng, ICD đồi hỏi can thiệp ngoại khoa, gồm tìm mạch máu và duy trì lâu dài máy. Tỷ lệ biến cố bất lợi liên quan đến phạm vi cấy máy từ 1,3% đến 11,0%, gồm chảy máu, tụt điện cực, tràn khí màng phổi, thủng tim, nhiễm trùng cấp tính và tử vong (0,4% -1,2%). [35] ICD cũng có tiềm năng bệnh suất dài hạn do suy yếu một số thành phần, rối loạn điện cực, sốc không phù hợp, tắc mạch và nhiễm trùng. Tuổi thọ điện cực (lead longevity) ≈ 85% từ 5 đến 10 năm sau khi cấy, lấy bỏ thường đòi hỏi rút điện cực đúng kỹ thuật với những nguy cơ đi kèm. [36-38] Các ICD dưới da được FDA được phê duyệt làm giẩm đi một số, nhưng không phải tất cả những mối lo tiềm tàng. [39] Mặc dù chức năng tương tự như một ICD truyền thống, hệ thống máy khử rung tim dưới da thiếu các điện cực trong tim do đó tránh được sự cần thiết phải đi vào mạch máu và các biến chứng tiềm ẩn dài hạn từ các phần cứng trong lòng mạch. Tuy nhiên, các ICD dưới da đưa đến nhiều mối nguy hiểm tương tự như ICD qua tĩnh mạch, bao gồm di lệch điện cực (2,5%), xói mòn da (1,7%), và nhiễm trùng (5,9%), cùng với một tỷ lệ 13% các sốc không phù hợp trong thời gian theo dõi . [40] Mặc dù ICD dưới da đã được chứng minh là có hiệu quả cắt các cơn VF, hiệu quả của các ICD dưới da so với các ICD qua tĩnh mạch trong việc cải thiện sự sống còn từ VF tự phát vẫn chưa được xác lập. [41]
Máy khử rung tim ngoài và ICD cung cấp liệu pháp cứu sinh tiềm năng cho nhịp tim nhanh ác tính. Xác định có đúng hay không và khi nào để triển khai phương pháp điều trị như vậy ở những bệnh nhân có nguy cơ cao đòi hỏi phải tạo thế cân bằng quan trọng giữa các bằng chứng sẵn có, sở thích của bệnh nhân, và theo ý kiếm của bác sĩ.
Xem xét kỹ thuật nhận cảm và khử rung của áo khử rung tim(WCD)
WCD có một số cơ chế nhận cảm và phóng năng lượng độc đáo phân biệt nó với hình thái khử rung khác. Các thiết bị WCD bao gồm 2 thành phần chính, một áo mặc và một khử rung theo dõi năng lượng pin. Áo có kích cỡ phù hợp với vòng ngực của bệnh nhân. Các hàng may mặc có kích thước chu vi lồng ngực và cân nặng của bệnh nhân và được sát dưới áo dưới làn da. Áo có chứa cả hai nhận cảm và điện cực khử rung. Một hệ thống 4 điện cực, 2 dây dẫn, nằm trong vành đai của áo, được sử dụng để ghi ECG bề mặt cho phân tích hình thái học và phát hiện các rối loạn nhịp tim. Các monitor thường được đeo trên thắt lưng hoặc dây đeo vai. Thiết bị WCD sử dụng tương tự và các bộ lọc kỹ thuật số, cũng như một số thuật toán để nhận ra nhiễu điện từ và các nguồn tiếng ồn khác. Các thuật toán phát hiện được sử dụng bằng các biểu hiện WCD độ nhạy 90% đến 100% và độ đặc hiệu là 98% đến 99% .[42,43] Tần số sốc không phù hợp trong nghiên cứu ban đầu đã ≈1% đến 2% .[43,44] Thiết bị WCD có thể lập trình, với tỷ lệ phát hiện cả khu vực VT và VF. (Hình 1 và 2)
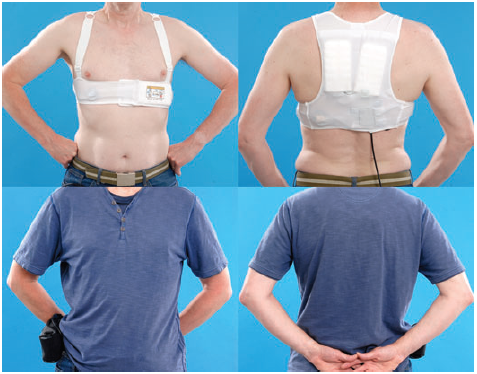
Hình 1.Áo khử rung và các chi tiết.
Khi WCD phát hiện rối loạn nhịp có khả năng, một thuật toán phát hiện và điều trị được bắt đầu. Quá trình kết hợp tương tác của bệnh nhân. Khi rối loạn nhịp đã đáp ứng các tiêu chí hình thái và tốc độ, phát hiện chính thức xảy ra, các thiết bị khởi tạo test phản ứng của bệnh nhân. Test này kết hợp rung, âm thanh và cảnh báo thị giác. Nếu bệnh nhân nhấn một nút phản ứng, các tập tin bị hủy bỏ. Nếu không có bệnh nhân đáp ứng được ghi lại, các điện cực khử rung xả gel lên da và cuối cùng là cung cấp một cú sốc qua một vector từ mỏm ra sau. Tùy thuộc vào loại rối loạn nhịp tim (VT hay VF) và lập trình thiết bị, thời gian phản ứng tổng thể (phát hiện gây sốc) có thể mất từ 25 đến 60s.[45] Năng lượng sốc WCD dao động giữa 75 và 150 J hai pha, tỷ lệ hiệu quảsốc giữa 69% và 99% đã được báo cáo. [42,46-48] Thiết bị WCD có khả năng cung cấp lên đến 5 cú sốc. Tuy nhiên, khi các thiết bị đã được xử lý một cơn rối loạn nhịp tim, áo và điện cực phải được thay thế. Mặc dù phần lớn các dữ liệu quan sát được từ người lớn, hàng loạt nhỏ đã báo cáo sử dụng WCD ở quần trẻ em, gồm bệnh nhân 9-17 tuổi. [49,50] Một thách thức quan trọng trong việc sử dụng trẻ em để phù hợp cho phần thân nhỏ hơn của trẻ em và thanh thiếu niên.

Hình 2.Hệ thống áo khử rung cho thấy thiết bị, áo,và monitor từ xa. Mũi tên (trên bên trái) chỉ bệnh nhân đáp ứng nút với nút thứ hai trên phía đối diện của thiết bị.
FDA chấp thuận sử dụng WCD ở những bệnh nhân được lựa chọn có nguy cơ ngừng tim đột ngột. Tuy nhiên, có một số chống chỉ định tương đối quan trọng. Bệnh nhân có tạo nhịp đơn cực (tâm nhĩ hoặc tâm thất) không thể sử dụng WCD vì các kích thích tạo nhịp biên độ lớn có thể cản trở phát hiện rối loạn nhịp tim. [51] Ngoài ra, bệnh nhân không thể phát hiện hoặc phản ứng với các kích thích thử nghiệm phản ứng cũng không phải ứng cử viên thích hợp cho WCD.
Ngoài những chống chỉ định điều trị WCD, cũng có một số hạn chế quan trọng. Một lần nữa, điều quan trọng cần lưu ý WCD không có khả năng tạo nhịp. bệnh nhân thoải mái vẫn còn là một thách thức với liệu pháp WCD, đặc biệt trong khoảng thời gian dài. Các đặc tính thêm vào bệnh nhân làm cho WCD ít lý tưởng hơn, gồm bề ngoài cơ thể quá cỡ (như, béo phì) và vết thương ngực hở hoặc đang lành. Với việc sử dụng các cú sốc bên ngoài, bệnh nhân cũng có thể gặp các tác dụng phụ, gồm nhưng không giới hạn chất lượng sống bị giảm sút thứ phát do đau và thậm chí bỏng da. Cuối cùng, ở thời điểm này, không có thử nghiệm ngẫu nhiên hoàn thành điều trị WCD. Vì vậy, không có dữ liệu dứt khoát có sẵn trên hiệu quả so sánh so với điều trị thay thế (hoặc không có).
Tuân thủ của bệnh nhân
Làm cho đúng là một thành phần quan trọng của hiệu quả điều trị WCD. Bệnh nhân được hướng dẫn để mang thiết bị ở tất cả các thời gian trừ khi tắm vòi sen hoặc tắm bồn. Tỉ lệ ngưng điều trị cao 22% đã được báo cáo, kết quả chủ yếu bệnh nhân thoải mái và liên quan đến thói quen sống.[46] Trong loạt quan sát lớn nhất cho đến nay, sử dụng hàng ngày> 90% trong hơn một nửa của nhóm, tỷ lệ bỏ thiết bị14 % .[48] Một số mối quan tâm đã được nêu lên về tần số tuân thủ trong các quần thể trẻ em. Tuy nhiên, dữ liệu còn hạn chế. Một nghiên cứu thuần tập 4 trẻ em bị bệnh cơ tim anthracycline gây ra thấy tuân thủ giới hạn trong một nửa bệnh nhân.[50] Thứ hai, nghiên cứu lớn cho thấy không có sự khác biệt trong việc tuân thủ giữa thanh niên (tuổi, 19-21 tuổi; n = 103) và những người ≤18 tuổi (n = 81); cả hai nhóm đã có một sự tuân thủ trung bình là 19 h / ngày (80% tuân thủ). [49]
Trải nghiệm lâm sàng với WCD
Một bản tóm tắt các nghiên cứu lâm sàng điều trị WCD có sẵn được thể hiện trong Bảng 2. Sau khi chứng minh hiệu quả sốc trong các tình huống đối chứng, [42] các đánh giá WCD về lâm sàng một cách hệ thống đầu tiên thể hiện so sánh Nghiên cứu khám phá Áo Khử rung (Wearable Defibrillator Investigative Trial: WEARIT) và Nghiên cứu Bắc cầu sang ICD ở các Bệnh nhân Nguy cơ Tử vong do Loạn nhịp (Bridge to ICD in Patients at Risk of Arrhythmic Death: BIROAD). [46] Nghiên cứu WEARIT ghi danh bệnh nhân suy tim có triệu chứng (NYHA III-IV) và LVEF <0,30 được coi có nguy cơ cao nhưng không đáp ứng yêu cầu hội đủ điều kiện cho một ICD. Tương tự như vậy, việc nghiên cứu BIROAD ghi danh bệnh nhân được coi có nguy cơ cao SD và trong vòng 4 tháng MI hoặc tái thông mạch máu phẫu thuật. Lý do cụ thể để xem xét WCD trong thuần tập BIROAD bao gồm nhưng không giới hạn đến loạn nhịp thất trong vòng 48 giờ bắc cầu động mạch vành tự thân (CABG), LVEF <0.30 sau khi CABG, ngất sau khi CABG và bệnh nhân từ chối ICD. Ở 2 nghiên cứu tiềm cứu này, trong đó ghi danh 289 bệnh nhân, 6 trong số 8 WCD nỗ lực khử rung (75%) đều thành công.
Bảng 2.Các nghiên cứu lâm sàng WCD*
|
Reference |
Patient Population |
Sample Size, n |
Adherence, h/d |
Duration of Therapy, d |
Appropriate Shock Rate, % |
Inappropriate Shock Rate, % |
Survival, % |
|
Epstein et al,52 2013 |
Patients 0–3 mo after AMI |
8453 |
21.8 (median) |
69±61 |
1.6 |
1.3 |
93 |
|
Mitrani et al,53 2013 |
Newly diagnosed cardiomyopathy or recent revascularization |
134 |
14±8 |
72±55 |
0 |
0 |
98 |
|
Zishiri et al,54 2013 |
Recent revascularization with left ventricular dysfunction |
809 |
NR |
79±69 (CABG) 81±183 (PCI) |
1.3 |
1.6 |
98 |
|
Kao et al,55 2012 |
HF patients listed for transplantation, with a new diagnosis, or receiving inotropes |
82 |
20±5 |
80±58 |
0 |
0 |
100 |
|
Saltzberg et al,56 2012 |
PeripartumNonischemic cardiomyopathy |
107 159 |
18±5 17±6 |
75±81 56±54 |
0 0.6 |
0 0 |
97 85 |
|
Rao et al,57 2011 |
Congenital structural heart disease Inherited arrhythmias |
43 119 |
19 (12–21) 19 (10–22) |
27 (10–55) 29 (7–68) |
0 2.5 |
0 5.9 |
87 97 |
|
Chung et al,48 2010 |
Aggregate US experience |
3569 |
20±5 |
53±70 |
1.7 |
1.9 |
99 |
|
Collins et al,49 2010 |
Age ≤18 y Age 19–21 y |
81 103 |
20 (1–24) 19 (1–24) |
29 (0–531) 35 (0–499) |
0 1.9
|
1.2 0.9 |
89 91 |
|
Klein et al,43 2010 |
Nationwide experience in Germany |
354 |
21 |
106 |
3.1 |
0.8 |
NR |
|
Feldman et al,46 2004 |
WEARIT/BIROAD clinical studies (HF patients or bridge to ICD for other indications) |
289 |
NR |
93 |
1.0 |
2.1 |
96 |
Tần số sốc được cho là tỷ lệ phần trăm (n bệnh nhân với bệnh nhân sốc / n WCD). AMI: nhồi máu cơ tim cấp tính; BIROAD: Cầu nối ICD ở Bệnh nhân có Nguy cơ Tử vong Loạn nhịp ; CABG: bắc cấu động mạch vành tự thân; HF: suy tim; ICD: máy khử dung tim có thể cấy; NR: không liên quan (thích hợp); PCI, can thiệp mạch vành qua da; WCD: áo khử rung tim; WEARIT: Nghiên cứu khám phá Áo Khử rung tim. * Dựa trên tìm kiếm trên Medline 01 tháng 7 năm 2013, được cập nhật vào ngày 2 tháng 12 năm 2013. Các nghiên cứu với ≥50 đối tượng được thu nhận.
Có 12 trường hợp tử vong, một nửa trong số đó đột ngột và xảy ra ở những bệnh nhân không mặc WCD theo hướng dẫn. Khoảng 1/4 dân số nghiên cứu (n = 68 289) không tiếp tục nghiên cứu do kết quả các khó chịu liên quan đến thiết bị hoặc các phản ứng bất lợi. Những nghiên cứu này đầu tiên chứng minh tính khả thi của WCD ở những bệnh nhân có nguy cơ cao cho SCD. Hơn nữa, chúng đã chứng minh hiệu quả hợp lý ở những bệnh nhân tuân thủ mang thiết bị.
Trên cơ sở dữ liệu từ một đăng ký sản xuất tại Hoa Kỳ từ năm 2002 đến năm 2006, tổng cộng 3569 bệnh nhân mang WCD cho ít nhất 1 ngày (có nghĩa là thời gian, 53 ± 70 ngày).48 WCD ngừng vì khó chịu hay có hại các phản ứng xảy ra ở 14%. Thời gian còn sử dụng được liên quan đến tỉ lệ tuân thủ. Chỉ định sử dụng WCD bao gồm không thể cấy ICD (23%), rối loạn nhịp thất trước khi lên kế hoạch cấy ICD (16%), MI mới xẩy ra (16%), trạng thái sau khi CABG (9%) và bệnh cơ tim mới chẩn đoán gần với LVEF ≤0.35 ( 28%). Trong tổng số 143.643 bệnh nhân / năm, đã có 80 biến cố VT dai dẳng / VF ở 59 bệnh nhân (1,7% / bệnh nhân / năm). Hầu hết các VT dai dẳng / VF xảy ra ở những bệnh nhân với một thiết bị đặt ngoài (tỉ lệ biến cố, 5,2%). Hiệu quả sốc đầu tiên 99% (n = 79 80), và sống sót sau VT / VF 90% (n = 72 80). Phù hợp với các nghiên cứu khác về các biến cố đột tử, [58], một số lượng đáng kể các ngừng tim đột ngột do các biến cố không phải VT / VF (25%), trong đó có 23 biến cố vô tâm thu.
So với đoàn hệ bệnh nhân nhận được ICD trung tâm đơn thuần (1996-2004) cho những chỉ định truyền thống, sự sống còn tương tự ở nhóm WCD (tỷ lệ tử vong 3,6% so với 4,4% trong 3 tháng; P = 0,256) .[48] Tuy nhiên, so sánh tần số biến cố giữa các đoàn hệ WCD và ICD này khó khăn do số liệu về nhân khẩu học và lâm sàng bị hạn chế. Nhìn chung, 2% bệnh nhân WCD đã nhận được một cú sốc không phù hợp (tỷ lệ 1,4% / tháng), nó tương đương với tần số sốc thích hợp (Bảng 2). Lý do những cú sốc WCD không phù hợp bao gồm nhiễu tín hiệu (68%), nhịp tim nhanh trên thất (27%), VT tạm thời (6%), nhận cảm quá mức (oversensing) những tín hiệu tim bình thường (4%), mất tín hiệu ECG (4%), và thất bại kích hoạt nút đáp ứng. Các dữ liệu khác cho thấy tỷ lệ sốc không thích hợp ở những bệnh nhân được điều trị với WCD có thể đạt 1,9% đến 5,9% trong vòng 2-3 tháng. [46,48,57] Ngược lại, tần số sốc ICD đã được chứng minh 13% qua 41 tháng . [59]
Ngoài những kinh nghiệm quốc gia tổng thể đã xuất bản, [48] một số nghiên cứu quan sát ở nhóm bệnh nhân được lựa chọn và các trung tâm đơn thuần đã được báo cáo. Trong cơ sở dữ liệu của nhà sản xuất WCD sử dụng ở 8453 bệnh nhân trong vòng 90 ngày MI (trung bình thời gian từ AMI để WCD, 16 ngày, 62% bệnh nhân đã được tái tuần hoàn; 77% với LVEF ≤0.30), 1,6% bệnh nhân nhận được những cú sốc thích hợp. [52]
WCD đã được sử dụng như một cầu nối cho đến khi hoặc phục hồi cơ tim hoặc ICD được cấy ở những bệnh nhân có bệnh cơ tim mới được chẩn đoán, bệnh nhân suy tim chức năng NYHA class IV và những người được liệt kê cho ghép tim. Trong một đăng ký WCD tiền cứu đa trung tâm 89 bệnh nhân có bệnh cơ tim giãn vô căn, 42% phục hồi cơ tim qua trải nghiệm và đã không phát triển chỉ định cho ICD vĩnh viễn.[55] Hơn nữa, không ai trong số các bệnh nhân có SCD hoặc đòi hỏi điều trị WCD. Tần số biến cố xuất hiện thấp hơn ở những bệnh nhân bệnh cơ tim mới được chẩn đoán (<1%) so với những bệnh nhân đáp ứng chỉ định ICD theo hướng dẫn hiện hành. [48,53] Tần số biến cố cũng thấp hơn ở các bệnh nhân vừa mới tái tuần hoàn, mặc dù dường như có sự thay đổi lớn hơn trong các tần số biến cố trong các nghiên cứu WCD (0% -1,6%; Bảng 2). Mặc dù tỷ lệ biến cố tổng thể thấp hơn ở những bệnh nhân có bệnh cơ tim mới được chẩn đoán hoặc mới tái thông mạch máu vành, dữ liệu quan sát hồi cứu cho thấy các WCD có thể mang lại lợi ích sống còn. Trong một so sánh 4149 bệnh nhân tái tuần hoàn gần đây và LVEF ≤0.35 người không nhận được ICD khi xuất viện với 809 bệnh nhân nhận WCD lúc xuất viện, sự tồn tại xu hướng điều chỉnh lớn hơn ở những người điều trị với WCD sau khi CABG (7% so với 3%; điều chỉnh tỷ lệ nguy hiểm, 0,42; CI 95%, 0,31-0,55) hoặc can thiệp mạch vành qua da (PCI, 10% so với 2%; tỷ lệ nguy cơ điều chỉnh (adjusted hazard ratio), 0,33; CI 95%, 0,21-0,52). Tuy nhiên, phù hợp với dữ liệu trước đây, chỉ có 1,3% số người được điều trị bằng WCD được điều trị thích hợp cho điều trị VT / VF.[54] WCD cũng có thể là một lựa chọn điều trị hợp lý ở bệnh nhi thích hợp có nguy cơ cao SCD. [44,50]
Mặc dù có một loạt sự tích lũy các dữ liệu quan sát sử dụng WCD trong thực hành lâm sàng, các câu hỏi về hiệu quả thiết bị cuối cùng sẽ yêu cầu nghiên cứu ngẫu nhiên. Nghiên cứu và Đăng ký Ngăn ngừa Đột tử Sớm Vest (Vest Prevention of Early Sudden Death Trial: VEST) [60] (NCT01446965) hiện đang đánh giá việc sử dụng của WCD sau MI. Nghiên cứu ngẫu nhiên bệnh nhân trong vòng 7 ngày kể từ ngày MI, người có LVEF ≤0.35. Nghiên cứu sẽ kiểm tra giả thuyết WCD sử dụng cải thiện sự sống còn 12 tháng sau khi MI.
Các chỉ định có khả năng cho điều trị WCD
Với sự thừa nhận WCD có thể được ủng hộ trong một loạt các tình huống lâm sàng, các khuyến nghị sau đây có nguồn gốc từ những kinh nghiệm tích lũy lâm sàng, dữ liệu quan sát có sẵn và bằng chứng tiền cứu. Các khuyến nghị được tổng hợp và tóm tắt trong Bảng 3.
Bảng 3.Các chỉ định và các khuyến cáo cho điều trị WCD
|
Chỉ định |
Class |
Mức độ bằng chứng |
|
Sử dụng WCDs là hợp lý khi có một dấu hiệu rõ ràng cho cấy / thiết bị vĩnh viễn kèm theo một chống chỉ định tạm thời hoặc gián đoạn trong việc chăm sóc ICD như nhiễm trùng.46,48 |
IIa |
C |
|
Sử dụng WCDs là hợp lý như một cầu nối để điều trị xác định hơn như ghép tim.46,55,61 |
IIa |
C |
|
Sử dụng WCDs có thể là hợp lý khi có lo ngại về một nguy cơ cao SCD có thể giải quyết theo thời gian hoặc với điều trị rối loạn chức năng thất trái; ví dụ, trong bệnh tim thiếu máu cục bộ vừa mới tái thông mạch máu, mới được chẩn đoán bệnh cơ tim giãn không do thiếu máu ở bệnh nhân bắt đầu điều trị nội theo hướng dẫn, hoặc bệnh cơ tim thứ phát (nhịp tim nhanh qua trung gian, tuyến giáp qua trung gian, vv), trong đó có khả năng điều trị nguyên nhân cơ bản.53,54,56 |
IIb |
C |
|
WCDs có thể thích hợp như điều trị bắc cầu trong các tình huống liên quan với tăng nguy cơ tử vong, trong đó ICD đã được chứng minh để giảm SCD nhưng không phải sống sót tổng thể chẳng hạn như trong vòng 40 ngày của MI.48,52 |
IIb |
C |
|
WCDs không nên được sử dụng khi nguy cơ không phải loạn nhịp được dự kiến sẽ chiếm ưu thế đáng kể hơn nguy cơ loạn nhịp, đặc biệt là ở những bệnh nhân không hy vọng sống sót > 6 tháng. |
III: No benefit |
C |
ICD: máy khử rung có thể cấy; MI: nhồi máu cơ tim, SCD: đột tử tim, WCD: áo khử rung tim.
Nhiễm trùng và việc lấy bỏ
Cấy ICD có thể bị biến chứng do nhiễm trùng ở ≈1% bệnh nhân và> 2% những người nhận được thay máy, [62] thường đòi hỏi lấy bỏ toàn bộ hệ thống để loại bỏ nhiễm trùng. Tùy thuộc vào thực tế của bác sĩ và bản chất của sự nhiễm trùng, hầu hết thời gian có sự chậm trễ giữa việc lấy ra và cấy hệ thống ICD mới. Nếu khoảng thời gian này ngắn hoặc bệnh nhân đòi hỏi phải chăm sóc nội trú vì lý do khác, theo dõi và tiếp cận để khử rung tim ngoài có thể thích hợp. Mặt khác, nếu chậm trễ kéo dài, các bác sĩ phải đối mặt với quyết định về việc liệu lưu bệnh nhân như bệnh nhân nội trú, để sốc điện bệnh nhân không có bảo vệ từ ICD, hoặc cung cấp WCD cho đến khi cấy ICD có thể được thực hiện một cách an toàn. Lợi ích tiềm năng và hiệu quả – chi phí của bắc cầu với WCD trong khoảng thời gian cấy lại ICD sau khi nhiễm trùng có thể cũng liên quan đến nguy cơ nền. Ví dụ, bệnh nhân với dụng cụ phòng ngừa thứ phát và người có ICD trước đó có thể có lợi ích nhiều hơn, trên cơ sở nguy cơ, hơn bệnh nhân có các thiết bị phòng ngưa tiên phát và chưa bao giờ được điều trị bằng ICD thích hợp.
Đôi khi, ICD được được lấy ra vì lý do khác hơn là nhiễm trùng (ví dụ, tắc tĩnh mạch). Trong những trường hợp này, cơ hội cấy lại ICD hoặc ICD dưới da nên có sẵn một cách cấp thời như vậy điều trị WCD hiếm khi cần thiết sau lấy bỏ.
Khuyến cáo
1. Sử dụng áo khử rung timlà hợp lý khi có một dấu hiệu rõ ràng cho một cấy / thiết bị vĩnh viễn đi kèm với một chống chỉ tạm thời hoặc gián đoạn trong việc chăm sóc ICD như nhiễm trùng (Class IIa; Cấp chứng cứ C) .[46,48]
Mặc dù thất bại của các thử nghiệm lâm sàng để chứng minh cải thiện sự sống còn với ICD cấy sớm sau MI, có một nguy cơ gia tăng SCD ngay 40 ngày sau khi AMI. Trong DINAMIT , [28] tỷ lệ nguy cơ tử vong loạn nhịp là 0,42 (P = 0,009) với trị liệu ICD, nhưng điều này đã được bù đắp bằng cách tăng tỷ lệ tử vong không do loạn nhịp. Kết quả tương tự đã được chứng minh trong các thử nghiệm IRIS. [29] WCD có thể có một vai trò như một cầu nối để phòng ngừa SCD trong 40 ngày đầu tiên sau nhồi máu cơ tim ở những bệnh nhân được xem là có nguy cơ tăng lên do tử vong loạn nhịp. Quần thể này là đối tượng quan trọng trong nghiên cứu VEST đã được nói ở trên, nghiên cứu lâm sàng ngẫu nhiên nên được giúp để làm rõ vai trò của WCD ở quần thể bệnh nhân này.
Khuyến cáo
1. WCD có thể là phù hợp như trị liệu bắc cầu trong các tình huống kết hợp với nguy cơ tử vong tăng lên trong đó ICDs đã cho thấy để giảm SCD nhưng sống sót toàn bộ như trong phạm vi 40 ngày MI (Class IIb; Level of Evidence C). 48.52
Sau CABG hoặc PCI
Bệnh nhân có LVEF ≤ 0.35 có tử suất cao hơn sau CABG so với những người có LVEF bảo tồn và họ tử vong trong giai đoạn sau phẫu thuật, một nửa bị SCD.[63] Mặt khác, lên đến 50% bệnh nhân sẽ chứng minh cải thiện đáng kể LVEF sau CABG.[64] Sống sót được cải thiện ở giai đoạn ngay sau CABG đã không được chứng minh với ICD.[65] Thậm chí còn có ít dữ liệu về cấy ICD sau khi PCI, nhưng các vấn đề về khả năng cải thiện trong LVEF là tương tự. Do đó, các Trung tâm Chăm sóc y khoa & Dịch vụ Cấp cứu y khoa Medicaid uỷ quyền giai đoạn chờ đợi 90 ngày cho đặt ICD phòng ngừa nguyên phát sau tái tuần hoàn với hoặc CABG hoặc PCI .[66] Tuy nhiên, bệnh nhân có nhiều yếu tố nguy cơ hoặc các đặc tính nguy cơ cao có thể cuối cùng đòi hỏi ICD sau 90 ngày. Trong thời kỳ nguy cơ SCD được suy đoán cho các cá thể này trong giai đoạn chờ đợi, WCD có thể cung cấp cầu nối dự phòng ở các bệnh nhân trong phạm vi 90 ngày kể từ ngày CABG hoặc PCI.[48,52,54]
Các bệnh nhân có đủ khả năng trước đó MI dai dẳng hoặc Trải qua Tái tuần hoàn (CABG hoặc PCI)
Một số bệnh nhân có thể đã đủ tiêu chuẩn cho cấy ICD phòng ngừa tiên phát nhưng đối với bất cứ lý do nào đó còn chưa nhận được ICD. Nếu những bệnh nhân này sau đó có MI dai dẳng hoặc trải qua tái thông mạch máu, không còn rõ ràng nguy cơ của họ có còn được xác định bằng các chỉ định trước đó hay không hoặc đã bị thay đổi do các biến cố tiếp theo. Một số nhà nghiên cứu biện hộ thời gian chờ đợi thích hợp (40 ngày sau khi MI hoặc 90 ngày sau khi CABG hoặc PCI) phải được cho phép trước khi cấy ICD ở bệnh nhân “đủ điều kiện trước đó.[67] Tuyến bố các chuyên gia đồng thuận của HRS /ACC/AHA về việc sử dụng các ICD ở những bệnh nhân không có hoặc không xuất hiện nhiều trong các thử nghiệm lâm sàng khẳng định những bệnh nhân trong vòng 90 ngày kể từ ngày tái thông mạch máu, người trước đó đã đủ điều kiện cho việc cấy ICD phòng ngừa tiên phát, những người trải qua tái tuần hoàn không thể dẫn đến cải tiến trong LVEF, không phải là người trong vòng 40 ngày sau khi MI, cấy ICD có thể hữu ích.[68] Ngoài ra, mang WCD cũng có thể thích hợp trong thời gian chờ đợi này ở những bệnh nhân trước đó đủ điều kiện cho ICD khi tái thông mạch máu đã không nhất thiết giải quyết được những nguy cơ trước đó. WCD có thể là một lựa chọn cầu nối hữu ích nếu có lý do để tin rằng sẽ có sự cải thiện với tái thông mạch máu như là kết quả của hoặc cơ tim ngủ đông của một trong hai chế độ ngủ đông cơ tim xa với hoại tử hoặc tái cấu trúc thất tiếp theo.
Bệnh cơ tim Giãn Không do thiếu máu mới được chẩn đoán
Trong tình huống bệnh cơ tim không do thiếu máu mới được chẩn đoán, lợi ích của ICD sớm sau chẩn đoán còn gây tranh cãi. Trong CAT, bệnh nhân mới được chẩn đoán bệnh cơ tim giãn không do thiếu máu và LVEF ≤0.30 đưa không có lợi từ cấy ICD.[27] Nhìn chung, nghiên cứu DEFINITE [25] đã thất bại chứng minh lợi ích được tính toán cho các bệnh nhân bệnh cơ tim giãn không do thiếu máu, suy tim NYHA class I đến III, LVEF ≤ 0.35 và các nghoại vị thất hoặc VT tạm thời; tuy nhiên, có một xu hướng giảm tỷ lệ tử vong với ICD (P = 0,08). SCD-HeFT[3] chứng minh giảm có ý nghĩa trong tử suất ở các bệnh nhân có NYHA class II hoặc II và LVEF ≤ 0.35 khi một ICD đã được cấy > 3 tháng kể từ chẩn đoán. Đáng chú ý, trong SCD-HeFT, tất cả các bệnh nhân được điều trị nội khoa với β-blockers và ACEI trước khi xác định LVEF và ngẫu nhiên. Tiềm năng cải thiện chức năng cơ tim với điều trị nội khoa được hướng dẫn nhắc nhở đòi hỏi do Các Trung tâm Chăm sóc y tế và Dịch vụ y khoa quyết định để cấy ICD cho chỉ định ngăn ngừa tiên phát ở thể loại này của các bệnh nhân được trì hoãn trong 3 tháng giữa các bệnh nhân tham gia đăng ký và 9 tháng đối với các bệnh nhân khác, sau khi xác định nhắc lại LVEF sau điều trị phù hợp.[66] Tuy nhiên, các hướng dẫn hiện thời nêu rõ khoảng thời gian cần thiết để xác định cải thiện LV chức năng với điều trị nội khoa theo hướng dẫn còn chưa chắc chắn [69] và tính toán thời gian cấy các ICD là quyết định đòi hỏi xem xét cần thận. Những bệnh nhân này với chẩn đoán gần đây của suy tim ở người triển vọng cải thiện chức năng tâm thất vẫn còn chưa biết đại diện cho quần thể xem xét điều trị WCD. Trong quần thể này, điều trị WCD có thể thích hợp ở những bệnh nhân có các dấu hiệu nguy cơ bổ sung cho tử vong loạn nhịp, gồm ngoại vị thất mức cao hoặc VT tạm thời.
Tiên lương Tim còn Không rõ
WCD lý tưởng cho các ứng dụng ngắn hạn hơn khi nguy cơ SCD đang thay đổi hoặc không chắc chắn hoặc tầm quan trọng của nguy cơ SCD không rõ ràng liên quan đến nguy cơ tử vong không do loạn nhịp hoặc tử suất toàn bộ. Ngoài các kịch bản phổ biến của bệnh nhân với rối loạn chức năng tâm thu thất trái sau MI hoặc bệnh cơ tim không do thiếu máu mới được chẩn đoán, có một số các tình huống lâm sàng khác, trong đó tiên lượng đặc biệt còn chưa rõ và do đó có thể dẫn đến việc xem xét cho điều trị WCD ở một số bệnh nhân. Bệnh cơ tim chu sinh là một ví dụ. Nghiên cứu đoàn hệ đã báo cáo tỷ lệ tử vong rất biến động trong khoảng từ 2% đến 56%, với một nửa trong số những biến cố xảy ra trong vòng 12 tuần sau đẻ. Phục hồi chức năng thất xảy ra trong 30% đến 50% bệnh nhân, thường trong vòng 6 tháng chẩn đoán.[70,71] Mặc dù nguy cơ tử vong này sớm, nguy cơ SCD không được mô tả rõ. Một nghiên cứu gần đây cho thấy SCD và loạn nhịp thất cần điều trị rất hiếm ở phụ nữ bị bệnh cơ tim chu sinh.[56] Viêm cơ tim, rối loạn chức năng cơ tim do catecholamine gây ra (bệnh cơ tim do stress hoặc bệnh cơ tim Takotsubo), bệnh cơ tim do qua trung gian nhịp tim nhanh, bệnh cơ tim qua trung gian tuyến giáp, bệnh cơ tim liên quan đến trastuzumab cung cấp các tình huống lâm sàng có khả năng tương tự, trong đó phục hồi tương đối có khả năng. Trong các tình huống khả năng cao cho tim phục hồi, vai trò của WCDs cuối cùng có thể được giới hạn cho những bệnh nhân đặc biệt có đặc tính có nguy cơ cao hoặc trong phòng ngừa thứ phát
Bệnh cơ tim có liên quan đến – lạm dụng các chất (như rượu, methamphetamine) cũng đặc biệt do những tiềm ẩn cho phục hồi thất với việc ngừng lạm dụng. WCDs cho công tác phòng chống SCD có thể hữu ích trong việc cung cấp thời gian để đánh giá sự tuân thủ các khuyến cáo về thuốc.[72]
Cũng có thể có sự không chắc chắn về tiên lượng ở giai đoạn cuối của suy tim. Các hướng dẫn được khuyến cáo chống lại cấy ICD vĩnh viễn ở những bệnh nhân không “hy vọng sống sót > 1 năm với tình trạng chức năng tốt.” [10] Tuy nhiên, cho dù bệnh nhân sẽ có tiên lượng kém như ở lại NYHA chức năng class IV với một sự sống còn ngắn hoặc sẽ ổn định vào NYHA chức năng class III với sự tồn tại lâu dài hợp lý có thể là khó khăn để xác định. Mặc dù tài liệu rộng lớn về tiên lượng suy tim với nhiều mô hình rủi ro suy tim xác nhận, khoảng tin cậy xung quanh tính toán trung bình cho sự sống còn thường khá rộng. Trong số những bệnh nhân mà mô hình nguy cơ dự đoán sống trung bình 1 năm, ≈25% sẽ chết trong vòng 6 tháng và 25% vẫn sẽ được sống ở 2 năm.[73] Trong một ví dụ khác về cách mô hình nguy cơ như vậy có thể phá vỡ trong ứng dụng thực tế , khi được sử dụng rộng rãi Mô hình Suy Tim Seattle được áp dụng cho một nhóm 138 bệnh nhân suy tim có triệu chứng NYHA III và IV, các mô hình xác định 6 bệnh nhân (4,3%) với tuổi thọ dự kiến ≤1 năm; tại 12 tháng theo dõi, 43 bệnh nhân (31%) đã chết.[74] Như vậy, việc áp dụng dự báo dân số tính toán cho từng bệnh nhân riêng biệt có thể có nhiều vấn đề, hướng dẫn trích dẫn điểm cắt khó khăn cho thực thi. Hơn nữa, hầu như không có mô hình bao gồm ước tính cho điểm cuối sống sót chẳng hạn chất lượng sống liên quan đến sức khỏe.[75] Vì vậy, trị liệu WCD có thể đặc biệt hữu ích ở những bệnh nhân tương đối không ổn định với suy tim nặng và có các đặc điểm nguy cơ cao cho SCD có thời gian thêm vào có thể làm rõ những hy vọng cho sống sót và chất lượng sống tiếp theo.
Khuyến cáo
1. Sử dụng WCDs có thể phù hợp khi có lo lắng về nguy cơ cao SCD có thể liên quan theo thời gian hoặc điều trị rối loạn chức năng thất trái, ví dụ, ở bệnh tim thiếu máu cục bộ với tái tuần hoàn mới thực hiện, bệnh cơ tim giãn không do thiếu máu mới được chẩn đoán ở các bệnh nhân đang bắt đầu điều trị nội khoa theo hướng dẫn, hoặc bệnh cơ tim thứ phát (qua trung gian nhịp nhanh, qua trung gian tuyến giáp…) nguyên nhân nền có khả năng được điều trị (Class IIb; Mức chứng cứ: C), 53,54,56
Mục đích khuyến cáo này không phải để gợi ý tất cả các bệnh nhân có bệnh cơ tim không do thiếu máu mới được chẩn đoán hoặc rối loạn chức năng thất trái đòi hỏi điều trị của WCD. Trong thực tế, sử dụng WCD kiểu tấm chăn theo cách này sẽ là không thích hợp và cũng không phù hợp với các bằng chứng lâm sàng có sẵn. Tuy nhiên, điều trị WCD ở một số bệnh nhân với các tính năng nguy cơ cao có thể hữu ích.
Tiên lượng không do tim không rõ
Các chỉ định cho cấy ICD thông thường có thể xảy ra trong bối cảnh các bệnh đi kèm không do tim có thể được chống chỉ định tương đối hoặc tạm thời cho cấy ICD. Một WCD có thể cho phép thêm thời gian để hiểu rõ hơn về mức độ nghiêm trọng và phục hồi các bệnh đi kèm như vậy. Một ví dụ tình huống SCD có chỉ định rõ rệt cho ngăn ngừa thứ phát với ICD nhưng trong tình huống đó biến cố xung quanh thời gian SCD đã gây ra các vần đề không phải tim cấp tính (như, các thiết lập của SCD với chỉ dẫn rõ ràng để phòng ngừa thứ cấp với một ICD nhưng trong đó các sự kiện xung quanh thời điểm SCD đã tạo ra các vấn đề không do tim cấp tính (ví dụ như, tổn thương não thiếu oxy hoặc tổn thương thận cấp tính) phục hồi còn chưa rõ. Một ví dụ thứ hai tình huống ICD phòng ngưa tiên phát, trong đó bệnh đang tác động qua lại nhau (ví dụ như ung thư) có thể thay đổi nguy cơ lợi ích hướng các quyết định về điều trị ICD. Do các lợi ích tuyệt đối của ngăn ngừa tiên phát của trị liệu ICD được nhìn nhận qua các năm, WCD có thể cho phép thời gian để đánh giá đáp ứng đối với hóa trị liệu ở bệnh nhân với các đặc tính nguy cơ cao tương đối cho SCD. Một tình huống khác trong đó WCD có thể thể hiện thay thế điều trị quan trọng cho lựa chọn các bệnh nhân nguy cơ giai đoạn cấp tính của sự phục hồi từ các thủ thuật xâm lấn hoặc ngoại khoa. Tuy nhiên, khi tiến triển còn không rõ với sự chắc chắn và các nguy cơ tử vong không do loạn nhịp vượt quá nhưng biến cố loạn nhịp nguy hiểm, WCD không có chỉ định.
Khuyến cáo
1. WCDs không nên được sử dụng khi nguy cơ không do loạn nhịp được dự kiến vượt hơn đáng kể nguy cơ loạn nhịp, đặc biệt ở những bệnh nhân không hy vọng sống sót> 6 tháng (Class III).
Các bệnh nhân Chờ Ghép tim và nhờ Hỗ trợ Tuần hoàn Cơ học
Các bệnh nhân đang chờ ghép tim nói chung có nguy cơ tử vong cao, bao gồm cả SCD, vì mức độ nghiêm trọng của bệnh tim của họ. Việc sử dụng inotropes để bắc cầu một số bệnh nhân chờ ghép tim có thể tăng thêm nguy cơ loạn nhịp thất ngắn hạn. Tuy nhiên, thời gian nguy cơ có thể được rút ngắn đáng kể bằng cách tìm được hiến tạng có thể chấp nhận được. Vì vậy, liệu pháp WCD có thể là một phương pháp hữu ích trong tình huống này. Thật không may, thời gian chờ đợi cho bệnh nhân được được lên danh sách cho cấy ghép có thể biến đổi nhiều và thường kéo dài, trong thời đại của hỗ trợ tuần hoàn cơ học, đã phát triển dần dần lâu hơn cho bệnh nhân không phải ở tình trạng 1A.[76,77] Vì vậy, trừ khi bệnh nhân được dự kiến sẽ vẫn trong tình trạng 1A hoặc đang ở tình trạng 1B trong một khu vực tìm tạng với thời gian chờ đợi tương đối ngắn (tức là <90 ngày), cấy ICD vĩnh viễn nhìn chung là phương pháp được lựa chọn, phù hợp với Hướng dẫn của các Hiệp hội Quốc tế Ghép Tim và Phổi cho chăm sóc các ứng viên ghép tim.[61] Một ICD vĩnh viễn cũng được ưa thích khi bệnh nhân đáp ứng các tiêu chí để điều trị tái đồng bộ tim.
Hỗ trợ Tuần hoàn Cơ học cũng có thể thay đổi năng động để xem xét lựa chọn điều trị cho SCD. Các nguy cơ của tổn thương huyết động do loạn nhịp thất biến đổi được làm giảm đi bằng dụng cụ hỗ trợ thất trái (left ventricular assist device: LVAD); cho bệnh nhân phụ thuộc vào chức năng thất phải, VT / VF có thể không được chịu đựng. Loạn nhịp thất cũng thường ở các bệnh nhân với LVAD. Do đó, cách tiếp cận chung đã được cặp đôi trị liệu LVAD với trị liệu ICD vĩnh viễn. Đối với những bệnh nhân bắc cầu LVAD ghép tim đã được lên danh sách ở trạng thái 1A và có nhóm máu thuận lợi và các kháng thể phản ứng thể hiện thấp (low panel). [77] Liệu pháp WCD có thể là một lựa chọn. Tuy nhiên, cho dù hiệu quả của WCDs trong trạng thái thiết bị LVAD được lựa chọn vẫn còn kém đặc trưng.
Khuyến cáo
1. Sử dụng WCDs là hợp lý như cầu nối để điều trị dứt khoát hơn chẳng hạn như ghép tim (Class IIa; Cấp chứng cứ C) .46.55.61
Cho phép thời gian cho việc ra quyết định của bệnh nhân
Mặc dù lợi ích sống còn rõ ràng về điều trị ICD trong quần thể lựa chọn, quyết định của bệnh nhân phải trải qua cấy ghép vĩnh viễn là một quá trình tương đối phức tạp và có thể đòi hỏi thời gian. Không giống như điều trị tái đồng bộ tim, β-blockers và kháng renin-angiotensin-aldosterone, trong đó cải thiện sự sống còn và chất lượng sống liên quan đến sức khỏe, ICD ngăn chăn tử vong nhưng không thay đổi về cơ bản tái cấu trúc (không có điều trị tái đồng bộ tim đồng thời). ICD cũng đi kèm với nguy cơ biến chứng trong quá trình cấy, nhiễm trùng, sốc không phù hợp, cần thiết cho theo dõi, nhập viện nhiều hơn và khả năng cho chịu đựng đau đớn của giai đoạn cuối của đời sống nhiều hơn. Như vậy, đặt ICD là một quyết định sở thích nhạy cảm đòi hỏi phải xem xét cân bằng để tăng cơ hội sống sót trong nguy cơ giảm chất lượng cuộc sống. Một WCD có thể cung cấp cho bệnh nhân bảo vệ tạm thời đối với SCD trong khi họ đạt được một sự hiểu biết tốt hơn về bệnh tim của họ, làm rõ giá trị của chúng, xác định mục tiêu tổng thể của việc chăm sóc và sau đó quyết định về sở thích của họ trong việc cấy ghép vĩnh viễn của một máy khử rung tim. [78]
Các Cần thiết Nghiên cứu Trong tương lai
Phân tầng nguy cơ vẫn còn là một thách thức lớn đối với lựa chọn bệnh nhân để điều trị WCD. Không giống như hầu hết các phương pháp điều trị tim mạch, được thiết kế để giảm nguy cơ lâu dài của các biến cố, WCDs nhằm giảm ngắn hạn hoặc có nguy cơ đột tử tạm thời. Do đó, ngoại suy các lợi ích của WCDs từ các nghiên cứu hoặc các phương pháp giảm nguy cơ lâu dài là không thích hợp và có khả năng nguy hiểm.
Một thách thức liên quan, làm thế nào để giải thích cho nguy cơ đan xen nhau của tử vong không do loạn nhịp được tồn tại do các bệnh nhân có các yếu tố nguy cơ cho tử vong loạn nhịp. Trong thử nghiệm Dinamit, một so sánh ngẫu nhiên ICD và không có ICD ở những bệnh nhân bị MI mới xẩy ra và LVEF < 0,35, không có sự khác biệt trong nguy cơ tử vong do mọi nguyên nhân. [28] Tuy nhiên, nguy cơ tử vong loạn nhịp tim thấp hơn ở nhóm ICD (tỷ lệ nguy hiểm, 0,42; P = 0,009), nhưng sống còn toàn bộ không có khác nhau, chủ yếu do bệnh nhân trong nhóm ICD có nguy cơ tử vong do tim, không phải do loạn nhịp cao hơn (tỷ lệ nguy hiểm , 1,72; P = 0,05). Giải thích có lẽ tốt nhất do nhiều yếu tố nguy cơ chiếm ưu thế cho SCD, gồm suy tim, rối loạn chức năng tâm thu thất trái, bệnh dẫn truyền và VT có thể tạo ra bằng kích thích có chương trình, cũng liên quan với tử vong do nguyên nhân không phải do loạn nhịp và không phải tim mạch. [79] Do đó, ngay cả ước tính nguy cơ dựa trên 30 ngày do mọi nguyên nhân và tử suất tim mạch, đó là điểm kết thúc an toàn chung trong các thử nghiệm lâm sàng của suy tim và MI, có thể không chính xác trong việc xác định lợi ích của liệu pháp WCD.
Đối với những lý do này, các thử nghiệm ngẫu nhiên được tiến hành là rất cần thiết. Các nghiên cứu đầy hứa hẹn nhất có thử nghiệm VEST nói trên, trong đó đã ghi danh > 1700 bệnh nhân trong năm 2015, dự kiến hoàn thành vào cuối năm 2016 (NCT01446965). [60] Trong những tình huống quân bình để ngẫu nhiên là không thể, tiến hành cẩn thận nghiên cứu quan sát có thể làm rõ thêm dự báo nguy cơ. Nghiên cứu các Áo khử rung timở các Bệnh nhân Suy tim (SWIFT; NCT01326624) là một nghiên cứu quan sát để đánh giá tỷ lệ khử rung tim trong 4 phân nhóm quan trọng: suy tim tiên tiến, LVEF ≤ 0.35 với chẩn đoán tái thông mạch máu hoặc suy tim trong vòng 90 ngày, AMI Killip lớp III IV, và những người đang chờ cấy lại ICD. [80]
Trong trường hợp không có số liệu so sánh, chi phí-hiệu quả điều trị vẫn chưa rõ ràng nhưng sẽ bị ảnh hưởng nhiều do số lượng bệnh nhân cần điều trị để ngăn ngừa 1 trường hợp loạn nhịp tim hoặc tử vong. Cải thiện sự phân tầng nguy cơ để giảm thiểu sử dụng ở những bệnh nhân có nguy cơ thấp do đó sẽ cải thiện đáng kể tổng chi phí cho mỗi người được cứu sống. Cuối cùng, đơn giản hơn, các thiết bị di động nhiều có thể làm tăng hiệu quả chăm sóc sức khỏe là kết quả sự tuân thủ của các bệnh nhân được cải thiện và khả năng chịu đựng, đưa ra chăm sóc được cải thiện cả tiếp cận công nghệ và chi phí thấp hơn.
Hạn chế
Mặc dù điều trị WCD càng được sử dụng trong thực hành lâm sàng, hiện nay, chỉ có dữ liệu sơ bộ tồn tại trên thực tế hiệu quả của can thiệp này trong việc cải thiện sự sống còn ở những bệnh nhân có nguy cơ cho SCD. Theo đó, cố vấn khoa học này cung cấp một khuôn khổ tạm thời dự kiến để hỗ trợ trong việc ra quyết định cho đến khi nhiều nghiên cứu dứt khoát là có sẵn.
Kết luận
SCD kết quả từ VT / VF vẫn là một nguyên nhân quan trọng và có khả năng ngăn ngừa được tử vong. Mặc dù có lợi ích rõ ràng của chúng, công nghệ máy khử rung tim hiện nay có những hạn chế và rủi ro. WCDs có thể phục vụ như là một phương tiện tạm thời loại bỏ tử vong do loạn nhịp ở bệnh nhân có nguy cơ SCD tạm thời hoặc những người có chỉ định cấy ICD có một rào cản tạm thời để cấy thiết bị vĩnh viễn. Những người cung cấp cần phải giữ nhiều yếu tố trong tâm trí và liên tục cân nhắc những rủi ro cá nhân và lợi ích cấy ICD và WCDs ở những bệnh nhân của họ. Hơn nữa, cuộc thảo luận về sở thích bệnh nhân là một phần không thể thiếu trong việc chăm sóc bệnh nhân và điều trị WCD. Nghiên cứu sâu hơn, bao gồm cả thử nghiệm ngẫu nhiên là cần thiết để thông báo tốt hơn việc sử dụng tối ưu của liệu pháp WCD.
Tài liệu tham khảo
1. Go AS, Mozaffarian D, Roger VL, Benjamin EJ, Berry JD, Borden WB, Bravata DM, Dai S, Ford ES, Fox CS, Franco S, Fullerton HJ, Gillespie C, Hailpern SM, Heit JA, Howard VJ, Huffman MD, Kissela BM, Kittner SJ, Lackland DT, Lichtman JH, Lisabeth LD, Magid D, Marcus GM, Marelli A, Matchar DB, McGuire DK, Mohler ER, Moy CS, Mussolino ME, Nichol G, Paynter NP, Schreiner PJ, Sorlie PD, Stein J, Turan TN, Virani SS, Wong ND, Woo D, Turner MB; on behalf of the American Heart Association Statistics Committee and Stroke Statistics Subcommittee. Heart disease and stroke statistics—2013 update: a report from the American Heart Association [published correction appears in Circulation. 2013;127:e841]. Circulation. 2013;127:e6–e245. doi: 10.1161/CIR.0b013e31828124ad.
2. Stecker EC, Vickers C, Waltz J, Socoteanu C, John BT, Mariani R, McAnulty JH, Gunson K, Jui J, Chugh SS. Population-based analysis of sudden cardiac death with and without left ventricular systolic dysfunction: two-year findings from the Oregon Sudden Unexpected Death Study. J Am Coll Cardiol. 2006;47:1161–1166. doi: 10.1016/j.jacc.2005.11.045.
3. Bardy GH, Lee KL, Mark DB, Poole JE, Packer DL, Boineau R, Domanski M, Troutman C, Anderson J, Johnson G, McNulty SE, Clapp-Channing N, Davidson-Ray LD, Fraulo ES, Fishbein DP, Luceri RM, Ip JH; Sudden Cardiac Death in Heart Failure Trial (SCD-HeFT) Investigators. Amiodarone or an implantable cardioverter-defibrillator for congestive heart failure. N Engl J Med. 2005;352:225–237. doi: 10.1056/ NEJMoa043399.
4. Moss AJ, Zareba W, Hall WJ, Klein H, Wilber DJ, Cannom DS, Daubert JP, Higgins SL, Brown MW, Andrews ML; Multicenter Automatic Defibrillator Implantation Trial II Investigators. Prophylactic implantation of a defibrillator in patients with myocardial infarction and reduced ejection fraction [published correction appears in N Engl J Med. 2005;352:2146]. N Engl J Med. 2002;346:877–883. doi: 10.1056/NEJMoa013474.
5. Buxton AE, Lee KL, Fisher JD, Josephson ME, Prystowsky EN, Hafley G. A randomized study of the prevention of sudden death in patients with coronary artery disease: Multicenter Unsustained Tachycardia Trial Investigators [published correction appears in N Engl J Med. 2000;342:1300]. N Engl J Med. 1999;341:1882–1890. doi: 10.1056/NEJM199912163412503.
6. A comparison of antiarrhythmic-drug therapy with implantable defibrillators in patients resuscitated from near-fatal ventricular arrhythmias: the Antiarrhythmics Versus Implantable Defibrillators (AVID) Investigators. N Engl J Med. 1997;337:1576–1583.
7. Moss AJ, Hall WJ, Cannom DS, Daubert JP, Higgins SL, Klein H, Levine JH, Saksena S, Waldo AL, Wilber D, Brown MW, Heo M. Improved survival with an implanted defibrillator in patients with coronary disease at high risk for ventricular arrhythmia: Multicenter Automatic Defibrillator Implantation Trial Investigators. N Engl J Med. 1996;335:1933–1940. doi: 10.1056/NEJM199612263352601.
8. Adler A, Halkin A, Viskin S. Wearable cardioverter-defibrillators. Circulation. 2013;127:854–860. doi: 10.1161/CIRCULATIONAHA. 112.146530.
9. Nichol G, Thomas E, Callaway CW, Hedges J, Powell JL, Aufderheide TP, Rea T, Lowe R, Brown T, Dreyer J, Davis D, Idris A, Stiell I; Resuscitation Outcomes Consortium Investigators. Regional variation in out-of-hospitalcardiac arrest incidence and outcome [published correction appears in JAMA. 2008;300:1763]. JAMA. 2008;300:1423–1431. doi: 10.1001/ jama.300.12.1423.
10. Epstein AE, DiMarco JP, Ellenbogen KA, Estes NA 3rd, Freedman RA, Gettes LS, Gillinov AM, Gregoratos G, Hammill SC, Hayes DL, Hlatky MA, Newby LK, Page RL, Schoenfeld MH, Silka MJ, Stevenson LW, Sweeney MO. 2012 ACCF/AHA/HRS focused update incorporated into the ACCF/ AHA/HRS 2008 guidelines for device-based therapy of cardiac rhythm abnormalities: a report of the American College of Cardiology Foundation/ American Heart Association Task Force on Practice Guidelines and the Heart Rhythm Society. Circulation. 2013;127:e283–e352. doi: 10.1161/ CIR.0b013e318276ce9b.
11. Ezekowitz JA, Armstrong PW, McAlister FA. Implantable cardioverter defibrillators in primary and secondary prevention: a systematic review of randomized, controlled trials. Ann Intern Med. 2003;138:445–452.
12. Nanthakumar K, Epstein AE, Kay GN, Plumb VJ, Lee DS. Prophylactic implantable cardioverter-defibrillator therapy in patients with left ventricular systolic dysfunction: a pooled analysis of 10 primary prevention trials. J Am Coll Cardiol. 2004;44:2166–2172. doi: 10.1016/j.jacc.2004.08.054.
13. Wilber DJ, Zareba W, Hall WJ, Brown MW, Lin AC, Andrews ML, Burke M, Moss AJ. Time dependence of mortality risk and defibrillator benefit after myocardial infarction. Circulation. 2004;109:1082–1084. doi: 10.1161/01.CIR.0000121328.12536.07.
14. Hess PL, Laird A, Edwards R, Bardy GH, Bigger JT, Buxton AE, Moss AJ, Lee KL, Hall WJ, Steinman R, Dorian P, Hallstrom A, Cappato R, Kadish AH, Kudenchuk PJ, Mark DB, Al-Khatib SM, Piccini JP, Inoue LY, Sanders GD. Survival benefit of primary prevention implantable cardioverter-defibrillator therapy after myocardial infarction: does time to implant matter? A meta-analysis using patient-level data from 4 clinical trials. Heart Rhythm. 2013;10:828–835. doi: 10.1016/j. hrthm.2013.02.011.
15. Solomon SD, Glynn RJ, Greaves S, Ajani U, Rouleau JL, Menapace F, Arnold JM, Hennekens C, Pfeffer MA. Recovery of ventricular function after myocardial infarction in the reperfusion era: the healing and early afterload reducing therapy study. Ann Intern Med. 2001;134:451–458.
16. Elefteriades JA, Tolis G Jr, Levi E, Mills LK, Zaret BL. Coronary artery bypass grafting in severe left ventricular dysfunction: excellent survival with improved ejection fraction and functional state. J Am Coll Cardiol. 1993;22:1411–1417.
17. Bax JJ, Poldermans D, Elhendy A, Cornel JH, Boersma E, Rambaldi R, Roelandt JR, Fioretti PM. Improvement of left ventricular ejection fraction, heart failure symptoms and prognosis after revascularization in patients with chronic coronary artery disease and viable myocardium detected by dobutamine stress echocardiography. J Am Coll Cardiol. 1999;34:163–169.
18. Murphy NF, OLoughlin C, Ledwidge M, McCaffrey D, McDonald K. Improvement but no cure of left ventricular systolic dysfunction in treated heart failure patients. Eur J Heart Fail. 2007;9:1196–1204. doi: 10.1016/j. ejheart.2007.10.001.
19. van Campen LC, Visser FC, Visser CA. Ejection fraction improvement by beta-blocker treatment in patients with heart failure: an analysis of studies published in the literature. J Cardiovasc Pharmacol. 1998;32(suppl 1):S31–S35
20. McNamara DM, Starling RC, Cooper LT, Boehmer JP, Mather PJ, Janosko KM, Gorcsan J 3rd, Kip KE, Dec GW; IMAC Investigators. Clinical and demographic predictors of outcomes in recent onset dilated cardiomyopathy: results of the IMAC (Intervention in Myocarditis and Acute Cardiomyopathy)-2 study [published correction appears in J Am Coll Cardiol. 2011;58:1832]. J Am Coll Cardiol. 2011;58:1112–1118. doi: 10.1016/j.jacc.2011.05.033.
21. Marchlinski FE, Jessup M. Timing the implantation of implantable cardioverter-defibrillators in patients with nonischemic cardiomyopathy. J Am Coll Cardiol. 2006;47:2483–2485. doi: 10.1016/j.jacc.2006.01.075.
22. Wong M, Staszewsky L, Latini R, Barlera S, Glazer R, Aknay N, Hester A, Anand I, Cohn JN. Severity of left ventricular remodeling defines outcomes and response to therapy in heart failure: Valsartan Heart Failure Trial (ValHeFT) echocardiographic data. J Am Coll Cardiol. 2004;43:2022–2027. doi: 10.1016/j.jacc.2003.12.053.
23. Solomon SD, Zelenkofske S, McMurray JJ, Finn PV, Velazquez E, Ertl G, Harsanyi A, Rouleau JL, Maggioni A, Kober L, White H, Van de Werf F, Pieper K, Califf RM, Pfeffer MA; Valsartan in Acute Myocardial Infarction Trial (VALIANT) Investigators. Sudden death in patients with myocardial infarction and left ventricular dysfunction, heart failure, or both [published correction appears in N Engl J Med. 2005;353:744]. N Engl J Med. 2005;352:2581–2588.doi: 10.1056/NEJMoa043938.
24. Pouleur AC, Barkoudah E, Uno H, Skali H, Finn PV, Zelenkofske SL, Belenkov YN, Mareev V, Velazquez EJ, Rouleau JL, Maggioni AP, Køber L, Califf RM, McMurray JJ, Pfeffer MA, Solomon SD; VALIANT Investigators. Pathogenesis of sudden unexpected death in a clinical trial of patients with myocardial infarction and left ventricular dysfunction, heart failure, or both. Circulation. 2010;122:597–602. doi: 10.1161/ CIRCULATIONAHA.110.940619.
25. Kadish A, Dyer A, Daubert JP, Quigg R, Estes NA, Anderson KP, Calkins H, Hoch D, Goldberger J, Shalaby A, Sanders WE, Schaechter A, Levine JH; Defibrillators in Non-Ischemic Cardiomyopathy Treatment Evaluation (DEFINITE) Investigators. Prophylactic defibrillator implantation in patients with nonischemic dilated cardiomyopathy. N Engl J Med. 2004;350:2151–2158.doi: 10.1056/NEJMoa033088.
26. Kadish A, Schaechter A, Subacius H, Thattassery E, Sanders W, Anderson KP, Dyer A, Goldberger J, Levine J. Patients with recently diagnosed nonischemic cardiomyopathy benefit from implantable cardioverterdefibrillators. J Am Coll Cardiol. 2006;47:2477–2482. doi: 10.1016/j. jacc.2005.11.090.
27. Bänsch D, Antz M, Boczor S, Volkmer M, Tebbenjohanns J, Seidl K, Block M, Gietzen F, Berger J, Kuck KH. Primary prevention of sudden cardiac death in idiopathic dilated cardiomyopathy: the Cardiomyopathy Trial (CAT). Circulation. 2002;105:1453–1458.
28. Hohnloser SH, Kuck KH, Dorian P, Roberts RS, Hampton JR, Hatala R, Fain E, Gent M, Connolly SJ; DINAMIT Investigators. Prophylactic use of an implantable cardioverter-defibrillator after acute myocardial infarction. N Engl J Med. 2004;351:2481–2488.doi: 10.1056/NEJMoa041489.
29. Steinbeck G, Andresen D, Seidl K, Brachmann J, Hoffmann E, Wojciechowski D, Kornacewicz-Jach Z, Sredniawa B, Lupkovics G, Hofgärtner F, Lubinski A, Rosenqvist M, Habets A, Wegscheider K, Senges J; IRIS Investigators. Defibrillator implantation early after myocardial infarction. N Engl J Med. 2009;361:1427–1436. doi: 10.1056/NEJMoa0901889.
30. Larsen MP, Eisenberg MS, Cummins RO, Hallstrom AP. Predicting survival from out-of-hospital cardiac arrest: a graphic model. Ann Emerg Med. 1993;22:1652–1658.
31. Link MS, Atkins DL, Passman RS, Halperin HR, Samson RA, White RD, Cudnik MT, Berg MD, Kudenchuk PJ, Kerber RE. Part 6: electrical therapies: automated external defibrillators, defibrillation, cardioversion, and pacing: 2010 American Heart Association guidelines for cardiopulmonary resuscitation and emergency cardiovascular care [published correction appears in Circulation. 2011;123:e235]. Circulation. 2010;122(suppl 3):S706–S719. doi: 10.1161/CIRCULATIONAHA.110.970954.
32. Gundry JW, Comess KA, DeRook FA, Jorgenson D, Bardy GH. Comparison of naive sixth-grade children with trained professionals in the use of an automated external defibrillator. Circulation. 1999;100:1703–1707.
33. Nichol G, Stiell IG, Laupacis A, Pham B, De Maio VJ, Wells GA. A cumulative meta-analysis of the effectiveness of defibrillator-capable emergency medical services for victims of out-of-hospital cardiac arrest. Ann Emerg Med. 1999;34(pt 1):517–525.
34. Bardy GH, Lee KL, Mark DB, Poole JE, Toff WD, Tonkin AM, Smith W, Dorian P, Packer DL, White RD, Longstreth WT Jr, Anderson J, Johnson G, Bischoff E, Yallop JJ, McNulty S, Ray LD, Clapp-Channing NE, Rosenberg Y, Schron EB; HAT Investigators. Home use of automated external defibrillators for sudden cardiac arrest. N Engl J Med. 2008;358:1793–1804. doi: 10.1056/NEJMoa0801651.
35. Brignole M. Are complications of implantable defibrillators under-estimated and benefits over-estimated? Europace. 2009;11:1129–1133. doi: 10.1093/europace/eup174.
36. Ezekowitz JA, Rowe BH, Dryden DM, Hooton N, Vandermeer B, Spooner C, McAlister FA. Systematic review: implantable cardioverter defibrillators for adults with left ventricular systolic dysfunction. Ann Intern Med. 2007;147:251–262.
37. Kleemann T, Becker T, Doenges K, Vater M, Senges J, Schneider S, Saggau W, Weisse U, Seidl K. Annual rate of transvenous defibrillation lead defects in implantable cardioverter-defibrillators over a period of >10 years. Circulation. 2007;115:2474–2480. doi: 10.1161/ CIRCULATIONAHA.106.663807.
38. Borleffs CJ, van Erven L, van Bommel RJ, van der Velde ET, van der Wall EE, Bax JJ, Rosendaal FR, Schalij MJ. Risk of failure of transvenous implantable cardioverter-defibrillator leads. Circ Arrhythm Electrophysiol. 2009;2:411–416. doi: 10.1161/CIRCEP.108.834093.
39. Bardy GH, Smith WM, Hood MA, Crozier IG, Melton IC, Jordaens L, Theuns D, Park RE, Wright DJ, Connelly DT, Fynn SP, Murgatroyd FD, Sperzel J, Neuzner J, Spitzer SG, Ardashev AV, Oduro A, Boersma L, Maass AH, Van Gelder IC, Wilde AA, van Dessel PF, Knops RE, Barr CS, Lupo P, Cappato R, Grace AA. An entirely subcutaneous implantable cardioverter-defibrillator. N Engl J Med. 2010;363:36–44. doi: 10.1056/ NEJMoa0909545.
40. Olde Nordkamp LR, Dabiri Abkenari L, Boersma LV, Maass AH, de Groot JR, van Oostrom AJ, Theuns DA, Jordaens LJ, Wilde AA, Knops RE. The entirely subcutaneous implantable cardioverter-defibrillator: initial clinical experience in a large Dutch cohort. J Am Coll Cardiol. 2012;60:1933– 1939. doi: 10.1016/j.jacc.2012.06.053.
41. Hauser RG. The subcutaneous implantable cardioverter-defibrillator: should patients want one? J Am Coll Cardiol. 2013;61:20–22. doi: 10.1016/j.jacc.2012.07.069.
42. Auricchio A, Klein H, Geller CJ, Reek S, Heilman MS, Szymkiewicz SJ. Clinical efficacy of the wearable cardioverter-defibrillator in acutely terminating episodes of ventricular fibrillation. Am J Cardiol. 1998;81:1253–1256.
43. Klein HU, Meltendorf U, Reek S, Smid J, Kuss S, Cygankiewicz I, Jons C, Szymkiewicz S, Buhtz F, Wollbrueck A, Zareba W, Moss AJ. Bridging a temporary high risk of sudden arrhythmic death: experience with the wearable cardioverter defibrillator (WCD). Pacing Clin Electrophysiol. 2010;33:353–367. doi: 10.1111/j.1540-8159.2009.02590.x.
44. Dillon KA, Szymkiewicz SJ, Kaib TE. Evaluation of the effectiveness of a wearable cardioverter defibrillator detection algorithm. J Electrocardiol. 2010;43:63–67. doi: 10.1016/j.jelectrocard.2009.05.010.
45. Knops RE, Kooiman KM, Ten Sande JN, de Groot JR, Wilde AA. First experience with the wearable cardioverter defibrillator in the Netherlands. Neth Heart J. 2012;20:77–81. doi: 10.1007/s12471-011-0227-9.
46. Feldman AM, Klein H, Tchou P, Murali S, Hall WJ, Mancini D, Boehmer J, Harvey M, Heilman MS, Szymkiewicz SJ, Moss AJ; WEARIT Investigators and Coordinators; BIROAD Investigators and Coordinators. Use of a wearable defibrillator in terminating tachyarrhythmias in patients at high risk for sudden death: results of the WEARIT/BIROAD [published correction appears in Pacing Clin Electrophysiol. 2004;27:following Table of Contents]. Pacing Clin Electrophysiol. 2004;27:4–9.
47. Reek S, Geller JC, Meltendorf U, Wollbrueck A, Szymkiewicz SJ, Klein HU. Clinical efficacy of a wearable defibrillator in acutely terminating episodes of ventricular fibrillation using biphasic shocks. Pacing Clin Electrophysiol. 2003;26:2016–2022.
48. Chung MK, Szymkiewicz SJ, Shao M, Zishiri E, Niebauer MJ, Lindsay BD, Tchou PJ. Aggregate national experience with the wearable cardioverter-defibrillator: event rates, compliance, and survival. J Am Coll Cardiol. 2010;56:194–203. doi: 10.1016/j.jacc.2010.04.016.
49. Collins KK, Silva JN, Rhee EK, Schaffer MS. Use of a wearable automated defibrillator in children compared to young adults. Pacing Clin Electrophysiol. 2010;33:1119–1124. doi: 10.1111/j.1540-8159. 2010.02819.x.
50. Everitt MD, Saarel EV. Use of the wearable external cardiac defibrillator in children. Pacing Clin Electrophysiol. 2010;33:742–746. doi: 10.1111/j.1540-8159.2010.02702.x.
51. LaPage MJ, Canter CE, Rhee EK. A fatal device-device interaction between a wearable automated defibrillator and a unipolar ventricular pacemaker. Pacing Clin Electrophysiol. 2008;31:912–915. doi: 10.1111/j.1540- 8159.2008.01110.x.
52. Epstein AE, Abraham WT, Bianco NR, Kern KB, Mirro M, Rao SV, Rhee EK, Solomon SD, Szymkiewicz SJ. Wearable cardioverter-defibrillator use in patients perceived to be at high risk early post-myocardial infarction. J Am Coll Cardiol. 2013;62:2000–2007. doi: 10.1016/j.jacc.2013.05.086.
53. Mitrani RD, McArdle A, Slane M, Cogan J, Myerburg RJ. Wearable defibrillators in uninsured patients with newly diagnosed cardiomyopathy or recent revascularization in a community medical center. Am Heart J. 2013;165:386–392. doi: 10.1016/j.ahj.2012.12.014.
54. Zishiri ET, Williams S, Cronin EM, Blackstone EH, Ellis SG, Roselli EE, Smedira NG, Gillinov AM, Glad JA, Tchou PJ, Szymkiewicz SJ, Chung MK. Early risk of mortality after coronary artery revascularization in patients with left ventricular dysfunction and potential role of the wearable cardioverter defibrillator. Circ Arrhythm Electrophysiol. 2013;6:117–128. doi: 10.1161/CIRCEP.112.973552.
55. Kao AC, Krause SW, Handa R, Karia D, Reyes G, Bianco NR, Szymkiewicz SJ; Wearable defibrillator use In heart Failure (WIF) Investigators. Wearable defibrillator use in heart failure (WIF): results of a prospective registry. BMC Cardiovasc Disord. 2012;12:123. doi: 10.1186/1471-2261-12-123.
56. Saltzberg MT, Szymkiewicz S, Bianco NR. Characteristics and outcomes of peripartum versus nonperipartum cardiomyopathy in women using a wearable cardiac defibrillator. J Card Fail. 2012;18:21–27. doi: 10.1016/j. cardfail.2011.09.004.
57. Rao M, Goldenberg I, Moss AJ, Klein H, Huang DT, Bianco NR, Szymkiewicz SJ, Zareba W, Brenyo A, Buber J, Barsheshet A. Wearable defibrillator in congenital structural heart disease and inherited arrhythmias. Am J Cardiol. 2011;108:1632–1638. doi: 10.1016/j. amjcard.2011.07.021.
58. Bloch Thomsen PE, Jons C, Raatikainen MJ, Moerch Joergensen R, Hartikainen J, Virtanen V, Boland J, Anttonen O, Gang UJ, Hoest N, Boersma LV, Platou ES, Becker D, Messier MD, Huikuri HV; Cardiac Arrhythmias and Risk Stratification After Acute Myocardial Infarction (CARISMA) Study Group. Long-term recording of cardiac arrhythmias with an implantable cardiac monitor in patients with reduced ejection fraction after acute myocardial infarction: the Cardiac Arrhythmias and Risk Stratification After Acute Myocardial Infarction (CARISMA) study. Circulation. 2010;122:1258–1264. doi: 10.1161/ CIRCULATIONAHA.109.902148.
59. van Rees JB, Borleffs CJ, de Bie MK, Stijnen T, van Erven L, Bax JJ, Schalij MJ. Inappropriate implantable cardioverter-defibrillator shocks: incidence, predictors, and impact on mortality. J Am Coll Cardiol. 2011;57:556–562. doi: 10.1016/j.jacc.2010.06.059.
60. ClinicalTrials.Gov. Vest Prevention of Early Sudden Death Trial and VEST Registry. http://clinicaltrials.gov/ct2/show/NCT01446965?term=v est+wearable&rank=1. Accessed November 14, 2014.
61. Gronda E, Bourge RC, Costanzo MR, Deng M, Mancini D, Martinelli L, Torre-Amione G, OHara ML, Chambers S. Heart rhythm considerations in heart transplant candidates and considerations for ventricular assist devices: International Society for Heart and Lung Transplantation guidelines for the care of cardiac transplant candidates—2006 [published correction appears in J Heart Lung Transplant. 2006;25:1276]. J Heart Lung Transplant. 2006;25:1043–1056. doi: 10.1016/j.healun.2006.06.005.
62. Nery PB, Fernandes R, Nair GM, Sumner GL, Ribas CS, Menon SM, Wang X, Krahn AD, Morillo CA, Connolly SJ, Healey JS. Device-related infection among patients with pacemakers and implantable defibrillators: incidence, risk factors, and consequences. J Cardiovasc Electrophysiol. 2010;21:786–790. doi: 10.1111/j.1540-8167.2009.01690.x.
63. Vaughan-Sarrazin MS, Hannan EL, Gormley CJ, Rosenthal GE. Mortality in Medicare beneficiaries following coronary artery bypass graft surgery in states with and without certificate of need regulation. JAMA. 2002;288:1859–1866.
64. Toda K, Mackenzie K, Mehra MR, DiCorte CJ, Davis JE, McFadden PM, Ochsner JL, White C, Van Meter CH Jr. Revascularization in severe ventricular dysfunction (15% < OR = LVEF < OR = 30%): a comparison of bypass grafting and percutaneous intervention. Ann Thorac Surg. 2002;74:2082–2087.
65. Bigger JT Jr. Prophylactic use of implanted cardiac defibrillators in patients at high risk for ventricular arrhythmias after coronary-artery bypass graft surgery. Coronary Artery Bypass Graft (CABG) Patch Trial Investigators. N Engl J Med. 1997;337:1569–1575. doi: 10.1056/ NEJM199711273372201.
66. Centers for Medicaid & Medicare Services. National coverage determination for implantable automatic defibrillators (20.4). 2005. https://www. cms.gov/medicare-coverage-database/details/ncd-details.aspx?NCDId=1 10&ncdver=2&NCAId=148&NcaName=Computed+Tomographic+Angi ography&IsPopup=y&bc=AAAAAAAAAEAAAA%3d%3d&. Accessed March 9, 2016.
67. Steinberg JS, Mittal S. The federal audit of implantable cardioverterdefibrillator implants: lessons learned. J Am Coll Cardiol. 2012;59:1270– 1274. doi: 10.1016/j.jacc.2011.12.026.
68. Kusumoto FM, Calkins H, Boehmer J, Buxton AE, Chung MK, Gold MR, Hohnloser SH, Indik J, Lee R, Mehra MR, Menon V, Page RL, Shen W-K, Slotwiner DJ, Stevenson LW, Varosy PD, Lisa Welikovitch. HRS/ACC/ AHA expert consensus statement on the use of implantable cardioverterdefibrillator therapy in patients who are not included or not well represented in clinical trials. Circulation. 2014;130:94–125.
69. Epstein AE, DiMarco JP, Ellenbogen KA, Estes NA 3rd, Freedman RA, Gettes LS, Gillinov AM, Gregoratos G, Hammill SC, Hayes DL, Hlatky MA, Newby LK, Page RL, Schoenfeld MH, Silka MJ, Stevenson LW, Sweeney MO. ACC/AHA/HRS 2008 guidelines for device-based therapy of cardiac rhythm abnormalities: a report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines (Writing Committee to Revise the ACC/AHA/NASPE 2002 Guideline Update for Implantation of Cardiac Pacemakers and Antiarrhythmia Devices) [published correction appears in Circulation. 2009;120:e34–e35]. Circulation. 2008;117:e350–e408. doi: 10.1161/ CIRCUALTIONAHA.108.189742.
70. Pearson GD, Veille JC, Rahimtoola S, Hsia J, Oakley CM, Hosenpud JD, Ansari A, Baughman KL. Peripartum cardiomyopathy: National Heart, Lung, and Blood Institute and Office of Rare Diseases (National Institutes of Health) workshop recommendations and review. JAMA. 2000;283:1183–1188.
71. Amos AM, Jaber WA, Russell SD. Improved outcomes in peripartum cardiomyopathy with contemporary. Am Heart J. 2006;152:509–513. doi: 10.1016/j.ahj.2006.02.008.
72. Schoppet M, Maisch B. Alcohol and the heart. Herz. 2001;26:345–352.
73. Henderson R, Keiding N. Individual survival time prediction using statistical models. J Med Ethics. 2005;31:703–706. doi: 10.1136/ jme.2005.012427.
74. Haga K, Murray S, Reid J, Ness A, ODonnell M, Yellowlees D, Denvir MA. Identifying community based chronic heart failure patients in the last year of life: a comparison of the Gold Standards Framework Prognostic Indicator Guide and the Seattle Heart Failure Model. Heart. 2012;98:579– 583. doi: 10.1136/heartjnl-2011-301021.
75. Allen LA, Gheorghiade M, Reid KJ, Dunlay SM, Chan PS, Hauptman PJ, Zannad F, Konstam MA, Spertus JA. Identifying patients hospitalized with heart failure at risk for unfavorable future quality of life. Circ Cardiovasc Qual Outcomes. 2011;4:389–398. doi: 10.1161/ CIRCOUTCOMES.110.958009.
76. Stehlik J, Edwards LB, Kucheryavaya AY, Benden C, Christie JD, Dipchand AI, Dobbels F, Kirk R, Rahmel AO, Hertz MI; International Society of Heart and Lung Transplantation. The Registry of the International Society for Heart and Lung Transplantation: 29th official adult heart transplant report—2012. J Heart Lung Transplant. 2012;31:1052–1064. doi: 10.1016/j.healun.2012.08.002.
77. Uriel N, Jorde UP, Woo Pak S, Jiang J, Clerkin K, Takayama H, Naka Y, Schulze PC, Mancini DM. Impact of long term left ventricular assist device therapy on donor allocation in cardiac transplantation. J Heart Lung Transplant. 2013;32:188–195. doi: 10.1016/j.healun.2012.11.010.
78. Allen LA, Stevenson LW, Grady KL, Goldstein NE, Matlock DD, Arnold RM, Cook NR, Felker GM, Francis GS, Hauptman PJ, Havranek EP, Krumholz HM, Mancini D, Riegel B, Spertus JA; on behalf of American Heart Association; Council on Quality of Care and Outcomes Research; Council on Cardiovascular Nursing; Council on Clinical Cardiology; Council on Cardiovascular Radiology and Intervention; Council on Cardiovascular Surgery and Anesthesia. Decision making in advanced heart failure: a scientific statement from the American Heart Association. Circulation. 2012;125:1928–1952. doi: 10.1161/CIR.0b013e31824f2173.
79. Buxton AE, Lee KL, Hafley GE, Pires LA, Fisher JD, Gold MR, Josephson ME, Lehmann MH, Prystowsky EN; MUSTT Investigators. Limitations of ejection fraction for prediction of sudden death risk in patients with coronary artery disease: lessons from the MUSTT study. J Am Coll Cardiol. 2007;50:1150–1157. doi: 10.1016/j.jacc.2007.04.095.
80. ClinicalTrials.Gov. Study of the Wearable Defibrillator in Heart-Failure Patients (SWIFT). http://clinicaltrials.gov/ct2/show/NCT01326624?term =swift+wearable&rank=1. Accessed November 14, 2014.
81. Circulation. published online March 28, 2016.







