S.D. Solomon, J.J.V. McMurray và Cộng sự
New England Journal of Medicine
Lược dịch và hiệu đính: TS.BS. NGUYỄN THANH HUÂN
Bộ Môn Lão Khoa, Đại học Y Dược TP.HCM
Khoa Nội Tim mạch, Bệnh viện Thống Nhất
TÓM TẮT
Bối cảnh
Thuốc ức chế kênh đồng vận chuyển natri-glucose 2 (SGLT2) làm giảm nguy cơ nhập viện vì suy tim và tử vong do tim mạch ở bệnh nhân suy tim mạn tính có phân suất tống máu (PSTM) thất trái giảm (≤40%). Vậy liệu thuốc ức chế SGLT2 có hiệu quả ở những bệnh nhân có PSTM thất trái cao hơn hay không vẫn còn là câu hỏi.
Phương pháp
Chúng tôi phân chia ngẫu nhiên 6263 bệnh nhân suy tim có PSTM thất trái >40% được điều trị với dapagliflozin (10 mg/lần/ngày) hoặc giả dược tương ứng, trên nền điều trị chuẩn. Tiêu chí chính là tiêu chí gộp của suy tim xấu đi (được định nghĩa là nhập viện ngoài kế hoạch do suy tim hoặc thăm khám khẩn cấp do suy tim) hoặc tử vong do tim mạch, được đánh giá bằng phân tích thời gian từ lúc bắt đầu theo dõi cho đến khi xảy ra biến cố (time-to-event).
Kết quả
Trong thời gian trung vị 2,3 năm, biến cố thuộc tiêu chí chính xảy ra trên 512/3131 bệnh nhân (16,4%) ở nhóm dapagliflozin và 610/3132 bệnh nhân (19,5%) ở nhóm giả dược (Hazard Ratio 0,82; khoảng tin cậy (KTC) 95%: 0,73 – 0,92; P<0,001). Suy tim xấu đi xảy ra trên 368 bệnh nhân (11,8%) ở nhóm dapagliflozin và 455 bệnh nhân (14,5%) ở nhóm giả dược (HR 0,79; KTC 95%: 0,69 – 0,91); tử vong do tim mạch xảy ra trên 231 bệnh nhân (7,4%) và 261 bệnh nhân (8,3%), tương ứng (HR 0,88; KTC 95%: 0,74 – 1,05). Tổng số biến cố và gánh nặng triệu chứng ở nhóm dapagliflozin thấp hơn so với nhóm giả dược. Kết quả được ghi nhận đồng nhất trên những bệnh nhân có PSTM thất trái ≥60% và những bệnh nhân có PSTM thất trái <60%, và kết quả đồng nhất ở các phân nhóm được xác định trước, bao gồm bệnh nhân có hoặc không có đái tháo đường. Tần suất các biến cố bất lợi là tương tự nhau ở hai nhóm.
Kết luận
Dapagliflozin làm giảm nguy cơ kết hợp của suy tim nặng hơn hoặc tử vong do tim mạch ở những bệnh nhân suy tim có PSTM giảm nhẹ hoặc bảo tồn. (ClinicalTrials.gov, NCT03619213.)
MỞ ĐẦU
Thuốc ức chế kênh đồng vận chuyển natri-glucose 2, ban đầu được phát triển như là thuốc hạ đường huyết để điều trị đái tháo đường (ĐTĐ) týp 2, giảm nguy cơ tử vong và các kết cục bất lợi khác cho bệnh nhân suy tim mạn tính có PSTM giảm (tức là PSTM thất trái ≤40%) và cho bệnh nhân mắc bệnh thận mạn tính, bất kể có hoặc không mắc kèm ĐTĐ týp 2. Các hướng dẫn lâm sàng hiện tại khuyến cáo mạnh mẽ việc sử dụng thuốc ức chế SGLT2 cho bệnh nhân suy tim mạn tính có PSTM thất trái giảm.
Hiện nay có rất ít lựa chọn điều trị bằng dược lý cho bệnh nhân suy tim có PSTM thất trái giảm nhẹ hoặc bảo tồn. Gần đây, empagliflozin được chứng minh làm giảm nguy cơ kết hợp của nhập viện do suy tim hoặc tử vong do tim mạch trên bệnh nhân bị suy tim PSTM thất trái >40%, một phát hiện cho thấy rằng lợi ích của thuốc ức chế SGLT2 có thể mở rộng cho tất cả bệnh nhân suy tim, bất kể phân suất tống máu thất trái. Lợi ích này, phần lớn đến từ việc giảm nhập viện cho suy tim, dường như giảm ở những bệnh nhân có PSTM trong khoảng cao hơn (≥65%).
Vẫn còn một số khoảng trống về bằng chứng liên quan đến lợi ích của thuốc ức chế SGLT2 trên bệnh nhân suy tim, bao gồm cả việc những lợi ích này có được duy trì hay không khi sử dụng trên bệnh nhân có PSTM cao hơn, bệnh nhân được khởi trị trong hoặc ngay sau khi nhập viện và trên bệnh nhân PSTM cải thiện (trước đây có PTMS giảm và sau đó được cải thiện >40%). Thử nghiệm Deliver được thiết kế để kiểm tra giả thuyết rằng dapagliflozin (thuốc ức chế SGLT2) sẽ làm giảm nguy cơ suy tim xấu đi hoặc tử vong do tim mạch cho bệnh nhân có PSTM giảm nhẹ hoặc được bảo tồn.
PHƯƠNG PHÁP
Thiết kế và giám sát thử nghiệm
DELIVER là thử nghiệm pha 3, quốc tế, đa trung tâm, phân nhóm song song, ghi nhận biến cố, mù đôi, ngẫu nhiên, có đối chứng, trên bệnh nhân suy tim mạn tính có PSTM thất trái >40% được điều trị với dapagliflozin hoặc giả dược, trên nền điều trị chuẩn. Ban chỉ đạo đã phối hợp với nhà tài trợ (AstraZeneca) để thiết kế và giám sát việc tiến hành thử nghiệm và phân tích dữ liệu. Đề cương thử nghiêm đã được phê duyệt bởi các hội đồng nghiên cứu, hội đồng đạo đức tại mỗi trung tâm.
Bệnh nhân tham gia thử nghiệm
Bệnh nhân đủ điều kiện thu tuyển nếu từ 40 tuổi trở lên; tình trạng suy tim ổn định, có hoặc không có ĐTĐ týp 2; có PSTM thất trái >40%; có bằng chứng về bệnh cấu trúc tim; và có peptid lợi niệu natri tăng. Những bệnh nhân PSTM thất trái trước đó thấp hơn 40% cũng có thể được đưa vào nghiên cứu với điều kiện PSTM tại thời điểm thu tuyển lớn hơn 40%. Bệnh nhân được thu tuyển có thể là ngoại trú hoặc trong thời gian nằm viện do suy tim.
Tiến trình và kết cục thử nghiệm
Tất cả các bệnh nhân được cung cấp giấy chấp thuận có hiểu biết về tham gia thử nghiệm. Bệnh nhân đáp ứng tiêu chí nhận bệnh và loại trừ được chỉ định ngẫu nhiên để nhận dapagliflozin (10mg/lần/ngày) hoặc giả dược phù hợp, trên nền điều trị chuẩn.
Tiêu chí chính là tiêu chí gộp của suy tim xấu đi (được định nghĩa là nhập viện ngoài kế hoạch do suy tim hoặc thăm khám khẩn cấp do suy tim) hoặc tử vong do tim mạch. Tiêu chí phụ là tổng biến cố suy tim xấu đi và tử vong do tim mạch, thay đổi triệu chứng so với mức nền vào dựa trên bảng đánh giá chất lượng sống của bệnh nhân suy tim KCCQ (Kansas City Cardiomyopathy Questionnaire, điểm số dao động từ 0 đến 100, với điểm số cao hơn cho thấy ít triệu chứng và ít hạn chế về thể chất hơn) tại tháng thứ 8, tử vong do tim mạch và tử vong do mọi nguyên nhân. Tất cả các biến cố suy tim xấu đi và tử vong đều được xem xét theo tiêu chí đã được định trước bởi ủy ban biến cố lâm sàng độc lập mà các thành viên của ủy ban không biết về sự phân chia trong thử nghiệm. Với mục đích làm sáng tỏ về tính an toàn của dapagliflozin, chỉ thu thập dữ liệu về biến cố bất lợi nghiêm trọng, biến cố bất lợi dẫn đến sự ngừng dapagliflozin hoặc giả dược, và các biến cố bất lợi được chọn lọc khác.
KẾT QUẢ
Bệnh nhân
Từ ngày 27/8/2018 đến ngày 30/12/2020, tổng cộng 10.418 bệnh nhân đã được sàng lọc tại 353 trung tâm ở 20 quốc gia; trong số những bệnh nhân này, 6263 người được phân ngẫu nhiên. Các đặc điểm nhân khẩu học và lâm sàng cân bằng giữa hai nhóm dapagliflozin và giả dược (Bảng 1). Có 444 bệnh nhân (14,2%) ngừng sử dụng dapagliflozin và 442 bệnh nhân (14,1%) ngừng sử dụng giả dược vì những lý do khác hơn là tử vong. Thời gian theo dõi trung vị là 2,3 năm (khoảng tứ phân vị là 1,7 đến 2,8).
Bảng 1. Đặc điểm các bệnh nhân tại thời điểm nhận vào nghiên cứu*
| Đặc điểm | Dapagliflozin
(N = 3131) |
Giả dược
( N = 3132) |
| Tuổi – năm | 71,8±9,6 | 71,5±9,5 |
| Nữ – n (%) | 1364 (43,6) | 1383 (44,2) |
| Chủng tộc – n (%)† | ||
| Châu Á | 630 (20,1) | 644 (20,6) |
| Da đen | 81 (2,6) | 78 (2,5) |
| Da Trắng | 2214 (70,7) | 2225 (71,0) |
| Khác | 206 (6,6) | 185 (5,9) |
| Khu vực địa lý – n (%) | ||
| Bắc Mỹ | 428 (13,7) | 423 (13,5) |
| Mỹ Latin | 602 (19,2) | 579 (18,5) |
| Châu Âu hoặc Ả Rập Saudi | 1494 (47,7) | 1511 (48,2) |
| Châu Á | 607 (19,4) | 619 (19,8) |
| Phân loại NYHA – n (%)‡ | ||
| II | 2314 (73,9) | 2399 (76,6) |
| III | 807 (25,8) | 724 (23,1) |
| IV | 10 (0,3) | 8 (0,3) |
| PSTM thất trái | ||
| Trung bình – % | 54,0±8,6 | 54,3±8,9 |
| Phân nhóm – n (%) | ||
| ≤49% | 1067 (34,1) | 1049 (33,5) |
| 50 – 59% | 1133 (36,2) | 1123 (35,9) |
| ≥60% | 931 (29,7) | 960 (30,7) |
| Tiền sử – n (%) | ||
| ĐTĐ týp 2 | 1401 (44,7) | 1405 (44,9) |
| Tăng huyết áp | 2755 (88,0) | 2798 (89,3) |
| PSTM thất trái trước đây ≤40% | 572 (18,3) | 579 (18,5) |
| eGFR – ml/phút/1,73 m2 | 61±19 | 61±19 |
* Giá trị cộng trừ có nghĩa là ±SD. Tỷ lệ phần trăm tổng cộng có thể không là 100% do làm tròn. eGFR biểu thị độ lọc cầu thận ước tính. † Chủng tộc được báo cáo bởi các nghiên cứu viên. ‡ Một bệnh nhân ở nhóm giả dược có NYHA loại I tại đầu vào và không được bao gồm trong phân tích biến số này.
Hiệu lực
Trong dân số chung, tiêu chí chính xảy ra trên 512 bệnh nhân (16,4%) ở nhóm dapagliflozin và 610 bệnh nhân (19,5%) ở nhóm giả dược (tỷ số nguy cơ HR 0,82; KTC 95%: 0,73 – 0,92; P <0.001) (Bảng 2 và Hình 1A). Kết quả phân tích tiêu chí chính trên bệnh nhân có PSTM thất trái dưới 60% tương tự như kết quả trên dân số chung (HR 0,83; KTC 95%: 0,73 – 0,95; P = 0,009).
Bảng 2. Kết quả tiêu chí chính, tiêu chí thứ phát và tiêu chí an toàn trên dân số chung*
| Biến số | Dapagliflozin (N = 3131) | Giả dược (N = 3132) | Hazard Ratio hoặc Rate Ratio hoặc Win Ratio
(KTC 95%) |
P | ||
| Giá trị | Biến cố/100 bệnh nhân-năm | Giá trị | Biến cố/100 bệnh nhân-năm | |||
| Tiêu chí hiệu quả | ||||||
| Tiêu chí chính – n (%) | 512 (16,4) | 7,8 | 610 (19,5) | 9,6 | 0,82 (0,73–0,92) | <0,001 |
| Nhập viện vì suy tim hoặc thăm khám khẩn cấp vì suy tim | 368 (11,8) | 5,6 | 455 (14,5) | 7,2 | 0,79 (0,69–0,91) | NA |
| Nhập viện vì suy tim | 329 (10,5) | 5,0 | 418 (13,3) | 6,5 | 0,77 (0,67–0,89) | NA |
| Thăm khám khẩn cấp vì suy tim | 60 (1,9) | 0,9 | 78 (2,5) | 1,1 | 0,76 (0,55–1,07) | NA |
| Tử vong do tim mạch | 231 (7,4) | 3,3 | 261 (8,3) | 3,8 | 0,88 (0,74–1,05) | NA |
| Tiêu chí phụ | ||||||
| Tổng biến cố suy tim xấu đi và tử vong do tim mạch | 815 | 11,8 | 1057 | 15,3 | 0,77 (0,67–0,89) | <0,001 |
| Thay đổi tổng điểm triệu chứng KCCQ tại tháng thứ 8 | — | — | — | — | 1,11 (1,03–1,21) | 0.009 |
| Thay đổi trung bình tổng điểm triệu chứng KCCQ tại tháng thứ 8 trên bệnh nhân sống sót | — | — | — | — | 2,4 (1,5–3,4) | NA |
| Tử vong do mọi nguyên nhân – n (%) | 497 (15,9) | 7,2 | 526 (16,8) | 7,6 | 0,94 (0,83–1,07) | NA |
| Tiêu chí an toàn – số biến cố/ tổng biến cố (%) | ||||||
| Bất kỳ biến cố bất lợi nào | 1361/3126 (43,5) | — | 1423/3127 45,5) | — | — | — |
| Bất kỳ biến cố bất lợi dẫn đến ngưng dapagliflozin hoặc giả dược | 182/3126 (5,8) | — | 181/3127 (5,8) | — | — | — |
| Bất kỳ biến cố bất lợi dẫn đến gián đoạn dapagliflozin hoặc giả dược | 436/3126 (13,9) | — | 494/3127 (15,8) | — | — | — |
| Bất kỳ biến cố cắt cụt chi nào | 19/3126 (0,6) | — | 25/3127 (0,8) | — | — | — |
| Bất kỳ biến cố bất lợi dẫn đến nguy cơ cắt cụt chi dưới | 188/3126 (6,0) | — | 199/3127 (6,4) | — | — | — |
| Bất kỳ biến cố nhiễm toan ceton đái tháo đường được xác định hoặc có thể | 2/3126 (0,1) | — | 0 | — | — | — |
| Bất kỳ biến cố hạ đường huyết lớn nào | 6/3126 (0,2) | — | 7/3127 (0,2) | — | — | — |
| Bất kỳ biến cố bất lợi hay nghiêm trọng nào dẫn đến ngưng dapagliflozin hoặc giả dược được gợi ý do giảm thể tích | 42/3126 (1,3) | — | 32/3127 (1,0) | — | — | — |
| Bất kỳ biến cố bất lợi hay nghiêm trọng nào ở thận dẫn đến ngừng dapagliflozin hoặc giả dược | 73/3126 (2,3) | — | 79/3127 (2,5) | — | — | — |
| Hoại thư Fournier | 0 | — | 0 | — | — | — |
*Tất cả tiêu chí điều trị hiển thị dưới dạng HR, ngoại trừ tổng số ca nhập viện vì suy tim và tử vong do tim mạch, được báo cáo là RR và sự thay đổi về KCCQ là WR. NA biểu thị không áp dụng.
Số ca tử vong do tim mạch và biến cố suy tim xấu đi lần đầu tiên và tái phát ở nhóm dapagliflozin thấp hơn so với nhóm giả dược trong dân số chung (HR 0,77; KTC 95%: 0,67 – 0,89; P <0,001) và trên bệnh nhân có PSTM dưới 60% (HR 0,77; KTC 95%: 0,65 – 0,90; P = 0,002). Tần suất mới xuất hiện của các biến cố thuộc tiêu chí chính ủng hộ nhóm dapagliflozin trên cả dân số chung và trên bệnh nhân có PSTM dưới 60%, bao gồm suy tim xấu đi (HR trên dân số chung là 0,79; KTC 95%: 0,69 – 0,91) và tử vong do tim mạch (HR 0,88; KTC 95%: 0,74 – 1,05) (Hình 1B và 1C), cũng như tử vong do mọi nguyên nhân (HR 0,94; KTC 95%: 0,83 – 1,07) (Hình 1D). Sự thay đổi điểm KCCQ tại tháng thứ 8 so với đầu vào cho thấy lợi ích của dapagliflozin so với giả dược về cải thiện các triệu chứng suy tim (tỷ số thành công [win ratio] là 1,11; KTC 95%: 1,03 – 1,21; P = 0,009; sự khác biệt trung bình có hiệu chỉnh với giả dược giữa thi điểm lúc đầu vào và tại thời điểm tháng thứ 8 là 2,4 điểm; KTC 95%: 1,5 – 3,4).
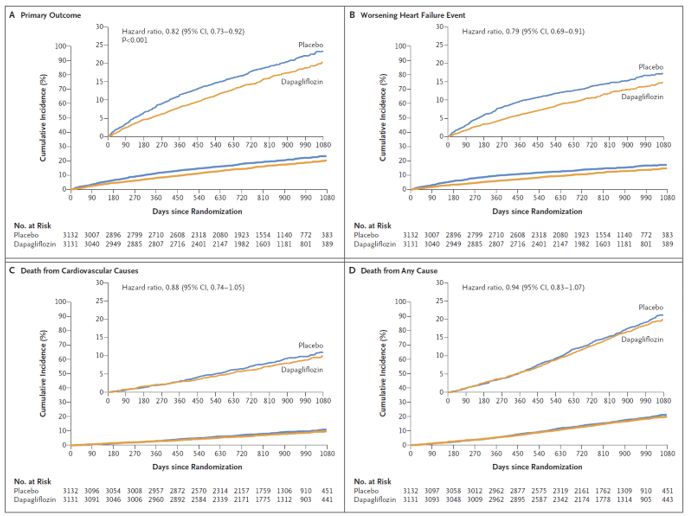
Hình 1. Kết quả trên dân số chung (Hình chụp từ tài liệu gốc)
Kết quả tiêu chí chính (Hình A), các tiêu chí thành phần của tiêu chí chính (suy tim xấu đi [Hình B], tử vong do tim mạch [Hình C]), tử vong mọi nguyên nhân (Hình D).
Tác dụng của dapagliflozin về tiêu chí chính đồng nhất trên tất cả các phân nhóm được xác định trước, bao gồm có hay không mắc kèm ĐTĐ týp 2; thời điểm thu dung có trong 30 ngày sau khi nhập viện do suy tim hay không; có PSTM thất trái cải thiện hay không (Hình 2). Phân tích độ nhạy với COVID-19 được định trước, trong đó dữ liệu bệnh nhân đã được kiểm duyệt tại thời điểm chẩn đoán COVID-19 cho thấy kết quả tương tự. Kết quả tổng thể cũng tương tự khi tử vong không phải do nguyên nhân tim mạch được tính đến như một nguy cơ cạnh tranh (tỷ số nguy cơ SHR (subdistribution Hazard Ratio) 0,82; KTC 95%: 0,73 – 0,92).
Tính an toàn
Nhìn chung, các biến cố bất lợi nghiêm trọng, bao gồm tử vong, được báo cáo trên 1361 bệnh nhân (43,5%) ở nhóm dapagliflozin và 1423 bệnh nhân (45,5%) ở nhóm giả dược (Bảng 2). Biến cố bất lợi dẫn đến việc ngừng dapagliflozin hoặc giả dược được báo cáo ở 182 bệnh nhân (5,8%) ở nhóm dapagliflozin và 181 bệnh nhân (5,8%) ở nhóm giả dược.
BÀN LUẬN
Trong thử nghiệm ngẫu nhiên, đối chứng giả dược bao gồm các bệnh nhân suy tim có phân suất tống máu giảm nhẹ hoặc bảo tồn, dapagliflozin làm giảm nguy cơ của tiêu chí chính, gộp của suy tim xấu đi hoặc tử vong do tim mạch, so với giả dược, với lợi ích không có sự khác biệt giữa bệnh nhân có PSTM thất trái ≥60% và bệnh nhân có PSTM thất trái <60% hoặc trên các phân nhóm khác. Các tiêu chí thành phần của tiêu chí gộp ít xảy ra trên nhóm dapagliflozin so với nhóm giả dược. Hơn nữa, dapagliflozin làm giảm tổng biến cố suy tim và tử vong do tim mạch và có gánh nặng triệu chứng thấp hơn so với giả dược. Tần suất các biến cố bất lợi tương tự như nhóm giả dược.
Trong một thử nghiệm trước đó (DAPA-HF Dapagliflozin và phòng ngừa các kết quả bất lợi trên suy tim), dapagliflozin làm giảm nguy cơ suy tim xấu đi hoặc tử vong do tim mạch trên bệnh nhân suy tim có PSTM thất trái ≤40%. Kết quả của thử nghiệm DELIVER mở rộng kết quả của thử nghiệm DAPA-HF cho bệnh nhân suy tim có PSTM >40% và phù hợp với kết quả chung của thử nghiệm EMPEROR-Preserved (Empagliflozin trên bệnh nhân suy tim mạn tính với PSTM bảo tồn), đánh giá tác dụng của empagliflozin trên bệnh nhân có PSTM thất trái >40%. Mặc dù thử nghiệm EMPEROR- Preserved cho thấy sự suy giảm lợi ích ở những bệnh nhân có PSTM thất trái cao nhưng thử nghiệm DELIVER không ghi nhận bằng chứng nào về sự không đồng nhất hiệu quả trên phổ PSTM. Trong thử nghiệm DELIVER, hiệu quả điều trị là như nhau trên bệnh nhân PSTM ≥60% và bệnh nhân có PSTM <60%. Phát hiện này cho thấy rằng lợi ích của việc ức chế SGLT2 có khả năng mở rộng trong toàn bộ phổ phân suất tống máu.
Thử nghiệm DELIVER được thiết kế với các tiêu chí tuyển chọn rộng hơn so với các thử nghiệm tương tự trước đây, DELIVER đã thu nhận những bệnh nhân đang nằm viện hoặc nhập viện gần đây – nhóm bệnh nhân hiện bị hạn chế về các liệu pháp điều trị, cũng như những bệnh nhân có PSTM thất trái cải thiện. Dữ liệu từ DELIVER cho thấy các nhóm bệnh nhân này cũng được hưởng lợi từ dapagliflozin. Các hướng dẫn gần đây nhất của Hiệp hội Tim Hoa Kỳ (AHA), Hiệp Hội Tim mạch Hoa Kỳ (ACC) và Hiệp hội Suy tim Hoa Kỳ (HFSA) khuyến cáo thuốc ức chế SGLT2 nhóm IIA, mức độ B, để điều trị suy tim PSTM giảm nhẹ hoặc bảo tồn. Kết quả của thử nghiệm DELIVER có thể dẫn đến thay đổi các hướng dẫn trong tương lai và cung cấp thêm bằng chứng để sử dụng rộng rãi hơn trong thực hành lâm sàng.
Thử nghiệm này có một số hạn chế. Việc sử dụng các tiêu chí tuyển chọn và loại trừ có thể đã hạn chế tính phổ quát của kết quả. Ít hơn 5% bệnh nhân đăng ký tham gia là người da đen. Do đại dịch COVID-19, việc đánh giá tại thời điểm 8 tháng về gánh nặng triệu chứng chỉ giới hạn ở bệnh nhân đã có kế hoạch đánh giá trước ngày 11 tháng 3 năm 2020, mặc dù kết quả giống nhau ở tất cả các bệnh nhân có sẵn dữ liệu. Bởi vì tất cả các phân nhóm trong thử nghiệm DELIVER đều không đủ độ mạnh, các kết quả từ các phân nhóm cần được diễn giải một cách thận trọng.
Cảm ơn AstraZeneca đã hỗ trợ nhằm mục đích cập nhật và giáo dục y khoa.
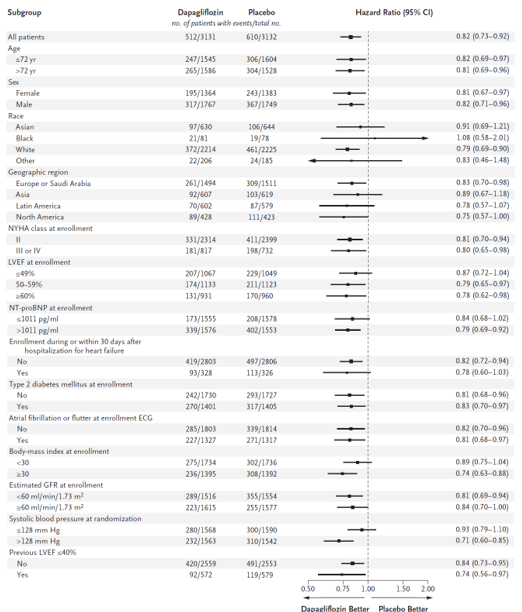
Hình 2: Kết quả tiêu chí chính trên các phân nhóm (Hình chụp từ tài liệu gốc)
TÀI LIỆU THAM KHẢO
S.D. Solomon, J.J.V. McMurray, et al. (2022), “Dapagliflozin in Heart Failure with Mildly Reduced or Preserved Ejection Fraction”, The New England Journal of Medicine, DOI: 10.1056/NEJMoa2206286.







