BS. TRƯƠNG NGỌC KHÔI NGUYÊN*
BS. NGUYỄN THANH HIỀN
*Khoa Tim mạch can thiệp, BV Đại học Y Dược TP. Hồ Chí Minh
Mở đầu
Phân suất tống máu (ejection fraction, EF) là thông số được sử dụng thông dụng nhất trong đánh giá và phân loại chức năng tâm thu. Thông thường, trong thực hành lâm sàng, phân suất tống máu được chấp nhận là bình thường nếu nằm trong khoảng 50-55%[1]. Suy tim được phân loại theo phân suất tống máu thất trái (left ventricular ejection fraction, LVEF) thành các nhóm như sau: suy tim với phân suất tống máu giảm (LVEF < 40%), suy tim với phân suất tống máu giảm nhẹ (LVEF 41-49%), và suy tim với phân suất tống máu bảo tồn (LVEF 50-65%). Sự xuất hiện của phân loại thứ tư, cụ thể là suy tim với phân suất tống máutrên mức bình thường (LVEF >65%), được đề xuất do nhóm này có tồn tại các cơ chế sinh lý bệnh học và nền tảng di truyền riêng biệt. Có ý kiến cho rằng không nên bao gồm nhóm suy tim có phân suất tống máu trên mức bình thường bên trong nhóm suy tim với phân suất tống máu bảo tồn do nhiều nghiên cứu gần đây cho thấy, sự tương quan giữa chỉ số EF và tỷ lệ rủi ro (hazard ratio) được phân bố theo hình dạng chữ U (Hình 1) [2].
Thuật ngữ
Theo cơ sở dữ liệu DIGITALIS, tỷ lệ suy tim được phân loại theo phân suất tống máu như sau: suy tim với phân suất tống máu giảm (HFrEF) chiếm 19%, suy tim với phân suất tống máu trung gian (HFmrEF) chiếm 22%, và suy tim phân suất tống máu bảo tồn (HFpEF) chiếm 59 %. Các báo cáo này cho thấy HFpEF chiếm một tỷ lệ đáng kể trong các trường hợp suy tim [3].Năm 2019, một nghiên cứu công bố trên tạp chí European Heart Journal đã trình bày dữ liệu đề cập đến một kiểu hình suy tim mới được đặc trưng bởi LVEF trên mức bình thường (EF ≥ 65%).
Mối quan hệ giữa tỷ lệ tử vong và LVEF phân bố theo hình dạng chữ U, việc gộp tất cả bệnh nhân HFpEF thành duy nhất một nhóm chưa được coi là thật sự đầy đủ.[3] Chẩn đoán suy tim với phân suất tống máu trên mức bình thường (heart failure with supranormal ejection fraction hay HFsnEF) cần có các triệu chứng suy tim, tăng nồng độ B-type natriuretic peptide trong máu, và dấu hiệu chức năng tâm thu thất trái bình thường đi kèm với rối loạn chức năng tâm trương hoặc kèm các dấu hiệu thay thế như phì đại thất trái, lớn nhĩ trái và rung nhĩ (tham khảo Bảng 1)[3]. Ngưỡng EF > 65% được chọn bởi hai lý do. Thứ nhất, hiệu quả điều trị của empagliflozin trong thử nghiệm EMPEROR-Preserve nhất quán trên toàn bộ phổ LVEF; tuy nhiên, hiệu quả bị giảm đi ở những người có LVEF vượt quá 65%[4, 5].Thứ hai, một nghiên cứu quan sát toàn diện bao gồm tất cả những người tham gia có kết quả siêu âm tim đã chứng minh rằng những người có LVEF > 65% có nguy cơ tử vong cao hơn so với những người có LVEFdao động từ 55-65%, bất kể tuổi tác và giới tính[6].
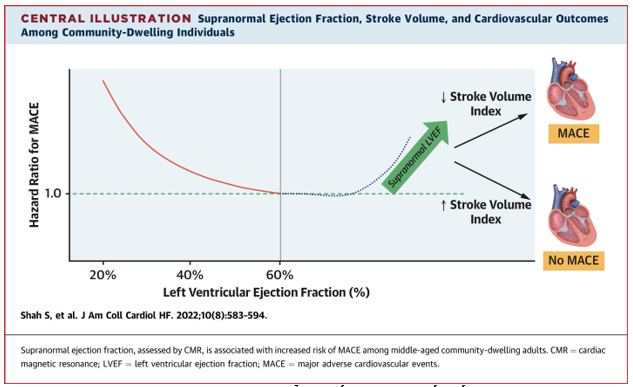
Hình 1. Liên quan EF trên bình thường, thể tích tống máu và biến cố tim mạch chính. (2)
Các nghiên cứu gần đây về suy tim phân suất tống máu trên mức bình thường (EFsnEF)
Một nghiên cứu cộng đồng bao gồm những người tham gia khỏe mạnh, không mắc bệnh tim mạch của 2 nghiên cứu: nghiên cứu MESA (Multi-Ethnic Study of Atherosclerosis) và nghiên cứu DHS (Dallas Heart Study) đãđược tiến hành, nhằm đánh giá mối liên quan giữa các nhóm phân suất tống máu trên mức bình thường vớicác biến cố tim mạch nặng (major adverse cardiovascular events hay MACE)[2].Trong nghiên cứu này, EF được đánh giá bằng phương pháp chụp cộng hưởng từ tim (CMR), cũng là tiêu chuẩn vàng trong đánh giá phân suất tống máu. Kết cục tổng hợp của MACE bao gồm: tử vong do nguyên nhân tim mạch, nhồi máu cơ tim không tử vong, đột quỵ, nhập viện do suy tim cấp tính và rung nhĩ. Tuy nhiên, tiêu chí của kết cục MACE này không bao gồm nhanh thất gây tử vong, rung thất, đột tử do tim hoặc rối loạn nhịp thất không gây tử vong[2]. Những người tham gia có EF vượt quá ngưỡng bình thường, tức EF lớn hơn 57% được đưa vào nghiên cứu. Sau khoảng thời gian theo dõi trung bình là 12 năm trong nhóm MESA và 11 năm trong nhóm DHS, người ta đã quan sát thấy rằng những người ở nhóm tứ phân vị LVEF cao nhất có nguy cơ MACE cao nhất so với những người ở nhóm tứ phân vị thấp hơn. Mối quan hệ này độc lập với các yếu tố nguy cơ tim mạch khác và các biến số gây nhiễu tiềm ẩn[2]. Phân tích nhóm cá thể có EF trên mức bình thườngtrong nhóm tứ phân vị cao cho thấy tỷ lệ người da trắng cao hơn, nhiều triệu chứng suy tim hơn, huyết áp tâm thu cao hơn, tỷ lệ sử dụng thuốc hạ huyết áp nhiều hơn, tỷ lệ hút thuốc lá ít hơn, tần số tim cao hơn và chỉ số calcium score cao hơn [2]. Mức NT-proBNPở những người trong nhómtứ phân vị có EF càng cao tăng đáng kể so với nhóm tứ phân vị thấp hơn trong đoàn hệ MESA, nhưng không có sự khác biệt đáng kể trong đoàn hệ DHS. So với nhóm tứ phân vị có EF trên mức bình thường ở ngưỡng thấp hơn,nhóm tứ phân vị EF cao hơn có chỉ số khối thất trái (LV mass index) thấp hơn, chỉ số thể tích cuối tâm trương thất trái(LV end diastolic volume index) và chỉ số thể tích cuối tâm thu thất trái (LV end systolic volume index) thấp hơn. Tuy nhiên, nhóm tứ phân vị EF cao hơncó chỉ số thể tích nhát bóp thất trái (LV stroke volume index) và chỉ số tim (cardiac index) cao hơn[2]. Trong quá trình tiếp tục theo dõi, các cá thể trải qua biến cố tim không thuận lợi là các cá thể có khối lượng cơ thất trái cao, độ dày của thành thất trái tăng và nồng độ NT-proBNP và troponin T hs tăng[2, 5].Cụ thể, LVEF càng cao có sự liên quan đáng kể với việc tăng nguy cơMACE ở những người có chỉ số thể tích nhát bóp thấp, nhưng không phải ở những người có chỉ số thể tích nhát bóp cao[2]. Nghiên cứu này có kích thước mẫu lớn và bao gồm các nhóm tham gia từ cộng đồng trong trạng thái khỏe mạnh. Tuy nhiên, các yếu tố gây nhiễu vẫn còn là một hạn chế. Việc loại trừ những bệnh nhân mắc bệnh tim mạch chỉ dựa trên cơ sở dữ liệu tự báo cáo có thể dẫn đến việc bỏ sót bệnh amyloidosis tim hoặc bệnh cơ tim phì đại dưới lâm sàng [2].
Thử nghiệm RELAX-AHF-2 là một thử nghiệm lâm sàng ngẫu nhiên, đa trung tâm nhằm đánh giá tác động của serelexin so với giả dược ở những bệnh nhân nhập viện do suy tim cấp tính[6]. Nghiên cứu đã cho thấy rằng, trong các nhóm phân loại LVEF càng cao thì tuổi và tỷ lệ phụ nữ cũng tăng lên. Ngoài ra, so với HFpEF, HFsnEF có tỷ lệ tử vong không do tim mạch cao hơn. Trong nghiên cứu này, LVEF > 65% có liên quan đến kết cục không thuận lợi ở những người tham gia là nữ. Tỷ lệtim có kích thước nhỏ ở nữ cao gấp đôi nam. Phụ nữ có xu hướng có chỉ số thể tích thất trái cuối tâm trương (LVEDV index) và thể tích thất trái cuối tâm trương (LVEDV) nhỏ hơn so với nam giới. Khi thất trái bị giảm kích thước,để tạo ra cung lượng tim đầy đủ,tim phải tăng phân suất tống máu hoặc nhịp tim, do đó dẫn đến mức tiêu thụ oxy nhiều hơn (Hình 2) [6,7].
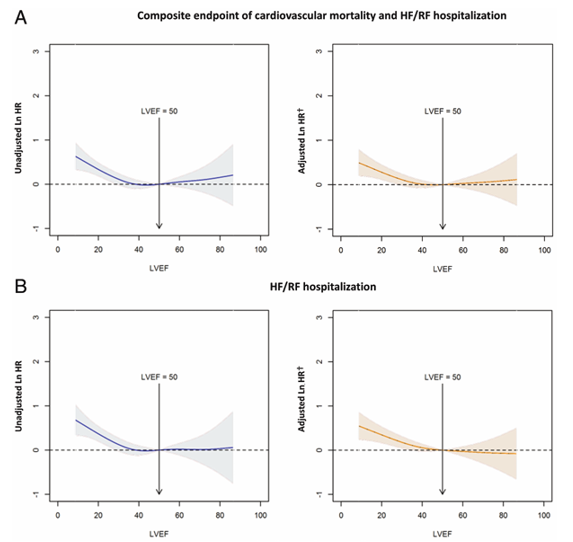

Hình 2. Các hình thái kết cục lâm sàng điều chỉnh theo các biến số. các hình thái kết cục có và không điều chỉnh theo các biến ban đầu với liên quan giửa LVEF và sau theo dõi 180 ngày: (A) tiêu chí gộp tử vong tim mạch và nhập viện suy tim/suy thận, (B) nhập viện vì suy tim/suy thận, (C) tử vong tim mạch, và (D) tử vong mọi nguyên nhân.
HR, tỉ số chênh.
† tiêu chí gộp và tái nhập viện do suy tim/suy thận ở thời điểm 180 ngay (n=4939) được điều chỉnh theo: điều trị hiện tại của nghiên cứu, tuổi, hen/COPD, rung nhĩ/flutter nhĩ, BUN, creatinin, phù, trầm cảm, Haemoglobin, tai biến mạch máu não, NT-proBNP, tổng liều lasix tĩnh mạch lúc ban đầu, tiền sử đái tháo đường, bệnh tắc nghẽn mạch máu ngoại biên, nhập viện suy tim trước đây, HA .
‡ tử vong tim mạch và tử vong mọi nguyên nhân được điều chỉnh theo: điều trị hiện tại của nghiên cứu, tuổi, hen/COPD, rung nhĩ/flutter nhĩ, BUN, creatinin, phù, BMI, Haemoglobin, tai biến mạch máu não, NT-proBNP, tổng liều lasix tĩnh mạch lúc ban đầu, tiền sử đái tháo đường, bệnh tắc nghẽn mạch máu ngoại biên, nhập viện suy tim trước đây, mạch, nhịp thở, giới, natri máu, HA (7).
Nền tảng di truyền của nhóm bệnh nhân có phân suất tống máu thất trái trên mức bình thường (snLVEF) đã được xác định thông qua các nghiên cứu kết hợp trên toàn bộ bộ gen (genome-wide association studies hay GWAS) được thực hiện trên hai nhóm dân số rất lớn, đó là Ngân hàng sinh học Vương quốc Anh (UK Biobank), bao gồm chủ yếu là các tình nguyện viên khỏe mạnh, và BioMe Biobank, bao gồm chủ yếu là bệnh nhân ngoại trú[4]. Trước đây, GWAS đã xác định thành công các locus có nguy cơ di truyền đáng kể liên quan đến một số bệnh tim mạch, bao gồm HFrEF[5]. GWAS đã xác định được 386 SNP có liên hệ đáng kể với snLVEF, trong đó có 16 SNP độc lập có liên hệ với snLVEF. Những SNP này được tích hợp vào thang điểm nguy cơ di truyền (genetic risk score, GRS)[4].Nghiên cứu còn xác định được cụ thể locus SEC23IP A và XKR6, vốn trước đây không được báo cáo trong các bệnh lý tim mạch khác[4]. Hệ số di truyền dựa trên SNP được ước tính là 30%. Kết quả mà GWAS cung cấp đã hỗ trợ mạnh mẽ cho việc thành lập khái niệm rằng snLVEF đại diện cho một dạng bệnh lý tim mạch riêng biệt [4]. Cũng trong nghiên cứu này, các nhà nghiên cứu khám phá được các triệu chứng của suy tim được ghi lại trong hồ sơ y tế điện tử và kết quả là cả snLVEF và snLVEF-GRS đều có liên quan đến các triệu chứng HF và các dấu ấn sinh học suy tim, nhưng không liên quan đến chẩn đoán suy tim. Điều này cho thấy rằng HFsnEFvẫn còn thiếu sự công nhận và chưa được chẩn đoán đầy đủ[4, 5].
Sinh lý bệnh và giải phẫu bệnh
Các bác sĩ lâm sàng thường cho rằng snLVEF không liên quan đến rối loạn tim mạch, nên suy tim với phân suất tống máu trên mức bình thường (HFsnEF) có thể không được chẩn đoán[4]. Thay vào đó, ban đầu, các bác sĩ sẽ đánh giá các dấu hiệu liên quan đến các chẩn đoán khác, bao gồm hở van hai lá, bệnh cơ tim phì đại, bệnh amyloidosis, hẹp van động mạch chủ có chênh áp thấp, tăng huyết áp, tình trạng cung lượng cao hoặc các bệnh lý cấp tính như nhiễm trùng huyết hoặc thiếu máu nặng để chẩn đoán tình trạng của bệnh nhân[4]. Càng ngày càng có nhiều bằng chứng cho thấy những bệnh lý này không liên quan với, hoặc không tương ứng với kiểu hình của snLVEF[4].
Việc thiếu hiểu biết toàn diện về các cơ chế sinh học làm tăng nguy cơ MACE ở những người có EF trên mức bình thường là một vấn đề cần lưu ý. Các bệnh tim mạch đi kèm như tăng huyết áp, bệnh cơ tim phì đại, amyloidosis tim, hẹp van động mạch chủ và hở van hai lá là các yếu tố cơ bản góp phần gây tái cấu trúc thất trái bệnh lý và tăng LVEF[5]. Tăng huyết áp xảy ra phổ biến nhất ở những người có EF trên mức bình thường so với những người có EF bình thường[5].Ngược lại, trong số những người không bị tăng huyết áp hoặc các bệnh đi kèm khác, điểm nguy cơ di truyền (GRS) của snLVEF được cho là có liên quan đến nguy cơ giảm tỷ lệ sống sót[5].
Cần lưu ý rằng có sự thay đổi mối liên hệ (effect modification) đáng kể do ảnh hưởng của chỉ số thể tích nhát bóp LV (LV stroke volume index) [2].LVEF cao hơn có sự tương quan với nguy cơ có kết cục MACE cao hơn chỉ ở những người có chỉ số thể tích nhát bóp thấp[2].Chỉ số thể tích nhát bóp thấpở những cá thể có phân suất tống máu thất trái bảo tồn thường được cho là do giảm kích thước và dày đồng tâm buồng tim [2].Tình trạng nói trên sẽ buộc tim phải co bóp ở mức vượt quá giá trị bình thường trong thời kỳ tâm thu[4].Những thay đổi trong cấu trúc được cho là sẽ làm tăng EF bằng cách rút ngắn và tăng độ dày sợi chéo (cross-fiber), do đó tăng cường tốc độ co bóp của tế bào cơ tim ở lớp nội tâm mạc[2]. Kết quả cuối cùng dẫn đến suy giảm chức năng tâm trương và thư giãn thất trái. Một cách giải thích khả thi cho tình trạng này là những người có cơ tim phì đại sẽ nhạy cảm với thiếu máu cơ tim hơn do tăng nhu cầu oxy bởi nhu cầu trao đổi chất tăng cao[3]. Ở những cá thể suy tim với phân suất tống máu bảo tồn, amyloidosis tim và hẹp van đông mạch chủ có kèm theo thể tích nhát bóp thấp sẽ tăng khả năng gặp phải các biến cố tim mạch bất lợi.
Các con đường nội tiết tố thần kinh được kích hoạt có khả năng đóng vai trò như một cơ chế góp phần vào sự tiến triển của HFsnEF. Việc kích hoạt hệ thống renin-angiotensin-aldosterone (RAAS) có liên quan đến diễn tiến của quá trình tái cấu trúc tim và suy giảm chức năng co bóp[3].Thật vậy, các kết quả nghiên cứu chỉ ra rằng những người có LVEF cao hơn có tuổi cao và LVEDV giảm. Một cơ chế khác được đề xuất là rối loạn chức năng vi mạch vành, có liên quan đến tình trạng tăng co bóp thất trái và tăng hoạt động giao cảm tim. Cơ chế này góp phần làm tăng nguy cơ biến cố tim mạch bất lợi ở những người có snLVEF (hình 3).

Hình 3: Cơ chế sinh lý bệnh của HFsnEF [3]
Các nghiên cứu gần đây đã chứng minh khuynh hướng di truyền đối với EF trên mức bình thường, với khả năng di truyền là 30%dựa trên các SNP liên quan đến các biến thể trong gen gây phì đại tim. Sự di truyền đa gen được khám phá thông qua các nghiên cứu kết hợp trên toàn bộ bộ gen GWAS, vì một SNP chung và duy nhất là không đủ để xác định bệnh lý tim mạch phức tạp. Điểm nguy cơ di truyền (GRS) được tính bằng cách gán điểm cho các SNP sao cho số lượng alene nguy cơ di truyền càng nhiều thì khả năng mắc bệnh càng cao[4].
Chẩn đoán
Theo hướng dẫn ESC về suy tim cấp và mạn, chẩn đoán suy tim cần dựa trên sự kết hợp giữa các triệu chứng, dấu hiệu, tăng natriuretic peptide và kết quả siêu tim. Suy tim với phân suất tống máu trên mức bình thường tức EF ³ 65% là một nhóm suy tim mới được đề suất. Chẩn đoán suy tim với phân suất tống máu trên mức bình thường (HFsnEF) cần có các triệu chứng suy tim, tăng nồng độ B-type natriuretic peptide trong máu,bằng chứng chức năng tâm thu thất trái bình thường và rối loạn chức năng tâm trương hoặc cócác dấu hiệu thay thế như phì đại thất trái, lớn nhĩ trái và rung nhĩ (tham khảo Bảng 1)[3]
Bảng 1. Tiêu chuẩn lâm sàng chẩn đoán HFsnEF[3]
| Loại | Tiêu chuẩn |
| Triệu chứng và/ hoặc dấu hiệu suy tim | Khó thở, khó thở kịch phát về đêm, giảm khả năng gắng sức, mệt mỏi, uể oải, phù chân |
| Tăng áp lực tĩnh mạch cảnh, phản hồi gan tĩnh mạch cảnh, gallop T3, mỏm tim lệch trái | |
| Phân suất tống máu thất trái | LVEF ³ 65% |
| Tăng natriuretic peptide | BNP > 35 pg/mL
và/ hoặc NT-proBNP > 125 pg/mL |
| Bằng chứng về rối loạn chức năng và cấu trúc tim có gây suy tim | Chỉ số thể tích nhĩ trái (left atrial volume index LAVI), chỉ số khối thất trái (LV mass index), E/e’, trung bình e’ vách và thành bên, strain thất trái hoặc vận tốc hở van (TRV) |
| Test gắng sức hoặc tăng áp lực đổ đầy thất trái được đánh giá bằng phương pháp xâm lấn | Test gắng sức tâm trương bằng siêu âm tim, áp lực mao mạch phổi bít (PCWP), áp lực cuối tâm trưông thất trái (LVEDP) |
Điều trị
Nền tảng của phương pháp điều trị truyền thống đối với bệnh suy tim (HF) với phân suất tống máu giảm (HFrEF; phân suất tống máu thất trái [LVEF] < 40%) là sự kết hợp của thuốc chẹn beta (BB), thuốc ức chế men chuyển hoặc thuốc ức chế thụ thể angiotensin và thuốc mineralocorticoid. Những tiến bộ gần đây trong điều trị HFrEF bao gồm việc bổ sung chất ức chế thụ thể angiotensin-neprilysin (ARNI) và chất ức chế chất vận chuyển natri-glucose 2 (SGLT2i). Tác dụng có lợi của ARB, BB và MRA cũng được chứng minh trong điều trị suy tim với phân suất tống máu giảm nhẹ (HFmrEF; LVEF 40–49%). Tuy nhiên, ở những bệnh nhân suy tim và phân suất tống máu bảo tồn (HFpEF; LVEF >50%) chỉ có SGLT2i được chứng minh là có lợi. Tuy nhiên, trong một nhóm bệnh nhân suy tim với là phân suất tống máu ‘trên mức bình thường’ (HFsnEF; LVEF >65%), các nhóm thuốc nói trên dường như không có tác động đáng kể nào trong việc giảm tỷ lệ tử vong hoặc bệnh tật[6,8].
Dựa trên sinh lý bệnh học của HFsnEF, việc sử dụng thuốc chẹn beta trong điều trị HFsnEF có thể có lợi do tác dụng làm chậm nhịp tim của chúng, có thể kéo dài thời gian đổ đầy tâm trương và tăng cường cung cấp oxy cho cơ tim[3].ACEis, ARBs, spironolactone đã được chứng minh là có khả năng làm chậm quá trình tái cấu trúc. Tuy nhiên, hiện chưa có các thử nghiệm nào đánh giá tác dụng của chúng cụ thể trên nhóm bệnh nhân HFsnEF. Các nghiên cứu tiến cứu và thử nghiệm lâm sàng là cần thiết để xác nhận hiệu quả lâm sàng của tất cả các loại thuốc[3].
Triển vọng tương lai
Sau khi nhóm phân loại suy tim mới được đề suất, trong tương lai có thể sẽ có nhiều nghiên cứu hơn nhằm đánh giá hiệu quả điều trị thuốc trên nhóm suy tim phân suất tống máu trên mức bình thường. Ức chế men chuyển hoặc ức chế thụ thể có thể là phương pháp điều trị hứa hẹn cho HFsnEF.
Kết luận
Các nghiên cứu hiện tại cho thấy rằng HFsnEF có các biểu hiện lâm sàng khác biệt có thể làm tăng nguy cơ tử vong do mọi nguyên nhân so với những bệnh nhân HFpEF khác.
- Marwick, T.H., Ejection fraction pros and cons: JACC state-of-the-art review. Journal of the American College of Cardiology, 2018. 72(19): p. 2360-2379.
- Shah, S., et al., Supranormal left ventricular ejection fraction, stroke volume, and cardiovascular risk: findings from population-based cohort studies. Heart Failure, 2022. 10(8): p. 583-594.
- Huang, Z., Y. Jiang, and Y. Zhou, Heart Failure with Supra-normal Left Ventricular Ejection Fraction–State of the Art. Arquivos Brasileiros de Cardiologia, 2021. 116: p. 1019-1022.
- Sinagra, G., A. Paldino, and M. Dal Ferro, Heart failure with supra‐normal left ventricular ejection fraction: distinct polygenic bases of an unrecognized phenotype. 2022, Wiley Online Library. p. 2128-2130.
- Forrest, I.S., et al., Genetic and phenotypic profiling of supranormal ejection fraction reveals decreased survival and underdiagnosed heart failure. European Journal of Heart Failure, 2022.
- Van Essen, B.J., et al., Characteristics and clinical outcomes of patients with acute heart failure with a supranormal left ventricular ejection fraction. European Journal of Heart Failure, 2023. 25(1): p. 35-42.
- Janwanishstaporn. S et al. Relationship between left ventricular ejection fraction and cardiovascular out comes following hospital ization for heart failure insights from the RELAX-AHF-2 trial. EuropeanJournalofHeartFailure (2020)22,726–738.
- Gu Jun et al. Characteristics, prognosis, and treatment response in HFpEF patients with high vs. normal ejection fraction. Front. Cardiovasc. Med. Volume 9 – 2022. https://doi.org/10.3389/fcvm.2022.944441







