1. Mở đầu
Các khuyến cáo được liệt kê trong hướng dẫn thực hành lâm sàng này, được dựa trên cơ sở bằng chứng được đưa ra bất cứ khi nào có thể.
TS PHẠM HỮU VĂN
Một nghiên cứu ban đầu bao gồm các tài liệu có nguồn gốc từ các nghiên cứu liên quan đến con người, được xuất bản bằng tiếng Anh và được lập chỉ mục trong MEDLINE (thông qua PubMed), EMBASE, Thư viện Cochrane, Cơ quan Nghiên cứu và Chất lượng Y tế và các cơ sở dữ liệu được lựa chọn khác có liên quan đến được thực hiện từ tháng 4 năm 2016 đến tháng 9 năm 2016. Các từ tìm kiếm chính gồm, nhưng không giới hạn, những điểm sau: đột tử tim (SCD), nhịp nhanh thất (VT), rung thất (VF), các co bóp thất sớm (PVC), máy khử rung tim có thể cấy, áo khử rung tim có thể mặc và triệt phá qua catheter (catheter ablation). Các nghiên cứu bổ sung có liên quan được công bố vào tháng 3 năm 2017, trong quá trình soạn thảo hướng dẫn, cũng đã xem xét các bản soạn thảo và thêm vào các bảng bằng chứng khi thích hợp.
Các bảng bằng chứng cuối cùng được đưa vào phần Bổ sung Dữ liệu Trực tuyến (http://circ.ahajournals.org/lookup/suppl/doi:10.1161/CIR.0000000000000549/-/DC2) và tóm tắt các bằng chứng được sử dụng các ban soạn thảo để xây dựng các khuyến cáo. Ngoài ra, ủy ban biên soạn đã xem xét các tài liệu liên quan đến loạn nhịp thất và đột tử (SCD) trước đây do ACC, AHA và Hội Nhịp tim (HRS) xuất bản. Tài liệu tham khảo được lựa chọn và xuất bản trong tài liệu này là đại diện và không bao gồm tất cả.
Chúng tôi tóm tắt toàn văn Hướng dẫn này và xin trân trọng giới thiệu với các đồng nghiệp trong nhiều kỳ của Chuyên đề Tim Mạch Học.
2. Dịch tễ học
2.1.Các khái niệm chung
Rối loạn nhịp thất (VA) ở bảng 5 gồm một phổ phạm vi từ phức bộ thất sớm (PVC) đến rung thất (VF), có biểu hiện lâm sàng phạm vi từ hoàn toàn không có triệu chứng đến ngừng tim. VA nguy hiểm đến tính mạng nhất đươc kết hợp với bệnh tim thiếu máu cục bộ, đặc biệt ở người lớn tuổi (1). Nguy cơ của VA và SCD thay đổi ở các quần thể cụ thể với các trạng thái tim nền khác nhau và với bệnh sử gia đình và các biến thể di truyền chuyên biệt, các biến thể này có ý nghĩa quan trọng cho việc nghiên cứu và áp dụng điều trị.
Bảng 5.Bảng các khái niệm của các thuật ngữ được sử dụng chung trong tư liệu này
|
Thuật ngữ |
Khái niệm hoặc mô tả |
|
Nhịp nhanh thất (2) |
Rối loạn nhịp tim với ≥ 3 phức hợp liên tiếp có nguồn gốc ở thất với tần số > 100 bpm (chiều dài vòng: < 600 ms). Các type VT: ● Dai dẳng: VT > 30 s hoặc đòi hỏi cắt cơn do tổn thương huyết động trong < 30s. ● Tạm thời / không dai dẳng: ≥3 nhát bóp, ngừng tự phát. ● Đơn hình: Hình thái QRS đơn thuần ổn định từ nhát bóp nọ đến nhát bóp kia. ● Đa hình: Thay đổi hoặc hình thái QRS nhiều dạng từ nhát bóp nọ đến nhát bóp kia. ● Hai hướng: VT với sự thay đổi luân phiên từ nhát bóp nọ đến nhát bóp kia ở trục mặt phẳng trán của QRS, thường nhận thấy ở trạng thái nhiễm độc digitalis hoặc VT đa hình do tăng tiết catecholamine VT đơn hình
VT đa hình
VT hai hướng (Bidirectional)
|
|
Xoắn đỉnh (Torsades de pointes) (2) |
Xoắn đỉnh là VT đa hình xuất hiện trong trạng thái khoảng QT kéo dài và được đặc trưng bằng biên độ QRS thay đổi và các kích cỡ nhỏ đi nhưng vẫn có thể nhìn thấy. Nó thường có chuỗi khởi đầu dài ngắn với khoảng ghép (coupling) dài từ nhát bóp VT đầu tiên và có thể biểu hiện với diễn biến tự nhiên của nhịp nhanh thất tạm thời (NSVT). Sự xoắn của các điểm, mặc dù có đặc tính, có thể không phải lúc nào cũng được nhìn thấy, đặc biệt là nếu cơn tạm thời hoặc chỉ một số giới hạn các chuyển đạo có thể ghi. Xoắn đỉnh có thể hậu quả từ nhịp chậm gồm block AV cao độ đưa đến chuỗi (sequence) dài ngắn (long-short) khởi đầu xoắn đỉnh.
|
|
Cuồng thất (Ventricular flutter) (2) |
VA đều ≈300 bpm (chiều dài vòng: 200 ms) suất hiện với hình dạng hình sin đơn hình; không có khoảng đẳng điện giữa các phức hợp QRS liên tiếp. |
|
Rung thất (2) |
Hoạt động điện không đều rõ ràng, nhanh với khả năng thay đổi đáng kể trong hình dạng các sóng điện tâm đồ, tần số thất thường > 300 bpm, chiều dài vòng: < 200 ms).
|
|
Ngừng tim đột ngột (2) |
SCA là ngừng hoạt động tim đột ngột như vậy nạn nhân trở nên không đáp ứng, với hoặc tiếp tục thở hổn hển hoặc không có bất kỳ cử động hô hấp nào, cũng như không có dấu hiệu tuần hoàn như biểu hiện mất cảm giác mạch đập. Ngừng tim được giả định do căn nguyên tim ngoại trừ người ta biết hoặc nhiều khả năng có nguyên nhân chấn thương, đuối nước, suy hô hấp hoặc ngạt thở, điện giật, quá liều thuốc, hoặc bất kỳ nguyên nhân không phải tim khác. |
|
Đột tử tim (SCD) (2) |
Tử vong đột ngột và bất ngờ xuất hiện trong vòng 1h từ khi khởi phát triệu chứng, hoặc xuất hiện ở các bệnh nhân được xác định tử vong trong phạm vi 24h khi không có triệu chứng và có khả năng do rối loạn nhịp tim hoặc thảm họa huyết động. |
|
Bão VT/VF (3) |
Bão VT / VF (bão điện hoặc bão loạn nhịp) đề cập đến trạng thái không ổn định về điện của tim được xác định có ≥ 3 đợt VT dai dẳng, VF hoặc các cú sốc thích hợp từ ICD trong vòng 24 giờ |
|
ICD ngăn ngừa tiên phát (2) |
Đặt ICD với mục đích ngăn ngừa SCD ở bệnh nhân không có VT dai dẳng hoặc SCA nhưng có nguy cơ gia tăng các biến cố này. |
|
ICD ngăn ngừa thứ phát (2) |
Đặt ICD ở bệnh nhân có SCA từ trước, VT dai dẳng, hoặc ngất do VA gây ra |
|
Bệnh cấu trúc tim* |
Thuật ngữ này bao gồm IHD, tất cả các type bệnh cơ tim, bệnh van tim, và bệnh tim bẩm sinh người lớn. |
|
Bệnh kênh của tim (4) |
Bệnh gây ra rối loạn nhịp tim do bất thường di truyền dẫn đến rối loạn chức năng của kênh ion tim (ví dụ, hội chứng QT dài, VT đa hình do catecholamine). |
* Định nghĩa của thuật ngữ này có thể khác nhau giữa các ấn phẩm. Tham khảo đăng lục cho định nghĩa được sử dụng trong tài liệu này. AV chỉ nhĩ thất; ICD chỉ máy khử rung tim có thể cấy, IHD chỉ bệnh tim thiếu máu cục bộ, NSVT chỉ nhịp nhanh thất tạm thời; SCA chỉ ngừng tim đột ngột, SCD chỉ đột tử do tim; VA chỉ rối loạn nhịp thất; VF chỉ rung thất; và VT chỉ nhịp nhanh thất.
2.1.1. VT tạm thời và các phức hợp thất sớm
Các phức hợp thất sớm (PVCs) thông thường và tăng lên theo tuổi. Mặc dù PVCs được nhận thấy ở quần thể quân đội khỏe mạnh chỉ khoảng 0.6% ở những người 50 tuổi (5) trên ECGs 12 chuyển đạo, theo dõi dài hạn hơn cho thấy PVCs ở khoảng 50% ở tất cả mọi người có hoặc không có bệnh tim (6). Sự có mặt của PVCs trong 2 phút theo dõi ở bệnh nhân trung niên trong nghiên cứu ARIC (Nguy cơ Xơ vữa động mạch Trong Cộng đồng: Atherosclerosis Risk In Communities) có liên quan đến tăng nguy cơ cả hai biến cố bệnh tim thiều máu cục bộ và tử suất, có hoặc không có bệnh tim thiếu máu cục bộ hiện hành (7, 8). Trong quần thể nói chung, PVC thường xuyên, được định nghĩa khi có ít nhất 1 PVC trên điện tim 12 chuyển đạo hoặc > 30 PVCs / giờ, có liên quan đến tăng nguy cơ tim mạch và tăng tỷ lệ tử vong (9). Trong một nghiên cứu từ Đài Loan ở bệnh nhân không có VT dai dẳng hoặc bệnh cấu trúc tim có theo dõi Holter liên tục 24h để đánh giá lâm sàng, PVCs đa ổ có liên quan đến tăng nguy cơ tử vong và các kết cục tim mạch xấu không tử vong (10). Trong cùng một quần thể, nhịp nhanh thất tạm thời (NSVT) liên quan độc lập với nguy cơ tử vong và các kết cục tim mạch bất lợi khác, gồm đột quỵ ((11). Một mối liên kết của PVC với nguy cơ đột quỵ tăng lên cũng đã nhận thấy trong quần thể ARIC (8).
Do một số nghiên cứu cho thấy mối liên hệ của PVC với các kết cục bất lợi, việc phát hiện PVCs, đặc biệt nếu đa ổ và thường xuyên, thường được coi là một yếu tố nguy cơ đối với các kết cục tim mạch bất lợi và những bệnh nhân này thường được đánh giá để đảm bảo rằng họ không có các tình trạng cơ bản ví dụ, bệnh tim thiếu máu cục bộ, rối loạn chức năng tâm thất trái [LV] đảm bảo điều trị tiếp theo để giảm nguy cơ. PVC và NSVT ở bệnh nhân bị bệnh tim mạch thường gặp và có liên quan đến kết cục bất lợi (12,13). Trong nghiên cứu CAST (Thử nghiệm ức chế Rối loạn Nhịp Tim), điều trị bệnh nhân sau nhồi máu (MI) đã nhận đươc các thuốc chống loạn nhịp (ví dụ: flecainide, encephalic, moricizine) làm tăng nguy cơ tử vong mặc dù ức chế được VA (14, 15). Điều trị PVC bằng các thuốc chống loạn nhịp không làm giảm tỷ lệ tử vong, ở dân số sau MI, điều trị với các thuốc block kênh natri class I (ví dụ quinidine, flecainide) làm tăng nguy cơ tử vong (15, 16). Tương tự như vậy, ở những bệnh nhân có LVEF giảm, class I, các thuốc chặn kênh natri và d-sotalol làm tăng nguy cơ tử vong (16, 17). Thuốc chẹn beta, thuốc chẹn kênh calcium nondihydropyridine và một số thuốc chống loạn nhịp có thể làm giảm triệu chứng hồi hộp (18).
PVCs xuất hiện trong quá trình test gắng sức có nguy cơ tử vong cao (19). Trong 1 nghiên cứu, PVCs xuất hiện trong quá trình phục hồi là một yếu tố tiên đoán tử vong mạnh mẽ hơn so PVCs xuất hiện lúc gắng sức (20). Tuy nhiên, PVCs phổ biến ở các vận động viên đã được đào tạo hay có hồi hộp, ở họ không đưa đến làm tăng nguy cơ tử vong trên cơ sở các nghiên cứu ở các thành viên nhỏ vận động viên, ít nhất ở họ không có các bất thường về tim mạch khác (21, 22). PVC phức tạp có thể không đại diện cho một phát hiện lành tính ở vận động viên có độ bền dẽo dai. Nghiên cứu điện sinh lý có thể cần thiết để đánh giá nguy cơ rối loạn nhịp (22). Các PVCs rất thường xuyên, > 10,000 đến 20.000 PVCs mỗi ngày, có thể kết hợp với giảm chức năng LV ở một số bệnh nhân có thể hồi phục khi kiểm soát các PVCs, được gọi là bệnh cơ tim do PVC gây ra (23, 24). (Xem phần 8.5 Bệnh cơ tim do PVC tạo ra). Rất hiếm khi, các PVC tự phát từ đường thoát có thể khởi khích VA ác tính ở các bệnh nhân không có bệnh cầu trúc tim (25, 26).
2.1.2. VT và VF trong quá trình hội chứng động mạch vành cấp (ACS)
Khoảng một nửa số bệnh nhân ngừng tim ngoài bệnh viện với nhịp đầu tiên được xác định là VF và họ sống sót đến nhập viện có bằng chứng nhồi máu cơ tim cấp (AMI) (27). Trong tất cả các trường hợp ngừng tim ngoài bệnh viện, > 50% sẽ có tổn thương động mạch vành đáng kể trên chụp động mạch vành cấp (27). Trong số bệnh nhân nhập viện với AMI, 5% đến 10% có VF hoặc VT dai dẳng trước khi đến bệnh viện, 5% khác sẽ có VF hoặc VT dai dẳng sau khi đến bệnh viện, hầu hết trong vòng 48 giờ kể từ khi nhập viện. Một nghiên cứu ở những bệnh nhân ACS ST không chênh lên được thực hiện catheter tim trong phạm vi 48h đã tìm thấy VT/VF ở 7,6% bệnh nhân, trong đó 60% các biến cố này trong vòng 48 giờ sau khi nhập viện (28). Nhịp thất bị động gia tăng (Accelerated idioventricular rhythm) là loạn nhịp thông thường ở các bệnh nhân có AMI, gồm các bệnh nhân MI ST chênh lên trải qua can thiệp mạch vành qua da tiên phát (PCI). Nhịp thất bị động gia tăng liên quan mật thiết hơn với mức độ nhồi máu so với tự tái tưới máu (29).
VA dai dẳng xuất hiện trong trạng thái ACS VT đa hình hoặc VF thường nhiều hơn so với VT đơn hình. Các yếu tố nguy cơ đối với VT / VF gồm tăng huyết áp trước, MI trước, sự thay đổi đoạn ST tại thời điểm biểu hiện và bệnh phổi tắc nghẽn mãn tính (30). Một nghiên cứu trên toàn quốc của Đan Mạch đã phát hiện ra 11,6% bệnh nhân có MI ST chênh lên đã được thực hiện PCAI có VF trước khi PCI, và VF đã liên quan đến tiêu thụ alcohol, đau ngực trước nhồi máu, khu vực nhồi máu phía trước và tắc mạch vành hoàn toàn trong thời gian chụp mạch vành (31). Trong một nhóm chọn lọc các bệnh nhân trải qua PCI tiên phát trong nghiên cứu lâm sàng, 5,7% đã phát triển VT dai dẳng hoặc VF, với hai phần ba các biến cố này xảy ra trước khi kết thúc catheter, và 90% trong vòng 48 giờ kể từ khi làm thủ thuật. VT hoặc VF sau khi PCI tiên phát có liên quan đến huyết áp thấp hơn, tần số tim cao hơn, dòng mạch vành không tốt khi kết thúc thủ thuật, và sự thoái lui của ST chênh lên không hoàn toàn (32). Điều quan trọng, ngược lại với một số nghiên cứu trước đó, VT hoặc VF bất cứ lúc nào cũng có nguy cơ tử vong cao hơn đáng kể trong vòng 90 ngày. VT hoặc VF trễ (sau 48 giờ ở bệnh viện) được kết hợp với nguy cơ tử vong cao hơn so với VT hoặc VF sớm (trong vòng 48 giờ kể từ khi ở bệnh viên) (33).
2.1.3. VT dai dẳng và VF Không Kết hợp Với Hội chứng mạch vành cấp (ACS)
Bệnh nhân bị bệnh tim cấu trúc có nguy cơ tăng lên cho VT dai dẳng và VF. VT dai dẳng không liên quan với ACS thường là đơn hình, thường do vào lại liên quan đến sẹo, nhưng nó có thể thoái hóa thành VF (34). Nguy cơ và yếu tố dự báo của VT đối với bệnh nhân mắc bệnh tim cấu trúc phụ thuộc vào type, mức độ nghiêm trọng và thời gian của bệnh tim cấu trúc, tăng lên cùng với mức độ nghiêm trọng của rối loạn chức năng tâm thất và hiện diện của HF có triệu chứng. VT đơn hình xuất hiện khi không có bệnh tim cấu trúc thường được cho là VT nguyên phát và thường do ổ tự động ở khu vực đặc trưng, dẫn đến các hình dáng điện tâm đò điển hình. VT đa hình và VF xảy ra khi không có bệnh tim cấu trúc hiếm gặp và có thể do bệnh kênh của tim (35, 36), hội chứng QT do thuốc gây ra (36), hoặc có thể nguyên phát (37, 38).
2.2. Đột tử tim (SCD)
2.2.1. Tỷ lệ SCD
Ngừng tim đột ngột (SCA) và kết quả phổ biến nhất của nó, SCD, tạo ra vấn đề lớn về sức khỏe cộng đồng, chiếm khoảng 50% số ca tử vong do tim mạch (1, 39), với ít nhất 25% các các biến cố tim có triệu chứng đầu tiên (1, 40, 41). Ngoài ra, các phân tích về mức độ SCD còn hạn chế, một phần do phạm vi ước lượng về nguy cơ trên cơ sở các phương pháp dịch tễ học khác nhau (42). Trong khoảng 20 đến 30 năm qua, SCD đã gây ra khoảng 230.000 đến 350.000 trường hợp tử vong mỗi năm ở Hoa Kỳ, với khoảng 450.000, tùy thuộc vào các phương pháp dịch tễ học, nguồn số liệu và các tiêu chí đưa vào (41, 43). Thấp nhất trong các cực điểm này đến từ ngoại suy tư liệu quốc gia từ các chương trình khu vực đặc biệt, trong khi tần số cao nhất gồm các nguyên nhân không phải tim của đột tử chẳng hạn như tắc phổi hoặc xuất huyết nội sọ. Số lượng trung bình phần lớn dựa trên các nghiên cứu xác nhận tử vong đòi hỏi mã gồm bệnh tim thiếu máu cục bộ.
Bản cập nhật số liệu thống kê tim mạch từ AHA năm 2017 ước tính tổng gánh nặng hàng năm của ngừng tim ngừng ngoài bệnh viện là 356.500 (44). Thêm 209.000 ngừng tim trong bệnh viên xuất hiện hàng năm (45). Trong số nhóm ngừng tim ngoài bệnh viện, khoảng 357.000 biến cố khởi kích phản ứng cấp cứu khẩn cấp, với 97% xảy ra ở người lớn > 18 tuổi.
Số liệu thống kê về sự sống sót đối với ngừng tim ngoài bệnh viện còn chưa thỏa mạn, với tần số tất cả sống sót được tính toán 10% (44). Trong số dưới phân nhóm 70% số trường hợp ngừng tim ngoài bệnh viện xảy ở nhà, tỉ lệ sống sót 6%. Các kết quả được báo cáo tốt nhất từ các khu vực với đăp ứng hồi sức cấp có thể thấy được mang tính cộng đồng và được phát triển cao, cùng với sự kết hợp của khu vực công cộng của ngừng tim, các nhân chứng bên cạnh sẵn sàng cung cấp CPR, người đáp ứng đầu tiên đến nhanh, nhịp có thể được sốc khi tiếp xúc khởi đầu, có thể sử dụng máy khử rung tự động ngoài (automated external defibrillators: AEDs), và có thể lợi từ hội sức tim phổi được hướng dẫn từ xa (CPR) (46, 47). Sự sống sót khi xuất viện sau khi ngừng tim ở bệnh viện ước tính 24% (48). Trong tất cả các trạng thái, tính toán sống sót biểu hiện tốt hơn khi nhịp được các người phản ứng có thể đánh sốc (VF, VT vô mạch), so với hoạt động điện vô mạch hoặc vô tâm thu (49). Mặc dù sự gia tăng rõ ràng về tần suất hoạt động điện vô mạch hoặc vô tâm thu có thể do đến trễ hơn của chăm sóc y tế, giảm đi trong tỷ lệ nhịp có khả năng sốc cũng đã được bổ xung, một phần đưa đến cải thiện trong chẩn đoán và điều trị bệnh tim câu trúc (40).
2.2.2. Quần thể dưới nhóm và dự báo nguy cơ
Dự báo nguy cơ đối với SCA và SCD là phức tạp. Phân tích nguy cơ được chia thành 2 loại chính: dự báo dân số nguy cơ và dự báo nguy cơ cá nhân (41, 50). Các dấu hiệu dịch tễ thông thường cung cấp cái nhìn sâu về xác suất cho sự phát triển của bệnh thiếu máu cục bộ trong phạm vi nhóm người chung, nhưng kiểm tra và xác nhận đầy đủ hồ sơ về phân tầng nguy cơ SCA của các cá thể trong dân cư nói chung hiện không tồn tại. Thách thức của việc xác định nguy cơ SCA ở các cá thế xuất phát từ mô hình quẩn thể được đặc trưng bằng các số lượng các biến cố lớn được làm giảm đi việc đưa vào mẫu số rất lớn (Hình 1). Dân số tổng thể có thể được phân nhóm thành các loại dựa trên sự lồng ghép tuổi, sự hiện diện và mức độ bệnh tật, và xác định các phân nhóm nhỏ, nguy cơ cao trong phạm vi quần thể mẫu chung lớn.
Tuổi tăng lên là một yếu tố dự báo mạnh mẽ cho SCA, nhưng không phải tuyến tính. Nguy cơ trong dân số nói chung, theo thời gian, bắt đầu từ 35 tuổi được ước tính là 1 / 1000 dân mỗi năm, tăng từ nguy cơ <1000 ở cuối của phổ đó, trẻ hơn đến nguy cơ cao hơn ở người cao tuổi (41). Tuy nhiên, phân tích nguy cơ suốt đời của SCD, bắt nguồn từ dữ liệu Framingham, cho thấy tỷ lệ SCD giảm trong những năm sau, đặc biệt ở những người > 75 tuổi (51). Dữ liệu cũng cho thấy SCD là phổ biến hơn ở nam giới so với nữ ở tất cả các nhóm lứa tuổi. Ngược lại, dân số trẻ em, vị thành niên và người trưởng thành trẻ có nguy cơ tổng cộng hàng năm 1 / 100.000, và có một chút nguy cơ SCD cao hơn ở cuối của khoảng tuổi trẻ hơn (41). Khoảng dao động liên quan đến tuổi tác, từ giữa 20 đến 35 đến 40 tuổi, được đặc trưng bằng gia tăng lên dốc trong nguy cơ của nhóm tuổi thanh niên đến nhóm tuổi trung niên, tương ứng với sự xuất hiện của bệnh tim thiếu máu cục bộ.
Mặc dù bệnh thiếu máu cục bộ vẫn là nền phổ biến nhất liên quan đến SCD, nhưng tỉ lệ mắc bệnh tim thiếu máu cục bộ – đột tử tim liên quan dường như đã giảm (52), với các dạng bệnh cơ tim khác nhau liên quan đến xơ cơ tim và tăng phì đại thất trái (LV) (53). Ngoài ra, xu hướng theo thời gian đã gợi ý bệnh nhân ngừng tim ngoài bệnh viện được nhập viện sống tại bệnh viện đang trở nên có khả năng nhiều hơn để có một trắc đồ lâm sàng nguy cơ cao, khi được đối lại với bệnh biểu hiện (54). Quần thể trẻ hơn – trẻ em, thanh thiếu niên, và người lớn trẻ – đã bị ảnh hưởng do môt loạt các rối loạn biểu hiện sớm hơn trong cuộc đời, gồm rối loạn di truyền cấu trúc và các bệnh kênh, viên cơ tim, bệnh tim bẩm sinh, và các rối loạn hiếm gặp khác (43). Trong khoảng thời gian chuyển tiếp, từ giữa những năm 20 đến giữa thập niên 30, nguyên nhân gây SCA và SCD gồm tỷ lệ bệnh di truyền thấp hơn và tỷ lệ bệnh thiếu máu cục bộ tăng lên (>40% trường hợp) (43).
Mặc dù tiến bộ nhỏ đã được đưa ra trong dự báo nguy cơ của SCA và SCD, thách thức lớn nhất là xác định các phân nhóm nguy cơ cao tương đối nhỏ ẩn trong phạm vi các quần thể lớn do người chưa biết vào 2 tháng 11 năm 2017 không được nhận biết bệnh nhưng có nguy cơ cao SCA khi biến cố tim đầu tiên của họ (Hình 1) [50]
Hình 1A. SCD Tần suất và Các Biến cố Toàn bộ (1)
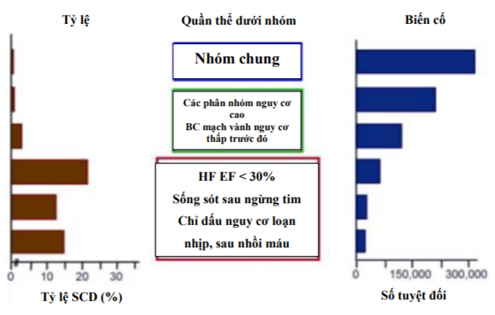
EF chỉ phân suất tống máu; và SCD: đột tử tim. BC: biến cố. HF: suy tim
Hình 1B. SCD và các phần lâm sàng (1)
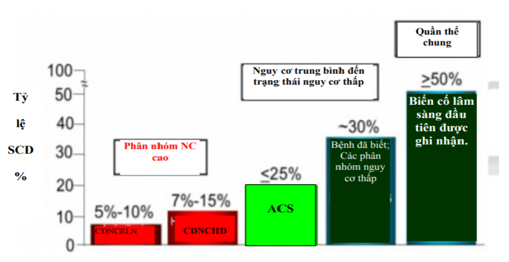
SCD chỉ đột tử tim. CDNCRLN: chỉ dấu nguy cơ rối loạn nhịp. CDNCHĐ: chỉ dấu nguy cơ huyết động. ACS: Hội chứng mạch vành cấp. NC: nguy cơ.
4. Đánh giá chung bệnh nhân có rối loạn nhịp thất (VA) được chứng minh bằng tư liệu hoặc nghi ngờ
4.1. Bệnh sử và khám xét thực thể
|
Khuyến cáo cho ngất * Các nghiên cứu được tham khảo ủng hộ khuyến cáo được tóm tắt trong Tài liệu Hỗ trợ onlien 1. |
||
|
COR |
LOE |
Khuyến cáo |
|
I |
B-NR |
1. Các bệnh nhân thẻ hiện ngất đối với họ VA được chứng minh bằng tư liệu, hoặc được cho nguyên nhân nhiều khả năng, nên được nhập viện để đánh giá, theo dõi và điều chỉnh (1-4). |
* Phần này qua thực hành đã được chấp nhận rõ ràng, và khuyến cáo mới đã được xác định chỉ được tập trung cho ngất
Tóm tắt
VA có thể tạo ra một phổ rộng các triệu chứng, và mức độ nghiêm trọng của các triệu chứng không nhất thiết phản ánh mức độ bệnh tim cấu trúc hoặc nguy cơ tiềm ẩn SCD. Các triệu chứng của VA gồm đánh trống ngực, hoặc các nhắt bóp lộn xộn hoặc thêm vào hoặc hồi hộp dai dẳng, thở ngắn, đau ngực, khó thở, gần ngất và ngất (5, 6). Hồi hộp cơ thể tương quan với VA nhưng thường được thông báo trong quá trình nhịp bình thường (7). Chẩn đoán phân biệt không dung nạp gắng sức, đau ngực, khó thở, tiền ngất, và ngất gồm VA nhưng cũng gồm những căn nguyên khác. Tuy nhiên, các triệu chứng trầm trọng hơn, đặc biệt ở những bệnh nhân bị bệnh tim cấu trúc đã biết hoặc bệnh tim cấu trúc được phát hiện hoặc bệnh tim điện học nên nỗ lực tập trung khám phá cho khả năng kết hợp với VA (Bảng 6). Việc làm sáng tỏ các yếu tố thúc đẩy, như căng thẳng về thể lực hoặc tinh thần, thuốc sử dụng hoặc bệnh cùng lúc, và các yếu tố làm giảm nhẹ là rất quan trọng.
Sự hiện diện của tiền sử gia đình bị SCD, bệnh tim thiếu máu cục bộ, bệnh tim van, bệnh cơ tim không do thiếu máu cục bộ (NICM), hoặc HF làm tăng mối quan tâm về sự có mặt của một trong những rối loạn này liên quan đến VA. Có được bệnh sử thuốc hoàn chỉnh là rất quan trọng. Các thuốc chống loạn nhịp và các loại thuốc khác có thể gây ra kéo dài QT và xoắn đỉnh (torsades de pointes) (www.crediblemeds.org) (8); một số loại thuốc cũng có thể gây mẫu điện tâm đồ type I Brugada và VF (www.brugadadrugs.org) (9, 10).
Bảng 6.Các xem xét Quan trọng trong Đánh giá Các bệnh nhân có VA đã biết hoặc Nghi ngờ
|
Thành phần |
Đánh giá và các Phát hiện Liên quan đến Nguy cơ VA và /hoặc SCD |
|
Bệnh sử |
1. Các triệu chứng / sự kiện liên quan đến rối loạn nhịp tim: Đau đầu, ngất, ngất, khó thở, đau ngực, ngưng tim 2. Triệu chứng liên quan đến bệnh tim: Khó thở khi nghỉ ngơi hoặc gắng sức, khó thở khi nằm, cơn khó thở kịch phát về ban đêm, đau ngực, phù 3. Các yếu tố thúc đẩy: Gắng sức, căng thẳng cảm xúc 4. Bệnh tim đã biết: Bệnh mạch vành, van tim (ví dụ, sa van hai lá), bệnh tim bẩm sinh, các bệnh khác 5. Yếu tố nguy cơ cho bệnh tim: Tăng huyết áp, tiểu đường, tăng lipid máu và hút thuốc 6. Các thuốc: • Các thuốc chống loạn nhịp • Các loại thuốc khác có khả năng kéo dài QT và xoắn đỉnh (torsades de pointes) • Thuốc có khả năng kích động hoặc làm trầm trọng VA Δ Thuốc kích thích bao gồm cocaine và amphetamine Δ Các chất bổ sung bao gồm steroid đồng hoá • Tương tác thuốc và thuốc có thể gây ra kéo dài QT và xoắn đỉnh (torsades de pointes) 7. Tiền sử bệnh: • Bệnh tuyến giáp • Thương tích thận cấp tính, bệnh thận mạn, hoặc bất thường điện giải • Đột quỵ hoặc các biến cố tắc nghẽn • Bệnh phổi • Động kinh (ngất do loạn nhịp có thể bị chẩn đoán nhầm như động kinh) • Sử dụng rượu hoặc ma túy bất hợp pháp • Sử dụng các loại thuốc mua tự do có thể gây ra kéo dài QT và xoắn đỉnh (torsades de pointes) • Va chạm các phương tiện giao thông không giải thích được |
|
Bệnh sử Gia đình |
1. SCD, SCA, hoặc đuối nước không giải thích được ở một người có quan hệ thứ nhất 2. SIDS hoặc sẩy thai tự phát lặp đi lặp lại do mối liên hệ tiềm tàng của họ với các bệnh kênh của tim 3. Bệnh tim • IHD • Bệnh cơ tim: Phì đại, giãn, ARVC • Bệnh tim bẩm sinh • Bệnh kênh của tim: Long QT, Brugada, QT ngắn, CPVT • Loạn nhịp tim • Rối loạn dẫn truyền, máy tạo nhịp tim / ICDs 4. Bệnh cơ thần kinh kết hợp với bệnh cơ tim • Loạn dưỡng cơ 5. Động kinh |
|
Khám |
1. Nhịp tim và tính đều đặn, huyết áp 2. Áp lực tĩnh mạch cảnh 3. Tiếng thổi 4. Xung mạch và tốc độ lan 5. Phù 6. Sẹo giải phẫu xương ức |
ARVC chỉ bệnh cơ tim thất phải gây rối loạn nhịp; CPVT: nhịp nhanh thất đa hình do tiết catecholamine; IHD: bệnh tim thiếu máu cục bộ; SCA: ngừng tim đột ngột; SCD: đột tử tim; SIDS: hội chứng đột tử ở trẻ sơ sinh (sudden infant death syndrome); và VA: rối loạn nhịp thất.
Những bệnh nhân có ngoại tâm thu nhịp đôi (bigeminy) và nhịp ba (trigeminy) với ảnh hưởng của nhịp chậm, mạch quay hụt và tăng huyết áp tương đối với áp lực xung rộng. Ảnh hưởng nhịp chậm từ các PVC có thể gây ra tính toán không chính xác về nhịp tim. Mặc dù các nhắt bóp sớm nghe tim có thể biết được, khám thực thể được tập chung chủ yếu vào tìm ra bằng chứng của bệnh tim thực thể. Sự dồn mạch cảnh hoặc xung ngoại biên giảm có thể là chỉ dấu của bệnh vữa xơ liên quan đến bệnh cơ tim thiếu máu cục bộ. Giãn tĩnh mạch cổ, rales ẩm, tiếng ngựa phi, và phù ngoại biên cung cấp bằng chứng của HF. Nghe có thể phát hiện tiếng thổi của tim phù hợp với bệnh van tim, chẳng hạn hẹp động mạch chủ hoặc hở hai lá, và có thể được kết hợp với HF và VA. Click giữa thì tâm thu chỉ ra sa van hai lá có thể kết hợp với VA (11-13). Nhiều VA không có triệu chứng và chỉ phát hiện trên điện tim hoặc đo từ xa. Các trường hợp như vậy làm nổi bật nhu cầu tìm kiếm bằng chứng về bệnh tim.
Văn bản Hỗ trợ Cụ thể – Khuyến cáo
1. VT nhanh, dai dẳng có thể gây ra ngất thứ phát do giảm đáng kể cung lượng tim, được tiếp theo bằng sự phục hồi nếu VT ngừng, hoặc SCA nếu VT vẫn tồn tại và không được điều trị kịp thời. Ngất hoặc SCA có thể biểu hiện đầu tiên của bệnh tim cấu trúc hoặc bệnh tim điện học (14), một số nạn nhân SCA có những cơn ngất “cảnh báo” đi trước (15). Ngất, hoặc cảnh báo sớm chóng mặt, chóng mặt, hoặc gần ngất, có thể là một yếu tố nguy cơ đối với SCA và SCD (2). Việc đánh giá khởi đầu ở mọi lứa tuổi tập trung vào việc phát hiện hoặc loại trừ bệnh tim. Ngất trong quá trình gắng sức nên nỗ lực đánh giá cần thận để loại trừ các nguyên nhân tim. Đánh giá tim bằng siêu âm tim, theo dõi di động, test gắng sức có thể được đảm bảo phụ thuộc vào các thông tim lâm sàng gợi ý (3, 4). Các nguyên nhân ngất do tim gồm VT dai dẳng, block AV cao độ hoặc nhịp xoang rất chậm hoặc các khoảng ngưng xoang kéo dài, nhịp nhanh trên thất (SVT), rối loạn chức năng các máy tạo nhịp, VA do các bệnh kênh của tim hoặc các hội chứng bệnh tim cấu trúc, như bệnh cơ tim phì đại (HCM) hoặc bệnh tim bẩm sinh (3, 4, 16). Các bệnh kênh và HCM đặc biệt quan trọng để xem xét ở vị thành niên và người lớn trẻ. Các nguyên nhân ngất do rối loạn nhịp thường kết hợp với các khoảng thời gian tiền triệu rất ngắn, hoawccj hồi hộp, cũng như bệnh tim tồn thại đã biết, đặc biệt bệnh sử LVEF thấp hoặc HF (1). Trong số các nguyên nhân tim không phải do rối loạn nhịp, cần cân nhắc đến thiếu máu cơ tim cục, hẹp động mạch chủ nặng, bệnh cơ tim phì đại (HCM), HF, cả rối loạn chức năng van nhân tạo, thuyên tắc phổi, các thuốc và sử dụng các thuốc ma túy (3).
TÀI LIỆU THAM KHẢO
1. Middlekauff HR, Stevenson WG, Stevenson LW, et al. Syncope in advanced heart failure: high risk of sudden death regardless of origin of syncope. J Am Coll Cardiol. 1993;21:110-6.
2. Myerburg RJ, Castellanos A. Cardiac arrest and sudden cardiac death – Chapter 39. In: Mann DL, Zipes DP, Libby P et al, eds. Braunwald’s Heart Disease: A Textbook of Cardiovascular Medicine. 10thed. Oxford, UK: Elsevier; 2015:821- 60.
3. Shen WK, Sheldon RS, Benditt DG, et al. 2017 ACC/AHA/HRS guideline for the evaluation and management of patients with syncope: a report of the American College of Cardiology/American Heart Association Task Force on Clinical Practice Guidelines and the Heart Rhythm Society. Circulation. 2017;136:e60-122.
4. Soteriades ES, Evans JC, Larson MG, et al. Incidence and prognosis of syncope. N Engl J Med. 2002;347:878-85.
5. Noda T, Shimizu W, Taguchi A, et al. Malignant entity of idiopathic ventricular fibrillation and polymorphic ventricular tachycardia initiated by premature extrasystoles originating from the right ventricular outflow tract. J Am Coll Cardiol. 2005;46:1288-94.
6. Viskin S, Rosso R, Rogowski O, et al. The “short-coupled” variant of right ventricular outflow ventricular tachycardia: a not-so-benign form of benign ventricular tachycardia? J Cardiovasc Electrophysiol. 2005;16:912-6.
7. Zimetbaum P, Josephson ME. Evaluation of patients with palpitations. N Engl J Med. 1998;338:1369-73.
8. Credible meds. Available at: http://www.crediblemeds.org. Accessed December26, 2016.
9. Brugada drugs. Available at: http://www.brugadadrugs.org. Accessed October 6, 2016.
10.Konigstein M, Rosso R, Topaz G, et al. Drug-induced Brugada syndrome: clinical characteristics and risk factors. Heart Rhythm. 2016;13:1083-7.
11.Basso C, Perazzolo MM, Rizzo S, et al. Arrhythmic mitral valve prolapse and sudden cardiac death. Circulation. 2015;132:556-66.
12.Nordhues BD, Siontis KC, Scott CG, et al. Bileaflet mitral valve prolapse and risk of ventricular dysrhythmias and death. J Cardiovasc Electrophysiol. 2016;27:463-8.
13.Sriram CS, Syed FF, Ferguson ME, et al. Malignant bileaflet mitral valveprolapse syndrome in patients with otherwise idiopathic out-of-hospital cardiac arrest. J Am Coll Cardiol. 2013;62:222-30.
14.Huikuri HV, Castellanos A, Myerburg RJ. Sudden death due to cardiac arrhythmias. N Engl J Med. 2001;345:1473-82.
15.Krahn AD, Healey JS, Simpson CS, et al. Sentinel symptoms in patients with unexplained cardiac arrest: from the Cardiac Arrest Survivors with Preserved Ejection Fraction Registry(CASPER). J Cardiovasc Electrophysiol. 2012;23:60- 6.
16.Ruwald MH, Hansen ML, Lamberts M, et al. The relation between age, sex, comorbidity, and pharmacotherapy and the risk of syncope: a Danish nationwide study. Europace. 2012;14:1506-14.
4.2. Đánh giá không thâm nhập
4.2.1. ECG 12 chuyển đạo và Test Gắng sức
|
Các khuyến cáo cho ECG 12 chuyển đạo và Test Gắng sức Các nghiên cứu tham khảo ủng hộ các khuyến cáo được tóm tắt trong phần Tư liệu hỗ trợ online 2. |
||
|
COR |
LOE |
Các khuyến cáo |
|
I |
B-NR |
1. Ở những bệnh nhân có nhịp nhanh phức hợp rộng, dai dẳng, ổn định huyết động, ECG 12 chuyển đạo trong quá trình nhịp nhanh nên được thu lượm (1-3). |
|
I |
B-NR |
2. Ở những bệnh nhân có triệu chứng VA liên quan đến gắng sức, nghi ngờ bệnh thiếu máu cục bộ, nhịp nhanh thất đa hình do catecholamine, test gắng sức treadmill là hữu dụng để đánh giá VA do gắng sức tạo ra (4, 5). |
|
I |
B-NR |
3. Ở các bệnh nhân có nghi ngờ VA hoặc VA được chứng minh bằng tư liệu, ECG 12 chuyển đạo nên được thu lượm trong nhịp xoang để tim bằng chứng bệnh tim (6). |
Văn bản Hỗ trợ Cụ thể – Khuyến cáo
1. ECG 12 chuyển đạo trong quá trình nhịp nhanh là test chẩn đoán đầu tiên nên được thực hiện ở bất kỳ bệnh nhân nào được xác nhận có nhịp nhanh QRS rộng ổn đinh trên monitor. VT là chẩn đoán ở hầu hết người lớn có nhịp tim nhanh phức hợp rộng và nền bệnh tim cấu trúc (3). Các tiêu chuẩn hỗ trợ chẩn đoán VT gồm phân ly AV, phức hợp QRS > 0,14 s, một sóng R một pha ở aVR, các hình thái QRS đặc biệt (ví dụ, phức hợp QRS concordant dương hoặc âm ở các chuyển đạo trước tim), không có phức hợp RS ở tất cả các chuyển đạo trước tim và khoảng RS > 100 ms trong ít nhất 1 chuyển đạo trước tim (2). Các ngoại lệ xảy ra, đặc biệt ở bệnh nhân bệnh tim mạch tiến triển và với việc sử dụng thuốc chống loạn nhịp (1). Đối với bệnh nhân tồn tại block nhánh bó từ trước, so sánh hình thái QRS ở nhịp xoang xoang với nhịp nhanh phức hợp rộng trong quá trình nhịp nhanh thường tương hợp.
2. Đối với các triệu chứng loạn nhịp liên quan đến gắng sức, gắng sức trong một trạng thái theo dõi có thể tái tạo các triệu chứng và / hoặc loạn nhịp liên quan, cho phép chẩn đoán. Test gắng sức đặc biệt quan trọng khi nhịp nhanh thất đa hình do tiết catecholamine. Tuy nhiên, các triệu chứng và kết quả có liên quan đến gắng sức và các phát hiện có thể không được tái tạo một cách thật sự với test gắng sức, và theo dõi điện tâm đồ dài hạn với các máy ghi ngoài hoặc cấy vào cơ thể có thể cần thiết.
3. ECG 12 chuyển đạo chỉ ra sự hiện diện của bệnh tim cấu trúc chẳng hạn như MI trước đó hoặc giãn lớn buồng tim có thể tăng khả năng các triệu chứng của bệnh nhân có thể do VA, hoặc nó có thể cung cấp bằng chứng về nền cơ bản cho VA. ECG cũng có thể bộc lộ bằng chứng về các rối loạn nhịp di truyền, như hội chứng QT dài, hội chứng Brugada và bệnh cơ tim thất phải gây rối loạn nhịp. Ở những bệnh nhân bệnh tim cấu trúc, thời gian QRS và sự có mặt của những bất thường dẫn truyền cung cấp thông tin tiên lượng (7-14). Dữ liệu về việc sử dụng sự thay đổi luân phiên sóng T vi điện thế và ECG tín hiệu trung bình cón chưa được thuyết phục, vì những test này thường không được sử dụng phổ biến trong thực hành lâm sàng (15-19); ngoại lệ có khả năng sử dụng ECG tín hiệu trung bình ở bệnh nhân bệnh cơ tim thất phải gây rối loạn nhịp (xem Phần 7.3).
TÀI LIỆU THAM KHẢO
1. Brugada P, Brugada J, Mont L, et al. A new approach to the differential diagnosis of a regular tachycardia with a wide QRS complex. Circulation. 1991;83:1649-59.
2. Wellens HJ, Bar FW, Lie KI. The value of the electrocardiogram in the differential diagnosis of a tachycardia with a widened QRS complex. Am J Med. 1978;64:27-33.
3. Steinman RT, Herrera C, Schuger CD, et al. Wide QRS tachycardia in the conscious adult. Ventricular tachycardia is the most frequent cause. JAMA. 1989;261:1013-6.
4. Elhendy A, Chandrasekaran K, Gersh BJ, et al. Functional and prognostic significance of exercise-induced ventricular arrhythmias in patients with suspected coronary artery disease. Am J Cardiol. 2002;90:95-100.
5. Grady TA, Chiu AC, Snader CE, et al. Prognostic significance of exercise-induced left bundle-branch block. JAMA. 1998;279:153-6.
6. Perez-Rodon J, Martinez-Alday J, Baron-Esquivias G, et al. Prognostic value of the electrocardiogram in patients with syncope: data from the group for syncope study in the emergency room (GESINUR). Heart Rhythm. 2014;11:2035- 44.
7. Baldasseroni S, Opasich C, Gorini M, et al. Left bundle-branch block is associated with increased 1-year sudden and total mortality rate in 5517 outpatients with congestive heart failure: a report from the Italian network on congestive heart failure. Am Heart J. 2002;143:398-405.
8. Buxton AE, Sweeney MO, Wathen MS, et al. QRS duration does not predict occurrence of ventricular tachyarrhythmias in patients with implanted cardioverter-defibrillators. J Am Coll Cardiol. 2005;46:310-6.
9. Desai AD, Yaw TS, Yamazaki T, et al. Prognostic significance of quantitative QRS duration. Am J Med. 2006;119:600- 6.
10.Dhar R, Alsheikh-Ali AA, Estes NA3rd, et al. Association of prolonged QRS duration with ventricular tachyarrhythmias and sudden cardiac death in the Multicenter Automatic Defibrillator Implantation Trial II (MADITII). Heart Rhythm. 2008;5:807-13.
11.Freedman RA, Alderman EL, Sheffield LT, et al. Bundle branch block in patients with chronic coronary artery disease: angiographic correlates and prognostic significance. J Am Coll Cardiol. 1987;10:73-80.
12.Iuliano S, Fisher SG, Karasik PE, et al. QRS duration and mortality in patients with congestive heart failure. Am Heart J. 2002;143:1085-91.
13.Kadish A, Dyer A, Daubert JP, et al. Prophylactic defibrillator implantation in patients with nonischemic dilated cardiomyopathy. N Engl J Med. 2004;350:2151-8.
14.Zimetbaum PJ, Buxton AE, Batsford W, et al. Electrocardiographic predictors of arrhythmic death and total mortality in the multicenter unsustained tachycardia trial. Circulation. 2004;110:766-9.
15.Costantini O, Hohnloser SH, Kirk MM, et al. The ABCD (Alternans Before Cardioverter Defibrillator) Trial: strategies using T-wave alternans to improve efficiency of sudden cardiac death prevention. J Am Coll Cardiol. 2009;53:471-9.
16.Monasterio V, Martinez JP, Laguna P, et al. Prognostic value of average T-wave alternans and QT variability for cardiac events in MADIT-II patients. J Electrocardiol. 2013;46:480-6.
17.Chow T, Kereiakes DJ, Onufer J, et al. Does microvolt T-wave alternans testing predict ventricular tachyarrhythmias in patients with ischemic cardiomyopathy and prophylactic defibrillators? The MASTER (Microvolt T Wave Alternans Testing for Risk Stratification of Post-Myocardial Infarction Patients) trial. J Am Coll Cardiol. 2008;52:1607-15.
18.Gupta A, Hoang DD, Karliner L, et al. Ability of microvolt T-wave alternans to modify risk assessment of ventricular tachyarrhythmic events: a meta-analysis. Am Heart J. 2012;163:354-64.
19.Bloomfield DM, Steinman RC, Namerow PB, et al. Microvolt T-wave alternans distinguishes between patients likely and patients not likely to benefit from implanted cardiac defibrillator therapy: a solution to the Multicenter Automatic Defibrillator Implantation Trial (MADIT) II conundrum. Circulation. 2004;110:1885-9.
4.2.2. Điện tâm đồ lưu động
|
Khuyến cáo cho điện tâm đồ lưu động Các nghiên cứu tham khảo ủng hộ các khuyến cáo được tóm tắt trong phần Tư liệu hỗ trợ online 3 và 4. |
||
|
COR |
LOE |
Các khuyến cáo |
|
I |
B-NR |
1. Theo dõi điện tâm đồ lưu động rất hữu ích để đánh giá xem các triệu chứng, gồm đánh trống ngực, tiền ngất hay ngất, có phải do VA gây ra hay không (1- 4). |
Văn bản Hỗ trợ Cụ thể – Khuyến cáo
1. Theo dõi điện tâm đồ lưu động thường được sử dụng để đánh giá hiệu quả của các phương pháp điều trị ngăn chặn loạn nhịp nhưng cần nhiều dữ liệu hơn về việc sử dụng lâm sàng trong thực hành này. Ghi điện tâm đồ liên tục hoặc từng lúc với theo dõi Holter hoặc ghi sự kiện giúp ích cho việc chẩn đoán nghi ngờ rối loạn nhịp tim, tính toán tần số của chúng, liên quan triệu chứng, và đánh giá đáp ứng với điều trị. Mặc dù hiệu suất của các test này tương đối thấp, nhưng VT đôi khi được chứng minh bằng tư liệu (4). Ghi Holter liên tục kéo dài 24 giờ phù hợp khi các triệu chứng xuất hiện ít nhất một lần mỗi ngày hoặc khi liên quan đến định lượng PVCs / NSVT để đánh giá chức năng thất trái giảm có liên quan đến VA. Đối với các triệu chứng rời rạc, theo dõi sự kiện hoặc “vi mạch” phù hợp hơn do chúng có thể được kích hoạt trong một thời gian dài và hiệu suất chẩn đoán tăng lên (2, 3). Các monitor điện tâm đồ có bản được dính chặt có thể ghi trong nhiều tuần và cho phép theo dõi 1 chuyển đạo ngắn hạn liên tục và kích hoạt của bệnh nhân khi có triệu chứng. Các nghiên cứu đã cho thấy sự tuân thủ của bệnh nhân thỏa đáng, cũng như phát hiện loạn nhịp; tuy nhiên, với một số monitor, rối loạn nhịp được phát hiện không được khám phá cho đến tận khi bản đưa trở lại phân tích (1, 4). Đánh giá hàng loạt với test gắng sức và / hoặc theo dõi lưu động 24h cũng được sử dụng để đánh giá gánh nặng nhịp và đáp ứng của VA với điều trị. Đáng chú ý, các monitor cấy đã được đề cập ở Phần 4.2.3. Điều quan trọng khi nghi ngờ VA ở bệnh nhân là cao, việc theo dõi bệnh nhân ngoại trú không phù hợp khi nỗ lực chẩn đoán và ngăn ngừa VA được đảm bảo. Điều quan trọng các triệu chứng phải tương quan chính xác với các rối loạn nhịp được phát hiện bằng theo dõi ECG lưu động.
Tài liệu tham khảo
1. Barrett PM, Komatireddy R, Haaser S, et al. Comparison of 24-hour Holter monitoring with 14-day novel adhesive patch electrocardiographic monitoring. Am J Med. 2014;127:95-7.
2. de Asmundis C, Conte G, Sieira J, et al. Comparison of the patient-activated event recording system vs. traditional 24 h Holter electrocardiography in individuals with paroxysmal palpitations or dizziness. Europace. 2014;16:1231-5.
3. Linzer M, Pritchett EL, Pontinen M, et al. Incremental diagnostic yield of loop electrocardiographic recorders in unexplained syncope. Am J Cardiol. 1990;66:214-9.
4. Turakhia MP, Hoang DD, Zimetbaum P, et al. Diagnostic utility of a novel leadless arrhythmia monitoring device. Am J Cardiol. 2013;112:520-4.
4.2.3. Theo dõi tim được cấy vào cơ thể
|
Khuyến cáo cho theo dõi tim cấy vào cơ thể Các nghiên cứu tham khảo ủng hộ các khuyến cáo được tóm tắt trong phần Tư liệu hỗ trợ online 5. |
||
|
COR |
LOE |
Khuyến cáo |
|
IIa |
B-NR |
1. Ở những bệnh nhân có triệu chứng lẻ tẻ (gồm ngất) có nghi ngờ liên quan đến VA, theo dõi tim được cấy có thể hữu ích (1-4). |
Văn bản Hỗ trợ Cụ thể – Khuyến cáo
1. Theo dõi tim cấy vào cơ thể cung cấp việc theo dõi nhịp liên tục và ghi lưu trữ điện đồ trên cơ sở hoạt động của bệnh nhân hoặc các thông số đã đươc đặt, cho phép giai đoạn theo dõi kéo dài vài năm. Dụng cụ này đòi hởi thủ thuật xâm lấn tối thiểu bằng gây tê khu vực để cấy vào. Ở bệnh nhân có các triệu chứng lẻ tẻ, kể cả ngất, các máy ghi có thể cấy hữu ích trong việc chẩn đoán nhịp nhanh nghiêm trọng (gồm VA) và nhịp chậm (2-4). Chúng thường được dành riêng cho những bệnh nhân theo dõi lưu động khác không thể phát hiện do không thường gặp các sự kiện. Tăng 25% hiệu suất trong chẩn đoán đã được mô tả sau khi không được phát hiện bằng theo dõi lưu động ngoài (5). Trong một nghiên cứu bệnh nhân ngất, theo dõi cấy với cơ thể đã có hiệu suất chẩn đoán lớn hơn so với các test “kinh điển” bằng theo dõi ngoài, test bàn nghiêng và nghiên cứu điện sinh lý (EPs) (2). Một nghiên cứu có hệ thống ở những bệnh nhân ngất đã kết luận việc sử dụng các thiết bị này cung cấp tỷ lệ chẩn đoán cao hơn và xu hướng giảm tái phát ngất sau chẩn đoán, khi so sánh với điều chỉnh kinh điển (3). Một nghiên cứu tiền cứu bệnh nhân sau MI, với LVEF <40%, đã chứng minh NSVT ( dài > 16 nhịp) ở 13%, VT (> 30 s) ở 3% và VF ở 3% bệnh nhân (1). Điều quan trọng tương quan chính xác các triệu chứng với các rối loạn nhịp tim được phát hiện bằng theo dõi các thiết bị cấy vào cơ thể.
Tài liệu tham khảo
1. Bloch Thomsen PE, Jons C, Raatikainen MJ, et al. Long-term recording of cardiac arrhythmias with an implantable cardiac monitor in patients with reduced ejection fraction after acute myocardial infarction: the Cardiac Arrhythmias and Risk Stratification After Acute Myocardial Infarction (CARISMA) study. Circulation. 2010;122:1258- 64.
2. Krahn AD, Klein GJ, Yee R, et al. Use of an extended monitoring strategy in patients with problematic syncope. Reveal Investigators. Circulation. 1999;99:406-10.
3. Solbiati M, Costantino G, Casazza G, et al. Implantable loop recorder versus conventional diagnostic workup for unexplained recurrent syncope. Cochrane Database Syst. Rev. 2016;4:CD011637.
4. Volosin K, Stadler RW, Wyszynski R, et al. Tachycardia detection performance of implantable loop recorders: results from a large ‘real-life’ patient cohort and patients with induced ventricular arrhythmias. Europace. 2013;15:1215-22.
5. Linzer M, Pritchett EL, Pontinen M, et al. Incremental diagnostic yield of loop electrocardiographic recorders in unexplained syncope. Am J Cardiol. 1990;66:214-9.
6. Turakhia MP, Hoang DD, Zimetbaum P, et al. Diagnostic utility of a novel leadless arrhythmia monitoring device. Am J Cardiol. 2013;112:520-4.
4.2.4. Hình ảnh học Tim Không xâm lấn
|
Khuyến cáo cho Hình ảnh học Tim Không xâm lấn Các nghiên cứu tham khảo ủng hộ các khuyến cáo được tóm tắt trong phần Tư liệu hỗ trợ online 6. |
||
|
COR |
LOE |
Các khuyến cáo |
|
I |
B-NR |
1. Ở các bệnh nhân có VA đã biết hoặc nghi ngờ có thể kết hợp với bệnh tim cấu trúc nền hoặc nguy cơ SCA, siêu âm tim được khuyến cáo để đánh giá cấu trúc và chức năng của tim (1, 2). |
|
IIa |
C-EO |
2. Ở các bệnh nhân biểu hiện VA nghi ngờ có bệnh tim cấu trúc, hình ảnh cộng hưởng từ tim (MRI) hoặc cắt lớp điện toán (CT) có thể hữu ích để phát hiện và xác định đặc điểm bệnh tim cấu trúc nền. |
Văn bản Hỗ trợ Đặc biệt Khuyến cáo
1. Đánh giá chức năng cơ tim toàn bộ và khu vực, cấu trúc và chức năng van tim, cùng với đánh giá bệnh tim bẩm sinh ở người trưởng thành được đòi hỏi ở các bệnh nhân có hoặc ở nguy cơ cao cho VA hoặc SCD, gồm bệnh nhân bị bệnh cơ tim, HF, MI trước, tiền sử gia đình bệnh cơ tim hoặc SCD, hoặc bệnh tim cấu trúc di truyền kết hợp với SCD. Siêu âm tim là kỹ thuật hình ảnh dễ sử dụng nhất và được sử dụng phổ biến nhất (1, 2). LVEF một dự báo mạnh mẽ, độc lập cho SCD và tử suất tim mạch và là yếu tố quyết định cho việc cấy ICD để dự phòng SCD tiên phát (1). Trong nghiên cứu SCD-HeFT (Đột tử tim trong suy tim) (2), lợi ích của ICD không phụ thuộc vào phương thức (tức là siêu âm tim, chụp mạch hạt nhân phóng xạ, hoặc chụp mạch tương phản) bằng cách đó đánh giá LVEF. Trong thực hành lâm sàng, nếu CT tim (3) hoặc MRI tim đã được thực hiện và cung cấp đánh giá đầy đủ, siêu âm tim có thể là không cần thiết. Khuyến cáo này cho hình ảnh khác với hướng dẫn ngất của ACC / AHA / HRS năm 2017 (4) áp dụng cho bệnh nhân không có VA.
2. VA hoặc SCA có thể biểu hiện đầu tiên của bệnh tim thiếu máu cục bộ, các quá trình tiến triển bệnh cơ tim, hoặc viêm cơ tim. CT tim và MRI tim cho phép đánh giá bệnh tim cấu trúc và đánh giá chức năng LV và RV gồm định lượng LVEF, khối lượng và thể tích LV, cấu trúc van tim và giải phẫu mạch vành gồm nguồn gốc động mạch vành dị thường. MRI tim có thể hữu ích trong việc đánh giá các sẹo cơ tim và quá trình thâm nhiễm và các quá trình truyền nhiễm rõ ràng như sự gia tăng gadolinium trễ (5-9). MRI tim cũng cung cấp đánh giá chức năng LV, RV, kích thước và mức độ xơ hóa chất lượng cao, và đặc biệt hữu ích trong bệnh cơ tim thất phải gây loạn nhịp và HCM.
Tài liệu tham khảo
1. Solomon SD, Zelenkofske S, McMurray JJ, et al. Sudden death in patients with myocardial infarction and left ventricular dysfunction, heart failure, or both. N Engl J Med. 2005;352:2581-8.
2. Gula LJ, Klein GJ, Hellkamp AS, et al. Ejection fraction assessment and survival: an analysis of the Sudden Cardiac Death in Heart Failure Trial (SCD-HeFT). Am Heart J. 2008;156:1196-200.
3. Rauch B, Schiele R, Schneider S, et al. OMEGA, a randomized, placebo-controlled trial to test the effect of highly purified omega-3 fatty acids on top of modern guideline-adjusted therapy after myocardial infarction. Circulation. 2010;122:2152-9.
4. Shen WK, Sheldon RS, Benditt DG, et al. 2017 ACC/AHA/HRS guideline for the evaluation and management of patients with syncope: a report of the American College of Cardiology/American Heart Association Task Force on Clinical Practice Guidelines and the Heart Rhythm Society. Circulation. 2017;136:e60-122.
5. Coleman GC, Shaw PW, Balfour PC Jr, et al. Prognostic value of myocardial scarring on CMR in patients with cardiac sarcoidosis: a systematic review and meta-analysis. JACC Cardiovasc Imaging. 2016;10:411-20.
6. Di Marco A, Anguera I, Schmitt M, et al. Late gadolinium enhancement and the risk for ventricular arrhythmias or sudden death in dilated cardiomyopathy: systematic review and meta-analysis. JACC Heart Fail. 2017;5:28-38.
7. Greulich S, Deluigi CC, Gloekler S, et al. CMR imaging predicts death and other adverse events in suspected cardiac sarcoidosis. JACC Cardiovasc Imaging. 2013;6:501-11.
8. Piers SR, Tao Q, van Huls van Taxis CF, et al. Contrast-enhanced MRI-derived scar patterns and associated ventricular tachycardias in nonischemic cardiomyopathy: implications for the ablation strategy.Circ Arrhythm Electrophysiol. 2013;6:875-83.
9. White JA, Fine NM, Gula L, et al. Utility of cardiovascularmagnetic resonance in identifying substrate for malignant ventricular arrhythmias. Circ Cardiovasc imaging. 2012;5:12-20.
4.2.5. Các chỉ dấu sinh học
|
Khuyến cáo các chỉ dấu sinh học Các nghiên cứu tham khảo ủng hộ các khuyến cáo được tóm tắt trong phần Tư liệu hỗ trợ online 7. |
||
|
COR |
LOE |
Các khuyến cáo |
|
IIa |
B-NR |
1. Ở những bệnh nhân bệnh tim cấu trúc, đo natriuretic peptide (BNP hoặc N-terminal pro-BNP) có thể hữu ích bằng cách thêm thông tin tiên lượng vào các yếu tố nguy cơ chuẩn để dự đoán SCD hoặc SCA (1-4). |
Văn bản Hỗ trợ Đặc biết cho Khuyến cáo
1. Các nồng độ natriuretic peptides-B-type natriuretic peptide (BNP) hoặc N-terminal pro-BNP liên quan đến tăng nguy cơ SCA và các điều trị ICD thích hợp, ngay cả sau khi điều chỉnh LVEF và các yếu tố nguy cơ khác (1-4). Những dấu hiệu sinh học này cũng tiên đoán tử vong do tim mạch không đột ngột và do đó không chuyên biệt cho nguy cơ SCD đơn thuần. Các peptide Natriuretic cũng đã được đánh giá để dự đoán SCD trong quần thể chung (5, 6). Trong Nghiên cứu Sức khoẻ của Điều dưỡng, N-Terminal BNP tăng lên là một chỉ dấu nguy cơ độc lập cho SCD ở phụ nữ được cho là sức khỏe (5). Đối với quần thể lớn tuổi, nồng độ giới han cao hơn của N-terminal pro-BNP có liên quan đến SCD trong thời gian theo dõi 16 năm (6). Các dấu ấn sinh học này cũng có thể có vai trò tiềm ẩn trong việc tạo điều kiện cho việc xác định các cá nhân có nguy cơ cao về SCD và VA trong dân số nói chung, đặc biệt ở những người có nguy cơ cao về bệnh tim thiếu máu cục bộ, nhưng cần phải nghiên cứu thêm. Việc sử dụng chỉ dấu sinh học đã không cho thấy hữu ích lựa chọn bệnh nhân cho ICD. Một nghiên cứu trên 4431 bệnh nhân cho thấy troponin có độ nhạy cao chỉ là yếu tố tiên đoán yếu cho SCD (7). Tuy nhiên, không có dữ liệu nào cho thấy troponin có độ nhạy cao có thể cải thiện các thuật toán tiên đoán SCD hiện nay hay không.
Tài liệu tham khảo
1. Ahmad T, Fiuzat M, Neely B, et al. Biomarkers of myocardial stress and fibrosis as predictors of mode of death in patients with chronic heart failure. JACC Heart Fail. 2014;2:260-8.
2. Scott PA, Barry J, Roberts PR, et al. Brain natriuretic peptide for the prediction of sudden cardiac death and ventricular arrhythmias: a meta-analysis. Eur J Heart Fail. 2009;11:958-66.
3. Levine YC, Rosenberg MA, Mittleman M, et al. B-type natriuretic peptide is a major predictor of ventricular tachyarrhythmias. Heart Rhythm. 2014;11:1109-16.
4. Berger R, Huelsman M, Strecker K, et al. B-type natriuretic peptide predicts sudden death in patients with chronic heart failure. Circulation. 2002;105:2392-7.
5. Korngold EC,Januzzi JL Jr., Gantzer ML, et al. Amino-terminal pro-B-type natriuretic peptide and high-sensitivity Creactive protein as predictors of sudden cardiac death among women. Circulation. 2009;119:2868-76.
6. Patton KK, Sotoodehnia N, DeFilippi C, et al. N-terminal pro-B-type natriuretic peptide is associated with sudden cardiac death risk: the Cardiovascular Health Study. Heart Rhythm. 2011;8:228-33.
7. Hussein AA, Gottdiener JS, Bartz TM, et al. Cardiomyocyte injury assessed by a highly sensitive troponin assay and sudden cardiac death in the community: the Cardiovascular Health Study. J Am Coll Cardiol. 2013;62:2112-20.
4.2.6. Xem xét di truyền trong các hội chứng rối loạn nhịp
|
Khuyến cáo cho Tư vấn Di truyền* |
||
|
COR |
LOE |
Các khuyên cáo |
|
I |
C-EO |
1. Ở bệnh nhân và các thành viên gia đình ở họ test di truyền để phân tầng nguy cơ cho SCA hoặc SCD được khuyến cáo, tư vấn di truyền là hữu ích. |
*Vui lòng tham khảo mục 7.9 để biết các khuyến cáo cụ thể về bệnh.
Tóm tắt
Việc chẩn đoán hầu hết các hội chứng rối loạn nhịp tim di truyền được dựa trên các đặc điểm lâm sàng và tiền sử gia đình. Sự tiện lợi của test di truyền đối với các hội chứng rối loạn nhịp di truyền có thể: 1) cung cấp cơ hội để xác nhận chẩn đoán lâm sàng nghi ngờ và đôi khi cung cấp thông tin tiên lượng đối với người được nghiên cứu di truyền đầu tiên và 2) cung cấp sàng lọc các thành viên gia đình bị ảnh hưởng khi đột biến gây bệnh được xác định ở người được nghiên cứu di truyền đầu tiên. Hiệu suất của test di truyền thay đổi tuy bệnh. Việc xác minh tính gây bệnh của các đột biến nghi ngờ là một lĩnh vực phát triển, và trình tự tiên đoán đã xác định được một số lượng ngày càng tăng của các biến thể có ý nghĩa không chắc chắn trong quần thể chung (1-5). Khám phá các type gene chó thể có ý nghĩa điều trị cho một số kiểu hình rối loạn nhịp chẳng hạn như hội chứng QT dài và bệnh Fabry (6-9), ở đó đột biến bệnh lý đơn gene đã được xác định rõ, nguy cơ cho các cá thể đột biến dương tính đã được nghiên cứu rộng, và điều trị hiệu quả liên quan đến đột biến có thẻ được thực hiện. Trong các bệnh khác, chẳng hạn hội chứng Brugada, vai trò của đột biến đơn gene gây bệnh rõ ràng ít chắc chắn hơn, và kiểu gen không cung cấp thông tin điều trị hoặc tiên lượng cho người được nghiên cứu di truyền (5, 10-12). Trong bệnh cơ tim thất phải gây rối loạn nhịp, vài cá thể dương tính đột biến không phát triển bệnh, cho thấy các đột biến và tương tác môi trường khác có thể ảnh hưởng đến sự phát triển lâm sàng của bệnh (13- 16). Điều quan trọng là sự vắng mặt của đột biến di truyền đã được xác định không loại trừ sự hiện diện của bệnh và do đó việc theo dõi tiếp tục và ra quyết định được thực hiện dựa trên kiểu hình lâm sàng. Type gene thường hữu ích nhất khi đột biến bệnh lý được xác nhận ở người được nghiên cứu di truyền, như tầm soát có thể được áp dụng đối với người thân ở giai đoạn tiền lâm sàng, cho phép thay đổi sinh hoạt, điều trị, hoặc tiếp tục theo dõi những người có đột biến gene dương tính (7 ). Xem Phần 7.9 để biết các khuyến cáo về bệnh.
Đối với những bệnh nhân trẻ (<40 tuổi) không mắc bệnh tim cấu trúc có ngừng tim không giải thích được, gần đuối nước không giải thích được, hoặc ngất khi gắng sức tái phát, test di truyền có thể rất quan trọng để xác định một hội chứng loạn nhịp di truyền được coi là nguyên nhân (17-23).
Văn bản Hỗ trợ Đặc biệt – Khuyến cáo
1. Quyết định tiến hành thử nghiệm di truyền đòi hỏi phải có thảo luận về việc sử dụng lâm sàng thông tin di truyền để thu thập được cho cả người được thử nghiệm trước tiên và các thành viên trong gia đình cũng như xem xét những liên quan quan trọng về tâm lý, tài chính, việc làm, tàn phế và bảo hiểm nhân thọ của các type gene dương tính (17, 18, 20, 24). Cân bằng quyền riêng tư của thông tin chăm sóc sức khoẻ cho người được test di truyền đầu tiên với “quyền biết” cho các thành viên trong gia đình và khả năng cung cấp thông tin thích hợp cho tất cả các thành viên trong gia đình bị ảnh hưởng một cách tiềm tàng có thể là thách thức trên nhiều mức độ, gồm biến đổi trong gia đình, khoảng cách gần về địa lý, và tiếp cận chăm sóc sức khỏe (25). Vì những lý do này, tư vấn di truyền thường thực hiện ra trước khi tiến hành test di truyền, và, theo quan điểm của bệnh nhân, được cung cấp bởi các cố vấn di truyền một cách tối ưu, nếu có, với sự hợp tác của các bác sĩ (26, 27). Cách tiếp cận kết hợp tư vấn di truyền với hướng dẫn y tế có thể cân bằng một cách hợp lý quyết định về việc test di truyền có mang lại lợi ích trên cơ sở cá nhân hay không.
Tài liệu tham khảo
1. Andreasen C, Refsgaard L, Nielsen JB, et al. Mutations in genes encoding cardiac ion channels previously associated with sudden infant death syndrome (SIDS) are present with high frequency in new exome data. Can J Cardiol. 2013;29:1104-9.
2. Jabbari J, Jabbari R, Nielsen MW, et al. New exome data question the pathogenicity of genetic variants previously associated with catecholaminergic polymorphic ventricular tachycardia. Circ Cardiovas Genetics. 2013;481-9.
3. Paludan-Muller C, Ahlberg G, Ghouse J, et al. Integration of 60,000 exomes and ACMG guidelines question the role of catecholaminergic polymorphic ventricular tachycardia-associated variants. Clin Genet. 2017;91:63-72.
4. Refsgaard L, Holst AG, Sadjadieh G, et al. High prevalence of genetic variants previously associated with LQT syndrome in new exome data. Eur J Hum Genet. 2012;20:905-8.
5. Risgaard B, Jabbari R, Refsgaard L, et al. High prevalence of genetic variants previously associated with Brugada syndrome in new exome data. Clin Genet. 2013;84:489-95.
6. Costa J, Lopes CM, Barsheshet A, et al. Combined assessment of sex- and mutation-specific information for risk stratification in type 1 long QT syndrome. Heart Rhythm. 2012;9:892-8.
7. Hershberger RE, Lindenfeld J, Mestroni L, et al. Genetic evaluation of cardiomyopathy–a Heart Failure Society of America practice guideline. J Cardiac Fail. 2009;15:83-97.
8. Kim JA, Lopes CM, Moss AJ, et al. Trigger-specific risk factors and response to therapy in long QT syndrome type 2. Heart Rhythm. 2010;7:1797-805.
9. Migdalovich D, Moss AJ, Lopes CM, et al. Mutation and gender-specific risk in type 2 long QT syndrome: implications for risk stratification for life-threatening cardiac events in patients with long QT syndrome. Heart Rhythm. 2011;8:1537-43.
10.Crotti L, Marcou CA, Tester DJ, et al. Spectrum and prevalence of mutations involving BrS1- through BrS12- susceptibility genes in a cohort of unrelated patients referred for Brugada syndrome genetic testing: implications for genetic testing. J Am Coll Cardiol. 2012;60:1410-8.
11.Probst V, Wilde AA, Barc J, et al. SCN5A mutations and the role of genetic background in the pathophysiology of Brugada syndrome. Circ Cardiovas Genetics. 2009;2:552-7.
12.Dintzis RZ. Genetic variation and the meiotic process.Res Publ Assoc Res Nerv Ment Dis. 1991;69:39-46.
13.Groeneweg JA, Bhonsale A, James CA, et al. Clinical presentation, long-term follow-up, and outcomes of 1001 arrhythmogenic right ventricular dysplasia/cardiomyopathy patients and family members. Circ Cardiovasc Genet. 2015;8:437-46.
14.Marcus FI, Edson S, Towbin JA. Genetics of arrhythmogenic right ventricular cardiomyopathy: a practical guide for physicians. J Am Coll Cardiol. 2013;61:1945-8.
15.Quarta G, Muir A, Pantazis A, et al. Familial evaluation in arrhythmogenic right ventricular cardiomyopathy: impact of genetics and revised task force criteria. Circulation. 2011;123:2701-9.
16.Rigato I, Bauce B, Rampazzo A, et al. Compound and digenic heterozygosity predicts lifetime arrhythmic outcome and sudden cardiac death in desmosomal gene-related arrhythmogenic right ventricular cardiomyopathy. Circ Cardiovasc Genet. 2013;6:533-42.
17.Ackerman MJ, Priori SG, Willems S, et al. HRS/EHRA expert consensus statement on the state of genetic testing for the channelopathies and cardiomyopathies: this document was developed as a partnership between the Heart Rhythm Society (HRS) and the European Heart Rhythm Association (EHRA). Europace. 2011;13:1077-109.
18.Gollob MH, Blier L, Brugada R, et al. Recommendations for the use of genetic testing in the clinical evaluation of inherited cardiac arrhythmias associated with sudden cardiac death: Canadian Cardiovascular Society/Canadian Heart Rhythm Society joint position paper. Can J Cardiol. 2011;27:232-45.
19.Kumar S, Peters S, Thompson T, et al. Familial cardiological and targeted genetic evaluation: low yield in sudden unexplained death and high yield in unexplained cardiac arrest syndromes. Heart Rhythm. 2013;10:1653-60.
20.Priori SG, Wilde AA, Horie M, et al. HRS/EHRA/APHRS expert consensus statement on the diagnosis and management of patients with inherited primary arrhythmia syndromes. Heart Rhythm. 2013;10:1932-63.
21.Tester DJ, Medeiros-Domingo A, Will ML, et al. Unexplained drownings and the cardiac channelopathies: a molecular autopsy series. Mayo Clin Proc. 2011;86:941-7.
22.Tzimas I, Zingraf JC, Bajanowski T, et al. The role of known variants of KCNQ1, KCNH2, KCNE1, SCN5A, and NOS1AP in water-related deaths. Int J Legal Med. 2016;130:1575-9.
23.Wang D, Shah KR, Um SY, et al. Cardiac channelopathy testing in 274 ethnically diverse sudden unexplained deaths. Forensic Sci Int. 2014;237:90-9.
24.Laedtke AL, O’Neill SM, Rubinstein WS, et al. Family physicians’ awareness and knowledge of the Genetic Information Non-Discrimination Act (GINA). J Genet Couns. 2012;21:345-52.
25.Vavolizza RD, Kalia I, Erskine AK, et al. Disclosing genetic information to family members about inherited cardiac arrhythmias: an obligation or a choice? J Genet Couns. 2015;24:608-15.
26.Christiaans I, van Langen IM, Birnie E, et al. Genetic counseling and cardiac care in predictively tested hypertrophic cardiomyopathy mutation carriers: the patients’ perspective. Am J Med Genet. Part A. 2009;149a:1444-51.
27.Hamang A, Eide GE, Rokne B, et al. Predictors of heart-focused anxiety in patients undergoing genetic investigation and counseling of long QT syndrome or hypertrophic cardiomyopathy: a one year follow-up. J Genet Counsel. 2012;21:72-84.
4.3. Test xâm lấn
4.3.1. Hình ảnh Tim Xâm lấn: Catheter Tim hoặc Chụp mạch CT
|
Khuyến cáo cho Hình ảnh Xâm lấn: Catheter Tim |
||
|
COR |
LOE |
Khuyến cáo |
|
I |
C-EO |
1. Ở những bệnh nhân đã phục hồi từ SCD không giải thích được, CT hoặc chụp mạch vành xâm lấn là hữu ích để khẳng định sự hiện diện hoặc vắng mặt của bệnh tim thiếu máu cục bộ và hướng dẫn quyết định cho tái tuần hoàn cơ tim. |
Văn bản Hỗ trợ Đặc biệt – Khuyến cáo
1. Mặc dù các nghiên cứu ngẫu nhiên còn chưa có, chụp mạch vành đóng vai trò quan trọng trong việc tính toán hoặc loại trừ sự hiện diện của bệnh tim thiếu máu tắc nghẽn đáng kể ở các bệnh nhân có SCA hoặc những người có VA nguy hiểm đến tính mạng (1-4). VT đa hình tái phát hoặc VF có thể là do thiếu máu cơ tim tiếp diễn liên quan đến tái tuần hoàn vành. Sự hiện diện của ST chênh lên ở ECG trước trước khi hồi sức hoặc sau khi hồi sức sớm gợi ý thiếu máu cục bộ và ACS tiềm ẩn đảm bảo chụp mạch khẩn trương và tái tuần hoàn (5). Sự chênh lên của ST cũng có thể là kết quả của co thắt mạch vành hoặc sốc điện (sốc bằng dòng điện môt chiều: DC). Sự vắng mặt chênh lên của ST sau ngừng tim không loại trừ tổn thương mạch vành tắc nghễn hoặc huyết khối. Chụp mạch vành có thể không đảm báo được nếu nguyên nhân SCA không phải do thiếu máu cơ tim cục bộ được xác định. Chụp mạch vành hoặc chụp CT mạch vành cũng có tầm quan trọng loại trừ sự hiện diện của nguồn gốc bất thường giải phẫu của động mạch vành có thể gây ra SCD.
Tài liệu tham khảo
1. Dumas F, Bougouin W, Geri G, et al. Emergency PCI in post-cardiac arrest patients without ST-segment elevation pattern: insights from the PROCAT II registry. JACC Cardiovasc Interv. 2016;9:1011-8.
2. Cronier P, Vignon P, Bouferrache K, et al. Impact of routine percutaneous coronary intervention after out-of-hospital cardiac arrest due to ventricular fibrillation. Crit Care. 2011;15:R122.
3. Spaulding CM, Joly LM, Rosenberg A, et al. Immediate coronary angiography in survivors of out-of-hospital cardiac arrest. N Engl J Med. 1997;336:1629-33.
4. Zanuttini D, Armellini I, Nucifora G, et al. Impact of emergency coronary angiography on in-hospital outcome of unconscious survivors after out-of-hospital cardiac arrest. Am J Cardiol. 2012;110:1723-8.
5. O’Gara PT, Kushner FG, Ascheim DD, et al. 2013 ACCF/AHA guideline for the management of ST-elevation myocardial infarction: a report of the American College of Cardiology Foundation/American Heart Association Task Force on Practice Guidelines.Circulation. 2013;127:e362-425.
4.3.2. Nghiên cứu điện sinh lý cho VA
|
Khuyến cáo nghiên cứu điện sinh lý Các nghiên cứu tham khảo ủng hộ các khuyến cáo được tóm tắt trong phần Tư liệu hỗ trợ online 8 và 9 |
||
|
COR |
LOE |
Khuyến cáo |
|
IIa |
B-R |
1. Ở những bệnh nhân bệnh cơ tim thiếu máu cục bộ, bệnh cơ tim không do thiếu máu cục bộ (NICM), hoặc bệnh tim bẩm sinh ở người lớn bị ngất hoặc những triệu chứng khác của VA và không có chỉ định cho ICD dự phòng tiên phát, nghiên cứu điện sinh lý có thể hữu ích để đánh giá nguy cơ VT dai dẳng (1- 7). |
|
III: no benefit |
B-R |
2. Ở những bệnh nhân đáp ứng các tiêu chuẩn cho cấy ICD, nghiên cứu điện sinh lý học vì lý do duy nhất tạo ra VA không được chỉ định cho phân tầng nguy cơ (8-11). |
|
III: no benefit |
B-R |
3. Nghiên cứu điện sinh lý không được khuyến cáo cho phân tầng nguy cờ cho VA trong tình huống hội chứng QT dài, nhịp nhanh thất đa hình do catecholamine, hội chứng QT ngắn hoặc hội chứng tái cực sớm (12-16) |
Tóm tắt
Nghiên cứu điện sinh lý học có thể được sử dụng để gây VA dai dẳng ở các bệnh nhân đã biết có VA hoặc nghi ngờ. Với sự xuất hiện của ICD và lợi ích của nó đã được chứng minh trong ngừa SCD nguyên phát và thứ phát, có ít chỉ định cho kích thích có chương trình để thúc đẩy VA. Các bệnh nhân HF và LVEF < 35% nói chung sẽ có chỉ định cho ICD và sự khởi phát chuyên biệt của VT / VF trước khi cấy là không cần thiết. Bệnh nhân có LVEF > 35% và ngất không được giải thích hoặc gần ngất có thể có lợi từ nghiên cứu điện sinh lý để xác định xem VT / VF là nguyên nhân gây ra triệu chứng và hướng dẫn điều trị tiếp theo. Thúc đẩy VT / VF thường được thực hiện trước khi triệt phá qua catheter nền loạn nhịp để hướng dẫn thủ thuật và xác định thành công của can thiệp sau triệt phá được thực hiện. Nghiên cứu điện sinh lý có thể được sử dụng để xác định cơ chế nhịp nhanh phức bộ rộng. Xem các Phần 7.3, 7.4, 7.6, 7.9.1.3, và 10.8 các khuyến cáo về nghiên cứu điện sinh lý đối với các trạng thái bệnh cụ thể.
Văn bản Hỗ trợ Đặc biệt – Khuyến cáo
1. Một nghiên cứu test điện sinh lý ở các bệnh nhân NICM có triệu chứng cho thấy 28% bệnh nhân có khả năng tạo ra VT / VF có liên quan đến tần số các biến cố ICD cao hơn trong quá trình theo dõi (17). Trong một nghiên cứu thuần tập tiền cứu 180 bệnh nhân bị thiếu máu cục bộ hoặc MICM và ngất, có thể tạo ra VT hoặc VF trong nghiên cứu điện sinh lý được tương quan với tử suất tim chỉ ở các bệnh nhân có bệnh tim thiếu máu cục bộ. Ở các bệnh nhân NICM, tử suất tim tương quan với LVEF nhưng không tương quan với khả năng tạo ra trên nghiên cứu điện sinh lý (18).
2. Ở các bệnh nhân đáp ứng các tiêu chuẩn cho cấy ICD (ví dụ HF và LVEF ≤ 35%), dữ liệu không ủng hộ sử dụng phổ biến nghiên cứu điện sinh lý đơn thuần cho phân tầng nguy cơ, chẳng hạn các bệnh nhân đã được chỉ ra để chứng minh lợi ích sống sót từ ICD (8-11). Tuy nhiên, nghiên cứu điện sinh lý học có thể hữu ích ở những bệnh nhân được lựa chọn nghi ngờ có kích thích sớm hoặc rối loạn nhịp trên thất như là nguyên nhân của các triệu chứng hoặc nhịp nhanh phức hợp rộng đảm bảo chẩn đoán xác định và điều trị dứt khoát. SVT dẫn đến VT / VF hoặc SVT dẫn truyền lệch hướng có thể cũng bị nghi ngờ ở các bệnh nhân trẻ hơn hoặc những người đó có LVEF bảo tồn. Tạo ra Khởi SVT và triệt phá có thể sau đó có thể được điều trị, không cần dùng ICD. Trong những trường hợp như vậy, không thể tạo ra VT / VF sau khi loại bỏ chất nền cho SVT sẽ được mong đợi.
3. Phân tầng nguy cơ đối với bệnh kênh thường được thực hiện trên cơ sở các triệu chứng, ECG (13, 19-24), test gắng sức treadmill (25-27) và kết quả xét nghiệm di truyền (28-32). Nghiên cứu điện sinh lý học (ví dụ kích thích thất có chương trình) không có giá trị tiên lượng cho phân tầng nguy cơ ở những bệnh nhân bệnh kênh (12-15).
Tài liệu tham khảo
1. Buxton AE, Lee KL, DiCarlo L, et al. Electrophysiologic testing to identify patients with coronary artery disease who are at risk for sudden death. Multicenter Unsustained Tachycardia Trial Investigators. N Engl J Med 2000;342:1937- 45.
2. Buxton AE, Lee KL, Hafley GE, et al. Relation of ejection fraction and inducible ventricular tachycardia to mode of death in patients with coronary artery disease: an analysis of patients enrolled in the multicenter unsustained tachycardia trial. Circulation. 2002;106:2466-72.
3. Costantini O, Hohnloser SH, Kirk MM, et al. The ABCD (Alternans Before Cardioverter Defibrillator) Trial: strategies using T-wave alternans to improve efficiency of sudden cardiac death prevention. J Am Coll Cardiol. 2009;53:471-9.
4. Bourke JP, Richards DA, Ross DL, et al. Routine programmed electrical stimulation in survivors of acute myocardial infarction for prediction of spontaneous ventricular tachyarrhythmias during follow-up: results, optimal stimulation protocol and cost-effective screening. J Am Coll Cardiol. 1991;18:780-8.
5. Bailey JJ, Berson AS, Handelsman H, et al. Utility of current risk stratification tests for predicting major arrhythmic events after myocardial infarction. J Am Coll Cardiol. 2001;38:1902-11.
6. Schmitt C, Barthel P, Ndrepepa G, et al. Value of programmed ventricular stimulation for prophylactic internal cardioverter-defibrillator implantation in postinfarction patients preselected by noninvasive risk stratifiers. J Am Coll Cardiol. 2001;37:1901-7.
7. Hilfiker G, Schoenenberger AW, Erne P, et al. Utility of electrophysiological studies to predict arrhythmic events. World J Cardiol. 2015;7:344-50. 8. Bardy GH, Lee KL, Mark DB, et al. Amiodarone or an implantable cardioverter-defibrillator for congestive heart failure. N Engl J Med. 2005;352:225-37.
9. Buxton AE, Lee KL, Fisher JD, et al. A randomized study of the prevention of sudden death in patients with coronary artery disease. Multicenter Unsustained Tachycardia Trial Investigators. N Engl J Med. 1999;341:1882-90.
10.Moss AJ, Hall WJ, Cannom DS, et al. Improved survival with an implanted defibrillator in patients with coronary disease at high risk for ventricular arrhythmia. Multicenter Automatic Defibrillator Implantation Trial Investigators. N Engl J Med. 1996;335:1933-40.
11.Moss AJ, Zareba W, Hall WJ, et al. Prophylactic implantation of a defibrillator in patients with myocardial infarction and reduced ejection fraction. N Engl J Med. 2002;346:877-83.
12.Bhandari AK, Shapiro WA, Morady F, et al. Electrophysiologic testing in patients with the long QT syndrome. Circulation. 1985;71:63-71.
13.Giustetto C, Di MF, Wolpert C, et al. Short QT syndrome: clinical findings and diagnostic-therapeutic implications. Eur Heart J. 2006;27:2440-7.
14.Giustetto C, Schimpf R, Mazzanti A, et al. Long-term follow-up of patients with short QT syndrome. J Am Coll Cardiol. 2011;58:587-95.
15.Mahida S, Derval N, Sacher F, et al. Role of electrophysiological studies in predicting risk of ventricular arrhythmia in early repolarization syndrome. J Am Coll Cardiol. 2015;65:151-9.
16.Priori SG, Napolitano C, Memmi M, et al. Clinical and molecular characterization of patients with catecholaminergic polymorphic ventricular tachycardia. Circulation. 2002;106:69-74.
17.Gatzoulis KA, Vouliotis AI, Tsiachris D, et al. Primary prevention of sudden cardiac death in a nonischemic dilated cardiomyopathy population: reappraisal of the role of programmed ventricular stimulation. Circ Arrhythm Electrophysiol. 2013;6:504-12.
18.Brembilla-Perrot B, Suty-Selton C, Beurrier D, et al. Differences in mechanisms and outcomes of syncope in patients with coronary disease or idiopathic left ventricular dysfunction as assessed by electrophysiologic testing. J Am Coll Cardiol. 2004;44:594-601.
19.Garson AJr, Dick M, Fournier A, et al. The long QT syndrome in children. An international study of 287 patients. Circulation. 1993;87:1866-72. 20.Hobbs JB, Peterson DR, Moss AJ, et al. Risk of aborted cardiac arrest or sudden cardiac death during adolescence in the long-QT syndrome. JAMA. 2006;296:1249-54.
21.Iribarren C, Round AD, Peng JA, et al. Short QT in a cohort of 1.7 million persons: prevalence, correlates, and prognosis. Ann Noninvasive Electrocardiol. 2014;19:490-500.
22.Kaufman ES, McNitt S, Moss AJ, et al. Risk of death in the long QT syndrome when a sibling has died. Heart Rhythm. 2008;5:831-6.
23.Kimbrough J, Moss AJ, Zareba W, et al. Clinical implications for affected parents and siblings of probands with longQT syndrome. Circulation. 2001;104:557-62.
24.Mazzanti A, Kanthan A, Monteforte N, et al. Novel insight into the natural history of short QT syndrome. J Am Coll Cardiol. 2014;63:1300-8.
25.Wong JA, Gula LJ, Klein GJ, et al. Utility of treadmill testing in identification and genotype prediction in long-QT syndrome. Circ Arrhythm Electrophysiol. 2010;3:120-5.
26.Walker BD, Krahn AD, Klein GJ, et al. Burst bicycle exercise facilitates diagnosis of latent long QT syndrome. Am Heart J. 2005;150:1059-63.
27.Waks JW, Sitlani CM, Soliman EZ, et al. Global electric heterogeneity risk score for prediction of sudden cardiac death in the general population: the Atherosclerosis Risk in Communities (ARIC) and Cardiovascular Health (CHS) Studies. Circulation. 2016;133:2222-34.
28.Priori SG, Napolitano C, Schwartz PJ, et al. Association of long QT syndrome loci and cardiac events among patients treated with beta-blockers. JAMA. 2004;292:1341-4.
29.Priori SG, Schwartz PJ, Napolitano C, et al. Risk stratification in the long-QT syndrome. N Engl J Med. 2003;348:1866- 74.
30.Wedekind H, Burde D, Zumhagen S, et al. QT interval prolongation and risk for cardiac events in genotyped LQTSindex children. Eur J Pediatr. 2009;168:1107-15.
31.Goldenberg I, Horr S, Moss AJ, et al. Risk for life-threatening cardiac events in patients with genotype-confirmed long-QT syndrome and normal-range corrected QT intervals. J Am Coll Cardiol. 2011;57:51-9.
5. Trị liệu cho điều trị hoặc ngăn ngừa VA
5.1. Trị liệu thuốc.
Ngoại trừ các thuốc chẹn beta (ví dụ: metoprolol succinate, carvedilol), không có bằng chứng từ các RCTs, các thuốc chống loạn nhịp cho VA cải thiên sống sót khi được sử dụng để phòng ngừa SCD tiên phát và thứ phát. Tuy nhiên, việc sử dụng các loại thuốc này là cần thiết ở một số bệnh nhân để kiểm soát loạn nhịp và cải thiện triệu chứng. Sử dụng thuốc cho VA được thảo luận và bất kỳ khuyến cáo nào đã được liệt kê, trong các phần tiếp theo. Hơn nữa, thúc đẩy loạn nhịp được tạo ra do thuốc được đề cập trong Phần 10.7.
Các thuốc chống loạn nhịp thường được phân loại theo biểu đồ 4 cấp của Vaughan Williams (class I: thuốc chẹn kênh natri nhanh, class II: thuốc chẹn bêta II, class III: chẹn dòng kali tái cực; class IV: thuốc chẹn kênh canxi nondihydropyridin) (1). Hệ thống này không đề cập đến sự phức tạp trong thuốc chống loạn nhịp, vì hầu hết các tác nhân có nhiều tác dụng. Bảng 7 cho biết các tác dụng, ảnh hưởng điện sinh lý, tác dụng dược lý, và các tác dụng phụ thường gặp của thuốc chống loạn nhịp.
Bảng 7.Các Đặc tính Dược lý của các thuốc chống loạn nhịp có khả năng cho điều trị VA
|
Các thuốc chống loạn nhịp (Class) và liều |
Sử dụng trong VA/SCA |
Đích |
Các ảnh hưởng điện sinh lý học |
Các đặc tính dược lý học |
Các tác dụng phụ thường gặp |
|
Acebutolol uống (PO) 200–1200 mg mỗi ngày hoặc lên đến 600 mg hai lần ngày (bid) |
VT, PVCs |
Beta 1, hoạt hóa giao cảm nội tại nhẹ |
Tần số xoang bị chậm lại do thời gian trơ của nút AV tăng lên |
t1/2 của chất chuyển hóa hoạt hoa Hoạt tính chuyển hóa: 8-13 h. (Bị kéo dài khi suy thận) Chuyển hóa: Gan Thải tiết: phân 60%, thận 40% |
Tim: Nhịp chậm, hạ huyết áp, HF, AVB Triệu chứng khác: Chóng mặt, mệt mỏi, lo lắng, bất lực, tăng / giảm ngủ |
|
Amiodarone (III) IV: 300 mg bolus cho VF/ VT ngừng vô mạch ; 150-mg bolus cho VT ổn định; 1 mg/min x 6 h, sau đó 0.5 mg/min x 18 h Uống (PO): 400 mg* q 8 đến 12 h trong 1– 2 tuần, sau đó 300- 400 mg hàng ngày; giảm liều đến 200 mg hàng ngày nếu có thể |
VT, VF, PVC, |
INa, ICa, IKr, IK1, IKs, Ito, thụ thể Beta, thụ thể Alpha, nuclear T3 receptor |
Tần số xoang bị chậm xuống QRS bị kéo dài QTc bị kéo dài Thời gian trơ nút AV tăng lên; DFT tăng lên |
t1/2: 26-107 ngày Chuyển hóa: Thải tiết qua gan: phân |
Tim: Hạ huyết áp, nhịp chậm, AVB, TdP, làm chậm VT dưới tần số phát hiện được ICD lập trình, ngưỡng khử rung tăng lên Các triệu chứng khác: Viêm mô màng ngoài tròng, bất thường tuyến giáp, thiếu máu, buồn nôn, nôn mửa, táo bón, nhạy cảm ánh sáng, đổi màu da, mất thẩm mỹ, chóng mặt, bệnh thần kinh ngoại vi, run, viêm gan, xơ gan, xơ phổi hay viêm phổi |
|
Atenolol (II) Uống (PO): 25–100 mg một lần hoặc hai lần ngày |
VT, PVC, ARVC, LQTS |
Beta 1 |
Tần số xoang bị chậm lại do thời gian trơ của nút AV tăng lên |
t1/2: 6–7 h (bị kéo dài với suy thận) Chuyển hóa: Thải tiết gan: phân 50%, thận 40% |
Tiem: Nhịp chậm, hạ huyết áp, HF, AVB Các triệu chứng khác: chóng mặt, mệt, trầm chảm, bất lực |
|
Bisoprolol (II) PO: 2.5–10 mg once daily |
VT, PVC |
Thụ thể Beta 1 |
Tần số xoang bị chậm xuống thời gian trơ nút AV tăng lên |
t1/2: 9–12 h Chuyển hóa: Thải tiết gan: phân |
Tim: Đau ngực, nhịp chậm, AVB Khác: Mệt mỏi, mất ngủ, tiêu chảy |
|
Carvedilol (II) uống (PO): 3.125–25 mg q 12 h |
VT, PVC |
Thụ cảm thể alpha Beta 1 và 2 |
Tần số xoang bị chậm xuống thời gian trơ nút AV tăng lên |
t1/2: 7–10 h Chuyển hóa: Thải tiết gan: phân |
Tim mạch: nhịp chậm, hạ huyết áp, AVB, phù, ngất Khác: tăng glucose, chóng mặt, mệt mỏi, tiêu chảy |
|
Diltiazem (IV) IV: 5-10 mg, mỗi ngày15-30 phút Thải tiết chậm: PO: 120-360 mg / ngày |
VT đặc biệt RVOT, LVT nguyên phát |
ICa-L |
Tần số xoang bị chậm xuống PR bị kéo dài dẫn truyền nút AV bị chậm xuống |
t1 / 2: Tiêm 2 – 5 giờ, phóng thích ngay 4,5-12 giờ, phóng thích kéo dài 12 giờ và suy gan nặng 14-16 h Chuyển hóa: Thải tiết gan: thận |
Tim: Hạ huyết áp, phù, HF, AVB, nhịp chậm, trầm trọng HFrEF Khác: Nhức đầu, phát ban, táo bón |
|
Esmolol (II) IV: 0.5 mg/kg bolus, 0.05 mg/kg/phút |
VT |
Thụ cảm thể Beta 1 |
Tần số xoang bị chậm xuống Trơ nút AV bị tăng lên |
t1 / 2: 9 phút Chuyển hóa: Phân hủy và thoái biên một phần RBC Thải tiết: thận |
Tim mạch: nhịp chậm, hạ huyết áp, HF, AVB Khác: Chóng mặt, buồn nôn |
|
Flecainide (IC) PO: 50–200 mg q 12 h |
VT, PVC (khi không có bệnh tim cấu trúc). Có vai trò điều trị bệnh nhân với CPVT |
INa, IKr, IKur |
PR kéo dài QRS kéo dài; DFT tăng lên |
t1/2: 7-22 giờ Chuyển hóa: Thải tiết gan: thận |
Tim: Rối loạn chức năng nút xoang, AVB, hội chứng Brugada thúc đẩy do thuốc. VT đơn hình ở bệnh nhân bị sẹo do cơ tim, trầm trọng HFrEF Khác: Chóng mặt, run, rối loạn thị lực, khó thở, buồn nôn |
|
Lidocaine (IB) IV: 1 mg / kg bolus, 1-3 mg / phút1-1,5 mg / kg. Lặp lại 0.5- 0.75 mg / kg bolus mỗi 5 – 10 phút (liều tích lũy tối đa 3 mg / kg). Truyền duy trì 1-4 mg / phút, mặc dù người ta có thể bắt đầu bắt đầu ở 0.5 mg / phút. |
VT, VF |
INa |
Ảnh hưởng không đáng kể lên hầu hết các khoảng thời gian; QTc có thể ngắn lại chút it |
Khởi đầu t1/2 7–30 phút; cuối 90–120 phút. Kéo dài trong HF, bệnh gan, sốc, bệnh thận nặng Chuyển hóa: thái tiết gan: thận |
Tim: Nhịp tim chậm, suy sụp huyết động, AVB, ngậm xoang Khác: mê sảng, rối loạn tâm thần, động kinh, buồn nôn, ù tai, khó thở, co thắt phế quản |
|
Metoprolol (II)IV: 5 mg mỗi 5 min đến 3 liều uống (PO): 25-100 mg Giải phóng kéo dài mỗi ngày hoặc mỗi 12 h |
VT, PVC |
Thụ thể Beta 1 |
Tần số xoang bị châm xuống Thỏi gian trơ nút AV bị tăng lên
|
t1/2: 3–4 giời Chuyển hóa: Thải tiết gan: thận |
Tim: nhịp chậm, hạ huyết áp, AVB Khác: Chóng mặt, mệt mỏi, tiêu chảy, trầm cảm, khó thở |
|
Mexiletine (IB) uống (PO): 150-300 mg, mỗi 8 h hoặc mỗi 12 giờ |
T, VF, PVC, có vai trò ở các bệnh nhân LQT3 |
INa |
Không có hiệu quả đáng kể lên hầu hết các khoảng thời gian; QTc có thể ngắn lại chút ít |
t1/2: 10–14 h Chuyển hóa: gan: thận |
Tim: HF, AVB Khác: chóng mặt, run, thất điểu, dị cảm, buồn nôn, rối loạn các tế bào máu (dyscrasias) |
|
Nadolol (II) PO: 40–320 mg daily |
VT, PVC, LQTS, CPVT |
Các thụ thể Beta 1 và 2 |
Tần số xoang bị chậm xuống thời gian trơ nút AV tăng lên |
t1/2: 20–24 giờ Chuyển hóa: Không Thải tiết: thận |
Tim: nhịp tim chậm, Hạ huyết áp, HF, AVB Khác: phù, chóng mặt, lạnh đầu chi, co thắt phế quản |
|
Procainamide (IA) IV: liều tấn công 10-17 mg / kg ở liều 20-50 mg / phút Liều duy trì: 1-4 mg / phút uống (PO) (Chuẩn bị SR): 500-1250 mg, 6 giờ |
VT |
INa, IKr |
QRS kéo dài QTc kéo dài; DFT tăng lên |
Chuyển hóa: H t1 / 2: 2-5 h; NAPA 6-8 h t 1/2 kéo dài trong rối loạn chức năng thận. Thiếu thận: hoạt động 11 giờ và NAPA 42 giờ Thải tiết: thận |
Tim: TdP; AVB, hạ huyết áp và trầm trọng HFrEF Khác: Các triệu chứng Lupus, tiêu chảy, buồn nôn, rối loạn các tế bào máu |
|
Propafenone (IC) uống (PO): Khởi phát ngay tức thì 150- 300 mg mỗi 8 giờ Thải tiết kéo dài 225-425 mg mỗi12 giờ |
VT, PVC (trong trường hợp không có bệnh tim cấu trúc) |
INa, IKr, IKur, Thụ cảm thể Beta, Alpha |
PR kéo dài QRS kéo dài; DFT tăng lên |
t1 / 2: 2-10 giờ hoặc 10-32 giời t1 / 2: chuyển hóa mở rộng 2- 10 giờ; chuyển hóa kém 10-32 giờ. Chuyển hóa: Thải tiết ở gan: thận |
Tim: HF, AVB, hội chứng Brugada do thuốc gây ra Khác: Chóng mặt, mệt mỏi, buồn nôn, tiêu chảy, khô miệng (xerostomia), run, thị lực mờ |
|
Propranolol (II) IV: 1-3 mg q 5 min đến tổng cộng 5 mg uống (PO): Thải tiết tực thời 10-40 mg mỗi 6 h; Thải tiết kéo dài 60-160 mg mỗi 12 giờ |
VT, PVC, LQTS |
Thụ cảm thể Beta 1 và 2, INa |
Tần số xoang bị chậm Thời gian trơ nút AV tăng lên |
t1/2: thải tiết ngay lập tức 3–6 giờ Thải tiết kéo dài 8–10 giờ Chuyển hóa: Thải tiết: thận |
Tim: Nhịp chậm, hạ huyết áp, HF, AVB Khác: rối loạn giấc ngủ, chóng mặt, ác mộng, tăng đường huyết, tiêu chảy, co thắt phế quản |
|
Quinidine (IA) uống: muối sulfat 200-600 mg mỗi 6 giờ đến mỗi 12 giờ muối gluconat 324-648 mg mỗi 8 h đến mỗi 12 giờ IV: liều tấn công: 800 mg trong 50 ml tiêm 50 mg / phút |
T, VF, (gồm hội chứng QT ngắn, Brugada)
|
INa, Ito, IKr, M, Thụ thể Alpha |
QRS kéo dài QTc kéo dài; DFT tăng lên |
t1 / 2: 6-8 giờ dài hơn trong HF, xơ gan và với người cao tuổi Chuyển hóa: Thải tiết ở gan: thận |
Tim: Ngất, TdP, AVB Khác: Chóng mặt, tiêu chảy, buồn nôn, viêm thực quản, nôn vọt, ù tai, mờ mắt, nổi ban, yếu, run; rối loạn tế bào máu |
|
Ranolazine (không phân loại) uống (PO): 500-1000 mg mỗi 12 giờ |
VT |
INa, IKr |
Tần số xoang bị chậm Tc bị kéo dài |
t1/2: 7 giờ Chuyển hóa: Thải tiết gan: thận 75%, F 25% |
Tim: Nhịp chậm, hạ huyết áp Khác: Nhức đầu, chóng mặt, ngất, buồn nôn, khó thở |
|
Sotalol (III) IV: 75 mg mỗi 12 giờ uống (PO): 80-120 mg mỗi 12 giờ, có thể tăng liều mỗi 3 ngày; tối đa 320 mg / ngày |
VT, VF, PVC |
IKr, thụ thể Beta 1 và 2 |
Tần số xoang bị chậm xuống QTc kéo dài Thời gian trơ của nút AV tăng lên DFT giảm xuống |
t1/2: 12 giờ Chuyển hóa: Không bài tiết: thận |
Tim: Nhịp chậm, hạ huyết áp, HF, ngất, TdP Khác: Mệt mỏi, chóng mặt, yếu, khó thở, viêm phế quản, trầm cảm, buồn nôn, tiêu chảy |
|
Verapamil (IV) IV: 2,5-5 mg mỗi 15-30 phút Thải tiết kéo gài uống (PO): 240-480 mg / ngày |
VT (đặc biết RVOT, LVT nguyen phat nhạy cảm với verapamil) |
ICa-L |
Tần số xoang bị chậm PR kéo dài Dẫn truyền nút AC bị chậm |
t1/2: 3–7 giờ Chuyển hóa: Thài tiết gan: thận |
Tim: Hạ huyết áp, phù, HF, AVB, nhịp chậm, trầm trọng HFrEF Khác: Nhức đầu, phát ban, tăng nướu, táo bón, chứng khó tiêu |
* Mặc dù đạt đến 800 mg mỗi 8 giờ có thể được sử dụng, liều cao hơn, của amiodarone được kết hợp với nguy cơ cao hơn của các biến cố bất lợi.
Alpha chỉ các thụ cảm thể alpha-adrenergic; ARVC: bệnh cơ tim thất phải gây loạn nhịp; AV: nhĩ thất; AVB: block nhĩ thất; Beta: thụ cảm thể beta-adrenergic; HF: suy tim; CPVT: nhịp nhanh thất đa hình do catecholamine; DFT: ngưỡng khử rung; F: phân; H, gan; ICa, dòng kệnh canxi type L; IK1, kệnh kali vào lưới nội nguyên sinh; IKACh, kêch kali được cổng thụ cảm thể muscarinic; IKATP, kênh kali adenosine được hoạt hóa; IKr, dòng kali lưới nội nguyên sinh trễ nhanh; IKs, dòng kali lưới nội nguyên sinh trễ chậm; IKur, dòng kali lưới nội nguyên sinh trễ nhanh; INa, dòng ntrai vào nhanh; Ito: dòng kali ra ngoài tạm thời; Ito, dòng kali ra tạm thời; LQTS: hội chứng QT dài; LVT: nhịp nhanh thất trái; M: muscarinic; Metab: chuyển hóa; NAPA, n-acetyl procainamide; PVC: phức bộ thất sớm; QTc: khoảng QT có điều chỉnh; t1/2: nửa đời sống; RVOT: đường ra thất phải; T3, triiodothyronine; TdP, torsades de pointes; U, urine; VT, nhịp nhanh thất; và VF, rung thất. Modified from Shleifer JW, et al. (2).
5.1.1. Các thuốc với các block kênh natri chiếm ưu thể
Trừ các tình huống đặc biệt, các chất chẹn kênh natri (các thuốc class I Vaughn-Williams) có vai trò hạn chế trong ngăn ngừa VT/SCD; điều này dựa trên cơ sở thiếu đi lợi ích sống sót và tử suất tăng lên đã được quan sát trong quá trình điều trị lâu dài ở các bệnh nhân bệnh tim thiếu máu cục bộ (xem phần 10.7). Các tình huống cụ thể trong đó blocker kênh natri đã được sử dụng để điều trị VT/SCA gồm: tiêm tĩnh mạch cho các bệnh nhân với VT/ ngừng tim trơ (đã biệt đã được biết rõ) (3); mexiletine uống cho hội chứng QT bẩm sinh dài (4); quinidine cho bệnh nhân có hội chứng Brugada; và flecainide cho bệnh nhân có nhịp nhanh thất đa hình do catecholamine (5). Những loại thuốc này cũng có thể được sử dụng trong các bệnh nhân ICD với VT trơ với thuốc và trơ với triệt phá.
Một loại thuốc mới hơn có lợi ích tiềm tàng, dựa trên dữ liệu rất hạn chế, là ranolazynin. Thuốc này, được phát triển và được FDA để nghị như là một thuốc chống đau thắt ngực, cung cấp blocker dòng kênh natri trễ tương đối chuyên biệt với việc block dòng kali tái cực pha 3 ít mạnh hơn; đó là, dòng kali thay đổi luân phiên trễ nhanh; IKr. Khả năng hiệu quả chống loạn nhịp trên lâm sàng được ủng hộ bằng các nghiên cứu cơ bản và mô hình thực nghiệm (6). Dữ liệu lâm sàng còn chưa đủ. Trong một nghiên cứu 12 bệnh nhân, ranolazine làm giảm các sốc ICD trong tình huống VT/VF kháng thuốc ở 11 bệnh nhân (7). Trong MERLIN TIMI (Metabolic Efficiency With Ranolazine for Less Ischemia in Non-ST-Elevation Acute Coronary Syndromes-Thrombolysis In Myocardial Infarction: Hiệu quả chuyển hóa với Ranolazine cho thiếu máu cục bộ nhẹ trong Hội chứng Mạch vành Cấp ST không chênh lên – Tiêu sợi huyết trong Nhồi máu Cơ tim) (36), ranolazine đã không làm giảm SCD nhưng làm giảm VT trong vài ngày đầu sau ACS ST không chênh lên (8). Trong 1 RCT, các bệnh nhân ICD nguy cơ cao bị thiếu máu cục bộ hoặc bệnh cơ tim không do thiếu máu cục bộ (NICM) được phân ngẫu nhiên đối với ranolazine 1000 mg hai lần một ngày đối lại với giả dược (9). Nguy cơ cao được xác định như sau: 1) có ICD dự phòng tiên phát không có bệnh sử VT/VF được chứng minh bằng tư liệu và với một trong những trạng thái sau: BUN 26 mg / dL, QRS > 120 msec, rung nhĩ, NSVT (VT tạm thời) hoặc > 500 VPBs được ghi nhận bằng Holter 24 giờ; 2) có ICD dự phòng tiên phát với tiền sử VT / VF đã được chứng minh bằng tư liệu phù hợp với điều trị bằng ICD hoặc NSVT không được điều trị; hoặc 3) có ICD ngăn ngừa thứ phát sau VT / VF hoặc ngừng tim được chứng minh bằng tư liệu. Ranolazine không giảm một cách có ý nghĩa tiêu chí đầu tiên của VT/VF đòi hỏi điều trị bằng ICD phù hợp hoặc tử vong. Trong một phân tích tiền cứu thứ phát, ranolazyn có liên quan đến giảm đi trong các biến cố VT một cách có ý nghĩa được điều trị với tạo nhịp chống nhịp nhanh (9).
5.1.2. Beta Blockers
Do thể hiện tính an toàn tuyệt vời của chúng và hiệu quả trong điều trị VA và giảm nguy cơ SCD, beta blockers thường là trị liệu chống loạn nhịp hàng đầu (10, 11). Hiệu quả chống loạn nhịp của chúng liên quan đến hiệu quả của block thụ thể adrenergic đối với cơ chế kích hoạt trung gian giao cảm, chậm tần số xoang, cũng như có thể ức chế phóng thích canxi quá mức do thụ thể ryanodine (12).
Beta blocker làm giảm tử suất do tất cả nguyên nhân và SCD ở các bệnh nhân có HF với EF giảm (HFrEF) (13-15). Mặc dù các beta blocker đã được chứng minh lâu dài làm giảm tử suất sau MI (MI) (16), dữ liệu đăng ký xác nhận sử dụng thuốc chẹn bêta sớm ở bệnh nhân nhồi máu cơ tim và các yếu tố nguy cơ gây sốc (> 70 tuổi, hiện diện 110 / phút có triệu chứng) được kết hợp với nguy cơ sốc và tử vong tăng lên (17). Trong tình trạng VT đa hình sau MI, beta blocker giảm tử suất (18). Betat blockers chấn áp VA ở một vài bệnh nhân có tim cấu trúc bình thường (19). Khi sử dụng phối hợp với các thuốc chống loạn nhịp ổn định màng tế bào, beta blocler có thể gia tăng hiệu quả chống loạn nhịp (20). Beta blockers (như nadolol, propranolol) cũng là điều trị hàng đầu đối với các bệnh kênh của tim (như hội chứng QT dài, nhịp nhanh thất đa hình do cathecholamine).
5.1.3. Amiodarone và Sotalol
Amiodaron có phổ hoạt động rộng bao gồm blocker thụ cảm thể beta và dòng natri, canxi và kali (nghĩa là một thuốc chặn đa kênh). Tất cả ảnh hưởng lâu dài của nó đối với sự sống sót còn là vấn đề gây tranh cãi, với hầu hết các nghiên cứu cho thấy không có lợi thế rõ ràng so với giả dược. Một vài nghiên cứu và một phân tích gộp của vài nghiên cứu lớn đã cho thấy giảm SCD bằng cách sử dụng amiodarone ở những bệnh nhân có rối loạn chức năng LV do MI và NICM trước (21-23), nhưng SCD-HeFT cho thấy không có lợi ích sống sót từ amiodarone so với giả dược (24). Một phân tích thứ cấp của SCD-HeFT cho thấy tăng nguy cơ tử vong với amiodarone ở những bệnh nhân với triệu chứng NYHA class III (NYHA) (25). Xem lại y văn một cách hệ thống ở các bệnh nhân nguy cơ cao (LVEF <40%, có hoặc không có bệnh mạch vành) đã kết luận, đối với phòng ngừa tiên phát, amiodarone so với không điều trị hoặc giả dược, làm giảm nguy cơ SCD (Risk ratio: 0.76 , 95% CI: 0.66-0.88) và tử vong do mọi nguyên nhân (Risk ratio: 0.88, 95% CI: 0.78-1.00), nhưng chất lượng của chứng cứ hỗ trợ rất thấp (26). Đối với phòng ngừa SCD thứ phát, một đánh giá hệ thống tương tự xác định hoặc nguy cơ hoặc không có lợi ích với amiodarone (26). So với liệu pháp chẹn beta và các thuốc chống loạn nhịp khác (gồm sotalol), amiodarone dường như làm giảm nguy cơ SCD và tử vong do mọi nguyên nhân (26). Amiodarone tiêm tĩnh mạch có vai trò làm giảm VF / VF tái phát trong suốt quá trình hồi sức (3, 27-29). Sử dụng lâu dài amiodarone có liên quan đến các tương tác thuốc phức tạp và một số tác dụng bất lợi liên quan đến phổi, gan, tuyến giáp, da và hệ thần kinh. Theo nguyên tắc chung, liệu pháp điều trị càng lâu và liều amiodarone càng cao, khả năng xảy ra các phản ứng phụ càng lớn sẽ buộc phải ngưng sử dụng thuốc (26). Vì lý do này, nên điều trị kéo dài ở những bệnh nhân trẻ bằng amiodarone như là một cầu nối để lựa chọn điều trị dứt điểm hơn như triệt phá qua catheter. Đánh giá cơ bản bệnh nhân có thể bao gồm ECG, các xét nghiệm chức năng gan, các xét nghiệm chức năng tuyến giáp, chụp X quang ngực và các xét nghiệm chức năng phổi (bao gồm khả năng lan truyền của phổi đối với carbon monoxide). Theo dõi độc tính thường gồm bệnh sử định kỳ và khám thực thể, cũng như đánh giá ECG, chụp X-quang ngực, và chức năng tuyến giáp, gan, và phổi. CT ngực có độ phân giải cao thường được dành riêng cho nghi ngời độc tính phổi(30).
Mặc dù sotalol có một số hiệu quả ức chế VA, nó có ảnh hưởng thúc đẩy rối loạn nhịp đáng kể và không cho thấy cải thiện sống sót (31). D-sotalol đã cho thấy trong nghiên cứu SWORD (Survival With Oral d-Sotalol: Sống sót bằng Uống d-Sotalol) đã làm tăng nguy cơ tử vong ở các bệnh nhân có suy tim (32). Không giống như amiodarone và nhiều thuốc chống loạn nhịp khác, sotalol đưa đến giảm ngưỡng khử rung (33). Cũng vậy, sotalol có thể đưa đến HF mất bù, và như vậy sử dụng thuốc ở các bệnh nhân LVEF < 20% nói chung nên tránh.
5.1.4. Blockers kênh canxi
Để điều trị hầu hết VA, blocker kênh canxi nondihydropyridines không có vai trò. Trên thực tế, verapamil tĩnh mạch được tiêm tĩnh mạch đối với VT dai dẳng đã được kết hợp với suy sụp huyết động, đặc biệt ở các bệnh nhân có MI trước đó (34, 35). Đối với các bệnh nhân có tim có cấu trúc bình thường, verapamil hoặc diltiazem có thể ức chế một số vị trí nguồn gốc đường ra (35-39). Verapamil đường uống và tiêm tĩnh mạch có hiệu quả trong điều trị LVT vào lại nội bó nguyên phát (idiopathic interfaccicular reentrant LVT) (38). Blocker kênh canxi không nên cho đối với các bệnh nhân có VT trong trạng thái HFrEF.
5.1.5. Các thuốc không phải chống loạn nhịp và các trị liệu
5.1.5.1. Điện giải
Sử dụng kali và magiê đã được đề xuất như là chất bổ xung hữu ích trong phòng ngừa VA (40, 41). Giảm kali và magiê máu thường là hậu quả của điều trị lợi tiểu trong HF, cả hai đều có liên quan đến VA trong giai đoạn MI cấp (41, 42) và có thể làm tăng nguy cơ xoắn đỉnh (torsades de pointes) ở bệnh nhân dùng thuốc hoặc với các trạng thái đã biết làm kéo dài khoảng QT (43). Trên thực tế, ở những bệnh nhân xoắn đỉnh, tiêm tĩnh mạch magnesium là phương pháp điều trị đầu tiên (44). Ở những bệnh nhân thiếu magiê và kali, magiê cần được bù đầy đủ để tạo điều kiện cho việc thay thế kali (45). Trong trường hợp kali, một số người khuyến cáo nên giữ mức kali giữa 4,5 mmol / L và 5 mmol / L để ngăn ngừa VA và SCD (46, 47). Một nghiên cứu quan sát lớn cho bệnh nhân MI cấp phát hiện thấy tỷ lệ tử vong thấp nhất ở bệnh nhân có nồng độ kali huyết thanh trong khoảng 3,5 mmol / L và < 4,5 mmol / L (48). Thật thú vị, tỷ lệ VA không tăng trừ khi kali < 3 mmol / L hoặc > 5 mmol / L. Tương tự như vậy, một thử nghiệm lớn, ngẫu nhiên, mù đôi về tiêm magiê tĩnh mạch trong giai đoạn sau MI đã chứng minh không có lợi trong tử vong 30 ngày (40). Nó vẫn còn hoàn toàn hợp lý để theo dõi kali và magiê trong suốt quá trình lợi tiểu tích cực và giai đoạn sau MI.
5.1.5.2. Lipids và A xit béo n-3
Cả hai điều trị a xít béo không bão hòa n-3 và statin có thể có vai trò trong ngăn ngừa SCD, được cho là do sự ổn định của màng lipid của tế bào cơ tim liên quan đến duy trì sự chênh lệch điện giải (49).
Các tư liệu đầu tiên được hứa hẹn về hiệu quả của axit béo không bão hòa n-3 trong việc giảm các biến cố tim mạch và SCD. Năm 2006, một phân tích tổng hợp lớn gồm 19 nghiên cứu quan sát và RCTs đã chứng minh được sự liên quan có ý nghĩa giữa tiêu thụ a xít béo đa không bão hòa n-3 và phòng ngừa SCD (50). Nghiên cứu Prevenzione GISSI ngẫu nhiên (Gruppo Italiano per lo Studio della Sopravvivenza nell’Infarto) ở người có MI vừa xẩy ra, đã xác định dầu cá 1 g / ngày làm giảm tử suất, do SCD ít đi (51). Tuy nhiên, các RCT tiếp theo không tái tạo lại những lợi ích này và đã cho thấy các axit béo không bão hoà n-3 không có hiệu quả (52-56). Vì các nghiên cứu cho thấy sự thiếu hụt liên tục có hại từ các axit béo không bão hoà n-3, các bệnh nhân có thể yên tâm về sự an toàn của chúng. Các dữ liệu dài hạn hy vọng sẽ làm rõ các kết quả trái ngược nhau.
Ngược lại, thuốc statin làm giảm rõ rệt tử vong và dường như làm giảm nguy cơ SCD liên quan đến bệnh tim thiếu máu cục bộ (57). Cơ chế chiếm ưu thế vẫn còn chưa rõ ràng. Ngăn ngừa vỡ các mảng bám mạch vành hoặc hiệu quả bảo vệ tim trực tiếp làm giảm VA đã được gợi mở. Các mô hình thiếu máu cục bộ / tái tưới máu chứng minh hiệu quả bảo vể tim của statin, một phân tích quan sát lớn đã quan sát hiệu quả này ở người (42, 56-58). Điều này đã được khám phá tiếp theo ở HF trong một số phân tích thứ cấp của các bệnh nhân dùng statin trong các nghiên cứu ICD phòng ngừa, gồm MADIT-CRT (Multicenter Automatic Defibrillator Implantation Trial-Cardiac Resynchronization Therapy: Điều trị Tái đồng bộ Tim – Nghiên cứu Cấy khử rung tim Tự động Đa trung tâm), SCD-HeFT, AVID (Antiarrhythmics versus Implantable Defibrillators: Chống loạn nhịp đối lại Cấy Khử rung) (59), và nghiên cứu DEFINITE (DEFibrillators In Non-Ischemic Cardiomyopathy Treatment Evaluation: Khử rung trong Đánh giá Điều trị Bệnh cơ tim Không do Thiếu máu cục bộ) cho thấy nguy cơ SCD ít hơn trong số các bệnh nhân sử dụng statin (58, 60-62). Tuy nhiên, hiệu quả chung này trong HF không được xác nhận trong 2 nghiên cứu ngẫu nhiên của rosuvastatim trong HF; CORONA (Controlled Rosuvastatin Multinational Trial in Heart Failure: Nghiên cứu Đa Quốc gia vể Rosuvastatin có Đối chứng trong Suy tim) và GISSI-HF (Gruppo Italiano per Serum della Sopravvivenza nell’Insufficienza Cardiaca-Heart Failure) (63, 64). Điều này chứng tỏ hiệu quả lợi ích của statin được khẳng định cho các quần thể có hoặc với nguy cơ bệnh tim do vữa xơ và / hoặc thiếu máu cục bộ, không phải HF nói chung.
Tài liệu tham khảo
1. Vaughan Williams EM. A classification of antiarrhythmic actions reassessed after a decade of new drugs. J Clin Pharmacol. 1984;24:129-47.
2. Schleifer JW, Sorajja D, Shen WK. Advances in the pharmacologic treatment of ventricular arrhythmias. Expert Opin Pharmacother. 2015;16:2637-51.
3. Kudenchuk PJ, Brown SP, Daya M, et al. Amiodarone, lidocaine, or placebo in out-of-hospital cardiac arrest. N Engl J Med. 2016;1711-22.
4. Mazzanti A, Maragna R, Faragli A, et al. Gene-specific therapy with mexiletine reduces arrhythmic events in patients with long QT syndrome type 3. J Am Coll Cardiol. 2016;67:1053-8.
5. Watanabe H, Chopra N, Laver D, et al. Flecainide prevents catecholaminergic polymorphic ventricular tachycardia in mice and humans. Nat Med. 2009;15:380-3.
6. Gupta T, Khera S, Kolte D, et al.. Antiarrhythmic properties of ranolazine: a review of the current evidence. Int J Cardiol. 2015;187:66-74.
7. Bunch TJ, Mahapatra S, Murdock D, et al. Ranolazine reduces ventricular tachycardia burden and ICD shocks in patients with drug-refractory ICD shocks. Pacing Clin Electrophysiol. 2011;34:1600-6
8. Scirica BM, Braunwald E, Belardinelli L, et al. Relationship between nonsustained ventricular tachycardia after nonST-elevation acute coronary syndrome and sudden cardiac death: observations from the metabolic efficiency with ranolazine for less ischemia in non-ST-elevation acute coronary syndrome-thrombolysis in myocardial infarction 36 (MERLIN-TIMI 36) randomized controlled trial. Circulation. 2010;122:455-62.
9. Zareba W , Daubert JP, Beck CA, et al. Ranolazine in High-Risk ICD Patients (RAID) Trial. Presented at: Heart Rhythm Society Annual Scientific Sessions. 2017;LBCT02-01:
10.Reiter MJ, Reiffel JA. Importance of beta blockade in the therapy of serious ventricular arrhythmias. Am J Cardiol. 1998;82:9I-19I.
11.Ellison KE, Hafley GE, Hickey K, et al. Effect of beta-blocking therapy on outcome in the Multicenter UnSustained Tachycardia Trial (MUSTT). Circulation. 2002;106:2694-9.
12.Reiken S, Wehrens XH, Vest JA, et al. Beta-blockers restore calcium release channel function and improve cardiac muscle performance in human heartfailure. Circulation. 2003;107:2459-66.
13.MERIT-HF Group. Effect of metoprolol CR/XL in chronic heart failure: Metoprolol CR/XL Randomised Intervention Trial in Congestive Heart Failure (MERIT-HF). Lancet. 1999;353:2001-7.
14.Packer M, Bristow MR, Cohn JN, et al. The effect of carvedilol on morbidity and mortality in patients with chronic heart failure. U.S. Carvedilol Heart Failure Study Group. N Engl J Med. 1996;334:1349-55.
15.Committees of the Cardiac insufficiency Bisoprolol Study II. The cardiac insufficiency Bisoprolol Study II (CIBIS-II): a randomised trial. Lancet. 1999;353:9-13.
16.A randomized trial of propranolol in patients with acute myocardial infarction. Mortality results. JAMA. 1982;247:1707-14.
17.Kontos MC, Diercks DB, Ho PM, et al. Treatment and outcomes in patients with myocardial infarction treated with acute beta-blocker therapy: results from the American College of Cardiology’s NCDR(R). Am Heart J. 2011;161:864- 70.
18.Nademanee K, Taylor R, Bailey WE, et al. Treating electricalstorm: sympathetic blockade versus advanced cardiac life support-guided therapy. Circulation. 2000;102:742-7.
19.Krittayaphong R, Bhuripanyo K, Punlee K, et al. Effect of atenolol on symptomatic ventricular arrhythmia without structural heart disease: a randomized placebo-controlled study. Am Heart J. 2002;144:e10.
20.Hirsowitz G, Podrid PJ, Lampert S, et al. The role of beta blocking agents as adjunct therapy to membrane stabilizing drugs in malignant ventricular arrhythmia. Am Heart J. 1986;111:852-60.
21.Connolly SJ. Meta-analysis of antiarrhythmic drug trials. Am J Cardiol. 1999;84:90R-93R.
22.Steinberg JS, Martins J, Sadanandan S, et al. Antiarrhythmic drug use in the implantable defibrillator arm of the Antiarrhythmics Versus Implantable Defibrillators (AVID) Study. Am Heart J. 2001;142:520-9.
23.Farre J, Romero J, Rubio JM, et al. Amiodarone and “primary” prevention of sudden death: critical review of a decade of clinical trials. Am J Cardiol. 1999;83:55D-63D.
24.Bardy GH, Lee KL, Mark DB, et al. Amiodarone or an implantable cardioverter-defibrillator for congestive heart failure. N Engl J Med. 2005;352:225-37.
25.Thomas KL, Al-Khatib SM, Lokhnygina Y, et al. Amiodarone use after acute myocardial infarction complicated by heart failure and/or left ventricular dysfunction may be associated with excess mortality. Am Heart J. 2008;155:87- 93.
26.Claro JC, Candia R, Rada G, et al. Amiodarone versus other pharmacological interventions for prevention of sudden cardiac death. Cochrane Database Syst. Rev. 2015;12:CD008093.
27.Kudenchuk PJ, Cobb LA, Copass MK, et al. Amiodarone for resuscitation after out-of-hospital cardiac arrest due to ventricular fibrillation. N Engl J Med. 1999;341:871-8.
28.Dorian P, Cass D, Schwartz B, et al. Amiodarone as compared with lidocaine for shock-resistant ventricular fibrillation. N Engl J Med. 2002;346:884-90.
29.Levine JH, Massumi A, Scheinman MM, et al. Intravenous amiodarone for recurrent sustained hypotensive ventricular tachyarrhythmias. Intravenous Amiodarone Multicenter Trial Group. J Am Coll Cardiol. 1996;27:67-75.
30.Epstein AE, Olshansky B, Naccarelli GV, et al. Practical management guide for clinicians who treat patients with amiodarone. Am J Med. 2016;129:468-75.
31.Kuhlkamp V, Mewis C, Mermi J, et al. Suppression of sustained ventricular tachyarrhythmias: a comparison of d,lsotalol with no antiarrhythmic drug treatment. J Am Coll Cardiol. 1999;33:46-52.
32.Waldo AL, Camm AJ, deRuyter H, et al. Survival with oral d-sotalol in patients with left ventricular dysfunction after myocardial infarction: rationale, design, and methods (the SWORD trial). Am J Cardiol. 1995;75:1023-7.
33.Page RL. Effects of antiarrhythmic medication on implantable cardioverter-defibrillator function. Am J Cardiol. 2000;85:1481-5.
34.Buxton AE, Marchlinski FE, Doherty JU, et al. Hazards of intravenous verapamil for sustained ventricular tachycardia. Am J Cardiol. 1987;59:1107-10.
35.Belhassen BHorowitz LN. Use of intravenous verapamil for ventricular tachycardia. Am J Cardiol. 1984;54:1131-3. 36.Griffith MJ, Garratt CJ, Rowland E, et al. Effects of intravenous adenosine on verapamil-sensitive “idiopathic” ventricular tachycardia. Am J Cardiol. 1994;73:759-64.
37.Gill JS, Blaszyk K, Ward DE, et al. Verapamil for the suppression of idiopathic ventricular tachycardia of left bundle branch block-like morphology. Am Heart J. 1993;126:1126-33.
38.Badhwar N, Scheinman MM. Idiopathic ventricular tachycardia: diagnosis and management. Curr Probl Cardiol. 2007;32:7-43.
39.Gill JS, Ward DE, Camm AJ. Comparison of verapamil and diltiazem in the suppression of idiopathic ventricular tachycardia. Pacing Clin Electrophysiol. 1992;15:2122-6.
40.Investigatorsin the Magnesium in Coronaries (MAGIC) Trial. Early administration of intravenous magnesium to highrisk patients with acute myocardial infarction in the Magnesium in Coronaries (MAGIC) Trial: a randomised controlled trial. Lancet. 2002;360:1189-96.
41.Cooper HA, Dries DL, Davis CE, et al. Diuretics and risk of arrhythmic death in patients with left ventricular dysfunction. Circulation. 1999;100:1311-5.
42.Kafka H, Langevin L, Armstrong PW. Serum magnesium and potassium in acute myocardial infarction. Influence on ventricular arrhythmias. Arch Intern Med. 1987;147:465-9.
43.Yan GX, Antzelevitch C. Cellular basis for the normal T wave and the electrocardiographic manifestations of the longQT syndrome. Circulation. 1998;98:1928-36.
44.Tzivoni D, Banai S, Schuger C, et al. Treatment of torsade de pointes with magnesium sulfate. Circulation. 1988;77:392-7.
45.Leier CV, Dei CL, Metra M. Clinical relevance and management of the major electrolyte abnormalities in congestive heart failure: hyponatremia, hypokalemia, and hypomagnesemia. Am Heart J. 1994;128:564-74.
46.Cohn JN, Kowey PR, Whelton PK, et al. New guidelines for potassium replacement in clinical practice: a contemporary review by the National Council on Potassium in Clinical Practice. Arch Intern Med. 2000;160:2429-36.
47.Macdonald JE, Struthers AD. What is the optimal serum potassium level in cardiovascular patients? J Am Coll Cardiol. 2004;43:155-61.
48.Goyal A, Spertus JA, Gosch K, et al. Serum potassium levels and mortality in acute myocardial infarction. JAMA. 2012;307:157-64.
49.Leaf A, Kang JX, Xiao YF, et al. Clinical prevention of sudden cardiac death by n-3 polyunsaturated fatty acids and mechanism of prevention of arrhythmias by n-3 fish oils. Circulation. 2003;107:2646-52.
50.Mozaffarian D, Rimm EB. Fish intake, contaminants, and human health: evaluating the risks and the benefits. JAMA. 2006;296:1885-99.
51.Marchioli R, Barzi F, Bomba E, et al. Early protection against sudden death by n-3 polyunsaturated fatty acids after myocardial infarction: time-course analysis of the results of the Gruppo Italiano per lo Studio della Sopravvivenza nell’Infarto Miocardico (GISSI)-Prevenzione. Circulation. 2002;105:1897-903.
52.Kromhout D, Giltay EJ, Geleijnse JM. n-3 fatty acids and cardiovascular events after myocardial infarction. N Engl J Med. 2010;363:2015-26.
53.Rauch B, SchieleR, Schneider S, et al. OMEGA, a randomized, placebo-controlled trial to test the effect of highly purified omega-3 fatty acids on top of modern guideline-adjusted therapy after myocardial infarction. Circulation. 2010;122:2152-9.
54.Burr ML, Ashfield-Watt PA, Dunstan FD, et al. Lack of benefit of dietary advice to men with angina: results of a controlled trial. Eur J Clin Nutr. 2003;57:193-200.
55.Galan P, Kesse-Guyot E, Czernichow S, et al. Effects of B vitamins and omega 3 fatty acids on cardiovascular diseases: a randomised placebo controlled trial. BMJ. 2010;341:c6273.
56.Bosch J, Gerstein HC, Dagenais GR, et al. n-3 fatty acids and cardiovascular outcomes in patients with dysglycemia. N Engl J Med. 2012;367:309-18.
57.LaRosa JC, He J, Vupputuri S. Effect of statins on risk of coronary disease: a meta-analysis of randomized controlled trials. JAMA. 1999;282:2340-6.
58.Buber J, Goldenberg I, Moss AJ, et al. Reduction in life-threatening ventricular tachyarrhythmias in statin-treated patients with nonischemic cardiomyopathy enrolled in the MADIT-CRT (Multicenter Automatic Defibrillator Implantation Trial with Cardiac Resynchronization Therapy). J Am Coll Cardiol. 2012;60:749-55.
59.Investigators in TAvIDA. A comparison of antiarrhythmic-drug therapy with implantable defibrillators in patients resuscitated from near-fatal ventricular arrhythmias. N Engl J Med. 1997;337:1576-83.
60.Mitchell LB, Powell JL, Gillis AM, et al. Are lipid-lowering drugs also antiarrhythmic drugs? An analysis of the Antiarrhythmics versus Implantable Defibrillators (AVID) trial. J Am Coll Cardiol. 2003;42:81-7.
61.Dickinson MG, Ip JH, Olshansky B, et al. Statin use was associated with reduced mortality in both ischemic and nonischemic cardiomyopathy and in patients with implantable defibrillators: mortality data and mechanistic insights from the Sudden Cardiac Death in Heart Failure Trial (SCD-HeFT). Am Heart J. 2007;153:573-8.
62.Goldberger JJ, Subacius H, Schaechter A, et al. Effects of statin therapy on arrhythmic events and survival in patients with nonischemic dilated cardiomyopathy. J Am Coll Cardiol. 2006;48:1228-33.
63.Kjekshus J, Apetrei E, Barrios V, et al. Rosuvastatin in older patients with systolic heart failure. N Engl J Med. 2007;357:2248-61.
64.Tavazzi L, Maggioni AP, Marchioli R, et al. Effect of rosuvastatin in patients with chronic heart failure (the GISSI-HF trial): a randomised, double-blind, placebo-controlled trial. Lancet. 2008;372:1231-9.
5.2. Ngăn ngừa SCD với các thuốc điều trị HF
|
Khuyến cáo cho ngăn ngừa SCD bằng thuốc Các nghiên cứu tham khảo ủng hộ các khuyến cáo được tóm tắt trong phần Tư liệu hỗ trợ online 10. |
||
|
COR |
LOE |
Các khuyến cáo |
|
I |
A |
1. Ở những bệnh nhân có HFrEF (LVEF < 40%), điều trị với ức chế bêta, chẹn thụ cảm thể mineralocorticoid và hoặc ức chế men chuyển, blocker thụ thể angiotensin, hoặc ức chể thụ thể neprilysin angiotensin được khuyến cáo để giảm SCD và tử suất do mọi nguyên nhân (1-8). |
Văn bản hỗ trợ đặc biệt – Khuyến cáo
1. Đối với các bệnh nhân có HF và chức năng LV suy giảm, điều trị nội khoa phù hợp là điều quan trọng để giảm SCD. Những liệu pháp này có những tác dụng có lợi khác nhau đối với cơ chế loạn nhịp tim. Thuốc chẹn beta làm giảm nhu cầu oxy cơ tim và khả năng kích thích điện, cũng như chống lại các tác động gây loạn nhịp của kích thích giao cảm. Các chất ức chế men chuyển angiotensin và blocker thụ thể angiotensin làm giảm tiền tải và hậu tải, giảm nhu cầu tiêu thụ ô xy của cơ tim, ngăn chặn hình thành antiotensin II, làm chậm tiến triển xơ hóa và tái cấu trúc thất. Các thuốc đối kháng thụ thể mineralocorticoid làm hạn chế mất kali, giảm xơ hóa, tăng hấp thu norepinephrine của cơ tim (7).
RCTs ở bệnh nhân HFrEF đã chứng minh liên tục điều trị kéo dài với beta blockers làm giảm tử suất do mọi nguyên nhân, VA và SCD (2, 4, 5, 9). Ba thuốc beta blockers (bisoprolol, carvedilol, metoprolol succinate thải tiết kéo dài) đã được chứng minh làm giảm tử suất ở những bệnh nhân có triệu chứng HFrEF hiện thời hoặc trước đó không có chống chỉ định với beta blocker. Các ức chế men chuyển angiotensin cũng giảm tử suất và SCD (3). Các thuốc chẹn thụ thể angiotensin được thêm vào thuốc ức chế men chuyển angiotensin cho thấy có lợi ích bổ sung đối với thuốc ức chế men chuyển angiotensin ở một nghiên cứu (10) nhưng không phải các RCT khác (8, 11). Liệu pháp điều trị với các chất đối kháng thụ thể mineralocorticoid, spironolactone và eplerenone cũng đã làm giảm ở cả hai tử suất do mọi nguyên nhân và SCD (6, 12, 13). Các nghiên cứu gần đây về thuốc ức chế thụ thể angiotensin-neprilysin (sacubitril / valsartan) so với thuốc ức chế men chuyển angiotensin chứng minh giảm SCD và tử suất do tim (14).
Tài liệu tham khảo
1. Yancy CW, Jessup M, Bozkurt B, et al. 2016 ACC/AHA/HFSA focused update on new pharmacological therapy for heart failure: an update of the 2013 ACCF/AHAguideline for the management of heart failure:a reportof theAmerican College of Cardiology/American Heart Association Task Force on Clinical Practice Guidelines and the Heart Failure Society of America. Circulation. 2016;134:e282-93.
2. Committees for Cardiac insufficiency Bisoprolol Study II. The cardiac insufficiency Bisoprolol Study II (CIBIS-II): a randomised trial. Lancet. 1999;353:9-13.
3. Cohn JN, Johnson G, Ziesche S, et al. A comparison of enalapril with hydralazine-isosorbide dinitrate in the treatment of chronic congestive heart failure. N Engl J Med. 1991;325:303-10.
4. Packer M, Bristow MR, Cohn JN, et al. The effect of carvedilol on morbidity and mortality in patients with chronic heart failure. U.S. Carvedilol Heart Failure Study Group. N Engl J Med. 1996;334:1349-55. 5. Dargie HJ. Effect of carvedilol on outcome after myocardial infarction in patients with left-ventricular dysfunction: the CAPRICORN randomised trial. Lancet. 2001;357:1385-90.
6. Pitt B, Remme W, Zannad F, et al. Eplerenone, a selective aldosterone blocker, in patients with left ventricular dysfunction after myocardial infarction. N Engl J Med. 2003;348:1309-21.
7. Al Chekakie MO. Traditional heart failure medications and sudden cardiac death prevention: a review. J Cardiovasc Pharmacol Ther. 2013;18:412-26.
8. Pfeffer MA, McMurray JJ, Velazquez EJ, et al. Valsartan, captopril, or both in myocardial infarction complicated by heart failure, left ventricular dysfunction, or both. N Engl J Med. 2003;349:1893-906.
9. Hjalmarson A, Goldstein S, Fagerberg B, et al. Effects of controlled-release metoprolol on total mortality, hospitalizations, and well-being in patients with heart failure: the Metoprolol CR/XL Randomized Intervention Trial in congestive heart failure (MERIT-HF). MERIT-HF Study Group. JAMA. 2000;283:1295-302.
10.McMurray JJV, Östergren J, Swedberg K, et al. Effects of candesartan in patients with chronic heart failure and reduced left-ventricular systolic function taking angiotensin-converting-enzyme inhibitors: the CHARM-Added trial. Lancet. 2003;362:767-71.
11.Cohn JN, Tognoni G. A randomized trial of the angiotensin-receptor blocker valsartan in chronic heart failure. N Engl J Med. 2001;345:1667-75.
12.Pitt B, Zannad F, Remme WJ, et al. The effect of spironolactone on morbidity and mortality in patients with severe heart failure. Randomized Aldactone Evaluation Study Investigators. N Engl J Med. 1999;341:709-17.
13.Zannad F, McMurray JJ, Krum H, et al. Eplerenone in patients with systolic heart failure and mild symptoms. N Engl J Med. 2011;364:11-21.
14.Desai AS, McMurray JJ, Packer M, et al. Effect of the angiotensin-receptor-neprilysin inhibitor LCZ696 compared with enalapril on mode of death in heart failure patients. Eur Heart J. 2015;36:1990-7.
5.3. Khử rung tim cho Điều trị VA và SCD
Xem phần 7, 10.2, 10.3, 10.8, và 10.9.
Khử rung tim có hiệu quả cao trong cắt VA nguy hiểm tính mạng. Điều trị này có thể được phóng ra bằng ICD qua tĩnh mạch, khử rung tim có thể cấy dưới da, khử rung tim bằng áo mặc hoặc khử rung tim ngoài. Các thiết bị này theo dõi nhịp tim liên tục. Các thiết bị này theo dõi nhịp tim liên tục và cung cấp điều trị để đáp lại nhịp nhanh để đáp ứng với nhịp tim nhanh khi gặp tần số phát hiện và khoảng thời gian loạn nhịp đã được lập trình. Phần lớn các ICD đường tĩnh mạch được cấy ở khu vực dưới đòn dưới sự hướng dẫn của soi quang tuyến. Các máy khử rung tim cấy dưới da được cấy ở bên trái của ngực trên xương sườn thứ sáu giữa đường nách giữa trái và đường nạch trước trái. ICDs với các chuyển đạo nhận cảm và tạo nhịp thượng tâm mạc còn được cấy ở một số bệnh nhân đặc biệt những người có các hình thái bệnh tim bẩm sinh.
ICD qua tĩnh mạch đã được áp dụng trong lâm sàng > 3 thập niên, các tư liệu mạnh mẽ từ các RCTs chất lượng cao ủng hộ áp dụng nó ở các quần thể bệnh nhân khác nhau gồm người sống sót sau ngừng tim, các bệnh nhân có VT và bệnh tim thực thể, cũng như các bệnh nhân có rối loạn chức năng LV đáng kể.
5.4. Triệt phá qua catheter
5.4.1. Xem xét chung
Triệt phá qua catheter là lựa chọn điều trị quan trọng cho các bệnh nhân có VA khi các thuốc chống loạn nhịp không có hiệu quả, không dung nạp, hoặc bệnh nhân không mong muốn. VA đơn hình thường có nguồn gốc hoặc thường có nguồn gốc hoặc nền có thể là đích cho triệt phá. Triệt phá là lựa chọn cho các bệnh nhân được lựa chọn với VT / VF đa hình chỉ nếu khởi phát PVC ổ hoặc nền có thể xác định. Chiến lược triệt phá, nguy cơ và kết quả liên quan đến cơ chế và định khu của VA. Đại đa số VA nguồn gốc sát với dưới nội tâm mạc và được tiếp cận qua tĩnh mạch (đối với tâm thất phải) hoặc qua động mạch chủ / qua vách liên thất (đối với thất trái). Một số bệnh làm xuất hiện VA từ dưới thượng tâm mạc, có thể phải được tiếp cận bằng lập bản đồ (mapping) thượng tâm mạc và triệt phá. Tiếp cận màng ngoài tim thường đạt được bằng chọc thủng qua da dưới bờ sườn. Thủ thuật triệt phá qua catheter thường liên quan đến nỗ lực tạo ra VT bằng kích thích tim có chương trình để khẳng định chẩn đoán và hướng dẫn triệt phá. Các vấn đề hạn chế thành công gồm không có khả năng gây loạn nhịp cho lập bản đồ (thường gặp với VA nguyên phát) hoặc nguồn gốc loạn nhịp từ một vị trí không thể tiếp cận được trong cơ tim (thường gặp ở một số bệnh cơ tim).
5.4.2. VA ở Các Bệnh nhân có bệnh tim dường như không do cấu trúc
Xem phần 8.
VA không kết hợp với bệnh tim cấu trúc nền hoặc hội chứng rối loạn nhịp di truyền thường được gọi là nguyên phát (idio). Đại đa số VA nguyên phát là đơn hình và trên cơ sở cơ chế ổ của hoạt động khởi phát hoặc tính tự động bất thường; số ít do vào lại. Đối với các bệnh nhân có triệu chứng, và ở những bệnh nhân này các thuốc chống loạn nhịp không có hiệu quả, không dung náp, hoặc bệnh nhân không mong muốn, triệt phá qua catheter là điều trị lựa chọn. Chiến lược triệt phá là để xác định vị trí nguồn gốc được biểu hiện sớm bằng vị trí sớm nhất của hoạt động điện, hoặc khi điều này thực hành, bằng lập bản đồ qua tạo nhịp. Triệt phá qua catheter các VA nguyên phát thường qua catheter nội tâm mạc, qua tiếp cận thượng tâm mạc qua tuần hoàn tĩnh mạch vành hoặc chọc qua bờ dưới sườn có thể đôi khi được đòi hỏi. Triệt phá thất bại các VA nguyên phát thường do không có khả năng để thúc đẩy loạn nhịp để cho phép lập bản đồ trong labo điện sinh lý hoặc nguồn gốc từ khu vực không tiếp cận được.
5.4.3. VT liên quan đến sẹo
Xem phần 8.
Đối với đa số các bệnh nhân bệnh tim cấu trúc, VT đơn hình dai dẳng do vào lại qua khu vực các sợi cơ tim còn sống sót được kết hợp với các khu vực xơ sẹo. Chiến lược triệt phá cho các vòng vào lại này để nhận biết và loại trừ các kênh cơ tim đang sống trong phạm vi sẹo thường kết hợp với đường dẫn truyền chậm làm dễ dàng cho vào lại. Đối với hầu hết VT liên quan đến MI trước đó, nền ở trên bề mặt dưới nội tâm mạc thất trái. Trong NICM, các vòng vào lại có nhiều thay đổi hơn ở khu vực, thường liên quan đến bề mặt thượng tâm mạc hoặc thất và thường lan rộng vào giữa cơ tim ở đó triệt phá có thể khó khăn để đạt được từ hoặc bề mặt. Trong tứ chứng Fallot các đường vào lại đặc biệt đã được xác định (1). Bản đồ điện giải phẫu giúp làm rõ mối liên quan của các bất thường điện sinh lý đối với giải phẫu tim thường được sử dụng. Các vùng vết sẹo có thể được đánh giá là các vùng điện thế trên điện đồ tương đối thấp. Đối với VT liên quan đến sẹo, không dung náp huyết động thường hạn chế lập bản đồ trong quá trình VT. Sau đó, triệt phá thường được hướng dẫn bằng cách lập bản đồ nền, trong đó các vùng sẹo và nền vòng vào lại điện thế được mô tả trên các bản đồ điện giải phẫu dựa trên các đặc tính của điện tâm đồ và và đặc tính tạo nhịp được đánh giá trong quá trình nhịp xoang hoặc tạo nhịp ổn định về huyết động. Việc triệt phá qua catheter các VT liên quan đến sẹo đòi hỏi mức độ tiến bộ của kinh nghiệm do người thực hiện, nhân viên labo điện sinh lý, bác sỹ gây mê cũng như khả năng của dụng cụ thủ thuật và lập bản đồ chuyên sâu, hình ảnh học, cũng như thiết bị triệt phá (2, 3).
Tài liệu tham khảo
1. Zeppenfeld K, Schalij MJ, Bartelings MM, et al. Catheter ablation of ventricular tachycardia after repair of congenital heart disease: electroanatomic identification of the critical right ventricular isthmus. Circulation. 2007;116:2241-52.
2. Priori SG, Blomstrom-Lundqvist C, Mazzanti A, et al. 2015 ESC guidelines for the management of patients with ventricular arrhythmias and the prevention of sudden cardiac death: the Task Force for the Management of Patients with Ventricular Arrhythmias and the Prevention of Sudden Cardiac Death of the European Society of Cardiology (ESC). Eur Heart J. 2015;36:2793-867.
3. Aliot EM, Stevenson WG, Almendral-Garrote JM, et al. EHRA/HRS expert consensus on catheter ablation of ventricular arrhythmias: developed in a partnership with the European Heart Rhythm Association (EHRA), a Registered Branch of the European Society of Cardiology (ESC), and the Heart Rhythm Society (HRS); in collaboration with the American College of Cardiology (ACC) and the American Heart Association (AHA). Heart Rhythm. 2009;6:886-933.
5.5. Các Thủ thuật Ngoại khoa và Tái tuần hoàn ở các Bệnh nhân Bệnh Tim Thiếu máu cục bộ
|
Các khuyến cáo cho Thủ thuật Ngoại khoa và Tái tuần hoàn ở các Bệnh nhân Bệnh Tim Thiếu máu cục bộ Các nghiên cứu tham khảo ủng hộ các khuyến cáo được tóm tắt trong phần Tư liệu hỗ trợ online 11. |
||
|
COR |
LOE |
Các khuyến cáo |
|
I |
B-NR |
1. Các bệnh nhân VA dai dẳng và sống sót sau SCA nên được đánh giá về bệnh tim thiếu máu cục bộ, cũng như được tái tuần hoàn phù hợp (1-4). |
|
I |
C-EO |
2. Ở các bệnh nhân có nguồn gốc động mạch vành bất thường được cho là nguyên nhân gây SCA, sửa chữa hoặc tái tuần hoàn được khuyến cáo. |
Văn bản Hỗ trợ Đặc biệt – Khuyến cáo
1. Thiếu máu cơ tim cục bộ là nguyên nhân của VT / VF đa hình dai dẳng, tái tuần hoàn là điều trị hiệu quả để ngăn chặn thiếu máu cơ tim cục bộ. Đối với những bệnh nhân VA đe dọa đến tính mạng, các nghiên cứu quan sát cho thấy những bệnh nhân trải qua bắc cầu động mạch vành tự thân (CABG) có tỷ lệ sống sót tốt hơn đáng kể sau khi tính toán các yếu tố dự đoán khác (1, 5). Nguy cơ SCD xuất hiện có thể so sánh với các bệnh nhân có bệnh tim thiếu máu cục bộ phức tạp được ngẫu nhiên điều trị với PCI đối lại với CABG (6). Đối với bệnh nhân LVEF thấp và bệnh tim thiếu máu để CABG, nguy cơ SCD thấp hơn với CABG so với điều trị nội khoa (2, 7). Các nghiên cứu quan sát cho thấy mối liên hệ giữa khả năng tử vong thấp hơn với việc tái tuần hoàn đối với SCA và CABG (3) hoặc PCI (4). Tái tuần hoàn đơn thuần thường không đủ để ngăn ngừa VT đơn hình dai dẳng tái phát; đánh giá tiếp theo về VT có thể tạo ra được xem xét thường xuyên nếu chức năng tâm thất bị giảm và / hoặc có sẹo hiện diện.
2. Nguồn gốc các động mạch vành ở động mạch chủ bất thường được phát hiện ở khoảng khoảng 1% bệnh nhân được chụp mạch vành thông thường và < 0,2% trẻ em và thanh thiếu niên được thực hiện siêu âm tim (8). Mặc dù bệnh tim thiếu máu cục bộ được phát hiện trong khoảng từ 24% đến 55% trường hợp SCD ở bệnh nhân trẻ <35 tuổi (9, 10), nguồn gốc các động mạch vành ở động mạch chủ bất thường là nguyên nhân SCD quan trọng ở người trẻ, được thông báo ở 10% đến 17% bệnh nhân được thu gom trong các nghiên cứu sau mổ (10, 11). Nguồn gốc bất thường của động mạch vành có thể được xác định bằng siêu âm tim, chụp mạch vành, chụp CT động mạch hoặc MRI tim. Ở những bệnh nhân SCA hoặc VA đe dọa tính mạng có liên quan đến thiếu máu cục bộ gây ra do nguồn gốc bất thường động mạch vành, sửa chữa và tái tuần hoàn được thực hiện để làm giảm thiếu máu cục bộ và giảm tái phát VA (6, 7, 12-14).
Tài liệu tham khảo
1. Cook JR, Rizo-Patron C, Curtis AB, et al. Effect of surgical revascularization in patients with coronary artery disease and ventricular tachycardia or fibrillation in the Antiarrhythmics Versus Implantable Defibrillators (AVID) Registry. Am Heart J. 2002;143:821-6.
2. Velazquez EJ, Lee KL, Jones RH, et al. Coronary-artery bypass surgery in patients with ischemic cardiomyopathy. N Engl J Med. 2016;374:1511-20.
3. Every NR, Fahrenbruch CE, Hallstrom AP, et al. Influence of coronary bypass surgery on subsequent outcome of patients resuscitated from out of hospital cardiacarrest. J Am Coll Cardiol. 1992;19:1435-9.
4. Dumas F, Bougouin W, Geri G, et al. Emergency PCI in post-cardiac arrest patients without ST-segment elevation pattern: insights from the PROCAT II registry. JACC Cardiovasc Interv. 2016;9:1011-8.
5. Ngaage DL, Cale AR, Cowen ME, et al. Early and late survival after surgical revascularization for ischemic ventricular fibrillation/tachycardia. Ann Thorac Surg. 2008;85:1278-81.
6. Milojevic M, Head SJ, Parasca CA, et al. Causes of death following PCI versus CABG in complex CAD: 5-year follow-up of SYNTAX. J Am Coll Cardiol. 2016;67:42-55.
7. Carson P, Wertheimer J, Miller A, et al. The STICH trial (Surgical Treatment for Ischemic Heart Failure): mode-ofdeath results. JACC Heart Fail. 2013;1:400-8.
8. Davis JA, Cecchin F, Jones TK, et al. Major coronary artery anomalies in a pediatric population: incidence and clinical importance. J Am Coll Cardiol. 2001;37:593-7.
9. Bagnall RD, Weintraub RG, Ingles J, et al. A prospective study of sudden cardiac death among children and young adults. N Engl J Med. 2016;374:2441-52.
10.Smallman DP, Webber BJ, Mazuchowski EL, et al. Sudden cardiac death associated with physical exertion in the US military, 2005-2010. BJ Sports Med. 2016;50:118-23.
11.Maron BJ, Doerer JJ, Haas TS, et al. Sudden deaths in young competitive athletes: analysis of 1866 deaths in the United States, 1980-2006. Circulation. 2009;119:1085-92.
12.Krasuski RA, Magyar D, Hart S, et al. Long-term outcome and impact of surgery on adults with coronary arteries originating from the opposite coronary cusp. Circulation. 2011;123:154-62.
13.Layser RB, Savage MP, Halpern EJ. Anomalous coronary arteries: analysis of clinical outcome based upon arterial course and surgical intervention in an adult population. Acad Radiol. 2016;23:1015-23.
14.Taylor AJ, Rogan KM, Virmani R. Sudden cardiac death associated with isolated congenital coronary artery anomalies. J Am Coll Cardiol. 1992;20:640-47.
5.5.1. Ngoại khoa cho Điều chỉnh Rối loạn nhịp
|
Khuyến cáo Ngoại khoa cho Điều chỉnh Rối loạn nhịp Các nghiên cứu tham khảo ủng hộ các khuyến cáo được tóm tắt trong phần Tư liệu hỗ trợ online 12 |
||
|
COR |
LOE |
Các khuyến cáo |
|
IIb |
C-LD |
1. Ở các bệnh nhân có VT đơn hình trơ với các thuốc chống loạn nhịp và các nỗ lực triệt phá qua catheter, triệt phá bằng ngoại khoa có thể là phù hợp (1-7). |
Văn bản Hỗ trợ Đặc biệt – Khuyến cáo
Ngoại khoa tim như một thủ thuật độc lập cho VT hiếm khi được thực hiện, nhưng có vai trò ở một số bệnh nhân có triệu chứng nặng, khi thuốc chống loạn nhịp và triệt phá qua catheter thất bại hoặc không thể, đặc biệt nếu thất bại trong việc triệt phá là do rối loạn nhịp tim phát sinh từ khu vực không thể tiếp cận được bằng catheter, chẳng hạn như sâu trong cơ tim, bên dưới mỡ thượng tâm mạc hoặc gần các động mạch vành. Triệt phá nhịp nhanh bằng phẫu thuật cũng có thể được thực hiện vào thời điểm các can thiệp phẫu thuật tim khác, chẳng hạn như trong phẫu thuật cắt bỏ phình lớn do MI trước, trong đó vùng biên giới thường là nền cho VT, hoặc đặt một thiết bị hỗ trợ LV (LVAD ) (5-7). Thủ thuật này đòi hỏi phải có đặc điểm chi tiết về loạn nhịp thông thường với hình ảnh học và lập bản đồ trước khi phẫu thuật, do đó cắt bỏ phẫu thuật tốt nhất được thực hiện tại các trung tâm tư vấn cấp ba với sự hợp tác giữa các nhà ngoại khoa có kinh nghiệm và các nhà điện sinh lý.
Tài liệu tham khảo
1. Anter E, Hutchinson MD, Deo R, et al. Surgical ablation of refractory ventricular tachycardia in patients with nonischemic cardiomyopathy. Circ Arrhythm Electrophysiol. 2011;4:494-500.
2. Bhavani SS, Tchou P, Saliba W, et al. Surgical options for refractory ventricular tachycardia. J Card Surg. 2007;22:533- 4.
3. Choi EK, Nagashima K, Lin KY, et al. Surgical cryoablation for ventricular tachyarrhythmia arising from the left ventricular outflow tract region. Heart Rhythm. 2015;12:1128-36.
4. Kumar S, Barbhaiya CR, Sobieszczyk P, et al. Role of alternative interventional procedures when endo- and epicardial catheter ablation attempts for ventricular arrhythmias fail.Circ Arrhythm Electrophysiol. 2015;8:606-15.
5. Mulloy DP, Bhamidipati CM, Stone ML, et al. Cryoablation during left ventricular assist device implantation reduces postoperative ventricular tachyarrhythmias. J Thorac Cardiovasc Surg. 2013;145:1207-13.
6. Patel M, Rojas F, Shabari FR, et al. Safety and feasibility of open chest epicardial mapping and ablation of ventricular tachycardia during the period of left ventricular assist device implantation. J Cardiovasc Electrophysiol. 2016;27:95- 101.
7. Sartipy U, Albage A, Straat E, et al. Surgery for ventricular tachycardia in patients undergoing left ventricular reconstruction by the Dor procedure. Ann Thorac Surg. 2006;81:65-71.
5.6. Điều biến tự động (Autonomic Modulation)
|
Các khuyến cáo cho điều biến tự động Các nghiên cứu tham khảo ủng hộ các khuyến cáo được tóm tắt trong phần Tư liệu hỗ trợ online 13 và 14. |
||
|
COR |
LOE |
Các khuyến cáo |
|
IIa |
C-LD |
1. Ở các bệnh nhân có VA có triệu chứng không nguy hiểm đến tính mạng, điều trị bằng beta blocker là phù hợp (1). |
|
IIb |
C-LD |
2. Ở các bệnh nhân với bão VT/VF ở người beta blocker, các thuốc chống loạn nhịp khác, triệt phá qua catheter không hiệu quả, không dung nạp, hoặt không thể, bóc bỏ giao cảm tim có thẻ là phù hợp (2-4). |
Tóm tắt
Hoạt động giao cảm là hoạt động thúc đẩy loạn nhịp và hoạt động phó giao cảm thường là chống rối loạn nhịp trong VT/VF. Điều biến hệ thống thần kinh tự trị nhằm mục đích ngăn ngừa loạn nhịp là một phương thức điều trị mới nổi lên. Để phòng ngừa VA, điều biến tự động có thể được thực hiện hoặc thông qua việc gián đoạn hoạt động của giao cảm đối với tim, block beta bằng thuốc hoặc thông qua sự kích thích đường phó giao cảm (ví dụ, kích thích dây thần kinh phế vị, kích thích tủy sống). Mặc dù điều chế tự trị đã chứng minh hiệu quả đối với một số điều kiện nhất định như hội chứng QT kéo dài và nhịp nhanh thất đa hình do catecholamine (xem Phần 7.9), bằng chứng còn hạn chế cho áp dụng phương pháp này cho nhóm VA rộng lớn hơn, nhưng các nghiên cứu đang được tiếp tục. Hiện tại, có rất ít dữ liệu về vai trò của kích thích thần kinh phế vị và các kích thích thần kinh tủy sống để ngăn ngừa VA / SCD ở người và do đó không có khuyến cáo chính thức nào được hỗ trợ (5).
Văn bản Hỗ trợ Đặc biệt – Khuyến cáo
1. Nhiều bệnh nhân VA không nguy hiểm đến tính mạng chỉ cần sự bảo hiểm, nhưng những người khác có các triệu chứng cần điều trị. Một RCT nhỏ ở những bệnh nhân VA có triệu chứng đã giảm đáng kể gánh nặng loạn nhịp với atenolol (1).
2. Bão VT / VF gây ra bệnh suất đáng kể và có liên quan đến tử suất tăng lên. Đối với bão VT / VF trơ với điều trị (thuốc, triệt phá qua catheter, bóc bỏ giao cảm tim đã cho thấy trong một vài nghiên cứu quan sát nhỏ (3, 6) và 1 RCT (4) để giảm gánh nặng loạn nhịp. Điều này đã chỉ ra cho việc bóc bỏ giao cảm tim bên trái hoặc cả hai bên, nó đã gợi ý bóc bỏ giao cảm tim hai bên có thể tốt hơn (3). Mặc dù số liệu còn hạn chế, nhưng bệnh suất đáng kể và các lựa chọn giới hạn ở những bệnh nhân này làm cho việc bóc bỏ giao cảm tim là sự lựa chọn hợp lý ở các bệnh nhân được lựa chọn.
Tài liệu tham khảo
1. Krittayaphong R, Bhuripanyo K, Punlee K, et al. Effect of atenolol on symptomatic ventricular arrhythmia without structural heart disease: a randomized placebo-controlled study. Am Heart J. 2002;144:e10.
2. Vaseghi M, Barwad P, Malavassi Corrales FJ, et al. Cardiac sympathetic denervation for refractory ventricular arrhythmias.J Am Coll Cardiol. 2017;69:3070-80.
3. Vaseghi M, Gima J, Kanaan C, et al. Cardiac sympathetic denervation in patients with refractory ventricular arrhythmias or electrical storm:intermediate and long-term follow-up. Heart Rhythm. 2014;11:360-6.
4. Schwartz PJ, Motolese M, Pollavini G. Prevention ofsudden cardiac death after a first myocardial infarction by pharmacologic or surgical antiadrenergic interventions. J Cardiovasc Electrophysiol. 1992;3:2-16.
5. Shen MJ, Zipes DP. Role of the autonomic nervous system in modulating cardiac arrhythmias. Circ Res. 2014;114:1004-21.
6. Ajijola OA, Lellouche N, Bourke T, et al. Bilateral cardiac sympathetic denervation for the management of electrical storm. J Am Coll Cardiol. 2012;59:91-2.
6. Điều chỉnh cấp thời các VA đặc biệt
|
Các khuyến cáo cho Điều chỉnh Ngừng Tim Các nghiên cứu tham khảo ủng hộ các khuyến cáo được tóm tắt trong phần Tư liệu hỗ trợ online 15 and 16. |
||
|
COR |
LOE |
Các khuyến cáo |
|
I |
A |
1. CPR cần thực hiện ở các bệnh nhân ngừng tim, theo thuật toán hồi sinh tim mạch cơ bản và tăng cường đã được xuất bản (1-3). |
|
I |
A |
2. Ở các bệnh nhân có VA không ổn định về mặt huyết động dai dẳng và tái phát sau sốc bằng năng lượng tối đa, amiodarone truyền tĩnh mạch nên được áp dụng để nỗ lực đạt được nhịp ổn định tiếp theo khử rung (1, 4-6). |
|
I |
A |
3. Các bệnh nhân biểu hiện VA có huyết động không ổn định nên cần thực hiện chuyển nhịp bằng dòng một chiều (1-3). |
|
I |
B-NR |
4. Ở các bệnh nhân có VT đa hình hoặc VF với MI ST chênh lên, chụp mạch và tái tuần hoàn cấp cứu được khuyến cáo (7-10). |
|
I |
C-EO |
5. Bệnh nhân có nhịp nhanh QRS rộng nên được coi như VT nếu chẩn đoán chưa rõ. |
|
IIa |
A |
6. Ở các bệnh nhân với VT ổn định về mặt huyết động, sử dụng procainamide có thể hữu ích để nỗ lực cắt cơn VT (11-13). |
|
IIa |
B-R |
7. Ở những bệnh nhân bị ngừng tim vì VF hoặc VT đa hình đã được xác nhận không đáp ứng với CPR, khử rung tim, và điều trị vận mạch, truyền lidocaine tĩnh mạch có thể có lợi (1, 4, 5, 14, 15). |
|
IIa |
B-R |
8. Ở các bệnh nhân có VT đa hình do thiếu máu cơ tim cục bộ, beta blocker tĩnh mạch có thể hữu ích (16, 17). |
|
IIa |
B-NR |
9. Ở các bệnh nhân có MI mới có VT/VF tái phát nhanh chóng mặc dù chuyển nhịp bằng dòng một chiều và thuốc chống loạn nhịp (bão VT/VF), beta blocker tĩnh mạch có thể hữu ích (17, 18). |
|
IIb |
A |
10. Ở các bệnh nhân ngừng tim, sử dụng epinephrine (1 mg mỗi 3 đến 5 phút) trong quá trình CPR có thể là phù hợp (1, 19-24) |
|
IIb |
B-R |
11. Ở các bệnh nhân với VT ổn định về huyết động, sử dụng amiodarone hoặc sotalol tĩnh mạch có thể được xem xét để nỗ lực cắt VT (5, 13, 25, 26). |
|
III: no benefit |
A |
12. Ở các bệnh nhân có ngừng tim, sử dụng epinephrine liều cao (>1 mg boluses) so sánh với liều chuẩn là không có lợi ích (19, 21). |
|
III: no benefit |
A |
13. Ở các bệnh nhân có VT trơ không liên quan đến xoắn đỉnh, sử dụng magiê tĩnh mạch là không có lợi ích (27, 28). |
|
III: harm |
B-NR |
14. Ở các bệnh nhân có AMI được nghi ngờ, sử dụng lidocaine hoặc amiodarone liều cao dự phòng cho ngăn chặn VT là có hại một cách tiềm ẩn (16, 29). |
|
III: harm |
C-LD |
15. Ở các bệnh nhân có nhịp nhanh phức hợp QRS rộng chưa rõ nguồn gốc, blocker kênh canxi (như verapamil và diltiazem) là có hại tiềm tàng (30, 31). |
Văn bản Hỗ trợ Đặc biệt – Khuyến cáo
1. Các cơ chế điện học phổ biến nhất đối với ngưng tim là VF và VT vô mạch, nhưng một số lượng lớn các cơn ngừng tim bắt đầu là nhịp tim chậm hoặc vô tâm thu. Sự sống sót đối với bệnh nhân có VT hoặc VF tốt hơn so với những người cơ chế nhịp chậm hoặc vô tâm thu (32). Sự xuất hiện nhanh chóng của nhân viên y tế là yếu tố chính quyết định sự sống sót. Một số chiến lược để đáp ứng ngưng tim bất ngờ, bao gồm khử rung nhanh và bắt đầu CPR cho ngừng tim được phát hiện, đã cải thiện xác suất sống sót cho các nạn nhân bị ngưng tim (2, 3). Tuy nhiên, số lượng tuyệt đối và tỷ lệ người sống sót vẫn còn thấp, ngoại trừ những tình huống đặc biệt có thời gian phản ứng cực nhanh đối với các nạn nhân trong VF hoặc VT như trong các đơn vị chăm sóc đặc biệt được theo dõi, ở đó tỷ lệ sống sót > 90% (33-36). Thời gian sống sót giảm rõ rệt sau 2 phút bắt đầu ngừng tim, do đó từ 4 đến 5 phút, tỷ lệ sống sót có thể là ≤ 25%, và 10 phút là 0% (33, 35, 36). Các hoạt động hồi sinh tăng cường, ngoài các vấn đề liên quan trực tiếp đến việc chuyển nhịp và khử rung để kiểm soát nhịp nhanh, đã dẫn đến việc tạo ra các quy trình toàn diện để hướng dẫn những người phản ứng. Các tài liệu AHA này bao gồm phạm vi rộng các tình huống lâm sàng và các xem xét về cơ chế (1, 37).
2. Quản lý điều trị amiodarone sau ít nhất 3 lần sốc thất bại và sử dụng epinephrine đã cải thiện tỷ lệ nhập viện khi so sánh với placebo (6) hoặc lidocaine 1,5 mg / kg (1, 4) trong RCT ở người lớn bị ngừng tim ngoài bệnh viện do VF trơ hoặc VT hình đa hình, mặc dù sự sống sót ở bệnh viện và tỷ lệ sống sót để suất viện và sống sót với hậu quả thần kinh thuận lợi đã không được cải thiện với amiodarone hoặc lidocaine (5). Tuy nhiên, trong phân nhóm bệnh nhân bị ngưng tim được chứng minh do VF khởi đầu trơ với sốc hoặc VT vô mạch, sống sót để ra viện sau sử dụng amiodarone là cao hơn với placebo (5). Việc sử dụng procainamide trong ngừng tim ngoài bệnh viện do VF hoặc VT vô mạch đã không được kết hợp với nhiều sốc hơn, can thiệp thuốc nhiều hơn, thời gian hồi sức dài hơn, và sống sót thấp hơn (38).
3. VA với không ổn định về huyết động, gồm VF và VT đơn hình và đa hình vô mạch, gây mất tri giác và đưa đến tử vong nếu không được điều trị. Thời gian ngắn để chuyên nhịp bằng dòng điện môt chiều là sự khẳng định lớn sống sót, và khử rung nên được thực hiện khi càng nhanh nếu có thể. CPR được sử dụng đến tận khi nhịp có hiệu quả được phục hồi. Nếu khử rung không thành công để tuần hoàn tự phát trở lại, người phản ứng tiếp tục các hoạt động hồi sinh tuần hoàn tăng cường (1-3).
4. Xác định nhanh và điều trị bệnh nhân ngừng tim ngoài bệnh viện liên quan đến tắc nghẽn mạch vành cấp tính có liên quan đến sự sống sót được cải thiện và hồi phục chức năng tốt hơn (37). Các trường hợp lâm sàng tắc nghẽn như nguyên nhân của ngừng tim không được dự đoán chắc chắn bằng các nhận định lâm sàng và điện tâm đồ (7), và chụp mạch vành cấp cứu nên được xem xét (hơn là trễ hơn khi nằm bệnh viện hoặc không làm gì cả) cho các bệnh nhân không ổn định với nghi ngờ căn nguyên tim mạch bất kể bệnh nhân có hôn mê hoặc tỉnh hay không (9, 39). Trong 1 nghiên cứu quan sát bệnh nhân hồi sinh từ SCA không có ST chênh lên và đã và chụp mạch máu, 1/3 được tìm thấy có tổn thương gây tử vong và can thiệp mạch vành có liên quan đến khả năng có hậu quả thần kinh tốt hơn.
5. Điều chỉnh khởi đầu của bất kỳ nhịp nhanh nào nên thực hiện theo các hướng dẫn hôi sinh tim mạch tăng cường của AHA đã được xuất bản (40). Chuyển nhịp ngay lập tức nên được thực hiện cho sự không ổn định về huyết động học có biểu hiện hoặc nếu có phát triển sau đó. Cần thu lượm ECG đối với nhịp ổn định. Nhịp nhanh phức bộ rộng, được xác định khi khoảng thời gian của QRS lớn ≥ 0.12 s (37), có thể do VT, SVT có dẫn truyền lệch hướng, nhịp nhanh kích thích sớm. Nhịp nhanh phức hợp QRS không đều có thể là VA với dẫn truyền lệch hướng, AF kích thích sớm (như AF sử dụng đường phụ cho đường xuôi), cuồng nhĩ, hoặc VT (37). Chẩn đoàn cần được xác định, tư vấn với các chuyên gia loạn nhịp được xem xét (37).
6. Trong 1 nghiên cứu, amiodarone hiệu quả hơn lidocaine khi cắt VT liên hồi với sống sót đực cải thiện trong 24 giờ (26). Đối với những bệnh nhân có VT ổn định và tái phát, không phải trong trạng thái AMI, procainamide tiêm tĩnh mạch đã được chứng minh tốt hơn so với lidocaine để cắt cơn loạn nhịp (11). Một thử nghiệm ngẫu nhiên trên 62 bệnh nhân nhận thấy procainamide vượt trội so với amiodarone để chấm dứt ổn định VT (13). Các tác dụng bất lợi, kể cả hạ huyết áp phổ biến hơn với amiodarone, nhưng sự khác biệt không có ý nghĩa thống kê. Procainamide và chất chuyển hóa n-acetylprocainamide có tính chất chặn kênh kali có thể làm kéo dài khoảng QT. Ở những bệnh nhân đã có QT kéo dài, dùng procainamide có thể kéo dài thêm khoảng QT và dẫn đến torsades de pointes (11, 12, 26).
7. Lidocaine tiêm tĩnh mạch là một thuốc chống loạn nhịp thay thế có tính quen thuộc lâu đời và phổ biến rộng rãi. So với các thuốc không phải chống loạn nhịp, lidocaine không làm tăng sự trở lại của tuần hoàn tự phát sau khử rung và không được kết hợp với cải thiện trong sự sống sót đưa đến xuất viện (4, 14, 41). Trong RCTs tiền cứu, mù, lidocaine ít hiệu quả hơn so với amiodarone trong việc cải thiện tỷ lệ nhập viện sau khi ngừng tim ngoài bệnh viện do VF trơ hoặc VT đa hình trơ với sốc; nhưng không có sự khác biệt giữa 2 thuốc trong sống sót để xuất viện (4, 5). Tuy nhiên, trong phân nhóm bệnh nhân SCA được chứng minh do VF hoặc VT vô mạch khởi đầu trơ với sốc, phân tích phân nhóm cho thấy sự sống sót khi xuất viện với lidocaine tốt hơn so với giả dược (5, 42).
8. Trong một phân tích gộp lớn các thuốc chống loạn nhịp trong trạng thái AMI, beta blockers được kết hợp với giảm có ý nghĩa trong tử suất (16). Beta blockers có thể có hiệu qua trong việc ức chế VF tái phát ở các bệnh nhân có MI mới xảy ra, với cải thiện sống sót được kết hợp (17).
9. Ở những bệnh nhân bị VT / VF tái phát (cơn bão VT / VF) trong trạng thái MI mới xẩy ra trơ với amiodarone và / hoặc lidocarine và chuyển nhịp nhắc lại, sử dụng beta blockes đã chỉ ra cải thiện sống sót trong 1 tuần. Đối với các trườn hợp đó không sống sót, tử suất chủ yếu do VF tái phát. Sống sót trong 1 năm cũng tốt hơn trong các trường hợp đó được điều trị bằng beta blockers (17, 18). Các biện pháp khác để làm giảm trương lực giao cảm gồm gây mê và gây tê nói chung cũng thường được sử dụng.
10. Epinephrine tạo ra các ảnh hưởng có tác dụng lợi ích ở bệnh nhân trong quá trình ngừng tim, trước hết do các ảnh hưởng alphaadrenergic (tức co mạch) (1). Những hiệu quả alpha-adrenergic này có thể làm tăng áp lực tưới máu mạch vành và não trong quá trình CPR. Giá trị và sự an toàn của các ảnh hương beta-adrenergic của epinephrine đang gây tranh cải do chúng có thể làm tăng hoạt động của cơ tim và giảm tưới máu dưới nội tâm mạc (1). Một thử nghiệm đánh giá các kết cục ngắn hạn và dài hạn khi so sánh liều chuẩn epinephrine với giả dược (23). Liều chuẩn Epinephrine được định nghĩa là 1 mg tiêm tĩnh mạch hoặc tủy xương (intraosseously) mỗi 3 đến 5 phút. Đối với cả hai sự sống sót đến khi xuất viện và sống sót đến khi xuất viện với hậu quả thần kinh tốt, không có lợi ích với liều epinephrine chuẩn; tuy nhiên, nghiên cứu này đã không đủ mạnh để phân tích một trong những kết quả này. Tuy nhiên, vẫn có cải thiện khả năng sống sót khi nhập viện và cải thiện khả năng tuần hoàn tự nhiên bằng sử dụng epinephrine liều chuẩn. Một số thử nghiệm đã so sánh hiệu quả của epinephrine liều chuẩn với liều epinephrine liều cao. Các thử nghiệm này không chứng minh được lợi ích của epinephrine liều cao đối với epinephrine liều chuẩn trong liên quan với tỷ lệ sống sót đến xuất viện với sự phục hồi thần kinh tốt, sống sót đến xuất viện, hoặc sống sót đến nhập viện (1, 19, 21, 22).
11. Amiodarone hiệu quả hơn lidocaine trong việc cắt cơn VT liên hồi với sống sót được cải thiện trong 24 giờ (26). Đối với những bệnh nhân có VT ổn định và tái phát, không phải trong trạng thái AMI, procainamide tiêm tĩnh mạch đã được chứng minh là tốt hơn so với lidocaine để cắt cơn loạn nhịp (11). Một RCT ở 62 bệnh nhân nhận thấy procainamide cao hơn amiodarone để cắt VT ổn định (13). Các tác dụng bất lợi, kể cả hạ huyết áp, thường gặp hơn với amiodarone, nhưng sự khác biệt không có ý nghĩa thống kê. Procainamide và chất chuyển hóa n-acetylprocainamide có tính chất chặn kênh kali có thể làm kéo dài khoảng QT. Ở những bệnh nhân đã có QT kéo dài, dùng procainamide có thể kéo dài thêm khoảng QT và dẫn tới xoắn đỉnh (11). Một RCT đơn thuần 33 bệnh nhân so sánh sotalol với lidocaine để điều trị cho các bệnh nhân có VT huyết động ổn định cho thấy VT đã được cắt cơn ở 69% bệnh nhân sử dụng sotalol và 18% dùng lidocaine (25). Tiêm tĩnh mạch sotalol đã được chấp thuận sử dụng tại Hoa Kỳ. Sotalol có đặc tính chặn kênh kali có thể kéo dài khoảng QT. Ở những bệnh nhân đã kéo dài thời gian QT, việc dùng sotalol có thể làm kéo dài khoảng QT và dẫn tới xoắn định (25).
12. Epinephrine có thể làm tăng áp lực tưới máu mạch vành và não trong quá trình CPR do hiệu quả co mạch của thuốc. Liều cao epinephrine (0,1 đến 0,2 mg / kg IV, so với liều chuẩn 1 mg) đã được nghiên cứu trong RCTs. Trong ngừng tim ngoài bệnh viện không đáp ứng với khử rung, sử dụng epinephrine liều cao đã cải thiện tỉ lệ sống sót khi nhập viện, nhưng không có sự khác biệt so với liều chuẩn epinephrine khi sống sót khi xuất viện (19). Không có sự cải thiện trong tỷ lệ sống sót lâu dài (21). Lưu ý, việc sử dụng vasopressin không còn được khuyến cáo ở hầu hết thuật toán hồi sinh tim mạch tăng cường mới đây (1).
13. Magiê có thể ngăn chặn tính tự động, ngăn chặn hậu khử cực sớm và trễ, cũng như ức ceehs dòng canxi vào cơ tim. Đó là hiệu quả trong ức chế VA liên quan đến hội chứng QT dài mắc phải. Tuy nhiên, 2 RCTs đã khám phá việc sử dụng magiê tĩnh mạch ở các bệnh nhân ngừng tim và VF trơ được nhận định là không có lợi ích (27, 28). Trong một nghiên cứu về ngừng tim ngoài bệnh viên, sử dụng 2 đến 4 gr magiê, tĩnh mạch không làm cải thiên sống sót để nhập viện (27). Trong một nghiên cứu tương tự liên quan tới ngừng tim bệnh nhân nội viện, magiê đã không cải thiện được sự trở lại tuần hoàn tự phát, sống sót đến 24h, hoặc sống sót để xuất viện (28). Có những trường hợp ngoại lệ như giảm kali máu đáng kể hoặc xoắn định tạo ra do thuốc trong đó sử dụng magiê tĩnh mạch đã được đảm bảo.
14. Một số nghiên cứu đã kiểm tra giả thuyết cho rằng sử dụng dự phòng các thuốc chống loạn nhịp có thể giảm tỷ lệ VA trong sau MI và đưa đến hậu quả tốt hơn. Một phân tích gộp các nghiên cứu đánh giá trong đó ức chế beta, các thuốc chống rối loạn nhịp class I như lidocaine và procainamide, và amiodarome đã được sử dụng trong tình huống AMI. Sử dụng phổ biến lidocaine và procainamide đã được kết hợp với tử suất tăng lên, ngược lại beta blockers được kết hợp với tần số tử suất thấp hơn một cách có ý nghĩa (16). Số liệu hạn chế với amiodarone dường như hứa hẹn, nhưng một nghiên cứu RCT tiếp theo có 1073 bệnh nhân nhận thấy dùng amiodarone liều cao dẫn đến tỷ lệ tử vong cao hơn, mặc dù liều amiodarone trung bình không ưu thế hơn giả dược (29).
15. Với rối loạn nhịp nhanh QRS rộng và ổn định, sự khác biệt giữa SVT với dẫn truyền lệch hướng và VT thường có thể bằng cách xem lại bệnh sử bệnh nhân và 12 chuyển đạo trong quá trình nhịp nhanh. Bệnh nhân có nhịp nhanh phức bộ QRS rộng và bệnh tim cấu trúc đã biết nên được cho là do VT cho đến khi được chứng minh phân biệt rõ. Việc sử dụng thuốc chẹn kênh canxi như verapamil cho bệnh nhân có VT có thể dẫn đến hạ huyết áp hoặc ngất (31). Ngoại trừ VT nhạy cảm với verapamil (vào lại nhánh bó) xuất hiện ở tim cấu trúc bình thường; nhưng điều này thường khó để ghi nhận lưc khởi đầu biểu hiện (30).
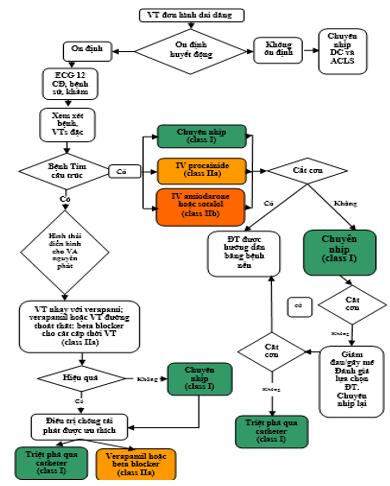
Hình 2. Điều chỉnh VT Đơn hình dai dẳng
Các màu tương ứng với các class khuyến cáo ở bảng 1. Xem phần 7, 8.1.3, 8.2.3, và 10 để thảo luận.
*Bệnh sử đã biết của nhậy cảm verapamil hoặc biểu hiện điện tâm đồ kinh điển. ACLS chỉ hội sinh tim mạch tăng cường: ECG chỉ điện tâm đồ; VA: rối loạn nhịp thất, và VT: nhịp nhanh thất.
Tài liệu tham khảo
1. Link MS, Berkow LC, Kudenchuk PJ, et al. Part 7: adult advanced cardiovascular life support: 2015 American Heart Association guidelines update for cardiopulmonary resuscitation and emergency cardiovascular care. Circulation. 2015;132(suppl 2):S444-64.
2. Stiell IG, Wells GA, Field B, et al. Advanced cardiac life support in out-of-hospital cardiac arrest. N Engl J Med. 2004;351:647-56.
3. Sasson C, Rogers MA, Dahl J, et al. Predictors of survival from out-of-hospital cardiac arrest:a systematic review and meta-analysis. Circ Cardiovasc Qual Outcomes. 2010;3:63-81.
4. Dorian P, Cass D, Schwartz B, et al. Amiodarone as compared with lidocaine for shock-resistant ventricular fibrillation. N Engl J Med. 2002;346:884-90.
5. Kudenchuk PJ, Brown SP, Daya M, et al. Amiodarone, lidocaine, or placebo in out-of-hospital cardiac arrest. N Engl J Med. 2016;1711-22.
6. Kudenchuk PJ, Cobb LA, Copass MK, et al. Amiodarone for resuscitation after out-of-hospital cardiac arrest due to ventricular fibrillation. N Engl J Med. 1999;341:871-8.
7. Spaulding CM, Joly LM, Rosenberg A, et al. Immediate coronary angiography in survivors of out-of-hospital cardiac arrest. N Engl J Med. 1997;336:1629-33.
8. Cronier P, Vignon P, Bouferrache K, et al. Impact of routine percutaneous coronary intervention after out-of-hospital cardiac arrest due to ventricular fibrillation. Crit Care. 2011;15:R122.
9. Zanuttini D, Armellini I, Nucifora G, et al. Impact of emergency coronary angiography on in-hospital outcome of unconscious survivors after out-of-hospital cardiac arrest. Am J Cardiol. 2012;110:1723-8.
10.Dumas F, Bougouin W, Geri G, et al. Emergency PCI in post-cardiac arrest patients without ST-segment elevation pattern: insights from the PROCAT II registry. JACC Cardiovasc Interv. 2016;9:1011-8.
11.Gorgels AP, van den Dool A, Hofs A, et al. Comparison of procainamide and lidocaine in terminating sustained monomorphic ventricular tachycardia. Am J Cardiol. 1996;78:43-6.
12.Markel DT, Gold LS, Allen J, et al. Procainamide and survival in ventricular fibrillation out-of-hospital cardiac arrest. Acad Emerg Med. 2010;17:617-23.
13.Ortiz M, Martin A, Arribas F, et al. Randomized comparison of intravenous procainamide vs. intravenous amiodarone for the acute treatment of tolerated wide QRS tachycardia: the PROCAMIO study. Eur Heart J. 2017;38:1329-35.
14.Herlitz J, Ekstrom L, Wennerblom B, et al. Lidocaine in out-of-hospital ventricular fibrillation. Does it improve survival? Resuscitation. 1997;33:199-205.
15.Kudenchuk PJ, Newell C, White L, et al. Prophylactic lidocaine for post resuscitation care of patients with out-ofhospital ventricular fibrillation cardiac arrest. Resuscitation. 2013;84:1512-8.
16.Teo KK, Yusuf S, Furberg CD. Effects of prophylactic antiarrhythmicdrug therapy in acute myocardial infarction. An overview of results from randomized controlled trials. JAMA. 1993;270:1589-95.
17.Nademanee K, Taylor R, Bailey WE, et al. Treating electrical storm: sympathetic blockade versus advanced cardiac life support-guided therapy. Circulation. 2000;102:742-7.
18.Piccini JP, Hranitzky PM, Kilaru R, et al. Relation of mortality to failure to prescribe beta blockers acutely in patients with sustained ventricular tachycardia and ventricular fibrillation following acute myocardial infarction (from the VALsartan In Acute myocardial iNfarcTion trial [VALIANT] Registry). Am J Cardiol. 2008;102:1427-32.
19.Callaham M, Madsen CD, Barton CW, et al. A randomized clinical trial of high-dose epinephrine and norepinephrine vs standard-dose epinephrine in prehospital cardiac arrest. JAMA. 1992;268:2667-72.
20.Donnino MW, Salciccioli JD, Howell MD, et al. Time to administration of epinephrine and outcome after in-hospital cardiac arrest with non-shockable rhythms: retrospective analysis of large in-hospital data registry. BMJ. 2014;348:g3028.
21.Gueugniaud PY, Mols P, Goldstein P, et al. A comparison of repeated high doses and repeated standard doses of epinephrine for cardiac arrest outside the hospital. European Epinephrine Study Group. N Engl J Med. 1998;339:1595-601.
22.Hagihara A, Hasegawa M, Abe T, et al. Prehospital epinephrine use and survival among patients with out-of-hospital cardiac arrest. JAMA. 2012;307:1161-8.
23.Jacobs IG, Finn JC, Jelinek GA, et al. Effect of adrenaline on survival in out-of-hospital cardiac arrest: a randomised double-blind placebo-controlled trial. Resuscitation. 2011;82:1138-43.
24.Koscik C, Pinawin A, McGovern H, et al. Rapid epinephrine administration improves early outcomes in out-ofhospital cardiac arrest. Resuscitation. 2013;84:915-20.
25.Ho DS, Zecchin RP, Richards DA, et al. Double-blind trial of lignocaine versus sotalol for acute termination of spontaneous sustained ventricular tachycardia. Lancet. 1994;344:18-23.
26.Somberg JC, Bailin SJ, Haffajee CI, et al. Intravenous lidocaine versus intravenous amiodarone (in a new aqueous formulation) for incessant ventricular tachycardia. Am J Cardiol 2002;90:853-9.
27.Hassan TB, Jagger C, Barnett DB. A randomised trial to investigate the efficacy of magnesium sulphate for refractory ventricular fibrillation. Emerg Med J. 2002;19:57-62.
28.Thel MC, Armstrong AL, McNulty SE, et al. Randomised trial of magnesium in in-hospital cardiac arrest. Duke Internal Medicine Housestaff. Lancet. 1997;350:1272-6.
29.Elizari MV, Martinez JM, Belziti C, et al. Morbidity and mortality following early administration of amiodarone in acute myocardial infarction. GEMICA study investigators, GEMA Group, Buenos Aires, Argentina. Grupo de Estudios Multicentricos en Argentina. Eur Heart J. 2000;21:198-205.
30.Belhassen B, Horowitz LN. Use of intravenous verapamil for ventricular tachycardia. Am J Cardiol. 1984;54:1131-3.
31.Buxton AE, Marchlinski FE, Doherty JU, et al. Hazards of intravenous verapamil for sustained ventricular tachycardia. Am J Cardiol. 1987;59:1107-10.
32.Zipes DP, Camm AJ, Borggrefe M, et al. ACC/AHA/ESC 2006 guidelines for management of patients with ventricular arrhythmias and the prevention of sudden cardiac death: a report of the American College of Cardiology/American Heart Association Task Force and the European Society of Cardiology Committee for Practice Guidelines. Circulation. 2006;114:e385-484.
33.Cobb LA, Fahrenbruch CE, Walsh TR, et al. Influence of cardiopulmonary resuscitation prior to defibrillation in patients with out-of-hospital ventricular fibrillation. JAMA. 1999;281:1182-8.
34.Cobb LA, Weaver WD, Fahrenbruch CE, et al. Community-based interventions for sudden cardiac death. Impact, limitations, and changes. Circulation. 1992;85(suppl):I98-102.
35.Weisfeldt ML, Becker LB. Resuscitation after cardiac arrest: a 3-phase time-sensitive model. JAMA. 2002;288:3035- 8.
36.Wik L, Hansen TB, Fylling F, et al. Delaying defibrillation to give basic cardiopulmonary resuscitation to patients with out-of-hospital ventricular fibrillation: a randomized trial. JAMA. 2003;289:1389-95.
37.Neumar RW, Otto CW, Link MS, et al. Part 8: adult advanced cardiovascular life support: 2010 American Heart Association guidelines for cardiopulmonary resuscitation and emergency cardiovascular care. Circulation. 2010;122(suppl 2):S729-67.
38.Connolly SJ, Hallstrom AP, Cappato R, et al. Meta-analysis of the implantable cardioverter defibrillator secondary prevention trials. AVID, CASH and CIDS studies. Antiarrhythmics vs implantable defibrillator study. Cardiac Arrest Study Hamburg. Canadian Implantable Defibrillator Study. Eur Heart J. 2000;21:2071-8.
39.Kern KB. Optimal treatment of patients surviving out-of-hospital cardiac arrest. JACC Cardiovasc Intervent. 2012;5:597-605.
40.Perkins GD, Jacobs IG, Nadkarni VM, et al. Cardiac arrest and cardiopulmonary resuscitation outcome reports: update of the Utstein Resuscitation Registry Templates for out-of-hospital cardiac arrest: a statement for healthcare professionals from a task force of the International Liaison Committee on Resuscitation (American Heart Association, European Resuscitation Council, Australian and New Zealand Council on Resuscitation, Heart and Stroke Foundation of Canada, InterAmerican Heart Foundation, Resuscitation Council of Southern Africa, Resuscitation Council of Asia); and the American Heart Association Emergency Cardiovascular Care Committee and the Council on Cardiopulmonary, Critical Care, Perioperative and Resuscitation. Circulation. 2015;132:1286-300.
41.Link MS, Myerburg RJ, Estes NA3rd. Eligibility and disqualification recommendations for competitive athletes with cardiovascular abnormalities: Task Force 12: emergency action plans, resuscitation, cardiopulmonary resuscitation, and automated external defibrillators: a scientific statement from the American Heart Association and American College of Cardiology. Circulation. 2015;132:e334-8.
42.Joglar JA, Page RL. Out-of-hospital cardiac arrest–are drugs ever the answer? N Engl J Med. 2016;374:1781-2.
TÀI LIỆU THAM KHẢO
1. Myerburg RJ, Junttila MJ. Sudden cardiac death caused by coronary heart disease. Circulation. 2012;125:1043-52.
2. Buxton AE, Calkins H, Callans DJ, et al. ACC/AHA/HRS 2006 key data elements and definitions for electrophysiological studies and procedures: a report of the American College of Cardiology/American Heart Association Task Force on Clinical Data Standards.Circulation. 2006;114:2534-70.
3. Sapp JL, Wells GA, Parkash R, et al. Ventricular tachycardia ablation versus escalation of antiarrhythmic drugs. N Engl J Med. 2016;375:111-21.
4. Priori SG, Wilde AA, Horie M, et al. HRS/EHRA/APHRS expert consensus statement on the diagnosis and management of patients with inherited primary arrhythmia syndromes. Heart Rhythm. 2013;10:1932-63. 5. Hiss RG, Lamb LE. Electrocardiographic findings in 122,043 individuals. Circulation. 1962;25:947-61.
6. Brodsky M, Wu D, Denes P, et al. Arrhythmias documented by 24 hour continuous electrocardiographic monitoring in 50 male medical students without apparent heart disease. Am J Cardiol. 1977;39:390-5.
7. Massing MW, Simpson RJ Jr, Rautaharju PM, et al. Usefulness of ventricular premature complexes to predict coronary heart disease events and mortality (from the Atherosclerosis Risk In Communities cohort). Am J Cardiol. 2006;98:1609-12.
8. Ofoma U, He F, Shaffer ML, et al. Premature cardiac contractions and risk of incident ischemic stroke. J Am Heart Assoc. 2012;1:e002519.
9. Ataklte F, Erqou S, Laukkanen J, et al. Meta-analysis of ventricular premature complexes and their relation to cardiac mortality in general populations. Am J Cardiol. 2013;112:1263-70.
10.Lin CY, Chang SL, Lin YJ, et al. Long-term outcome of multiform premature ventricular complexes in structurally normal heart. Int J Cardiol. 2015;180:80-5.
11.Lin CY, Chang SL, Chung FP, et al. Long-term outcome of non-sustained ventricular tachycardia in structurally normal hearts. PloS One. 2016;11:e0160181.
12.Ruberman W, Weinblatt E, Goldberg JD, et al. Ventricular premature complexes and sudden death after myocardial infarction. Circulation. 1981;64:297-305.
13.Ruberman W, Weinblatt E, Goldberg JD, et al. Ventricular premature beats and mortality after myocardial infarction. N Engl J Med. 1977;297:750-7.
14.The Cardiac Arrhythmia Suppression Trial II Investigators. Effect of the antiarrhythmic agent moricizine on survival after myocardial infarction. The Cardiac Arrhythmia Suppression Trial II Investigators. N Engl J Med. 1992;327:227- 33.
15.Echt DS, Liebson PR, Mitchell LB, et al. Mortality and morbidity in patients receiving encainide, flecainide, or placebo. The Cardiac Arrhythmia Suppression Trial. N Engl J Med. 1991;324:781-8. 16.Morganroth J, Goin JE. Quinidine-related mortality in the short-to-medium-term treatment of ventricular arrhythmias. A meta-analysis. Circulation. 1991;84:1977-83.
17.Waldo AL, Camm AJ, deRuyter H, et al. Effect of d-sotalol on mortality in patients with left ventricular dysfunction after recent and remote myocardial infarction. The SWORD Investigators. Survival With Oral d-Sotalol. Lancet. 1996;348:7-12.
18.Ling Z, Liu Z, Su L, et al. Radiofrequency ablation versus antiarrhythmic medication for treatment of ventricular premature beats from the right ventricular outflow tract: prospective randomized study. Circ Arrhythm Electrophysiol. 2014;7:237-43.
19.Jouven X, Zureik M, Desnos M, et al. Long-term outcome in asymptomatic men with exercise-induced premature ventricular depolarizations. N Engl J Med. 2000;343:826-33.
20.Frolkis JP, Pothier CE, Blackstone EH, et al. Frequent ventricular ectopy after exercise as a predictor of death. N Engl J Med. 2003;348:781-90.
21.Biffi A, Pelliccia A, Verdile L, et al. Long-term clinical significance of frequent and complex ventricular tachyarrhythmias in trained athletes. J Am Coll Cardiol. 2002;40:446-52.
22.Heidbüchel H, Hoogsteen J, Fagard R, et al. High prevalence of right ventricular involvementin endurance athletes with ventricular arrhythmias: role of an electrophysiologic study in risk stratification. Eur Heart J. 2003;24:1473-80.
23.Kanei Y, Friedman M, Ogawa N, et al. Frequent premature ventricular complexes originating from the right ventricular outflow tract are associated with left ventricular dysfunction. Ann Noninvasive Electrocardiol. 2008;13:81-5.
24.Lee GK, Klarich KW, Grogan M, et al. Premature ventricular contraction-induced cardiomyopathy: a treatable condition. Circ Arrhythm Electrophysiol. 2012;5:229-36.
25.Viskin S, Rosso R, Rogowski O, et al. The “short-coupled” variant of right ventricular outflow ventricular tachycardia: a not-so-benign form of benign ventricular tachycardia? J Cardiovasc Electrophysiol. 2005;16:912-6.
26.Noda T, Shimizu W, Taguchi A, et al. Malignant entity of idiopathic ventricular fibrillation and polymorphic ventricular tachycardia initiated by premature extrasystoles originating from the right ventricular outflow tract. J Am Coll Cardiol. 2005;46:1288-94.
27.Dumas F, Cariou A, Manzo-Silberman S, et al. Immediate percutaneous coronary intervention is associated with better survival after out-of-hospital cardiac arrest: insights from the PROCAT (Parisian Region Out of hospital Cardiac ArresT) registry. Circ Cardiovasc Interv. 2010;3:200-7.
28.Gupta S, Pressman GS Figueredo VM. Incidence of, predictors for, and mortality associated with malignant ventricular arrhythmias in non-ST elevation myocardial infarction patients. Coron Artery Dis. 2010;21:460-5.
29.Terkelsen CJ, Sorensen JT, Kaltoft AK, et al. Prevalence and significance of accelerated idioventricular rhythm in patients with ST-elevation myocardial infarction treated with primary percutaneous coronary intervention. Am J Cardiol. 2009;104:1641-6.
30.Al-Khatib SM, Granger CB, Huang Y, et al. Sustained ventricular arrhythmias among patients with acute coronary syndromes with no ST-segment elevation: incidence, predictors, and outcomes. Circulation. 2002;106:309-12.
31.Jabbari R, Engstrom T, Glinge C, et al. Incidence and risk factors of ventricular fibrillation before primary angioplasty in patients with first ST-elevation myocardial infarction: a nationwide study in Denmark. J Am Heart Assoc. 2015;4:e001399.
32.Mehta RH, Starr AZ, Lopes RD, et al. Incidence of and outcomes associated with ventricular tachycardia or fibrillation in patients undergoing primary percutaneous coronary intervention. JAMA. 2009;301:1779-89.
33.Volpi A, Cavalli A, Franzosi MG, et al. One-year prognosis of primary ventricular fibrillation complicating acute myocardial infarction. The GISSI (Gruppo Italiano per lo Studio della Streptochinasi nell’Infarto miocardico) investigators. Am J Cardiol. 1989;63:1174-8.
34.El-Sherif N, Smith RA, Evans K. Canine ventricular arrhythmias in the late myocardial infarction period. 8. Epicardial mapping of reentrant circuits. CircRes. 1981;49:255-65.
35.Ackerman MJ, Priori SG, Willems S, et al. HRS/EHRA expert consensus statement on the state of genetic testing for the channelopathies and cardiomyopathies: this document was developed as a partnership between the Heart Rhythm Society (HRS) and the European Heart Rhythm Association (EHRA). Europace. 2011;13:1077-109.
36.Nannenberg EA, Sijbrands EJ, Dijksman LM, et al. Mortality of inherited arrhythmia syndromes: insight into their natural history. Circ Cardiovasc Genet. 2012;5:183-9.
37.Haïssaguerre M, Shah DC, Jais P, et al. Role of Purkinje conducting system in triggering of idiopathic ventricular fibrillation. Lancet. 2002;359:677-8.
38.Haïssaguerre M, Shoda M, Jais P, et al. Mapping and ablation of idiopathic ventricular fibrillation. Circulation. 2002;106:962-7.
39.Goldberger JJ, Buxton AE, Cain M, et al. Risk stratification for arrhythmic sudden cardiac death: identifying the roadblocks. Circulation. 2011;123:2423-30.
40.Fishman GI, Chugh SS, DiMarco JP, et al. Sudden cardiac death prediction and prevention: report from a National Heart, Lung, and Blood Institute and Heart Rhythm Society Workshop. Circulation. 2010;122:2335-48.
41.Myerburg RJ. Sudden cardiac death: exploring the limits of our knowledge. J Cardiovasc Electrophysiol. 2001;12:369- 81.
42.Kong MH, Fonarow GC, Peterson ED, et al. Systematic review of the incidence of sudden cardiac death in the United States. J Am Coll Cardiol. 2011;57:794-801.
43.Mozaffarian D, Benjamin EJ, Go AS, et al. Heart disease and stroke statistics—2016 update: a report from the American Heart Association. Circulation. 2016;133:e38-360.
44.Benjamin EJ, Blaha MJ, Chiuve SE, et al. Heart disease and stroke statistics—2017 update: a report fromthe American Heart Association. Circulation. 2017;135:e146-603.
45.Merchant RM, Yang L, Becker LB, et al. Incidence of treated cardiac arrest in hospitalized patients in the United States. Crit Care Med. 2011;39:2401-6.
46.Institute of Medicine. Committee on the Treatment of Cardiac Arrest: Current Status and Future Directions: Strategies to improve cardiac arrest survival: a time to act.Washington, DC: National Academic Press; 2015.
47.Jollis JG, Granger CB. Improving care of out-of-hospital cardiac arrest: next steps. Circulation. 2016;134:2040-2.
48.Daya MR, Schmicker R, May SH, et al. Current burden of cardiac arrest in the United States: report from the Resuscitation Outcomes Consortium. Paper commissioned by the Committee on the Treatment of Cardiac Arrest: Current Status and Future Directions. 2015.
49.Myerburg RJ, Halperin H, Egan DA, et al. Pulseless electric activity: definition, causes, mechanisms, management, and research priorities for the next decade: report from a National Heart, Lung, and Blood Institute workshop. Circulation. 2013;128:2532-41.
50.Myerburg RJ, Goldberger JJ. Sudden cardiac arrest risk assessment: population science and the individual risk mandate. JAMA Cardiol. 2017;2:689-94.
51.Bogle BM, Ning H, Mehrotra S, et al. Lifetime risk for sudden cardiac death in the community. J Am Heart Assoc. 2016;5:e002398.
52.Junttila MJ, Hookana E, Kaikkonen KS, et al. Temporal trends in the clinical and pathological characteristics of victims of sudden cardiac death in the absence of previously identified heart disease. Circ Arrhythm Electrophysiol. 2016;9:e003723.
53.Hookana E, Junttila MJ, Puurunen VP, et al. Causes of nonischemic sudden cardiac death in the current era. Heart Rhythm. 2011;8:1570-5.
54.Wong MK, Morrison LJ, Qiu F, et al. Trends in short- and long-term survival among out-of-hospital cardiac arrest patients alive at hospital arrival. Circulation. 2014;130:1883-90.







