 Từ năm 1930, Louis Wolff, Sir John Parkinson, và Paul Dudley White đã mô tả 11 bệnh nhân có một dạng điện tâm đồ đặc biệt và thường xuất hiện những cơn nhịp tim nhanh. ECG cho thấy các đặc trưng là khoảng PR ngắn kèm dạng
Từ năm 1930, Louis Wolff, Sir John Parkinson, và Paul Dudley White đã mô tả 11 bệnh nhân có một dạng điện tâm đồ đặc biệt và thường xuất hiện những cơn nhịp tim nhanh. ECG cho thấy các đặc trưng là khoảng PR ngắn kèm dạng
Bệnh viện Nhân Dân 115
Từ năm 1930, Louis Wolff, Sir John Parkinson, và Paul Dudley White đã mô tả 11 bệnh nhân có một dạng điện tâm đồ đặc biệt và thường xuất hiện những cơn nhịp tim nhanh. ECG cho thấy các đặc trưng là khoảng PR ngắn kèm dạng block nhánh, hội chứng này sau đó được gọi là Wolff-Parkinson-White (WPW syndrome). Những hiểu biết càng nhiều về hội chứng này cho thấy khi tim nhanh, các triệu chứng thay đổi rất đa dạng từ nhẹ như hồi hộp đến nặng như ngất và nguy hiểm hơn là đột tử. Ngày nay, với việc sử dụng thường quy ECG trong khám bệnh ở nhiều chuyên khoa khác nhau, trước các thủ thuật y khoa và đặc biệt là kiểm tra sức khỏe định kỳ, càng ngày các bác sỹ càng gặp nhiều những người có ECG dạng WPW mà bệnh nhân không có các triệu chứng gợi ý bệnh lý tim mạch. Vậy, thái độ xử trí của chúng ta trước các trường hợp này như thế nào? Bài viết dưới đây sẽ nêu quan điểm hiện nay về vấn đề này.
I. SINH LÝ BỆNH
Năm 1943, các nhà khoa học đã chứng minh trong hội chứng WPW có những bó dẫn truyền bất thường (bó Kent) nối từ nhĩ xuống thất và không đi qua hệ thống nút nhĩ-thất (nút AV). Xung động từ nhĩ xuống thất qua bó Kent nhanh hơn và gây khử cực thất sớm hơn khi qua nút AV nên hội chứng WPW còn được gọi là hội chứng kích thích sớm (preexcitation syndrome). Khi đó, thất sẽ được khử cực từ cả hai xung động: một qua nút AV và một qua đường phụ (bó Kent).
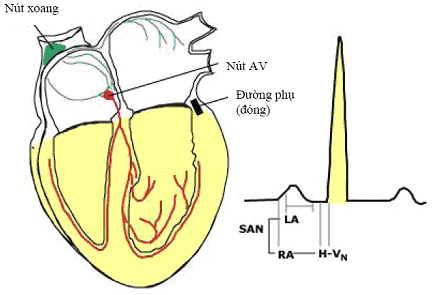
Những khảo sát điện sinh lý cho thấy bó Kent có thể định vị ở bất cứ nơi nào trong rãnh nhĩ thất hay trong vách liên thất. Thường gặp nhất là thành bên tim trái (50%), sau vách liên thất (30%), trước vách liên thất bên phải (10%) và thành bên tim phải (10%) (hình 1). Khoảng 13% những người có kích thích sớm có nhiều hơn một đường phụ[1]
Bất thường trên tim khác[2]: hầu hết bệnh nhân không có các bệnh lý về cấu trúc tim ngoại trừ nhóm bệnh theo tuổi. Bệnh tim bẩm sinh (nếu có) thường là các bất thường bên tim phải. Bệnh Ebstein là loại tim bẩm sinh có liên quan mạnh nhất đến hội chứng WPW; 10%-20% bệnh nhân loại này có ít nhất một đường phụ; đa số đường phụ ở thành tự do thất phải và sau vách liên thất bên phải[3]. Liên quan giữa sa 2 lá và đường phụ bên trái cũng được ghi nhận, tuy nhiên nhiều khả năng là cùng tồn tại ngẫu nhiên. Dạng WPW gia đình có liên quan đến bệnh cơ tim phì đại.
II. BIỂU HIỆN TRÊN ECG
II.1. Kích thích sớm
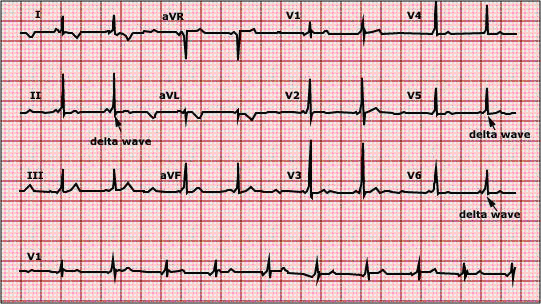
ECG trong hội chứng WPW có 2 đặc điểm chính (hình 2):
- Khoảng PR ngắn (nhỏ hơn 0,12 giây) do xung động dẫn truyền qua đường phụ nhanh hơn.
- Phức bộ QRS là sự kết hợp giữa khử cực thất sớm do xung động từ nhĩ xuống thất qua đường phụ và khử cực thất trễ hơn do xung động qua nút AV. Phần đầu của phức bộ QRS là chậm do đây là dẫn truyền chậm từ sợi cơ đến sợi cơ và gọi là sóng delta. Dẫn truyền qua đường phụ càng nhanh thì lượng cơ tim được khử cực từ đường phụ càng lớn, sóng delta càng lớn càng nổi trội và QRS càng rộng (hình 3, 4, 5, 6).
Khi một người có ECG theo các tiêu chuẩn trên và không có biểu hiện bệnh thì gọi là ECG dạng WPW(WPW pattern) hay WPW không triệu chứng. Khi bệnh nhân vừa có ECG dạng WPW vừa có các rối loạn nhịp đặc trưng thì gọi là hội chứng WPW (WPW syndrome).
Hình 2. ECG dạng WPW(mũi tên chỉ sóng delta)[4]
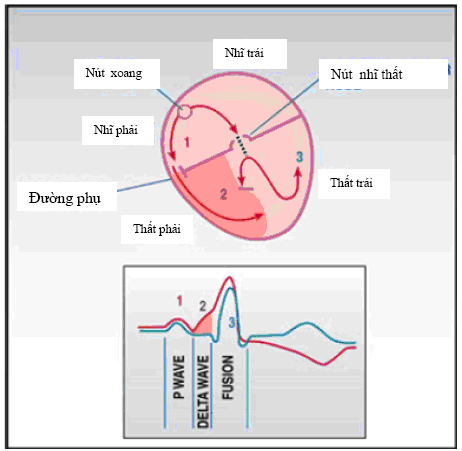
Hình 3. Sơ đồ giải thích ECG trong WPW. “1”-khử cực nhĩ tạo sóng P trên ECG. “2”- khử cực thất qua đường phụ tạo sóng delta. “3”- khử cực thất theo đường nút AV. “2” và “3” cùng khử cực thất tạo phần cuối của phức bộ QRS.
Hình 4. Sơ đồ mô tả ECG trong trường hợp không có đường phụ hay đường phụ bị đóng. “SAN”-nút xoang phát xung động khử cực nhĩ phải, nhĩ trái. “LA”-khử cực nhĩ trái. “RA”- khử cực nhĩ phải. “H”- khử cực bó His. “VN“- khử cực thất bình thường.

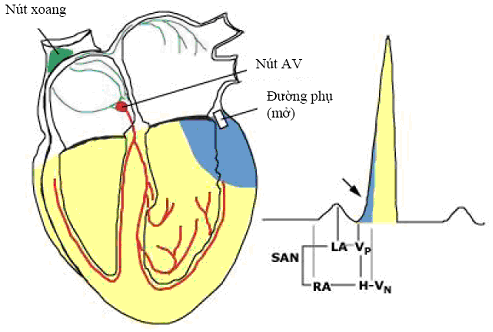
Hình 5. Sơ đồ mô tả ECG trong trường hợp đường phụ mở. Xung động qua đường phụ khử cực sớm thất-“VP“. Vùng xám ở thất là vùng được khử cực sớm từ xung động qua đường phụ. Mũi tên chỉ sóng delta.
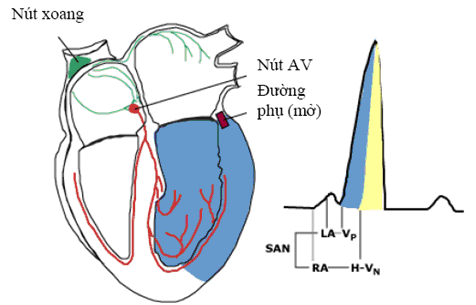
Hình 6. Sơ đồ mô tả ECG trong trường hợp đường phụ mở và có nút AV dẫn truyền chậm. Thất đuợc khử cực bằng đường phụ nhiều hơn. Sóng delta rõ, phức bộ QRS rộng.
Khoảng PR[5]. Do xung động dẫn truyền tắt
và không qua nút AV nên khoảng PR trong WPW ngắn hơn bình thường.
QRS. Có hai dạng QRS trong WPW[1] :
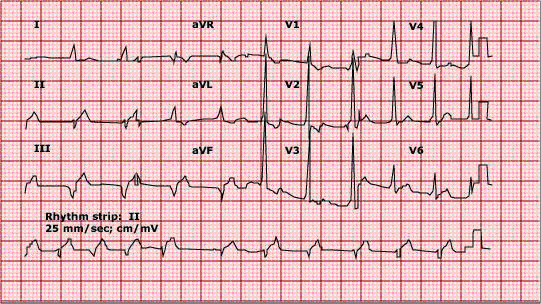
- Type A, do đường phụ ở bên trái, sóng R cao ở chuyển đạo V1-V3 (sóng delta dương hay đi lên) (Hình 7)
- Type B: do đường phụ ở bên phải, dạng QS ở chuyển đạo V1-V3 (sóng delta âm hay đi xuống) (Hình 8)
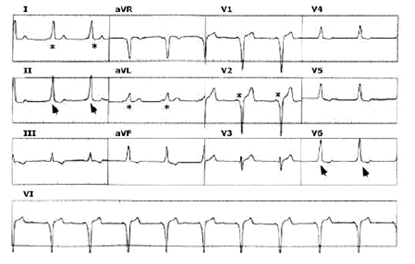
Hình 7. ECG dạng WPW type A(mũi tên chỉ sóng delta)[4]
Hình 8. ECG dạng WPW type B (*chỉ PR ngắn, mũi tên chỉ sóng delta)[4]
II.2. Các mức độ kích thích sớm
II.2.1. Các yếu tố ảnh hưởng đến kích thích sớm
Mức độ kích thích sớm tùy thuộc vào lượng cơ thất bị khử cực bằng đường phụ và biểu hiện trên ECG là PR ngắn và QRS rộng. Mức độ ngắn PR và độ rộng QRS tùy thuộc vào nhiều yếu tố[6]:
- Vị trí của đường phụ. Khoảng cách từ vị trí phát xung động trong nhĩ đến điểm nối phía nhĩ của đường phụ đóng vai trò quan trọng trong mức độ kích thích sớm. Điểm nối phía nhĩ của đường phụ càng gần nút xoang, xung động càng nhanh đến đường phụ, mức độ kích thích sớm càng lớn.
- Thời gian dẫn truyền trong nhĩ. Đây là thời gian mà xung động cần để truyền từ nút xoang đến đường phụ và nút AV. Khi đường phụ bên trái, dẫn truyền từ nút xoang đến đường phụ lớn hơn đến nút AV làm giảm mức độ kích thích sớm. Thời gian này có thể bị kéo dài do bệnh lý hay do thuốc.
- Thời gian dẫn truyền của đường phụ. Thời gian mà xung động cần để đi qua đường phụ được xác định dựa vào chiều dài đường phụ và vận tốc dẫn truyền. Thời gian này có thể bị ảnh hưởng do thuốc.
- Thời gian dẫn truyền nút AV. Nếu dẫn truyền qua nút AV càng nhanh, khử cực thất càng bình thường trước khi xung động qua đường phụ, làm giảm kích thích sớm. Thời gian này bị ảnh hưởng do các tình trạng sinh lý (thay đổi trương lực giao cảm), bệnh lý, hay do thuốc.
- Do có nhiều yếu tố ảnh hưởng đến kích thích sớm, nên cùng một đường phụ, ECG không phải luôn luôn đồng dạng.
II.2.2. Các mức độ kích thích sớm[6]:
Kích thích sớm tối đa (maximal preexitation). Hình 9-A minh họa cơ chế kích thích sớm tối đa qua đường phụ bên phải. Xung động từ nút xoang đến đường phụ nhanh hơn đến nút AV và gây khử cực thất sớm tối đa. ECG không có đoạn PR (P và sóng delta trùng lấp vào nhau) và QRS rộng, không thấy sóng delta.
Kích thích sớm với khử cực thất kết hợp (preexitation with fusion). Hình 9-B-C minh họa cơ chế khử cực thất kết hợp từ hai đường (đường phụ và đường qua nút AV). Hình 9-B, trường hợp có đường phụ bên phải và hình 9-C là trường hợp có đường phụ bên trái. ECG ghi nhận PR ngắn, QRS rộng và sóng delta.
Không có kích thích sớm (WPW syndrome with zero preexitation). Một số thuật ngữ khác có ý nghĩa tương tự như hội chứng WPW không bằng chứng (nonevident WPW syndrome) hay hội chứng WPW tiềm tàng (latent WPW syndrome). Đây là trường hợp không có biểu hiện kích thích sớm trên ECG bề mặt, nhưng kích thích sớm được chứng minh trong khảo sát điện sinh lý, thủ thuật vagal, hay khi cho thuốc ức chế kênh calcium. Block nút AV thoáng qua làm cho khử cực thất chỉ bằng đường phụ, ghi được sóng delta rõ, QRS rộng. Thường gặp là trường hợp đường phụ ở mặt bên tim trái. Ngoài ra, còn có thể gặp trong một số trường hợp đặc biệt (như thay đổi kích thích sớm do thay đổi trương lực giao cảm, kích thích sớm ngắt quãng, so le kích thích sớm, và hiệu ứng phong cầm-xem II.3). Đây là trường hợp khó chẩn đoán. Bệnh nhân có thể có triệu chứng như hồi hộp, ngất đồng thời có nguy cơ đột tử khi rung nhĩ. Trong cơn, ECG ghi được các loại rối loạn nhịp có thể xuất hiện ở WPW, nhưng ngoài cơn ECG lại bình thường. Do đó, theo khuyến cáo ngừa đột tử của hội tim mạch và trường môn Hoa Kỳ, nên khảo sát điện sinh lý cho bệnh nhân có ngất nghi ngờ do rối loạn nhịp mà các xét nghiệm không xâm lấn không kết luận được (class IIa-mức bằng chứng B)[7]. Hình 9-D minh họa cơ chế trong WPW có PR và QRS bình thường.
Hình 9. Các mức độ kích thích sớm[6].
II.3. Các trường hợp đặc biệt
Không có kích thích sớm ở WPW. Hội chứng kích thích sớm và sóng delta có thể không thấy rõ ở bệnh nhân nhịp xoang có đường phụ ở mặt bên tim trái (left-lateral) dẫn truyền xuôi chiều. Trong bệnh cảnh này, thời gian xung động từ nhĩ đến đường phụ lớn hơn đến nút AV nên đã làm hạn chế tối thiểu khử cực sớm của thất[1] (hình 10).
- Phức bộ QRS lớn hơn hay bằng 0,12 giây do có kích thích sớm thất (sóng delta), và có thể nhầm với block nhánh phải hay trái.
- Phần cuối cùng của QRS thường là bình thường do dẫn truyền bình thường qua nút AV và khử cực thất qua mạng Purkinje. Điều này ngược với trong block nhánh có sự dẫn truyền chậm xảy ra ở phần cuối hoặc toàn bộ QRS. Do đó, sự hiện diện của sóng q ở chuyển đạo V6 cho phép loại trừ WPW.
- Bất thường khử cực gây ra bất thường tái cực làm biến đổi ST-T. Trục của thay đổi ST-T thứ phát thường ngược chiều với sóng delta và phức bộ QRS.
- Có thể nhận ra kích thích sớm khi có ngoại tâm thu nhĩ. Hình 11 cho thấy PR bằng 0,12s khi nhịp xoang nhưng chỉ còn 0,09 trong ngoại tâm thu nhĩ do thời gian dẫn truyền xung động từ nút xoang đến điểm nối phía nhĩ của đường phụ lớn
hơn từ ổ ngoại vị nhĩ đến đường phụ. Khi nghi ngờ có kích thích sớm, có thể thực hiện thủ thuật vagal hay tiêm adenosin để gây block nút AV thoáng qua, lúc này sự khử cực thất chỉ bằng đường phụ, sóng delta rõ, QRS rộng[6]. - Không có kích thích sớm không có nghĩa là bệnh nhân không có các cơn rối loạn nhịp. Bệnh nhân có thể có tất cả các loại loạn nhịp trong hội chứng WPW. Trong rung nhĩ, không phải kích cỡ sóng delta mà là thời gian trơ có hiệu quả (effective refractory period) quyết định tần số đáp ứng thất[6].
Hình 10. ECG với WPW có đường phụ mặt bên tim trái. Hình A: khoảng PR và phức bộ QRS gần như bình thường trên ECG bề mặt. Hình B: ECG trong lúc kích nhịp tại xoang vành gần đường phụ, gây kích thích sớm tối đa, phức bộ QRS rộng.
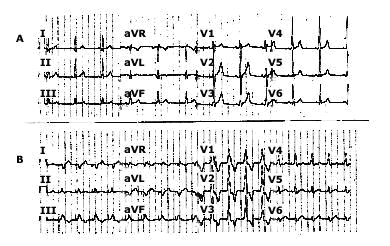
Hình 11. Lộ rõ kích thích sớm với ngoại tâm thu nhĩ[6].
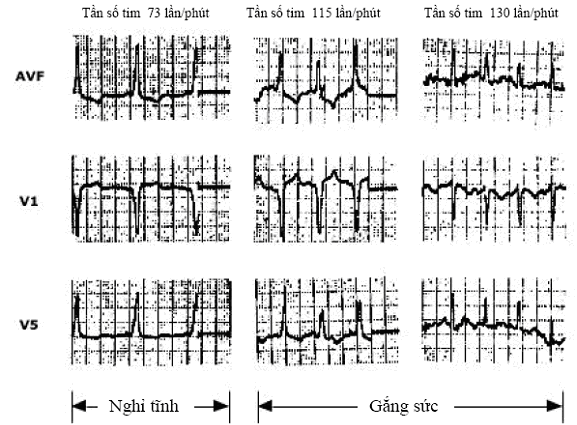
Thay đổi kích thích sớm do thay đổi trương lực giao cảm. Kích thích sớm có thể ít thấy rõ trong nhanh xoang khi dẫn truyền nút AV ngắn do tăng trương lực giao cảm và giảm trương lực đối giao cảm. Xung động sẽ qua nút AV nhanh hơn qua đường phụ và gây khử cực thất bình thường (hình 12).
Hình 12. Thay đổi kích thích sớm khi thay đổi tần số tim. Khi tim nhanh (trong gắng sức), kích thích sớm giảm tối thiểu, QRS hẹp, không thấy rõ sóng delta.
Kích thích sớm ngắt quãng (Intermittent preexcitation). Kích thích sớm ngắt quãng nên phân biệt với thay đổi kích thích sớm do thay đổi trương lực giao cảm. Trong thay đổi kích thích sớm do thay đổi trương lực giao cảm, kích thích sớm sẽ ít thấy rõ khi nhịp xoang nhanh lên và ngược lại. Trong khi đó, kích thích sớm ngắt quãng thật sự đặc trưng là khi không có thay đổi tần số tim nhưng có sự mất đột ngột sóng delta, bình thường hóa khoảng QRS, tăng khoảng PR khi đo ECG liên tục. Đây là dấu hiệu đáng tin cậy cho thấy đường phụ có thời gian trơ xuôi chiều tương đối dài và không thể dẫn truyền quá nhanh [5].
Kích thích sớm so le (preexcitation alternans). Một phức bộ QRS rộng và sóng delta xen kẽ với một phức bộ QRS bình thường. Nó cho thấy đường phụ có thời gian trơ xuôi chiều tương đối dài.
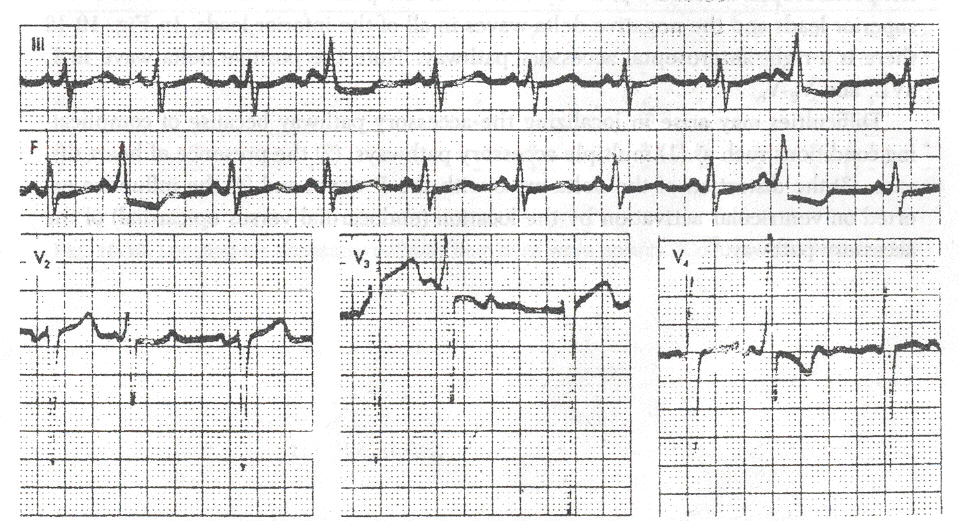
Hiệu ứng phong cầm (concertina effect). Một tình trạng khác có thể do đường phụ có thời gian trơ tương đối dài là dạng “concertina”. Đây là hiện tượng thay đổi khoảng PR và độ rộng QRS có tính chu kỳ, kích thích sớm dần dần lộ rõ trong một số nhát bóp và sau đó có sự giảm dần kích thích sớm ở các nhát bóp tiếp theo mặc dù tần số tim tương đối hằng định[5] (hình 13, 14).
Hình 13. Hiệu ứng concertina trong WPW. Trên cùng một đạo trình cho thấy khoảng PR ngắn dần và QRS rộng dần do lẫn sóng delta vào QRS. Sóng P gần như trộn lẫn vào QRS (mũi tên). Hai phức bộ QRS cuối cùng có sự trở lại khoảng PR gần như bình thường và QRS hẹp[5]
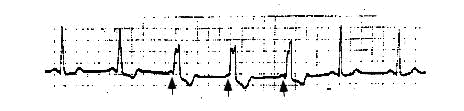
Hình 14. Hiệu ứng concertina trong WPW. Trên đạo trình DII ghi liên tục, sau phức bộ thứ năm có khoảng ngừng xoang, sau đó, khoảng PR dài hơn và kế tiếp khoảng PR dần dần ngắn lại gọi là hiệu ứng concertina[5].
Đường phụ với đặc tính dẫn truyền giảm (decremental conduction). Xấp xỉ khoảng 10% bệnh nhân có đặc tính này, khả năng dẫn truyền chậm khi tần số kích thích cao, tương tự như nút AV. Nó có giá trị bảo vệ làm giới hạn tần số thất trong rung nhĩ hay cuồng nhĩ. Tuy nhiên, đặc tính này có thể chỉ theo một hướng: xuôi chiều hay ngược chiều.
Dẫn truyền ẩn (concealed accessory pathway). Đa số đường phụ có thể dẫn truyền theo cả hai hướng, nhưng một số đường phụ chỉ dẫn truyền được một chiều. Đường phụ chỉ dẫn truyền xuôi chiều ít gặp, thường băng qua rãnh nhĩ thất bên phải, và thường có đặc tính dẫn truyền giảm. Đường phụ chỉ dẫn truyền ngược chiều thường gặp hơn với tần suất khoảng 16%. Do không gây kích thích sớm thất nên ECG khi nhịp xoang cho thấy hình ảnh PR và QRS bình thường và được gọi là “dẫn truyền ẩn”. Hầu hết đường phụ ẩn không có đặc tính dẫn truyền giảm và vì vậy dễ gây dẫn truyền ngược từ thất đến nhĩ và tạo ra nhịp nhanh vòng vào lại nhĩ thất (orthodromic atrioventricular reentrant tachycardia). Tuy nhiên, do đường phụ chỉ dẫn truyền ngược từ thất lên nhĩ nên tim sẽ được bảo vệ trong rung nhĩ[6].
II.4. Chẩn đoán phân biệt
ECG dạng WPW có thể bị chẩn đoán nhầm là nhồi máu cơ tim, block nội thất, hay dầy thất. Sóng delta âm có thể nhầm với sóng Q bất thường của nhồi máu, QRS rộng giống như trong block nhánh, QRS cao có thể chẩn đoán nhầm với dầy thất. Luôn chẩn đoán ECG dạng WPW với các dấu hiệu PR ngắn, sóng delta, và QRS rộng.
III. DỊCH TỄ HỌC
III.1. Tần suất WPW không triệu chứng[2]
Tần suất ECG dạng WPW khoảng 0,15%-0,25% dân số. Tần suất này tăng đến 0,55% ở những người có quan hệ huyết thống đời thứ nhất với bệnh nhân, điều này gợi ý đến yếu tố di truyền. Tần suất mới mắc mỗi năm của WPW rất thấp 0,004% trong một dân số đa chủng tộc, trong đó 50% là không triệu chứng. Tần suất cao gấp 2 lần ở nam, đạt đỉnh cao nhất trong năm đầu tiên của cuộc sống và đạt đỉnh cao thứ hai ở thanh niên trẻ tuổi (young adulthood)[8].
ECG dạng WPW có thể hiện diện ngắt
quãng, có thể biến mất vĩnh viễn theo thời gian. Trong dân số ở vùng Olmsted, 22% người có ECG dạng WPW tại thời điểm nghiên cứu nhưng lại không được ghi nhận trước đó; 40% số này không thấy biểu hiện kích thích sớm khi đo các ECG sau đó[8]. Những điều này cũng được báo cáo trong các nghiên cứu nhỏ hơn. Một nghiên cứu trên 29 bệnh nhân có ECG dạng WPW, được đánh giá điện sinh lý tối thiểu cách nhau 3 năm, trong quá trình theo dõi, 9 bệnh nhân (31%) có dẫn truyền xuôi chiều tự nhiên biến mất. Nghiên cứu ở Manitoba, Canada trên 19 người có WPW không triệu chứng, đến 40 tuổi, có 15 người (79%) ghi nhận không còn sóng delta.
Sự hiện diện ngắt quãng và/hoặc mất vĩnh viễn kích thích sớm có thể cho thấy nhóm đường phụ này có thời gian trơ cơ bản tương đối dài hơn (relatively longer baseline refractory period), mà làm cho nó nhạy cảm hơn với thoái hóa theo tuổi và những thay đổi của trương lực giao cảm so với nhóm có kích thích sớm vĩnh viễn[8].
Mặt khác, bệnh nhân với ECG dạng WPW có thể tiến triển từ không triệu chứng thành có triệu chứng. Trong nghiên cứu về 228 người có ECG dạng WPW theo dõi trong 12 năm, tần suất rối loạn nhịp mới mắc mỗi năm là 1% năm[9].
III.2. Tần suất hội chứng WPW
Tần suất hội chứng WPW thấp hơn tần suất người có ECG dạng WPW. Trong nghiên cứu ở 22 500 người khoẻ mạnh, ECG dạng WPW được thấy ở 0,25%, chỉ 1,8% trong số bệnh nhân này là có rối loạn nhịp[2].
Những loại rối loạn nhịp trong hội chứng WPW. Xấp xỉ 80% bệnh nhân rối loạn nhịp có nhịp nhanh vòng vào lại nhĩ thất, 15-30% có rung nhĩ, và 5% có cuồng nhĩ. Tần suất đột tử thay đổi từ 0-0,39% mỗi năm trong nhiều nghiên cứu[9,10]. Hầu hết cho thấy không có đột tử ở bệnh nhân không triệu chứng[11].
Rối loạn nhịp có liên quan đến tuổi có biểu hiện kích thích sớm trên ECG. Nghiên cứu ở dân số vùng Olmsted cho thấy trong số những người không triệu chứng, có đến một phần ba người dưới 40 tuổi cuối cùng cũng xuất hiện triệu chứng, so với không cá nhân nào trong số người lớn hơn 40 tuổi[8]. Kết quả tương tự trên 162 người WPW không triệu chứng, trong thời gian theo dõi, những người có tiến triển thành rối loạn nhịp có tuổi trung bình nhỏ hơn so với những người không có rối loạn nhịp (20 so với 37 tuổi)[10].
Câu hỏi đặt ra và hiện vẫn chưa có lời giải là liệu sự tiến triển thành rối loạn nhịp ở người khởi đầu không triệu chứng có liên quan đến sự khởi phát rối loạn nhịp trong khảo sát điện sinh lý, những đặc tính dẫn truyền xuôi chiều của đường phụ, hay tình trạng kích thích sớm ngắt quãng không[10].
Hội chứng WPW cũng có thể biến mất theo thời gian. Một báo cáo thực hiện trên 113 bệnh nhân hội chứng WPW có cơn nhịp nhanh vào lại nút nhĩ thất trong 9 năm: 23% bệnh nhân mất dẫn truyền xuôi chiều và kích thích sớm; 8% mất dẫn truyền ngược chiều trong đường phụ[2].
III.3. WPW gia đình
3,4 % những bệnh nhân có hội chứng WPW có thân nhân đời thứ nhất có hội chứng kích thích sớm[2]. Khảo sát bản đồ gen trên 3 gia đình có nhiều người bị hội chứng WPW cho thấy gen gây ra WPW nằm tại vị trí 7q34-q36 trên nhiễm sắc thể, đây là đột biến theo tính trội ở nhiễm sắc thể thường. Đột biến xảy ra trên gen PRKAG2 có chức năng mã hóa tiểu đơn vị điều hòa gamma-2 của men protein kinase[12,13].
Dạng di truyền WPW có liên quan đến bệnh cơ tim phì đại gia đình có thể do những đột biến trên gen PRKAG2 hay trên gen LAMP2 (bệnh Danon)[2].
IV. THÁI ĐỘ XỬ TRÍ
Theo hướng dẫn của hội tim mạch và trường môn tim mạch Hoa Kỳ, hội tim mạch châu Âu (ESC) năm 2003, bệnh nhân với ECG dạng WPW đơn thuần thì không cần đánh giá hay điều trị thêm; tuy nhiên, hướng dẫn cũng gợi ý rằng cắt đốt có thể thực hiện ở những bệnh nhân này. Khuyến cáo mềm dẻo này dựa vào cân nhắc giữa nguy cơ xuất hiện các rối loạn nhịp nguy hiểm nếu không điều trị so với các biến chứng nghiêm trọng khi cắt đốt.
IV.1. Phân tầng nguy cơ
Nhiều tác giả cho rằng với bệnh nhân có ECG dạng WPW, nên phân tầng nguy cơ đột tử bằng các xét nghiệm không xâm lấn và/hoặc thăm dò điện sinh lý để chọn lựa phương pháp điều trị tối ưu. Tuy nhiên, hướng dẫn 2003 của hội tim mạch và trường môn Hoa Kỳ chưa đưa ra bảng phân tầng nguy cơ.
Cơ chế đột tử ở bệnh nhân có WPW là rung thất. Rung thất thường xảy ra trong các cơn rung nhĩ do các xung động của nhĩ sẽ truyền nhanh xuống thất qua đường phụ. Nhận định nguy cơ đột tử cao cho phép có cơ sở để tiến hành các điều trị phức tạp hơn.
Vẫn còn chưa đạt được đồng thuận trong nhận định các yếu tố tiên đoán sự tiến triển của triệu chứng và/hoặc đột tử. Một vài yếu tố sau gợi ý khả năng xuất hiện triệu chứng:
- Tuổi trẻ hơn
- Giới nam
- Xuất hiện nhịp nhanh vào lại nhĩ thất hay rung nhĩ trong khảo sát điện sinh lý
- Nhiều đường phụ
- Thời gian trơ của đường phụ ngắn.
Một vài đường phụ có đặc tính dẫn truyền giảm, giống như đặc tính của nút AV, có nghĩa là vận tốc dẫn truyền chậm hơn khi tần số tim cao hơn. Khi đó, tần số thất trong rung nhĩ có thể bị giới hạn do vận tốc dẫn truyền giảm khi tim nhanh.
Tuy nhiên, hầu hết đường phụ là dẫn truyền nhanh, giống như đặc tính của mạng lưới Purkinje. Khi đó, tần số thất trong rung nhĩ bị giới hạn do thời gian trơ của đường phụ chứ không phải do vận tốc dẫn truyền đường phụ. Bệnh nhân có dẫn truyền nhanh nhưng có thời gian trơ dài sẽ có nguy cơ bị đột tử thấp, và ngược lại nguy cơ đột tử cao ở bệnh nhân có thời gian trơ ngắn.
IV.2. Đánh giá không xâm lấn
Mặc dù thời gian trơ chính xác của đường phụ thường đo được trong thăm dò điện sinh lý, nhưng vẫn có thể biết được các đường phụ có thời gian trơ dài bằng các xét nghiệm không xâm nhập. Loại đường phụ có thời gian trơ dài này có thể biểu hiện bằng tình trạng kích thích sớm ngắt quãng. Như phần IV.1 đã đề cập, loại này khó có thể dẫn truyền nhanh trong rung nhĩ, khả năng ít gây rung thất, và có nguy cơ đột tử thấp. Kích thích sớm ngắt quãng có thể gặp trong các trường hợp sau:
- ECG khi nghỉ (gặp trong các dạng: kích thích sớm ngắt quãng, kích thích sớm so le, hiệu ứng phong cầm)
- ECG khi gắng sức (đây là dạng thay đổi kích thích sớm do thay đổi trương lực giao cảm)
< li> Sau test thuốc (sau khi cho thuốc ức chế kênh natri bằng đường tĩnh mạch như procainamide): những BN sau dùng thuốc có thời gian trơ của đường phụ dài sẽ có tiên lượng tốt hơn (biểu hiện bằng mất sóng delta trên ECG hoặc giảm tần số thất trong rung nhĩ…)
Do đó, có thể cho bệnh nhân có ECG dạng WPW thực hiện test gắng sức hay test thuốc (procainamide) để đánh giá nguy cơ đột tử. Những bệnh nhân không có yếu tố nguy cơ thấp này, đặc biệt dưới 35-40 tuổi, có thể xem xét thăm dò điện sinh lý tiếp theo để phân tầng nguy cơ và điều trị.
Tuy nhiên, giá trị tiên đoán của các test không xâm lấn vẫn chưa được nghiên cứu đầy đủ. Vì vậy, đánh giá này có thể chỉ loại trừ được một thiểu số bệnh nhân. Tất cả các bệnh nhân khác nên xem xét thực hiện test xâm nhập. Vẫn chưa có bằng chứng lợi ích rõ rệt khi chọn test không xâm lấn là test sàng lọc để phân tầng nguy cơ.
IV.3. Đánh giá bằng test xâm lấn
Đối với người có nguy cơ cao tiến triển triệu chứng, phân tầng nguy cơ bằng thăm dò điện sinh lý và điều trị cho những bệnh nhân này bằng cắt đốt được đánh giá là hữu ích. Tuy nhiên, những rối loạn nhịp đe dọa tính mạng thì hiếm nhưng những biến chứng nghiêm trọng xảy ra đến 2 % người làm test này. Vì vậy, vẫn còn chưa rõ liệu thăm dò điện sinh lý có làm giảm thực sự tần suất bệnh và tử vong không.
V. KẾT LUẬN
WPW không triệu chứng luôn là vấn đề quan tâm của các bác sỹ lâm sàng đặc biệt đối với bác sỹ tim mạch. Nhìn chung, bệnh nhân có nguy cơ đột tử rất thấp. Tuy nhiên, đối với nhóm người trẻ tuổi có nhiều khả năng chuyển thành có triệu chứng, và khi đó sẽ làm thay đổi tiên lượng. Một điều hạn chế là còn ít các nghiên cứu về phân tầng nguy cơ ở bệnh nhân WPW không triệu chứng, do đó vẫn chưa có một hướng dẫn đầy đủ về nhóm bệnh này. Có thể xem xét các test không xâm lấn để bước đầu phân tầng nguy cơ và để chọn lựa các đối tượng cần làm thêm khảo sát điện sinh lý; nhưng đồng thời vai trò của điện sinh lý cũng cần được xác định thêm.
Tài liệu tham khảo
1. Arnsdorf MF, Podrid PJ (2007),”Electrocardiographic features of the Wolff-Parkinson-White pattern”, UpToDate (15.3).
2. Arnsdorf MF, Podrid PJ (2007 ),”Epidemiology of the Wolff-Parkinson-White syndrome”, UpToDate (15.3).
3. Attenhofer Jost CH, Connolly HM, O’Leary PW (2005),”Left heart lesions in patients with Ebstein anomaly”, Mayo Clin Proc (80), pp. 361.
4. Philip J Podrid MD (2007),”ECG tutorial: Preexcitation syndromes”, UpToDate (15.3).
5. Knight BP, Arnsdorf MF (2007),”Anatomy, pathophysiology and localization of accessory pathways in the preexcitation syndrome”, UpToDate (15.3).
6. Marriot HJL, Conover MB,” Preexcitation and its arrhythmias”, in Advanced concepts in arrhythmias, Mosby (1989), pp. 141-173
7. Zipes DP, Camm AJ, Borggrefe M (2006),” ACC/AHA/ESC 2006 Guidelines for Management of Patients With Ventricular Arrhythmias and the Prevention of Sudden Cardiac Death-Executive Summary A Report of the American College of Cardiology/American Heart Association Task Force and the European Society of Cardiology Committee for Practice Guidelines (Writing Committee to Develop Guidelines for Management of Patients With Ventricular Arrhythmias and the Prevention of Sudden Cardiac Death)”, J Am Coll Cardiol (48), pp. 1064.
8. Munger TM, Packer DL, Hammill SC (1993),”A population study of the natural history of Wolff-Parkinson-White syndrome in Olmsted County, Minnesota, 1953 to 1989″, Circulation (87), pp. 866.
9. Fitzsimmons PJ, McWhirter PD, Peterson DW, and Kruyer WB ( 2001),”The natural history of Wolff-Parkinson-White syndrome in 228 military aviators: A long-term follow-up of 22 years “, Am Heart J (142), pp. 530.
10. Pappone C, Santinelli V, Rosanio S (2003),”Usefulness of invasive electrophysiologic testing to stratify the risk of arrhythmic events in asymptomatic patients with Wolff-Parkinson-White pattern. Results from a large prospective long-term follow-up study”, J Am Coll Cardiol (41), pp. 239.
11. Todd DM, Klein GJ, Krahn AD (2003),”Asymptomatic Wolff-Parkinson-White syndrome: is it time to revisit guidelines?” J Am Coll Cardiol (41), pp. 245.
12. Gollob MH, Green MS, Tang AS (2001),”Identification of a gene responsible for familial Wolff-Parkinson-White syndrome”, N Engl J Med (344), pp. 1823.
13. Gollob MH, Seger JJ, Gollob TN (2001),”Novel PRKAG2 mutation responsible for the genetic syndrome of ventricular preexcitation and conduction system disease with childhood onset and absence of cardiac hypertrophy”, Circulation (104), pp. 3030.