(Lược dịch và tham khảo từ bài báo của tác giả Vincenzo Acerbo1)
ThS.BS. LÊ THỊ LAN HƯƠNG, PGS.TS.BS. PHẠM NGUYỄN VINH
Bệnh viện đa khoa Tâm Anh TP. Hồ Chí Minh
Tóm tắt
Bệnh động mạch vành (CAD) là nguyên nhân phổ biến nhất gây suy tim phân suất tống máu giảm (HFrEF). Ngày nay, những tiến bộ y học đóng vai trò quan trọng trong việc cải thiện tiên lượng cho bệnh nhân CAD và HfrEF. Tuy nhiên, tỷ lệ tử vong ở nhóm bệnh này vẫn cao và vai trò của chiến lược tái thông mạch vành bằng phẫu thuật bắc cầu hoặc/hoặc can thiệp qua da vẫn còn đang tranh luận. Các thử nghiệm lâm sàng về tái thông mạch vành ở bệnh nhân suy tim phân suất tống máu giảm như thử nghiệm STICH và REVIVED đã cố gắng đưa ra câu trả lời cho vấn đề này. Mặc dù vậy, kết quả của hai thử nghiệm này không cung cấp câu trả lời chắc chắn về đối tượng bệnh nhân nào được hưởng lợi từ tái thông mạch vành, đồng thời bác bỏ quan điểm mang tính lịch sử về tính sống – còn cơ tim và giả thuyết về cơ tim ngủ đông (hibernation). Do đó, thực tế lâm sàng đặt ra câu hỏi mới về cách lựa chọn bệnh nhân thích hợp cho chiến lược tái thông mạch vành. Và mục tiêu của bài viết nhằm cung cấp cái nhìn tổng quan và bằng chứng hiện có của tái thông động mạch vành ở bệnh nhân CAD kèm suy giảm chức năng thất trái, đồng thời đề xuất những góc nhìn mới về cách lựa chọn và quản lý bệnh nhân thuộc nhóm nguy cơ cao này.
1. Giới thiệu
Bệnh động mạch vành (CAD) là nguyên nhân phổ biến nhất gây suy tim phân suất tống máu giảm (HFrEF) và là nguyên nhân hàng đầu gây tử vong trên toàn thế giới2,3. Quản lý điều trị đối tượng bệnh nhân này vẫn còn là một thách thức và nhiều tranh cãi trong thời đại hiện nay3-6. Những tiến bộ trong các liệu pháp y tế bao gồm: thuốc mới và thiết bị cấy ghép, đã cải thiện đáng kể kết cục lâm sàng ở bệnh nhân bệnh cơ tim thiếu máu cục bộ. Tuy nhiên, ngoài liệu pháp nội khoa tối ưu, vẫn có những tranh luận về tác động của chiến lược tái thông động mạch vành trong bối cảnh lâm sàng này. Các thử nghiệm như STICH7 và REVIVED8 đã nghiên cứu vai trò của tái thông động mạch vành thông qua phẫu thuật bắc cầu động mạch vành (CABG) hoặc can thiệp qua da (PCI) ở những bệnh nhân suy giảm chức năng thất trái do thiếu máu cục bộ cơ tim. Kết quả của những thử nghiệm này đặt ra những câu hỏi về giá trị của tính sống – còn cơ tim và giả thuyết cơ tim ngủ đông, tạo ra sự không chắc chắn về việc chọn bệnh nhân lý tưởng cho tái thông động mạch vành như quan điểm trước đây. Trong bài viết, chúng tôi sẽ thảo luận về vai trò của tái thông động mạch vành trong bệnh cơ tim thiếu máu cục bộ và đưa ra các gợi ý thực tiễn về cách lựa chọn và quản lý bệnh nhân trong thực hành lâm sàng.
2. Lý thuyết về hibernation cơ tim
Thuật ngữ “cơ tim ngủ đông” lần đầu tiên được đề xuất bởi Tiến sĩ George Diamond năm 19789 và sau đó được phổ biến bởi Tiến sĩ Shahbudin Rahimtoola vào năm 198510. Ban đầu, khái niệm “cơ tim ngủ đông” định nghĩa vùng cơ tim được cung cấp máu bởi nhánh mạch vành bị hẹp chỉ đủ để duy trì sự sống, nhưng không đủ để duy trì khả năng co bóp bình thường. Trong điều kiện lưu lượng máu thấp (giảm cung cấp oxy), cơ tim đáp ứng bằng cách giảm chức năng, giảm trao đổi chất để thích nghi (giảm nhu cầu oxy), mục đích giảm thiểu thiếu máu cục bộ và ngăn ngừa hoại tử cơ tim.
Tác giả Rahimtoola11 báo cáo trường hợp điển hình của cơ tim ngủ đông ở bệnh nhân chụp mạch vành ghi nhận tắc LAD, suy tim phân suất tống máu giảm LVEF 37% kèmvô động thành trước và mỏm thất trái. Tuy nhiên, sau khi sử dụng nitroglycerin, EF cải thiện lên 51% và cải thiện vận động vùng thành trước – mỏm thất trái. Điều này cho thấy hồi phục chức năng co bóp những ở vùng vô động trước khi dùng nitroglycerin, chứng tỏ rằng vùng cơ tim này còn sống. Bệnh nhân này được phẫu thuật bắc cầu mạch vành đến nhánh LAD. Tám tháng sau phẫu thuật, chức năng co bóp thất trái EF đạt 76% và vùng thành trước – mỏm thất trái vận động bình thường. Vì vậy, một vùng cơ tim ban đầu vô động, nhưng hồi phục sau khởi kích bằng nitroglycerin và được xem là “ngủ đông”, cuối cùng đã phục hồi hoàn toàn sau khi được tái thông mạch vành.
Các giả thuyết về đánh giá sống – còn cơ tim có giá trị quan trọng ở bệnh nhân mắc bệnh cơ tim thiếu máu cục bộ. Dựa trên các mô hình thực nghiệm của hiện tượng “cơ tim ngủ đông” giúp xác định những bệnh nhân có cơ tim còn sống—những người có khả năng cao hơn sẽ hưởng lợi từ tái thông động mạch vành. Hiện tượng ngủ đông cơ tim là một quá trình động, được đặc trưng bởi rối loạn chức năng co bóp có thể phục hồi do tình trạng thiếu máu cục bộ kéo dài và lặp đi lặp lại. Tình trạng này làm giảm chức năng cơ tim, mục đích giúp duy trì sự sống còn của tế bào cơ tim12. Hiện tượng này liên quan đến các giai đoạn khác nhau của tình trạng rối loạn chức năng cơ tim do thiếu máu cục bộ, từ hiện tượng cơ tim choáng váng (tức là rối loạn chức năng co bóp trong vài giờ hoặc vài ngày sau một giai đoạn thiếu máu ngắn) đến hiện tượng ngủ đông cơ tim (tức là suy giảm khả năng co bóp kéo dài do các đợt thiếu máu cục bộ tái phát, có thể được khôi phục một phần hoặc hoàn toàn nếu cung cấp đủ cung cầu oxy của cơ tim) đến quá trình hình thành sẹo (cơ tim ngủ đông ở giai đoạn tiến triển bị xơ hóa)13
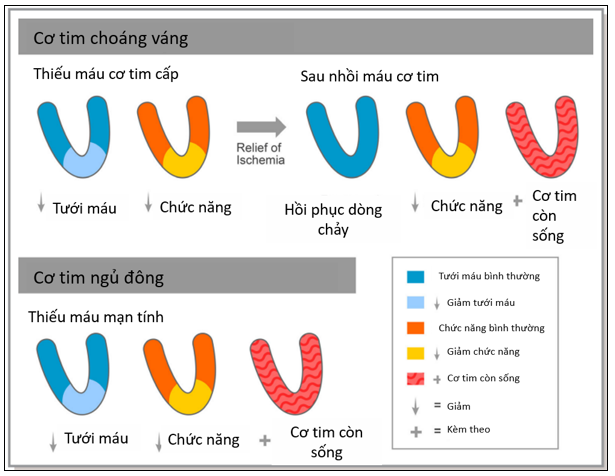
Hình 1: Mô tả về cơ tim choáng váng và cơ tim ngủ đông14
3. Bằng chứng thực nghiệm
Từ giả thuyết về cơ tim ngủ đông, từ những năm 2000 đến nay, nhiều phân tích gộp, và các thử nghiệm lâm sàng được thực hiện, với mục đích nhằm trả lời câu hỏi: liệu rằng sống – còn cơ tim có giúp phân loại bệnh động mạch vành kèm suy tim phân suất tống máu giảm được hưởng lợi từ tái tưới máu mạch vành. Ở đây, chúng tôi xin phép phân tích các phân tích tổng hợp và thử nghiệm lớn STICH, ISCHEMIA và REVIVED
3.1 Phân tích tổng hợp của Kevin C. Allman15
Năm 2002, tác giả Kevin C. Allman15 đưa ra phân tích tổng hợp dựa trên 24 nghiên cứu nhằm đánh giá sống – còn cơ tim và vai trò của tái thông mạch vành trên bênh nhân bệnh mạch vành mạn kèm suy tim phân suất tống máu giảm. Phân tích tổng hợp gồm 3088 bệnh nhân với phân suất tống máu trung bình 32 ± 8%, theo dõi trung bình trong 25 ± 10 tháng. Phương thức đánh giá sống còn cơ tim chủ yếu là siêu âm tim Dobutamine và chụp SPECT. Kết quả nghiên cứu cho thấy vai trò của đánh giá sống – còn cơ tim qua các phương thức hình ảnh không xâm lấn, và đối với cơ tim còn sống cho thấy tái thông mạch vành giúp cải thiện tiên lượng sống còn ở những bệnh nhân bệnh động mạch vành mạn kèm suy giảm chức năng thất trái. Đối với cơ tim hoại tử (không còn sống) không ghi nhận sự khác biệt trong chiến lược điều trị tái thông hay điều trị nội khoa.
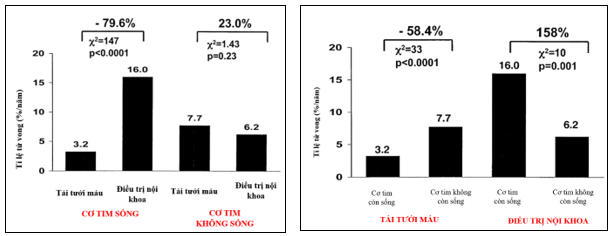
Hình 2: Lợi ích tái tưới máu ở nhóm cơ tim còn sống qua phân tích tổng hợp15
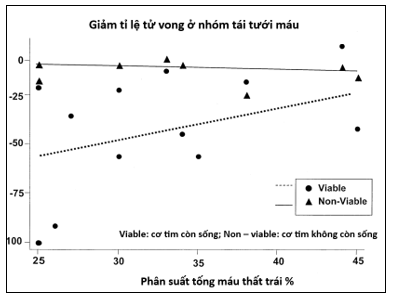
Hình 3: Dự đoán giảm tỉ lệ tử vong ở nhóm cơ tim còn sống15
Phân tích hồi qui để tiên đoán mối liên quan giữa phân suất tống máu thất trái (EF) và tỷ lệ tử vong ở bệnh nhân có cơ tim còn sống (hình tròn) so với cơ tim không còn sống (hình tam giác). Đối với bệnh nhân CAD kèm suy tim phân suất tống máu thất trái thấp, nhóm cơ tim còn sống có khả năng cải thiện tỷ lệ sống – còn (đường nét đứt) so với nhóm cơ tim không còn sống (đường nét liền)với p < 0,0001.
3.2 Thử nghiệm STICH7
Thử nghiệm STICH là thử nghiệm lâm sàng ngẫu nhiên có nhóm chứng, thực hiện từ năm 2002 đến 2007. Đối tượng nghiên cứu 1.212 bệnh nhân bệnh động mạch vành có phân suất tống máu thất trái giảm (LVEF ≤ 35%) và có thể thực hiện CABG. Giả thuyết nghiên cứu liệu CABG kết hợp với điều trị nội khoa tối ưu (OMT) có thể cải thiện tiên lượng sống còn tốt hơn so với OMT đơn thuần không? Các bệnh nhân được phân ngẫu nhiên thành 2 nhóm CABG + OMT (nhóm CABG gồm 610 bệnh nhân) hoặc chỉ OMT đơn thuần (nhóm OMT gồm 602 bệnh nhân). Nhóm bệnh nhân không tham gia thử nghiệm STICH gồm: hẹp thân chung ≥ 50% hoặc đau thắt ngực CCS III hoặc IV theo phân loại của Hiệp hội Tim mạch Canada. Thời gian nghiên cứu theo dõi trung bình là 56 tháng. Kết quả nghiên cứu ghi nhận không có sự khác biệt về tiêu chí chính là tỷ lệ tử vong do mọi nguyên nhân giữa nhóm CABG + OMT (36%) và nhóm OMT đơn thuần (41%)7. Tuy nhiên nhóm CABG + OMT có xu hướng cải thiện triệu chứng lâm sàng tốt hơn so với chỉ OMT đơn thuần (HR= 0.86, KTC 95% = 0.72–1.04, p= 0.12), và nhóm CABG có tỷ lệ tử vong do nguyên nhân tim mạch thấp hơn nhóm OMT (28% so với 33%; HR = 0.81; KTC 95% = 0.66 – 1.00; p = 0.05) và tỷ lệ nhập viện do nguyên nhân tim mạch cũng thấp hơn (58% so với 68%; HR = 0.74, KTC 95% = 0.64–0.85, p < 0.001)16.
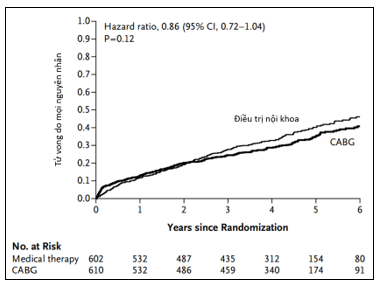
Hình 4: Không có khác biệt về tiêu chí chính giữa nhóm CABG + OMT so với OMT đơn thuần trong nghiên cứu STICH7
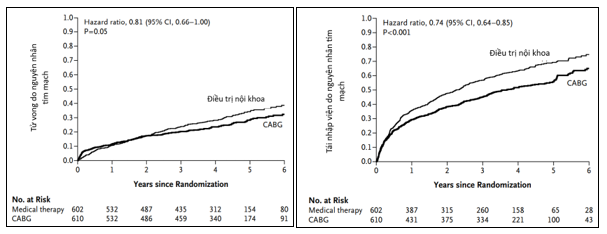
Hình 5: Khác biệt về tỉ lệ tử vong do nguyên nhân tim mạch và tái nhập viện do nguyên nhân tim mạch giữa nhóm CABG + OMT so với OMT đơn thuần16
3.3 Thử nghiệm STICHES (nghiên cứu STICH mở rộng)17
Thử nghiệm STICHES17 là phần mở rộng của thử nghiệm STICH với thời gian theo dõi được kéo dài thêm 5 năm. Trong thời gian theo dõi gần 10 năm (trung bình 9.8 năm) cho thấy tiêu chí chính là tỷ lệ tử vong do mọi nguyên nhân thấp hơn đáng kể ở nhóm CABG so với nhóm OMT (HR = 0.84, KTC 95% = 0.73–0.97, p = 0.02)17. Tương tự như STICH, các phân tích kết quả phụ cho thấy lợi ích nhất quán từ CABG: tử vong do nguyên nhân tim mạch xảy ra ở 246 bệnh nhân (40.5%) ở nhóm CABG và 297 bệnh nhân (49.3%) ở nhóm OMT (HR = 0.79, KTC 95% = 0.66–0.93, p = 0.006), và tử vong do bất kỳ nguyên nhân nào hoặc nhập viện vì nguyên nhân tim mạch xảy ra ở 467 bệnh nhân (76,6%) trong nhóm CABG và 524 bệnh nhân (87,0%) trong nhóm OMT (HR = 0,72, 95% CI = 0,64–0,82, P < 0,001).
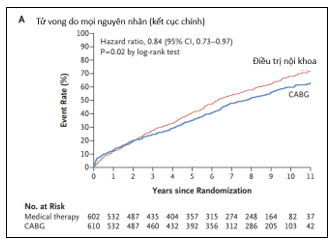
Hình 6: Nhóm CABG + OMT làm giảm 16% tỉ lệ tử vong chung so với nhóm điều trị nội khoa đơn thuần17
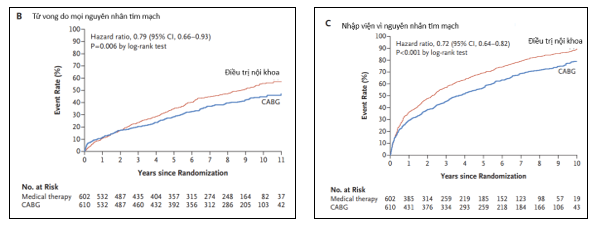
Hình 7: Nhóm CABG + OMT làm giảm 21% tỉ lệ tử vong tim mạch và giảm 28% tỉ lệ tái nhập viện vì nguyên nhân tim mạch so với OMT đơn thuần17
3.4 Phân tích về thử nghiệm STICH:
- Tác động của tuổi đến tiên lượng dài hạn sau CABG
Thử nghiệm STICHES cho thấy, kết hợp CABG với OMT đã kéo dài thời gian sống trung bình thêm 1,5 năm với giảm 16% nguy cơ tương đối và giảm 8% nguy cơ tuyệt đối về tỷ lệ tử vong do mọi nguyên nhân17. Tuy nhiên, các tác giả cho rằng lợi ích của CABG lên kết quả lâm sàng có thể bị ảnh hưởng bởi tuổi tác tại thời điểm phẫu thuật. Ở nhóm bệnh nhân độ tuổi trẻ hơn, CABG mang lại lợi ích lớn hơn so với bệnh nhân lớn tuổi, những người có nguy cơ cao hơn về các biến chứng sau phẫu thuật và tử vong không do nguyên nhân tim mạch.
Trong một phân tích dưới nhóm sau thử nghiệm STICHES, Petrie và cs18 đã chia nhóm theo các phần tư dựa trên độ tuổi (Q1 ≤ 54 tuổi, Q2 từ 54 đến ≤ 60 tuổi, Q3 từ 60 đến ≤ 67 tuổi, và Q4 > 67 tuổi) nhằm trả lời câu hỏi: liệu tất cả bệnh nhân có nhận được cùng lợi ích từ CABG bất kể tuổi tác hay không? Kết quả phân tích cho thấy CABG kết hợp với OMT làm giảm đáng kể tỷ lệ tử vong do nguyên nhân tim mạch trên tất cả các nhóm tuổi, cho thấy bệnh nhân trẻ tuổi nhận được lợi ích lớn hơn so với bệnh nhân lớn tuổi. Ngoài ra, kết quả nghiên cứu không chỉ ra lợi ích về giảm tỷ lệ tử vong do mọi nguyên nhân ở nhóm bệnh nhân trên 67 tuổi (HR = 0,82, 95% CI = 0,63–1,06). Các tác giả cho rằng nhận định này do nhiều yếu tố, gồm: tỷ lệ tử vong ở bệnh nhân lớn tuổi thường khả năng do các nguyên nhân ngoài tim mạch. Thực tế, tỷ lệ tử vong liên quan đến tim mạch chiếm tỷ lệ nhỏ hơn (62%) trong nhóm bệnh nhân lớn tuổi nhất, so với 79% ở nhóm bệnh nhân trẻ tuổi nhất18. Ở những bệnh nhân cao tuổi, CABG có thể không làm giảm (và thậm chí có thể làm tăng) tỷ lệ tử vong không do nguyên nhân tim mạch bởi vì gánh nặng bệnh lý đồng mắc. Do đó, làm tăng nguy cơ biến chứng sau phẫu thuật và tử vong không do tim mạch18.
Phân tích này giúp đưa ra cách tiếp cận chọn lọc (dựa trên độ tuổi) có thể có lợi, vì hầu hết các lợi ích liên quan đến CABG được quan sát thấy ở những bệnh nhân dưới 60 tuổi với bệnh ba nhánh mạch vành kèm suy giảm chức năng thất trái19. Điều này cũng cho thấy điểm hạn chế thử nghiệm STICH là độ tuổi của các bệnh nhân tham gia (tuổi trung bình: 60 tuổi), trái ngược với thực hành lâm sàng hiện nay, trong đó tuổi của bệnh nhân bệnh mạch vành mạn kèm suy tim thường trên 75 tuổi20. Do đó, vẫn chưa rõ liệu tỷ lệ rủi ro–lợi ích của CABG có thuận lợi ở những bệnh nhân trên 60 tuổi hay không, vì nhóm này không đại diện đầy đủ trong thử nghiệm STICH.
- Đánh giá lợi ích của hồi phục chức năng thất trái?
Qua thử nghiệm STICH, việc đánh giá khả năng sống – còn cơ tim để lựa chọn chiến lược CABG7, cho thấy hồi phục chức năng thất trái không phải là cơ chế quan trọng nhất để cải thiện kết cục lâm sàng. Việc ngăn ngừa tổn thương cơ tim, bảo vệ phần cơ tim còn sống tránh khỏi các biến cố vành cấp trong tương lai, và ngăn ngừa các trường hợp đột tử do loạn nhịp thất, có lẽ góp phần đáng kể vào việc cải thiện kết quả lâm sàng7. Việc tái thông động mạch vành đảm bảo sự ổn định chức năng và điện học của các tế bào cơ tim, và độc lập với cải thiện chức năng tâm thu thất trái. Nghiên cứu cho thấy, đảm bảo lưu lượng máu vào vùng cơ tim ngủ đông ở đoạn xa của vị trí tắc mãn tính để ngăn ngừa các biến cố cấp tính và loạn nhịp là lợi ích chính của tái thông động mạch vành ở bệnh nhân mắc bệnh cơ tim thiếu máu cục bộ21.
- Đánh giá thiếu máu cục bộ cơ tim
Do thiếu dữ liệu về tác động của tình trạng thiếu máu cục bộ cơ tim ở bệnh nhân mắc bệnh động mạch vành (CAD) kèm giảm chức năng thất trái, Panza và cs22 tiến hành phân tích dưới nhóm của thử nghiệm STICH. Giả thuyết nghiên cứu là đánh giá thiếu máu cục bộ cơ tim có thể xác định những bệnh nhân hưởng lợi ích từ CABG + OMT so với OMT đơn thuần. Phân tích này gồm 399 bệnh nhân được đánh giá tình trạng thiếu máu cục bộ cơ tim bằng cách sử dụng SPECT hoặc siêu âm tim gắng sức bằng Dobutamine (DSE). Thiếu máu cục bộ được phân tích theo cả hai cách: nhị giá và biến liên tục. Trắc nghiệm gắng sức đã xác định 256 bệnh nhân (64% dân số nghiên cứu) có thiếu máu cục bộ cơ tim và 143 bệnh nhân (36% dân số nghiên cứu) không có biểu hiện thiếu máu cục bộ. Ngược lại, khi thiếu máu cục bộ được phân tích dưới dạng biến liên tục, tỷ lệ cơ tim bị thiếu máu trung bình là 12,2 ± 11,5% trong nghiên cứu STICH, trong đó 199 bệnh nhân cho thấy có bất thường tưới máu từ mức độ vừa đến nặng (tức là > 10% thể tích cơ thất trái)22. Tuy nhiên, phân tích dưới nhóm về tính sống – còn cơ tim, không tìm ra mối liên quan giữa thiếu máu cục bộ ảnh hưởng đến kết cục lâm sàng giữa nhóm CABG và điều trị OMT đơn thuần, gồm tỉ lệ tử vong chung (p = 0,28), tử vong do tim mạch (p = 0,07), hoặc nhập viện do nguyên nhân tim mạch (p = 0,79). Hơn nữa, không có sự tương tác nào được tìm thấy giữa tác động của CABG so với OMT và tình trạng có/không có thiếu máu cục bộ cơ tim đối với tỷ lệ tử vong do mọi nguyên nhân hoặc bất kỳ tiêu chí phụ nào22. Tuy nhiên, như tác giả Panza cũng phân tích, kết quả này là phân tích dưới nhóm thực hiện sau nghiên cứu STICH, và chia nhóm đánh giá tình trạng thiếu máu cục bộ không ngẫu nhiên, do đó có thể không cho thấy hiệu quả có lợi của tái tưới máu ở bệnh nhân mắc bệnh cơ tim do thiếu máu cục bộ. Tương tự các hướng dẫn của Hội tim mạch Châu Âu, phân tích dưới nhóm cho thấy lựa chọn chiến lược CABG ở bệnh nhân bệnh cơ tim thiếu máu cục bộ nên được dựa trên nhiều tiêu chí lâm sàng khác ngoài việc chỉ đánh giá hiện diện của thiếu máu cục bộ cơ tim.
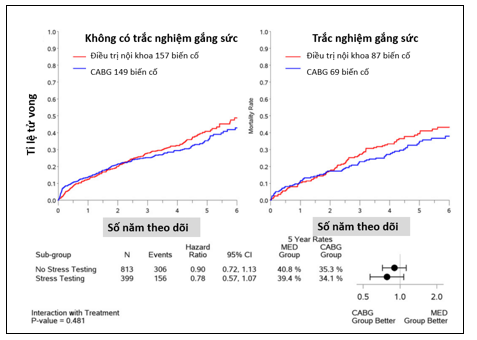
Hình 8: Không có khác biệt về tỉ lệ tử vong giữa nhóm có và không có trắc nghiệm gắng sức để đánh giá thiếu máu cục bộ cơ tim theo thử nghiệm STICH22
3.5 Nghiên cứu ISCHEMIA – tín hiệu tích cực về tái thông động mạch dựa trên thiếu máu cục bộ23
Trái ngược với phân tích dưới nhóm của nghiên cứu STICH, phân tích dưới nhóm của thử nghiệm ISCHEMIA23 gợi ý rằng chiến lược tái tưới máu dựa trên thiếu máu cục bộ có thể mang lại hiệu quả có lợi ở những bệnh nhân có tiền sử suy tim hoặc suy chức năng thất trái. Phân tích dưới nhóm cho thấy những bệnh nhân mắc bệnh tim thiếu máu cục bộ ổn định kèm suy tim có tiên lượng xấu hơn so với những bệnh nhân không suy tim, và nhóm bênh nhân CAD kèm suy tim được điều trị bằng chiến lược tái tưới máu ban đầu có kết cục lâm sàng tốt hơn so với nhóm OMT đơn thuần, trong khi không có sự khác biệt nào ở những bệnh nhân không mắc suy tim/LVD. Tuy nhiên, cần lưu ý rằng kết quả có lợi của chiến lược tái tưới máu trong thử nghiệm ISCHEMIA chỉ giới hạn trong một nhóm nhỏ 28 bệnh nhân mắc suy tim phân suất tống máu thất trái giảm từ nhẹ đến trung bình (35 đến 45%), khiến cho các kết quả này chỉ mang tính giả định24.
Ngoài ra, nghiên cứu hồi cứu của tác giả Miller và Bonow25 cũng cho thấy lợi ích tái tưới máu ở bệnh nhân CAD. Nghiên cứu gồm 54522 bệnh nhân, theo dõi trung bình trong 8 năm, đánh giá thiếu máu cơ tim bằng hình ảnh tưới máu cơ tim trên chụp cắt lớp điện toán phát xạ đơn photon (SPECT MPI), thực hiện trong vòng 10 năm từ 1992 đến 2012. Trong đó, chiến lược tái tưới máu sớm được thực hiện trên 2688 bệnh nhân PCI và 1228 bệnh nhân CABG. Kết quả nghiên cứu ghi nhận, chiến lược tái tưới máu bao gồm cả PCI và CABG đều làm giảm tỷ lệ tử vong do mọi nguyên nhân, tăng tỉ lệ sống – còn so với điều trị nội đơn thuần, đặc biệt ở nhóm bệnh nhân thiếu máu cục bộ cơ tim > 15% (đối với PCI: HR = 0.70, p = 0.002, đối với CABG p = 0.73, p = 0,008). Vì kết quả với tái tưới máu tương tự nhau đối với cả PCI và CABG, cho thấy rằng quyết định giữa PCI và CABG để tái tưới máu sớm nên được xác định bởi giải phẫu động mạch vành, đặc điểm của bệnh nhân, chứ không phải bởi gánh nặng thiếu máu cục bộ.
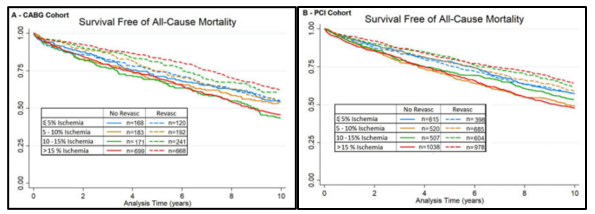
Hình 9: Cải thiện tiên lượng sống – còn sau tái tưới máu theo nghiên cứu của tác giả Miller và Bonow25
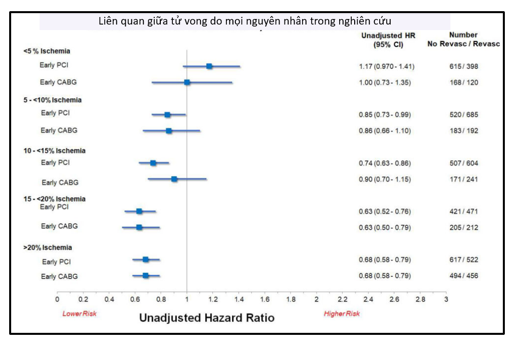
Hình 11: So sánh tỉ lệ tử vong giữa điều trị tái tưới máu bằng PCI hoặc CABG và điều trị nội khoa của tác giả Miller và cs25
Trong nghiên cứu này, chiến lược tái tưới máu dù là PCI hay CABG đều có lợi ích hơn so với điều trị nội khoa đơn thuần. Và đối tượng được hưởng lợi nhiều nhất là nhóm thiếu máu cơ tim nặng > 15%. Tuy vậy cho đến nay, chưa có thử nghiệm lâm sàng ngẫu nhiên có nhóm chứng nào được thực hiện để đánh giá ý nghĩa tiên lượng của thiếu máu cục bộ cơ tim ở bệnh nhân mắc bệnh cơ tim thiếu máu cục bộ; do đó, dựa trên bằng chứng hiện tại, hiện chưa có bằng chứng thuyết phục nào để thực hiện tái tưới máu cơ tim ở đối tượng này.
4. Vai trò và lợi ích của đánh giá sống – còn và thiếu máu cục bộ cơ tim hiện nay
Dựa trên các phân tích dưới nhóm về khả năng sống – còn cơ tim và thiếu máu cục bộ cơ tim trong thử nghiệm STICH, vai trò của cơ tim còn sống hoặc thiếu máu cục bộ trong việc lựa chọn điều trị và tiên lượng ở bệnh nhân mắc bệnh cơ tim do thiếu máu cục bộ không rõ ràng, vì các thực nghiệm không tìm được mối liên quan nào giữa lợi ích của CABG và kết quả trắc nghiệm gắng sức. Đánh giá tính sống – còn cơ tim qua các thử nghiệm, không cải thiện về tiên lượng dài hạn cho bệnh nhân. Kết quả các nghiên cứu và đồng thuận các chuyên gia đều đồng thuận rằng nhiều yếu tố quyết định đến giảm tỉ lệ tử vong ở bệnh nhân suy tim do CAD, không chỉ do tái tưới máu mà còn tiến bộ của thuốc trong điều trị nội khoa26 và các thiết bị tái đồng bộ27. Mặt khác, chiến lược tái tưới máu chỉ có lợi khi có thiếu máu cục bộ cơ tim nghiêm trọng (> 15% LV); do đó trong thực hành lâm sàng, quyết định tái tưới máu dựa trên thiếu máu cục bộ không làm cải thiện tiên lượng sống còn, mà chỉ cải thiện triệu chứng lâm sàng khi không đáp ứng với OMT.
Dựa trên các bằng chứng của thử nghiệm lâm sàng, Panza và cs22 và Liga và cs24 đề xuất thay đổi trong việc ứng dụng khả năng sống – còn và thiếu máu cục bộ cơ tim trong trong quản lý bệnh nhân bệnh cơ tim do thiếu máu cục bộ có đủ điều kiện phẫu thuật tái tưới máu. Khái niệm quan trọng trong đề xuất của hai tác giả đó là lượng cơ tim còn sống hoặc thiếu máu cục bộ nên được đánh giá như một biến liên tục, không phải biến nhị giá. Do đó không nên phân loại bệnh nhân thành hai nhóm “ cơ tim còn sống hoặc có thiếu máu cục bộ” và “cơ tim không còn sống hoặc không thiếu máu cục bộ”. Thay vào đó, quyết định chiến lược CABG không dựa vào có hay không có cơ tim còn sống, mà tập trung vào các đặc điểm như sau: (1) khối lượng và sự phân bố các vùng cơ tim còn sống và (2) giải phẫu mạch vành phù hợp với vùng cơ tim còn để tái tưới máu bằng phẫu thuật. Ngoài ra, trắc nghiệm gắng sức nhằm đánh giá tình trạng thiếu máu cục bộ chỉ nên chỉ định khi có các triệu chứng đau thắt ngực hoặc tương đương, và chỉ định phẫu thuật tái tưới nên thực hiện đối với bệnh nhân có tình trạng thiếu máu cục bộ nghiêm trọng.
5. THỬ NGHIỆM REVIVED-BCIS2
Năm 2022, Hiệp hội can thiệp tim mạch Anh công bố kết quả thử nghiệm REVIVED (REVIVED-BCIS2)8. Đây là thử nghiệm lâm sàng ngẫu nhiên có nhóm chứng. Dựa trên kết quả thử nghiệm STICH, mục đích thử nghiệm REVIVED để kiểm định giả thuyết: liệu rằng kết hợp PCI và OMT có thể mang lại lợi ích sống còn tốt hơn so với chỉ điều trị OMT đơn thuần ở bệnh nhân mắc bệnh cơ tim do thiếu máu cục bộ. Chiến lược PCI sẽ vượt qua các nguy cơ thủ thuật và nguy cơ liên quan đến CABG. Nghiên cứu này gồm 700 bệnh nhân có phân suất tống máu thất trái (LVEF) ≤ 35%, bệnh động mạch vành lan rộng (điểm BCIS ≥ 6) và có bằng chứng về tính sống – còn cũng như thiếu máu cục bộ ≥ 4 vùng cơ tim theo phân loại chi phối mạch vành. Tất cả bệnh nhân được chia nhóm ngẫu nhiên thành hai nhóm: một nhóm tiến hành PCI + OMT (gồm 347 bệnh nhân) và OMT đơn thuần (353 bệnh nhân). Tiêu chuẩn loại trừ trong nghiên cứu REVIVED gồm: bênh nhân có nhồi máu cơ tim cấp trong 4 tuần trước hoặc có biến cố suy tim cấp mất bù hoặc loạn nhịp thất trong vòng 72 giờ trước khi phân nhóm ngẫu nhiên. Thời gian theo dõi trung bình trong nghiên cứu là 41 tháng (tương tự như trong thử nghiệm STICH). Kết quả nghiên cứu ghi nhận không có sự khác biệt về tỉ lệ nhập viện do suy tim hoặc kết cục chính là tử vong do mọi nguyên nhân giữa nhóm PCI (37,2%) và nhóm OMT (38%) [HR = 0.99, KTC 95% = 0.78–1. 27, p = 0.96) (Bảng 1). Đánh giá về tiêu chí phụ gồm thay đổi LVEF sau 6 tháng sau 12 tháng, cũng không ghi nhận sự khác biệt giữa 2 nhóm. Điểm số chất lượng cuộc sống cao hơn đối với nhóm PCI ở sau 6 tháng và 12 tháng, nhưng sự khác biệt này giảm dần sau 24 tháng.
Bảng 1: So sánh kết quả của thử nghiệm STICH – STICHES và REVIVED
| Biến cố | Thử nghiệm STICH – STICHES | Thử nghiệm REVIVED | ||||||
| CABG
(n = 610) |
OMT
(n = 602) |
Lợi ích CABG
(95%CI) |
p | PCI
(n = 347) |
OMT (n = 353) | Lợi ích PCI
(95%CI) |
p | |
| Tử vong do mọi nguyên nhân | 218
(36%) |
244
(41%) |
0.86
(0.72–1.04) |
0.12 | 110
(31.7%) |
115
(32.6%) |
0.98
(0.75–1.27) |
|
| Tử vong do mọi nguyên nhân hoặc nhập viện vì suy tim | 290
(48%) |
324
(54%) |
0.84
(0.71–0.98) |
0.03 | 129
(37.2%) |
134
(38%) |
0.99
(0.78–1.27) |
0.96 |
| Tử vong do nguyên nhân tim mạch | 168
(28%) |
201
(33%) |
0.81
(0.66–1.00) |
0.05 | 76
(21.9%) |
88
(24.9%) |
0.88
(0.65–1.20) |
|
| Tử vong do mọi nguyên nhân khi theo dõi dài hạn | 359
(58.9%) |
398
(66.1%) |
0.84
(0.73–0.97) |
0.02 | ||||
| Tử vong do mọi nguyên nhân hoặc nhập viện vì suy tim khi theo dõi dài hạn | 404
(66.2%) |
450
(74.8%) |
0.81
(0.71–0.93) |
0.002 | ||||
| Tử vong do mọi nguyên nhân hoặc nhập viện vì suy tim khi theo dõi dài hạn | 247 (40.5%) | 297
(49.3%) |
0.79
(0.66–0.93) |
0.006 | ||||
6. So sánh giữa hai nghiên cứu STICH và REVIVED
Hai thử nghiệm REVIVED8 và STICH7 đều được thiết kế với mục đích đánh giá lợi ích của tái tưới máu ở bệnh nhân bệnh cơ tim thiếu máu cục bộ, tuy nhiên các quần thể bệnh nhân giữa hai nghiên cứu này khác nhau một vài đặc điểm. So với bệnh nhân ở nghiên cứu STICH, bệnh nhân trong thử nghiệm REVIVED có độ tuổi lớn hơn 10 tuổi (Tuổi trung bình 70 tuổi); có gánh nặng CAD lớn hơn (do bao gồm cả tổn thương thân chung) và quan trọng là nhận được liệu pháp điều trị nội khoa tiến bộ hơn theo các khuyến cáo hiện hành. Trong nghiên cứu REVIVED, điều trị nội khoa tối ưu bao gồm các loại thuốc chứng minh cải thiện tiên lượng ở bệnh nhân suy tim gồm: kháng thụ thể mineralocorticoid (MRAs) và thuốc ức chế thụ thể angiotensin và neprilysin (ARNI) và SGLT-2. Hơn nữa, trong nghiên cứu REVIVED bệnh nhân được hưởng lợi ích từ các thiết bị cấy ghép như: liệu pháp tái đồng bộ thất (CRT) hoặc máy phá rung (ICD). Ngược lại, nghiên cứu STICH được tuyển chọn từ năm 2002 đến 2007, và vào thời điểm đó, điều trị nội khoa được khuyến cáo loại I cho HfrEF chỉ bao gồm: thuốc ức chế men chuyển angiotensin, thuốc chẹn beta và digitalis28. Hơn nữa, lợi ích của ICDs trong phòng ngừa đột tử được báo cáo vào năm 2004–2005. Các đặc điểm dân số nguy cơ cao kết hợp tiến bộ trong điều trị nội khoa có thể giải thích một phần cho kết quả lâm sàng tương tự của thử nghiệm REVIVED-BCIS2 và thử nghiệm STICH. Do đó, có thể cần một thử nghiệm ngẫu nhiên so sánh lợi ích CABG với PCI và OMT để ước tính lợi ích của tái tưới máu bằng CABG hoặc PCI trong STICH(ES) và REVIVED-BCIS2, đặc biệt trong bối cảnh hai nghiên cứu này sử dụng các quần thể bệnh nhân và các phương pháp tái tái máu khác nhau.
- Mô hình “sàng lọc ảo” mô phỏng một thử nghiệm lâm sàng so sánh CABG hoặc PCI
Nhằm cung cấp thêm thông tin và tính khả thi của một thử nghiệm ngẫu nhiên có nhóm chứng về lợi ích của phương pháp tái tưới máu, Pathak và cs29, sử dụng mô hình “sàng lọc ảo” (in silico). Mục đích nghiên cứu so sánh chiến lược CABG và PCI ở bệnh nhân bệnh nhiều nhánh mạch vành kèm suy tim, nhằm đánh giá hiệu quả giảm tỷ lệ tử vong do mọi nguyên nhân hoặc nhập viện vì tim mạch trong 5 năm của từng phương pháp. Nghiên cứu gồm 13.519 bệnh nhân suy tim, được lấy từ dữ liệu thống kê các đợt nhập viện (HES) ở Anh, với dữ liệu cá nhân của bệnh nhân từ thử nghiệm STICH. Các tác giả sử dụng thống kê ưu việt từ khoa học máy tính (computational statistical methods), để phân nhóm mô phỏng ngẫu nhiên gồm: 1174 bệnh nhân nhóm CABG và 872 bệnh nhân nhóm PCI. Kết quả của Pathak và cs29 gợi ý rằng: đối với bệnh nhân bệnh nhiều nhánh mạch vành kèm suy tim, tỷ lệ tử vong và nhập viện vì tim mạch trong 5 năm thấp hơn ở nhóm CABG so với PCI(51.1% ở nhóm CABG và 70.0% ở nhóm PCI)29. Mặc dù nghiên cứu “sàng lọc ảo” có những hạn chế nhất định, tuy nhiên nghiên cứu này nhấn mạnh tính khả thi của thử nghiệm đối đầu ngẫu nhiên có nhóm chứng giữa CABG so với PCI. Mặt khác tác giả Pathak và cs29 đưa ra quan điểm nên lựa chọn CABG ở bệnh nhân bệnh cơ tim do thiếu máu cục bộ đủ điều kiện phẫu thuật. Theo khuyến cáo của Châu Âu, có sự khác biệt giữa khuyến cáo của hội tim mạch can thiệp Châu Âu năm 2018 và Khuyến cáo suy tim năm 2021 về chiến lược CABG trên đối tượng nguy cơ cao: bệnh nhiều nhánh mạch vành ± tổn thương thân chung. Theo ESC/EACTS 2018 khuyến cáo mạnh mẽ CABG trên đối tượng nguy cơ cao này, với mức độ chứng cứ loại I-B. Tuy nhiên, theo khuyến cáo suy tim ESC năm 2021, CABG ưu tiên lựa chọn đối với bệnh nhân bệnh tim thiếu máu cục bộ, kèm đái tháo đường hoặc tổn thương thân chung với mức độ chứng cứ thấp hơn là loại II-A.
7. Bằng chứng hiện tại và các khoảng trống?
Trái ngược với phân tích dưới nhóm của thử nghiệm ISCHEMIA , thử nghiệm REVIVED-BCIS2 cho thấy trên bệnh nhân bệnh động mạch vành mạn kèm suy tim, chiến lược tái tưới máu động mạch vành qua da không vượt trội so với điều trị nội khoa tối ưu trong tiên lượng sống còn ở bệnh nhân không có triệu chứng hoặc có ít triệu chứng. Cho nên, theo dõi dài hạn từ thử nghiệm REVIVED đang được mong đợi để cung cấp thêm bằng chứng chắc chắn. Khi phân tích sâu về thử nghiệm REVIVED-BCIS2, số ca nhồi máu cơ tim ở nhóm OMT gần gấp đôi so với nhóm PCI (lần lượt là 9% và 5%). Ngoài ra, chỉ định ICD ở nhóm PCI thấp hơn nhóm OMT (14% nhóm OMT và 5.9% ở nhóm 5.9%).
Tuy nhiên, vẫn còn nhiều câu hỏi chưa được giải đáp. Đầu tiên, suy giảm chức năng thất trái và bệnh mạch vành có thể là hai tình trạng lâm sàng khác nhau cùng tồn tại mà không nhất thiết phải liên quan đến nhau, đặc biệt trong các trường hợp suy chức năng thất nặng mà không đi kèm với tổn thương mạch vành nặng, tức là bệnh nhân chỉ có bệnh một/hai nhánh mạch vành – đây là tình trạng của khoảng một nửa bệnh nhân trong thử nghiệm REVIVED30. Và phân suất tống máu giảm nghiêm trọng có thể là hậu quả của bệnh van tim hoặc viêm cơ tim, hoặc bệnh cơ tim vô căn. Do đó, câu hỏi quan trọng mà các bác sĩ lâm sàng cần xác chẩn qua việc kết hợp các xét nghiệm chức năng không xâm lấn và xâm lấn: liệu rằng CAD là nguyên nhân chính gây ra suy giảm chức năng thất trái hay là hai bệnh cùng tồn tại? Thứ hai, chưa đủ thông tin về tầm quan trọng giải phẫu và mức độ hẹp mạch vành đối với tính sống – còn hoặc thiếu máu cục bộ cơ tim31. Các phân tích bổ sung và dữ liệu theo dõi từ thử nghiệm REVIVED-BCIS2 đang rất được mong đợi, đặc biệt mối liên quan giữa tính sống – còn cơ tim và hồi phục chức năng thất trái, để có kết luận chắc chắn đối với thực hành lâm sàng. Cuối cùng, ngay cả từ những thử nghiệm RCTs, cũng chưa đưa ra kết luận cuối cùng về lợi ích tái tưới máu ở bệnh nhân bệnh tim thiếu máu cục bộ kèm suy giảm chức năng thất trái so với điều trị nội khoa đơn thuần. Các tác giả Vincenzo Acerbo và Arturo Cesaro1 đã đưa ra sơ đồ tiếp cận đối với bệnh nhân CAD kèm phân suất tống máu giảm như sau:
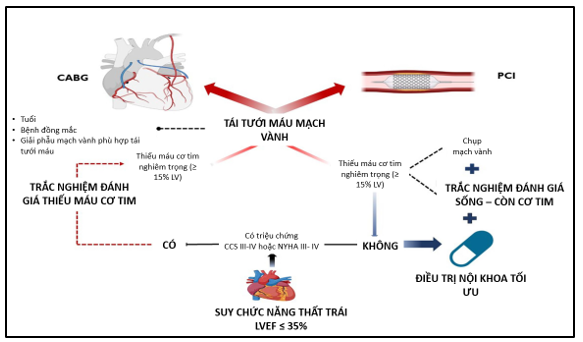
Hình: Đề xuất lưu đồ tiếp cận đối với bệnh nhân CAD kèm suy tim LVEF ≤ 35%
8. Kết luận
Trong khoảng hơn một thập kỷ qua, những tiến bộ đáng nổi bật của liệu pháp điều trị, cùng với việc ra đời các loại thuốc mới đã chứng minh cải thiện tiên lượng cho bệnh nhân mắc bệnh động mạch vành và suy tim. Điều này đưa ra những tranh luận về vai trò hiện tại của tái thông động mạch vành trong bối cảnh lâm sàng hiện nay. Nghiên cứu STICH cho thấy phẫu thuật bắc cầu động mạch vành (CABG) làm giảm tỉ lệ tử vong khi theo dõi 10 năm, mặc dù lợi ích này không đáng kể trong giai đoạn theo dõi 5 năm đầu tiên. Ngược lại, kết quả của nghiên cứu REVIVED-BCIS2 cho thấy can thiệp động mạch vành qua da (PCI) không mang lại lợi ích sống – còn so với điều trị nội khoa. Trong thực hành hiện nay, tỉ lệ tử vong ở nhóm bệnh nhân suy tim do thiếu máu cục bộ cơ tim còn cao, vì thế nhấn mạnh tầm quan trọng của việc xác định phương pháp điều trị tốt nhất cho từng bệnh nhân (tức là CABG, PCI, hoặc chỉ OMT). Ngoài ra, dữ liệu các nghiên cứu cho thấy bệnh lý đồng mắc, tuổi và tính sống – còn cơ tim và giải phẫu mạch vành phù hợp cho việc tái thông là những yếu tố quan trọng để lựa chọn và hướng dẫn chiến lược điều trị tối ưu. Hiện nay các bằng chứng chưa thống nhất, nên cầm thêm các nghiên cứu và chờ đợi kết quả dài hạn từ thử nghiệm REVIVED để hiểu rõ hơn vai trò của tái thông động mạch vành ở bệnh nhân mắc bệnh cơ tim thiếu máu cục bộ.
TÀI LIỆU THAM KHẢO
- Acerbo V, Cesaro A, Scherillo G, et al. Understanding the role of coronary artery revascularization in patients with left ventricular dysfunction and multivessel disease. Heart Failure Reviews. 2023;28(6):1325-1334.
- Pavo N, Prausmüller S, Bartko PE, Goliasch G, Hülsmann M. Neprilysin as a biomarker: challenges and opportunities. Cardiac failure review. 2020;6
- McDonagh TA, Metra M, Adamo M, et al. 2021 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure: Developed by the Task Force for the diagnosis and treatment of acute and chronic heart failure of the European Society of Cardiology (ESC) With the special contribution of the Heart Failure Association (HFA) of the ESC. European heart journal. 2021;42(36):3599-3726.
- Palmiero G, Cesaro A, Vetrano E, et al. Impact of SGLT2 inhibitors on heart failure: from pathophysiology to clinical effects. International Journal of Molecular Sciences. 2021;22(11):5863.
- Cesaro A, Gragnano F, Calabro P, et al. Prevalence and clinical implications of eligibility criteria for prolonged dual antithrombotic therapy in patients with PEGASUS and COMPASS phenotypes: Insights from the START-ANTIPLATELET registry. International journal of cardiology. 2021;345:7-13.
- Elgendy IY, Mahtta D, Pepine CJ. Medical therapy for heart failure caused by ischemic heart disease. Circulation research. 2019;124(11):1520-1535.
- Velazquez EJ, Lee KL, Deja MA, et al. Coronary-artery bypass surgery in patients with left ventricular dysfunction. New England Journal of Medicine. 2011;364(17):1607-1616.
- Perera D, Clayton T, O’Kane PD, et al. Percutaneous revascularization for ischemic left ventricular dysfunction. New England Journal of Medicine. 2022;387(15):1351-1360.
- Diamond GA, Forrester JS, deLuz PL, Wyatt H, Swan H. Post-extrasystolic potentiation of ischemic myocardium by atrial stimulation. American heart journal. 1978;95(2):204-209.
- Rahimtoola S. A perspective on the three large multicenter randomized clinical trials of coronary bypass surgery for chronic stable angina. Circulation research. 1985;72(6 Pt 2):V123-35.
- Rahimtoola SH. Coronary bypass surgery for chronic angina–1981. A perspective. Circulation research. 1982;65(2):225-241.
- Heusch G. Myocardial stunning and hibernation revisited. Nature Reviews Cardiology. 2021;18(7):522-536.
- Gerber BL, Rousseau MF, Ahn SA, et al. Prognostic value of myocardial viability by delayed-enhanced magnetic resonance in patients with coronary artery disease and low ejection fraction: impact of revascularization therapy. Journal of the American College of Cardiology. 2012;59(9):825-835.
- Kloner RA. Stunned and hibernating myocardium: where are we nearly 4 decades later? Journal of the American Heart Association. 2020;9(3):e015502.
- Allman KC, Shaw LJ, Hachamovitch R, Udelson JE. Myocardial viability testing and impact of revascularization on prognosis in patients with coronary artery disease and left ventricular dysfunction: a meta-analysis. Journal of the American College of Cardiology. 2002;39(7):1151-1158.
- Velazquez EJ, Bonow RO. Revascularization in severe left ventricular dysfunction. Journal of the American College of Cardiology. 2015;65(6):615-624.
- Velazquez EJ, Lee KL, Jones RH, et al. Coronary-artery bypass surgery in patients with ischemic cardiomyopathy. New England Journal of Medicine. 2016;374(16):1511-1520.
- Petrie MC, Jhund PS, She L, et al. Ten-year outcomes after coronary artery bypass grafting according to age in patients with heart failure and left ventricular systolic dysfunction: an analysis of the extended follow-up of the STICH trial (Surgical Treatment for Ischemic Heart Failure). Circulation research. 2016;134(18):1314-1324.
- Ryan M, Morgan H, Chiribiri A, Nagel E, Cleland J, Perera D. Myocardial viability testing: all STICHed up, or about to be REVIVED? European Heart Journal. 2022;43(2):118-126.
- Conrad N, Judge A, Tran J, et al. Temporal trends and patterns in heart failure incidence: a population-based study of 4 million individuals. The Lancet. 2018;391(10120):572-580.
- Gersh BJ, De Mets D. Revascularization in ischaemic cardiomyopathy: how to interpret current evidence. European Heart Journal. 2023;44(5):365-367.
- Panza JA, Holly TA, Asch FM, et al. Inducible myocardial ischemia and outcomes in patients with coronary artery disease and left ventricular dysfunction. Journal of the American College of Cardiology. 2013;61(18):1860-1870.
- Lopes RD, Alexander KP, Stevens SR, et al. Initial invasive versus conservative management of stable ischemic heart disease in patients with a history of heart failure or left ventricular dysfunction: insights from the ISCHEMIA trial. Circulation research. 2020;142(18):1725-1735.
- Liga R, Colli A, Taggart DP, Boden WE, De Caterina R. Myocardial revascularization in patients with ischemic cardiomyopathy: for whom and how. Journal of the American Heart Association. 2023;12(6):e026943.
- Miller RJ, Bonow RO, Gransar H, et al. Percutaneous or surgical revascularization is associated with survival benefit in stable coronary artery disease. European Heart Journal-Cardiovascular Imaging. 2020;21(9):961-970.
- Cleland J, Pennell D, Ray S, et al. Myocardial viability as a determinant of the ejection fraction response to carvedilol in patients with heart failure (CHRISTMAS trial): randomised controlled trial. The Lancet. 2003;362(9377):14-21.
- Ypenburg C, Schalij MJ, Bleeker GB, et al. Impact of viability and scar tissue on response to cardiac resynchronization therapy in ischaemic heart failure patients. European heart journal. 2007;28(1):33-41.
- Members C, Hunt SA, Baker DW, et al. ACC/AHA guidelines for the evaluation and management of chronic heart failure in the adult: executive summary a report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines (Committee to Revise the 1995 Guidelines for the Evaluation and Management of Heart Failure). Circulation research. 2001;104(24):2996-3007.
- Pathak S, Lai FY, Miksza J, et al. Surgical or percutaneous coronary revascularization for heart failure: an in silico model using routinely collected health data to emulate a clinical trial. European Heart Journal. 2023;44(5):351-364.
- Kirtane AJ. REVIVE-ing a weak heart—details matter. New England Journal of Medicine. 2022;387(15):1426-1427.
- Vergallo R, Liuzzo G. The REVIVED-BCIS2 trial: percutaneous coronary intervention vs. optimal medical therapy for stable patients with severe ischaemic cardiomyopathy. Eur Heart Journal. 2022;







