10. Kiểm soát tần số trong rung nhĩ.
Kiểm soát tần số là một phần không thể tách rời trong việc điều chỉnh bệnh nhân AF và thường đủ để cải thiện các triệu chứng liên quan đến AF. So với việc phòng ngừa đột quỵ và kiểm soát nhịp, có rất ít bằng chứng rõ ràng cho biết mẫu và cường độ tốt nhất của điều trị kiểm soát tần số, với phần lớn các dữ liệu thu được từ các thử nghiệm chéo ngắn hạn và các nghiên cứu quan sát [41,526-528].
TS Phạm Hữu Văn
Kiếm soát tần số bằng thuốc có thể đạt được cho kiểm soát tần số ngắn hạn và cấp thời với beta blocker, digoxin, chẹn kênh canxi diltiazem và verapamil, hoặc điều trị phối hợp (Bảng 15). Một số thuốc chống loạn nhịp cũng có đặc tính hạn chế tần số (amiodarone, dronedaron, sotalol, và một số mức độ propafenone), nhưng chỉ nên dùng cho những bệnh nhân cần điều trị kiếm soát nhịp (xem chương 11).
Bẳng 15. Điều trị kiểm soát tần số trong rung nhĩ
|
Điều trị |
Kiếm soát tần số đường tĩnh mạch cấp |
Kiếm soát tần số uống dài hạn |
Các tác dụng phụ |
Nhận xét |
|
Beta-blockersa |
||||
|
Bisoprolol |
Not available |
1.25–20 mg once daily or split. |
Bất lợi phổ biến nhất đã được thông báo.Các triệu chứng buồn ngủ, nhức đầu, phù ngoại biên, các triệu chứng đường hô hấp trên.Các triệu chứng đường hô hấp,Rối loạn da dầy ruột và chóng mặt. Tác dụng phụ gồm nhịp chậm, block AV và hạ huyết áp. |
Co thắt phế quản rất hiếm – trong trường hợp hen phế quản, các thuốc beta 1 chọn lọc được khuyến cáo (tránh carvedilol). Chống chỉ định trong suy tim cấp và bệnh sử co thắt phế quản nặng. |
|
Carvedilol |
Not available |
3.125–50 mg twice daily. |
||
|
Metoprolol |
2.5–10 mg intravenous bolus (repeated as required).
|
100–200 mg total daily dose (according to preparation). |
||
|
Nebivolol |
Not available |
2.5–10 mg once daily or split. |
||
|
Calcium-channel blockers |
||||
|
Diltiazem |
15–25 mg intravenous bolus (repeated as required).
|
60 mg 3 lần hàng ngày đến 360 mg toàn bộ liều mỗi ngày (120–360 mg lần ngày được sửa đổi). |
Bất lợi phổ biến nhất đã được thông báo.Các triệu chứng chóng mặt, khó chịu, lười biếng, nhức đầu, nóng bừng, rối loạn dạ dầy ruột và phù. Tác dụng phụ gồm nhịp tim chậm, block AV và hạ huyết áp (hạ huyết áp kéo dài có thể với verapamil). |
Sử dụng thận trọng khi kết hợp với thuốc beta blockers. Giảm liều với suy gan và bắt đầu với liều nhỏ hơn trong suy thận. Chống chỉ định trong suy LV với ứ trệ phổi hoặc LVEF < 40%. |
|
Verapamil |
2.5–10 mg intravenous bolus (nhắc lại khi được đòi hỏi).
|
40–120 mg 3 lần ngày (120–480 mg đưa ra được sửa đổi mỗi lần ngày). |
||
|
Cardiac glycosides |
||||
|
Digoxin |
0.5 mg tĩnh mạch bolus (0.75–1.5 mg qua 24h trong các liều được pha loãng).
|
0.0625–0.25 mg liều hàng ngày |
Bất lợi phổ biến nhất được báo cáo. Các triệu chứng rối loạn tiêu hóa, chóng mặt, nhìn mờ, nhức đầu và phát ban. Trong trạng thái nhiễm độc (nồng độ trong huyết thanh > 2 ng /ML), digoxin thúc đẩy rối loạn nhịp và có thể làm nặng suy tim, đặc biệt với hạ kali máu đồng thời |
Mức độ huyết tương cao kết hợp với tăng nguy cơ tử vong. Kiểm tra chức năng thận trước khi bắt đầu và điều chỉnh liều ở bệnh nhân bị CKD. Chống chỉ định ở các bệnh nhân có nhịp nhanh thất có đường phụ và bệnh cơ tim phì đại với tắc nghẽn đường ra. |
|
Digitoxin |
0.4–0.6 mg tĩnh mạch bolus. |
0.05–0.3 mg liều hàng ngày. |
||
|
Các chỉ định chuyên biệt |
||||
|
Amiodarone
|
300 mg tĩnh mạch được pha loãng trong 250 mL 5% dextrose qua 30–60 phút (tốt hơn qua tĩnh mạch trung tâm)b
|
200 mg daily |
Hạ huyết áp, nhịp tim chậm, buồn nôn, QT kéo dài, độc phổi, biến đổi màu da, rối loạn chức năng tuyến giáp, cặn giác mạc và phản ứng da với bên ngoài. |
Đề xuất như điều trị bổ trợ ở bệnh nhân kiểm soát tần số tim không thể đạt được sử dụng điều trị phối hợp. |
AF: rung nhĩ; CKD: bệnh thận mạn; i.v.: trong tĩnh mạch; LV: thất trái; LVEF: phân suất tống máu thất trái.
aMột số thuốc chẹn beta khác cũng có sẵn, nhưng không được khuyến cáo là liệu pháp điều trị kiểm soát tần số chuyên biệt trong AF. Gồm atenolol (25-100 mg x 1 lần / ngày với thời gian bán hủy ngắn), propranolol [không chọn lọc, 1 mg / 1 phút và lặp lại 3 mg ở khoảng thời gian 2 phút (cấp thời) hoặc 10-40 mg ba Lần mỗi ngày (dài hạn)], hoặc labetalol [không chọn lọc, 1-2 mg / phút (cấp thời)].
bNếu tiếp tục đòi hỏi amiodarone, tiếp theo với 900 mg i.v. trong 24 giờ pha loãng trong 500-1000 mL qua tĩnh mạch trung tâm.
10.1 Kiểm soát tần số cấp thời
Trong bối cảnh AF khởi phát mới cấp tính, bệnh nhân thường cần kiểm soát tần số tim. Các bác sĩ nên đánh giá các nguyên nhân cơ bản làm tần số tim tăng cao, chẳng hạn như nhiễm trùng, mất cân bằng nội tiết, thiếu máu và tắc mạch phổi. Đối với việc kiểm soát tần số cấp thời, thuốc chẹn beta và diltiazem / verapamil được ưa thích hơn digoxin vì khởi phát nhanh và hiệu quả trên trương lực giao cảm cao. [528-532] Lựa chọn thuốc (Bảng 15) và tần số tim mục tiêu sẽ phụ thuộc vào đặc điểm bệnh nhân, triệu chứng, LVEF và huyết động học, nhưng cách tiếp cận ban đầu với tần số tim không chặt chẽ (lenient) dường như có thể chấp nhận. Điều trị phối hợp có thể được đòi hỏi (Hình 14). Ở những bệnh nhân có HFrEF, thuốc chẹn bêta, digitalis (digoxin hoặc digitoxin) hoặc dùng phối hợp chúng nên được sử dụng [218,533] vì diltiazem và verapamil có thể có hiệu quả inotrop âm tính ở những bệnh nhân có LVEF <40% .[222,534,535] Ở những bệnh nhân nặng và những người có rối loạn chức năng LV tâm thu suy giảm nặng, amiodarone tiêm tĩnh mạch có thể được sử dụng khi tần số tim đưa đến huyết động không ổn dịnh. [536-538] Chuyển nhịp khẩn cấp cần được xem xét ở các bệnh nhân không ổn định (xem chương 11.1).
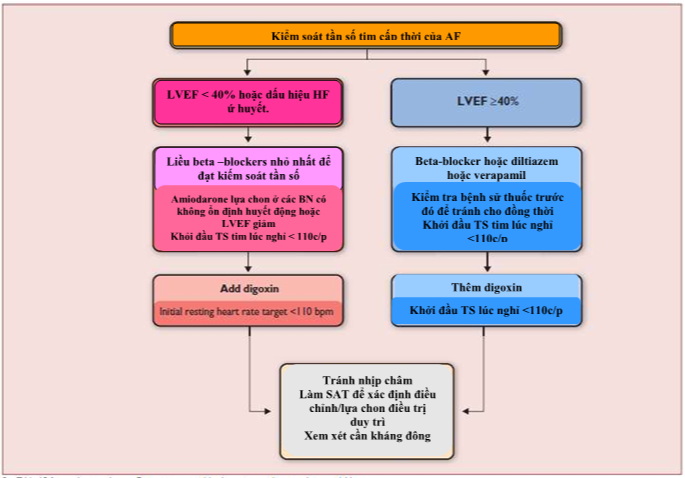
Hình 14. Kiểm soát tần số tim cấp thời ở các bệnh nhân rung nhĩ.
Xem bảng liều thuốc ở bảng 15. Digitoxin là thay thể phù hợp cho digoxin, nếu có.AF: rung nhĩ. LVEF: phân suất tổng máu. c/p: chu kỳ /phút.
10.2 Kiểm soát tần số bằng thuốc dài hạn
10.2.1 Beta-blockers
Đơn trị liệu chẹn thụ thể beta adrenicgic (beta adrenoreceptor) thường là thuốc kiểm soát tần số trước tiên, [539] trên cơ sở quan sát rộng lớn kiểm soát tần số cấp thời tốt hơn digoxin. Thật thú vị, lợi ích tiên đoán của thuốc chẹn beta ở bệnh nhân HFrEF có nhịp xoang không có ở các bệnh nhân bị AF. Trong phân tích gộp ở mức độ bệnh nhân riêng lẻ của các nghiên cứu ngẫu nhiên có đối chứng(RCTs), các thuốc chẹn beta không làm giảm tử suất do mọi nguyên nhân so với giả dược ở những người có AF ở thời điểm khởi đầu (HR 0,97, 95% CI 0,83-1,14, P = 0,73), trong khi đó lợi ích rõ ràng ở bệnh nhân nhịp xoang. (HR 0,73, KTC 95% 0,67-0,80, P <0,001) [23] Phân tích, bao gồm 3066 người tham gia có HFrEF và AF, cho thấy sự nhất quán trên tất cả các phân nhóm và kết cục, không có sự không đồng nhất giữa 10 RCTs (I [2] = 0%). Mặc dù mất đi lợi ích tiên đoán này trong HFrEF, Ban Đặc nhiệm vẫn coi các thuốc beta-blockers là thuốc kiểm soát tần số hữu ích hàng đầu ở tất cả các bệnh nhân AF, dựa trên tiềm năng cải thiện triệu chứng và chức năng do kiểm soát tần số, thiếu sự nguy hại từ các nghiên cứu đã được công bố, cũng như khả năng dung nạp tốt ở tất cả mọi lứa tuổi ở cả nhịp xoang và rung nhĩ. [23,540]
10.2.2 Các blockers kênh calcium không dihydropyridine
Verapamil hoặc diltiazem cung cấp sự kiểm soát tần số hợp lý ở bệnh nhân AF. [541] Verapamil hoặc diltiazem có thể cải thiện các triệu chứng liên quan đến loạn nhịp, so với các thuốc chẹn beta, làm giảm khả năng gắng sức và B – type natriuretic peptide bị tăng lên trong một nghiên cứu nhỏ các bệnh nhân nguy cơ thấp với LVEF bảo tồn.[542]
10.2.3 Digitalis
Các glycosid tim như digoxin và digitoxin đã được sử dụng trong hơn hai thế kỷ, mặc dù việc kê đơn thuốc đã giảm đều trong 15 năm qua.[543] Trong nghiên cứu ngẫu nhiên Nhóm Xem xét Digitalis (Digitalis Investigation Group) (DIG), digoxin không ảnh hưởng đến tử vong so với giả dược ở bệnh nhân HFrEF có nhịp xoang (RR 0.99, 95% CI 0.91-1.07), nhưng giảm nhập viện (RR 0.72, 95% CI 0.66 – 0.79). [544, 545]. Đã không có các RCTs của digoxin đối đầu ở các bệnh nhân AF. [546] Các nghiên cứu quan sát kết hợp sử dụng digoxin với tử suất vượt quá ở bệnh nhân AF, [547-549] nhưng sự kết hợp này nhiều khả năng do sự lựa chọn và kê đơn bị ảnh hưởng hơn là nguy hiểm do digoxin, [550-553] đặc biệt là digoxin thường được kê đơn cho bệnh nhân nặng hơn.[225] Trong một thử nghiệm cơ học chéo 47 bệnh nhân với HFrEF và AF, không có sự khác biệt về nhịp tim, huyết áp, khoảng cách đi bộ, hoặc LVEF giữa carvedilol và digoxin, mặc dù beta-blockers đã làm tăng nồng độ peptide natriuretic B, Carvedilol / digoxin cải thiện LVEF, và ngừng digoxin đã làm LVEF bị giảm.[554] Các so sánh với các điều trị kiểm soát tần số khác trên cơ sở các nghiên cứu nhỏ và ngắn hạn cho thấy không hoặc sự khác biệt nhỏ trong dự trữ gắng sức, chất lượng sống, hoặc LVEF được so sánh với digoxin. [526,554-558] Liều digoxin thấp hơn (≤250 μg một lần / ngày), tương ứng với nồng độ digoxin huyết thanh từ 0,5-0,9 ng / mL, có thể liên quan đến tiên lượng tốt hơn [225].
10.2.4 Amiodarone
Amiodaron có thể hữu ích để kiểm soát tần số như một phương sách cuối cùng. Danh sách lớn các tác dụng có hại ngoài tim được kết hợp với amiodarone biện giải nó là thuốc để giành ở các bệnh nhân không thể kiểm soát tần số tim bằng điều trị phối hợp (ví dụ như beta-blocker hoặc verapamil / diltiazem kết hợp với digoxin).Tóm lại, có một sự cân bằng cho việc sử dụng các thuốc kiểm soát tần số khác nhau trong AF. Sự lựa chọn của beta-blocker, diltiazem / verapamil, digoxin, hoặc liệu pháp phối hợp được thực hiện trên cơ sở cá thể, sau khi xem xét các đặc điểm bệnh nhân và sở thích bệnh nhân. Tất cả các phương pháp điều trị có sẵn có tiềm ẩn các tác dụng bất lợi và bệnh nhân nên được khởi đầu với liều thấp và chuẩn liều tăng dần để đạt cải thiện triệu chứng. Trong thực tế, việc đạt được nhịp tim <110chu kỳ/phút (c/p). thường sẽ đòi hỏi điều trị kết hợp (hình 15). Lợi ích của các chiến lược kiểm soát tần số khác nhau về triệu chứng, chất lượng sống, hậu quả trung gian khác đang được xem xét. [559]
Amiodarone có thể hữu ích trong kiểm soát tần số như là phương án cuối cùng. Một loạt các tác dụng phu liên quan đến amiodarone làm cho nó trở thành một thuốc để giành ở các bệnh nhân có tần số tim không thể kiếm soát được với điều trị phối hợp (ví dụ beta-blocker hoặc verapamil / diltiazem kết hợp với digoxin).
Nói tóm lại, có sự cân nhắc cho việc sử dụng các thuốc kiểm soát tần số khác nhau trong AF. Việc lựa chọn thuốc chẹn beta, diltiazem / verapamil, digoxin hoặc liệu pháp phối hợp nên được thực hiện trên cơ sở tính cá thể, sau khi xem xét đặc điểm của bệnh nhân và sự ưu tiên bệnh nhân. Tất cả các liệu pháp sẵn có có thể có tác dụng phụ và bệnh nhân nên được điều trị ban đầu với liều thấp và tăng cường để đạt được sự cải thiện triệu chứng. Trên thực tế, đạt được nhịp tim <110 c/p. Thường sẽ cần điều trị kết hợp (Hình 15). Lợi ích của các chiến lược kiểm soát tần số khác nhau về triệu chứng, chất lượng sống và các kết cục trung gian khác đang được nghiên cứu.[559]
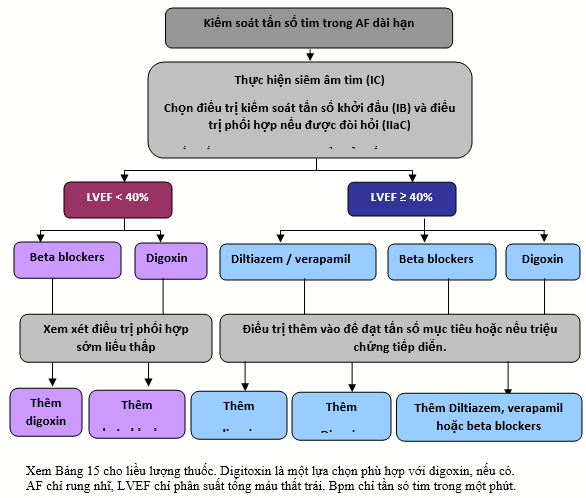
Hình 15.Kiểm soát tần số tim dài hạn ở các bệnh nhân rung nhĩ.
10.3 Mục tiêu tần số tim trong rung nhĩ
Mục tiêu tần số tim tối ưu ở bệnh nhân AF không rõ ràng. Nghiên cứu RACE II (Rate Control Efficacy in Permanent Atrial Fibrillation) đã ngẫu nhiên so sánh 614 bệnh nhân AF vĩnh viễn với tần số tim mục tiêu hoặc <80 c/p. lúc nghỉ hoặc <110 c/p. trong quá trình gắng sức trung bình, hoặc với mục tiêu nhịp tim không chặt chẽ (lenient) là <110 c/p. Không có sự khác biệt về kết hợp các biến cố lâm sàng (14,9% ở nhóm kiểm soát tần số nghiêm ngặt, 12,9% ở nhóm không chặt chẽ), [560] NYHA class hoặc nhập viện.[560,561] Các kết quả tương tự cũng được nhận thấy trong một phân tích tổng hợp AFFIRM (Atrial Fibrillation Follow-up Investigation of Rhythm Management) và thử nghiệm RACE (1091 người), mặc dù có sự khác biệt về tần số tim nhỏ hơn và không có sự ngẫu nhiên. [562] Cần lưu ý nhiều bệnh nhân ‘kiểm soát tần số thích hợp’ (tần số tim lúc nghỉ 60-100 c/p.) có triệu chứng nghiêm trọng, nói lên điều chỉnh thêm.[194] Tuy nhiên, kiểm soát tần số không chặt chẽ là cách tiếp cận khởi đầu có thể chấp nhận, bất kể tình trạng suy tim, trừ khi các triệu chứng đòi hỏi phải kiểm soát chặt chẽ hơn.
10.4 Triệt phá nút nhĩ thất và tạo nhịp
Triệt phá nút nhĩ thất / bó His và cấy máy tạo nhịp VVI có thể kiểm soát được tần số thất khi thuốc thất bại trong việc kiểm soát tần số và triệu chứng. Đây là một thủ thuật tương đối đơn giản với tần số biến chứng thấp và nguy cơ tử suất dài hạn thấp [563,564], đặc biệt khi máy tạo nhịp được cấy vài tuần trước khi triệt phá nút nhĩ thất và tần số tạo nhịp khởi đầu sau triệt phá ở tần số 70-90 c/p. [565,566] Thủ thuật không làm chức năng LV xấu đi [567] và có thể thậm chí cải thiện LVEF ở các bệnh nhân lựa chọn. [568–570] Ở các bệnh nhân HFrEF được lựa chọn được điều trị với tạo nhịp hai buồng thất (điều trị tài đồng bộ tim). AF có thể chấm dứt, [571] mặc dù hiệu quả ‘kiểm soát nhịp’ như vậy của điều trị tái đồng bộ thường nhỏ và cần được khằng định rõ ràng [572]. Triệt phá nút AV làm cho bệnh nhân phụ thuộc máy tạo nhịp lúc nghỉ trong cuộc sống của họ, hạn chế triệt phá nút AV và tạo nhịp đối với các bệnh nhân triệu chứng của họ không thể điều trị bằng thuốc kiểm soát tần số hoặc bằng các can thiệp kiểm soát nhịp phù hợp (xem Đội Tim AF, chương 11.6). Lựa chọn điều trị tạo nhịp (tạo nhịp thất phải hoặc tạo nhịp hai thất có hoặc không có khử rung tim) sẽ phụ thuộc vào đặc tính của bệnh nhân, LVEFF.[573,574]
Các khuyến cáo cho kiểm soát tần số (KC 1)
|
Các khuyến cáo |
Classa |
Levelb |
Ref C |
|
Beta-blockers, digoxin, diltiazem, hoặc verapamil được khuyến cáo để kiểm soát tần số tim ở các bệnh nhân AF có LVEF ≥40%. |
I |
B |
225, 526, 528, 531, 532, 541, 555, 575 |
|
Beta-blockers và / hoặc digoxin được khuyến cáo để kiểm soát tần số tim ở các bệnh nhân AF có LVEF <40%. |
I |
B |
23, 225, 526, 533, 554, 575, 576 |
|
Điều trị phối hợp gồm các các thuốc kiểm soát tần số khác nhau nên được xem xét nếu một thuốc duy nhất không đạt được mục tiêu tần số tim cần thiết. |
IIa |
C |
23, 554, 577 |
|
Ở bệnh nhân có huyết động học không ổn định hoặc LVEF giảm trầm trọng, amiodarone có thể được xem xét để kiểm soát tần số tim cấp thời. |
IIb |
B |
536 –538 |
|
Ở bệnh nhân có AF vĩnh viễn (nghĩa là không còn nỗ lực để phục hồi nhịp xoang được lên kế hoạch), không nên thường xuyên sử dụng thuốc chống loạn nhịp để kiểm soát tần số. |
III (harm) |
A |
41, 578, 579 |
|
Tần số tim lúc nghỉ <110 c/p (tức là kiểm soát nhịp không chặt chễ) nên được coi là mục tiêu tần số khởi đầu cho điều trị kiếm soát tần số. |
IIa |
B |
560 |
|
Các chiến lược kiểm soát nhịp hơn chiến lược kiểm soát tần số nên được xem xét như một điều chỉnh ưu tiên trong AF do kích thích sớm và AF trong quá trình thai nghén. |
IIa |
C |
|
|
Triệt phá nút AV nên được xem xét để kiếm soát tần số tim ở các bệnh nhân không đáp ứng hoặc kém chịu đựng để điều trị kiểm soát tần số và nhịp, chấp nhận các bệnh nhân này sẽ trở nên phụ thuộc máy tạo nhịp. |
IIa |
B |
184, 564,569 |
AF: rung nhĩ; c/p: chu kỳ trên phút; LVEF: phân suất tống máu thất trái.
• Digitoxin là thuốc thay thế digoxin phù hợp, nếu có. Ở những bệnh nhân suy tim có phân suất tống máu giảm (LVEF <40%), các thuốc chẹn beta được khuyến cáo là bisoprolol, carvedilol, metoprolol tác dụng kéo dài và nebivolol.
aClass các khuyến cáo.
bMức độ bằng chứng.
cTài liệu tham khảo ủng hộ các khuyến cáo.
11. Điều trị kiểm soát nhịp trong rung nhĩ
Khôi phục và duy trì nhịp xoang xoang là một phần không thể tách rời trong điều chỉnh AF. Các thuốc chống loạn nhịp tăng gấp hai lần tần số nhịp xoang phù hợp so với placebo [580-584] Triệt phá qua catheter hoặc điều trị phối hợp thường hiệu quả khi các thuốc chống loạn nhịp phối hợp [226,585–587] Mặc dù nhiều bác sĩ lâm sàng cho rằng việc duy trì nhịp xoang có thể cải thiện kết cục ở bệnh nhân AF, [588] tất cả các nghiên cứu đã so sánh kiểm soát nhịp và kiểm soát tần số đối với kiểm soát tần số đơn thuần (với kháng đông thích hợp) Các thuốc chống loạn nhịp có thể làm tăng nguy cơ viêm xoang , [588] Tất cả các thử nghiệm so sánh kiểm soát nhịp và kiểm soát tần số để kiểm soát tần số đơn thuần (với thuốc kháng đông thích hợp) đã dẫn đến các kết cục trung hòa. [41,578,579,582,589-593] Liệu điều chỉnh kiểm soát nhịp hiện đại có liên quan đến việc triệt phá qua catheter, điều trị phối hợp và điều trị sớm đưa đến giảm trong các biến cố tim mạch lớn hiện đang được điều tra, như trong EAST – AFNET 4 (Điều trị Sớm Rung nhĩ để ngăn ngừa Đột quỵ) [40] và nghiên cứu CABANA (Triệt phá qua catheter đối lại Điều trị Thuốc Chống loạn nhịp trong Rung nhĩ). Hiện tại, điều trị kiểm soát nhịp được chỉ định để cải thiện triệu chứng ở các bệnh nhân AF có triệu chứng trên điều trị kiểm soát tần số đầy đủ.
11.1 Phục hồi nhịp xoang cấp thời
11.1.1 Các thuốc chống loạn nhịp cho phục hồi nhịp xoang cấp thời (‘chuyển nhịp bằng thuốc’)
Các thuốc chống loạn nhịp có thể khôi phục lại nhịp xoang ở bệnh nhân AF (chuyển nhịp bằng thuốc) như cho thấy trong các nhiên cứu đối chứng nhỏ, phân tích gộp [41,584,595,596] và trong một số thử nghiệm có đối chứng lớn hơn. [597-605] Ngoài châu Âu, dofetilide có sẵn và có thể chuyển nhịp AF vừa khởi phát. [606] Chuyển nhịp bằng thuốc khôi phục nhịp xoang ở khoảng 50% các bệnh nhân với AF vừa mới khởi phát (Bảng 16). [607–609] Trong ngắn hạn, chuyển nhịp bằng điện phục hồi nhịp xoang nhanh hơn và hiệu quả hơn chuyển nhịp bằng thuốc và được liên quan với nhập viện ngắn hơn [607-609].[609-613] Chuyển nhịp bằng thuốc, ngược lại, không đòi hỏi giảm đau hoặc nhịn ăn (Hình 16).
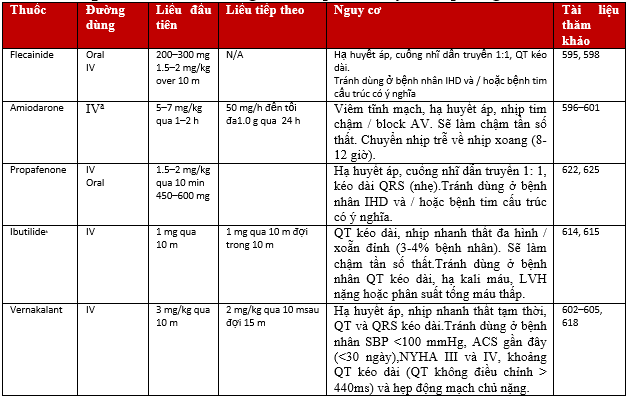
Bảng 16.Các thuốc chống loạn nhịp cho chuyển nhịp bằng thuốc.
ACS: hội chứng mạch vành cấp; AV: nhĩ – thất; IHD: bệnh tim thiếu máu cục bộ; i.v.: trong tĩnh mạch; LVH: phì đại thất trái; NYHA: Hội Tim New York; SBP: huyết áp tâm thu. m: phút. h: giờ.
aSử dụng mạch máu ngoại biên lớn và thay đổi sang amiodarone uống trong phạm vi 24h sử dụng đường tĩnh mạch (đường trung tâm).
bIbutilide chỉ có thể có ở các nước châu Âu được lựa chọn.
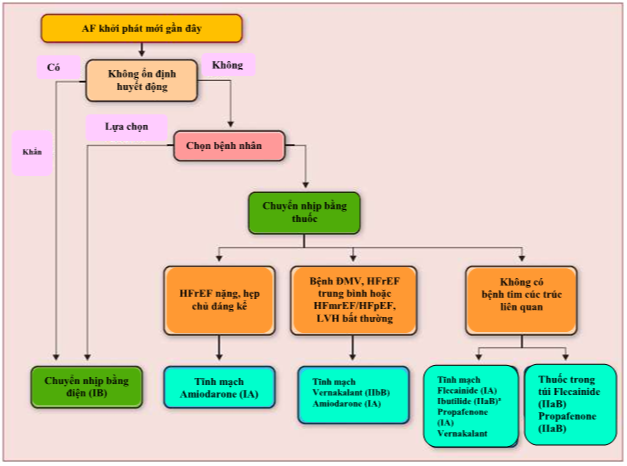
Hình 16. Điều chỉnh kiểm soát nhịp rung nhĩ khởi phát mới
AF: rung nhĩ. ĐMV: động mạch vành. HFrEF: suy tim phân suất tống máu giảm. HFmrEF: suy tim phân suất phạm vi trung bìn. HFpEF: suy tim phân suất tống máu bảo tồn.
Flecainide và propafenone có hiệu quả để chuyển nhịp bằng thuốc,[595,602-605,614,615] nhưng việc sử dụng chúng chỉ giới hạn ở những bệnh nhân không có bệnh tim cấu trúc. Ibutilide là một phương pháp thay thế nếu có, nhưng có nguy cơ gây torsades de pointes. [615] Vernakalant [602-605] có thể được dùng cho bệnh nhân suy tim nhẹ (NYHA Class I hoặc II), bao gồm những người bị bệnh tim thiếu máu, miễn là họ không có hạ huyết áp hay xơ vữa động mạch nặng.[616-618] Amiodaron có thể được sử dụng ở bệnh nhân suy tim và ở những bệnh nhân bị bệnh thiếu máu cục bộ (mặc dù bệnh nhân suy tim nặng đã bị loại khỏi hầu hết các thử nghiệm lâm sàng AF).[596] Amiodarone cũng làm chậm nhịp tim 10-12 chu kỳ / phút sau 8-12 giờ khi tiêm tĩnh mạch.[596] Cả hai amiodarone và flecainide đều có hiệu quả hơn sotalol trong việc khôi phục nhịp xoang.[600,601,619]
11.1.2 ‘Viên thuốc bỏ túi’ chuyển nhịp được bệnh nhân thực hiện
Ở những bệnh nhân được lựa chọn với các cơn AF kịch phát có triệu chứng không thường xuyên, một liều đơn của thuốc uống flecainide (200-300 mg) hoặc propafenone (450-600 mg) có thể được bệnh nhân tự điều trị ở nhà (‘ điều trị viên thuốc trong túi’) để khôi phục nhịp xoang, sau khi an toàn đã được thiết lập ở bệnh viện.[620] Phương pháp này có vẻ ít hiệu quả hơn so với chuyển nhịp trên cơ sở bệnh viện,[621] nhưng thực tế và cung cấp sự kiểm soát và đảm bảo với các bệnh nhân được lựa chọn.
11.1.3 Chuyển nhịp bằng điện
Chuyển nhịp bằng điện một chiều trực tiếp đồng bộ chuyển từ AF về nhịp xoang nhanh chóng và hiệu quả, cũng như phương pháp lựa chọn ở các bệnh nhân tổn thương huyết động nặng có AF khởi phát mới (Hình 16). [626-628] Chuyển nhịp bằng điện có thể được thực hiện an toàn ở các bệnh nhân được điều trị an thần bằng midazolam tĩnh mạch và / hoặc propofol tĩnh mạch. Theo dõi liên tục huyết áp và oxy trong suốt quá trình điều trị là rất quan trọng. [629] Đôi khi có thể thấy bỏng da. Atropine tĩnh mạch hoặc isoproterenol, hoặc tạo nhịp qua da tạm thời, nên có sẵn để giảm nhẹ nhịp chậm sau chuyển nhịp. Máy khử rung dạng sóng hai pha có hiệu quả hơn dạng sóng một pha và trở thành tiêu chuẩn kỹ thuật. [626,628] Các vị trí điện cực trước – sau tạo ra một trường sốc mạnh hơn ở tâm nhĩ trái so với các điện cực ở vị trí nằm trước bên, cũng như khôi phục nhịp xoang hiệu quả hơn. [626.627.630]
Điều trị bằng amiodaron (cần vài tuần điều trị), [631,632] sotalol, [631] ibutilide, [633] hoặc vernakalant [634] có thể cải thiện hiệu quả chuyển nhịp bằng điện, cũng như hiệu quả tương tự như đối với flecainide [584] và propafenone. [635] Beta-blockers, [636] verapamil, diltiazem, [637-639] và digoxin [640,641] không chắc chắn cắt được AF hoặc làm dễ dàng cho chuyển nhịp bằng điện. Khi điều trị bằng thuốc chống loạn nhịp được lên kế hoạc để duy trì nhịp xoang sau chuyển nhịp, có thể bắt đầu điều trị 1-3 ngày trước khi chuyển nhịp (amiodarone: vài tuần) để thúc đẩy chuyển nhịp bằng thuốc và để đạt được mức độ thuốc hiệu quả. [584.601]
11.1.4 Kháng đông ở các bệnh nhân trải qua chuyển nhịp
Chuyển nhịp tim đưa đến nguy cơ đột quỵ ở các bệnh nhân không được kháng đông, [642] nguy cơ này giảm đáng kể do dùng thuốc kháng đông[643] Khởi đầu ngay lập tức kháng đông là quan trọng ở tất cả các bệnh nhân được lên kế hoạch chuyển nhịp. [644-646] Các bệnh nhân AF đã hơn 48 giờ nên được bắt đầu OAC ít nhất 3 tuần trước khi chuyển nhịp và tiếp tục cho đến 4 tuần sau đó (ở bệnh nhân không cần kháng đông lâu dài). OAC nên được tiếp tục vô hạn ở những bệnh nhân có nguy cơ bị đột quỵ. Thực tiễn này chưa bao giờ được đánh giá trong các thử nghiệm đối chứng, nhưng dường như an toàn trong một bộ dữ liệu quan sát lớn từ Phần Lan [647] . Khi chuyển nhịp sớm được yêu cầu, TOE có thể loại trừ phần lớn thrombus tâm nhĩ trái, cho phép chuyển nhịp ngay lập tức. [648,649] Các nghiên cứu đang được tiến hành sẽ thông báo về tính an toàn và hiệu quả của thuốc kháng đông được khởi đầu mới gần đây sử dung NOAC ở bệnh nhân dự kiến chuyển nhịp.
11.2 Điều trị thuốc chống loạn nhịp dài hạn
Mục đích của liệu pháp chống loạn nhịp là cải thiện các triệu chứng liên quan đến AF.[41,580] Do đó, quyết định bắt đầu điều trị thuốc chống loạn nhịp kéo dài cần cân bằng gánh nặng triệu chứng, phản ứng có hại của thuốc có thể xảy ra, cũng như sở thích của bệnh nhân. Các nguyên tắc của liệu pháp chống loạn nhịp được phác thảo trong Hướng dẫn của ESC năm 2010 [369] vẫn còn phù hợp và cần được tuân theo:
1. Điều trị nhằm giảm các triệu chứng liên quan đến AF;
2. Hiệu quả của thuốc chống loạn nhịp để duy trì nhịp xoang là khiêm tốn;
3. Liệu pháp trị liệu chống loạn nhịp thành công về lâm sàng có thể làm giảm hơn là loại bỏ tái phát AF;
4. Nếu một thuốc chống loạn nhịp “thất bại”, đáp ứng có thể chấp nhận về lâm sàng có thể đạt được với thuốc khác;
5. Thúc đầy loạn nhịp do thuốc hoặc các phản ứng phụ ngoài tim thường gặp;
6. Xem xét an toàn hơn hiệu quả trước hết nên hướng dẫn sự lựa chọn thuốc chống loạn nhịp.
Điều trị thuốc chống loạn nhịp tăng khoảng gấp đôi sự duy trì nhịp xoang so với không điều trị. [580] Không có tác động đáng kể nào đối với tử suất hoặc các biến chứng tim mạch, nhưng liệu pháp kiểm soát nhịp có thể làm tăng nhẹ nguy cơ nhập viện (thường do AF) [41,578,579,582,589-593] Để giảm nguy cơ tác dụng phụ, [201,580] thời gian điều trị chống loạn nhịp ngắn hơn dường như là một mong muốn. Ví dụ, điều trị ngắn hạn (4 tuần) với Flecainide trong 4 tuần sau khi nhồi máu cơ tim đã được dung nạp tốt và phòng ngừa AF tái phát được nhiều nhất (80%) khi so sánh với điều trị dài hạn. Liệu pháp chống loạn nhịp tim ngắn hạn cũng được sử dụng để tránh AF tái phát sớm sau khi triệt phá qua catheter, cũng có thể hợp lý ở những bệnh nhân được cho là thuốc chống loạn nhịp có nguy cơ tăng tác dụng phụ hoặc những người có nguy cơ AF tái phát.
Ngoài trị liệu chống loạn nhịp và triệt phá qua catheter (xem chương 11.3), điều chỉnh các trạng thái tim mạch đồng thời có thể làm giảm gánh nặng triệu chứng trong AF và giúp duy trì nhịp xoang. [203,204,296,312] Điều này gồm giảm cân, kiểm soát huyết áp, điều trị suy tim, tăng khả năng tim và hô hấp, cũng như các biện pháp khác (xem chương 7).
11.2.1 Lựa chọn thuốc chống loạn nhịp cho điều trị dài hạn: trước hết là an toàn !
Thông thường, sự an toàn của thuốc chống loạn nhịp sẽ quyết định sự lựa chọn khởi đầu của thuốc chống loạn nhịp (Hình 17). Có các loại thuốc chống loạn nhịp chính sau đây có khả năng để phòng ngừa AF:
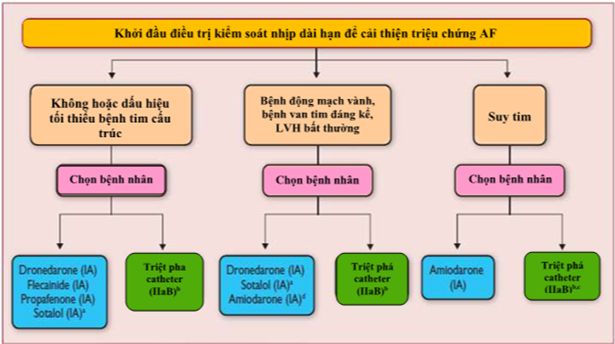
Hình 17.Khởi đầu điều trị kiểm soát nhịp dài hạn ở các bệnh nhân rung nhĩ có triệu chứng.
AF: rung nhĩ. LVH: phì đại thất trái
aSotalol đòi hỏi đánh giá cẩn thận nguy cơ thúc đẩy loạn nhịp.
bTriệt phá catheter nên cô lập các tĩnh mạch phổi và có thể thực hiện sử dụng qua catheter tần số radio hoặc bóng lạnh.
c Triệt phá catheter là điều trị đầu tiên, thường phục hồi cho bệnh nhân suy tim do bệnh cơ tim nhịp nhanh.
d Amiodarone là điều trị lựa chọn thứ hai ở nhiều bệnh nhân do các tác dụng phụ ngoài tim của thuốc.
11.2.1.1 Amiodarone
Amiodaron là một chất ngăn chặn đa kênh hiệu quả, làm giảm tần số thất và an toàn cho bệnh nhân suy tim.[552,651] Thúc đẩy loạn nhịp Torsades de pointes có thể xảy ra, cũng như khoảng QT và các sóng TU nên được theo dõi trong quá trình điều trị (xem Bảng 17). [652] Amiodaron thường gây ra các phản ứng phụ ngoài tim, đặc biệt là điều trị dài hạn [653,654], làm cho nó là điều trị hàng thứ 2 ở những bệnh nhân thích hợp với các thuốc chống loạn nhịp khác. Amiodaron dường như không thích hợp với liệu pháp từng đợt ngắn hạn (trừ sau triệt phá qua catheter), [655] có lẽ vì thời gian nửa đời sống sinh học kéo dài.
Bảng 17.Các thuốc chống loạn nhịp uống được sử dụng để duy trì nhịp xoang sau chuyển nhịp
|
Thuốc |
Liều |
Chống chỉ định chính và chú ý |
Dấu hiệu cảnh báo Đảm bảo ngừng thuốc |
Chậm dẫn truyền AV |
Theo dõi ECG được gợi ý trong thời gian khởi đầu |
|
Amiodarone |
600 mg ở những liều cho trong 4 tuần, 400 mg trong 4 tuần, sau 200 mg mỗi ngày |
Chú ý khi sử dụng điều trị phối hợp với thuốc làm QT dài và ở BN với bệnhSAN hoặc nút AV và dẫn truyền. Liều VKAs và digitalis nên được giảm. Nguy cơ bệnh cơ tim tăng lên với. Chú ý ở BN có bệnh gan tồn tại trước. |
QT kéo dài >500 ms |
10–12 nhịp /phút trong AF |
Ban đầu, 1 tuần, 4 tuần.
|
|
Dronedarone |
400 mg Hai lần ngày |
Chống chỉ định trong NYHA Class III hoặc IV hoặc suy tim không ổn định, trong quá trình điều trị phối hợp với các thuốc làm QT dài, hoặc CYP3A4 inhibitors mạnh (như. verapamil, diltiazem, thuốc kháng nấm, azole), và khi CrCl <30 ml/min. Liều digitalis, beta-blockers, và một vài statins cần được giảm liều. Tăng creatinine trong huyết tương 0.1–0.2 mg/dL thường gặp và không phản ánh suy chức năng thận . |
Kéo dài QT >500 ms |
10–12 nhịp /phút trong AF |
Khởi đầu, 1 tuần, 4 tuần
|
|
Flecainide
Flecainide thải tiết chậm |
100–150 mg Hai lần ngày 200 mg Một lần ngày |
Chống chỉ định nếu CrCl <50 mg/mL, bệnh gan, IHD hoạc phân suất LV giảm. Chú ý sự hiện diện bệnh của SAN hoặc nút AV hoặc dẫn truyền. CYP2D6 inhibitors (như. fluoxetine hoặc chống trầm cảm tricyclic) làm tăng nồng độ trong huyết tương. |
QRS duration increases >25% above baseline |
None |
Khởi đầu, ngày 1, ngày 2–3 |
|
Propafenone
Propafenone SR |
150–300 mg three times daily 225–425 mg twice daily |
Chống chỉ định trong IHD hoặc phân suất tống máu LV. Chú ý khi có bệnh SAN hoặc nút AV và dẫn truyền, suy thận hoặc gan và hen phế quản. Tăng nồng độ digoxin và warfarin. |
Khoảng QRS tăng>25% Trên mức khởi đầu |
Nhẹ |
Khởi đầu, ngày 1, ngày 2–3 |
|
d,l sotalol |
80–160 mg twice daily |
Chống chỉ định khi có hiện diện phì đại LV đáng kể, suy tim tâm thu, hen phế quản, QT kéo dài từ trước, hạ kali máu, CrCl<50 mg/mL. Rối loạn chức năng thận đòi hỏi phù hợp liều cẩn thận.
|
Khoảng QT >500 ms, kéo dài QT>60 ms so với khởi đầu điều trị
|
Tương tự liều blockers cao
|
Khởi đầu, ngày 1, ngày 2–3 |
|
|
|
|
|
|
|
AF: rung nhĩ; AV: nhĩ – thất; bpm: nhịp /phút; CrCl: độ lọccreatinine; CYP2D6: cytochrome P450 2D6; CYP3A4: cytochrome P450 3A4;
ECG: điện tâm đồ; IHD: bệnh tim thiếu máu cục bộ; LV: thất trái; LVEF: phân suất tống máu; NYHA: Hội Tim New York; SAN: nút xoang; VKA: kháng vitamin K.
11.2.1.2 Dronedarone
Dronedarone duy trì nhịp xoang, giảm tần số thất, cũng như ngăn ngừa nhập viện do bệnh tim mạch (chủ yếu là do AF) và tử vong tim mạch ở những bệnh nhân có AF kịch phát hoặc dai dẳng hoặc cuồng nhĩ có ít nhất một bệnh tim mạch kèm theo [583,588,656] Dronedaron tăng tỷ lệ tử vong ở bệnh nhân suy tim mất bù mới xẩy ra (có hoặc không có AF)[657] và ở bệnh nhân có AF vĩnh viễn, trong đó nhịp xoang xoang không phục hồi. [658] Dronedaron làm tăng creatinine huyết thanh, phản ánh sự giảm bài tiết creatinin hơn là giảm chức năng thận [659].
11.2.1.3 Flecainide và propafenone
Fletainide và propafenone có hiệu quả trong việc phòng ngừa AF tái phát,[581,584,620] chỉ nên sử dụng ở những bệnh nhân không có bệnh cơ tim thiếu máu cục bộ đáng kể hoặc suy tim để tránh nguy cơ loạn nhịp thất đe dọa tính mạng.[660] Tần số thất cao do chuyển từ AF sang cuồng nhĩ với dẫn truyền 1: 1 do flecainide hoặc propafenone có thể ngăn ngừa được bằng cách sử dụng trước beta-blocker, verapamil hoặc diltiazem.
11.2.1.4 Quinidine và disopyramide
Quinidin và disopyramid có liên quan đến sự gia tăng tỷ lệ tử vong do mọi nguyên nhân (OR 2,39, 95% CI 1,03-5,59, số cần thiết để làm hại 109, KTC 95% 34-4985) theo dõi 1 năm, [580,661] do loạn nhịp thất (torsades de pointes).[580,661] Mặc dù hiệu quả chống loạn nhịp thường gặp ở liều cao hơn, nhưng chúng thường ít được sử dụng để kiểm soát nhịp trong AF. Disopyramide có thể hữu ích trong AF ‘trung gian qua phế vị’ (ví dụ AF xảy ra ở vận động viên và / hoặc trong giấc ngủ [76]) và đã được chứng minh là làm giảm gradient dòng ra thất trái và cải thiện triệu chứng ở bệnh nhân bệnh cơ tim phì đại. [662-664]
11.2.1.5 Sotalol
Sotalol có nguy cơ liên quan đến torsades de pointes [1% trong nghiên cứu Ngăn ngừa Rung Nhĩ Sau Chuyển nhịp Chống Rối loạn nhịp (Prevention of Atrial Fibrillation After Cardioversion: PAFAC) [118]. D-enantiomer được kết hợp với tử suất tăng lên so với placebo ở các bệnh nhân có rối loạn chức năng LV sau nhồi máu cơ tim,[665] khả năng do rối loạn nhịp thất (OR 2,47, 95% CI 1,2-5,05, số cần thiết để có hại 166, 95% KTC 61-1159). [580,665] Mặt khác, d, l-sotalol đã được sử dụng trong các bệnh nhân AF không có dấu hiệu an toàn trong hai thử nghiệm đối chứng [581,601]
11.2.1.6 Dofetilide
Dofetilide là một blocker kênh kali khác chủ yếu có ở bên ngoài châu Âu. Dofetilide phục hồi và duy trì nhịp xoang ở bệnh nhân suy tim, [666] đôi khi ở những bệnh nhân trơ với các thuốc chống loạn nhịp khác.[667] Nhìn chung, có vẻ thận trọng để hạn chế sử dụng quinidine, disopyramide, dofetilide và sotalol vào các tình huống đặc biệt. Hơn nữa, tránh phối hợp các thuốc chống loạn nhịp làm kéo dài QT để kiểm soát nhịp trong AF (Bảng 17).
11.2.2 Điện tâm đồ 12 chuyển đạo như là một công cụ để nhận biết nguy cơ thúc đẩy rối loạn nhịp
Xác định bệnh nhân có nguy cơ loạn nhịp tim có thể giúp làm giảm nguy cơ thúc đẩy rối loạn nhịp của các thuốc chống loạn nhịp. [668] Ngoài các đặc điểm lâm sàng đã đề cập ở trên, theo dõi khoảng PR, QT và QRS trong thời gian khi bắt đầu điều trị thuốc chống loạn nhịp có thể xác định bệnh nhân có nguy cơ cao thúc đẩy rối loạn nhịp do thuốc gây ra trong điều trị dài hạn hơn.[669-671] Ngoài ra, Sự hiện diện của ‘các sóng TU bất thường’ là một dấu hiệu sắp xẩy ra torsades de pointes.[652] Phân tích ECG định cho các dấu hiệu thúc đẩy rối loạn nhịp đã được sử dụng thành công trong các nghiên cứu thuốc chống loạn nhịp mới đây. [118, 584, 672] Đặc biệt, theo dõi ECG được sử dụng một cách hệ thống trong 1 – 3 ngày ở các bệnh nhân nhận được flecainide, propafenone, hoặc sotalol để xác định những người có nguy cơ thúc đẩy rối loạn nhịp. [118.584.601] Dựa trên thực hành được đánh giá này, để người ta gọi ý ghi ECG ở tất cả các bệnh nhân trước khi khởi đầu các thuốc chống loạn nhip. ECG được lên lịch trình trong quá trình khởi đầu dường như là phù hợp (Bảng 17).
11.2.3 Các thuốc chống loạn nhịpmới
Một số hợp chất ức chế dòng kali siêu nhanh (IKur) và các chất ức chế các kênh ion không điển hình khác trong quá trình phát triển lâm sàng. [673-675] Các thuốc này không có sẵn trong sử dụng lâm sàng hiện nay. Ranolazine cấu thành chống đau thắt ngực ức chế dòng kali và natri cũng như tăng chuyển hóa glucose trong tiêu biến chuyển hóa acid béo tự do, bằng cách này làm gia tăng hiệu quả sử dụng ô xy. [676,677] Ranolazine an toàn ở các bệnh nhân nhồi máu ST không chênh lên và đau thắt ngực không ổn định được lượng giá trong MERLIN (Metabolic Efficiency With Ranolazine for Less Ischemia in Non ST-Elevation Acute Coronary Syndrome). [678] Trong một phân tích post hoc ghi ECG liên tục thu được trong quá trình 7 ngày đầu tiên sau chỉ định ngẫu nhiên bệnh nhân với ranolazine có xu hướng các cơn AF ít hơn so các bệnh nhân với placebo [75 (2,4%) so với 55 (1,7%); P = 0.08]. [679] Trong nghiên cứu HARMONY (Nghiên cứu đánh giá hiệu quả của Ranolazine và Dronedarone khi dùng đơn độc và kết hợp ở bệnh nhân bị rung nhĩ), liều ranolazine cao nhất (750 mg 2 lần / ngày) và dronedarone (225 mg hai lần ngày) làm giảm nhẹ gánh nặng AF ở 134 đối tượng với các cơn AF và máy tạo nhịp hai buồng. [680] Các nghiên cứu nhỏ, mức độ mở cho thấy ranolazine có thể làm tăng tác dụng chống loạn nhịp của amiodarone trong việc chuyển nhịp, [681-683] ngược lại kết quả từ nghiên cứu đối chứng của ranolazine và phối hợp ranolazine-dronedarone để ngăn ngừa AHRE (cơn tần số nhĩ cao) ở bệnh nhân tạo nhịp còn chưa rõ. [684] Hiện nay, không có đủ bằng chứng để khuyến cáo ranolazine như một thuốc chống loạn nhịp, đơn thuần hoặc phối hợp với các thuốc chống loạn nhịp khác. Lưu ý, thuốc ‘blocker kênh funny’, iabradine, được sử dụng cho chứng đau thắt ngực và suy tim, làm tăng nguy cơ AF. [685]
11.2.4 Hiệu quả chống loạn nhịp của các thuốc không phải chống loạn nhịp
Các thuốc ức chế ACE hoặc thuốc ARB dường để ngăn ngừa AF khởi phát mới ở những bệnh nhân suy giảm chức năng LV và ở những bệnh nhân tăng huyết áp có phì đại thất trái. [219, 236, 237, 239, 246, 250, 686] Cần phải nghiên cứu thêm ức chế Neprilysin, dường như không làm tăng hiệu quả này [224]. Một nghiên cứu đoàn hệ Đan Mạch cũng cho thấy điều trị ban đầu tăng huyết áp không biến chứng với thuốc ức chế ACE hoặc ARB làm giảm AF xuất hiện so với các thuốc chống tăng huyết áp khác [245]. Điều trị ARB không làm giảm gánh nặng AF ở những bệnh nhân bị AF không có bệnh tim mạch [241] Do đó, chất ức chế ACE hoặc ARB có thể không có tác dụng liên quan chống loạn nhịp trực tiếp. Tuy nhiên, có thể xem xét thêm các chất ức chế ACE hoặc ARB vào các thuốc chống loạn nhịp để làm giảm sự tái phát của AF sau chuyển nhịp.[248,249,687]
So với giả dược, thuốc chẹn beta có liên quan đến giảm nguy cơ AF khởi phát mới ở bệnh nhân có HFrEF và nhịp xoang. [23] Các thuốc chẹn beta cũng được báo cáo làm giảm các triệu chứng tái phát triệu chứng, [580.636.688] nhưng phát hiện này có thể dẫn đến hiệu quả của việc kiểm soát tần số, điều này sẽ giải thích AF không có triệu chứng thường nhiều hơn.
Điều trị bằng statin quanh phẫu thuật đưa đến làm giảm nguy cơ AF quanh phẫu thuật ở một số RCTs nhỏ.[689,690] Tuy nhiên, một thử nghiệm đối chứng với placebo đủ mạnh đã chỉ ra không có hiệu quả của điều trị rosuvastatin quanh phẫu thuật trong AF sau phẫu thuật[691]. Điều trị bằng statin không ngăn chặn được sự phát triển AF trong các tình huống khác. [692,693] Tương tự, các axit béo không bão hòa không thể hiện lợi ích thuyết phục.[241,694-698] Vai trò của các thuốc đối kháng aldosterone trong việc điều trị AF không được nghiên cứu rộng rãi ở người. Mặc dù các bằng chứng sơ bộ từ các thử nghiệm eplerenone đang khuyến khích để phòng ngừa ban đầu,[243] hiện nay không có bằng chứng mạnh mẽ để đưa ra bất kỳ khuyến cáo nào cho việc sử dụng các chất đối kháng aldosterone để phòng ngừa AF thứ phát [699-701]
Các khuyến cáo cho điều trị kiểm soát nhịp (KC 2)
|
Các khuyến cáo |
Classa |
Levelb |
Rifec |
|
Các khuyến cáo chung |
|||
|
Điều trị kiểm soát nhịp được chỉ định để cải thiện triệu chứng ở BN AF. |
I |
B |
120, 586, 601 |
|
Điều chỉnh các yếu tố nguy cơ tim mạch và tránh khởi kích AF nên là mục đích ở các BN điều trị kiểm soát nhịp để làm dễ dàng duy trì nhịp xoang.
|
IIa |
B |
203, 204, 296, 312 |
|
Ngoại trừ AF có liên quan đến mất ổn định về huyết động, lựa chọn giữa chuyển nhịp bằng điện và thuốc nên được hướng dẫn do sự ưu tiên của bệnh nhân và thày thuốc. |
IIa |
C |
|
|
Chuyển nhịp AF |
|||
|
Chuyển nhịp AF bằng điện được khuyến cáo ở các bệnh nhân có không ổn định huyết học cấp tính để khôi phục cung lượng tim |
I |
B |
612, 702-704 |
|
Chuyển nhịp AF (điện hoặc thuốc) được khuyến cáo ở những bệnh nhân có triệu chứng với AF dai dẳng hoặc dai dẳng kéo dài như một phần của điều trị kiểm soát nhịp. |
I |
B |
584,601, 627,628, 648, 705 |
|
Điều trị trước bằng amiodarone, flecainide, ibutilide, hoặc propafenone nên được xem xét để gia tăng thành công của chuyển nhịp bằng điện và ngăn ngừa AF tái phát. |
IIa |
B |
248, 584, 633 |
|
Ở những bệnh nhân không có bệnh sử bệnh tim thiếu máu cục bộ hoặc cấu trúc, flecainide, propafenone hoặc vernakalant được khuyến cáo dùng cho chuyển nhịp AF khởi phát mới bằng thuốc. |
I |
A |
602605,614, 618,622, 706,707 |
|
Ở bệnh nhân không có bệnh sử bệnh tim thiếu máu cục bộ hoặc cấu trúc, nên xem xét dùng ibutilide để chuyển nhịp AF bằng thuốc. |
IIa |
B |
|
|
Ở những bệnh nhân AF được lựa chọn và bệnh tim cấu trúc hoặc thiếu máu cục bộ không có ý nghĩa, liều uống flecainide hoặc propafenone đơn thuần (phương pháp thuốc ‘trong túi’) nên được xem xét cho các bệnh nhân hướng đến chuyển nhịp, đánh giá sự an toàn tiếp theo. |
IIa |
B |
620, 621 |
|
Ở các bệnh nhân thiếu máu cục bộ và / hoặc bệnh tim cấu trúc, amiodarone được khuyến cáo dùng cho chuyển nhịp AF. |
I |
A |
597–601 |
|
Vernakalant có thể được xem xét như là sự thay thế amiodarone để chuyển nhịp AF bằng thuốc ở các bệnh nhân không có hạ huyết áp, suy tim nặng hoặc bệnh tim cấu trúc nặng (đặc biệt hẹp động mạch chủ). |
IIb |
B |
602–605, 616, 618 |
|
Ngăn ngừa đột quỵ ở những bệnh nhân được được lựa chọn chuyển nhịp AF |
|||
|
Kháng đông bằng heparin hoặc NOAC nên được bắt đầu càng sớm càng tốt trước mỗi lần chuyển nhịp AF hoặc cuồng nhĩ. |
IIa |
B |
708, 709 |
|
Đối với chuyển nhịp AF /AFl (cuồng nhĩ), kháng đông có hiệu lực được khuyến cáo tối thiểu 3 tuần trước chuyển nhịp. |
I |
B |
648, 708 |
|
Siêu âm tim qua thực quản (TOE) được khuyến cáo để loại trừ huyết khối trong tim khi lựa chọn kháng đông trước thủ thuật khi chuyển nhịp được lên kế hoạch sớm. |
I |
B |
648, 708 |
|
Chuyển nhịp sớm có thể được thực hiện không cần TOE ở các bệnh nhân được khảng định khoảng thời gian AF <48 giờ. |
IIa |
B |
648 |
|
Ở những bệnh nhân có nguy cơ đột quỵ, điều trị kháng đông nên được tiếp tục dài hạn sau chuyển nhịp theo khuyến cáo kháng đông dài hạn, không phân biệt phương pháp chuyển nhịp hoặc duy trì nhịp xoang xoang rõ ràng. Ở những bệnh nhân không có các yếu tố nguy cơ đột quỵ, kháng đông được khuyến cáo trong 4 tuần sau chuyển nhịp. |
I |
B |
353, 710 |
|
Ở các bệnh nhân có huyết khối được TOE xác định, kháng đông có hiệu lực được khuyến cáo ít nhất 3 tuần. |
I |
C |
|
|
TOE lặp lại để đảm bảo khẳng định thrombus nên được xem xét trước chuyển nhịp. |
IIa |
C |
|
|
Các thuốc chống loạn nhịp duy trì nhịp xoang dài hạn / ngăn ngừa AF tái phát |
|||
|
Việc lựa chọn AAD cần phải được đánh giá cẩn thận, có tính đến hiện diện đồng bệnh suất, nguy cơ tim mạch và khả năng thúc đẩy loạn nhịp nặng, các ảnh hưởng độc ngoài tim, sở thích của bệnh nhân, cũng như gánh nặng triệu chứng. |
I |
A |
41, 580 |
|
Dronedarone, Flecainide, Propafenone, hoặc Sotalol được khuyến cáo để ngăn ngừa AF tái phát có triệu chứng ở những bệnh nhân có chức năng tâm thất trái bình thường và không có phì đại thất trái bệnh lý. |
I |
A |
581, 583, 584, 588, 601 |
|
Dronedaron được khuyến cáo để ngăn ngừa AF tái phát có triệu chứng ở bệnh nhân có bệnh mạch vành ổn định, cũng như không có suy tim. |
I |
A |
583, 588 |
|
Amiodarone được khuyến cáo để ngăn ngừa AF tái phát có triệu chứng ở các bệnh nhân suy tim. |
I |
B |
596–598 |
|
Amiodarone hiệu quả nhiều hơn trong ngăn ngừa AF tái phát so với AAD khác, nhưng ảnh hưởng độc ngoài tim thường gặp và tăng theo thời gian. Cho lý do này, AAD khác nên được xem xét đầu tiên. |
IIa |
C |
596–598 |
|
Các bệnh nhân điều trị AAD nên được đánh giá định kỳ để khẳng định đủ điều kiện của thuốc cho điều trị |
IIa |
C |
583, 588, 657, 658, 660 |
Các khuyến cáo cho điều trị kiểm soát nhịp (tiếp theo)
|
Các khuyến cáo |
Classa |
Levelb |
Rifec |
|
AAD để duy trì nhịp xoang lâu dài / ngăn ngừa AF tái phát (tiếp theo) |
|||
|
Ghi ECG trong quá trình khởi đầu điều trị AAD nên được xem xét để theo dõi nhịp tim, phát hiện kéo dài khoảng QRS và QT, cũng như xuất hiện block AV. |
IIa |
B |
582-584, 588, 601 |
|
Điều trị AAD không được khuyến cáo ở các bệnh nhân khoảng QT kéo dài (> 0.5 giây) hoặc những người có bệnh nút xoang nhĩ đáng kể hoặc rối loạn chức năng nút AV không có máy tạo nhịp vĩnh viễn hoạt động. |
III (có hại) |
C |
|
|
Bổ sung tạo nhịp nhĩ khi nhịp chậm do điều trị thuốc tạo ra hoặc làm trầm trọng rối loạn chức năng nút xoang nên được xem xét để cho phép tiếp tục điều trị AAD ở các bệnh nhân có triệt phá AF được giảm đi hoặc không có chỉ định. |
IIa |
B |
711, 712 |
|
Tiếp tục điều trị AAD sau giai đoạn trống sau triệt phá AF cần được xem xét để duy trì nhịp xoang khi tái phát dường như có khả năng. |
IIa |
B |
713 |
|
Ảnh hưởng chống loạn nhịp của các thuốc không phải chống loạn nhịp |
|||
|
ACE-Is, ARBs và beta blockers nên được xem xét để ngăn ngừa AF khởi phát mới ở bệnh nhân suy tim và phân suất tống máu giảm. |
IIa |
A |
23, 219,236, 237,239, 250,714 |
|
ACE-và ARB nên được xem xét ngăn ngừa AF khởi phát mới ở bệnh nhân tăng huyết áp, đặc biệt phì đại phì đại LV. |
IIa |
B |
238, 246,686, 714 |
|
Việc điều trị trước với ACE-Is hoặc ARBs có thể được xem xét ở những bệnh nhân AF tái phát trên nền chuyển nhịp bằng điện và nhận được điều trị thuốc chống loạn nhịp. |
IIb |
B |
236, 237,248, 249 |
|
ACE-Is hoặc ARBs không được khuyến cáo để dự phòng thứ phát AF kịch phát ở những bệnh nhân có ít hoặc không có bệnh tim cơ. |
III (không lợi) |
B |
241, 697 |
ACE: men chuyển; AF: rung nhĩ; ARB: chẹn thụ thể angiotensin; CHA2DS2-VASc: C: suy tim, H: tăng huyết áp, A: tuổi ≥75 (găp 2), D: tiểu đường, S: đột quỵ (gấp 2), V: bệnh mạch máu, A: tuổi 65–74, S: giới (nữ); ECG: điện tâm đồ; LV: thất trái; LVH: phì đại thất trái; NOAC: kháng đông uống không phải vitamin K; TOE: siêu âm tim qua thực quản. AAD: thuốc chống loạn nhịp.
aClass khuyến cáo.
bMức độ bằng chứng.
cTài liệu ủng hộ các khuyến cáo.
11.3 Triệt phá qua catheter
Kể từ khi mô tả ban đầu về các yếu tố kích hoạt trong các tĩnh mạch phổi khởi đầu AF kịch phát [108], triệt phá qua catheter AF đã phát triển từ thủ thuật theo một quy trình thực nghiệm chuyên biệt đến điều trị rộng rãi để ngăn ngừa AF tái phát. [587.715] Điều này chủ yếu đạt được thông qua việc cô lập các tĩnh mạch phổi, có thể đòi hỏi sự cô lập hoàn toàn để có hiệu quả đầy đủ, [716] và triệt phá thêm ở thành nhĩ sau trái. Triệt phá AF, khi được thực hiện tại các trung tâm có kinh nghiệm do đội được huấn luyện phù hợp, hiệu quả nhiều hơn điều trị bằng thuốc chống loạn nhịp trong duy trì nhịp xoang, cũng như tần số biến chứng, mặc dù không đáng kế, tương tự tần số biến chứng đối với các thuốc chống loạn nhịp. [585,717]
11.3.1 Chỉ định
Triệt phá AF qua catheter có hiệu quả trong việc khôi phục và duy trì nhịp xoang ở những bệnh nhân AF kịch phát có triệu chứng, dai dẳng, cũng như có thể dai dẳng kéo dài, nói chung là điều trị hàng thứ 2 sau điều trị bằng thuốc chống loạn nhịp thất bại hoặc không dung nạp. [185,586,713,717-720] Như điều trị hàng đầu cho AF kịch phát, các nghiên cứu ngẫu nhiên chỉ ra chỉ cải thiện khiêm tốn kết quả nhịp với triệt phá qua catheter so với điều trị thuốc chống loạn nhịp [585,721-723] Tần số biến chứng là tương tự, khi triệt phá được thực hiện ở các trung tâm thành thạo, biện minh cho triệt phá qua catheter là phương pháp điều trị đầu tiên ở bệnh nhân được lựa chọn có AF kịch phát, những người đòi hỏi điều trị can thiệp. Có ít dữ liệu báo cáo về hiệu quả và sự an toàn của triệt phá qua catheter ở những bệnh nhân có AF dai dẳng hoặc dai dẳng kéo dài, nhưng tất cả đều cho thấy tỷ lệ tái phát thấp hơn sau khi triệt phá so với điều trị bằng thuốc chống loạn nhịp có hoặc không có chuyển nhịp (Hình 2) [185,717,723 -726.1039] Ở những bệnh nhân trải qua tái phát AF có triệu chứng mặc dù điều trị thuốc chống loạn nhịp, tất cả các RCTs đều cho thấy sự duy trì nhịp xoang tốt hơn với triệt phá qua catheter so với các thuốc chống loạn nhịp [586,713,727,728] Không có chỉ định hiện tại về triệt phá qua catheter để ngăn ngừa các kết cục tim mạch (hoặc mong muốn ngừng thuốc kháng đông), hoặc để giảm nhập bệnh viện.[40,594]
11.3.2 Kỹ thuật và công nghệ
Cô lập hoàn toàn tĩnh mạch phổi (pulmonary vein isolation: PVI) ở cấp độ tâm nhĩ là mục tiêu tốt nhất được chứng minh bằng tư liệu cho triệt phá qua catheter, [716,729-731] có thể đạt được bằng cách triệt phá bằng tần số radio từng điểm một sát nhau (point by point), các tổn thương thành đường bao quanh các tĩnh mạch phổi, hoặc triệt phá bằng bóng đông lạnh (cryoballoon), với các kết quả tương tự. [732-734] Cô lập hoàn toàn tĩnh mạch phổi có kết quả nhịp tốt hơn cô lập không hoàn toàn.[716] PVI được thử nghiệm ban đầu ở các bệnh nhân có AF kịch phát, nhưng dường như không kém hơn cho triệt phá rộng rãi hơn trong AF dai dẳng [729,735]. Triệt phá mở rộng hơn đã được sử dụng ở các bệnh nhân có AF dai dẳng, nhưng còn chưa đủ tư liệu để hướng dẫn sử dụng kỹ thuật này hiện nay. [117,718,719,735-737] Các thủ thuật triệt phá được tăng cường (ngoài PVI) luôn yêu cầu thủ thuật kéo dài hơn và bức xạ ion hóa nhiều hơn, tạo ra nguy cơ tiềm tàng cho bệnh nhân. Nhịp nhanh vào lại nhĩ trái vòng lớn tương đối không phổ biến sau PVI (≈5%). Cũng có vẻ như rất hiếm sau triệt phá bóng lạnh [734], nhưng có thể xảy ra ở 25% bệnh nhân sau khi triệt phá thay đổi nền nhĩ trái, thường là do các đường triệt phá không hoàn toàn. Vì vậy, đối với bệnh nhân có AF kéo dài, triệt phá các vòng (rotors), hoặc dàn đều nói chúng các đường tổn thương hoặc triệt phá bổ xung không dường như được chứng minh là đúng trong thủ thuật đầu tiên. [735,738,739] Tuy nhiên, triệt phá bổ xung cho PVI hoàn chỉnh [716] có thể được xem xét ở những bệnh nhân có AF tái phát sau thủ thuật triệt phá đầu tiên [719, 740,741]. Ở những bệnh nhân được chứng minh cuồng nhĩ phụ thuộc eo (isthmus) nhĩ phải trên nền triệt phá AF, triệt phá eo nhĩ phải được khuyến cáo. Test adenosine để xác định những bệnh nhân cần triệt phá bổ xung vẫn còn nhiều tranh cãi sau khi được đánh giá trong một số báo cáo. [739,742-744] Triệt phá còn gọi là “các vòng” (rotors), được hướng dẫn bằng mapping bề mặt cơ thể hoặc mapping nội tâm mạc, đang được đánh giá và không thể sử dụng lâm sàng phổ cập hiện nay.
11.3.3 Kết quả và các biến chứng
11.3.3.1 Kết quả triệt phá rung nhĩ qua catheter
Kết quả nhịp sau khi triệt phá AF qua catheter AF khó để dự đoán ở từng bệnh nhân. [173,227,713,728] Hầu hết các bệnh nhân đều cần nhiều hơn một thủ thuật để đạt được kiểm soát triệu chứng. [713,726,728] Nói chung, kết quả nhịp tốt hơn và các biến chứng liên quan đến thủ thuật ít hơn có thể được dự kiến ở các bệnh nhân trẻ hơn với bệnh sử AF ngắn và các cơn thường, ngắn không có bệnh tim cấu trúc. [745] Triệt phá qua catheter hiệu quả hơn điều trị thuốc chống loạn nhịp để duy trì nhịp xoang (Hình 2) [746,1039] Nhịp xoang không có các tái phát AF có triệu chứng nặng được xác nhận đến 70% bệnh nhân AF kịch phát, khoảng 50% AF dai dẳng. [713, 728, 735] Tái phát AF rất chậm sau nhiều năm nhịp xoang không phải là hiếm và có thể phản ánh sự tiến triển của bệnh, với những liên can quan trọng cho việc tiếp tục các điều trị AF. [728] Nhiều biến đã được xác định là các yếu tố nguy cơ tái phát sau triệt phá AF bằng catheter, nhưng độ mạnh dự đoán của chúng yếu. Do đó, quyết định triệt phá qua catheter nên dựa trên cơ sở quá trình ra quyết định chia sẻ [747] (xem Chương 8), sau khi giải thích kỹ lưỡng về những lợi ích tiềm ẩn và rủi ro cũng như các lựa chọn khác như thuốc chống loạn nhịp hoặc chấp nhận các triệu chứng hiện tại không điều trị kiểm soát nhịp. [175]
11.3.3.2 Các biến chứng của triệt phá rung nhĩ qua catheter
Có sự cần thiết rõ ràng để nắm được một cách có hệ thống các biến chứng trong thực hành lâm sàng để cải thiện chất lượng các thủ thuật triệt phá AF. [175] Độ dài trung bình của thời gian nằm viện ở bệnh nhân AF trải qua triệt phá lần đầu của họ như một phần của Chương trình Nghiên cứu Quan sát Châu Âu ( EURObservation Research Program: EORP) là 3 ngày (khoảng giữa 2-4 ngày) dựa trên dữ liệu ở 1391 bệnh nhân từ các bệnh viện thực hiện ít nhất 50 lần triệt phá mỗi năm. Từ năm đến bảy phần trăm bệnh nhân sẽ bị biến chứng nghiêm trọng sau triệt phá qua catheter, và 2-3% sẽ gặp các biến chứng đe dọa đến mạng sống nhưng thường có thể điều trị được. [727,748-750] Tử vong trong thủ thuật đã được báo cáo nhưng hiếm gặp (<0,2% ). [751] Các biến chứng nghiêm trọng nhất là đột quỵ / TIA (<1%), tamponade tim (1-2%), hẹp tĩnh mạch phổi và tổn thương thực quản nghiêm trọng dẫn đến các lỗ thông thực quản nhĩ vài tuần sau triệt phá (Bảng 18). ‘Đột quỵ im lặng’ (tức là các tổn thương chất trắng phát hiện được bằng MRI não) đã được quan sát thấy ở khoảng 10% bệnh nhân điều trị bằng triệt phá bằng tần số radio qua catheter và bóng lạnh. [752] Các biến chứng sau thủ thuật bao gồm đột quỵ có nguy cơ cao nhất trong tuần đầu tiên, [753] tamponade màng ngoài tim vài ngày sau triệt phá qua catheter[751] và rò thực quản, thường trở thành rõ ràng sau 7-30 ngày sau triệt phá. Phát hiện kịp thời các lỗ rò thực quản có thể cứu mạng sống và nên dựa trên bộ ba đặc trưng của nhiễm trùng nhưng không có ổ rỏ ràng, đau sau xương ức, cũng như đột quỵ hoặc TIA [748].
Bảng 18. Các biến chứng liên quan để triệt phá rung nhĩ qua catheter
|
Tính nghiêm trọng của biến chứng |
Loại biến chứng |
Tỷ lệ 727, 748,750, 754-759 |
|
Biến chứng nguy hiểm đến tính mạng |
Tử vong quanh thủ thuật |
<0.2% |
|
Tổn thương thực quản (thủng/rò)a |
<0.5% |
|
|
Đột quỵ quanh thủ thuật (gồm TIA/tắc khí) |
< 1% |
|
|
Tamponade tim |
1–2% |
|
|
Biến chứng nặng |
Hẹp động mạch phổi |
<1% |
|
Liệt dây thần kinh hoành kéo dài |
1–2% |
|
|
Biến chứng mạch máu |
2-4% |
|
|
Các biến chứng nặng khác |
≈1% |
|
|
Các biến chứng trung bình hoặc nhẹ |
1–2% |
|
|
Tầm quan trọng còn chưa rõ |
Tắc mạch não không triệu chứng (đột quỵ im lặng)b |
5-20% |
|
|
Nhiễm xạ |
|
TIA: đột quỵ tạm thời.
aRò thực quản nên được nghi ngờ ở các bệnh nhân có biểu hiện với bộ ba của nhiễu trùng không đặc hiệu, đau ngực, đột quỵ hoặc TIA trong những tuần đầu tiên sau thủ thuật triệt phá. Nó đòi hỏi điều trị ngay lập tức.
b<10% cho triệt phá bóng lạnh hoặc tần số radio, >20% cho triệt phá bằng tần số radio theo giai đoạn.
11.3.4 Kháng đông: trước, trong và sau triệt phá
Bệnh nhân được kháng đông với VKAs nên tiếp tục điều trị trong thời gian triệt phá. (với INR 2-3) [760]Thuốc kháng đông với NOACs là một sự thay thế cho warfarin [478,761-765] Không có dấu hiệu không an toàn từ các nhóm nghiên cứu quan sát được điều trị với NOAC không bị gián đoạn trải qua triệt phá qua catheter ở các trung tâm có kinh nghiệm. [761,763,766,767] Nghiên cứu đối chứng đầu tiên so sánh điều trị NOAC và VKA tiếp tục ở các bệnh nhân triệt phá AF, liên quan đến khoảng 200 bệnh nhân, gần đây đã được công bố, [768] cũng như một số bộ số liệu quan sát [761,769,770]. So sánh VKA với NOAC không bị gián đoạn ở những bệnh nhân triệt phá AF (ví dụ: AXAFA – AFNET 5 (Thuốc kháng đông máu sử dụng các chất ức chế trực tiếp Xa apixaban trong triệt phá AF qua catheter: So sánh điều trị kháng vitamin K, NCT02227550) và RE-CIRCUIT (Đánh giá Ngẫu nhiên dabigatran etexilate So với warfarin trong triệt phá tĩnh mạch phổi: đánh giá các Chiến lược kháng đông khác biệt quanh thủ thuật; NCT02348723)]. Trong quá trình triệt phá, heparin nên được cho để duy trì thời gian cục máu hoạt hóa > 300 giây. Kháng đông máu nên được duy trì trong ít nhất 8 tuần sau khi triệt phá cho tất cả các bệnh nhân. Tỉ lệ thực sự của các biến cố huyết khối tắc nghẽn mạch sau khi triệt phá qua catheter chưa bao giờ được nghiên cứu một cách có hệ thống và nguy cơ đột quỵ được nghi ngờ đã được chọn từ các thuần tập không phải triệt phá AF. Mặc dù các nghiên cứu quan sát gợi ý tỷ lệ đột quỵ tương đối thấp trong vài năm đầu tiên sau triệt phá AF qua catheter, [737,771-776] nguy cơ lâu dài tái phát AF và độ an toàn của thuốc kháng đông ở bệnh nhân đã được triệt phá cần được xem xét. Nếu không có dữ liệu thử nghiệm có đối chứng, OAC sau triệt phá qua catheter nên theo các khuyến cáo kháng đông nói chung, bất kể kết quả nhịp được giả định.
11.3.5 Triệt phá rung nhĩ ở các bệnh nhân suy tim
Triệt phá qua catheter, so với điều trị amiodarone, làm giảm đáng kể AF tái phát ở những bệnh nhân AF với HFrEF [777] Những bệnh nhân được chọn lọc với HFrEF và AF có thể đạt được hồi phục chức năng tâm thu sau triệt phá qua catheter (có thể phản ánh bệnh cơ tim do nhịp nhanh). Một số thử nghiệm nhỏ hơn cho thấy chức năng LV cải thiện sau khi triệt phá qua catheter ở bệnh nhân HFrEF [185,226-228,778,779] và giảm tỷ lệ nhập viện, [720,777] đặc biệt ở những bệnh nhân không nhồi máu cơ tim trước. [780] Các thử nghiệm lớn hơn cần bảo đảm để khẳng định những phát hiện này. Triệt phá qua catheter có thể đòi hỏi ở những bệnh nhân này. Do đó, các chỉ định triệt phá qua catheter ở bệnh nhân HFrEF cần được cân bằng cẩn thận, cũng như các thủ thuật được thực hiện ở các trung tâm có kinh nghiệm.
11.3.6 Theo dõi sau triệt phá qua catheter
Bệnh nhân và bác sĩ tham gia vào quá trình theo dõi sau triệt phá qua catheter phải biết các dấu hiệu và triệu chứng của các biến chứng muộn để cho phép điều trị nhanh chóng (Bảng 18). Bệnh nhân cũng nên lưu ý AF tái phát có triệu chứng và không triệu chứng thường xuyên sau triệt phá qua catheter.[119, 781, 782]Tương tự với mục tiêu chính của điều trị kiểm soát nhịp, các cơn không triệu chứng thường không khởi động điều trị kiểm soát nhịp tiếp theo trong chăm sóc thông thường. Bệnh nhân nên được bác sỹ chuyên khoa nhịp khám ít nhất một lần trong 12 tháng đầu tiên sau triệt phá. Các lựa chọn kiểm soát nhịp khác cần được xem xét ở những bệnh nhân tái phát có triệu chứng, bao gồm cả thảo luận trong Nhóm Tim (Hình 17, Hình 19).
11.4 Ngoại khoa rung nhĩ
11.4.1 Phẫu thuật rung nhĩ đồng thời
Thủ thuật tạo các đường rối Cox đã được thực hiện cách đây 30 năm như là một kỹ thuật “cắt và may”, bao gồm cô lập tâm nhĩ trái phía sau, kết nối với vòng van hai lá phía sau, kết nối tĩnh mạch chủ trên van ba lá, kết nối tĩnh mạch chủ trên dưới, cũng như loại bỏ tiểu nhĩ trái (LAA) (Hình 18) [783] Qua đó, thủ thuật tạo các đường rối Cox tạo ra các đường rối điện học của các đoạn xung nút xoang tìm đường đến nút nhĩ thất trong khi ngăn chặn các dẫn truyền rung. Thủ thuật tạo đường rối Cox và các hình thức phẫu thuật AF khác thường đơn giản hơn, chủ yếu được sử dụng ở những bệnh nhân trải qua các phẫu thuật tim mở khác. [461,466,784-798] Trong một tổng quan hệ thống được thực hiện theo các hướng dẫn này, việc thực hiện phẫu thuật AF đã đạt được thoát khỏi AF tăng lên (RR 1,94, 95% CI 1,51-2,49, n = 554 từ 7 RCTs) (Hình 3) [1040] Bệnh nhân trải qua thủ thuật tạo đường rối Cox đòi hỏi phải cấy máy tạo nhịp thường xuyên hơn (RR 1.69, 95% CI 1.12-2.54, n = 1631 từ 17 RCTs), không có sự khác biệt có thể nhận thấy ở các kết cục hoặc biến chứng khác. Các kết quả này được củng cố bằng các phân tích cơ sở dữ liệu của Hiệp hội Bác sỹ ngoại khoa Lồng ngực gồm 67389 bệnh nhân AF đã trải qua phẫu thuật tim hở: tử suất hoặc bệnh suất chủ yếu đã không bị ảnh hưởng do ngoại khoa AF đồng thời .(OR điều chỉnh 1,00, KTC 95% 0,83-1,20) nhưng cấy máy tạo nhịp tim thường xuyên hơn (OR điều chỉnh 1,26, KTC 95% 1,07-1,49). [799] Các dự báo AF tài phát sau ngoại khoa gồm giãn nhĩ trái, lớn tuổi, bệnh sử AF > 10 năm và AF không phải kịch phát. [800-804]. Về loại AF, PVI phẫu thuật dường như có hiệu quả trong AF kịch phát. [805] Các mô hình tổn thương hai nhĩ có thể ảnh hưởng nhiều hơn trong AF dai dẳng và dai dẳng kéo dài. [797,803,806] Việc điều chỉnh các bệnh nhân có AF liên quan đến triệu chứng trải qua phẫu thuật tim được trình bày ở Hình 19, với sự đóng góp quan trọng của Đội Tim AF để tư vấn và Thông báo sự lựa chọn của bệnh nhân.
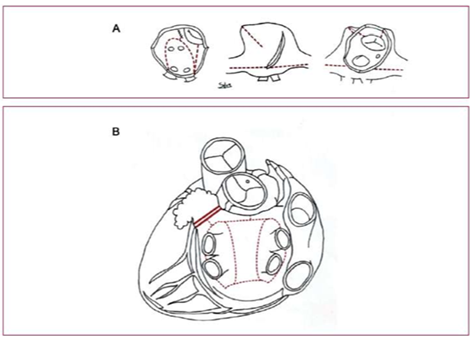
Hình 18. A: Nhóm thương tổn phẫu thuật cho thủ thuật tạo đường rối Cox. Quan sát của bác sỹ phẫu thuật cho thấy tổn thương nhĩ trái (hinh bên trái) và tổn thương nhĩ phải (giữa và bên phải). B: Các tổn thương ở tâm nhĩ trái trong thủ thuật phẫu thuật xâm lấn tối thiểu (đường không liên tục), bao gồm cả loại bỏ tiểu nhĩ trái (đường đôi).
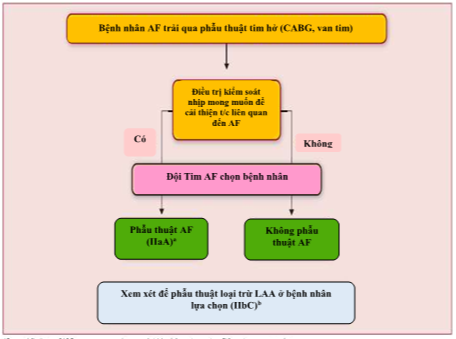
Hình 19.Kiểm soát nhịp bằng phẫu thuật ở các bệnh nhân rung nhĩ trải qua ngoại khoa tim.
AF: rung nhĩ. CABG: bác cầu động mạch vành tự thân. LAA: tiểu nhĩ trái. PVI: cô lập các tĩnh mạch phổi.
aPhẫu thuật AF có thể PVI trong AF kịch phát và tạo rối hai nhĩ trong AF dai dẳng hoặc dai dẳng kéo dài.
bKháng đông uống nên được tiếp tục ở các bệnh nhân có nguy cơ đột quỵ không phân biệt phẫu thuật AF hoặc loại bỏ LAA.
11.4.2 Phẫu thuật kiểm soát nhịp đơn thuần
Công nghệ hiện tại (ví dụ: tần số radio lưỡng cực hoặc nhiệt lạnh) làm cho thủ thuật tạo đường rối Cox dễ dàng hơn, có thể làm được và nhiều hơn, thông qua mở lồng ngực tối thiều. [786,807,808] PVI qua nội soi lồng ngực với tần số radio lưỡng cực ngăn chặn tái phát AF kịch phát (69-91% không bị loạn nhịp trong 1 năm, xem nhóm tổn thương Hình 18B), [468,809,810] và dường như có hiệu quả ở những bệnh nhân trơ với triệt phá qua catheter. [811] Thời gian trung bình nằm viện để triệt phá qua nội soi lồng ngực thay đổi từ 3,6 đến 6,0 ngày [468,812,813]. Nghiên cứu FAST ((Atrial Fibrillation Catheter Ablation vs. Surgical Ablation Treatment), và một nghiên cứu nhỏ khác [814] đã gợi ý phẫu thuật AF qua nội soi lồng ngực có thể hiệu quả hơn triệt phá qua catheter để duy trì nhịp xoang, [468.814] trong khi cũng gây ra nhiều biến chứng hơn (Bảng 19)[815]. Để cải thiện kết quả, các tổn thương rộng hơn đã được thực hiện, bao gồm các đường nối giữa PVI (“tổn thương hình hộp”) và các đường hướng đến vòng hai lá. [812,819-822] Để cải thiện hình thành các tổn thương xuyên thành. [812,823-825] Mặc dù kinh nghiệm ban đầu với triệt phá hỗn hợp cùng một lúc cho thấy sự hứa hẹn, thời gian thủ thuật và tần số biến chứng chảy máu cao hơn[812,823]
Bảng 19.Các biến chứng của phẫu thuật rung nhĩ qua nội soi lồng ngực
|
Biến chứng |
Tần số 468, 815, 822, 826 |
|
Chuyển sang mở xương ức |
0 – 1.6% |
|
Cấy máy tạo nhịp |
0 – 3.3% |
|
Dẫn lưu khí màng phổi |
0 – 3.3% |
|
Tamponade màng ngoài tim |
0 – 6,0% |
|
Đột quỵ thiếu máu cục bộ tạm thời (TIA)a |
0 – 3.0% |
aTần số tắc mạch não không triệu chứng còn chưa rõ.
11.5 Chọn kiểm soát nhịp sau điều trị thất bại
Không có đủ bằng chứng để củng cố các khuyến cáo rõ ràng về cách điều trị bệnh nhân AF tái phát sau triệt phá qua catheter. Tái phát AF sớm hoặc nhịp nhanh nhĩ sau triệt phá (xảy ra trong vòng 8 tuần) có thể được điều trị bằng chuyển nhịp. Nhiều loạt các bệnh nhân trải qua triệt phá AF gồm những người điều trị thuốc chống loạn nhịp thất bại. Vì vậy, xem xét điều trị bằng triệt phá ở bệnh nhân tái phát có triệu chứng trên nền điều trị thuốc chống loạn nhịp thường phù hợp. Ngoài ra, thử nghiệm một loại thuốc chống loạn nhịp khác cũng có thể được xem xét. Kết hợp thuốc chống loạn nhịp với triệt phá (‘điều trị hỗn hợp’, xem Chương 12) cần được xem xét dựa trên những tác động có thể và hiệp lực của những thuốc này với việc triệt phá AF, có thể đem lại lợi ích cho bệnh nhân, ở họ trước đây điều trị đơn độc không có hiệu quả. Kiểm soát tần số không kiểm soát nhịp, triệt phá ngoại khoa, hoặc triệt phá qua catheter lại cũng nên được xem xét (Hình 20). Sự ưu tiên của bệnh nhân và việc tiếp cận điều trị ở địa phương là những cân nhắc quan trọng để thông tin lựa chọn điều trị ở các bệnh nhân cần điều trị kiểm soát nhịp tiếp theo sau điều trị khởi đầu thất bại.
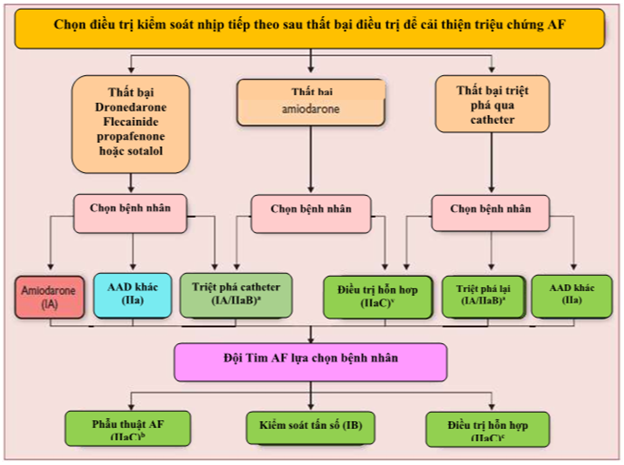
Hình 20.Lựa chọn điều trị kiểm soát nhịp sau điều trị thất bại
AF: rung nhĩ. AAD: các thuốc chống loại nhịp.
aTriệt phá qua catheter nên đạt đích PVI. IA cho AF kịch phát, IIaB cho AF dai dẳng hoặc dai dẳng kéo dài.
bPhẫu thuật AF có thể PVI (như trong AF kịch phát) hoặc phẫu thuật tạo rối (như trong điều trị AF trơ với điều trị hoặc AF dai dẳng hoặc dai dẳng kéo dài).
cĐiều trị hỗn hợp liên quan đến phối hợp các thuốc chống loạn nhịp, triệt phá qua catheter, và/hoặc phẫu thuật AF.
11.6 Đội Tim Rung nhĩ
Theo tính phức tạp của các lựa chọn điều trị khác nhau ở những bệnh nhân điều trị kiểm soát nhịp thất bại vẫn đòi hỏi hoặc yêu cầu điều trị kiểm soát nhịp tiếp theo, Nhóm Công tác này đề nghị các quyết định liên quan đến phẫu thuật AF hoặc triệt phá AF mở rộng nên dựa trên cơ sở hướng dẫn từ Đội Tim AF. Điều này cũng sẽ áp dụng cho việc thay đổi sang chiến lược kiểm soát tần số ở những bệnh nhân AF có các triệu chứng nghiêm trọng (EHRA III hoặc IV). Độ Tim AF gồm có một bác sĩ tim mạch có chuyên môn về trị liệu chống loạn nhịp, bác sĩ điện sinh lý can thiệp và một bác sĩ phẫu thuật tim có kinh nghiệm trong việc lựa chọn bệnh nhân phù hợp, các kỹ thuật và công nghệ cho phẫu thuật triệt phá AF (hình 20). Các Đội Tim AF như vậy – cũng như một cơ sở hợp tác để hỗ trợ tiếp tục tương tác giữa các bác sĩ chăm sóc liên tục, bác sĩ tim mạch AF, các nhà điện sinh lý can thiệp và cả các bác sỹ phẫu thuật AF – nên được thiết lập để cung cấp hướng dẫn tối ưu và cuối cùng cải thiện kết quả nhịp cho bệnh nhân cần can thiệp kiểm soát nhịp phức tạp.
Các khuyến cáo triệt phá rung nhĩ qua catheter và ngoại khoa rung nhĩ. (KC 3)
|
Các khuyến cáo |
Classa |
Levelb |
Refc |
|
|
Triệt phá AF kịch phát có triệu chứng qua catheter được khuyến cáo để cải thiện triệu chứng AF ở các bệnh nhân tái phát AF có triệu chứng đang dùng các thuốc chống loạn nhịp. (amiodarone, dronedarone, flecainide, propafenone, sotalol) và ở người thích kiểm soát nhịp tiếp theo, khi được các nhà điện sinh lý được huấn luyện phù hợp thực hiện và thực hiện thủ thuật ở các trung tâm có kinh nghiệm. |
I |
A |
585-587,713, 727 |
|
|
Triệt phá cuồng nhĩ thông thường nên được xem xét để ngăn ngừa cuồng nhĩ tái phát như một phần thủ thuật triệt phá AF nếu được chứng minh bằng tư liệu hoặc xảy ra trong quá trình triệt phá AF. |
IIa |
B |
827 |
|
|
Triệt phá AF qua catheter nên được xem xét như điều trị hàng đầu đề ngăn ngừa AF tái phát và cải thiện triệu chứng ở các bệnh nhân không lựa chọn có AF tái phát có triệu chứng như sự thay thế điều trị thuốc chống loạn nhịp, xem xét lựa chọn bệnh nhân, lợi ích và nguy cơ. |
IIa |
B |
585 |
|
|
Tất cả các bệnh nhân nên uống thuốc kháng đông ít nhất 8 tuần sau khi triệt phá qua catheter (IIaB) hoặc triệt phá phẫu thuật (IIaC). |
IIa |
B |
C |
727 |
|
Kháng đông ngăn ngừa đột quỵ nên được tiếp tục vô thời hạn sau triệt phá AF qua catheter hoặc phẫu thuật thành công ở các bệnh nhân có nguy cơ đột quỵ cao. |
IIa |
C |
|
|
|
Khi triệt phá AF qua catheter được lên kế hoạch, tiếp tục uống kháng đông VKA (IIaB) hoặc NOAC (IIaC) nên được xem xét trong quá trình thủ thuật, duy trì hiệu quả kháng đông. |
IIa |
B |
C |
760, 768 |
|
Triệt phá qua catheter nên nhằm mục tiêu cô lập tĩnh mạch phổi sử dụng triệt phá qua catheter bằng tần số radio hoặc bóng nhiệt lạnh. |
IIa |
B |
585, 715, 716, 734, 735 |
|
|
Triệt phá AF nên được xem xét ở các bệnh nhân AF có triệu chứng và suy tim có phân suất tống máu giảm để cải thiện triệu chứng và chức năng tim khi bệnh cơ tim do nhịp nhanh được nghi ngờ. |
IIa |
C |
185, 226-228, 720, 777-779, 828 |
|
|
Triệt phá AF nên được xem như là một chiến lược để tránh cấy máy tạo nhịp tim ở những bệnh nhân có nhịp tim chậm liên quan đến AF. |
IIa |
C |
829, 830 |
|
|
Triệt phá qua catheter hoặc phẫu thuật nên được xem xét ở các bệnh nhân có AF dai dẳng hoặc dai dẳng kéo dài có triệt chứng trơ với điều trị AAD để cải thiện triệu chứng, lựa chọn bệnh nhân, lợi ích và nguy cơ, được Đội Tim AF hỗ trợ. |
IIa |
C |
468, 735, 777, 831, 832, 1040 |
|
|
Phẫu thuật cô lập tĩnh mạch phổi thượng tâm mạc xâm lấn tối thiểu nên được xem xét ở các bệnh nhân có AF có triệu chứng khi triệt phá qua catheter đã thất bại. Các quyết định ở các bệnh nhân như vầy nên được Đội Tim AF hỗ trợ. |
IIa |
B |
468 812, 819, 823 |
|
|
Phẫu thuật tạo rối, có thể thông qua một phương pháp xâm lấn tối thiểu, được nhân viên được huấn luyện đầy đủ thực hiện ở một trung tâm có kinh nghiệm, nên được Đội Tim AF xem xét như là một lựa chọn điều trị cho bệnh nhân AF có triệu chứng trơ dai dẳng hoặc sau triệt phá AF để cải thiện triệu chứng. |
IIa |
C |
808, 832 |
|
|
Phẫu thuật tạo rối, cả hai nhĩ tốt hơn, nên được xem xét ở bệnh nhân trải qua phẫu thuật tim để cải thiện các triệu chứng do AF, cân bằng nguy cơ gia tăng của thủ thuật và lợi ích của điều trị kiểm soát nhịp. |
IIa |
A |
461, 466, 790, 791, 796, 797 |
|
|
Phẫu thuật tạo rối, cả hai nhĩ tốt hơn, nên được xem xét ở bệnh nhân trải qua phẫu thuật tim để cải thiện các triệu chứng do AF, cân bằng nguy cơ gia tăng của thủ thuật và lợi ích của điều trị kiểm soát nhịp. |
IIa |
A |
461, 466, 790, 791, 796, 797 |
|
|
Tạo rối đồng thời hai nhĩ hoặc cô lập tĩnh mạch phổi có thể được xem xét ở các bệnh nhân AF không triệu chứng trải qua phẫu thuật tim. |
IIb |
C |
796, 797, 833 |
|
AF: rung nhĩ; NOAC: kháng đông uống không phải kháng vitamin K; VKA: kháng vitamin K.
aClass các khuyến cáo.
bMức độ bằng chứng.
cTài liệu ủng hộ khuyến cáo.
(Còn nữa…)







