Nguyễn Thanh Hiền, Trần Nguyễn Thu Thủy*
*Khoa TM can thiệp, BV Nhân dân 115
Ngững chữ viết tắt:
-BN: bệnh nhân; ĐT: điều trị; GLUT: Glucose Transporter ; ĐTĐ2: đái tháo đường type 2; MACE: biến cố tim mạch chính; NC: nghiên cứu; SGLT2i: Sodium–glucose co-transporter 2 inhibitors; SGLT1: Sodium–glucose co-transporter 1; PXTM: phân xuất tống máu; ST: suy tim; TM: tim mạch; TN: Thử nghiệm; TV: tử vong
Nhóm thuốc SGLT2 ban đầu được dự định là một phương pháp ĐT hỗ trợ cho bệnh ĐTĐ2, nhưng đến thời điểm hiện tại nhóm thuốc này đã trở thành một trụ cột không ngờ của phác đồ ĐT ST. Trong vài năm gần đây, giới y học đã chứng kiến sự gia tăng chóng mặt của nhóm thuốc này, bắt đầu với kết quả tình cờ của các TN đánh giá mức độ an toàn của liệu pháp ĐT tăng cường đường huyết ở những BN TM và đỉnh điểm là việc chứng minh giảm tỷ lệ nhập viện vì ST và TM, và giảm tỷ lệ TV trong quần thể ST chuyên biệt. Lợi ích trên ĐT ST tim của SGLT2i không phụ thuộc vào tình trạng đường huyết của BN, nhưng các cơ chế bảo vệ TM nổi bật vẫn là một chủ đề của các cuộc tranh luận và nghiên cứu khoa học đang diễn ra. Các bác sĩ TM cũng như các bác sĩ lâm sàng khác nên làm quen với các chỉ định, lợi ích của nhóm thuốc này và việc cân nhắc sử dụng thuốc trên lâm sàng. Trong bài viết này, chúng tôi sẽ thảo luận về những lợi ích của SGLT2i trong ĐT ST rút ra từ các kết quả TN lâm sàng ngẫu nhiên lớn, đến các cơ chế tác dụng tiềm tàng của nhóm thuốc này, và ứng dụng ĐT hiện nay (1).
- CƠ CHẾ SINH LÝ CỦA SGLT
Màng tế bào được cấu tạo phần lớn từ phospholipid và không cho phép thấm qua các phân tử lớn, phân cực như glucose. Do đó, vận chuyển glucose qua màng tế bào cần có các protein vận chuyển màng chuyên biệt. Có hai loại chất vận chuyển glucose ở màng tế bào người: chất vận chuyển có điều kiện (GLUT), và chất vận chuyển tích cực (SGLT). Vận chuyển glucose qua SGLT xảy ra bằng cách vận chuyển tích cực, quá trình bao gồm hấp thụ glucose dựa vào chênh lệch (gradien) nồng độ của nó bằng cách sử dụng năng lượng được cung cấp bởi gradien natri qua màng, được duy trì bởi Na + / K + ATPase. Có 12 thành viên của họ SGLT ở người, với hai thành viên tham gia vào quá trình hấp thụ glucose ở thận. SGLT đầu tiên được phát hiện, được chỉ định là SGLT-1, được nhân bản từ các tế bào ruột của người vào năm 1987 và sau đó được phát hiện trong một số mô khác bao gồm thận, tim, khí quản và tuyến tiền liệt. SGLT-2, hầu như chỉ được tìm thấy trong thận, được đặc trưng hóa vài năm sau đó. SGLT-2 là chất vận chuyển dung lượng cao có ái lực thấp nằm trong biểu mô của đoạn 1 của ống lượn gần và chịu trách nhiệm cho khoảng 90% tái hấp thu glucose đã lọc. Khoảng 10% tải lượng lọc còn lại được tái hấp thu bởi SGLT-1, một chất vận chuyển có ái lực cao-năng suất thấp nằm ở đoạn 2 của ống lượn gần và đoạn 3 của ống thẳng gần. Tuy nhiên, nếu phong tỏa hoàn toàn dược lực học của SGLT-2 sẽ chỉ dẫn đến bài tiết từ 50-60% glucose đã lọc do sự điều tiết ngược dòng của SGLT-1.
Sự vận chuyển Glucose từ dịch lọc cầu thận qua tế bào biểu mô ống thận và vào máu được minh hoạ trong hình 1. Một khi có sự vận chuyển tích cực nhờ vào SGLT2 dẫn đến glucose hấp thu qua màng vào tế bào biểu mô, glucose sau đó được vận chuyển đến các tiểu mao mạch cầu thận nhờ vào chất vận chuyển glucose mặt dưới bên tế bào biểu mô ống thận – GLUT1, cùng có trong tế bào có SGLT1; và GLUT2, có trong tế bào có SGLT2 (2,3).
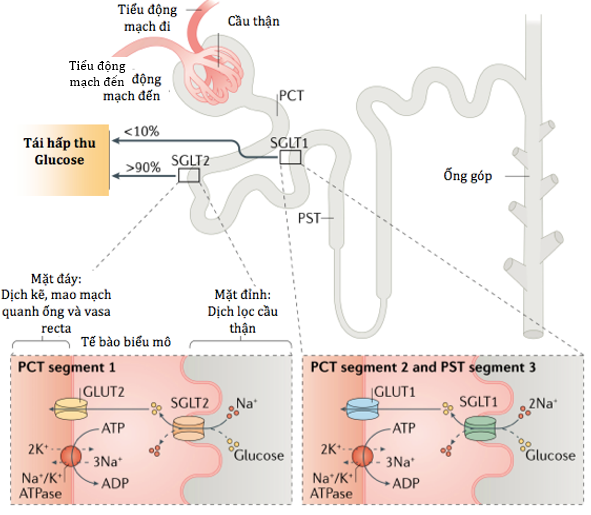
Hình 1: Tái hấp thu glucose ở thận.Phần lớn (>90%) glucose được tái hấp thu nhờ chất đồng vận chuyển natri – glucose 2 (SGLT2) trong đoạn 1 của ống lượn gần (OLG) trong khi phần còn lại (<10%) được tái hấp thu ở đoạn 2 của OLG và đoạn 3 của ống thẳng gần (OTG). Một khi sự vận chuyển tích cực qua SGLT dẫn đến sự hấp thu glucose qua màng đỉ vào tế bào biểu mô, sau đó quá trình vận chuyển glucose đến tiểu mao mạch cầu thận xảy ra thông qua các chất vận chuyển glucose được tạo thuận lợi nhờ GLUT1, xảy ra cùng trong tế bào có SGLT1; và GLUT2, trong tế bào có SGLT2 (3).
- LỢI ÍCH TRÊN SUY TIM ĐƯỢC THẤY TRONG CÁC THỬ NGHIỆM TIM MẠCH
TN SGLT2i trên kết quả TM đầu tiên là NC EMPA-REG OUTCOME (Empagliflozin, kết cục tim mạch và tử vong trên bệnh nhân đái tháo đường (ĐTĐ) típ 2) vào năm 2015, thu nhận 7020 BN mắc ĐTĐ típ 2 và có bệnh TM. Mặc dù mục tiêu chính là chỉ khảo sát độ an toàn của Empagliflozin đối với TM, TN đã bất ngờ chứng minh được giảm 14% biến cố TM chính (MACE: TV do mọi nguyên nhân, TV TM, nhồi máu cơ tim không TV và đột quị), giảm 38% tỷ lệ TV do tim mạch, giảm 32% tử vong do mọi nguyên nhân và giảm 32% nhập viện vì ST. Có được kết quả đáng chú ý này, các nhà NC đã tiến hành đánh giá sau khi ghi nhận Empagliflozin làm giảm các biến cố TM một cách đáng kể bất kể BN từng được chẩn đoán lâm sàng ST (bao gồm ST PXTM bảo tồn hay giảm), BN có nguy cơ ST, hoặc BN có yếu tố nguy cơ tim mạch (4,5).
Kết quả này được tiếp nối với NC CANVAS (NC đánh giá TM trên thuốc Canagliflozin) tiến hành vào năm 2017, thu nhận 10.142 BN mắc ĐTĐ típ 2 có các yếu tố nguy cơ hoặc có bệnh TM đã biết. Tương tự như EMPA-REG OUTCOME, NC CANVAS cho thấy giảm 14% MACE. Lợi ích TM được ghi nhân trên khoảng 14% BN có tiền sử ST với PXTM giảm hoặc bảo tồn. Hơn nữa, trong số những BN có tiền sử ST, NC cũng cho thấy có giảm TV do TM và giảm nhập viện do ST (6).
Một NC khác được công bố vào năm 2019, DECLARE – TIMI 58 (ảnh hưởng của Dapagliflozin đối với các biến cố TM– tiêu sợi huyết trong nhồi máu cơ tim) thu nhận 17.160 BN có ĐTĐ típ 2 và có yếu tố nguy cơ bệnh TM, nhưng kết quả cho thấy không giảm biến cố TM chính, có thể do phần lớn BN trong NC không mắc bệnh TM.
Tuy nhiên, một phân tích hậu kỳ đánh giá BN theo tình trạng ST ban đầu cho thấy Dapagliflozin làm giảm nhập viện do ST dù cho BN có ST PXTM giảm, và giảm TV do TM cũng như TV do mọi nguyên nhân trên những BN ST PXTM giảm (7,8).
Một phân tích tổng hợp trên cả 3 NC trên về tác dụng của SGLT2 trên TM cho thấy SGLT2i làm giảm nguy cơ TV do TM hoặc nhập viện vì ST lên đến 23% và mức giảm này không phụ thuộc vào tiền sử ST trước đó (Bảng 1). Một NC tương tự cũng cho thấy sự giảm đáng kể nhập viện do ST ở những BN có chức năng thận xấu. Ghi nhận này hứa hẹn những kết quả khả quan về kết cục ST trên các NC về nhóm SGLT2i ở quần thể BN ST mà chúng ta cần thiết phải NC sâu hơn (9).
- SGLT2i VÀ CÁC THỬ NGHIỆM DÀNH RIÊNG CHO SUY TIM
- Suy tim phân suất tống máu giảm (PSTM)
TN SGLT2i lớn đầu tiên được thiết kế đặc biệt nhằm đánh giá những BN ST PXTM giảm là DAPA-HF (Dapagliflozin và phòng ngừa các kết cục có hại trong suy tim), TN này thu nhận tổng cộng 4744 BN ST có triệu chứng NYHA II – IV và PSTM ≤ 40% (bảng 2). NC này cho thấy giảm 26% kết cục TV cộng dồn do TM, số lần nhập viện do ST và số lần khám cấp cứu vì ST. Điều quan trọng thu được từ NC này cho thấy lợi ích trên TM không phụ thuộc vào tình trạng ĐTĐ2, trong đó dân số NC ĐTĐ2 chỉ chiếm 42%. Ngoài ra, các phân tích hậu kiểm cũng cho thấy lợi ích nhất quán của Dapagliflozin bất kể việc ĐT cơ bản có hay không sử dụng thuốc lợi tiểu, thuốc kháng aldosteron, hoặc valsartan/sacubitril. Các phân tích này chứng minh Dapagliflozin làm giảm tổng số lần nhập viện do ST (lần đầu và tái phát) và việc tăng cường điều trị ST cho BN ngoại trú. Kết quả của DAPA-HF đã đưa đến một chỉ định mới của FDA vào tháng 5/2020 đối với Dapagliflozin để giảm nguy cơ TV do TM và nhập viện do ST ở BN ST PSTM giảm (NYHA II – IV) (10,11).
NC tiếp theo sau đó là thử nghiệm EMPEROR-REDUCED (Thử nghiệm Empagliflozin trên bệnh nhân suy tim mạn tính có giảm PSTM), thu nhận 3730 BN ST có triệu chứng NYHA II-IV và PSTM ≤ 40%. Empagliflozin đã được chứng minh làm giảm 25% TV cộng dồn do TM và nhập viện do ST, mặc dù không cho thấy có mối liên quan có ý nghĩa thống kê riêng lẻ với biến cố TV do TM. Tương tự DAPA-HF, kết quả từ TN EMPEROR-REDUCED không phụ thuộc vào tình trạng ĐTĐ2 của nhóm nghiên cứu. Những BN trong NC được ĐT theo khuyến cáo và không ghi nhận bất cứ tương tác thuốc nào khi sử dụng cùng với kháng Aldosteron. Empagliflozin cũng đã được chứng minh có cải thiện sớm và kéo dài chất lượng cuộc sống khi khảo sát bảng câu hỏi KCCQCSS (Kansas City Cardiomyopathy Questionnaires-Clinical Summary Score), cũng như giảm tổng các biến cố ST trên BN nội và ngoại trú. Tương tự Dapagiflozin, FDA đã chấp thuận cho chỉ định của Empagliflozin trong định điều trị BN ST PSTM giảm (12-14).
Một NC khác đã công bố kết quả là NC SOLOIST-WHF (Ảnh hưởng của Sotagliflozin đối với các biến cố tim mạch ở bệnh nhân ĐTĐ típ 2 có suy tim) nhằm kiểm tra hiệu quả của Sotagliflozin trên BN ĐTĐ2 và ST PSTM giảm hoặc bảo tồn đã ổn định sau khi nhập viện ĐT ST gần đây (15). Mặc dù TN này phải kết thúc sớm do thiếu hụt kinh phí trong hoàn cảnh dịch COVID-19, NC đã thu nhận 1222 BN (trong đó 79% dân số có PSTM < 50%) và đã chứng minh làm giảm 29% biến cố TV cộng dồn do TM, số lần nhập viện và cần khám sớm vì ST, kết quả này có ý nghĩa thống kê đến 28 ngày theo dõi. Hơn nữa, những dữ liệu tổng hợp từ SOLOIST-WHF và SCORED (TN ảnh hưởng của Sotagliflozin đối với các biến cố TM và thận ở BN ĐTĐ típ 2 và BN suy thận trung bình có yếu tố nguy cơ TM) đã được chứng minh giảm 27% tổng TV do TM, số lần nhập viện và khám sớm vì ST, mối liên quan có ý nghĩa thống kê bất kể PSTM giảm hay bảo tồn (16). Một phân tích khác tập trung vào kết quả chung cuộc cũng cho thấy rằng Sotagliflozin làm tăng số ngày sống và tăng tỷ lệ xuất viện (17). Ngoài ra, một số thử nghiệm bổ sung cho SGLT2i trên ST đang được tiến hành được trình bày ở bảng 3 (3).
- Suy tim PSTM bảo tồn
Trong phân tích gộp của NC SOLOIST-WHF và SCORED, Sotagliflozin trở thành thuốc đầu tiên cho thấy lợi ích rõ ràng trên những BN suy tim có PSTM bảo tồn. Tuy nhiên, NC SOLOIST không được thiết kế để đánh giá ST PSTM bảo tồn như là giả thiết ban đầu, và nhóm BN ST PSTM bảo tồn chỉ chiếm 21%. Như vậy việc cần thiết hiện nay là tiến hành một thử nghiệm cho SGLT2i trên nhóm đối tượng ST PSTM bảo tồn (3).
Được công bố vào tháng 8/2021, NC EMPEROR-PRESERVED (Empagliflozin – đánh giá kết quả thử nghiệm trên BN ST mạn với PSTM bảo tồn) thu nhận 5988 BN có PSTM > 40%, NYHA II – IV, và có một đợt nhập viện vì ST trong vòng 12 tháng trước đó. Các điểm cắt của PSTM dao động từ > 40% đến < 50%, ≥ 50% đến < 60%, và ≥ 60%. Sau quá trình theo dõi trung bình 26,2 tháng Empagliflozin chứng minh giảm đáng kể tiêu chí cộng gộp của TV TM và nhập viện vì ST (HR 0,79; KTC 95% 0,69 – 0,90), và giảm tiêu chí nhập viện vì ST đơn thuần (HR 0,71; KTC 95% 0,60 – 0,83). Tuy nhiên Empagliflozin không làm giảm đáng kể nguy cơ TV TM (HR 0,91; KTC 95% 0,76 – 1,09). Những lợi ích của Empagliflozin đã được chứng minh cho thấy không phụ thuộc vào tình trạng đường huyết và PSTM, mặc dù cần lưu ý khả năng mang lại lợi ích rất ít ở những người có PSTM ≥ 60% (18).
NC phân tích gộp EMPEROR – POOLED dựa trên NC EMPEROR-REDUCED và EMPEROR-PRESERVED đánh giá ảnh hưởng của Empagliflozin trên các biến cố chính của thận trong ST, được định nghĩa là sự giảm nặng và không hồi phục của eGFR hoặc cần phải ĐT thay thế thận. NC này đã chứng minh Empagliflozin làm giảm các biến cố chính của thận (2,8% so với 3,5% của giả dược). Tuy nhiên giữa hai thử nghiệm có sự không đồng nhất đáng kể đã được ghi nhận (p= 0,016 đối với tương tác). Cụ thể, tỷ số nguy cơ đối với các biến cố thận chính trong NC EMPEROR-REDUCED là 0,51 (KTC 95% 0,33 – 0,79) so với trong NC EMPEROR-PRESERVED là 0,95 (KTC 95% 0,73 – 1,24), cho thấy lợi ích trên thận chủ yếu xảy ra ở những BN ST PSTM giảm. Vì sinh lý bệnh học của ST PSTM giảm và bảo tồn có khá nhiều điểm khác nhau nên không có gì ngạc nhiên khi tác động qua lại giữa tim và thận giữa hai kiểu hình ST này cũng khác nhau. Cuối cùng, thực tế là nghiên cứu EMPEROR-PRESERVED đã chứng minh có sự chậm lại đáng kể trong mức độ giảm eGFR trung bình hàng năm (-1,25 so với 2,62, với p < 0,001), cho thấy rằng chỉ số eGFR không phải là một đại diện vững chắc trong đánh giá kết cục thận trong dân số BN ST nói chung (19).
Các kết quả từ TN EMPEROR-PRESERVED rất quan trọng đối với các ĐT ít ỏi của ST PSTM bảo tồn. TN lớn tiếp theo đối với SGLT2i trên đối tượng ST PSTM bảo tồn là DELIVER (Đánh giá Dapagliflozin trong việc cải thiện chất lượng cuộc sống của BN ST có PSTM bảo tồn) dự kiến sẽ hoàn thành vào tháng 1/2022 và sẽ công bố trong thời gian tới (3).
- SO SÁNH CÁC THUỐC RIÊNG LẺ TRONG NHÓM SGLT2i
Nếu không có những TN tiến cứu so sánh đối đầu, thật khó để các nhà lâm sàng có thể ngoại suy những điểm tương đồng cũng như khác biệt giữa các thuốc riêng lẻ trong nhóm SGLT2i để xác định tính ưu việt. Các dữ liệu sẵn có cho thấy sự không nhất quán trong hiệu quả giữa các thuốc thuộc cùng nhóm SGLT2i đối với kết cục lâm sàng “khó nhằn” như MACE hay TV do TM, cũng như trên từng tình trạng bệnh, và độ nặng của bệnh. Những khác biệt trong dân số BN NC, thiết kế NC hoặc dược động học của các thuốc có thể là nguyên nhân dẫn đến sự không đồng nhất này. Tuy nhiên, lợi ích nhất quán trên sự giảm nhập viện do ST được chứng minh ở tất cả các NC cũng như các phân tích dưới nhóm. Một phân tích tổng hợp từ 6 TN lâm sàng đã minh chứng cho sự không đồng nhất trên hiệu quả đối với TV TM; và lợi ích nhất quán trong giảm nhập viện do ST giữa 4 thuốc thuộc nhóm SGLT2i (18).
Nghiên cứu DAPA-HF là thử nghiệm lâm sàng duy nhất đến thời điểm này cho thấy lợi ích trên TV trong quần thể ST có PSTM giảm. Những lý do lý giải việc thiếu dữ liệu để đánh giá lợi ích trên TV của NC EMPEROR-REDUCED đã được đề cập. Trong đó, các nhà NC nhấn mạnh rằng, mặc dù cả hai nghiên cứu đều không đủ mạnh để đánh giá TV TM, tỷ lệ TV trong NC EMPEROR-REDUCED thấp hơn một cách đáng kể so với NC DAPA-HF (500 trường hợp TV TM trong DAPA-HF so với 389 trường hợp TV trong EMPEROR-REDUCED). NC EMPEROR-REDUCED thu nhận những BN có PSTM thấp hơn và NT-proBNP cao hơn khi so sánh với TN DAPA-HF (các chỉ số lần lượt là 27,7% với 31,2% và 1887 so với 1428pg/mL). Như vậy, có vẻ đáng ngạc nhiên là một dân số “bệnh nhiều hơn” lại ít bị TV do TM nói chung hơn. Tuy nhiên sự khác biệt này có thể lý giải là do tỷ lệ biến số NC về kết cục lâm sàng của EMPEROR-REDUCED cao hơn, dẫn tới thời gian theo dõi ngắn hơn (16 tháng so với 18,2 tháng), và tỷ lệ TV do TM thấp hơn. Hơn nữa, một phân tích tổng hợp của cả hai NC trên cho thấy sự giảm 14% trong TV TM (HR 0,86; KTC 95% 0,76 – 0,98, p = 0,027) và một kết luận khác có lẽ cũng quan trọng không kém là không chứng minh được sự khác biệt có ý nghĩa trên hiệu quả của hai thuốc sử dụng trong 2 NC trên (18,20).
NC SOLOIST-WHF mở rộng thêm những phát hiện từ hai NC trước là DAPA-HF và EMPEROR-REDUCDE. TN SOLOIST-WHF là NC đầu tiên có thiết lập khảo sát tính an toàn và hiệu quả của việc khởi đầu SGLT2i trên những BN ST cấp đã được ĐT ổn định, hoặc trước đó đã xuất viện, hay vừa xuất viện một thời gian ngắn. Kết cục TV do TM không ghi nhận được từ NC này trong bối cảnh NC bị kết thúc sớm (bởi thiếu hụt kinh phí) với thời gian theo dõi trung bình bị rút ngắn là 9 tháng. Gần đây, TN EMPULS gồm 530 BN với chẩn đoán chính là ST cấp mới hoặc ST mạn mất bù cấp bất kể PXTM được chỉ định ngẫu nhiên dùng Empagliflozin 10 mg 1 lần/ngày hoặc giả dược. Các BN được phân nhóm ngẫu nhiên trong thời gian nằm viện với lâm sàng ổn định (thời gian trung bình từ lúc nhập viện đến khi phân nhóm là 3 ngày) và được ĐT cho đến 90 ngày. Kết cục chính của TN là các lợi ích lâm sàng, được định nghĩa gồm TV do mọi nguyên nhân, số lần ST và thời gian từ lúc ĐT đến biến cố ST đầu tiên, hoặc sự thay đổi với khác biệt từ 5 điểm trở lên so với ban đầu bằng thang điểm “Tổng điểm triệu chứng bệnh cơ tim của thành phố Kansas” tại thời điểm sau 90 ngày. Có nhiều BN được điều trị bằng Empagliflozin cho thấy có lợi ích lâm sàng hơn khi so sánh với nhóm dùng giả được (tỷ số chênh 1.36; KTC 95%, 1.09–1.68; P= 0.0054), điều này đáp ứng với tiêu chí chính của nghiên cứu. Các lợi ích lâm sàng được ghi nhận ở cả hai nhóm ST cấp mới và ST mạn mất bù cấp bất kể PXTM, và có hay không có ĐTĐ. Empagliflozin được dung nạp khá tốt; các tác dụng ngoại ý nghiêm trọng được báo cáo ở nhóm dùng Empagliflozin và dùng giả dược lần lượt là 32.3% và 43.6%. Những phát hiện từ NC này chỉ ra rằng việc bắt đầu khởi trị Empagliflozin trên những BN nhập viện vì STcấp được dung nạp khá tốt và mang lại nhiều lợi ích lâm sàng đáng kể sau 90 ngày ĐT (21).
Mặc dù SOLOIST-WHF cung cấp bằng chứng cho thấp SGLT2i có thể làm giảm nhập viện do suy tim ở những bệnh nhân suy tim có PSTM bảo tồn, EMPEROR-PRESERVED lại là thử nghiệm trên đối tượng suy tim PSTM bảo tồn với quy mô lớn cho thấy lợi ích của nhóm thuốc SGLT2i. Chúng ta vẫn còn chờ đợi kết quả từ một nghiên cứu khác, thử nghiệm DELIVER, để có thể đối chiếu và so sánh.
Điều cuối cùng, tính chọn lọc tương đối trên thụ thể SGLT2 của các thuốc trong nhóm không được biểu hiện bằng sự khác biệt về mặt lâm sàng trong các thử nghiệm ngẫu nhiên có đối chứng với quy mô lớn. Empagliflozin cho thấy tỷ lệ chọn lọc giữa SGLT2 so với SGLT1 là 2700, so với Dapagliflozin là 1200, và Sotagliflozin là 20 (22). Tuy nhiên kết quả từ các nghiên cứu DAPA-HF, EMPEROR-REDUCED và SOLOIST-WHF có vẻ tương đối khá giống nhau.
- ƯỚC ĐOÁN CÁC CƠ CHẾ TÁC ĐỘNG CỦA THUỐC
Các kết quả không được dự đoán trước chứng minh lợi ích TM của SGLT2i trong các TN lâm sàng đầu tiên của nhóm thuốc này cũng như trong các NC tiếp theo đó đã xác nhận kết quả khả quan trên quần thể BN ST, điều này thúc đẩy một loạt các nghiên cứu về cơ chế tác động của các thuốc này. Nhóm SGLT2i dường như có tác động toàn thân trên nhiều phân tử và hệ thống sinh lý qua trung gian độc lập với hoạt động chống tăng đường huyết (23). Phần này chúng ta sẽ cùng nhìn lại toàn cảnh các ước đoán cơ chế tác động của thuốc, được phân chia dựa trên có lợi ích trực tiếp hay gián tiếp lên cơ tim (hình 2).
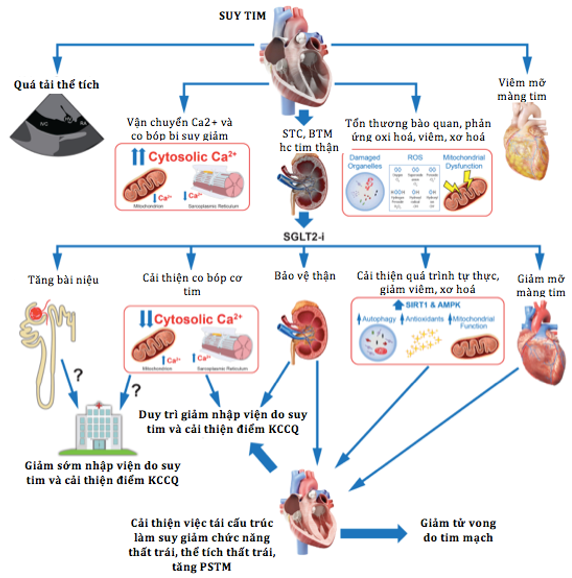
Hình 2. Các cơ chế đề xuất trên tác dụng lợi ích của SGLT2 đối với ST. Rất nhiều cơ chế có lợi của SGLT2i trong ST đã được công nhận, bao gồm tăng bài niệu, cải thiện khả năng vận chuyển Ca2+, bảo vệ trục tim thận, và giảm viêm trong nhiều con đường, bao gồm cả những cơ chế phát sinh từ mỡ màng tim. Các cơ chế giảm sớm nhập viện do ST, và cải thiện điểm số bệnh cơ tim của thành phố Kansas (KCCQ) vẫn còn chưa được biết rõ, nhưng có thể có liên quan đến việc tăng cường bài niệu và cải thiện sự co bóp cơ tim. Các dữ liệu về hình ảnh học đã chứng minh khả năng tu sửa tích cực trong tái cấu trúc dài hạn, điều này có thể được giải thích bằng sự suy giảm của các con đường gây viêm và xơ hoá.
(Các chữ viết tắt trong hình: STC – suy thận cấp, BTM – bệnh thận mạn, hc – hội chứng, PSTM – phân suất tống máu)(3)
- Các cơ chế có lợi ích trực tiếp lên cơ tim
- Giảm gánh nặng oxi hoá và tổn thương ty thể, đồng thời cải thiện quá trình tự thực hồng cầu
Đặc điểm nổi bật của nhóm SGLT2i là khả năng làm tăng hồng cầu một cách nhất quán qua các thử nghiệm lâm sàng. Điều thú vị là việc tăng hematocrit được xem như là biến số có mối quan hệ thống kê mạnh nhất với sự giảm số lần nhập viện do ST và TV TM. Tuy nhiên sự tăng khối lượng tế bào hồng cầu thông qua các chất tương tự như erythropoietin không cho thấy lợi ích trên những BN ST mạn, ngay cả trong tình trạng hematocrit thấp. Một giả thuyết cho rằng hematocrit tăng có thể là một dấu ấn sinh học cho các cơ chế tiềm tàng mang lại lợi ích trong ST. SGLT2i gây ra trạng thái thiếu chất dinh dưỡng dẫn đến hoạt động phiên mã của một loạt gen liên quan đến việc thích nghi với tình trạng đói tế bào. Đặc biệt những enzyme hoạt động như cảm biến năng lượng thấp bao gồm sirtuin 1 (SIRT1: sensors include sirtuin 1) và protein kinase kích hoạt adenosine monophosphate (AMPK: adenosine monophosphate-activated proteinkinase). SIRT1 làm giảm gánh nặng oxi hoá bằng cách cải thiệu hoạt động oxi hoá và AMPK bảo vệ chức năng của ty thể. Hơn nữa, SIRT1 và AMPK phát tín hiệu kích thích sự tự thực, đây là một quá trình cần thiết giúp loại bỏ những tế bào của các cơ quan bị tổn thương, như đã biết những tổn thương là nguồn gốc chính của hàng loạt phản ứng oxi hoá và rối loạn chức năng tế bào ở cơ tim (hình 2).
Ngoài việc gây ra trạng thái như bị đói, SGLT2 cũng dẫn đến tình trạng giả thiếu oxi. Cụ thể SIRT1 (được kích hoạt bởi SGLT2) hoạt hoá yếu tố cảm ứng giảm oxy – 2a (HIF-2a: hypoxia-inducible factor-2a), và một thụ thể giảm oxi máu là yếu tố điều chỉnh chính cho quá trình tổng hợp erythropoietin. Kết quả là sự gia tăng hematocrit được chứng minh trong các thử nghiệm lâm sàng của SGLT2i có thể đóng vai trò như một dấu ấn sinh hoá của một chuỗi enzyme phức tạp làm giảm gánh nặng oxi hoá và cải thiện chức năng ty thể (3,24).
- Giảm xơ hoá và cải thiện quá trình tái tạo thất trái
Một số TN lâm sàng liên quan đến SGLT2i, chẳng hạn như NC DAPA-HF, đã chứng minh giảm tỷ lệ TVvới sự cải thiện đường cong sống còn sau nhiều tháng theo dõi. Điều này có thể gợi ý khả năng có sự thúc đẩy quá trình tạo thuật lợi cho tái tạo thất trái về lâu dài, như ở các thuốc chẹn beta, thuốc ƯCTT, ức chế neprilysin và nhóm kháng Aldosteron.
Thật vậy, một số mô hình nghiên cứu SGLT2i trên chuột cho thấy sự giảm xơ hoá cơ tim thông qua biểu hiện của yếu tố tăng trưởng β, collagen típ I và III, matrix metalloproteinase 7, fibronectin 1 cũng như sự điều chỉnh của bộ chuyển đổi tín hiệu và chất kích hoạt tín hiệu phiên mã 3 (STAT3: signal transducer and activator of transcription 3).
Những phát hiện từ các NC trong phòng thí nghiệm này được ủng hộ từ các dữ liệu lâm sàng trong nghiên cứu EMPA-HEART CardioLink-1 (tác dụng của Empagliflozin trên khối lượng thất trái ở những BN có ĐTĐ típ 2 và bệnh mạch vành), đánh giá tác động của Empagliflozin lên việc tái tạo thất trái ở những BN đã có bệnh ĐTĐ2, bệnh mạch vành và PSTM bình thường. Tại thời điểm 6 tháng, Empagliflozin cho thấy chỉ số khối lượng thất trái giảm đáng kể so với giả dược được chứng minh qua hình ảnh cộng hưởng từ tim (-2,6 so với -0,01g/m2; p = 0,01). Cần lưu ý rằng trong NC chỉ có 6% BN có tiền sử ST mạn tính. Gần đây hơn, nghiên cứu EMPA-TROPISM (Liệu lợi ích tim mạch của Empagliflozin có độc lập với tác động giảm đường huyết) đã đánh giá việc tái tạo thất trái của Empagliflozin trên 84 BN không có ĐTĐ, và có ST PSTM giảm. Những BN này ST NYHA II – III và PSTM trung bình 36,5%. Sau 6 tháng theo dõi, Empagliflozin cho thấy có sự giảm đáng kể thể tích thất trái cuối tâm trương và thể tích thất trái cuối tâm thu (các chỉ số lần lượt là -25,1 so với -1,5ml; và -26,2 so với -0,5ml, cả hai so sánh đều có p < 0,001). Ngoài ra, Empagliflozin cho thấy sự cải thiện PSTM, giảm khối lượng thất trái và cải thiện test 6 phút đi bộ (25-27).
- Cải thiện khả năng xử lý canxi của tế bào cơ tim
Tác động quan trọng ngoài mục tiêu chính của SGLT2i có thể liên quan tới ái lực cao của nhóm thuốc này khi liên kết với chất trao đổi Natri – Hydrogen exchanger- 1 (NHE-1) được tìm thấy trong tế bào cơ tim. ST dẫn đến tăng đáp ứng sai của NHE-1, là nguyên nhân gây ra tình trạng quá tải canxi và natri có liên quan đến cơ chế sinh bệnh học của bệnh cơ tim. Việc ức chế NHE-1 làm giảm Na+ và Ca2+ trong tế bào đồng thời làm tăng Ca2+ trong ty thể, chính điều này có thể giúp cho việc cải thiện sự đồng bộ co – bóp của cơ tim, và giảm việc tạo ra các phản ứng oxi hoá của tythể .
Một dấu hiệu phân tử khác của ST là sự điều hoà Ca2+/calmodulin kinase II (CaMKII) dẫn đến tăng rò rỉ Ca2+ từ lưới cơ chất làm rối loạn chức năng co bóp. Empagliflozin đã được chứng minh làm giảm sự rò rỉ Ca2+ qua trung gian CaMKII này từ lưới cơ chất trong tế bào cơ tim của chuột và người. CaMKII cũng có liên quan đến con đường phì đại cơ tim, giãn nỡ và chết tế bào, điều này có thể cung cấp một phương pháp bảo vệ tim khác qua trung gian SGLT2i (3,28,29).
- Cải thiện năng lượng sinh học của tim
Trên tim của một người lớn khoẻ mạnh, hoạt động cơ tim được cung cấp năng lượng chủ yếu dựa vào quá trình oxy hoá axit béo tự do của ty thể. Một mức độ thấp hơn là dựa vào oxy hoá glucose. Ngược lại, ở người ST, phương thức sản xuất năng lượng ưu tiên dựa vào quá trình chuyển hoá ceton. Điều này đã được giả thuyết như là một sự thay đổi mang tính thích ứng do tính hiệu quả của quá trình trao đổi chất bị tăng cường và sự sản xuất năng lượng khi ceton được xem như nguồn dinh dưỡng cơ tim chủ yếu. SGLT2i đã được chứng minh có thể gây ra trạng thái lúc đói với sự gia tăng quá trình oxi hoá axit béo và tạo ceton. Do đó người ta cho rằng SGLT2i làm trung gian cho các tác động có lợi trên TM bằng cách thúc đẩy quá trình tạo năng lượng sinh học hiệu quả hơn. Ngoài ra trên mô hình thí nghiệm ở heo bị ST do thiếu máu cục bộ không ĐTĐ, Empagliflozin làm giảm tái cấu trúc cơ tim bất lợi, cũng như gây ra sự chuyển đổi từ glucose làm chất nền cơ tim thành ceton, axit béo, và axitamin chuỗi nhánh, mặc dù các nhà khoa học đã không chứng minh được liệu sự thay đổi này là nguyên nhân dẫn đến lợi ích TM hay chỉ là một dấu ấn sinh học ngẫu nhiên (3,30).
- Các cơ chế có lợi ích gián tiếp lên cơ tim
- Giảm tình trạng viêm
Ngoài lợi ích kháng viêm trong việc giảm thiểu gánh nặng oxi hoá, SGLT2i đã được chứng minh làm giảm vô số các con đường gây viêm khác ở chuột và người, bao gồm sự giảm hoạt hoá thể viêm NLRP3/ ASC (nucleotide-binding oligomerization domain, leucine rich repeat and pyrin domain containing protein/ apoptosis-associated speck-like protein containing a caspase recruitment domain) , giảm sự lắng đọng của lipid gây độc cho tim, và giảm một loạt các hoạt chất trung gian gây viêm và cytokine bao gồm interleukin 1β, interleukin-6, yếu tố nhân kappa B, yếu tố hoại tử u α và CRP có độ nhạy cao (31,32).
- Giảm tích tụ mỡ vùng nội tâm mạc và những vùng không thuộc nội tâm mạc
Một số SGLT2i đã cho thấy làm giảm lượng mỡ thượng tâm mạc, vùng mô có hoạt tính chuyển hoá chuyên tiết ra các cytokine profibrotic và tiền viêm. Mỡ thượng tâm mạc chia sẻ nguồn cung cấp máu chung với cơ tim và không bị chia cắt với cơ tim bởi màng cơ tim. Do đó mỡ thượng tâm mạc có thể gây ra tác động tiêu cực trực tiếp lên cơ tim qua các chất trung gian tiền viêm. Ngoài ra, SGLT2i đã được chứng minh làm giảm mỡ nội tạng ngoài tâm mạc và mỡ dưới da. Hơn thế, các mô hình thí nghiệm trên chuột đã chỉ ra rằng SGLT2i có thể làm giảm tình trạng viêm qua trung gian mỡ bằng cách giảm tỷ lệ đại thực bào M1 chống viêm, với đại thực bào M2 chống viêm (33,34).
- Tăng cường bài niệu
Một giả thuyết phổ biến liên quan đến cơ chế của SGLT2i trong việc giảm số lần nhập viện do ST tác dụng tăng lợi tiểu thứ phát sau tăng thải glucose niệu và natri niệu. SGLT2i làm tăng tiết nước tiểu 300ml/ngày sau 24 giờ với tác dụng tăng tiết niệu giảm dần sau 12 tuần. Việc tăng natri niệu được xem như là tác dụng cộng hưởng của tương tác giữa SGLT2 và chất trao đổi Natri-Hydro 3 (NHE3) tại ống lượng gần của nephron thận cho kết quả ức chế ngoài mục tiêu NHE3. Một NC cho thấy tác dụng lợi tiểu của SGLT2i có thể còn mạnh hơn khi kết hợp với thuốc lợi tiểu quai. Hơn nữa, sự gia tăng hematocrit được quan sát thấy trong các TN về SGLT2i là biến số mạnh nhất liên quan đến việc giảm nhập viện vì ST và giảm tử vong do TM. Tác dụng lợi tiểu của SGLT2 xuất hiện nhanh chóng, nên việc tăng cường bài niệu này có thể là nguyên nhân giải thích cho giảm tỷ lệ nhập viện vì ST được ghi nhận sớm trong các nghiên cứu DAPA-HF và EMPEROR-REDUCED. Ngoài ra việc cải thiện sớm chất lượng cuộc sống qua khảo sát bảng điểm KCCQ-CSS được quan sát thấy trong NC EMPEROR-REDUCED cũng phù hợp về mặt thời gian với tác động sinh lý này. Những BN ST PSTM bảo tồn thường không đáp ứng với các thuốc điều trị ST mà không có tác dụng lợi tiểu, cũng như tác dụng hỗ trợ trong việc kiểm soát thể tích được xem như là một cơ chế khả dụng để giảm tần số nhập viện vì ST. Các phân tích dưới nhóm về tương tác giữa các thuốc lợi tiểu quai và kháng Aldosteron trong nghiên cứu này cũng sẽ được công bố trong thời gian tới.
Tuy nhiên một số nhà khoa học cũng nên ra vài lập luận chống lại tầm quan trọng của tác dụng bài niệu. Thứ nhất, tác dụng gây bài niệu thoáng qua được gây ra bởi SGLT2i sẽ không phù hợp với việc giảm nhập viện do ST kéo dài được quan sát thấy trong các TN lâm sàng. Thứ hai, mặc dù một số NC nhỏ đã cho thấy tác dụng hiệp đồng bài niệu giữa SGLT2i và nhóm thuốc lợi tiểu quai, tác dụng này không được ghi nhận trong các TN lâm sàng lớn hơn. Hơn nữa, trong một phân tích dưới nhóm của NC DAPA-HF cho thấy không có sự khác biệt về mục tiêu NC chính giữa các phân nhóm lợi tiểu quai, từ nhóm không sử dụng đến các nhóm có sử dụng với các liều tăng dần. Thứ ba, trong thử nghiệm EMPA-RESPONSE-AHF, nghiên cứu Empagliflozin trong quần thể suy tim PSTM giảm đợt mất bù cấp, Empagliflozin thất bại trong việc giảm điểm khó thở, điều này được cho là không nhất quán với một thuốc có hiệu quả trong ST sung huyết. Cuối cùng, các TN đã không chứng minh được sự giảm của NT-proBNP, điều mà đáng ra sẽ được ghi nhận do tác dụng lợi tiểu. Do đó, những bằng chứng chống lại tầm quan trọng của tác dụng lợi tiểu khi sử dụng SGLT2i đáng được NC thêm (3,35, 36).
- Cải thiện trục tim – thận
SGLT2i đã cho thấy một tác dụng nổi bật trên kết cục thận trong các TN lâm sàng. Các cơ chế tiềm năng có lợi cho thận bao gồm giảm áp lực cầu thận, giảm gánh nặng oxi hoá và viêm, điều hoà hệ thần kinh giao cảm. Giữa tim và thân có một tác động qua lại quan trọng, khi có một sự rối loạn chức năng của cơ quan này sẽ dẫn đến rối loạn hoạt động của cơ quan kia. Người ta nhận thấy có một tỷ lệ đáng kể BN ST PSTM giảm bị rối loạn chức năng thận. Tầm quan trọng của trục tim – thận trong ST PSTM giảm có thể được nhấn mạnh bởi bằng chứng cho thấy SGLT2i làm giảm nhập viện do ST nhiều hơn trong nhóm có mức độ chức năng thận xấu hơn. Tuy nhiên kết quả của NC EMPEROR-POOLED cho thấy tác động qua lại giữa tim và thận có thể khác nhau trên bệnh nhân suy tim PSTM bảo tồn (37, 38).
- Ức chế hệ thần kinh giao cảm
Đáp ứng thần kinh giao cảm bất thường và cơ chế của các liệu pháp dược lý được thiết lập để làm giảm đáp ứng thần kinh này đã khiến một số nhà khoa học cho rằng SGLT2i có thể hoạt động theo một khuôn mẫu tương tự. Không có đáp ứng tăng nhịp tim mặc dù có giảm thể tích và huyết áp cho thấy việc ức chế thành công hệ thần kinh giao cảm. Noradrenalin đã được chứng minh làm tăng biểu hiện của SGLT2 trong tế bào thận của người, gợi ý cho việc có sự tương tác giữa SGLT2 với hệ thần kinh giao cảm. Hơn nữa, sử dụng dapagliflozin trên thí nghiệm ở chuột ghi nhận giảm nồng độ tyrosine hydroxylase và noradrenaline ở thận và tim, là những chất đại diện cho hệ thần kinh giao cảm. Ngoài ra, quá trình khử các chất của hệ thần kinh giao cảm trong thí nghiệm trên chuột không mắc bệnh tăng huyết áp và ĐTĐ, cho kết quả giảm nồng độ SGLT2 ở thận và đồng thời cải thiện huyết áp. (39,40).
- ỨNG DỤNG LÂM SÀNG CỦA SGLT2 ĐỐI VỚI BỆNH NHÂN SUY TIM
Các bác sĩ lâm sàng nên sử dụng SGLT2i cho BN ST như thế nào? Tại đây, chúng tôi đưa ra một vài cân nhắc có liên quan đến việc bắt đầu sử dụng nhóm thuốc này, thông tin được tóm tắt trong Bảng 4 và hình 4.
- Khi nào bắt đầu sử dụng SGLT2
Trong các nghiên cứu DAPA-HF, EMPEROR-REDUCED, và EMPEROR-PRESERVED, SGLT2i đã chứng minh được lợi ích bất chấp tình trạng ĐTĐ. DAPA-HF và EMPEROR-REDUCED NC về khởi trị thuốc SGLT2 trên những BN ST có PSTM giảm với tình trạng ST mạn tính, cần ĐT và ST còn bù; trong khi nghiên cứu EMPEROR-PRESERVED khảo sát SGLT2i trên nhóm BN ST PSTM bảo tồn, tình trạng ST mạn tính, cần điều trị và ST còn bù. Ngược lại, NC SOLOIST-WHF và EMPULS đã cho thấy, việc khởi trị SGLT2i ở những BN ST có PSTM giảm hoặc bảo tồn mới nhập viện gần đây sau khi tình trạng lâm sàng ổn định là an toàn, điều này dẫn đến một số tranh cãi về việc bắt đầu sử dụng SGLTi2 sớm trước khi xuất viện hoặc một thời gian ngắn sau xuất viện (3).
Tổng hợp 3 NC RCT với tổng số 1831 BN được thu nhận cho thấy: Việc khởi trị nhóm thuốc SGLT2i trên những BN ST cấp làm giảm nguy cơ tái nhập viện do ST (OR 0.52; KTC 95% [0.42, 0.65]) và cải thiện điểm số Bệnh cơ tim của thành phố Kansas (trung bình khác biệt điểm số trước và sau khởi trị 4.12; KTC 95 [0.1.89, 6.53]). Không có khác biệt có ý nghĩa thống kê trên TV do mọi nguyên nhân đối với những BN ST cấp được khởi trị bằng SGLT2i (OR 0.70; KTC 95% [0.46, 1.08]). Đồng thời SGLT2i trên nhóm đối tượng NC không làm tăng nguy cơ tổn thương thận cấp tính (OR 0.76; KTC 95% [0.50, 1.16]), hay hạ huyết áp (OR 1.17; KTC 95% [0.80, 1.71]), hoặc làm hạ đường huyết (OR 1.51; KTC 95% [0.86, 2.65]). Kết luận cho thấy việc khởi trị SGLT2i trên những BN nhập viện vì ST cấp trong thời gian nằm việc hoặc thời điểm sớm sau khi xuất viện (trong vòng 3 ngày) làm giảm nguy cơ tái nhập viện do ST và cài thiện kết cục lâm sàng mà không có tác dụng phụ nào đáng kể (hình 3) (41).
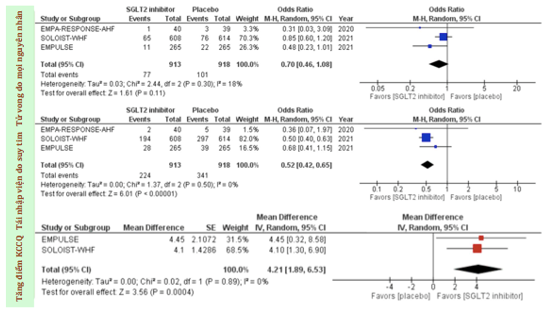
Hình 3 Biểu đồ Forest khảo sát kết cục có lợi của việc khởi trị SGLT2i trên ST cấp. Các biến cố trong phân tích đại diện cho tổng số biến cố mà không phải thời gian tính đến thời điểm có biến cố (41).
(Các chữ viết tắt trong hình: SGLT2: chất đồng vận chuyển Natri-glucose 2; HF: suy tim: KCCQ: bảng câu hỏi đánh giá bệnh cơ tim của thành phố Kansas; CI khoảng tin cậy, M-H phép kiểm Mantel – Haenszel)
Như vậy, từ các dữ liệu cho thấy khởi trị SGLT2i có thể an toàn trong bệnh cảnh tại phòng khám hoặc quanh khoảng thời gian nhập viện. Có ít sự đồng thuận hơn và hầu như không có bằng chứng về thứ tự bắt đầu điều trị SGLT2 so với các nhóm thuốc như chẹn beta, ARNI và kháng Aldosteron trong ST PSTM giàm. Một điều chắc chắn là tác động tối thiểu của SGLT2 lên huyết áp (làm giảm ~ 3-5mmHg) ít bị hạn chế hơn so với các thuốc điều trị ST khác. Một đánh giá khác gợi ý SGLT2i nên được cân nhắc sử dụng sớm hơn so với các thuốc khác do khả năng làm giảm nhập viện do ST và tác dụng bảo vệ chống lại rối loạn chức năng thận, một tác dụng được nhận thấy ngay khi bắt đầu sử dụng giống như đối với việc dùng kháng Aldosteron. Có lẽ điểm quan trọng nhất là SGLT2i mang lại lợi ích TM đáng kể cho BN ST PSTM giảm bất kể phương thức ĐT ST ban đầu. Do đó, thuốc SGLT2i nên được xem là một trong những ĐT nền tảng cho ST PSTM giảm và việc khởi trị nên được ưu tên trên đối tượng BN này. Ngoài ra, với sự ít ỏi trong các lựa chọn ĐT ST PSTM bảo tồn, kết quả của TN EMPEROR-PRESERVED đã cung cấp bằng chứng cho việc sử dụng Empagliflozin trong nhóm BN này (3,42).
- Chức năng thận
Điều quan trọng cần biết là việc sử dụng SGLT2i sẽ làm giảm sớm hơn tốc độ lọc cầu thận ước tính (eGFR) vào khoảng 3-6mL/phút/1,73m2; tuy nhiên các bác sĩ lâm sàng không nên ngưng điều trị. Ngược lại, đây là nhóm thuốc bảo vệ thận, eGFR sẽ hồi phục một phần sau 12 tuần và quan trọng hơn độ dốc của sự suy giảm tổng thể eGFR sẽ giảm sau đó.
Sự suy giảm eGFR ban đầu sẽ biểu hiện rõ hơn ở những BN có chức năng thận bình thường so với những BN suy thận mạn tính. Cơ chế giảm eGFR là kết quả sự ức chế tái hấp thu natri ở ống lượn gần, dẫn đến tăng vận chuyển natri từ ống lượn xa sang macula densa (các tế bào đóng gói trong ống biểu mô noại biên của bộ phận bài tiết trong thận, ở cạnh cầu thận: theo từ điển bách khoa Y-học Anh Việt). Tín hiệu này làm cho phức hợp cạnh cầu thận gây ra tăng thể tích tuần hoàn hiệu quả và tăng áp lực động mạch thận dẫn đến phát tín hiệu gây co tiểu động mạch trung tâm. Hơn nữa, dữ liệu từ nhiều nghiên cứu bao gồm các thử nghiệm lâm sàng thực tế và các định nghĩa về tổn thương thận cấp đã chỉ ra rằng SGLT2i thực sự làm giảm nguy cơ tổn thương thận cấp.
Có tồn tại một ngưỡng eGFR nào mà các bác sĩ lâm sàng không nên sử dụng thuốc SGLT2i không? Hiện tại chưa có một dữ liệu chắc chắn nào để chứng minh tác hại (cũng như lợi ích) của việc khởi trị SGLT2 trên nhóm BN bệnh thận mạn giai đoạn V, do đó các khuyến cáo thực hành dựa trên các tiêu chí chọn bệnh của các thử nghiệm lâm sàng lớn. Dapagliflozin đã được nghiên cứu ở những BN có eGFR thấp đến 25ml/phút/1,73m2trong DAPA-CKD và eGFR đến ngưỡng 30ml/phút/1,73m2 ở DAPA-HF; trong khi tiêu chí loại trừ đối với hai nghiên cứu EMPEROR-REDUCED và EMPEROR-PRESERVED là eGFR < 20ml/phút/1,73m2. Hơn nữa, một điểm khác biệt quan trọng là có thể tiếp tục sử dụng Dapagliflozin an toàn khi eGFR giảm xuống dưới 25ml/phút/1,73m2 miễn là thuốc được bắt đầu sử dụng trên ngưỡng này. Nên ngừng thuốc nếu bệnh nhân suy thận tiến triển cần phải lọc máu (43,44).
- KHUYẾN CÁO
Vào tháng 1/2021, Hiệp hội trường môn Tim Mạch Hoa Kỳ đã công bố Bảng cập nhật ĐT năm 2021 cho Quyết định đồng thuận của các chuyên gia của Hiệp Hội Tim Mạch Hoa Kỳ năm 2017 về Tối ưu hoá ĐT ST, trong đó nhóm thuốc SGLT2i được xếp vào nhóm ĐT nhóm 1. Khuyến cáo này đề nghị liệu trình ĐT ở những BN ST PSTM giảm giai đoạn C, bắt đầu bằng nhóm ƯCMC/ƯCTT/ARNI hoặc nhóm chẹn beta, theo bất cứ thứ tự nào; sau đó có thể xem xét thuốc kháng Aldosteron và SGLT2i. Cụ thể SGLT2i được khuyến cáo cho những BN ST có triệu chứng NYHA II – IV và đáp ứng tiêu chí eGFR ≥ 30 ml/phút/1,73m2 khi dùng Dapagliflozin và ≥ 20 ml/phút/1,73m2 cho Empagliflozin. Tài liệu không đề cập đến thuốc khác thuộc nhóm này (45).
Tháng 8/2021, Hiệp hội tim mạch Châu Âu đã phát hành Hướng dẫn chẩn đoán và ĐT ST cấp và mạn, trong đó xếp loại Dapagliflozin và Empagliflozin thuộc NHÓM I-A cho ĐT BN ST PSTM giảm (EF ≤ 40%, và NYHA II – IV) mà đã được ĐT UCTT/ARNI, chẹn beta, và kháng Aldosteron trước đó, việc bổ sung ĐT này nhằm làm giảm nguy cơ TV do TM hoặc tránh tình trạng ST nặng hơn (46).
Tương tự, đầu năm 2022, hiệp hội tim mạch Mĩ/trường môn Tim mạch Mỹ/hội ST Mĩ cũng đưa ra khuyến cáo ĐT ST, trong đó cũng nhấn mạnh đến vai trò của Dapagliflozin và Empagliflozin cho ĐT ST (nhóm IA) với 2/10 điểm chính sau (47,48):
(1). ĐT ST theo khuyến cáo hiện nay đã mở rộng thành 4 nhóm thuốc, bao gồm: 1) nhóm ức chế hệ renin-angiotensin (RASi) và thuốc ức chế thụ thể angiotensin – neprilysin (ARNi), hoặc nhóm thuốc ức chế men chuyển (ACEi), hoặc ức chế thụ thể (ARB) đơn thuần; 2) nhóm ức chế beta; 3) nhóm thuốc kháng thụ thể mineralocorticoid (MRA); và 4) nhóm thuốc ức chế đồng vận chuyển natri-glucose 2 (SGLT2i).
(2). Các khuyến cáo mới đã được cập nhật cho việc sử dụng SGLT2i trên BN ST. Đối với những BN ST mạn PXTM giảm có triệu chứng, SGLT2i được khuyến cáo làm giảm nhập viện do ST và giảm TV do TM, bất kể có hay không có ĐTĐ2 (Phân nhóm khuyến cáo 1A). SGLT2i có thể có lợi ích trên những BN STPXTM giảm nhẹ hoặc bảo tồn (phân nhóm khuyến cáo 2A).
- KẾT LUẬN
Nhóm thuốc SGLT2I là một sự bổ sung tình cờ cho liệu pháp ĐT ST. Đã có nhiều TN lâm sàng ngẫu nhiên có đối chứng lớn chứng minh độ an toàn cũng như hiệu quả của nhóm thuốc này trong việc giảm nhập viện do ST và giảm TV TM ở BN ST PSTM giảm có triệu chứng, bất kể tình trạng đường huyết và có thể bắt đầu khởi trị trong bệnh cảnh ST cấp hoặc mạn . Việc sử dụng SGLT2i cũng có vai trò trong việc giảm nhập viện do ST trên những BN ST PSTM bảo tồn. Cơ chế hoạt động bảo vệ TM, cụ thể là trong bệnh cảnh ST PSTM giảm vẫn là một chủ đề tiếp tục được tranh luận và NC. Các bác sĩ chuyên khoa TM, thận học, nội tiết học, cũng như bác sĩ chăm sóc sức khoẻ ban đầu nên tập làm quen với việc sử dụng các loại thuốc này, bao gồm những thay đổi sinh lý, và thay đổi trong các thông số xét nghiệm dự đoán được cũng như các tác dụng phụ tiềm ẩn. Tương lai đối với SGLT2i vẫn còn khá thú vị và đáng trông chờ khi mà vẫn còn rất nhiều tn đang được tiến hành.
Bảng 1: Các thử nghiệm về kết cục tim mạch sớm trên nhóm thuốc SGLT2i (3)
| EMPA-REG OUTCOME | CANVAS | DECLARE-TIMI 58 | |
| Thuốc | Empagliflozin 10mg hoặc 25mg so với giả dược | Canagliflozin 100mg hoặc 300mg so với giả dược | Dapagliflozin 10mg so với giả dược |
| Nhóm BN nghiên cứu | · 7020 bệnh nhân ĐTĐ típ 2 và có bệnh tim mạch
· eGFR ≥ 30 ml/phút/1,73m2 |
· 10142 bệnh nhân ĐTĐ típ 2 và có bệnh tim mạch hoặc có ≥ yếu tố nguy cơ tim mạch
· eGFR ≥ 30 ml/phút/1,73m2 |
· 17160 bệnh nhân ĐTĐ típ 2 và có bệnh tim mạch hoặc có các yếu tố nguy cơ tim mạch
· eGFR ≥ 60 ml/phút/1,73m2 |
| Tiền sử ST (PSTM giảm hoặc bảo tồn) | 706 (10,1%) | 1461 (14,4%) | 1724 (10,0%) |
| Kết cục chính | 3 biến cố tim mạch chính MACE (HR 0,86; KTC 95% 0,74 – 0,99) | 3 biến cố tim mạch chính MACE (HR 0,86; KTC 95% 0,75 – 0,97) | 3 biến cố tim mạch chính MACE (HR 0,93; KTC 95% 0,84 – 1,03) |
| Kết cục nhập viện do ST | HR 0,65; KTC 95% 0,5 – 0,85 | HR 0,67; KTC 95% 0,52 – 0,87 | HR 0,73; KTC 95% 0,61 – 0,88 |
| Tử vong do TM | HR 0,62; KTC 95% 0,49 – 0,77 | HR 0,87; KTC 95% 0,72 – 1,06 | HR 0,98; KTC 95% 0,82 – 1,17 |
| Các phân tích sau nghiên cứu | Các biến cố tim mạch giảm, bất kể:
· Tiền sử suy tim · Tỷ số nguy cơ nền · Nguy cơ tim mạch nền |
· Lợi ích bất kể suy tim PSTM giảm hay bảo tồn
· Lợi ích lớn hơn trên bệnh nhân không có bệnh sử suy tim
|
· Giảm nhập viện do suy tim bất kể tiền sử suy tim
· Giảm tử vong do tim mạch ở những bệnh nhân suy tim PSTM giảm |
Bảng 2: Các thử nghiệm ngẫu nhiên có đối chứng lớn trên suy tim của nhóm thuốc SGLT2i (3)
| DAPA-HF | EMPEROR-REDUCED | SOLOIST-WHF | EMPEROR-PRESERVED | |
| Thuốc | Dapagliflozin 10mg so với giả dược | Empagliflozin 10mg so với giả dược | Sotagliflozin 400mg so với giả dược | Empagliflozin 10mg so với giả dược |
| Nhóm bệnh nhân nghiên cứu | · 4744 bệnh nhân suy tim PSTM giảm mạn tính, cần điều trị (PSTM ≤ 40%, NYHA II-IV)
· 45% có ĐTĐ típ 2 · eGFR ≥ 30 ml/phút/1,73m2 |
· 3730 bệnh nhân suy tim PSTM giảm mạn tính, cần điều trị (PSTM ≤ 40%, NYHA II-IV)
· 50% có ĐTĐ típ 2 · eGFR ≥ 20 ml/phút/1,73m2 |
· 1222 bệnh nhân suy tim PSTM giảm (79%) hoặc PSTM bảo tồn (21%) nhập viện vì suy tim cấp
· Đã chuyển sang lợi tiểu đường uống · 100% có ĐTĐ típ 2 · eGFR ≥ 30 ml/phút/1,73m2 |
· 5988 bệnh nhân suy tim mạn tính PSTM bảo tồn, cần điều trị (PSTM > 40%, NYHA II-IV)
· 49% có ĐTĐ típ 2 · eGFR ≥ 20 ml/phút/1,73m2 |
| Kết cục chính | Nhập viện vì suy tim hoặc tử vong do tim mạch, bao gồm nhập cấp cứu và cần điều trị suy tim bằng thuốc đường tĩnh mạch (HR 0,74; KTC 95% 0,65 – 0,85) | Nhập viện vì suy tim hoặc tử vong do tim mạch(HR 0,75; KTC 95% 0,65 – 0,86) | Nhập viện vì suy tim, cần khám sớm vì suy tim, hoặc tử vong do tim mạch(HR 0,67; KTC 95% 0,52 – 0,85) | Nhập viện vì suy tim hoặc tử vong do tim mạch(HR 0,79; KTC 95% 0,69 – 0,90) |
| Kết cục nhập viện do ST | HR 0,70; KTC 95% 0,59 – 0,83 | HR 0,69; KTC 95% 0,59 – 0,81 | Không được đánh giá | HR 0,71; KTC 95% 0,60 – 0,83 |
| TV DO TM | HR 0,82; KTC 95% 0,69 – 0,98 | HR 0,92; KTC 95% 0,75 – 1,12 | HR 0,84; KTC 95% 0,58 – 1,22 | HR 0,91; KTC 95% 0,76 – 1,09 |
| Các phân tích sau NC | · Lợi ích bất kể liệu pháp ĐT ST trước đó
· Giảm nhập viện do suy tim lần đầu và tái diễn · Giảm điều trị suy tim tăng cường đối với bệnh nhân ngoại trú |
· Cải thiện sớm và duy trì chất lượng cuộc sống dựa trên bảng câu hỏi KCCQ-CSS
· Giảm nhập viện do suy tim lần đầu và tái diễn ·
|
· Phân tích gộp với nc SCORED cho thấy giảm các kết cục chính bất kể suy tim PSTM giảm hay bảo tồn
· Tăng số ngày sống còn và giảm số ngày nhập viện điều trị |
· Phân tích gộp EMPEROR cho thấy sự không đồng nhất đáng kể giữa suy tim PSTM giảm và suy tim PSTM bảo tồn liên quan đến các biến cố thận chính.
|
Bảng 3: Chọn lọc một số nghiên cứu về suy tim trên SGLT2 đang diễn ra (3)
| Nghiên cứu | Mã số NC | Thuốc | Nhóm dân số nghiên cứu | Số bn
tuyển chọn |
Kết cục chính |
| Suy tim mạn tính
· DETERMINE-REDUCED · CHIEF-HF · DELIVER |
03877237 04252287 03619213 |
Dapagliflozin Canagliflozin Dapagliflozin |
Suy tim PSTM giảm Suy tim PSTM giảm và bảo tồn Suy tim PSTM bảo tồn |
313 476 6263 |
Test đi bộ 6 phút và bảng câu hỏi KCCQ Bảng câu hỏi KCCQ Thời gian đến tử vong do tim mạch, lần đầu nhập viện vì suy tim hoặc cần khám sớm vì suy tim |
| Suy tim cấp
· DAPA ACT HF-TIMI 68
· EMPULSE |
04363697
04157751 |
Dapagliflozin
Empagliflozin |
Suy tim PSTM giảm
Suy tim PSTM giảm và bảo tồn |
2400
530 |
Thời gian đến tử vong tim mạch hoặc suy tim nặng hơn Tử vong do mọi nguyên nhân, biến cố suy tim, và bảng câu hỏi KCCQ (tính tỷ số Win) |
| NMCT và suy tim
· EMPACT-MI
· DAPA-MI |
04509674
04564742 |
Empagliflozin
Dapagliflozin |
NMCT không/có STCL với suy tim mới NMCT không/có STCL với suy tim mới |
3312
6400 |
Thời gian đến lần đầu nhập viện vì suy tim, hoặc tử vong do mọi nguyên nhân Thời gian đến lần đầu nhập viện vì suy tim, hoặc tử vong do tim mạch |
Bảng 4: Các cân nhắc lâm sàng khi sử dụng thuốc SGLT2
| Cân nhắc lâm sàng | Tiếp cận |
| Thời điểm khởi trị | · Trước khi xuất viện do đợt suy tim cấp hoặc trong khi đến phòng khám do suy tim mạn tính, bất kể tình trạng tiểu đường |
| Chức năng thận | · Empagliflozin khởi trị với eGFR > 20ml/phút/1,73m2
· Dapagliflozin khởi trị với eGFR > 25ml/phút/1,73m2 · An toàn sử dụng Dapagliflozin cho đến thời điểm cần lọc máu nếu khởi trị trên ngưỡng chức năng thận thích hợp (tiếp tục Empagliflozin với cùng điều kiện khi được FDA cập nhật chỉ định) |
| Biến cố bất lợi | · Tăng nhiễm trùng đường sinh dục à cần tư vấn cho bệnh nhân về các dấu hiện/triệu chứng và khuyến khích vệ sinh
· Nhiễm trùng đường tiết niệu à tương tự giữa nhóm thuốc và giả dược trong nhiều nghiên cứu, nhưng tăng ở nhóm dùng thuốc trong nc EMPEROR-PRESERVED, khuyến khích vệ sinh · Nhiễm toan ceton do ĐTĐ àkhuyên bệnh nhân ngưng thuốc nếu giảm ăn hoặc cần nhịn ăn trước phẫu thuật. |

Hình 4. SGLT2i thời điểm khởi trị và cách thức khởi trị. Dữ liệu dựa trên các tiêu chí thu nhận bệnh từ các nghiên cứu DAPA-HF, EMPEROR-Reduced và EMPULSE (50).
Tài liệu tham khảo
- WG et al: Cardiac, renal, and metabolic effects of sodium–glucose co-transporter 2 inhibitors: a position paper from the European Society of Cardiology ad-hoc task force on sodium–glucose co-transporter 2 inhibitors. European Journal of Heart Failure (2021). doi:10.1002/ejhf.2286
- Wright EM, Loo DDF, Hirayama BA. Biology of human sodium glucose transporters. Physiological Reviews. 2011; 91: 733–794.
- T, Gong. T: SGLT2 inhibitors: a new pillar of the heart failure regimen. Rev. Cardiovasc. Med. 2021 vol. 22(4), 1253-1269.
- Fitchett D, ZinmanB,Wanner C, Lachin JM, Hantel S, SalsaliA,et al. Heart failure outcomes with empagliflozin in patients with type 2 diabetes at high cardiovascular risk: results of the EMPA-REG OUTCOME® trial. European Heart Journal. 2016; 37: 1526–1534.
- Fitchett D, Inzucchi SE, Cannon CP, McGuire DK, Scirica BM, Johansen OE, et al. Empagliflozin Reduced Mortality and Hospitalization for Heart Failure across the Spectrum of Cardiovascular Risk in the EMPA-REG OUTCOME Trial. Circulation. 2019; 139: 1384–1395.
- Neal B, Perkovic V, Mahaffey KW, de Zeeuw D, Fulcher G, Erondu N, et al. Canagliflozin and Cardiovascular and Renal Events in Type 2 Diabetes. The New England Journal of Medicine. 2017; 377: 644–657.
- Wiviott SD, Raz I, Bonaca MP, Mosenzon O, Kato ET, Cahn A, et al. Dapagliflozin and Cardiovascular Outcomes in Type 2 Diabetes. New England Journal of Medicine. 2019; 380: 347–357
- Kato ET, Silverman MG, Mosenzon O, Zelniker TA, Cahn A, Furtado RHM,et al. Effect of Dapagliflozin on Heart Failure and Mortality in Type 2 Diabetes Mellitus. Circulation. 2019; 139: 2528– 2536.
- Zelniker TA, Wiviott SD, Raz I, Im K, Goodrich EL, Bonaca MP, et al. SGLT2 inhibitors for primary and secondary prevention of cardiovascular and renal outcomes in type 2 diabetes: a systematic review and meta-analysis of cardiovascular outcome trials. The Lancet. 2019; 393: 31–39
- McMurray JJV, Solomon SD, Inzucchi SE, Køber L, Kosiborod MN, Martinez FA, et al. Dapagliflozin in Patients with Heart Failure and Reduced Ejection Fraction. New England Journal of Medicine. 2019; 381: 1995–2008.
- FDA approves new treatment for a type of heart failure. FDA News Release. 2020. Available at: https: //www.fda.gov/news-events/press-announcements/fda-a pproves-new-treatment-type-heart-failure (Accessed: 1 September 2021).
- Packer M, Anker SD, Butler J, Filippatos G, Pocock SJ, Carson P, et al. Cardiovascular and Renal Outcomes with Empagliflozin in Heart Failure. New England Journal of Medicine. 2020; 383: 1413–1424.
- Packer M, Anker SD, Butler J, Filippatos G, Ferreira JP, Pocock SJ, et al. Effect of Empagliflozin on the Clinical Stability of Patients with Heart Failure and a Reduced Ejection Fraction. Circulation. 2021; 143: 326–336.
- FDA to Review Eli Lilly’s Jardiance for Heart Failure. FDA News. 2021. Available at: https://www.fdanews.com/articles/200849-f da-to-review-eli-lillys-jardiance-for-heart-failure (Accessed: 1 September 2021)
- Bhatt DL, Szarek M, Steg PG, Cannon CP, Leiter LA, McGuire DK,et al. Sotagliflozin in Patients with Diabetes and Recent Worsening Heart Failure. New England Journal of Medicine. 2021; 384: 117–128.
- Bhatt DL, Szarek M, Pitt B, Cannon CP, Leiter LA, McGuire DK, et al. Sotagliflozin in Patients with Diabetes and Chronic Kidney Disease. New England Journal of Medicine. 2021; 384: 129–139
- Szarek M, Bhatt DL, Steg PG, Cannon CP, Leiter LA, McGuire DK, et al. Effect of Sotagliflozin on Total Hospitalizations in Patients with Type 2 Diabetes and Worsening Heart Failure. Annals of Internal Medicine. 2021; 174: 1065–1072
- McMurray JJV. EMPEROR‐Reduced: confirming sodium– glucose co‐transporter 2 inhibitors as an essential treatment for patients with heart failure with reduced ejection fraction. European Journal of Heart Failure. 2020; 22: 1987–1990. Solomon SD, Boer RA, DeMets D, Hernandez AF, Inzucchi SE, Kosiborod MN, et al. Dapagliflozin in heart failure with preserved and mildly reduced ejection fraction: rationale and design of the DELIVER trial. European Journal of Heart Failure. 2021; 23: 1217–1225
- McGuire DK, ShihWJ, Cosentino F, Charbonnel B, Cherney DZI, Dagogo-Jack S, et al. Association of SGLT2 Inhibitors with Cardiovascular and Kidney Outcomes in Patients with Type 2 Diabetes. JAMA Cardiology. 2021; 6: 148.
- Zannad F, Ferreira JP, Pocock SJ, Anker SD, Butler J, Filippatos G, et al. SGLT2 inhibitors in patients with heart failure with reduced ejection fraction: a meta-analysis of the EMPEROR-Reduced and DAPA-HF trials. The Lancet. 2020; 396: 819–829.
- Voors AA, Angermann CE, Teerlink JR, et al: The SGLT2 inhibitor empagliflozin in patients hospitalized for acute heart failure: a multinational randomized trial. Nature Medicine, VOL 28; March 2022: 568–574
- Zelniker TA, Braunwald E. Clinical Benefit of Cardiorenal Effects of Sodium-Glucose Cotransporter 2 Inhibitors. Journal of the American College of Cardiology. 2020; 75: 435–447.
- Genuardi MV, Mather PJ. The dawn of the four-drug era? SGLT2 inhibition in heart failure with reduced ejection fraction. Therapeutic Advances in Cardiovascular Disease. 2021; 15: 175394472110026.
- Packer M. Critical examination of mechanisms underlying the reduction in heart failure events with SGLT2 inhibitors: identification of a molecular link between their actions to stimulate erythrocytosis and to alleviate cellular stress. Cardiovascular Research. 2021; 117: 74–84.
- Li C, Zhang J, Xue M, Li X, Han F, Liu X, et al. SGLT2 inhibition with empagliflozin attenuates myocardial oxidative stress and fibrosis in diabetic mice heart. Cardiovascular Diabetology. 2019; 18: 15.
- Heerspink HJL, Perco P, Mulder S, Leierer J, Hansen MK, Heinzel A, et al. Canagliflozin reduces inflammation and fibrosis biomarkers: a potential mechanism of action for beneficial effects of SGLT2 inhibitors in diabetic kidney disease. Diabetologia. 2019; 62: 1154–1166.
- Lee T, Chang N, Lin S. Dapagliflozin, a selective SGLT2 Inhibitor, attenuated cardiac fibrosis by regulating the macrophage polarization via STAT3 signaling in infarcted rat hearts. Free Radical Biology & Medicine. 2017; 104: 298–310.
- Uthman L, Baartscheer A, Bleijlevens B, Schumacher CA, Fiolet JWT, Koeman A, et al. Class effects of SGLT2 inhibitors in mouse cardiomyocytes and hearts: inhibition of Na+/H+ exchanger, lowering of cytosolic Na+ and vasodilation. Diabetologia. 2018; 61: 722–726.
- Packer M. Reconceptualization of the Molecular Mechanism by which Sodium-Glucose Cotransporter 2 Inhibitors Reduce the Risk of Heart Failure Events. Circulation. 2019; 140: 443–445.
- Voros G, Ector J, Garweg C, Droogne W, Van Cleemput J, Peersman N, et al. Increased Cardiac Uptake of Ketone Bodies and Free Fatty Acids in Human Heart Failure and Hypertrophic Left Ventricular Remodeling. Circulation: Heart Failure. 2018; 11: e004953.
- Kim SR, Lee S, Kim SH, Kim JH, Choi E, Cho W, et al. SGLT2 inhibition modulates NLRP3 inflammasome activity via ketones and insulin in diabetes with cardiovascular disease. Nature Communications. 2020; 11: 2127
- Bonnet F, Scheen AJ. Effects of SGLT2 inhibitors on systemic and tissue low-grade inflammation: the potential contribution to diabetes complications and cardiovascular disease. Diabetes & Metabolism. 2018; 44: 457–464
- Camarena V, Sant D, Mohseni M, Salerno T, Zaleski ML, Wang G, et al. Novel atherogenic pathways from the differential transcriptome analysis of diabetic epicardial adipose tissue. Nutrition, Metabolism, and Cardiovascular Diseases. 2017; 27: 739–750.
- Miyachi Y, Tsuchiya K, Shiba K, Mori K, Komiya C, Ogasawara N, et al. A reduced M1-like/M2-like ratio of macrophages in healthy adipose tissue expansion during SGLT2 inhibition. Scientific Reports. 2018; 8: 16113.
- Hallow KM, Helmlinger G, Greasley PJ, McMurray JJV, Boulton DW. Why do SGLT2 inhibitors reduce heart failure hospitalization? a differential volume regulation hypothesis. Diabetes, Obesity & Metabolism. 2018; 20: 479–487
- Nassif ME, Windsor SL, Tang F, Khariton Y, Husain M, Inzucchi SE, et al. Dapagliflozin Effects on Biomarkers, Symptoms, and Functional Status in Patients With Heart Failure With Reduced Ejection Fraction. Circulation. 2019; 140: 1463–1476.
- Margonato D, Galati G, Mazzetti S, Cannistraci R, Perseghin G, Margonato A, et al. Renal protection: a leading mechanism for cardiovascular benefit in patients treated with SGLT2 inhibitors. Heart Failure Reviews. 2021; 26: 337–345
- FDA to Review Eli Lilly’s Jardiance for Heart Failure. FDA News. 2021. Available at: https://www.fdanews.com/articles/200849-f da-to-review-eli-lillys-jardiance-for-heart-failure (Accessed: 1 September 2021).
- Scheen AJ. Effect of SGLT2 Inhibitors on the Sympathetic Nervous System and Blood Pressure. Current Cardiology Reports. 2019; 21: 70
- Verma S. Are the Cardiorenal Benefits of SGLT2 Inhibitors Due to Inhibition of the Sympathetic Nervous System? JACC: Basic to Translational Science. 2020; 5: 180–182
- HM ,Al’Aref. SJ , Khan. MS et al: Efcacy and safety of sodium-glucose cotransporter 2 inhibitors initiation in patients with acute heart failure, with and without type 2 diabetes: a systematic review and meta-analysis. Cardiovascular Diabetology (2022) 21:20. https://doi.org/10.1186/s12933-022-01455-2
- McMurray JJV, Packer M. How should we Sequence the Treatments for Heart Failure and a Reduced Ejection Fraction? Circulation. 2021; 143: 875–877
- Meraz-Muñoz AY, Weinstein J, Wald R. EGFR Decline after SGLT2 Inhibitor Initiation: the Tortoise and the Hare Reimagined. Kidney360. 2021; 2: 1042–1047.
- Zelniker TA, Braunwald E. Mechanisms of Cardiorenal Effects of Sodium-Glucose Cotransporter 2 Inhibitors. Journal of the American College of Cardiology. 2020; 75: 422–434.
- Maddox TM, Januzzi JL, Allen LA, Breathett K, Butler J, Davis LL,et al. 2021 Update to the 2017 ACC Expert Consensus Decision Pathway for Optimization of Heart Failure Treatment: Answers to 10 Pivotal Issues about Heart Failure with Reduced Ejection Fraction. Journal of the American College of Cardiology. 2021; 77: 772–810.
- McDonagh TA, Metra M, Adamo M, Gardner RS, Baumbach A, Böhm M, et al. 2021 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure. European Heart Journal. 2021. (in press)
- Heidenreich et al: 2022 AHA/ACC/HFSA Guideline for the Management of Heart Failure. Journal of the American College of Cardiology. Volume 79, Issue 17, 3 May 2022, Pages e263-e421.
- 2022 AHA/ACC/HFSA Heart Failure Guideline: Key Perspectives
- D et al: Sodium–glucose co-transporter 2 inhibitors as an early, first-line therapy in patients with heart failure and reduced ejection fraction. European Journal of Heart Failure (2021). doi:10.1002/ejhf.2397
- D et al: Sodium–glucose co-transporter 2 inhibitors as an early, first-line therapy in patients with heart failure and reduced ejection fraction. European Journal of Heart Failure (2022) 24, 431–441







